“变废为宝、爱护环境、节约资源”从我做起.宁宁同学收集一些家庭装修时废弃大理石碎片,并设计下图装置来测取二氧化碳,该反应
 Nazgul11052022-10-04 11:39:541条回答
Nazgul11052022-10-04 11:39:541条回答 碳,该反应装置通过粗铜丝调节能随时控制反应的发生.
碳,该反应装置通过粗铜丝调节能随时控制反应的发生.回答有关问题:
(1)大理石应放在______中,装置A中反应化学方程式为______.
(2)装置A中的粗铜线能否用粗铁线代替______,原因可用化学方程式为:______.
(3)用装置B收集CO2,验满时应把燃着的木条放在(填字母)______处,若观察到______的现象,证明已集满二氧化碳.
(4)某同学建议宁宁改用排水法收集二氧化碳,认为这种收集二氧化碳较纯净,你认为该同学的建议可采纳吗?______,你的理由是______.
(5)将A装置中的粗铜线及小药瓶除去,还可制备氧气,请写出用过氧化氢溶液和二氧化锰制氧气的反应化学方程式
| ||
| ||

已提交,审核后显示!提交回复
共1条回复
 penny7275 共回答了21个问题
penny7275 共回答了21个问题 |采纳率90.5%- 解题思路:(1)根据大理石是块状固体和实验室制取二氧化碳的反应原理分析.
(2)根据铁能和稀盐酸反应生成氯化亚铁和氢气分析.
(3)根据二氧化碳既不燃烧也不支持燃烧分析检验方法.
(4)根据二氧化碳能溶于水又能和水反应分析.
(5)根据用过氧化氢和二氧化锰制取氧气的反应分析.(1)大理石是块状固体应放在药瓶中和实验室制取二氧化碳的反应原理:CaCO3+2HCl=CaCl2+H2O+CO2↑,故答案:药瓶;CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)铁能和稀盐酸反应生成氯化亚铁和氢气,故答案:不能;Fe+2HCl=FeCl2+H2↑.
(3)二氧化碳既不燃烧也不支持燃烧,故验满就将燃着的木条放在集气瓶口看是否熄灭,故答案:a;燃着的木条熄灭.
(4)二氧化碳能溶于水又能和水反应,所以不能用排水法收集,故答案:不可以;二氧化碳能溶于水且能和水反应.
(5)用过氧化氢和二氧化锰制取氧气的反应:2H2O2
MnO2
.
2H2O+O2↑.点评:
本题考点: 二氧化碳的实验室制法.
考点点评: 本题拓展了实验室中常温型的气体发生装置,使反应随时发生随时终止,平时对二氧化碳和氧气的制取和收集知识必须非常牢固. - 1年前
相关推荐
- 有什么变废为宝的例子吗?大家有什么变废为宝的好例子说说看!
 豆米07201年前1
豆米07201年前1 -
 情缘999 共回答了20个问题
情缘999 共回答了20个问题 |采纳率80%1.小朋友喝过的奶粉罐四个,用布或纸包住粘好,上面加一块小胶合板,可以做玩耍时用的小桌子,罐里还可以装一些他们的玩具.注意罐的盖子用按钉按在胶盒板上后,要处理一下钉子头,用锤子将钉头敲平,再用热熔胶粘一下,这样就不会被让孩子扎到.
2.纸制纸巾盒,可以在下面切个口,表面用喜欢的布或者纸粘一下,竖着粘在墙上,里面放上面巾纸,从切口处抽取面巾纸.
3.纸制的大饮料盒,比如大牛奶盒、大果汁盒,外面用布粘成或者缝成小衬衫形,在衬衫口袋处切出小口,可以装硬币.
4.如果只有一种规格相同大小的纸盒多个,可以粘上一种纸,侧面按梯形裁剪,将书装在里面,竖成一排,可以让书架很整齐.
5.不用的各种塑料瓶,比如洗衣液的、消毒液的,可以做成沙滩玩具.
6.用光了的双面胶的硬纸胶芯,用一个宽的做盒身,一个窄的做盒盖,各加一个底,再用薄海绵(比如过期证书里面的那种)和布封成外套,里面用单面胶将盒身与盒盖粘住(起到折叶的作用),外面做个搭扣,可以用小树枝或者小扣子,就是个漂亮的小礼物盒.
7.玻璃瓶子外边用麻绳缠成一圈一圈的,再粘上彩色的纽扣,可以作成花瓶.1年前查看全部
- “人类只有一个地球!”为了保护人类赖以生存的环境,下列做法中不正确的是( )。 A.回收处理垃圾,变废为宝 B.废旧电
“人类只有一个地球!”为了保护人类赖以生存的环境,下列做法中不正确的是( )。
A.回收处理垃圾,变废为宝 B.废旧电池中含有汞(Hg 2 + )等,会污染地下水与土壤,必须回收处理 C.为了谋取利益,捕杀、贩卖野生动物 D.开发新能源,逐步减少使用化石燃料  danshunubu1年前1
danshunubu1年前1 -
 成日挨地小便 共回答了15个问题
成日挨地小便 共回答了15个问题 |采纳率93.3%C
捕杀、贩卖野生动物是违法犯罪行为,也是破坏生态平衡的行为,我们应予以制止。1年前查看全部
- (2013•淄川区模拟)采用合理的化学工艺可以减少工业废水对环境的污染,同时还能最大限度的变废为宝.某兴趣小组的同学从某
(2013•淄川区模拟)采用合理的化学工艺可以减少工业废水对环境的污染,同时还能最大限度的变废为宝.某兴趣小组的同学从某工厂排出的含有硫酸铜的废水中取了一烧杯,向其中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸产生气泡.则滤渣中一定含有的物质是______(写化学式),用化学方程式表示产生气泡的原因:______.题目中出现的金属中,常用作导线的是______(写名称):暴露在空气中的铁制品,容易与空气中的______等物质作用而生锈,需要认真做好铁的防锈工作.
 ningguoren1年前1
ningguoren1年前1 -
 nihao1987 共回答了12个问题
nihao1987 共回答了12个问题 |采纳率91.7%解题思路:铜不能和稀盐酸反应,铁能和稀盐酸反应生成氯化亚铁和氢气;
铜的导电能力仅次于银,常常用于制作导线;
铁与氧气和水充分接触时容易生锈,水和氧气同时存在是铁生锈的必要条件.充分反应后过滤,向滤渣中加入稀盐酸产生气泡,说明铁粉过量,则滤渣中一定含有铜和铁,化学式分别是Cu、Fe.
故填:Cu、Fe.
铁和稀盐酸反应的化学方程式为:Fe+2HCl=FeCl2+H2↑.
故填:Fe+2HCl=FeCl2+H2↑.
因为铜具有良好的导电性,常常用于制作导线.
故填:铜.
铁制品,容易与空气中的水、氧气等物质作用而生锈.
故填:水、氧气.点评:
本题考点: 金属的化学性质;金属的物理性质及用途;金属锈蚀的条件及其防护;酸的化学性质.
考点点评: 铁与氧气和水充分接触时容易生锈,水和氧气同时存在是铁生锈的必要条件;如果缺少水或缺少氧气,或者缺少氧气和水,铁就不容易生锈.1年前查看全部
- 下列课题不属于化学学科研究领域的是( ) A.发明新的药物以解除病人痛苦 B.变废为宝,使废旧塑料变成燃料 C.电脑软
下列课题不属于化学学科研究领域的是( ) A.发明新的药物以解除病人痛苦 B.变废为宝,使废旧塑料变成燃料 C.电脑软件的不断升级 D.开发新能源和新材料,改善人类生存条件  潇雨寒韵1年前1
潇雨寒韵1年前1 -
 ri23901 共回答了22个问题
ri23901 共回答了22个问题 |采纳率81.8%A、发明新的药物以解除病人痛苦,与合成新物质有关,是化学研究的范畴,故此选项错误.
B、废旧塑料变成燃料,涉及到物质的燃烧变化,属化学研究的范畴,故此选项错误.
C、电脑软件升级不涉及物质的问题,不是化学研究的范畴,故此选项正确.
D、开发新能源和新材料,改善人类生存条件,也是与物质的变化有关,是化学研究的范畴,故此选项错误.
故选C1年前查看全部
- 地球上的资源是有限的,请你想一想在我们的周围,在我们日常生活中,在我们家里,哪些东西可以变废为宝呢?
 giant_k1年前1
giant_k1年前1 -
 lxxlxl 共回答了15个问题
lxxlxl 共回答了15个问题 |采纳率86.7%淘米水
矿泉水瓶
可乐瓶
易拉罐
油桶
纸皮箱
书,纸,报纸,纸包装盒
一次性的塑料杯子,饮料瓶,超市用的那种便利袋
废旧家电,胶底鞋,破铜烂铁
喝完了的茶叶晒干可以做枕芯,可以除湿,可以做柴火烧.
剩饭菜可以做花肥.1年前查看全部
- 为了增强市民的环保意识,变废为宝,我市已实施垃圾分类回收.生活垃圾一般分为三类:可回收垃圾、不可回收垃圾和有害垃圾.现有
 为了增强市民的环保意识,变废为宝,我市已实施垃圾分类回收.生活垃圾一般分为三类:可回收垃圾、不可回收垃圾和有害垃圾.现有如下垃圾:①矿泉水瓶②口香糖③菜叶④易拉罐⑤果皮,其中属于可回收垃圾的是( )
为了增强市民的环保意识,变废为宝,我市已实施垃圾分类回收.生活垃圾一般分为三类:可回收垃圾、不可回收垃圾和有害垃圾.现有如下垃圾:①矿泉水瓶②口香糖③菜叶④易拉罐⑤果皮,其中属于可回收垃圾的是( )
A..①③④⑤
B.②③⑤
C.①④
D.①④⑤ 名字太长不好潜水1年前1
名字太长不好潜水1年前1 -
 誉寓 共回答了20个问题
誉寓 共回答了20个问题 |采纳率95%①塑料瓶经过回收后可以再加工成塑料瓶,故①正确,
②口香糖经过食用后,变成了其他的东西,不可再进行回收,故②错误,
③菜叶不具有回收的价值,故③错误,
④易拉罐经过回收后的金属可以在进行利用,故④正确,
⑤果皮属于不可回收的垃圾,回收的价值相当小,故⑤错误,
故选C.1年前查看全部
- 垃圾处理成为城市建设及可持续性发展的一个重要问题.现在人们已经可以变废为宝:利用垃圾中的可燃物质燃烧发电.研究表明,生活
垃圾处理成为城市建设及可持续性发展的一个重要问题.现在人们已经可以变废为宝:利用垃圾中的可燃物质燃烧发电.研究表明,生活垃圾的平均热值约为6.27×106J/kg.如果利用垃圾作为燃料建立发电厂,每燃烧1t生活垃圾,可以发电240kW•h.那么:
(1)生活垃圾燃烧发电的效率是多少?
(2)请你谈谈对城市建垃圾发电厂的看法,以及你对人们在生活中收集垃圾有何建议. 关卿卿1年前1
关卿卿1年前1 -
 deeptouch 共回答了17个问题
deeptouch 共回答了17个问题 |采纳率88.2%解题思路:(1)已知生活垃圾的平均热值和燃烧的质量,可求释放的能量,产生的电能与释放能量的比值就是目前生活垃圾发电的效率.
(2)建立垃圾发电厂有利于节约能源,清理垃圾同时有利于环境的保护.(1)1t生活垃圾完全燃烧放出的热量为:Q放=mq=1×103kg×6.27×106J/kg=6.27×109J;
1t生活垃圾发出的电能为:W电=240kW•h=240×3.6×106J=8.64×108J;
∴垃圾燃烧发电的效率:η=
W电
Q放×100%=
8.64×108J
6.27×109J×100%≈13.78%
(2)看法:建立垃圾发电厂使能源再次利用,有利于节约能源,又有利于环境保护;
建议:可将垃圾分类回收.
答:(1)生活垃圾发电的效率是13.78%;
(2)建立垃圾发电厂使能源再次利用,有利于节约能源,又有利于环境保护;收集垃圾时将垃圾分类回收.点评:
本题考点: 能量利用效率.
考点点评: 本题主要考查了燃料燃烧的放热计算,能量的利用率的计算以及怎样提高能量的利用率,很具有现实的意义.1年前查看全部
- 作文,(变废为宝)
 breaklove1年前3
breaklove1年前3 -
 烂白菜wa 共回答了23个问题
烂白菜wa 共回答了23个问题 |采纳率78.3%“哎呀,大事不妙,盘子摔坏了!都怪你!”小刚埋怨的说道.咦,这是怎们一回事呢?原来小刚正在完成老师布置的家庭作业:洗碗.
刚端着一铁盘子去……邻居家的小军破门而入,一不小心把小刚抱着的盘子,打碎了两个.小刚正在发泄呢.“可这也不能怪我呀!我又不知道你在洗碗,你说我有什么用呀?”小军没理由的反驳着.“如果你进来敲门的话就不会发生这事!你说怎们办?”小刚急着快要哭出来了.
小军急中生智、绞尽脑汁,终于想出了办法说:“有办法了!”他叫小刚把盘子捡起来,小刚自己暂时还想不出办法.,只好听他的.“拿去吧!”“好,那你再帮我我去拿水彩笔、水彩颜料和调色板!”小军像老板指挥奴隶一样.
没过一会功夫,小刚就把小军需要的东西拿来了.小军先对小刚卖了个关子:“哈哈,让你来见识见识我本人的魔法有多高,哈哈……”
首先小军先在调色板上滴了几滴水,然后把毛笔在上蘸了蘸,其次挤上颜料,又用毛笔在上蘸了一下,便在破碎的盘子上挥笔就画,终于我们的“画家”画好了,一个栩栩如生的鱼诞生在盘子上,小刚看了羡慕极了,也开心地画起来,不知不觉,小刚也画好了.
“我们的杰作不能白画,必须让大人知道我们的天赋(画画).”“有了!我们挂在墙上吧.”“聪明!我们用绳子编成一个麦兜然后把盘子放在里面就行了!”说完他们又齐心协力动起手来!
挂好后,小军和小刚开始欣赏起他们的成绩,心里产生了一种成就感.小军不停的发出赞叹声:“真是变废为宝呀!”小刚随声附和到:“这可真漂亮呀!”
看着这两个画,你知道变废为宝的意思了吧?1年前查看全部
- (2012•肇庆二模)研究CO、NO、NO2等气体的性质,以便消除污染或变废为宝,可以保护环境、节约资源.试运用所学知识
 (2012•肇庆二模)研究CO、NO、NO2等气体的性质,以便消除污染或变废为宝,可以保护环境、节约资源.试运用所学知识,解决下列问题:
(2012•肇庆二模)研究CO、NO、NO2等气体的性质,以便消除污染或变废为宝,可以保护环境、节约资源.试运用所学知识,解决下列问题:
(1)生产水煤气过程中有以下反应:
①C(s)+CO2(g)⇌2CO(g)△H1;
②CO(g)+H2O(g)⇌H2(g)+CO2(g)△H2;
③C(s)+H2O(g)⇌CO(g)+H2(g)△H3;
若平衡表达式为K=
,则它所对应的化学反应方程式是(填序号)______;上述反应△H1、c(H2)•c(CO) c(H2O)
△H2、△H3之间的关系为______.
(2)不同温度下反应②的平衡常数如下表所示.则△H2______ 0(填“<”“>”);在500℃时,把等物质的量浓度的CO和H2O(g)充入反应容器,达到平衡时c(CO)=0.005mol/L、c(H2)=0.015mo/L,则CO的平衡转化率为______.
(3)对反应2NO2(g)⇌N2O4(g)△H<0,在温度为T1、T2时,平衡体系N2O4的体积分数随压强变化曲线如右上图所示.则T1______T2(填“>”或“<”);增大压强,平衡向______反应方向移动;B、C两点的平衡常数B______C(填“>”或“<”).温度/℃ 400 500 800 平衡常数K 9.94 9 1  千年烟囱1年前1
千年烟囱1年前1 -
 4hqkakfdr 共回答了21个问题
4hqkakfdr 共回答了21个问题 |采纳率85.7%解题思路:(1)根据方程式之间的关系结合盖斯定律确定焓变关系;
(2)升高温度,平衡向吸热反应方向移动,根据移动方向和平衡常数的关系判断反应热;
根据平衡常数计算反应的CO的物质的量浓度,再结合转化率公式计算一氧化碳的转化率;
(3)根据温度、压强对该反应的影响分析,化学平衡常数只与温度有关.(1)根据平衡表达式为K=
c(H2)•c(CO)
c(H2O)知,生成物中含有氢气、一氧化碳两种气体,反应物中含有水蒸气,则符合条件的只有③,所以该反应是③;
将方程式①+②得③,所以其焓变得△H1+△H2═△H3(或△H2═△H3-△H1,或△H1═△H3-△H2,
故答案为:③;△H1+△H2═△H3(或△H2═△H3-△H1,或△H1═△H3-△H2;
(2)根据表中数据知,升高温度,化学平衡常数减小,说明平衡向逆反应方向移动,则正反应是放热反应,△H2<0,根据反应方程式中各物质的关系式知,平衡时,c(CO)=0.005mol/L、c(H2)=0.015mo/L,
参加反应的c(CO)=c(H2)=0.015mo/L,一氧化碳的转化率=[0.015mol/L/0.005mol/L+0.015mol/L]×100%=75%,
故答案为:<;75%;
(3)该反应的正反应是放热反应,相同压强下,由C到A,四氧化二氮的体积分数增大,平衡向正反应方向移动,说明温度降低,则T1<T2;该反应的正反应是气体体积减小的可逆反应,增大压强,平衡向正反应方向移动,温度越高,平衡常数越小,所以B>C,
故答案为:<;正;>.点评:
本题考点: 体积百分含量随温度、压强变化曲线;用盖斯定律进行有关反应热的计算;化学平衡常数的含义.
考点点评: 本题考查了外界条件对化学平衡移动的影响、盖斯定律等知识点,这些知识点都是考试热点,会根据反应方程式特点及外界条件来分析解答,难度中等.1年前查看全部
- 为了增强市民环保意识变废为宝,在城市率先实行垃圾分类.通常,绿色箱用来装可回收再利用垃圾,黄色箱用来装不可回收垃圾.以下
为了增强市民环保意识变废为宝,在城市率先实行垃圾分类.通常,绿色箱用来装可回收再利用垃圾,黄色箱用来装不可回收垃圾.以下物质:①废旧报纸 ②废铜线 ③一次性塑料盒 ④口香糖 ⑤果皮 ⑥空矿泉水瓶 ⑦废铁锅,能扔进绿色垃圾箱的是( )
A.①③⑤⑦
B.③④⑤⑥
C.①②⑥⑦
D.①②③⑥⑦ ll的记忆1年前1
ll的记忆1年前1 -
 yangqiuxia 共回答了23个问题
yangqiuxia 共回答了23个问题 |采纳率82.6%解题思路:在某些市区街道,我们会看到绿色、黄色、红色的垃圾箱,其中,绿色的是投放可回收垃圾的,黄色的为不可回收垃圾,红色的投放有毒有害垃圾.不同颜色的垃圾箱分级回收不同种类的垃圾.例如:(1)不可回收垃圾:主要是厨房垃圾,包括果皮、菜皮、剩饭菜等;(2)可回收垃圾:纸类、塑料、橡胶、金属、玻璃等;(3)有毒有害垃圾:电池、荧光灯管、水银温度计、油漆桶、药品、化装品等绿色垃圾箱用来回收再利用垃圾,可回收再利用的垃圾包括了纸类、塑料、橡胶、金属、玻璃等.所以,废旧报纸、废铜丝、空矿泉水瓶、废铁锅,是属于可回收垃圾.
能放入绿色垃圾箱的是①②③⑥⑦.
故选D.点评:
本题考点: "三废"处理的必要性和一般原则.
考点点评: 此题是与环保相关的试题,是中考的热门考点.通过试题,让学生掌握垃圾分类的相关知识,有利学生树立垃圾分类的观念,提高环保意识1年前查看全部
- 东风汽车公司冲压厂冲压汽车零件的废料都是等腰三角形的小钢板,如图,其中AB=AC,该冲压厂为了降低汽车零件成本,变废为宝
东风汽车公司冲压厂冲压汽车零件的废料都是等腰三角形的小钢板,如图,其中AB=AC,该冲压厂为了降低汽车零件成本,变废为宝,把这些废料再加工成红星农业机械厂粉碎机上的零件,销售给红星农业机械厂,这些零件的形状都是矩形.现在要把如图所示的等腰三角形钢板切割后再焊接成
 两种不同规格的矩形,每种矩形的面积正好等于该三角形的面积,每次切割的次数最多两次(切割的损失可以忽略不计).
两种不同规格的矩形,每种矩形的面积正好等于该三角形的面积,每次切割的次数最多两次(切割的损失可以忽略不计).
(1)请你设计两种不同的切割焊接方案,并用简要的文字加以说明;
(2)若要把该三角形废料切割后焊接成正方形零件(只切割一次),则该三角形需满足什么条件. pantinggirl1年前1
pantinggirl1年前1 -
 ct_流风 共回答了16个问题
ct_流风 共回答了16个问题 |采纳率87.5%解题思路:(1)根据等腰三角形和矩形的性质,可有两种不同的切割焊接方案:a、作△ABC底边BC的高AD,沿AD切割,然后如图焊接即可;b、作等腰△ABC的中位线DE,再作等腰△ADE的高AF,沿DE、AF切割,再按如图焊接即可;
(2)根据正方形的性质可得,该三角形需满足条件是:∠B=∠C=45°(或△ABC是等腰直角三角形或△ABC的高AD=[1/2]BC).(1)规格一:作△ABC底边BC的高AD,如图(a),沿AD切割,然后如图(b)焊接即可;规格二:作等腰△ABC的中位线DE,再作等腰△ADE的高AF,沿DE、AF切割,如图(c),再按如图(d)焊接即可.(2)∠B=∠C=45°(或...
点评:
本题考点: 作图—应用与设计作图.
考点点评: 此题主要考查等腰三角形、矩形和正方形的性质.1年前查看全部
- 右边的漫画主要体现了 变废为宝 [ ] A.辩证否定的实质是既克服又保留
右边的漫画主要体现了 
变废为宝[ ]A.辩证否定的实质是既克服又保留
B.量变达到一定程度就会引起质变
C.矛盾主次方面在一定条件下相互转化
D.主次矛盾在一定条件下可以相互 ppbbtv1年前1
ppbbtv1年前1 -
 wfjdpx 共回答了19个问题
wfjdpx 共回答了19个问题 |采纳率89.5%C1年前查看全部
- 化学家在当今环境问题上的最新构想是“变废为宝,资源循环”.例如,燃料(1)燃烧燃烧产物(2)太阳能或生物能燃料,这样既可
化学家在当今环境问题上的最新构想是“变废为宝,资源循环”.例如,燃料
燃烧产物(1)燃烧
燃料,这样既可解决能源问题,又能消除污染.上述构想中两个转化过程的变化( )(2)太阳能或生物能
A.均为物理变化
B.(1)为物理变化,(2)为化学变化
C.均为化学变化
D.(1)为化学变化,(2)为物理变化 Fancesom1年前1
Fancesom1年前1 -
 思吉 共回答了8个问题
思吉 共回答了8个问题 |采纳率87.5%解题思路:有新物质生成的变化叫化学变化,没有新物质生成的变化叫物理变化.化学变化的特征是:有新物质生成.判断物理变化和化学变化的依据是:是否有新物质生成.燃料燃烧生成新物质,属于化学变化,燃烧产物通过光合作用得到新燃料,也属于化学变化.A、没有新物质生成的变化叫物理变化,燃料燃烧生成新物质,燃烧产物通过光合作用得到新燃料,都属于化学变化,故选项错误;
B、燃料燃烧生成新物质,属于化学变化,不是物理变化;燃烧产物通过光合作用得到新燃料,也属于化学变化,故选项错误;
C、燃料燃烧生成新物质,属于化学变化,燃烧产物通过光合作用得到新燃料,也属于化学变化,故选项正确;
D、燃料燃烧生成新物质,属于化学变化,燃烧产物通过光合作用得到新燃料,也属于化学变化,不是物理变化,故选项错误;
故选C点评:
本题考点: 化学变化和物理变化的判别.
考点点评: 本考点考查了物理变化和化学变化的区别,基础性比较强,只要抓住关键点:是否有新物质生成,问题就很容易解决.本考点主要出现在选择题和填空题中.1年前查看全部
- 为增强市民环保意识,变废为宝,人们正逐渐采用垃圾分类回收.在某些市区街道的垃圾箱中,绿色箱用来装可回收再利用垃圾,黄色箱
为增强市民环保意识,变废为宝,人们正逐渐采用垃圾分类回收.在某些市区街道的垃圾箱中,绿色箱用来装可回收再利用垃圾,黄色箱用来装不可回收的垃圾.以下能放入绿色垃圾箱的是( )
①废旧报纸;②废铜丝;③一次性塑料餐盒;④口香糖;⑤果皮;⑥空矿泉水瓶;⑦废铁锅A.①③⑤⑦ B.③④⑤⑥ C.①②⑤⑦ D.①②⑥⑦  200012081年前1
200012081年前1 -
 niannian520025 共回答了21个问题
niannian520025 共回答了21个问题 |采纳率90.5%绿色垃圾箱用来回收再利用垃圾,可回收再利用的垃圾包括了纸类、塑料、橡胶、金属、玻璃等.所以,废旧报纸、废铜丝、空矿泉水瓶、废铁锅,是属于可回收垃圾.
能放入绿色垃圾箱的是①②⑥⑦.
故选D.1年前查看全部
- 废电池处理不当不仅会造成浪费,还会对环境造成严重污染,对人体健康也存在极大的危害。有同学想变废为宝,他的以下想法你认为不
废电池处理不当不仅会造成浪费,还会对环境造成严重污染,对人体健康也存在极大的危害。有同学想变废为宝,他的以下想法你认为不正确的是 [ ]A.把锌皮取下洗净,用于实验室制氢气
B.碳棒取出洗净,用做电极
C.把铜帽取下洗净,回收利用
D.电池内部填有NH 4 Cl等化学物质,将废电池中的黑色糊状物当做化肥用 freeboy_tai1年前1
freeboy_tai1年前1 -
 huisaisi 共回答了19个问题
huisaisi 共回答了19个问题 |采纳率94.7%D1年前查看全部
- (2014•枣庄二模)某工业酸性废液中含有大量的Cu2+、Fe2+、Fe3+、Cl-等离子,变废为宝,从废液中回收铜并将
(2014•枣庄二模)某工业酸性废液中含有大量的Cu2+、Fe2+、Fe3+、Cl-等离子,变废为宝,从废液中回收铜并将铁的化合物全部转化为FeCl3溶液再利用.其流程如下:

请回答下列有关问题:
(1)试剂①最好选用______.
a、Na2O2 b、Cl2 c、HNO3 d、KMnO4
(2)在该酸性废液中加入过量铁粉先后发生______个化学反应,请写出第二阶段反应的离子方程式______.
(3)简述检验混合物A中是否含有Fe3+______.
(4)加入试剂②至得到纯铜所需要的基本操作有______. echo98021年前1
echo98021年前1 -
 cdxsjsw 共回答了31个问题
cdxsjsw 共回答了31个问题 |采纳率87.1%解题思路:从废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用,则废液中加过量Fe粉,混合物A为FeCl2、Fe和Cu等混合物,过滤滤渣为Fe和Cu,滤渣中加过量盐酸,因Cu与盐酸不反应,则滤液为FeCl2,将滤液中通入氯气可反应得到FeCl3溶液,然后结合实验过程及化学用语来解答.从废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用,则废液中加过量Fe粉,混合物A为FeCl2、Fe和Cu等混合物,过滤滤渣为Fe和Cu,滤渣中加过量盐酸,因Cu与盐酸不反应,则滤液为FeCl2,将滤液中通入氯气可反应得到FeCl3溶液,
(1)加入试剂①,可氧化FeCl2得到FeCl3,为避免引入新杂质,可通入氯气,故答案为:b;
(2)酸性废液中含有大量的Cu2+、Fe2+、Fe3+、Cl-等离子,加入过量Fe粉,因氧化性:Fe3+>Cu2+>H+,
可分别以此发生:2Fe3++Fe=3Fe2+、Cu2++Fe=Fe2++Cu、2H++Fe=Fe2++H2↑等,第二阶段反应的离子方程式为Cu2++Fe=Fe2++Cu,
故答案为:3;Cu2++Fe=Fe2++Cu;
(3)一般离子KSCN溶液来检验铁离子,实验操作为取少量混合物A于试管中,滴加几滴KSCN溶液,溶液不变红色,则证明原溶液中不含有Fe3+,
故答案为:取少量混合物A于试管中,滴加几滴KSCN溶液,溶液不变红色,证明无Fe3+;
(4)试剂②为盐酸,可与铁反应,反应后过滤、洗涤、干燥,可得到铜,故答案为:溶解、过滤、洗涤、干燥.点评:
本题考点: 物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题以实验的形式考查混合物的分离、提纯,注意发生的化学反应及元素守恒的角度来分析是解答本题的关键,(3)为学生解答的易错点和难点,题目难度中等.1年前查看全部
- 能否告诉我生活中几个变废为宝的例子,谢谢!
 zhouwei2251年前4
zhouwei2251年前4 -
 C236714199 共回答了23个问题
C236714199 共回答了23个问题 |采纳率91.3%喝完的饮料瓶用来插花
用塑料杯做挂饰、灯笼
洗米水浇花1年前查看全部
- “人类只有一个地球!”为了保护人类赖以生存的环境,下列做法不正确是 A.回收处理垃圾,变废为宝 B.农作物收割后留下大量
“人类只有一个地球!”为了保护人类赖以生存的环境,下列做法不正确是
A.回收处理垃圾,变废为宝 B.农作物收割后留下大量秸秆可作为垃圾就地焚烧 C.逐步减少使用化石燃料 D.开发新能源  gt54881年前1
gt54881年前1 -
 hurry510 共回答了15个问题
hurry510 共回答了15个问题 |采纳率93.3%B
A、回收处理垃圾,可以变废为宝,保护环境,节约资源,故选项说法正确;
B、农作物收割后留下大量秸秆就地焚烧,可产生大量的空气污染物,污染环境,故选项说法错误;
C、逐步减少使用化石燃料,能减少环境污染,故选项说法正确;
D、开发新能源,逐步减少使用化石燃料,能减少环境污染,故选项说法正确;1年前查看全部
- 大的矿泉水瓶子如何变废为宝
 杠杠zhk1年前2
杠杠zhk1年前2 -
 lily665 共回答了15个问题
lily665 共回答了15个问题 |采纳率80%可做成笔筒、餐具筒 然后可以在瓶盖上扎一些孔做饭时洒调料(避免放多)还可以把瓶子的底部适当剪掉一块儿做成小铲子
还可做成塑料花蓝,1年前查看全部
- 当今化学家在环境问题上的最新构想是:“变废为宝,实现物质资源的循环。”例如:CH 4 、CH 3 OH 燃烧产物(CO
当今化学家在环境问题上的最新构想是:“变废为宝,实现物质资源的循环。”例如:CH 4 、CH 3 OH  燃烧产物(CO 2 、H 2 O)
燃烧产物(CO 2 、H 2 O) 燃料(CH 4 、CH 3 OH等),此构想一旦实现,既能解决能源问题的危机,又能达到消除大气污染的目的。此构想中两个转化过程的变化为:
燃料(CH 4 、CH 3 OH等),此构想一旦实现,既能解决能源问题的危机,又能达到消除大气污染的目的。此构想中两个转化过程的变化为:[ ]
A.①为物理变化 ②为化学变化
B.②为物理变化 ①为化学变化
C.均为物理变化
D.均为化学变化 冻结41年前1
冻结41年前1 -
 妙dd心 共回答了30个问题
妙dd心 共回答了30个问题 |采纳率90%D1年前查看全部
- 生活中你如何变废为宝?
 金属狂云1年前1
金属狂云1年前1 -
 ruiwang 共回答了20个问题
ruiwang 共回答了20个问题 |采纳率75%自己做到力所能及的事
如:书,纸,报纸,纸包装盒等,都可以收集在一起,可以卖给收废品的,我们可以得一点坐公车的钱,他们则可以让纸品循环利用.
一次性的塑料杯子,饮料瓶,超市用的那种便利袋,易拉罐,也是可以变卖的.
再有废旧家电,胶底鞋,破铜烂铁都可以卖出.
用完了的电池不能乱丢,会污染环境,应该集中放进电池回收箱.
旧衣服可以捐给贫困地区,或剪开做抹布,拖地也行.物尽其用.
喝完了的茶叶晒干可以做枕芯,可以除湿,可以做柴火烧.
各种坚果皮都可以烧,像我们这边做腊肉,这是熏肉最好的材料了
剩饭菜可以做花肥.1年前查看全部
- 化学家在当今环境问题上的最新构想是“变废为宝,资源循环”.
化学家在当今环境问题上的最新构想是“变废为宝,资源循环”.
例如:燃料(CH 4 、CH 3 OH等)、燃烧产物(CO 2 、H 2 O等)、燃料①燃烧
(CH 4 、CH 3 OH等),这样既可解决能源问题,又能消除污染.上述构想中的①、②两个转化过程的变化为( )②太阳能或生物能 A.均为物理变化 B.①为物理变化,②为化学变化 C.①为化学变化,②为物理变化 D.均为化学变化  喜欢女孩的数学1年前1
喜欢女孩的数学1年前1 -
 四处溜达的可卡 共回答了17个问题
四处溜达的可卡 共回答了17个问题 |采纳率100%燃料燃烧生成水和二氧化碳,属于化学变化;水和二氧化碳在太阳能或生物能的作用下生成甲烷、甲醇等,属于化学变化.
故选D.1年前查看全部
- 为了增强市民的环保意识,变废为宝,我市已实施垃圾分类回收.生活垃圾一般分为三类:可回收垃圾、不可回收垃圾和有害垃圾.现有
 为了增强市民的环保意识,变废为宝,我市已实施垃圾分类回收.生活垃圾一般分为三类:可回收垃圾、不可回收垃圾和有害垃圾.现有如下垃圾:①矿泉水瓶②口香糖③菜叶④易拉罐⑤果皮,其中属于可回收垃圾的是( )
为了增强市民的环保意识,变废为宝,我市已实施垃圾分类回收.生活垃圾一般分为三类:可回收垃圾、不可回收垃圾和有害垃圾.现有如下垃圾:①矿泉水瓶②口香糖③菜叶④易拉罐⑤果皮,其中属于可回收垃圾的是( )
A..①③④⑤
B.②③⑤
C.①④
D.①④⑤ ww一个人1年前1
ww一个人1年前1 -
 爱车111 共回答了17个问题
爱车111 共回答了17个问题 |采纳率94.1%①塑料瓶经过回收后可以再加工成塑料瓶,故①正确,
②口香糖经过食用后,变成了其他的东西,不可再进行回收,故②错误,
③菜叶不具有回收的价值,故③错误,
④易拉罐经过回收后的金属可以在进行利用,故④正确,
⑤果皮属于不可回收的垃圾,回收的价值相当小,故⑤错误,
故选C.1年前查看全部
- 为了变废为宝,控制温室效应,工业上可用CO 2 来生产甲醇。一定条件下发生如下反应:CO 2 (g)+3H 2 (g)
为了变废为宝,控制温室效应,工业上可用CO 2 来生产甲醇。一定条件下发生如下反应:CO 2 (g)+3H 2 (g)
 CH 3 OH(g)+H 2 O(g)。如图表示该反应进行过程中能量(单位为kJ·mol -1 )的变化。在体积为1 L的恒容密闭容器中,充入1 mol CO 2 和3 mol H 2 ,下列措施中不能使c(CH 3 OH)增大的是
CH 3 OH(g)+H 2 O(g)。如图表示该反应进行过程中能量(单位为kJ·mol -1 )的变化。在体积为1 L的恒容密闭容器中,充入1 mol CO 2 和3 mol H 2 ,下列措施中不能使c(CH 3 OH)增大的是
A.降低温度 B.充入He(g),使体系压强增大 C.将H 2 O(g)从体系中分离出来 D.再充入1 mol CO 2 和3 mol H 2  cavenchow1年前1
cavenchow1年前1 -
 tancheng0627 共回答了18个问题
tancheng0627 共回答了18个问题 |采纳率88.9%B
根据图所给的信息知,该反应是放热反应,A、C、D项的操作都可使平衡向正向移动,c(CH 3 OH)增大,充入不参加反应的氦气,没有改变体系中各物质的浓度,平衡不移动,c(CH 3 OH)不变。1年前查看全部
- 2014年1月19日,我省举办节能减排暨建筑垃圾回收利用论坛,支招建筑垃圾“变废为宝”.建筑垃圾中废塑料、废橡胶制品属于
2014年1月19日,我省举办节能减排暨建筑垃圾回收利用论坛,支招建筑垃圾“变废为宝”.建筑垃圾中废塑料、废橡胶制品属于( )
A.金属材料
B.有机合成材料
C.无机非金属材料
D.复合材料 仙兔1年前1
仙兔1年前1 -
 废话可以少说两句 共回答了21个问题
废话可以少说两句 共回答了21个问题 |采纳率90.5%解题思路:根据已有的知识进行分析,塑料、合成橡胶属于有机合成材料,据此解答.塑料、合成橡胶属于有机合成材料,观察选项,故选B.
点评:
本题考点: 合成材料的使用及其对人和环境的影响.
考点点评: 本题考查了常见材料的类别,完成此题,可以依据其成分进行.1年前查看全部
- (2011•营口)现代社会,“变废为宝”已成为节约能源的重要途径,例如“填埋”和“焚烧”垃圾都可发电,这样既处理了垃圾,
(2011•营口)现代社会,“变废为宝”已成为节约能源的重要途径,例如“填埋”和“焚烧”垃圾都可发电,这样既处理了垃圾,又起到了节能减排的效果.经研究表明每焚烧1t垃圾可发电8.1×108J.请同学们计算一下1t垃圾发电产生的这些能量
(1)相当于完全燃烧多少kg的汽油放出的热量?(汽油的热值q=3×107J/kg)
(2)可使效率为30%的汽车匀速前进多少km?(汽车匀速前进受到的摩擦力f=648N)
(3)如果这些能量全部被水吸收,可将多少kg10℃的水烧开?[c水=4.2×103J/(kg•℃)在一个标准大气压下.结果保留整数]. xtayfjppygl1年前1
xtayfjppygl1年前1 -
 鑫岩 共回答了18个问题
鑫岩 共回答了18个问题 |采纳率94.4%解题思路:(1)知道1t垃圾发电产生的能量W电,利用Q放=mq=W电求汽油的质量;
(2)因为汽车匀速前进,所以汽车的牵引力等于阻力,又知道W=30%×Q放,利用功的公式求汽车前进的距离;
(3)由题知,垃圾产生的能量全部被水吸收,即Q吸=Q放,知道水的比热容、水的初温和末温,利用Q吸=cm水(t-t0)=Q放求水的质量.(1)由题知,Q放=W电=8.1×108J,
而Q放=mq,
∴汽油的质量:
m=
Q放
q=
8.1×108J
3×107J/kg=27kg;
(2)∵汽车匀速前进,
∴F=f=648N,
由题知,W=Fs=30%×Q放=30%×8.1×108J=2.43×108J,
∴s=[W/F]=
2.43×108J
648N=375000m=375km;
(3)由题知,垃圾产生的能量全部被水吸收,即Q吸=Q放=8.1×108J,
∵Q吸=cm水(t-t0),
∴m水=
Q吸
c(t−t0)
=
8.1×108J
4.2×103J/(kg•℃)×(100℃−10℃)
=2143kg.
答:(1)相当于完全燃烧27kg的汽油;
(2)可供汽车匀速前进375km;
(3)能把2143kg的10℃的水烧开.点评:
本题考点: 热量的计算;密度公式的应用;燃料的热值.
考点点评: 本题考查了学生对吸热公式、功的公式、燃料完全燃烧放热公式的掌握和运用,知识点多、综合性强,计算时要求灵活运用公式.1年前查看全部
- 如何将废干电池变废为宝?
 欲残阳1年前1
欲残阳1年前1 -
 哭泣的拉面 共回答了18个问题
哭泣的拉面 共回答了18个问题 |采纳率94.4%电池头部用小钉钉3个洞,加点盐,然后用蜡封住,可以用久一点…
用小电流充一下电池,也可以缓解电量,不过有点危险哦
楼主精神可嘉,赞!1年前查看全部
- 某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+.为了减少污染并变废为宝,某化学兴趣小组设计如下流程
某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+.为了减少污染并变废为宝,某化学兴趣小组设计如下流程图从该废水中回收硫酸亚铁和金属铜.

请回答下列问题:
(1)填写下列试剂的化学式A______,D______;
(2)操作Ⅰ、Ⅱ在实验室中所用的玻璃仪器是______;
(3)操作Ⅲ的名称是______;
(4)硫酸亚铁晶体(FeSO4•7H2O)易变质,请设计一个简单实验证明硫酸亚铁晶体没有变质______. gaintcross1年前1
gaintcross1年前1 -
 rfvan 共回答了19个问题
rfvan 共回答了19个问题 |采纳率78.9%解题思路:某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+,先加过量铁(A),过滤,得到C溶液为FeSO4,B为Cu和多余的铁,再向B中加过量稀硫酸,过滤得到的E为Cu,F为FeSO4;
(1)根据以上分析判断;
(2)操作Ⅰ、Ⅱ为过滤;
(3)从FeSO4溶液中提取溶质晶体采用蒸发结晶;
(4)亚铁离子变质会生成铁离子,根据检验铁离子的方法分析.某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+,先加过量铁(A),过滤,得到C溶液为FeSO4,B为Cu和多余的铁,再向B中加过量稀硫酸,过滤得到的E为Cu,F为FeSO4,
(1)根据以上分析可知A为铁粉,D为稀硫酸,故答案为:Fe,H2SO4;
(2)操作Ⅰ、Ⅱ为过滤,过滤时使用的玻璃仪器有漏斗、玻璃棒、烧杯,故答案为:漏斗、玻璃棒、烧杯;
(3)操作Ⅲ是从FeSO4溶液中提取溶质晶体采用蒸发结晶,故答案为:蒸发结晶;
(4)亚铁离子变质会生成铁离子,检验铁离子一般用硫氰化钾溶液,其操作为:取少量固体于试管中,加水溶解,再加入了硫氰化钾溶液,不变红色,证明没有变质;如果变红色,证明已经变质了;
故答案为:取少量固体于试管中,加水溶解,再加入了硫氰化钾溶液,不变红色,证明没有变质;如果变红色,证明已经变质了.点评:
本题考点: 金属的回收与环境、资源保护.
考点点评: 本题考查了工艺流程图的分析判断,解答本题要充分理解各种物质的性质,从而得出正确的结论,应熟悉混合物的分离方法,掌握过滤和蒸发结晶分离方法的使用条件及实验操作,题目难度中等.1年前查看全部
- 化学练习册上的一个燃料→(燃烧)燃烧产物→(太阳能或生物能)→燃料原题是当今环境问题上较为理想的构想是‘变废为宝资源循环
化学练习册上的一个
燃料→(燃烧)燃烧产物→(太阳能或生物能)→燃料
原题是
当今环境问题上较为理想的构想是‘变废为宝资源循环’如 燃料(燃烧)→燃烧产物(太阳能或生物能)→燃料。这样既可以解决能源问题,又能消除污染。
呵呵,最上面的式子确实有点问题 fdgdhfjj1年前3
fdgdhfjj1年前3 -
 xckdfui 共回答了18个问题
xckdfui 共回答了18个问题 |采纳率94.4%燃料指的是煤炭、石油、天然气等物质,燃烧形成燃烧产物不用解释,所谓的燃烧产物包括水、二氧化碳以及一些矿物质等等,这些物质一方面可以通过植物经过光合作用(比如水和二氧化碳作原料,矿物质作化肥)形成植物本身的一部分(煤炭、石油就是通过植物、动物的尸体形成的),一方面一些微生物能够将燃烧产物中的物质转化为沼气等等,生成的植物、化石、沼气都可以作为燃料,于是便有了这个循环过程1年前查看全部
- (2012•惠安县质检)某化工厂的废液里含有大量的硝酸银.为了防止废液污染环境,变废为宝,进行如下处理:
(2012•惠安县质检)某化工厂的废液里含有大量的硝酸银.为了防止废液污染环境,变废为宝,进行如下处理:
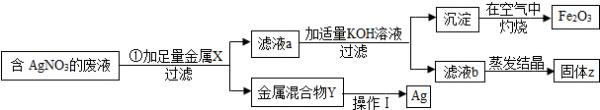
请回答:
(1)金属X是______(填化学式),加入过量金属X的目的是______.
(2)步骤①中反应的化学方程式为______.
(3)请简述操作Ⅰ的实验方法:______.
(4)固体Z在农业生产中是一种化学肥料,它属于______(填标号)
a.氮肥b.磷肥c.钾肥d.复合肥. gto211721年前1
gto211721年前1 -
 灵魂在等待 共回答了19个问题
灵魂在等待 共回答了19个问题 |采纳率84.2%解题思路:(1)在金属活动性顺序中,位置在前的金属能把位于其后的金属从其盐溶液中置换出来.根据题意,产物中得到含铁的物质.说明加入的较活泼的金属是铁,据此分析回答有关的问题;
(2)根据铁与硝酸银的反应,写出反应的方程式;
(3)根据铁能被磁铁吸附分析;
(3)根据固体Z含有的农作物需要的营养元素分析.由题意可知,产物中得到含铁的物质,说明加入的较活泼的金属是铁.含硝酸银的废液加足量的铁粉后,铁与硝酸银反应生成银和硝酸亚铁,过滤得到金属是铁、银的混合物,利用磁铁吸附可以将铁吸附掉,得到了银.在滤液中加入适量氢氧化钾溶液,氢氧化钾与硝酸亚铁反应生成氢氧化亚铁沉淀和硝酸钾,过滤后的滤液b中含有硝酸钾,蒸发结晶析出硝酸钾;硝酸钾中含有钾、氮元素,是一种复合肥.由以上分析可知:
(1)金属X是Fe 加入过量铁的目的是:将硝酸银中的银全部置换出来;
(2)铁与硝酸银反应的化学方程式为:Fe+2AgNO3═Fe(NO3)2+2Ag;
(3)操作Ⅰ的实验方法:利用磁铁吸附铁,剩余的是银;
(4)由于固体Z是硝酸钾,含有钾、氮两种元素,属于复合肥.
故答为:(1)Fe,将硝酸银中的银全部置换出来;(2)Fe+2AgNO3═Fe(NO3)2+2Ag;(3)利用磁铁吸附铁,剩余的是银;(4)d.点评:
本题考点: 金属活动性顺序及其应用;常见化肥的种类和作用.
考点点评: 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.1年前查看全部
- 下列说法没有科学尤其是化学依据的是( ) A.点石成金 B.变废为宝 C.塑料回收 D.资源再生
 yaansky1年前1
yaansky1年前1 -
 非凡的爱斯基摩人 共回答了16个问题
非凡的爱斯基摩人 共回答了16个问题 |采纳率100%A、根据质量守恒定律,参加反应前的物质是“石”,没有金元素,反应后也不可能产生金.故A适合;
B、每个家庭都有许多旧物品,这些物品往往成为鸡肋,扔之可惜,留着又没地方.我们充分发挥自己的想像力,把它们利用起来,可以变废为宝.故B不适合;
C、塑料回收既可废物利用,又保护了环境.故C不适合;
D、资源再生是指生产和消费过程中产生的废物作为资源加以回收利用.借助这一方法,所有的原料和能源将在原料资源、生产、消费、二次原料资源的循环中得到最合理的利用,同时不致破坏环境.故D不适合.
故选A.1年前查看全部
- 生活中的哪些东西可以变废为宝?实用的,常见的.
 萧萧糖1年前1
萧萧糖1年前1 -
 清洁工2号 共回答了16个问题
清洁工2号 共回答了16个问题 |采纳率68.8%矿泉水瓶可以剪掉上半部分后,用下半部分做刷牙缸,上半部分可以用来当简易漏斗.1年前查看全部
- 现代社会,“变废为宝”已成为节约能源的重要途径,例如将垃圾“焚烧”可以发电,这样既处理了垃圾,又起到了节能减排的效果.经
现代社会,“变废为宝”已成为节约能源的重要途径,例如将垃圾“焚烧”可以发电,这样既处理了垃圾,又起到了节能减排的效果.经研究表明每焚烧1t垃圾可放出热量8.4×108J.请同学们计算一下1t垃圾焚烧产生的这些能量
(1)相当于完全燃烧多少kg的汽油放出的热量?(汽油的热值q=3×107J/kg)
(2)可使效率为30%的汽车匀速前进多少km?(汽车匀速前进受到的摩擦力f=1680N)
(3)如果这些能量全部被水吸收,可将多少kg20℃的水在一个标准大气压下烧开?[c水=4.2×103 J/(kg•℃)]. 52140091年前1
52140091年前1 -
 AHTC2006 共回答了21个问题
AHTC2006 共回答了21个问题 |采纳率90.5%解题思路:(1)知道1t垃圾发电产生的能量W电,利用Q放=mq=W电求汽油的质量;
(2)因为汽车匀速前进,所以汽车的牵引力等于阻力,又知道W=30%×Q放,利用功的公式求汽车前进的距离;
(3)由题知,垃圾产生的能量全部被水吸收,即Q吸=Q放,知道水的比热容、水的初温和末温,利用Q吸=cm水(t-t0)=Q放求水的质量.(1)由题知,Q放=W电=8.4×108J,
∵Q放=mq,
∴汽油的质量:
m=
Q放
q=
8.4×108J
3×107J/kg=28kg;
(2)∵汽车匀速前进,
∴F=f=1680N,
由题知,W=Fs=30%×Q放=30%×8.4×108J=2.52×108J,
∴s=[W/F]=
2.52×108J
1680N=1.5×105m=150km;
(3)由题知,垃圾产生的能量全部被水吸收,即Q吸=Q放=8.4×108J,
∵Q吸=cm水(t-t0),
∴m水=
Q吸
c(t−t0)=
8.4×108J
4.2×103J/(kg•℃)×(100℃−20℃)=2.5×103kg.
答:(1)相当于完全燃烧28kg的汽油;
(2)可供汽车匀速前进150km;
(3)能把2.5×103kg的20℃的水烧开.点评:
本题考点: 热平衡方程的应用;功的计算公式的应用.
考点点评: 本题考查了学生对吸热公式、功的公式、燃料完全燃烧放热公式的掌握和运用,知识点多、综合性强,计算时要求灵活运用公式.1年前查看全部
- 为了增强市民的环保意识,变废为宝,去年年底我市在全区率先实行垃圾分类回收。市区街道的垃圾箱中,绿色箱用来装可回收再利用垃
为了增强市民的环保意识,变废为宝,去年年底我市在全区率先实行垃圾分类回收。市区街道的垃圾箱中,绿色箱用来装可回收再利用垃圾,黄色箱用来装不可回收垃圾。以下物质能扔进绿色垃圾箱的是 ①废旧报纸 ②废铜丝 ③一次性塑料饭盒 ④口香糖 ⑤果皮 ⑥空矿泉水瓶 ⑦废铁锅 [ ]A .①③⑤⑦
B .③④⑤⑥
C .①②⑤⑦
D .①②⑥⑦ 一只猫1年前1
一只猫1年前1 -
 mopychen 共回答了23个问题
mopychen 共回答了23个问题 |采纳率95.7%D1年前查看全部
- 目前工业上有一种用CO 2 来生产燃料甲醇的方法,可以将CO 2 变废为宝。
目前工业上有一种用CO 2 来生产燃料甲醇的方法,可以将CO 2 变废为宝。
(1)已知在常温常压下:
①2CH 3 OH(l)+3O 2 (g)= 2CO 2 (g)+4H 2 O(g) △H= _ 1275.6 kJ·mol -1
②2CO(g)+ O 2 (g)= 2CO 2 (g)△H= _ 556.0 kJ·mol -1
③H 2 O(l) = H 2 O(g) △H="+" 44.0 kJ·mol -1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式 。
(2)某同学利用甲醇燃料电池为电源,设计了一种电解法制取Fe(OH) 2 的实验装置(如图),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。则电源中a极为 极(填“正”或“负”),其电极反应式为 。装置上端A极电极材料是 (填化学式),B电极上的电极反应式为 。
(3)将不同量的CO(g)和H 2 O(g)分别通入体积为2L的恒容密闭容器中,进行反应:CO(g) +H 2 O(g) CO 2 (g) + H 2 (g),得到如下三组数据:
CO 2 (g) + H 2 (g),得到如下三组数据:实验组 温度/℃ 起始量/mol 平衡量/mol 达到平衡所需时间/min H 2 O CO CO 2 1 650 2 4 1.6 5 2 900 1 2 0.4 3 3 900 1 2 0.4 1
①该反应的正反应为 (填“吸”或“放”)热反应。
②实验1中,以v(H 2 )表示的平均反应速率为可能相似的问题-
1年前1个回答
你能帮帮他们吗
Copyright © 2022 YULUCN.COM - 雨露学习互助 - 17 q. 0.056 s. - webmaster@yulucn.com 萍水难相逢1年前1
萍水难相逢1年前1 -
 仇二爷 共回答了16个问题
仇二爷 共回答了16个问题 |采纳率81.3%(1)CH 3 OH(l)+ O 2 (g)=" CO" (g)+2H 2 O(l) △H= _ 447.8 kJ·mol -1 (2分);
(2)正(1分),O 2 +4e - +2H 2 O=4OH -1年前查看全部
- 某化学兴趣小组在刷洗试管时,用力过猛,造成试管底被穿通,留下圆形小孔.在老师的启发下,兴趣小组变废为宝.将细铜丝揉成小球
 某化学兴趣小组在刷洗试管时,用力过猛,造成试管底被穿通,留下圆形小孔.在老师的启发下,兴趣小组变废为宝.将细铜丝揉成小球垫在试管底部,配上带单孔橡皮塞的导管和烧杯,装配了一个在实验室制取气体的装置,如图所示.
某化学兴趣小组在刷洗试管时,用力过猛,造成试管底被穿通,留下圆形小孔.在老师的启发下,兴趣小组变废为宝.将细铜丝揉成小球垫在试管底部,配上带单孔橡皮塞的导管和烧杯,装配了一个在实验室制取气体的装置,如图所示.
(1)若用此装置制取二氧化碳,在试管内的铜丝球上方应盛放块状______ (填药品名称,下同),发生反应的化学方程式______;若用此装置制取氢气.在试管内的铜丝球上方应盛放______发生反应的化学方程式______.
(2)制备气体之前,都必须要捡查装置的气密性.写出你检查该装置气密性的方法:______.
(3)若用过氧化氢溶液和二氧化锰粉末制取氧气,能不能使用该装置______(填“能”或“不能”),说明你的理由:______. ldj01021年前1
ldj01021年前1 -
 wt7658 共回答了24个问题
wt7658 共回答了24个问题 |采纳率95.8%解题思路:(1)根据二氧化碳的制取就是固体大理石(或石灰石)和液体稀盐酸的反应,可判断在试管内的铜丝球上方应盛放的物质;根据反应物和生成物,即可写出化学反应式.
(2)检查装置的气密性装置气密性检验有多种方法,原理都是根据装置内外的压强差形成水柱或气泡,据此分析即可.
(3)根据反应物的状态来分析.(1)由于此题很大的变化是“试管底部有了一个小孔”;
所以试管不能用来盛液体,但是可以用来放置固体大理石或锌粒,然后用单孔橡皮塞塞住,将整体放入酸中,即可控制反应速度.
二氧化碳的制取就是固体大理石(或石灰石)和液体稀盐酸的反应,可知在干燥管内的铜网上应盛放的物质是大理石(或石灰石);
故反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
氢气的制取就是固体锌粒和液体稀盐酸或稀硫酸的反应,可知在试管内的铜网上应盛放的物质是锌粒;
故反应的化学方程式为:Zn+2HCl=ZnCl2+H2↑.
(2)检查装置气密性的原理都是根据装置内外的压强差形成水柱或气泡;
故该装置检查气密性的方法是:关闭止水夹(或用手指堵住导管),将通底试管插入水中,观察试管内的液面是否缓慢上升(或将试管通底部分浸入水中,再用手握试管,观察通底处是否有气泡冒出).
(3)因为二氧化锰是一种粉末状药品,所以不能用此装置来制取氧气.
故答案为:
(1)石灰石(或大理石);CaCO3+2HCl=CaCl2+H2O+CO2↑;锌粒;Zn+2HCl=ZnCl2+H2↑.
(2)关闭止水夹(或用手指堵住导管),将通底试管插入水中,观察试管内的液面是否缓慢上升(或将试管通底部分浸入水中,再用手握试管,观察通底处是否有气泡冒出).
(3)不能;因为二氧化锰是粉末状的.点评:
本题考点: 二氧化碳的实验室制法;实验室制取氧气的反应原理;氢气的制取和检验;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查实验装置的选取和化学反应式的书写,属于基础知识范畴,只要同学们能细心就可做好此题.特别注意检查装置的气密性必须是在密闭装置中.1年前查看全部
- (2013•济南一模)目前工业上有一种用CO2来生产燃料甲醇的方法,可以将CO2变废为宝.
 (2013•济南一模)目前工业上有一种用CO2来生产燃料甲醇的方法,可以将CO2变废为宝.
(2013•济南一模)目前工业上有一种用CO2来生产燃料甲醇的方法,可以将CO2变废为宝.
(1)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=_1275.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H=_556.0kJ•mol-1
③H2O(l)=H2O(g)△H=+44.0kJ•mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式______
(2)某同学利用甲醇燃料电池为电源,设计了一种电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生大量的白色沉淀,且较长时间不变色.则电源中a极为______极(填“正”或“负”),其电极反应式为______.装置上端A极电极材料是______(填化学式),B电极上的电极反应式为______.
(3)将不同量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中,进行反应:CO(g)+H2O(g)⇌CO2(g)+H2(g),得到如下三组数据:
①该反应的正反应为______(填“吸”或“放”)热反应.实验组 温度/℃ 起始量/mol 平衡量/mol 达到平衡所需时间/min H2O CO CO2 1 650 2 4 1.6 5 2 900 1 2 0.4 3 3 900 1 2 0.4 1
②实验1中,以v(H2)表示的平均反应速率为______.
③900℃时,按CO(g)、H2O(g)、CO2(g) 和 H2(g)的物质的量分别是0.8mol、1.0mol、0.6mol和0.8mol分别加入该容器,则此时反应的v(正)______v(逆)(填“>”“<”或“=”中之一).
④实验3跟实验2相比,改变的条件可能是______. bengbu百合静静开1年前1
bengbu百合静静开1年前1 -
 21473126 共回答了18个问题
21473126 共回答了18个问题 |采纳率94.4%解题思路:(1)依据热化学方程式和盖斯定律计算得到;
(2)燃料电池中燃料在负极发生氧化反应依,在正极反应还原反应,依据装置分析判断生成氢氧化亚铁的电极位置和反应原理;
(3)①依据温度变化,平衡时二氧化碳的浓度变化分析判断反应热量变化;
②依据反应速率概念计算得到;
③依据浓度商和平衡常数比较分析判断;
④数据分析,实验3和实验2达到相同的平衡状态,但反应速率加快,达到平衡的时间缩短;反应可能是加入了催化剂或增大压强,因为反应前后气体压强不变;(1)①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=_1275.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H=_556.0kJ•mol-1
③H2O(l)=H2O(g)△H=+44.0kJ•mol-1
依据热化学方程式和盖斯定律①-②-③×4得到CH3OH(l)+O2(g)=CO (g)+2H2O(l)△H=_447.8 kJ•mol-1;
故答案为:CH3OH(l)+O2(g)=CO (g)+2H2O(l)△H=_447.8 kJ•mol-1;
(2)甲醇燃料电池为电源电解法制取Fe(OH)2的实验装置,通电后,溶液中产生大量的白色沉淀,且较长时间不变色,说明氢氧化亚铁在B电极附近生成,所以电极A为电解池的阳极,B为电解池的阴极,电源a为正极,电极反应为氧气得到电子得到电子发生还原反应,O2+4e-+2H2O=4OH-;连接正极的A电极是铁,目的是铁做阳极失电子生成亚铁离子,和阴极生成的氢氧根离子反应生成白色沉淀氢氧化亚铁;b为负极,连接电极B电极反应为:2H++2 e-=H2↑;
故答案为:正,O2+4e-+2H2O=4OH-,Fe,2H++2 e-=H2↑(或2H2O+2e-=H2+2OH-);
(3)①CO(g)+H2O(g)⇌CO2(g)+H2(g),反应前后气体体积不变,起始量减少一半,平衡不动,应平衡时二氧化碳浓度为0.8mol/L,所以依据图表数据可知温度升高平衡状态向逆向进行,说明正反应是放热反应;
故答案为:放;
②CO(g)+H2O(g)⇌CO2(g)+H2(g)
起始量(mol)2 4 0 0
变化量(mol)1.6 1.6 1.61.6
平衡量(mol)0.42.41.61.6
实验1中,以v(H2)表示的平均反应速率=
1.6mol
2L
5min=0.16mol/(L•min);
故答案为:0.16mol/(L•min);
③900°C平衡状态下平衡常数计算为
CO(g)+H2O(g)⇌CO2(g)+H2(g)
起始量(mol) 1 2 00
变化量(mol) 0.4 0.4 0.4 0.4
平衡量(mol)0.6 1.6 0.4 0.4
K=
c(CO2)c(H2)
c(CO)c(H2O)=
0.4mol
2L×
0.4mol
2L
0.6mol
2L×
1.6mol
2L=0.17
按CO(g)、H2O(g)、CO2(g) 和 H2(g)的物质的量分别是0.8mol、1.0mol、0.6mol和0.8mol分别加入该容器
Qc=
c(CO2)c(H2)
c(CO)c(H2O)=
0.6mol
2L×
0.8mol
2L
0.8mol
2L×
1mol
2L=0.6>K
反应逆向进行,v(正)<v(逆)
故答案为:<;
④实验3跟实验2相比,达到相同的平衡状态,反应前后气体体积不变,反应速率增大,说明增大压强或加入催化剂符合,改变的条件可能是使用了催化剂;加大了压强;
故答案为:使用了催化剂;加大了压强;点评:
本题考点: 用盖斯定律进行有关反应热的计算;化学平衡的影响因素;电解原理.
考点点评: 本题考查了热化学方程式和盖斯定律计算应用,原电池,电解池原理分析,化学平衡的分析判断,平衡常数、反应速率的计算应用,题目难度中等.1年前查看全部
- 求数学题过程及答案在学校开展“变废为宝”的活动中,育才中学预备班三个班级的少先队员共收集废电池40千克,其中预备1班收集
求数学题过程及答案
在学校开展“变废为宝”的活动中,育才中学预备班三个班级的少先队员共收集废电池40千克,其中预备1班收集废电池的千克数占总数的25%,且男生与女生收集废电池的千克数之比为3:7,问预备1班男女各收集废电池多少千克?
 damon21191年前1
damon21191年前1 -
 samuelgod 共回答了23个问题
samuelgod 共回答了23个问题 |采纳率87%第一步算出1班收集了的电池数为40*25%=10千克
男生收集电池数位3/(3+7)=3/10
则男生收了10*3/10=3千克
那么女生收了10-3=7千克1年前查看全部
- (2004•贵阳)为了增强市民的环保意识,变废为宝,2004年5月初,贵阳市将中山路、神奇路上的垃圾箱全部更换为分类回收
(2004•贵阳)为了增强市民的环保意识,变废为宝,2004年5月初,贵阳市将中山路、神奇路上的垃圾箱全部更换为分类回收垃圾箱.此次摆放的垃圾箱分类标志明显,绿色箱用来装可再利用垃圾,黄色箱用来装不可再利用垃圾.以下物质应扔进黄色垃圾箱的是( )
A.废旧报纸
B.果皮
C.铝制饮料罐
D.废旧电池 johnnymanlau1年前1
johnnymanlau1年前1 -
 win15163 共回答了20个问题
win15163 共回答了20个问题 |采纳率80%解题思路:根据金属和废纸在回收后,可以经过重新的加工后,在进行利用来分析.金属和纸在回收后,经过一系列的处理后,可以被重新的利用,而果皮属于不可回收垃圾,在土壤中可以直接的腐烂,不会对环境造成污染.电池属于有毒垃圾,需要单独处理.
故选B.点评:
本题考点: "三废"处理的必要性和一般原则;绿色化学.
考点点评: 在解此类题时,首先分析该资源是否会对环境造成污染,然后再分析是否具有回收利用的价值,最后再进行分析解答.1年前查看全部
- 某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+.为了减少污染并变废为宝,工厂计划从该废水中回收硫酸
某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+.为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜.请根据流程图,在下方的括号内填写物质名称(或主要成分的化学式)或操作方法,完成回收硫酸亚铁和铜的简单实验方案.加入
( )|——( )
|—( )———|
加入 | 加入 |
( ) | ( )|——( )—|
工业废水——————| |
操作 | |
( ) |——( )—————————|—(FeSO4·7H2O)
操作:
( )
工业废水加入()操作()然后上下两框,然后又是加入()操作()然后再上下两框,最后是(FeSO4·7H2O)还有操作().这样回答比较清楚. tyang5131年前1
tyang5131年前1 -
 goldfish1980 共回答了22个问题
goldfish1980 共回答了22个问题 |采纳率95.5%钠离子含量很少,当它为杂质,不管他.先往废水中加过量的铁,过滤,分离出硫酸亚铁和铁和铜的混合物,硫酸亚铁放在下面一空,铁和铜在上面一空,向铁和铜中加入适量硫酸,过滤,分离出铜和硫酸亚铁,将上下所得硫酸亚铁混合,再经过蒸发浓缩冷却结晶过滤得到FeSO4·7H2O1年前查看全部
- 为了增强市民的环保意识,变废为宝,早在2003 年哈尔滨市在南岗区宣化街率先实行垃圾 分类回收。
为了增强市民的环保意识,变废为宝,早在2003 年哈尔滨市在南岗区宣化街率先实行垃圾 分类回收。在此街道垃圾箱,绿色箱用来装可回收再利用垃圾,黄色箱用来装不可回收垃圾,黑色箱用来装有毒垃圾。以下物质:①废旧报纸;②废铜丝;③一次性塑料饭盒;④口香 糖嚼剩下的胶姆基;⑤果皮;⑥空矿泉水瓶;⑦废铁锅。能扔进绿色垃圾箱的是 [ ]A. ①③⑤⑦
B. ③④⑤⑥
C. ①②⑤⑦
D. ①②⑥⑦ 窗台上的花猫1年前1
窗台上的花猫1年前1 -
 大象111 共回答了9个问题
大象111 共回答了9个问题 |采纳率100%D1年前查看全部
- 英语翻译四氯化硅是生产多晶硅的废料,对环境有很大的破坏作用,对四氯化硅的利用不仅能够变废为宝,还能够促进新产业的发展.本
英语翻译
四氯化硅是生产多晶硅的废料,对环境有很大的破坏作用,对四氯化硅的利用不仅能够变废为宝,还能够促进新产业的发展.本文根据四氯化硅与氢氧化钙的水解反应原理,设计出四氯化硅与氢氧化钙的反应制备出硅酸钙的工艺,全面分析工艺组成中的四氯化硅水解系统、原硅酸脱水系统、硅酸钙生成系统的特点,研究工艺过程的影响因素,通过试验,制备出的硅酸钙符合国家标准;在此基础上探讨了工艺副产物的利用.本文的研究有助于解决多晶硅生产废物的严重污染问题,又可大幅度降低多晶硅生产成本,极大提高产业经济效益,对发展***多晶硅和太阳能产业具有十分重要的作用. ss2010081年前1
ss2010081年前1 -
 ysy_f 共回答了20个问题
ysy_f 共回答了20个问题 |采纳率90%The silicon tetrachloride is produces the polycrystalline silicon the waste material, has the very big destructive effect to the environment, not only can recycle waste to the silicon tetrachloride use, but also can promote the new industrial development.This article according to the silicon tetrachloride and the calcium hydroxide hydrolitic reaction principle, designs the silicon tetrachloride and the calcium hydroxide response prepares the calcium silicate the craft, analyzes in the craft composition comprehensively the silicon tetrachloride hydrolysis system, the ortho-silicic acid dehydration system, the calcium silicate production system characteristic, the research technological process influence factor, through the experiment, the calcium silicate which prepares conforms to the national standards; Has discussed the craft by-product use in this foundation.This article research is helpful to the solution polycrystalline silicon production waste serious contamination concern, also may reduce the polycrystalline silicon production cost large scale, enhances the industrial economic efficiency enormously, to develops our country polycrystalline silicon and the solar energy industry has the extremely vital role.1年前查看全部
- 某工厂的工业废水含有大量硫酸亚铁较多的铜离子和少量的钠离子,为了减少污染变废为宝,请设计发难回收硫
某工厂的工业废水含有大量硫酸亚铁较多的铜离子和少量的钠离子,为了减少污染变废为宝,请设计发难回收硫
共有两步操作,加入了两种化学药品.最后有一步得到了FeSO4.7H2O andy_pc1年前1
andy_pc1年前1 -
 diaocheng 共回答了23个问题
diaocheng 共回答了23个问题 |采纳率91.3%这是正确答案: 先加过量铁,过滤出Cu,Fe,滤液是FeSO8溶液;在Cu,Fe中加稀H8SO8,滤出铜,滤液与第一步滤液一样,所以合一块,进行蒸发,浓缩,冷却结晶,过滤,就得到FeSO8·8H8O,多给我点分啊1年前查看全部
- :废纸.矿泉水瓶,易拉灌,生锈铁钉,四个哪个可以通过化学变化变废为宝(回收)写出有关化学方程式(注意配平)
 yinuo60631年前3
yinuo60631年前3 -
 an_xx 共回答了27个问题
an_xx 共回答了27个问题 |采纳率100%当然是生绣的铁钉了.方程式:Fe2O3+3CO2==2Fe+3CO2
1个三氧化二铁分子和3个一氧化碳分子在高温的条件下生成2个铁分子和3个二氧化碳分子.1年前查看全部
- 有一工厂的废水,含有硝酸银,为净化废水,防止环境污染,变废为宝,某初中的化学兴趣小组设计了两种净化废水的方案.
有一工厂的废水,含有硝酸银,为净化废水,防止环境污染,变废为宝,某初中的化学兴趣小组设计了两种净化废水的方案.
方案一:在废水中加入足量的稀盐酸.
方案二:在废水中加入足量的铁粉.
请你评价一下,哪一种方案更好,为什么?
______. mingyuan51年前1
mingyuan51年前1 -
 inma 共回答了18个问题
inma 共回答了18个问题 |采纳率100%方案一生成氯化银,无法再继续处理,所以选方案二,具体步骤大致是:(1)放入足量铁粉(2)过滤(3)固体中加入稀硫酸(4)过滤、洗涤、干燥,得到银.故答案为:方案二好,方案一生成氯化银,初中学生无法继续处理;步骤:(1)放入足量铁粉,(2)过滤,(3)固体中加入稀硫酸,(4)过滤、洗涤、干燥,得到银.1年前查看全部
- 某工厂排出的废水中含有大量的Fe2+、Cu2+和SO42-.为了减少污染,变废为宝,工程师们设计了如下流程,以回收铜和硫
某工厂排出的废水中含有大量的Fe2+、Cu2+和SO42-.为了减少污染,变废为宝,工程师们设计了如下流程,以回收铜和硫酸亚铁.请回答:

(1)原料①为______(填化学式).
(2)写出加入原料②后反应的离子方程式:______.
(3)若在实验室中完成该流程,操作②需要用到的玻璃仪器的名称是______、
______、______;整个实验操作过程中不可能用到的装置是______(填字母).
 青天大人1年前1
青天大人1年前1 -
 william蟑螂 共回答了18个问题
william蟑螂 共回答了18个问题 |采纳率83.3%解题思路:(1)根据该题要求:回收铜且不引进新的杂质判断原料①;
(2)先判断操作①后的固体成分,再根据流程图知:操作①后的溶液中的溶质与操作②后的溶液中的溶质相同写离子方程式;
(3)根据混合物的状态确定实验操作,根据实验操作确定实验仪器;根据各装置用途确定选项;(1)根据题意知,该物质能和铜离子反应且不引进新的杂质离子,所以只能是铁,故答案为:Fe.
(2)操作①中加入过量的铁才能使铜离子完全反应,所以所得固体的成分是铁和铜;分离铁和铜且回收铜,所以加入某物质与铁反应,与铜不反应,且与铁反应后的物质与操作①所得溶液中溶质的成分一样,加入的物质只能是稀硫酸,所以发生的离子反应为Fe+2H+═Fe2++H2↑,故答案为:Fe+2H+═Fe2++H2↑.
(3)操作②的分离是固体、液体分离,所以应用过滤的方法,故用到的玻璃仪器有玻璃棒、漏斗、烧杯;
操作①、②的分离是固体、液体分离,所以应用过滤的方法;操作③是蒸发掉水分,使溶质从溶液中析出,所以应用蒸发结晶的方法;
a、该装置是过滤装置,分离固体和液体;
b、该装置是萃取装置,根据溶解度的不同分离;
c、该装置是蒸发结晶装置,分离溶剂和溶质;
d、该装置是蒸馏装置,根据沸点的不同分离液体和液体;
所以选bd
故答案为:玻璃棒、漏斗、烧杯;bd.点评:
本题考点: 金属的回收与环境、资源保护;常见金属元素的单质及其化合物的综合应用;物质的分离、提纯的基本方法选择与应用.
考点点评: 本题考查了学生对高中化学实验装置图的理解和掌握程度.1年前查看全部
- 有一工厂的废水,含有 有一工厂的废水,含有硝酸银,为净化废水,防止环境污染,变废为宝,某初中的化学兴趣小组设计了两种净化
有一工厂的废水,含有
有一工厂的废水,含有硝酸银,为净化废水,防止环境污染,变废为宝,某初中的化学兴趣小组设计了两种净化废水的方案.
方案一:在废水中加入足量的稀盐酸.
方案二:在废水中加入足量的铁粉. 请你评价一下,哪一种方案更好,然后将实验方案设计完整. ktuktr1年前1
ktuktr1年前1 -
 闲云自在 共回答了13个问题
闲云自在 共回答了13个问题 |采纳率92.3%方案二好,方案一生成氯化银,初中学生无法继续处理;
步骤:
(1)放入足量铁粉,
(2)过滤,
(3)固体中加入稀硫酸,
(4)过滤、洗涤、干燥,得到银.1年前查看全部
- 某化学兴趣小组在刷洗试管时,用力过猛.造成试管底被穿通,留下圆形小孔.在老师的启发下.兴趣小组变废为宝,将细铜丝揉成小球
 某化学兴趣小组在刷洗试管时,用力过猛.造成试管底被穿通,留下圆形小孔.在老师的启发下.兴趣小组变废为宝,将细铜丝揉成小球垫在试管底部,配上带单孔橡皮塞的导管和烧杯,装配了一个在实验室制取气体的装置,如图所示.该装置的优点是______(写一条),制备气体之前,都必须要捡查装置的气密性.写出你检查该装置气密性的方法:______.
某化学兴趣小组在刷洗试管时,用力过猛.造成试管底被穿通,留下圆形小孔.在老师的启发下.兴趣小组变废为宝,将细铜丝揉成小球垫在试管底部,配上带单孔橡皮塞的导管和烧杯,装配了一个在实验室制取气体的装置,如图所示.该装置的优点是______(写一条),制备气体之前,都必须要捡查装置的气密性.写出你检查该装置气密性的方法:______.  bt西域河马1年前1
bt西域河马1年前1 -
 w_c_l 共回答了13个问题
w_c_l 共回答了13个问题 |采纳率84.6%解题思路:凡是有气体参加或产生的实验,实验前一定要检查装置的气密性;
实验设计是实验内容的重要组成部分,实验设计是否科学,直接影响实验结论.实验过程中,关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止;
打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行,该装置的优点是能够随时使反应进行或停止.
故填:能够随时使反应进行或停止.
检查该装置气密性的方法:向烧杯中加水至浸没试管底部,导管连接注射器,打开开关,把注射器活塞缓缓向外抽出一部分,如果水在试管中上升形成一段液柱,过一会儿后,液柱不下降,说明装置不漏气.
故填:向烧杯中加水至浸没试管底部,导管连接注射器,打开开关,把注射器活塞缓缓向外抽出一部分,如果水在试管中上升形成一段液柱,过一会儿后,液柱不下降,说明装置不漏气.点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;检查装置的气密性.
考点点评: 科学地设计实验,是实验成功的前提条件之一,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.1年前查看全部
大家在问
- 1描写可爱的小孩子说话时的词语
- 2已知总体的各个体的值由小到大依次为2,3,3,7,a,b,12,13.7,18.3,20,且总体的中位数为10.5,平均
- 3中文大意Y.M.C.A ---- Berk & The Virtual Band
- 4怎样详细推导证明引力势能和重力势能的一致性?
- 5(28分)依据图文材料及所学知识,完成下列问题。
- 6数学题:25*64*125=?快些
- 7有书名的好词好句100字
- 8谁能说出《小兵张嘎》中胖墩的特点
- 9下列几个关于力学问题的说法中正确的是( )
- 10根号1乘3加1=2,根号2乘4加1=3,根号3乘5加1=4,根号4乘6加1=5.你发现了什么规律?试用含n的式子表示出来
- 11作文(70分)根据以下材料,自选角度,自拟题目,写一篇不少于800的文章。做个简单的实验:一只手正常握住沙子,另一只手用
- 12A、B、C、D、E,五个人如下排列:
- 13读句子,选出正确的图。 He likes sports. [
- 14请高手提供一段大约三分钟的,在餐厅里的英文对话?
- 15Judy _______ a rest after a long walk.



