(1)3.01×1022个OH-与______molNH3的质量相等,与______gNa+含有的离子数相同.
 男人夜曲2022-10-04 11:39:540条回答
男人夜曲2022-10-04 11:39:540条回答(2)同温同压下,同体积的氨气和硫化氢气体(H2S)的质量比为______,同质量的氨和硫化氢气体的体积比为______;若二者氢原子数相等,它们的体积比为______.

已提交,审核后显示!提交回复
共0条回复
相关推荐
- 某气体物质的质量为6.4g,含有6.02×1022个分子,则该气体的相对分子质量是( )
某气体物质的质量为6.4g,含有6.02×1022个分子,则该气体的相对分子质量是( )
A. 64
B. 32
C. 96
D. 124 tyz15963211年前0
tyz15963211年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 某气体物质的质量为6.4g,含有6.02×1022个分子,则该气体的相对分子质量是( )
某气体物质的质量为6.4g,含有6.02×1022个分子,则该气体的相对分子质量是( )
A. 64
B. 32
C. 96
D. 124 星夜VIP公主1年前0
星夜VIP公主1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 某硫酸钠溶液中含有3.01×1022个Na+,则该溶液中SO42-的物质的量是()
某硫酸钠溶液中含有3.01×1022个Na+,则该溶液中SO42-的物质的量是()
(8)某硫酸钠溶液中含有3.01×1022个Na+,则该溶液中SO42-的物质的量是(),
(9)1.204×1024个水分子的物质的量是().1molH2SO4中氧原子数为().
(10)1molMgCl2中氯离子数为(),离子总数约为().
(11)1mol CuSO4·5H2O含有多少()个Cu2+,含有()mol水分子.
(12)2molCO(NH2)2中含()mol碳原子,()mol氧原子,()mol氮原子,()mol氢原子,所含氧原子数跟()molH2O中所含氧原子数相等. fanasan1年前3
fanasan1年前3 -
 无理由架你 共回答了20个问题
无理由架你 共回答了20个问题 |采纳率90%(8)0.25mol
(9)20mol 4NA
(10)2NA 3NA
(11)6.02*10^23 5
(12)2 2 4 8 21年前查看全部
- 某气体物质的质量为6.4g,含有6.02×1022个分子,则该气体的相对分子质量是( )
某气体物质的质量为6.4g,含有6.02×1022个分子,则该气体的相对分子质量是( )
A. 64
B. 32
C. 96
D. 124 chentony8212151年前0
chentony8212151年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 某气体的质量为3.2g,含有的是3.01×1022个分子,则该气体的相对分子质量是( )
某气体的质量为3.2g,含有的是3.01×1022个分子,则该气体的相对分子质量是( )
A. 32
B. 64
C. 32 g/mol
D. 64 g/mol 心慰1年前0
心慰1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 1.6g某物质中含有6.02×1022个分子,则该物质的相对分子质量为( )
1.6g某物质中含有6.02×1022个分子,则该物质的相对分子质量为( )
A. 16
B. 64
C. 32
D. 96 pq39t1年前0
pq39t1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 铜片、锌片连接后浸入稀硫酸中构成原电池,当导线上通过3.01×1022个电子时,锌失去电子______mol,锌片质量减
铜片、锌片连接后浸入稀硫酸中构成原电池,当导线上通过3.01×1022个电子时,锌失去电子______mol,锌片质量减少______g.铜片表面析出氢气______L(标准状况).
 股祸人心1年前1
股祸人心1年前1 -
 桃碧 共回答了22个问题
桃碧 共回答了22个问题 |采纳率86.4%解题思路:锌比铜活泼,形成原电池反应时,锌为负极,发生氧化反应,电极反应式为Zn-2e-=Zn2+,铜为正极,发生还原反应,电极反应式为2H++2e-=H2↑,结合电极反应式进行相关的计算.锌比铜活泼,形成原电池反应时,锌为负极,发生氧化反应,电极反应式为Zn-2e-=Zn2+,铜为正极,发生还原反应,电极反应式为2H++2e-=H2↑,
当导线上通过3.01×1022个电子时,转移电子为
3.01×1022
6.02×1023/mol=0.05mol,锌失去电子0.05mol,锌片质量减少为[1/2]×0.05mol×65g/mol=1.625g,铜片表面析出氢气体积为0.025mol×22.4L/mol=0.56L,
故答案为:0.05;1.625;0.56.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查原电池知识,为高考常见题型,侧重于学生的分析能力和计算能力的考查,注意把握电极反应式的书写,题目难度不大.1年前查看全部
- 在0℃和101KPa下,2.00gHe、3.01×1022个N2、1.60gO2混合,该混合气体的体积是( )
在0℃和101KPa下,2.00gHe、3.01×1022个N2、1.60gO2混合,该混合气体的体积是( )
A.13.44 L
B.7.84 L
C.10.08 L
D.无法计算 一捧土鳖1年前1
一捧土鳖1年前1 -
 UMIWING 共回答了23个问题
UMIWING 共回答了23个问题 |采纳率82.6%解题思路:通过n=[m/M]求出He、O2的物质的量,通过n=
求出N2的物质的量,从而得到混合气体总物质的量,代入公式V=n•Vm计算体积.N NA n(He)=[2.00g/4g/mol]=0.5mol,n(O2)=[1.60g/32g/mol]=0.05mol,n(N2)=
3.01×1022
6.02×1023mol−1=0.05mol,则混合气体的总物质的量为:0.5mol+0.05mol+0.05mol=0.6mol,该混合气体的体积V=n•Vm=0.6mol×22.4L/mol=13.44L,
故选:A.点评:
本题考点: 气体摩尔体积.
考点点评: 本题考查了以物质的量为中心的计算,题目难度不大,明确标准状况下Vm=22.4L/mol、NA的数值是解题的关键.1年前查看全部
- 铜片、锌片连接后浸入稀硫酸中构成原电池,当导线上通过3.01×1022个电子时,锌失去电子______mol,锌片质量减
铜片、锌片连接后浸入稀硫酸中构成原电池,当导线上通过3.01×1022个电子时,锌失去电子______mol,锌片质量减少______g.铜片表面析出氢气______L(标准状况).
 蜡笔小晨1年前1
蜡笔小晨1年前1 -
 jack054009 共回答了17个问题
jack054009 共回答了17个问题 |采纳率100%解题思路:锌比铜活泼,形成原电池反应时,锌为负极,发生氧化反应,电极反应式为Zn-2e-=Zn2+,铜为正极,发生还原反应,电极反应式为2H++2e-=H2↑,结合电极反应式进行相关的计算.锌比铜活泼,形成原电池反应时,锌为负极,发生氧化反应,电极反应式为Zn-2e-=Zn2+,铜为正极,发生还原反应,电极反应式为2H++2e-=H2↑,
当导线上通过3.01×1022个电子时,转移电子为
3.01×1022
6.02×1023/mol=0.05mol,锌失去电子0.05mol,锌片质量减少为[1/2]×0.05mol×65g/mol=1.625g,铜片表面析出氢气体积为0.025mol×22.4L/mol=0.56L,
故答案为:0.05;1.625;0.56.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查原电池知识,为高考常见题型,侧重于学生的分析能力和计算能力的考查,注意把握电极反应式的书写,题目难度不大.1年前查看全部
- 1cm3的水里含3.35×1022个水分子,一滴水珠的体积是20mm3,它里面有多少个水分子?如果让微生物来喝水,每秒钟
1cm3的水里含3.35×1022个水分子,一滴水珠的体积是20mm3,它里面有多少个水分子?如果让微生物来喝水,每秒钟喝进106个水分子,需要多长时间才能喝完这滴水?
 dodoluo1年前3
dodoluo1年前3 -
 hungry0331 共回答了10个问题
hungry0331 共回答了10个问题 |采纳率100%解题思路:结合数学上的倍数关系,一滴水的体积0.02cm3是1cm3的 0.02倍,分子个数也就是3.35×1022的0.02倍;每分钟喝掉106个水分子,计算总的分钟数中有多少个106,也就是多少分钟.如此分析题中涉及的几个倍数关系,运算细心就可得到答案.因为1cm3的水里含3.35×1022个水分子,
则一滴水所含水分子个数为
0.02mm3
1cm3×3.35×1022=6.7×1020;
微生物喝水所用时间为
6.7×1020
106=6.7×1014s;
答:一滴水含有6.7×1020个水分子;微生物喝掉一滴水用6.7×1014秒.点评:
本题考点: 密度公式的应用.
考点点评: 此题考查了有关分子的知识,分子相当小,分析清楚题目中有关的倍数关系,就可得到答案,运算要细心.1年前查看全部
- 物理八下第七章中的一道题1克食盐中约有1.04×1022个分子,把1克食盐投入一个水库中,已知水库的蓄水量为4×109米
物理八下第七章中的一道题
1克食盐中约有1.04×1022个分子,把1克食盐投入一个水库中,已知水库的蓄水量为4×109米3,如果食盐分子均匀分布在水库的水中,那么每立方厘米的是中约含有__________个食盐分子. 鸟人飞1年前1
鸟人飞1年前1 -
 hcb1230 共回答了19个问题
hcb1230 共回答了19个问题 |采纳率84.2%(1.04×10^22)/(4×10^9×10^6)=2.6×10^6个1年前查看全部
- 已知在某温度、101kPa的条件下3.01×1022个X气体分子的体积约为1.24L,则该条件下28g 氮气的
已知在某温度、101kPa的条件下3.01×1022个X气体分子的体积约为1.24L,则该条件下28g 氮气的体积约为( )
A.22.4L/mol
B.24.8L
C.2.48L/mol
D.22.4L 凡人㊣1年前0
凡人㊣1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 1cm3的水里含3.35×1022个水分子,一滴水珠的体积是20mm3,它里面有多少个水分子?如果让微生物来喝水,每秒钟
1cm3的水里含3.35×1022个水分子,一滴水珠的体积是20mm3,它里面有多少个水分子?如果让微生物来喝水,每秒钟喝进106个水分子,需要多长时间才能喝完这滴水?
 水贴工具箱1年前1
水贴工具箱1年前1 -
 tymsy 共回答了20个问题
tymsy 共回答了20个问题 |采纳率100%解题思路:结合数学上的倍数关系,一滴水的体积0.02cm3是1cm3的 0.02倍,分子个数也就是3.35×1022的0.02倍;每分钟喝掉106个水分子,计算总的分钟数中有多少个106,也就是多少分钟.如此分析题中涉及的几个倍数关系,运算细心就可得到答案.因为1cm3的水里含3.35×1022个水分子,
则一滴水所含水分子个数为
0.02mm3
1cm3×3.35×1022=6.7×1020;
微生物喝水所用时间为
6.7×1020
106=6.7×1014s;
答:一滴水含有6.7×1020个水分子;微生物喝掉一滴水用6.7×1014秒.点评:
本题考点: 密度公式的应用.
考点点评: 此题考查了有关分子的知识,分子相当小,分析清楚题目中有关的倍数关系,就可得到答案,运算要细心.1年前查看全部
- 下列说法正确的是( )A.1molH2O中含有1mol氧和2mol氢B.1mol任何物质都含有6.02×1022个原子
下列说法正确的是( )
A.1molH2O中含有1mol氧和2mol氢
B.1mol任何物质都含有6.02×1022个原子
C.SO42-的摩尔质量是96g/mol
D.同质量的H2和Cl2含有的分子数相同 轻风一缕1年前1
轻风一缕1年前1 -
 songfang_2005 共回答了21个问题
songfang_2005 共回答了21个问题 |采纳率85.7%解题思路:A、从化学用语的规范使用分析;
B、从物质可以由分子、原子、离子构成分析;
C、从摩尔质量的概念分析判断;
D、从物质的量相同,分子数相同分析判断.A、物质的量是微观粒子的概念,使用必须指明何种微粒,应为1molH2O中含有1molO和2molH,故A错误;
B、1mol任何物质都含有6.02×1023个微粒,故B错误;
C、SO42-的摩尔质量是96g/mol,故C正确;
D、同质量的H2和Cl2,摩尔质量不同,气体物质的量不同,分子数不同,故D错误;
故选C.点评:
本题考点: 阿伏加德罗常数.
考点点评: 本题考查了物质的量的意义和表达,摩尔质量的概念,阿伏伽德罗常数的应用,质量与物质的量的计算关系.1年前查看全部
- 现有4.0g NaA,其中含6.02×1022个Na+.(A表示原子或原子团)
现有4.0g NaA,其中含6.02×1022个Na+.(A表示原子或原子团)
(1)NaA的相对分子质量为______.
(2)将此NaA完全溶解在46.0g水中,所得溶液的质量分数为______.
(3)若上述溶液的密度近似为1.0g/cm3,则该溶液的物质的量浓度为______. 6696382281年前0
6696382281年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 0.8g某物质含有3.01×1022个分子,该物质的相对分子质量约为( )
0.8g某物质含有3.01×1022个分子,该物质的相对分子质量约为( )
A. 8
B. 16
C. 64
D. 160 泥湿达春绿1年前0
泥湿达春绿1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 1g食盐中约有1.04×1022个分子,把1g食盐投入一个水库中,已知水库的蓄水量为4×109m3,如果食盐分子均匀分布
1g食盐中约有1.04×1022个分子,把1g食盐投入一个水库中,已知水库的蓄水量为4×109m3,如果食盐分子均匀分布在水库的水中,那么每立方厘米的水中约含有______个食盐分子.
 4750011年前1
4750011年前1 -
 蔷花红莲 共回答了16个问题
蔷花红莲 共回答了16个问题 |采纳率81.3%解题思路:解答此题的关键是掌握物质的组成,分子是组成物质的最小的颗粒,在不同状态下,分子自身不变,保持物质的物理属性.然后把4×109m3换算成立方厘米,即可求出答案.4×109m3=4×1015cm3
1.04×1022
4×1015=2.6×106(个)
故填2.6×106.点评:
本题考点: 分子和原子组成物质.
考点点评: 此题主要考查学生对物质的组成的了解和掌握,同时,又考查了学生的简单计算能力.1年前查看全部
- 下列叙述正确的是( )A.2.24 L NH3中含有6.02×1022个氮原子B.100
下列叙述正确的是( )
A.2.24 L NH3中含有6.02×1022个氮原子
B.100 mL 1 mol/L 的Na2CO3溶液中含有6.02×1022个CO32-
C.将4 g NaOH溶于100 g蒸馏水,所得溶液物质的量浓度是0.1 mol/L
D.将7.8 g Na2O2放入足量的水中,反应时转移6.02×1022个电子 b1uering1年前0
b1uering1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 下列有关叙述正确的是下列有关叙述正确的是A.1L 0.1mol/L的醋酸中有6.02×1022个CH3COO-B.1mo
下列有关叙述正确的是
下列有关叙述正确的是
A.1L 0.1mol/L的醋酸中有6.02×1022个CH3COO-
B.1mol葡萄糖分子中含有3.01×1024个-OH
C.电解1L饱和食盐水,当pH=10时,反应中有6.02×1022个电子转移
D.一定条件下将2molSO2和1molO2混合充分反应,有2.408×1024个电子转移 依水桥1年前3
依水桥1年前3 -
 becket1986 共回答了12个问题
becket1986 共回答了12个问题 |采纳率100%2NaCl + 2H2O ==通电== 2NaOH + Cl2↑ + H2↑
又pH=10 故生成NaOH的浓度为1*10^-4mol/L
又电解1L饱和食盐水,故NaOH为0.0001mol
又每生成1molNaOH转移电子数为1mol
所以生成0.0001molNaOH转移电子数为0.0001mol即6.02×10^19个1年前查看全部
- (1)4.9g某物质含有3.01×1022个分子,则该物质的摩尔质量是______.
(1)4.9g某物质含有3.01×1022个分子,则该物质的摩尔质量是______.
(2)在标准状态下,15g由CO和CO2组成的混合气体的体积为10.08L,在这种混合气体中,CO与CO2的物质的量之比为______. 不曾栓你1年前0
不曾栓你1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 0.8g某物质含有3.01×1022个分子,该物质的相对分子质量约为______.
 办公室比尔1年前0
办公室比尔1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 已知一元弱酸(HA)溶液中含有1.01 已知一元弱酸(HA)溶液中含有1.01×1022个HA分子
已知一元弱酸(HA)溶液中含有1.01 已知一元弱酸(HA)溶液中含有1.01×1022个HA分子
如题
已知一元弱酸(HA)溶液中含有1.01×1022个HA分子.则HA的电离度为 ( )
A、10% B、9.8% C、1.0% D、0.98% gaokeddk1年前2
gaokeddk1年前2 -
 Laudyson_guan 共回答了16个问题
Laudyson_guan 共回答了16个问题 |采纳率93.8%闷死`!当然是C咯1年前查看全部
- 某气体物质的质量为6.4g,含有6.02×1022个分子,则该气体的相对分子质量是( )
某气体物质的质量为6.4g,含有6.02×1022个分子,则该气体的相对分子质量是( )
A. 64
B. 32
C. 96
D. 124 蛮族驸马1年前0
蛮族驸马1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 如图所示的原电池装置.Cu电极反应式为______.当导线上通过3.01×1022个电子时,锌片质量减少______g(
 如图所示的原电池装置.
如图所示的原电池装置.
Cu电极反应式为______.当导线上通过3.01×1022个电子时,锌片质量减少______g(保留小数点后三位). 招个江公不让勃1年前1
招个江公不让勃1年前1 -
 可人之2000 共回答了20个问题
可人之2000 共回答了20个问题 |采纳率85%解题思路:该装置构成原电池,锌易失电子作负极、Cu作正极,电极反应式为:Zn-2e-=Zn2+、2H++2e-=H2↑,再结合锌和转移电子之间的关系式计算.该装置构成原电池,锌作负极、Cu作正极,负极上锌失电子发生氧化反应,电极反应式为:Zn-2e-=Zn2+,正极上氢离子得电子发生还原反应,电极反应式为2H++2e-=H2↑,电子的物质的量=
3.01×1022
6.02×1023/mol=0.05mol,
设参加反应的Zn的质量为x
Zn-2e-=Zn2+,
65g 2mol
x 0.05mol
65g:2mol=x:0.05mol
x=[65g×0.05mol/2mol]=1.625g,
故答案为:2H++2e-=H2↑;1.625.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查了原电池原理,正确书写电极反应式是解本题关键,再结合各个物理量之间的关系式计算,题目难度不大.1年前查看全部
- 某硫酸钠溶液中含有3.01×1022个Na+,则溶液中SO42-的物质的量是______,该溶液中Na2SO4的质量为_
某硫酸钠溶液中含有3.01×1022个Na+,则溶液中SO42-的物质的量是______,该溶液中Na2SO4的质量为______克.
 相间不如偶遇1年前0
相间不如偶遇1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- A.(选修模块3-3)(1)镀铜的工艺应用很广泛.如果镀膜内铜原子的个数要求是8×1022个/米2,取1g铜,均匀镀在物
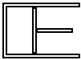 A.(选修模块3-3)
A.(选修模块3-3)
(1)镀铜的工艺应用很广泛.如果镀膜内铜原子的个数要求是8×1022个/米2,取1g铜,均匀镀在物体表面时,则能镀膜的面积为______米2.(已知铜的摩尔质量为64g/mol,结果保留两位有效数字)
(2)固定在水平面上的气缸内封闭着一定质量的理想气体,气缸壁是导热的,缸外环境保持恒温,大气压强恒定不变,活塞与气缸壁光滑接触且不漏气.现用水平外力拉活塞缓慢地向右移动一段距离,在此过程中,下列说法正确的是
A.该气体温度不变,压强减小
B.该气体压强不变,温度降低
C.水平外力大小不变
D.因为有水平外力作用,此过程违反热力学第二定律
(3)题(2)所研究的过程中,如果环境温度发生变化,气缸中的气体推动活塞做功3×105J,同时吸收热量为2×105J,则此过程中理想气体的内能是增加还是减少?增加或减少了多少? wukaikui1年前1
wukaikui1年前1 -
 为什么你要伤我 共回答了19个问题
为什么你要伤我 共回答了19个问题 |采纳率78.9%解题思路:(1)根据质量求出铜的物质的量,进而可以求得铜的原子的个数,再计算镀膜的面积;
(2)向右移动,气体的体积增加,气体对外做功,根据热力学第一定律来分析气体的内能的变化;
(3)根据热力学第一定律来分析气体的内能的变化.(1)1g铜的物质的量为n=[m/M]=[1/64]mol,
1g铜的原子的个数为N=nNA=[1/64]×6.02×1023个
能镀膜的面积为
1
64×6.02×1023
8×1022=0.12m2,
(2)气体的体积变大,对外做功,
由于,活塞缓慢地向右移动的,并且气缸壁是导热的,缸外环境保持恒温,所以气体的温度不变,体积变大,所以压强减小,所以A正确,B错误;
在向右移动的过程中,气体的压强逐渐的减小,根据活塞的受力平衡可得,水平外力逐渐的变大,所以C错误;
在变化的过程中,气体不断的从外界吸收热量,此过程没有违反热力学第二定律,所以D错误.
故选A.
(3)气缸中的气体推动活塞做功3×105J,是对外做功,所以W=-3×105J,
吸收热量为Q=2×105J,
根据△E=W+Q=-3×105J+2×105J=-1×105J,
所以气体的内能减少1×105J.
故答案为:
(1)0.12 (2)A (3)减少,1×105J点评:
本题考点: 理想气体的状态方程;热力学第一定律.
考点点评: 利用热力学第一定律判断气体的内能变化的时候要注意做功W和热量Q的符号,对外做功和放热为负的,对气体做功和吸热为正的.1年前查看全部
- 下列说法中正确的是( )A.CO2的摩尔质量为44gB.6.02×1022个H2SO4分子的质量为9.8gC.标准状况
下列说法中正确的是( )
A.CO2的摩尔质量为44g
B.6.02×1022个H2SO4分子的质量为9.8g
C.标准状况下,22.4L盐酸所含的质量为36.5g
D.同温同压下,无法判断等物质的量的CH4和CO原子个数比 天地无真情1年前1
天地无真情1年前1 -
 yunpeng_jia 共回答了14个问题
yunpeng_jia 共回答了14个问题 |采纳率85.7%解题思路:A.二氧化碳的摩尔质量是44g/mol;
B.根据n=
计算硫酸的物质的量,再根据m=nM计算其质量;N NA
C.标况下22.4LHCl的物质的量为1mol,其质量为36.5g,而盐酸是HCl的水溶液;
D.根据各分子含有原子数目计算.A.1mol二氧化碳的质量是44g,二氧化碳的摩尔质量是44g/mol,故A错误;
B.硫酸的物质的量
6.02×1022
6.02×1023mol−1=0.1mol,其质量=0.1mol×98g/mol=9.8g,故B正确;
C.标况下22.4LHCl的物质的量为1mol,其质量为36.5g,盐酸是HCl的水溶液,22.4L盐酸的质量远远大于36.5g,故C错误;
D.同温同压下,等物质的量的CH4和CO原子个数比=5:2,故D错误,
故选B.点评:
本题考点: 物质的量的相关计算.
考点点评: 本题考查物质的量有关计算,比较基础,C选项为易错点,学生容易把HCl与盐酸进行混淆.1年前查看全部
- 25mL氯化钙溶液中含Cl-数为3.01×1022个(22为上标),此氯化钙溶液的物质的量浓度为( )
25mL氯化钙溶液中含Cl-数为3.01×1022个(22为上标),此氯化钙溶液的物质的量浓度为( )
A.4mol/L B.2mol/L C.1mol/L D.0.5mol/L 王苏阳1年前4
王苏阳1年前4 -
 消失的瞬间1 共回答了19个问题
消失的瞬间1 共回答了19个问题 |采纳率84.2%C
Cl-数为3.01×1022个,1mol的物质的量是6.02x10^23个
说明Cl-的物质的量是0.05mol
则Ca2+的物质的量是0.025mol
氯化钙的物质的量是0.025mol
此氯化钙溶液的物质的量浓度为0.025mol/0.025L=1mol/L1年前查看全部
- 某硫酸钠溶液中含有3.01×1022个Na+,则溶液中SO42-的物质的量是______,该溶液中Na2SO4的质量为_
某硫酸钠溶液中含有3.01×1022个Na+,则溶液中SO42-的物质的量是______,该溶液中Na2SO4的质量为______克.
 盼望你在我身边1年前0
盼望你在我身边1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 0.8g某物质含有3.01×1022个分子,该物质的相对分子质量约为______.
 Ivangu1年前0
Ivangu1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
大家在问
- 1She thinks only of herself ;she doesn't other people.
- 2汹涌的江水冲上提岸.改成拟人句急
- 3“形容规模宏大,气势雄壮的样子”的成语是?
- 4求一篇英语作文:写一篇英语短文给报社.
- 5(2011•黄冈模拟)如图A、B、C、D、E是初中化学中常见的五种物质,且它们都含有一种相同的元素.其中A是胃酸的主要成
- 6我有击倒他不会啦,我笨,请亲们伴我一步一步写出来.
- 7数学一元一次方程折扣应用题?某商店中的一批钢笔按售价的八折出售仍能获得20%的利润,求商店在定价时的期望利润率?(原定价
- 8我想请你教我如何看地图 用英语怎么说呐?
- 999乘以102减1484,怎样简便运算?
- 10定语从句In our university there are several big parks ____we stu
- 11not until/until的句型用法.
- 12Xiao Li was supposed __________ her homework before nine o’c
- 13英语第八单元课文,说打扰一下,我刚来到这个小镇,英语课文帮我照下来,书忘带回来了,,快啊,,,,,,,,,,,,
- 14英语翻译One summer afternoon her bell rang,she went to the front
- 15His brother work/worked as a bus driver in London.
