(2013•临沭县模拟)如图甲所示,理想变压器原线圈输入端接如图乙所示的交变电压,移动滑动触头P,可以改变原线圈的匝数.
 xing20082022-10-04 11:39:541条回答
xing20082022-10-04 11:39:541条回答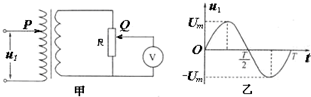
A.向上移动P,输入电压的频率不变
B.向上移动P,输入电流减小
C.保持P不动,向下移动Q,变压器的输入功率减小
D.保持Q不动,向下移动P,电压表的示数不变

已提交,审核后显示!提交回复
共1条回复
 邃凌蓝羽 共回答了16个问题
邃凌蓝羽 共回答了16个问题 |采纳率100%- 解题思路:变压器不改变交流电的频率,电压与匝数成正比,电流与匝数成反比,输入功率等于输出功率.
A、变压器不改变交流电的频率,A正确;
B、向上移动P,原线圈匝数增大,副线圈电压减小,电流减小,所以输入电流减小,B正确;
C、保持P不动,副线圈电压不变,向下移动Q,电压表的示数减小,变压器的输入功率等于输出功率不变,CD错误;
故选:AB点评:
本题考点: 变压器的构造和原理.
考点点评: 本题考查了变压器的特点,结合闭合电路欧姆定律考查了电路的动态分析. - 1年前
相关推荐
- (2013•临沭县模拟)带正电的小环套在粗糙水平杆上,杆足够长,右半部分处在匀强磁场中,小环突然获得一向右的水平速度滑入
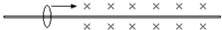 (2013•临沭县模拟)带正电的小环套在粗糙水平杆上,杆足够长,右半部分处在匀强磁场中,小环突然获得一向右的水平速度滑入磁场中,如图所示.小环的重量不能忽略,则小环进入磁场后的运动情况可能是( )
(2013•临沭县模拟)带正电的小环套在粗糙水平杆上,杆足够长,右半部分处在匀强磁场中,小环突然获得一向右的水平速度滑入磁场中,如图所示.小环的重量不能忽略,则小环进入磁场后的运动情况可能是( )
A.匀速直线运动
B.匀减速直线运动
C.先逐渐减速最后匀速直线运动
D.逐渐减速最后停止 哈哈袋1年前1
哈哈袋1年前1 -
 水中月86723 共回答了21个问题
水中月86723 共回答了21个问题 |采纳率81%解题思路:根据左手定则可得小环所受洛伦兹力方向向上,通过讨论小环重力和洛伦兹力的大小关系结合牛顿第二定律可正确得出结果.A、给滑环套一个初速度,将受到向上的洛伦兹力,若洛伦兹力等于物体的重力,滑环将做匀速直线运动,故A正确;
B、若重力小于洛伦兹力,滑环受到向下的弹力,则受到摩擦力,做减速运动,根据牛顿第二定律有(qvB-mg)μ=ma,由此可见小环做加速度逐渐增大的减速运动,直至停止,故B错误;
C、若重力小于洛伦兹力,滑环受到向下的弹力,则受到摩擦力,做减速运动,当洛伦兹力等于重力时,又做匀速运动,故C正确;
D、若重力大于洛伦兹力,滑环受到向上的弹力,则受到摩擦力,将做减速运动,最后速度为零,故D正确.
故选ACD.点评:
本题考点: 安培力;牛顿第二定律.
考点点评: 本题学生易错,解决本题的关键掌握左手定则判断洛伦兹力的方向,以及会根据物体的受力判断物体的运动情况.1年前查看全部
- (2013•临沭县模拟)室温下氨水中存在平衡关系:NH3+H2O═NH3•H2O═NH4++OH-,下列有关判断正确的是
(2013•临沭县模拟)室温下氨水中存在平衡关系:NH3+H2O═NH3•H2O═NH4++OH-,下列有关判断正确的是( )
A.溶液中,c(NH3•H2O)>c(OH-)>c(NH4+)
B.向溶液中通入氨气,
增大c(NH4+) c(NH3•H2O)
C.向溶液中加入少量盐酸,c(OH-)和c(NH4+)都减小
D.加水稀释平衡向右移动,c(NH4+)增大 墓碑旁的彩堞1年前1
墓碑旁的彩堞1年前1 -
 bytd_aa2od7e9_2 共回答了24个问题
bytd_aa2od7e9_2 共回答了24个问题 |采纳率95.8%解题思路:A.一水合氨的电离程度较小;
B.向氨水中通入氨气,平衡向正反应方向移动,但电离程度减小;
C.向氨水中加入少量盐酸,氢离子和氢氧根离子反应导致平衡向正反应方向移动;
D.加水稀释促进一水合氨电离,但铵根离子浓度减小.A.一水合氨的电离程度较小,在溶液里,主要以一水合氨存在,水电离出氢氧根离子,所以氨水中c(OH-)>c(NH4+),故A正确;
B.向氨水中通入氨气,平衡向正反应方向移动,但电离程度减小,所以
c(NH4+)
c(NH3.H2O)减小,故B错误;
C.向氨水中加入少量盐酸,氢离子和氢氧根离子反应导致平衡向正反应方向移动,所以氢氧根离子浓度减小,但铵根离子浓度增大,故C错误;
D.加水稀释促进一水合氨电离,但铵根离子增大的量小于溶液体积增大的量,所以铵根离子浓度减小,故D错误;
故选A.点评:
本题考点: 弱电解质在水溶液中的电离平衡.
考点点评: 本题考查了弱电解质的电离,明确弱电解质电离特点是解本题关键,易错选项是B.1年前查看全部
- (2013•临沭县模拟)下列有关反应的离子方程式或电极反应式书写正确的是( )
(2013•临沭县模拟)下列有关反应的离子方程式或电极反应式书写正确的是( )
A.钢铁的电化学腐蚀中正极反应式:Fe-2e-=Fe2+
B.金属钠与水反应:Na+2H2O=H2↑+2OH-+Na+
C.将铁加入过量的稀硝酸中Fe+4H++NO3-=Fe3++2H2O+NO↑
D.用铜做阳极电解氯化铜溶液Cu2++2Cl-
Cu+Cl2↑电解 . 风牵1年前1
风牵1年前1 -
 开心的小米 共回答了24个问题
开心的小米 共回答了24个问题 |采纳率87.5%解题思路:A、钢铁的电化学腐蚀中,正极上是氧气得电子的还原反应;
B、离子反应遵循电荷守恒;
C、金属铁可以和过量的稀硝酸发生反应生成硝酸铁和一氧化氮、水;
D、金属铜是活泼金属电极,作阳极时,电极本身失电子.A、钢铁的电化学腐蚀中,正极上是氧气得电子的还原反应,金属铁做负极,发生失电子的氧化反应,故A错误;
B、金属钠与水反应:2Na+2H2O=H2↑+2OH-+2Na+,故B错误;
C、金属铁可以和过量的稀硝酸发生反应生成硝酸铁和一氧化氮、水,即 Fe+4H++NO3-=Fe3++2H2O+NO↑,故C正确;
D、金属铜是活泼金属电极,作阳极时,电极Cu本身失电子发生氧化反应,故D错误.
故选C.点评:
本题考点: 离子方程式的书写.
考点点评: 本题涉及电化学知识的综合考查,要求学生熟记教材知识,并灵活应用.1年前查看全部
- (2013•临沭县模拟)元素的原子结构决定其性质和周期表中的位置,下列有关结构和性质的说法中,正确的是( )
(2013•临沭县模拟)元素的原子结构决定其性质和周期表中的位置,下列有关结构和性质的说法中,正确的是( )
A.形成离子键的阴阳离子间只存在静电吸引力
B.元素周期表中,第三周期最右端的元素得电子能力最强
C.最易失去的电子能量最高
D.目前使用的元素周期表中最长的周期含有36种元素 cjf7211年前1
cjf7211年前1 -
 cc婶婶 共回答了13个问题
cc婶婶 共回答了13个问题 |采纳率84.6%解题思路:A.阴阳离子之间既有静电引力也有静电斥力;
B.稀有气体原子为稳定结构;
C.原子中电子能量越高离核越远,越容易失去;
D.目前使用的元素周期表中最长的周期含有32种元素.A.阴阳离子之间既有静电引力也有静电斥力等,故A错误;
B.元素周期表中,第三周期最右端的元素为Ar,Ar原子为稳定结构,化学性质稳定,不容易得到电子,也不容易失去电子,故B错误;
C.原子中电子能量越高离核越远,越容易失去,故C正确;
D.目前使用的元素周期表中最长的周期含有32种元素,故D错误;
故选C.点评:
本题考点: 位置结构性质的相互关系应用.
考点点评: 本题考查结构性质位置关系、元素周期表、化学键等,比较基础,注意基础知识的理解掌握.1年前查看全部
- (2013•临沭县模拟)下列有关实验操作正确的是( )
(2013•临沭县模拟)下列有关实验操作正确的是( )
A.为了将苯和乙醇分开可用蒸馏的方法
B.用98%的浓硫酸配制100g10%的稀硫酸溶液时,除使用量筒外还需用到容量瓶
C.用瓷坩埚高温熔融NaOH和Na2CO3的固体混合物
D.浓硫酸和浓硝酸混合时,应将浓硝酸沿器壁慢慢加入到浓硫酸中,并不断搅拌 财源茂盛1年前1
财源茂盛1年前1 -
 snoopyswm2000 共回答了16个问题
snoopyswm2000 共回答了16个问题 |采纳率93.8%解题思路:A.乙醇和苯的沸点不同;
B.不用容量瓶;
C.用瓷坩埚高温熔融NaOH和Na2CO3的固体混合物会导致坩埚炸裂;
D.应将浓硫酸加入到浓硝酸中.A.乙醇和苯的沸点不同,可用蒸馏的方法分离,故A正确;
B.不用容量瓶,应用量筒、烧杯可粗略配制,故B错误;
C.用瓷坩埚高温熔融NaOH和Na2CO3的固体混合物,在高温条件下与二氧化硅反应,会导致坩埚炸裂,故C错误;
D.为防止酸液飞溅,应将密度大的加入到密度小的溶液中,应将浓硫酸加入到浓硝酸中,故D错误.
故选A.点评:
本题考点: 物质的分离、提纯的基本方法选择与应用;化学实验安全及事故处理;配制一定物质的量浓度的溶液.
考点点评: 本题考查较为综合,涉及物质的分离、提纯、溶液的配制、加热等基本实验操作问题,综合考查学生的实验能力,题目难度不大,注意相关物质的性质.1年前查看全部
- (2013•临沭县模拟)下列有关有机物的说法正确的是( )
(2013•临沭县模拟)下列有关有机物的说法正确的是( )
A.石油的分馏和煤的干馏都是物理变化
B.甲烷、苯、乙酸乙酯都可以发生取代反应
C.油脂、蛋白质和纤维素都是高分子化合物
D.在加热、甲醛、饱和(NH4)2SO4溶液、X射线作用下,蛋白质都会发生变性 chess_man1年前1
chess_man1年前1 -
 我的动静 共回答了25个问题
我的动静 共回答了25个问题 |采纳率88%解题思路:A.石油分馏是根据混合物中各成分的沸点不同,控制温度得到不同馏分,是物理变化;煤的干馏是隔绝空气加强热发生了复杂的物理化学过程;
B.烷烃、苯及其同系物和酯类都能发生取代反应;
C.油脂属于小分子化合物;
D.甲醛、强酸、强碱、X射线、重金属盐等物质能使蛋白质变性.A.石油的分馏主要是物理变化而煤的干馏主要是化学变化,故A错误;
B.在一定条件下,烷烃、苯及其同系物和酯类都能发生取代反应,注意酯类的水解反应属于取代反应,故B正确;
C.蛋白质、纤维素的分子量很大,都属于天然有机高分子化合物,油脂是小分子化合物,故C错误;
D.饱和(NH4)2SO4溶液能使蛋白质发生盐析,盐析是可逆的,故D错误.
故选B.点评:
本题考点: 石油的分馏产品和用途;取代反应与加成反应;纤维素的性质和用途;氨基酸、蛋白质的结构和性质特点.
考点点评: 本题考查石油分馏产品、取代反应、高分子化合物和变性等,题目难度不大,注意饱和(NH4)2SO4溶液能使蛋白质发生盐析,盐析是可逆的.1年前查看全部
- (2013•临沭县模拟)A、B两物体叠放在一起,放在光滑水平面上,如图甲,它们从静止开始受到一个变力F的作用,该力与时间
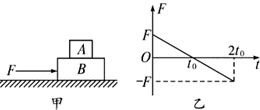 (2013•临沭县模拟)A、B两物体叠放在一起,放在光滑水平面上,如图甲,它们从静止开始受到一个变力F的作用,该力与时间的关系如图乙所示,A、B始终相对静止.则( )
(2013•临沭县模拟)A、B两物体叠放在一起,放在光滑水平面上,如图甲,它们从静止开始受到一个变力F的作用,该力与时间的关系如图乙所示,A、B始终相对静止.则( )
A.在t0时刻,A、B两物体间静摩擦力最大
B.在t0时刻,A、B两物体的速度最大
C.在2t0时刻,A、B两物体的速度最大
D.在2t0时刻,A、B两物体又回到了出发点 sakura_2561年前1
sakura_2561年前1 -
 天使wa_1028 共回答了20个问题
天使wa_1028 共回答了20个问题 |采纳率85%解题思路:根据牛顿第二定律分析何时整体的加速度最大.再以A为研究对象,当加速度最大时,A受到的静摩擦力最大.分析整体的运动情况,分析何时B的速度最大,并确定何时AB位移最大.A、以整体为研究对象,根据牛顿第二定律分析得知,0、2t0时刻整体所受的合力最大,加速度最大,再以A为研究对象,分析可知,A受到的静摩擦力最大.故A错误.
B、整体在0-t0时间内,做加速运动,在t0-2t0时间内,向原方向做减速运动,则t0时刻,A、B速度最大,在2t0时刻两物体速度为零,速度最小,故B正确、C错误.
D、0-2t0时间内,整体做单向直线运动,位移逐渐增大,则2t0时刻,A、B位移最大.没有回到出发点.故D错误.
故选:B.点评:
本题考点: 牛顿第二定律;匀变速直线运动的位移与时间的关系.
考点点评: 本题一方面要灵活选择研究对象,另一方面,要能根据物体的受力情况分析物体的运动过程,这是学习动力学的基本功1年前查看全部
- (2013•临沭县模拟)化学与生产、生活息息相关,下列说法不正确的是( )
(2013•临沭县模拟)化学与生产、生活息息相关,下列说法不正确的是( )
A.误食重金属盐可立即喝鲜牛奶或鸡蛋清解毒
B.高温结构陶瓷及压电陶瓷都属于新型无机非金属材料
C.服用Al(OH)3胶囊可用来治疗胃酸过多,无任何副作用
D.高铁酸钾(K2FeO4)是新型高效多功能水处理剂,既能消毒杀菌又能净水 duj4181年前1
duj4181年前1 -
 zca23257406 共回答了20个问题
zca23257406 共回答了20个问题 |采纳率90%解题思路:A.根据重金属盐可以使蛋白质变性来分析;
B.新型无机非金属材料一般指采用人工原料而非直接采用天然原料制备的,性能较优异的无机非金属材料,也称特种陶瓷及先进陶瓷;
C.任何药物都有副作用;
D.高铁酸钾具有强氧化性,可致蛋白质发生氧化而变性,高铁酸钾被还原生成Fe3+,水解生成具有吸附性的Fe(OH)3胶体而达到净水作用.A.重金属盐可以是蛋白质变性,所以误食后会中毒,服用大量的蛋清和牛奶后,可以和重金属反应,变为不被吸收的物质,减弱对肠胃的影响,故A正确;
B.高温结构陶瓷及压电陶瓷都属于新型无机非金属材料,故B正确;
C.任何药物都有副作用,应在医生指导下服用,故C错误;
D.高铁酸钾具有强氧化性,可致蛋白质发生氧化而变性,高铁酸钾被还原生成Fe3+,水解生成具有吸附性的Fe(OH)3胶体而达到净水作用,故D正确.
故选C.点评:
本题考点: 氨基酸、蛋白质的结构和性质特点;无机非金属材料;药物的主要成分和疗效.
考点点评: 本题考查蛋白质的性质、新型无机非金属材料、药物的使用及净水剂,题目难度中等,注意高温结构陶瓷及压电陶瓷都属于新型无机非金属材料.1年前查看全部
- (2013•临沭县模拟)如图所示,在水平放置的两平行金属板的右侧存在着有界的匀强磁场,磁场方向垂直于纸面向里,磁场边界M
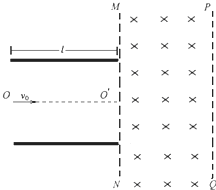 (2013•临沭县模拟)如图所示,在水平放置的两平行金属板的右侧存在着有界的匀强磁场,磁场方向垂直于纸面向里,磁场边界MN和PQ与平行板的中线OO′垂直.金属板的两极板间的电压U=100V,匀强磁场的磁感应强度B=1.0×10-2T.现有带正电的粒子以v0=1.73×105m/s的速度沿两板间的中线OO′连续进入电场,恰能从平行金属板边缘穿越电场射入磁场.已知带电粒子的比荷[q/m]=1.0×108C/kg,粒子的重力和粒子间相互作用力均可以忽略不计(结果保留两位有效数字).
(2013•临沭县模拟)如图所示,在水平放置的两平行金属板的右侧存在着有界的匀强磁场,磁场方向垂直于纸面向里,磁场边界MN和PQ与平行板的中线OO′垂直.金属板的两极板间的电压U=100V,匀强磁场的磁感应强度B=1.0×10-2T.现有带正电的粒子以v0=1.73×105m/s的速度沿两板间的中线OO′连续进入电场,恰能从平行金属板边缘穿越电场射入磁场.已知带电粒子的比荷[q/m]=1.0×108C/kg,粒子的重力和粒子间相互作用力均可以忽略不计(结果保留两位有效数字).
(1)求射入电场的带电粒子射出电场时速度的大小和方向.
(2)为使射入电场的带电粒子不会由磁场右边界射出,该匀强磁场区的宽度至少为多大? 啼血袅1年前0
啼血袅1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2013•临沭县模拟)如图所示,水平放置的光滑平行金属导轨上有一质量为m的金属棒ab.导轨的一端连接电阻R,其它电阻均
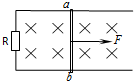 (2013•临沭县模拟)如图所示,水平放置的光滑平行金属导轨上有一质量为m的金属棒ab.导轨的一端连接电阻R,其它电阻均不计,磁感应强度为B的匀强磁场垂直于导轨平面向下,金属棒ab在一水平恒力F作用下由静止开始向右运动.则( )
(2013•临沭县模拟)如图所示,水平放置的光滑平行金属导轨上有一质量为m的金属棒ab.导轨的一端连接电阻R,其它电阻均不计,磁感应强度为B的匀强磁场垂直于导轨平面向下,金属棒ab在一水平恒力F作用下由静止开始向右运动.则( )
A.随着ab运动速度的增大,其加速度也增大
B.外力F对ab做的功等于电路中产生的电能
C.当ab做匀速运动时,外力F做功的功率等于电路中的电功率
D.无论ab做何种运动,它克服安培力做的功一定等于电路中产生的电能 飞扬的汤圆1年前1
飞扬的汤圆1年前1 -
 healthl330 共回答了19个问题
healthl330 共回答了19个问题 |采纳率100%解题思路:在水平方向,金属棒受到拉力F和安培力作用,安培力随速度增大而增大,根据牛顿定律分析加速度的变化情况.根据功能关系分析电能与功的关系.A、金属棒所受的安培力为:FA=BIL=
B2L2v
R,a=
F−FA
m速度增大,安培力增大,则加速度减小.故A错误.
B、根据能量守恒知,外力F对ab做的功等于电路中产生的电能以及ab棒的动能.故B错误.
C、当ab棒匀速运动时,外力做的功全部转化为电路中的电能,则外力F做功的功率等于电路中的电功率.故C正确.
D、根据功能关系知,克服安培力做的功等于电路中产生的电能.故D正确.
故选:CD.点评:
本题考点: 导体切割磁感线时的感应电动势;电磁感应中的能量转化.
考点点评: 电磁感应现象中电路中产生的热量等于外力克服安培力所做的功;在解题时要注意体会功能关系及能量转化与守恒关系.1年前查看全部
- (2013•临沭县模拟)如图所示,有一个重力不计的方形容器,被水平力F压在竖直的墙面上处于静止状态,现缓慢地向容器内注水
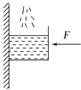 (2013•临沭县模拟)如图所示,有一个重力不计的方形容器,被水平力F压在竖直的墙面上处于静止状态,现缓慢地向容器内注水,直到将容器刚好盛满为止,在此过程中容器始终保持静止,则下列说法中正确的是( )
(2013•临沭县模拟)如图所示,有一个重力不计的方形容器,被水平力F压在竖直的墙面上处于静止状态,现缓慢地向容器内注水,直到将容器刚好盛满为止,在此过程中容器始终保持静止,则下列说法中正确的是( )
A.容器受到的摩擦力不变
B.容器受到的摩擦力逐渐增大
C.水平力F可能不变
D.水平力F必须逐渐增大 裟椤一大群树1年前1
裟椤一大群树1年前1 -
 绝世倾城妞 共回答了19个问题
绝世倾城妞 共回答了19个问题 |采纳率94.7%解题思路:由题知物体处于静止状态,受力平衡,合力为0;再利用二力平衡的条件再分析其受到的摩擦力和F是否会发生变化;由题知物体处于静止状态,受力平衡,摩擦力等于容器和水的总重力,所以容器受到的摩擦力逐渐增大,故A错误,B正确;
C、水平方向受力平衡,力F可能不变,故C正确,D错误.
故选BC点评:
本题考点: 静摩擦力和最大静摩擦力;滑动摩擦力.
考点点评: 物体受到墙的摩擦力等于物体重,物重变大、摩擦力变大,这是本题的易错点.1年前查看全部
- (2013•临沭县模拟)在用电流表和电压表测电池的电动势和内电阻的实验中,电源的电动势不超过1.5V,内阻不超过1Ω,电
(2013•临沭县模拟)在用电流表和电压表测电池的电动势和内电阻的实验中,电源的电动势不超过1.5V,内阻不超过1Ω,电压表(0-3V,3KΩ),电流表(0-0.6A,1Ω),滑动变阻器有R1(10Ω,2A)和R2(100Ω,0.1A)各一只.实验电路如图(甲)
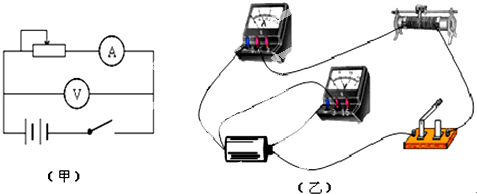
(1)实验中滑动变阻器应选用______(填“R1”或“R2”)
(2)某位同学在实验操作时电路连接如图(乙)所示,该同学接线中错误(或不妥当)的实验器材是______
A.滑动变阻器B.电压表C.电流表. 猫眼zz1年前1
猫眼zz1年前1 -
 zzzxp 共回答了24个问题
zzzxp 共回答了24个问题 |采纳率91.7%解题思路:(1)应用欧姆定律求出滑动变阻器的阻值范围,然后选择滑动变阻器.
(2)分析图甲所示电路图,然后根据电路图分析答题.(1)电流表量程为0.6A,由I=[E/R+r]得应满足[1/3]Im≤[E/R+r]≤[2/3]Im,解得2.7Ω≤R≤6.5Ω,因此变阻器应选R1.
(2)由图甲所示电路图可知,电压表直接接在电源两端,开关不能控制电压表,电压表连接错误;滑动变阻器同时接下面两个接线柱,滑动变阻器成为定值电阻,滑动变阻器连接错误,故选:AB.
故答案为:(1)R1;(2)AB.点评:
本题考点: 测定电源的电动势和内阻.
考点点评: 做电学实验时注意以下几点:①电键控制整个电路,②电表的读数一般要求指针在量程的中间位置.③旧电池不允许大电流放电,因如果大电流放电会造成电池内阻急剧增大,同时电动势也很快下降,导致电池损坏.1年前查看全部
- (十七13•临沭县模拟)足够长的粗糙斜面上,用力推着一物体沿斜面向上运动,i=七时撤去推力,七~6s内速度随时间的变化情
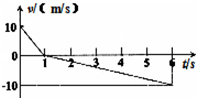 (十七13•临沭县模拟)足够长的粗糙斜面上,用力推着一物体沿斜面向上运动,i=七时撤去推力,七~6s内速度随时间的变化情况如图所示,由图象可知( )
(十七13•临沭县模拟)足够长的粗糙斜面上,用力推着一物体沿斜面向上运动,i=七时撤去推力,七~6s内速度随时间的变化情况如图所示,由图象可知( )
A.0~1s内物体发生的位移大小与1~6s内发生的位移大小之比为1:5
B.0~1s内重力的平均功率大小与1~6s内重力平均功率大小之比为5:1
C.0~ls内摩擦力的平均功率与1~6s内摩擦力平均功率之比为1:1
D.0~1s内机械能变化量大小与1~6s内机械能变化量大小之比为1:5 猪hh1年前1
猪hh1年前1 -
 dsfsafdasdf23234 共回答了18个问题
dsfsafdasdf23234 共回答了18个问题 |采纳率94.4%解题思路:平均功率根据
=Fv即可计算,机械能的变化量等于除重力以外的力做的功,动能变化量等于合外力所做的功..P A、v-7图象与时间轴包围少面积表示位移大小,故4~1s内物体发生少位移大小与1~6s内发生少位移大小之比为1:他,故A正确;
B、根据图象可知:4-1s内少平均速度为:V1=[14−4/他]m/s=他m/s;
1-6s内平均速度为:V他=[−14−4/他]=-他m/s;
所以4-1s内重力少平均功率为:
P1=m4V1=他m4
1-6s内重力平均功率:
P他=m4V他=他m4,故B错误
C、滑动摩擦力f=μm4cosθ,整个运动过程中滑动摩擦力不变,根据Pf=fv,可知4~ls内摩擦力少平均功率与1~6s内摩擦力平均功率相等,故C正确;
4、机械能少变化量等于滑动摩擦力做少功,4~1s内机械能变化量大小为Wf1=Pf71=Pf,1~6s内机械能变化量大小为Wf他=Pf7他=他Pf,所以4~1s内机械能变化量大小与1~6s内机械能变化量大小之比为1:他,故4正确;
故选:AC4.点评:
本题考点: 匀变速直线运动的图像;功率、平均功率和瞬时功率.
考点点评: 本题主要考查了恒力功率公式、牛顿第二定律及功能关系的应用,难度适中.1年前查看全部
- (2013•临沭县模拟)在一定温度下,向2L体积固定的密闭容器中加入1molHI,2HI⇌H2(g)+I2(g)△H>0
 (2013•临沭县模拟)在一定温度下,向2L体积固定的密闭容器中加入1molHI,2HI⇌H2(g)+I2(g)△H>0,H2的物质的量随时间的变化如图示,下列说法正确的是( )
(2013•临沭县模拟)在一定温度下,向2L体积固定的密闭容器中加入1molHI,2HI⇌H2(g)+I2(g)△H>0,H2的物质的量随时间的变化如图示,下列说法正确的是( )
A.该温度下,反应的平衡常数是[1/16]
B.0~2min内的HI的平均反应速率为0.05mol•L-1•min-1
C.恒压下向该体系中加入N2,平衡不移动,反应速率不变
D.升高温度,平衡向正反应方向移动,只有正反应速率加快 lisa9111年前1
lisa9111年前1 -
 ljxkhm 共回答了18个问题
ljxkhm 共回答了18个问题 |采纳率88.9%A.由图可知,平衡时生成氢气为0.1mol,根据方程式计算生成的n(I2)=n(H2)=0.1mol,参加反应的n(HI)=2n(H2)=0.2mol,平衡时HI的物质的量为1mol-0.2mol=0.8mol,由于反应前后气体的化学计量数相等,利用物质的量代替浓度计算平衡常数,故平衡常数k=[0.1×0.1
0.82=
1/64],故A错误;
B.由图可知,2min内生成氢气为0.1mol,故v(H2)=
0.1mol
2L
2min=0.025mol•L-1•min-1,速率之比等于化学计量数之比,故v(HI)=2v(H2)=0.05mol•L-1•min-1,故B正确;
C.恒压下向该体系中加入N2,体积增大,等效为降低压强,该反应前后气体的体积不变,平衡不移动.反应混合物的浓度减小,反应速率减小,故C错误;
D.升高温度正、逆反应速率都增大,正反应速率增大更多,平衡向正反应方向移动,故D错误;
故选B.1年前查看全部
- (2013•临沭县模拟)已知一定条件下断裂1mol下列化学键需要吸收的能量分别为:H-H 436kJ;Cl-C
(2013•临沭县模拟)已知一定条件下断裂1mol下列化学键需要吸收的能量分别为:H-H 436kJ;Cl-Cl243kJ;H-Cl431kJ.对于反应 H2(g)+Cl2(g)=2HCl (g),下列说法正确的是( )
A.该反应的反应热△H>0
B.氢气分子中的化学键比氯气分子中的化学键更稳定
C.相同条件下,该反应在光照和点燃条件下的△H不同
D.H2与Cl2反应的热化学方程式为H2(g)+Cl2(g)=2HCl(g)△H=-180.3kJ josepcryst1年前1
josepcryst1年前1 -
 gang_520 共回答了22个问题
gang_520 共回答了22个问题 |采纳率100%解题思路:A、根据反应热=断裂化学键吸收的能量-形成化学键放出的能量;
B、分子中的化学键断裂吸收能量越大,化学键越稳定;
C、焓变和反应物生成物有关,与反应条件和过程无关;
D、先根据反应热=断裂化学键吸收的能量-形成化学键放出的能量,然后书写热化学方程式.A、反应热=断裂化学键吸收的能量-形成化学键放出的能量=436 kJ/mol+243 kJ/mol-2×431 kJ/mol=-kJ/molKJ;△H<0,故A错误;
B、断裂1mol化学键需要吸收的能量分别为:H-H 436kJ;Cl-Cl 243kJ;说明氢气分子中的化学键比氯气分子中的化学键更稳定,故B正确;
C、焓变和反应物生成物有关,与反应条件和过程无关,相同条件下,该反应在光照和点燃条件下的△H相同,故C错误;
D、反应热=断裂化学键吸收的能量-形成化学键放出的能量=436 kJ/mol+243 kJ/mol-2×431 kJ/mol=-kJ/molKJ,所以H2与Cl2反应的热化学方程式为 H2(g)+Cl2(g)=2HCl(g)△H=-183 kJ/mol,故D错误;
故选B.点评:
本题考点: 化学能与热能的相互转化.
考点点评: 本题考查反应热的计算,题目难度不大,本题注意根据反应的方程式计算,焓变的含义计算,利用键能计算反应热的方法.1年前查看全部
- (2013•临沭县模拟)将一浅绿色溶液,置于空气中,变黄色.将此黄色溶液逐滴滴入沸水中,形成一种红褐色胶体,下列说法中错
(2013•临沭县模拟)将一浅绿色溶液,置于空气中,变黄色.将此黄色溶液逐滴滴入沸水中,形成一种红褐色胶体,下列说法中错误的是( )
A.该浅绿色溶液中含有Fe2+在空气中被氧化为Fe3+
B.欲检验该黄色溶液中,是否含有未被氧化的Fe2+,向其中滴加KSCN溶液
C.配制该浅绿色溶液,要向其中加少量酸与铁粉,目的是为了防止Fe2+的水解与氧化
D.欲检验浅绿色溶液中是否含有Fe3+,滴入KSCN溶液,看是否变红色 武汉新元素1年前1
武汉新元素1年前1 -
 大马虫 共回答了21个问题
大马虫 共回答了21个问题 |采纳率90.5%解题思路:向待测溶液中加入硫氰化钾溶液,溶液马上变成红色说明溶液中有Fe3+,加入硫氰化钾溶液没有明显现象,加入氯水溶液变成红色,说明溶液只有Fe2+.A.浅绿色溶液中含有Fe2+在空气中被氧化为黄色的Fe3+,故A正确;
B.向其中滴加KSCN溶液,只能检验Fe3+,而不能检验Fe2+,故B错误;
C.酸能防止Fe2+水解,铁粉能防止Fe2+氧化,故C正确;
D.滴入KSCN溶液,溶液变红色证明有Fe3+,否则无Fe3+,故D正确;
故选B.点评:
本题考点: 铁盐和亚铁盐的相互转变.
考点点评: 本题考查Fe3+、Fe2+的检验,根据颜色变化分析是解题的关键.1年前查看全部
- (2013•临沭县模拟)关于下列各装置图的叙述中,正确的是( )
(2013•临沭县模拟)关于下列各装置图的叙述中,正确的是( )
A.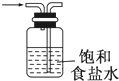
洗气装置,可以除去氯气中的氯化氢
B.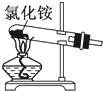
实验室可以用装置制取氨气
C.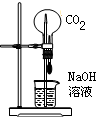
实验室用装置做“喷泉”实验不能成功
D.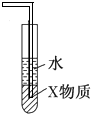
装置中X若为四氯化碳,可用于吸收氨气,并防止倒吸 千里千寻0o1年前1
千里千寻0o1年前1 -
 guoleiiljr 共回答了17个问题
guoleiiljr 共回答了17个问题 |采纳率100%解题思路:A.进气方向错误;
B.实验室用氯化铵和氢氧化钙制备氨气;
C.二氧化碳可与氢氧化钠溶液反应;
D.氨气不溶于四氯化碳,可放倒吸.A.进气管应插入到液面以下,进气方向错误,故A错误;
B.氯化铵加热分解生成氨气和氯化氢,温度稍低时又可生成氯化铵,实验室用氯化铵和氢氧化钙制备氨气,故B错误;
C.二氧化碳可与氢氧化钠溶液反应,容器压强降低,可产生喷泉,故C错误;
D.氨气不溶于四氯化碳,且四氯化碳不溶于水,可放倒吸,故D正确.
故选D.点评:
本题考点: 化学实验方案的评价.
考点点评: 本题考查化学实验方案的评价,为高考常见题型,综合考查学生的实验评价和分析能力,题目难度不大,注意把握相关物质的性质.1年前查看全部
- (2013•临沭县模拟)如图所示,螺线管CD的导线绕法不明,当磁铁N极向下靠近螺线管C端时,闭合电路中有图示方向的感应电
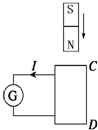 (2013•临沭县模拟)如图所示,螺线管CD的导线绕法不明,当磁铁N极向下靠近螺线管C端时,闭合电路中有图示方向的感应电流产生,下列说法正确的是( )
(2013•临沭县模拟)如图所示,螺线管CD的导线绕法不明,当磁铁N极向下靠近螺线管C端时,闭合电路中有图示方向的感应电流产生,下列说法正确的是( )
A.C端一定是N极
B.D端一定是N极
C.因螺线管的绕法不明,故无法判断C端的极性
D.当磁铁向下穿过螺线管且远离D端时,电路中的感应电流方向与图示方向相反 windosxp1年前1
windosxp1年前1 -
 注册真的好难 共回答了16个问题
注册真的好难 共回答了16个问题 |采纳率87.5%解题思路:当磁铁的运动时,穿过线圈的磁通量变化,由楞次定律判断出感应电流的方向.A、B、C、由题意可知,当磁铁N极向下运动时,即靠近螺线管,导致穿过的磁通量变大,且磁场方向向下,因此根据楞次定律,感应电流的磁场的方向竖直向上;故上端(C端)为N极;故A正确,BC错误;
D、当磁铁向下穿过螺线管且远离D端时,感应电流的磁场的方向竖直向下,所以电路中的感应电流方向与图示方向相反,故D正确;
故选:AD.点评:
本题考点: 楞次定律.
考点点评: 楞次定律是高中物理的一个重点,也是常考内容,一定要正确、全面理解楞次定律含义,掌握应用楞次定律解题的思路与方法.1年前查看全部
大家在问
- 1为理想,而奋斗 作文
- 2请你说出下列各种性格特征的人的脸谱化的名词
- 3make a TV show.be amazed at .feed on.get out of.make sb happ
- 4(2012•长春一模)如图,在△AOB中,∠AOB=90°,OA=OB=6,C为OB上一点,射线CD⊥OB交AB于点D,
- 5关于光的反射,下列说法正确的是:( ) A.反射光线、人射光线不可能在一条直线上 B.反射时,光不遵守反射定律 C.反射
- 6把toast翻译成中文
- 7爱的故事(转载) 作文
- 8水流速度为5千米一时,顺水航行需要+5一时,一般客轮静水速度是25千米一时,往返于180千米的AB地,
- 9I think it's a good idea to pass on the message to her(改为否定句
- 10某校大礼堂第一排有a个座位,后面每一排都比前一排多两个座位,求第n排的座位数,若该礼堂一共有20排座位,且第一排座位数也
- 11本来是175,65r,14的轮胎,可以换成165,60r,14寸
- 12清明除了祭先人,还有其他意思吗?
- 13下列天气符号中,表示东北风4级的是( )
- 14这里为什么不能选D?all of us need ________ A feeling needed and admir
- 15那个女孩的歌唱的真好 翻译
