锂水电池以金属锂和钢板为电极材料,以LiOH为电解质,则放电时正极有氢气生成.
 id-yan2022-10-04 11:39:543条回答
id-yan2022-10-04 11:39:543条回答
锂水电池以金属锂和钢板为电极材料,以LiOH为电解质,则放电时正极有氢气生成.
我以为是吸氧腐蚀,结果答案是析氢,咋个判断出来的?
我以为是吸氧腐蚀,结果答案是析氢,咋个判断出来的?

已提交,审核后显示!提交回复
共3条回复
 怎么都被占用了啊 共回答了12个问题
怎么都被占用了啊 共回答了12个问题 |采纳率91.7%- 总反应是 2Li +2H2O ==2LiOH +H2
O2没它的事,放出H2是析氢腐蚀 - 1年前
 你走后我一无所有 共回答了27个问题
你走后我一无所有 共回答了27个问题 |采纳率- 因为有氢气生成啊
- 1年前
 月满西楼188 共回答了18个问题
月满西楼188 共回答了18个问题 |采纳率- 高中电化学是不是以电池为例子介绍的?不知现在高中化学课本啥样了,不过只要搞清楚电荷是如何转移的,就很容易理清电化学了。在以后高等化学中,会更详细
- 1年前
相关推荐
- 一种锂水电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电.下列说法正确的是( )
一种锂水电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电.下列说法正确的是( )
A 钢板是电池的负极 B该电池中锂被氧化,铁被还原 C放电时负极生成氢氧根离子,向正极移动 D电池总反应式为2LI+2H2O=2LiOH+H2 利记1年前3
利记1年前3 -
 顺春哥 共回答了19个问题
顺春哥 共回答了19个问题 |采纳率89.5%A、电池以金属锂和钢板为电极材料,LiOH 为电解质,锂做负极,钢板为正极,钢板上发生还原反应,故A正确;
B、放电时电子流向为负极--导线--正极,故B错误;
C、原电池中,阴离子移向原电池的负极,即放电时OH-向负极移动,故C错误;
D、锂水电池中,自发的氧化还原反应是金属锂和水之间反应生成氢氧化锂和氢气,即总反应为:2Li+2H2O═2LiOH+H2↑,故D错误.
故选:A1年前查看全部
- 研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源.该电池以金属锂和钢板为电极材料,
研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源.该电池以金属锂和钢板为电极材料,
以LiOH为电解质
,使用时加入水即可放电.关于该电池的下列说法不正确的是
A.水既是氧化剂又是溶剂 B.放电时正极上有氢气生成
C.放电时OH-向正极移动 D.总反应为:2Li+2H2O=2LiOH+H2
正确答案为C,请帮我写一下正负极反应式, hq26708471年前1
hq26708471年前1 -
 马爱利 共回答了18个问题
马爱利 共回答了18个问题 |采纳率88.9%看这个锂水电池的名称,总反应就是2Li+2H2O=2LiOH+H2
负极:Li-e-+OH-=LiOH
正极:H2O+2e-=H2+2OH-(2H++2e-=H2)1年前查看全部
- 有一种锂水电池,可作为鱼雷和潜艇的储备电源.电池以金属锂和钢板为电极材料,LiOH 为电解质,使用时加入水即可
有一种锂水电池,可作为鱼雷和潜艇的储备电源.电池以金属锂和钢板为电极材料,LiOH 为电解质,使用时加入水即可放电.关于该电池的说法正确的是( )
A.钢板为正极,钢板上发生还原反应
B.放电时电子的流动方向是”正极→导线→负极”
C.放电过程中OHˉ向正极作定向移动
D.总反应为:2Li+2 H+═2Li++H2↑ 哭泣的小害虫1年前1
哭泣的小害虫1年前1 -
 山关行足_山关望 共回答了13个问题
山关行足_山关望 共回答了13个问题 |采纳率100%解题思路:锂水电池中,自发的氧化还原反应是金属锂和水之间反应生成氢氧化锂和氢气的过程,根据原电池的工作原理以及电极反应特点和规律来回答.A、电池以金属锂和钢板为电极材料,LiOH 为电解质,锂做负极,钢板为正极,钢板上发生还原反应,故A正确;
B、放电时电子流向为负极--导线--正极,故B错误;
C、原电池中,阴离子移向原电池的负极,即放电时OH-向负极移动,故C错误;
D、锂水电池中,自发的氧化还原反应是金属锂和水之间反应生成氢氧化锂和氢气,即总反应为:2Li+2H2O═2LiOH+H2↑,故D错误.
故选:A.点评:
本题考点: 化学电源新型电池.
考点点评: 本题考查电化学的热点-锂离子电池,根据总反应式判断出正负极和阴阳极的反应,从化合价变化的角度分析.1年前查看全部
- 研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水
研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电。关于该电池的下列说法不正确的是
A.水既是氧化剂又是溶剂 B.放电时正极上有氢气生成 C.放电时OH - 向正极移动 D.总反应为:2Li+2H 2 O="==" 2LiOH+H 2 ↑  kaijie7263131年前1
kaijie7263131年前1 -
 tinaming 共回答了17个问题
tinaming 共回答了17个问题 |采纳率100%C
考生可能迅速选出C项是错误,因为原电池放电时OH - 是向负极移动的。这个考点在备考时训练多次。这种电池名称叫锂水电池。可推测其总反应为:2Li+2H 2 O="==" 2LiOH+H 2 ↑。再写出其电极反应如下:(—)2Li—2e — =2Li + (+)2H 2 O+2e — =2OH — +H 2 ↑
结合选项分析A、B、D都是正确的。此题情景是取材于新的化学电源,知识落脚点是基础,对原电池原理掌握的学生来说是比较容易的。1年前查看全部
- (2014•广东模拟)我国科学家发明的一种可控锂水电池的工作原理如图所示.下列有关说法不正确的是( )
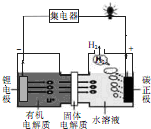 (2014•广东模拟)我国科学家发明的一种可控锂水电池的工作原理如图所示.下列有关说法不正确的是( )
(2014•广东模拟)我国科学家发明的一种可控锂水电池的工作原理如图所示.下列有关说法不正确的是( )
A.电池工作时,铿锂离子向正极移动
B.有机电解质可用水溶液代替
C.电池总反应为2Li+2H2O═2LiOH+H2↑
D.该装置不仅可提供电能,还可得到清洁的氢气 ansen12251年前1
ansen12251年前1 -
 SGZ17BTBBS 共回答了23个问题
SGZ17BTBBS 共回答了23个问题 |采纳率78.3%解题思路:A、原电池工作时,电解质中的阳离子移向正极;
B、金属Li可以和水之间反应生成氢氧化锂和氢气;
C、原电池的反应是自发的氧化还原反应;
D、原电池是将化学能转化为电能的装置,根据电池的产物来回答.A、该原电池工作时,电解质中的阳离子锂离子会移向正极,故A正确;
B、由于金属Li可以和水之间反应生成氢氧化锂和氢气,但是和有机电解质不反应,所以有机电解质不可用水溶液代替,故B错误;
C、金属Li可以和水之间反应生成氢氧化锂和氢气应是自发的氧化还原反应,即为2Li+2H2O═2LiOH+H2↑,故C正确;
D、该原电池是将化学能转化为电能的装置,装置不仅可提供电能,并且反应产物是氢气,能提供能源,故D正确.
故选B.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查学生原电池的工作原理知识,注意能量的转化等知识,知识的归纳和梳理是解题的关键,难度不大.1年前查看全部
大家在问
- 1下面的具体要怎么做才好:1.怎样快速了解她对数学的兴趣是?2.怎样提高她对数学的兴趣?3.我该对教学材料作何准备(试卷?
- 2公式如何化出来的?
- 3《社戏》这篇课文中中为什么说“一离赵庄,月光又显得格外皎洁”?
- 4“爱就要大声勇敢的说出来” 翻译成英文……谢谢
- 5『改为第三人称转述句』老师对我说:“萍萍身体不好...
- 6声音的传播速度除了与介质种类有关外,还与温度有关,声音在15°的空气中的传播速度约为多少?
- 7第九题 求P Q 05年西北大学一道考研数学题
- 8错过 作文
- 9判断下列句子各属于什么描写,把正确选项填在括号内。
- 10What ___ to her yesterday evening?空白处填什么?
- 11这是反问句还是设问句,还有,怎么把它变成陈述句
- 12音标都有什么?中元音有:后元音有:合口双元音有:集中双元音有:摩擦音清有:摩擦音浊有:破擦音清有:破擦音浊有:
- 13These books will provide us with all the information we need
- 14文言文阅读《晏子使楚》。
- 15英语翻译you are the Princess of the legends这句是:你是传说中的公主.再加个”原来”呢
