在①清洁的海水②铁片③氧气④水⑤饮料⑥硫磺⑦二氧化碳⑧一氧化碳八种物质中,属于混合物的是_____,属于纯净物的是___
 yinan882022-10-04 11:39:541条回答
yinan882022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 bbwlbjoftje 共回答了24个问题
bbwlbjoftje 共回答了24个问题 |采纳率87.5%- 15,234678,236,478
- 1年前
相关推荐
- 化学设计实验有一含碎菜叶、碎塑料薄膜、泥沙,还具有一定臭味的生活污水,处理又可做清洁用水【中水】.请设计方案出去这些杂质
化学设计实验
有一含碎菜叶、碎塑料薄膜、泥沙,还具有一定臭味的生活污水,处理又可做清洁用水【中水】.请设计方案出去这些杂质和臭味.思考 生活污水回收处理的目的是什么? mymusic1年前1
mymusic1年前1 -
 痛苦浪漫 共回答了22个问题
痛苦浪漫 共回答了22个问题 |采纳率100%设计实验 首先得知道目的.
二次利用.
最关键的是有实际意义,不能成本太高,不易操作.
第一步:沉淀过滤,这个很简单,可以用漏勺将碎菜叶、碎塑料薄膜滤除,沉淀将沙子去除,也可以将污水流过 滤网(一般可以用没用的旧窗帘-必须透水的)滤除杂质.
第二步:活性碳去除异味,但是估计得比较多.
.
这个比较难 等高人指点1年前查看全部
- 风能是一种清洁能源,按可再生能源和不可再生能源来分,风能属于______能源.水稻是喜温植物,春季育秧时,通常傍晚向秧田
风能是一种清洁能源,按可再生能源和不可再生能源来分,风能属于______能源.水稻是喜温植物,春季育秧时,通常傍晚向秧田灌水,早晨将水放出,以防霜冻.隐含的物理知识是,水的比热容较______(选填“大”或“小”).气温降低时,水能放出较多的______(选填“温度”、“内能”或“热量”).
 kannu1年前1
kannu1年前1 -
 robiliuy 共回答了13个问题
robiliuy 共回答了13个问题 |采纳率92.3%解题思路:①能从自然界源源不断获得或可重复利用的能源是可再生能源;不能从自然界源源不断获得或不可重复利用的能源是不可再生能源,
②水的比热容比较大,质量一定时,在吸收或释放相同热量的情况下,温度变化越小.①风能可以从自然界源源不断获得,是可再生能源.
②水的比热容是常见物体中最大的;
根据Q放=Cm(t-t0),气温降低时,由于水的比热容比较大,在质量一定时,水可以放出更多的热量.
故答案为:可再生.大;热量.点评:
本题考点: 水的比热容的特点及应用.
考点点评: 物理知识就是应用于生活的,我们要学会利用物理知识改变我们的生活、解释我们生活中的物理现象,这也是中考的一个出题方向.1年前查看全部
- (2013•芜湖模拟)二甲醚(CH3OCH3)被称为21世纪的新型燃料,清洁、高效,有优良的环保性能,以二甲醚、空气、氢
(2013•芜湖模拟)二甲醚(CH3OCH3)被称为21世纪的新型燃料,清洁、高效,有优良的环保性能,以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池.有关说法不正确的是( )
A.该燃料电池中通入二甲醚的一极为负极
B.二甲醚作为汽车燃料不会产生氮的氧化物和碳氢化合物的污染
C.在燃料电池中二甲醚最终转化为CO2和H2O
D.消耗0.5 mol二甲醚可以向外电路提供6mol e- tikki1年前1
tikki1年前1 -
 我塞 共回答了19个问题
我塞 共回答了19个问题 |采纳率84.2%解题思路:该电池属于燃料电池,负极上燃料二甲醚失电子发生氧化反应,电极反应式为CH3OCH3+160H--12e-═2CO32-+11H2O,正极上氧气得电子发生还原反应,电极反应式为3O2+12e-+6H2O=12OH-,结合物质间的关系式解答.A.该燃料电池中,二甲醚失电子发生氧化反应,所以通入二甲醚的电极是负极,电极反应式为CH3OCH3+160H--12e-═2CO32-+11H2O,故A正确;
B.二甲醚属于有机物,燃烧生成二氧化碳和水,所以不产生氮的氧化物和碳氢化合物的污染,故B正确;
C.碱性电池中,二氧化碳能和氢氧根离子反应生成碳酸根离子,所以二甲醚最终转化为碳酸根离子和水,故C错误;
D.消耗0.5 mol二甲醚可以向外电路提供电子的物质的量=0.5mol×2×(4+2)=6mol,故D正确;
故选C.点评:
本题考点: 化学电源新型电池.
考点点评: 本题考查了原电池原理,明确正负极上发生的电极反应式是解本题关键,注意电极反应式的书写要结合电解质溶液的酸碱性,为易错点.1年前查看全部
- A、B、C、D四种元素,A元素的单质是最清洁的燃料,B元素的单质是空气里最多的气体,C元素是地壳中最多的元素,D 2+
A、B、C、D四种元素,A元素的单质是最清洁的燃料,B元素的单质是空气里最多的气体,C元素是地壳中最多的元素,D 2+ 离子核外有10个电子.回答下列问题:
(1)写出四种元素的名称或符号:A______、B______、C______、D______;
(2)A、B、C三种元素组成的一种碱的化学式为______;
(3)D的单质在C的单质中燃烧的化学方程式为______. haining1111年前1
haining1111年前1 -
 shyshy 共回答了10个问题
shyshy 共回答了10个问题 |采纳率100%(1)根据题意:A元素的单质是最清洁的燃料,可推断A元素为:氢或H;
B元素的单质是空气里最多的气体,可推断B元素为:氮或N;
C元素是地壳中最多的元素为氧,可推断C元素为:氧或O;
D 2+ 离子核外有10个电子,则D元素的质子数为:2+8+2=12,可推知D元素为:或镁Mg;
故答案为:氢或H;氮或N;氧或O;镁或Mg;
(2)根据碱指电离时产生的阴离子全部都是氢氧根离子的化合物;可推断由H,N,O 3种元素组成的碱为:NH 3 ?H 2 O;
故答案为:NH 3 ?H 2 O;
(3)根据书写化学方程式的步骤:写配注等,镁在氧气中燃烧的化学方程式为:2Mg+O 2
点燃
.
2MgO;
故答案为:2Mg+O 2
点燃
.
2MgO.1年前查看全部
- 英语翻译展示盒包装、方便、快捷,满足家庭、办公对高档次清洁的需求
 CT0304071年前1
CT0304071年前1 -
 shanghaipuchun 共回答了17个问题
shanghaipuchun 共回答了17个问题 |采纳率88.2%展示盒包装、方便、快捷,满足家庭、办公对高档次清洁的需求
XX is of dispaly box package,convenient amd efficienct,and it meets the requirements of housholds and offices over high-end cleanliness1年前查看全部
- 我想问的是,怎么写一篇采访校园清洁阿姨的新闻报道,是什么样的格式哦?
 zengshengh1年前1
zengshengh1年前1 -
 crhy 共回答了20个问题
crhy 共回答了20个问题 |采纳率80%没有规定的格式.首先写清楚清洁阿姨的年龄,家庭自然状况,是否家庭生活中有现实生活中的困难...早上大家还在朦胧中,阿姨就开始了辛勤的劳动,不怕脏和累,多举证一些工作实例...1年前查看全部
- 「看,窗户需要清洁了」英文翻译
 画侠ZTK1年前1
画侠ZTK1年前1 -
 gnodiah 共回答了12个问题
gnodiah 共回答了12个问题 |采纳率91.7%look !the window needs cleaning!( the window needs to be cleaned )1年前查看全部
- 英语翻译只要良好、清洁的工作环境才能保证(施工)工作质量
 kahlúa1年前3
kahlúa1年前3 -
 还15孩 共回答了19个问题
还15孩 共回答了19个问题 |采纳率100%Only a sound and clean working environment can ensure work quality.
赞同二楼1年前查看全部
- 下列做法中,符合安全用电要求的是( ) A.小明妈妈经常边看电视边用湿抹布清洁电视机 B.正在洗菜的小明发现电水壶中的
下列做法中,符合安全用电要求的是( ) A.小明妈妈经常边看电视边用湿抹布清洁电视机 B.正在洗菜的小明发现电水壶中的水开了,立即去拔电源插头 C.不断开开关,直接更换不亮的电灯泡 D.发现家用电器或电线着火时,先切断电源再灭火  540771年前1
540771年前1 -
 tom2010 共回答了20个问题
tom2010 共回答了20个问题 |采纳率95%A、水属于电的良导体,用湿抹布擦拭带电的电视机,容易引起触电事故.故A错误;
B、正在洗菜的小明的手上有水,水是电的良导体,用湿手去拔电源插头时,容易引起触电事故.故B错误;
C、不断开开关,直接更换不亮的电灯泡,由于灯泡上带电,容易引起触电事故.故C错误;
D、发现家用电器或电线着火时,首先要切断电源再去灭火.正确.
故选D.1年前查看全部
- 氢能源是一种重要的清洁能源。现有两种可产生H 2 的化合物甲和乙。将6.00 g甲加热至完全分解,只得到一种短周期元素的
氢能源是一种重要的清洁能源。现有两种可产生H 2 的化合物甲和乙。将6.00 g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72 LH 2 (已折算成标准状况)。甲与水反应也能产生H 2 ,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到H 2 和另一种单质气体丙,丙在标准状态下的密度为1.25 g/L。请回答下列问题:
(1)甲的化学式是_________;乙的电子式是__________。
(2)甲与水反应的化学方程式是__________________________________。
(3)气体丙与金属镁反应的产物是_______(用化学式表示)。
(4)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式_________。有人提出产物Cu中可能还含有Cu 2 O,请设计实验方案验证之______________。(已知Cu 2 O+2H + ==Cu+Cu 2+ +H 2 O)
(5)甲与乙之间_______(填“可能”或“不可能”)发生反应产生H 2 ,判断理由是________。 冰柠凯蒂1年前0
冰柠凯蒂1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 埃及境内可大力发展的清洁能源是( )
埃及境内可大力发展的清洁能源是( )
A.石油
B.天然气
C.太阳能
D.煤炭 yer5551年前1
yer5551年前1 -
 青苔上的小妖 共回答了18个问题
青苔上的小妖 共回答了18个问题 |采纳率88.9%解题思路:埃及除北部地中海沿岸属地中海气候外,大部分地区属热带沙漠气候,最高气温可达40℃以上,年降水量大多不足50毫米,终年炎热,干燥少雨.埃及大部分地区海拔在200~700米之间,90%以上的土地为沙漠,是一个名副其实的沙漠之国,由于降水稀少,光照充足,太阳能成为埃及境内大力发展的清洁能源.
故选:C.点评:
本题考点: 埃及及其首都.
考点点评: 考查埃及能源的开发和利用,要理解记忆.1年前查看全部
- “节能减排、低碳生活”的主题旨在倡导节约能源和利用清洁能源,减少温室气体二氧化碳的排放。下列措施中不符合该主题的是
“节能减排、低碳生活”的主题旨在倡导节约能源和利用清洁能源,减少温室气体二氧化碳的排放。下列措施中不符合该主题的是

A.广泛使用太阳能和风能等清洁能源 B.回收利用废旧金属 C.多少用一次性筷子 D.减少使用私家车次数,多乘公交车或骑自行车  fishyss1年前1
fishyss1年前1 -
 空气涯 共回答了17个问题
空气涯 共回答了17个问题 |采纳率94.1%C
1年前查看全部
- 中译英:这些清洁女工的工资是按天数付给的.(day)
 水落音1年前8
水落音1年前8 -
 小虾MI 共回答了19个问题
小虾MI 共回答了19个问题 |采纳率78.9%These cleaning women are paid by the day.1年前查看全部
- 查反义词:淘气—( ) 清洁---( ) 和平---( )
 清理门户大爷11年前1
清理门户大爷11年前1 -
 wetfgewqukkeu 共回答了28个问题
wetfgewqukkeu 共回答了28个问题 |采纳率92.9%淘气—(乖巧 ) 清洁---(肮脏 ) 和平---( 战乱)1年前查看全部
- 下列叙述正确的是( )①用植物纤维制造出的机动车燃料,属清洁的可再生能源②可用甲醛溶液浸泡海产品,使海产品保鲜③变质的
下列叙述正确的是( )
①用植物纤维制造出的机动车燃料,属清洁的可再生能源
②可用甲醛溶液浸泡海产品,使海产品保鲜
③变质的油脂有难闻的刺激性气味,是由于油脂发生了水解反应
④蜂蚁叮咬人的皮肤时将分泌物注入人体,此时可在患处涂抹小苏打溶液或稀氨水
⑤提倡在生活中不用塑料袋,是为了防止白色污染.
A. ①④⑤
B. ②③④
C. ①③⑤
D. ①②③④⑤ xuedaolangzi1年前1
xuedaolangzi1年前1 -
 zzjzhff2 共回答了18个问题
zzjzhff2 共回答了18个问题 |采纳率100%解题思路:①植物纤维可再生;
②甲醛有毒;
③油脂发生氧化反应而产生异味;
④小苏打或稀氨水可以和甲酸发生反应;
⑤白色污染是指用聚苯乙烯、聚丙烯、聚氯乙烯等高分子化合物制成的各类生活塑料制品使用后被弃置成为固体废物,由于随意乱丢乱扔,难于降解处理,以致造成城市环境严重污染的现象;①植物纤维可再生,制造出的机动车燃料是清洁能源,故①正确;
②甲醛有毒,不可用甲醛溶液浸泡食用海产品以保鲜,故②错误;
③变质的油脂有难闻的特殊气味,是油脂发生氧化反应而产生异味,故③错误;
④小苏打或稀氨水可以和甲酸发生反应,可以用涂抹小苏打或稀氨水来缓解蜂蚁叮咬,故④正确;
⑤提倡在生活中不用塑料袋,可减少白色污染,故⑤正确.
故选A.点评:
本题考点: 清洁能源;常见的生活环境的污染及治理;甲醛;油脂的性质、组成与结构.
考点点评: 本题考查清洁能源、食品添加剂、油脂的氧化、蚁酸是甲酸、白色污染等,难度不大,注意变质的油脂有难闻的特殊气味,是油脂发生氧化反应而产生异味.1年前查看全部
- PCR 清洁试剂盒是什么
 爽口VS爽心1年前1
爽口VS爽心1年前1 -
 素面红颜 共回答了18个问题
素面红颜 共回答了18个问题 |采纳率83.3%就是DNA的纯化,把PCR产物里面的剩下的DNA聚合酶,缓冲离子,primer等去除,只保留PCR产物1年前查看全部
- 实验完毕后,都要做好清洁.如果显微镜的镜头有一些灰尘,下列的方法中,最好的一种是( )
实验完毕后,都要做好清洁.如果显微镜的镜头有一些灰尘,下列的方法中,最好的一种是( )
A.把手洗净,用手指擦掉灰尘
B.对着镜头呵口气,再用衣服擦
C.放在温水中洗净,再晾干
D.用擦镜纸沿着一个方向擦 天下久无君1年前1
天下久无君1年前1 -
 为发言的dd1 共回答了12个问题
为发言的dd1 共回答了12个问题 |采纳率83.3%解题思路:显微镜的镜头是放大的关键部位,若出现划痕就不能清晰地观察到物像.故要保护镜头,专门擦镜头的纸叫擦镜纸.A、显微镜的镜头上有灰尘,用手擦拭,因为灰尘是颗粒能够划伤显微镜;B、对着镜头呵气,再用衣服的角擦拭干净,这种做法是不正确的,因为对镜头呵气,也不能除去灰尘,用衣服角擦拭镜头,可能会划伤镜头;C、镜头上...
点评:
本题考点: 显微镜的基本构造和使用方法.
考点点评: 熟练地掌握显微镜的使用操作才能较容易地完成此类题目.1年前查看全部
- 天然气是一种高效、低能耗、污染小的清洁能源。天然气的主要成分是 ( ) A.CH 2 =CH 2 B.CO C.
天然气是一种高效、低能耗、污染小的清洁能源。天然气的主要成分是 ()
A.CH 2 =CH 2 B.CO C.CH 4 D.H 2  是游民1年前1
是游民1年前1 -
 爱与哀愁77 共回答了16个问题
爱与哀愁77 共回答了16个问题 |采纳率87.5%C
天然气的主要成份为甲烷CH 4 ,答案为C1年前查看全部
- 资阳市某单位积极参加四川省第八届“三优一学”创建文明城市竞赛活动,计划对办公大楼外墙进行清洁工作.如图所示,若施工吊篮质
资阳市某单位积极参加四川省第八届“三优一学”创建文明城市竞赛活动,计划对办公大楼外墙进行清洁工作.如图所示,若施工吊篮质量m 1 =60kg,清洁设备质量m 2 =30kg,现需要将人和设备从三楼底提升到十二楼顶,一自重G=600N的清洁工人用力500N以图示方式完成.已知楼层高度均为3m,取g=10N/kg,不计绳重及各处摩擦.求:
(1)此人在提升吊篮过程中所做的总功为多少?
(2)此人在提升吊篮过程中做功的效率为多少?
(3)为保证此人能以这种方式升降吊篮,吊篮内最多还能装载多重的物件?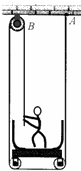
 骷髅oo1年前1
骷髅oo1年前1 -
 看来看见就 共回答了19个问题
看来看见就 共回答了19个问题 |采纳率94.7%(1)人在提升吊篮过程中所做的总功W=G 总 h=[(60kg+30kg)×10N/kg+600N]×30m=45000J;
(2)人在提升吊篮过程中做的有用功W 有用 =Gh=[(30kg×10N/kg)+600N]×30m=27000J,
人在提升吊篮过程中做功的效率η=
W 有用
W 总 ×100%=
27000J
45000J ×100%=60%,
(3)设还能G 1 重的物件,则
【(60kg+30kg)×10N/kg+600N+ G 1 】
3 =600N,
解得G 1 =300N.
答:(1)此人在提升吊篮过程中所做的总功为40500J.
(2)此人在提升吊篮过程中做功的效率为60%,
(3)为保证此人能以这种方式升降吊篮,吊篮内最多还能装载300N重的物件.1年前查看全部
- 天然气是一种清洁能源,2M3的天然气完全RAM少能放出-------J的热量? 热值取7.1*10的七次方
 南方木棉紅851年前2
南方木棉紅851年前2 -
 迈克尔欧文 共回答了4个问题
迈克尔欧文 共回答了4个问题 |采纳率1.42×1081年前查看全部
- (2012•镇江一模)A、B可发生中和反应,D是生活中最常见的液体.通常情况下,F、G、I为气体,且F是一种清洁能源.x
(2012•镇江一模)A、B可发生中和反应,D是生活中最常见的液体.通常情况下,F、G、I为气体,且F是一种清洁能源.x是目前应用最广泛的金属,y常用作食品干燥剂.各物质间的转化关系如图所示(个别产物略去).
 (1)B俗称______.B溶液可用来检验二氧化碳,其反应的化学方程式为______.
(1)B俗称______.B溶液可用来检验二氧化碳,其反应的化学方程式为______.
(2)反应⑤中,将B的固体粉末与(NH4)2SO4等混合研磨,可区别______肥与钾肥.
(3)反应③发生时放出大量热,化学方程式为______.反应④的实验现象是______ 方程式3Fe+2O2
Fe3O4点燃 .3Fe+2O2
Fe3O4点燃 .
(4)金属x也能与硫酸铜溶液反应,其化学方程式为______.反应②的化学方程式为______. 米781年前1
米781年前1 -
 jolene78 共回答了23个问题
jolene78 共回答了23个问题 |采纳率91.3%解题思路:找准解题突破口,直接得出物质的化学式,F是一种清洁能源,说明F是氢气,x是目前应用最广泛的金属,说明X是铁,y常用作食品干燥剂,说明y是氧化钙,A、B可发生中和反应,说明AB是酸和碱的反应,D是生活中最常见的液体,说明D是水,然后逐步推导得出其他物质的化学式.(1)B能用来检验二氧化碳的存在,说明B是氢氧化钙,俗称熟石灰或消石灰;
故本题答案为:熟石灰或消石灰,CO2+Ca(OH)2=CaCO3↓+H2O;
(2)将B的固体粉末与(NH4)2SO4等混合研磨,则铵态氮肥遇碱能生成有刺激性气味的气体,可区别氮肥和钾肥;
故本题答案为:铵态氮;
(3)是生活中最常见的液体,说明D是水,能通电分解生成氢气和氧气,F是一种清洁能源,说明F是氢气,则G是氧气,y常用作食品干燥剂,能与水反应生成氢氧化钙,说明y是氧化钙,x是目前应用最广泛的金属,说明x是铁,铁和氧气在点燃的条件下生成四氧化三铁,燃烧的现象是:剧烈燃烧,火星四射,放出热量,生成黑色固体;
故本题答案为:CaO+H2O=Ca(OH)2,剧烈燃烧,火星四射,生成黑色固体;3Fe+2O2
点燃
.
Fe3O4
(4)铁能与硫酸铜反应生成硫酸亚铁和铜,A、B可发生中和反应,则A为酸,能与铁反应生成氯化亚铁,说明A是盐酸,与氢氧化钙反应生成了氯化钙,氯化钙能与碳酸钠反应生成碳酸钙沉淀和氯化钠;
故本题答案为:Fe+CuSO4=FeSO4+Cu,CaCl2+Na2CO3═CaCO3↓+2NaCl.点评:
本题考点: 物质的鉴别、推断;铵态氮肥的检验;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 此题为框图式物质推断题,完成此类题目,关键是找准解题突破口,直接得出结论,然后利用顺向或逆向或两边向中间推,逐一导出其他结论.1年前查看全部
- 煤经气化和液化两个物理变化过程,可变为清洁能源为什么错了?
 ct9806351年前2
ct9806351年前2 -
 济公大师 共回答了23个问题
济公大师 共回答了23个问题 |采纳率91.3%煤气化是一个热化学过程.以煤或煤焦为原料,以氧气(空气、富氧或纯氧)、水蒸气或氢气等作气化剂,在高温条件下通过化学反应将煤或煤焦中的可燃部分转化为气体燃料的过程.1年前查看全部
- 我国著名发明家邹德俊发明的“吸盘式” 挂衣钩如图1-2-15,将它紧压在平整、清洁的竖直瓷砖墙面上时,可挂上衣帽等物品.
我国著名发明家邹德俊发明的“吸盘式” 挂衣钩如图1-2-15,将它紧压在平整、清洁的竖直瓷砖墙面上时,可挂上衣帽等物品.如果挂衣钩的吸盘压紧时,它的圆面直径为1/10√πm,吸盘圆面压在墙上有4/5的面积跟墙面完全接触,中间1/5未接触部分间无空气.已知吸盘面与墙面之间的动摩擦因数为0.5,则这种挂钩最多能挂多重的物体?(大气压器p0=1.0×105Pa)
我的问题是,P=FS面积为什么不是圆面积的4/5而是完整圆面积? 塞外飞车1年前2
塞外飞车1年前2 -
 lngk 共回答了22个问题
lngk 共回答了22个问题 |采纳率90.9%你的问题在于:你忽略了摩擦力的一个重要性质——摩擦力与接触面积无关.
滑动摩擦力(包括最大静摩擦力)的计算公式是:
f = μN;
其中:
μ 是滑动摩擦因数:与物体和支撑面的接触面的粗糙度有关,而与接触面积无关;
N 是正压力:指的是 “物体与支撑面之间的相互作用力,在垂直它们的接触面方向上的分量”.因为 “相互作用力” 其实是一对作用力和反作用力,所以,上面所说的正压力可以是这二者中的任意一个.记住:正压力只要求与接触面垂直,却没有要求从 “谁” 指向 “谁”.
本题摩擦力所涉及的两物体是:吸盘和墙面;所以,所求的 “正压力” 就是:
吸盘对墙面的压力;或:墙面对吸盘的支持力;
而根据吸盘在此方向上受力平衡,可知:
墙面对吸盘的支持力 = 大气对吸盘上的全部大气压力;
所以,求大气压力时所用的面积,是全部而不是 4/5.1年前查看全部
- 氢气是最清洁的燃料,计算200g氢气完全燃烧生成水的质量.
 hitbit200021年前2
hitbit200021年前2 -
 langjitianya328 共回答了17个问题
langjitianya328 共回答了17个问题 |采纳率94.1%解题思路:根据化学方程式的有关计算方法、步骤和格式,进行计算即可.设,200 g H2完全燃烧生成水的质量为x.
2H2+O2
点燃
.
2H2O
436
200gx
[4/200g=
36
x]
x=1800 g
答:200 g H2完全燃烧生成水的质量为1800 g.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 本题重点考查了化学方程式的有关计算方法、步骤和格式;它是一道很传统的根据化学方程式计算的题目.解答时,只要细心地分析审题后,按照有关化学方程式的计算步骤和格式,进行计算即可.1年前查看全部
- A、B、C三种元素,A元素的单质是最清洁的燃料;B元素的单质能在C元素的单质中剧烈燃烧,火星四射,生成黑色固体;B元素的
A、B、C三种元素,A元素的单质是最清洁的燃料;B元素的单质能在C元素的单质中剧烈燃烧,火星四射,生成黑色固体;B元素的单质是目前世界上年产量最高的金属.
(1)写出下列元素的名称或符号:A______;
(2)写出B、C二种元素组成的一种化合物的名称:______;
(3)写出B元素的单质在C元素的单质中剧烈燃烧的化学方程式3Fe+2O2
Fe3O4点燃 .3Fe+2O2.
Fe3O4点燃 . 渡边一1年前1
渡边一1年前1 -
 y_tina 共回答了18个问题
y_tina 共回答了18个问题 |采纳率94.4%解题思路:本题属于推断题,根据题目给出的信息:A元素的单质是最清洁的燃料,因此A元素的单质是氢气,A元素是氢元素;B元素的单质能在C元素的单质中剧烈燃烧,火星四射,生成黑色固体;铁在氧气中燃烧生成四氧化三铁,铁元素的单质是目前世界上年产量最高的金属,B是铁元素,C是氧元素;B、C二种元素组成的化合物是氧化铁或四氧化三铁.(1)A元素的单质是最清洁的燃料,因此A元素的单质是氢气,A元素是氢元素,故答案为:氢元素或H;
(2)铁在氧气中燃烧生成四氧化三铁,铁元素的单质是目前世界上年产量最高的金属,B是铁元素,C是氧元素,B、C二种元素组成的化合物是氧化铁或四氧化三铁等;故答案为:氧化铁或四氧化三铁等;
(3)铁在氧气中燃烧生成四氧化三铁,配平即可,故答案为:3Fe+2O2
点燃
.
Fe3O4点评:
本题考点: 物质的鉴别、推断;元素的符号及其意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 本考点属于物质的推断题,是通过对实验方法和过程的探究,在比较鉴别的基础上,得出了正确的实验结论.此考点主要出现在填空题和实验题中.1年前查看全部
- A、B、C、D四种元素,A元素的单质是最清洁的燃料,B元素的单质是空气里最多的气体,C元素是地壳中最多的元素,D2+离子
A、B、C、D四种元素,A元素的单质是最清洁的燃料,B元素的单质是空气里最多的气体,C元素是地壳中最多的元素,D2+离子核外有10个电子.回答下列问题:
(1)写出四种元素的名称或符号:A______、B______、C______、D______;
(2)A、B、C三种元素组成的一种碱的化学式为______;
(3)D的单质在C的单质中燃烧的化学方程式为2Mg+O2
2MgO点燃 .2Mg+O2.
2MgO点燃 . 熊猫貔貅1年前1
熊猫貔貅1年前1 -
 zhanglaomi 共回答了17个问题
zhanglaomi 共回答了17个问题 |采纳率94.1%(1)根据题意:A元素的单质是最清洁的燃料,可推断A元素为:氢或H;
B元素的单质是空气里最多的气体,可推断B元素为:氮或N;
C元素是地壳中最多的元素为氧,可推断C元素为:氧或O;
D2+离子核外有10个电子,则D元素的质子数为:2+8+2=12,可推知D元素为:或镁Mg;
故答案为:氢或H;氮或N;氧或O;镁或Mg;
(2)根据碱指电离时产生的阴离子全部都是氢氧根离子的化合物;可推断由H,N,O 3种元素组成的碱为:NH3•H2O;
故答案为:NH3•H2O;
(3)根据书写化学方程式的步骤:写配注等,镁在氧气中燃烧的化学方程式为:2Mg+O2
点燃
.
2MgO;
故答案为:2Mg+O2
点燃
.
2MgO.1年前查看全部
- 氢能源是一种重要的清洁能源.现有两种可产生H2的化合物甲和乙.将6.00g甲加热至完全分解,只得到一种短周期元素的金属单
氢能源是一种重要的清洁能源.现有两种可产生H2的化合物甲和乙.将6.00g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72L的H2(已折算成标准状况).甲与水反应也能放出H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液.化合物乙的式量为19,乙与水反应也能产生氢气;化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状况下的密度为1.25g•L-1.请回答下列问题:
(1)甲与水反应的化学方程式是______.
(2)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式2NH4H+5CuO
5Cu+N2↑+5H2O△ .2NH4H+5CuO.有人提出生成的产物Cu中可能还混有Cu2O,请设计实验方案验证之.(已知:Cu2O+2H+=Cu+Cu2++H2O)______.
5Cu+N2↑+5H2O△ . sa_tsui1年前1
sa_tsui1年前1 -
 相约07 共回答了12个问题
相约07 共回答了12个问题 |采纳率83.3%解题思路:甲加热至完全分解,只得到一种短周期元素的金属单质和6.72L H2,则甲中含有H元素,甲与水反应能产生H2,同时产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液,应为Al(OH)3,综上可知,甲中含有Al和H两种元素,n(H2)=[6.72L/22.4L/mol]=0.3mol,则m(H)=0.3mol×2×1g/mol=0.6g,则6.00g甲中含有m(Al)=6.00g-0.6g=5.4g,n(Al)=[5.4g/27g/mol]=0.2mol,所以n(Al):n(H)=0.2mol:0.6mol=1:3,则甲的化学式为AlH3;
乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状况下的密度为1.25g/L,则丙的相对原子质量为1.25×22.4=28,应为N2,化合物乙的式量为19,分子中只能有1个N原子,故含有H原子数目=[19−14/1]=5,分子式为NH5,乙与水反应也能产生氢气,应为NH4H,据此解答.甲加热至完全分解,只得到一种短周期元素的金属单质和6.72L H2,则甲中含有H元素,甲与水反应能产生H2,同时产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液,应为Al(OH)3,综上可知,甲中含有Al和H两种元素,n(H2)=[6.72L/22.4L/mol]=0.3mol,则m(H)=0.3mol×2×1g/mol=0.6g,则6.00g甲中含有m(Al)=6.00g-0.6g=5.4g,n(Al)=[5.4g/27g/mol]=0.2mol,所以n(Al):n(H)=0.2mol:0.6mol=1:3,则甲的化学式为AlH3;
乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状况下的密度为1.25g/L,则丙的相对原子质量为1.25×22.4=28,应为N2,化合物乙的式量为19,分子中只能有1个N原子,故含有H原子数目=[19−14/1]=5,分子式为NH5,乙与水反应也能产生氢气,应为NH4H,
(1)由上述分析可知,甲的化学式是AlH3,AlH3与水发生水解反应,反应的方程式为:AlH3+3H2O=Al(OH)3↓+3H2↑,
故答案为:AlH3+3H2O=Al(OH)3↓+3H2↑;
(2)乙的化学式是NH4H,NH4H在加热条件下与CuO反应可生成Cu、氮气和水,该反应的化学方程式为:2NH4H+5CuO
△
.
5Cu+N2↑+5H2O,要判断产物中是否含有Cu2O,可加入稀硫酸检验溶液是否变蓝,方法是:取样后加H2SO4,如果溶液变蓝,说明产物中含有Cu2O,反之则无Cu2O,
故答案为:2NH4H+5CuO
△
.
5Cu+N2↑+5H2O;取样后加H2SO4,如果溶液变蓝,说明产物中含有Cu2O,反之则无Cu2O.点评:
本题考点: 无机物的推断.
考点点评: 本题考查无机物的推断,属于计算型推断,注意根据反应的现象以及数据判断甲乙两种物质,侧重考查学生对知识的迁移应用,题目难度中等.1年前查看全部
- 2011广东厚街国际车展上,展出的新能源车型和清洁能源车型比任何一届车展都多,据此回答。
2011广东厚街国际车展上,展出的新能源车型和清洁能源车型比任何一届车展都多,据此回答。
若新能源汽车被广泛使用,将产生的积极影响是A.缓解城市交通压力 B.减轻大气污染 C.促进经济快速发展 D.提高能源利用率  鹿角的奶酪1年前1
鹿角的奶酪1年前1 -
 wuyonggui 共回答了12个问题
wuyonggui 共回答了12个问题 |采纳率91.7%B
本题考查新能源。新能源相比较常规能源的一大优势是清洁,环保。1年前查看全部
- 甲醇是基础有机化工原料和新型清洁燃料,广泛用于制造各种燃料电池。工业上以甲烷和水蒸气为原料制备甲醇,反应过程如下。
甲醇是基础有机化工原料和新型清洁燃料,广泛用于制造各种燃料电池。工业上以甲烷和水蒸气为原料制备甲醇,反应过程如下。
反应Ⅰ:CH 4 (g)+H 2 O(g) CO(g)+3H 2 (g) △H1
CO(g)+3H 2 (g) △H1
反应Ⅱ:CO(g)+2H 2 (g) CH 3 OH(g) △H2
CH 3 OH(g) △H2
(1)如图是反应1进行过程中的能量变化示意图。根据图象判断,升高温度,反应I的平衡常数将____________ (填“增大”、“减小”或“不变”)。反应I的逆反应的活化能为___________(用含E1、E2的表达式表示)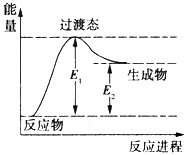
(2)已知在催化剂和一定压强下,反应?能自发进行。若保持容器容积不变,下列措施可增加该反应中CO转化率的是___________(填字母)。
A.适当降低温度
B.将甲醇从反应体系中分离出来
C.充入He,使体系总压强增大
D.按原比例再充入CO和H 2
(3)一种甲醇燃料电池以多孔石墨为电极,一极通入甲醇蒸气,另一极通入氧气,电解质溶液为4L 1 moI/L的KOH溶液。当有3 mol甲醇放电时,电解质溶液中各种离子的浓度由大到小的顺序为_________________
(4)下图甲是一种甲醇燃料电池的结构示意图,甲醇提供质子和电子,电子经外电路到达另一极与氧气反应,电池总反应为2CH 3 OH+3O 2 2CO 2 +4H 2 O。
2CO 2 +4H 2 O。
①M电极的电极反应式为______________________________。
②以上述电池做电源,用乙图所示装置,在实验室中模拟铝制品表面“钝化”处理的过程中,发现Al电极附近逐渐变浑浊并有气泡逸出,原因是(用离子方程式表示):______________。Al电极应接燃料电池的___________(填“M”或“N”)极。 llc4444441年前1
llc4444441年前1 -
 1000712 共回答了29个问题
1000712 共回答了29个问题 |采纳率86.2%1年前查看全部
- (2010•河池)自去年秋季以来,我市部分县受到严重的旱灾,人畜饮水都非常困难.为此农村打井兴建简易的自来水厂,喝上清洁
(2010•河池)自去年秋季以来,我市部分县受到严重的旱灾,人畜饮水都非常困难.为此农村打井兴建简易的自来水厂,喝上清洁的水.
(1)地下水的酸碱度可用pH试纸pH试纸测定.
(2)自然界的水经过一系列净化处理后,成为比较清洁的自来水.下列与自来水的净化过程无关的是CC(填序号)
A.过滤B.消毒C.电解
(3)硬水给生活和生产带来很多麻烦,平时可用肥皂水肥皂水来区分硬水和软水.
(4)水在自然界中不断循环,下列有关水蒸发的说法,正确的是AA(填序号).
A.水分子不断运动B.水分子变大C.水分子间的间隔变小. 娃哈哈uzd41年前1
娃哈哈uzd41年前1 -
 lanjianbee 共回答了22个问题
lanjianbee 共回答了22个问题 |采纳率90.9%(1)酸碱度的测定要用pH试纸,故答案为:pH试纸;
(2)净化水的方法有:沉淀、过滤、吸附、消毒、蒸馏等,故答案为:C;
(3)硬水和软水的区分方法是加肥皂水,泡沫较多的是软水,较少或没有的是硬水,故答案为:肥皂水;
(4)水蒸发水是物理变化,水分子受热运动速率增大,水分子没有变化.故答案为:A;1年前查看全部
- 在治理北京的大气和水污染的措施中,不可行的是( ) A.抑制水中所有动植物的生长 B.公共汽车改用清洁燃料车 C.禁止
在治理北京的大气和水污染的措施中,不可行的是( ) A.抑制水中所有动植物的生长 B.公共汽车改用清洁燃料车 C.禁止使用含硫高的劣质煤 D.禁止排放未经处理的废水  lucyzy20051年前1
lucyzy20051年前1 -
 dtdy 共回答了17个问题
dtdy 共回答了17个问题 |采纳率94.1%A、水中有的动植物生长有利于净化水,故A错误;
B、公共汽车改用清洁燃料车能减少对空气的污染,故B正确;
C、含硫高的劣质煤燃烧能产生二氧化硫气体,容易形成酸雨,故C正确;
D、排放未经处理的废水容容易污染水体,所以禁止排放废水,故D正确.
故选A.1年前查看全部
- 开发使用清洁能源,发展“低碳经济”正成为科学家研究的主要课题.氢气、甲醇是优质的清洁燃料,可制作燃料电池.
 开发使用清洁能源,发展“低碳经济”正成为科学家研究的主要课题.氢气、甲醇是优质的清洁燃料,可制作燃料电池.
开发使用清洁能源,发展“低碳经济”正成为科学家研究的主要课题.氢气、甲醇是优质的清洁燃料,可制作燃料电池.
(1)甲烷水蒸气转化法制H2的主要转化反应如下:
CH4(g)+H2O(g)⇌CO(g)+3H2(g)△H=+206.2kJ•mol-1
CH4(g)+2H2O(g)⇌CO2(g)+4H2(g)△H=+165.0kJ•mol-1
上述反应所得原料气中的CO能使合成氨的催化剂中毒,必须除去.工业上常采用催化剂存在下CO与水蒸气反应生成易除去的CO2,同时可制得等体积的氢气的方法.此反应称为一氧化碳变换反应,该反应的热化学方程式是______.
(2)生产甲醇的原料CO和H2来源于:CH4(g)+H2O(g)⇌CO(g)+3H2(g)△H>0
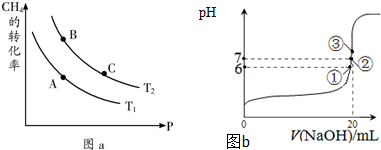
①一定条件下CH4的平衡转化率与温度、压强的关系如图a.则A、B、C三点处对应平衡常数(KA、KB、KC)的大小关系为______.(填“<”、“>”、“=”);
②100℃时,将1mol CH4和2mol H2O通入容积为1L的定容密封容器中,发生反应,能说明该反应已经达到平衡状态的是______.
a.容器内气体密度恒定
b.单位时间内消耗0.1mol CH4同时生成0.3molH2
c.容器的压强恒定
d.3v正(CH4)=v逆(H2)
(3)25℃时,在20mL0.1mol/L氢氟酸中加入VmL0.1mol/L NaOH溶液,测得混合溶液的pH变化曲线如图b所示,下列说法正确的是______.
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(Na+)=0.1mol/L
(4)长期以来,一直认为氟的含氧酸不存在.1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H-O-F.HFO与水反应得到HF和化合物A,该反应的化学方程式为______. eiowenig1年前1
eiowenig1年前1 -
 美yy大uu卡特 共回答了23个问题
美yy大uu卡特 共回答了23个问题 |采纳率91.3%解题思路:(1)根据盖斯定律书写目标热化学方程式;
(2)①平衡常数只受温度影响,处于等温线上各点平衡常数相等,由图可知,压强一定时,温度T2条件下,甲烷的转化率更大,则反应进行的程度更大;
②达到平衡状态时,正逆反应速率相等,各物质的浓度不变,百分含量不变,以及由此衍生其它一些物理量不变,据此结合选项判断;
(3)A.酸或碱抑制水电离,含有弱根离子的盐促进水电离;
B.根据电荷守恒计算;
C.根据电荷守恒计算;
D.等物质的量的氢氟酸和氢氧化钠恰好反应生成氟化钠,溶液呈碱性,根据电荷守恒判断,注意等体积混合时,不水解离子浓度变为原来的一半;
(4)电负性F>O,故H-O-F中F元素表现-1价,与水反应生成HF,发生水解反应,可推知A为H-O-O-H.(1)已知:①CH4(g)+H2O(g)⇌CO(g)+3H2(g)△H=+206.2kJ•mol-1
②CH4(g)+2H2O(g)⇌CO2(g)+4H2(g)△H=+165.0kJ•mol-1
根据盖斯定律,②-①得:CO(g)+H2O(g)⇌CO2(g)+H2(g)△H=-41.2 kJ•mol-1,
故答案为:CO(g)+H2O(g)⇌CO2(g)+H2(g)△H=-41.2 kJ•mol-1;
(2)①平衡常数只受温度影响,B、C处于等温线上,平衡常数相等,由图可知,压强一定时,温度T2条件下,甲烷的转化率更大,则反应进行的程度更大,比温度T1时的平衡常数大,故平衡常数KC=KB>KA,
故答案为:KC=KB>KA;
②a.100℃时,反应混合物都是气体,混合气体总质量不变,容器的容积不变,容器内气体密度始终不变,不能说明得到平衡,故a错误;
b.单位时间内消耗0.1mol CH4同时生成0.3molH2,反应始终按此比例进行,不能说明到达平衡,故b错误;
c.随反应进行混合气体总物质的量增大,容器容积不变,压强增大,当容器的压强恒定时,说明到达平衡,故c正确;
d.3v正(CH4)=v逆(H2),不能物质的正逆速率之比等于化学计量数之比,反应到达平衡,故d正确,
故答案为:cd;
(3)A.氢氟酸抑制水电离,氟化钠促进水电离,所以pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的不相等,故错误;
B.①点时pH=6,溶液中存在电荷守恒,c(F-)+c(OH-)=c(Na+)+c(H+),所以c(F-)-c(Na+)=c(H+)-c(OH-)=9.9×10-7mol/L,故正确;
C.②点时,溶液呈中性,c(OH-)=c(H+),溶液中存在电荷守恒,c(F-)+c(OH-)=c(Na+)+c(H+),所以c(F-)=c(Na+),故正确;
D.③点时V=20mL,此时溶液中溶质在氟化钠,溶液呈碱性,根据电荷守恒知c(F-)<c(Na+),但等体积混合时不水解的离子浓度变为原来的一半,所以c(F-)<c(Na+)=0.05mol/L,故错误;
故选BC;
(4)电负性F>O,故H-O-F中F元素表现-1价,与水反应生成HF,发生水解反应,可推知A为H-O-O-H,该反应的化学方程式为:H2O+HFO=HF+H2O2,
故答案为:H2O+HFO=HF+H2O2.点评:
本题考点: 转化率随温度、压强的变化曲线;热化学方程式;化学平衡状态的判断.
考点点评: 本题比较综合,涉及热化学方程式、化学平衡图象及影响因素、平衡常数、平衡状态判断、弱电解质的电离、离子浓度比较等,(3)中注意溶液中离子浓度等量关系,经常考虑电荷守恒、物料守恒、质子恒等式等.1年前查看全部
- (2014•浙江模拟)二甲醚(CH3OCH3)以其优良的性质,被称为21世纪的新型“清洁能源”,在未来可能替代柴油和液化
 (2014•浙江模拟)二甲醚(CH3OCH3)以其优良的性质,被称为21世纪的新型“清洁能源”,在未来可能替代柴油和液化气作为洁净液体燃料使用.工业上以C0和H2为原料生产CH30CH3的新工艺主要发生三个反应:
(2014•浙江模拟)二甲醚(CH3OCH3)以其优良的性质,被称为21世纪的新型“清洁能源”,在未来可能替代柴油和液化气作为洁净液体燃料使用.工业上以C0和H2为原料生产CH30CH3的新工艺主要发生三个反应:
①CO(g)+2H2(g)⇌CH3OH(g)△H1=-91KJ•mol-1
②2CH30H(g)⇌CH30CH3(g)+H20(g)△H2=-24KJ•mol-1
③CO(g)+H2O(g)⇌CO2(g)+H2(g)△H3=-41KJ•mol-1
回答下列问题:
(1)写出新工艺的总反应的热化学方程式:______,平衡常数表达式K=c(CH3OCH3)c(CO2) c3(CO)c3(H2) .c(CH3OCH3)c(CO2) c3(CO)c3(H2)
(2)一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是______(填字母代号).
a.低温高压b.加入催化剂c.减少CO2的浓度d.增加CO的浓度
(3)在某温度下,2L密闭容器中发生反应①,起始时CO、H2的物质的量分别为2mol和6mol,3min后达到平衡,测得CO的转化率为60%,则3min内CO的平均反应速率为______.若同样条件下起始时CO的物质的量为4mol,达到平衡后CH3OH为2.4mol,则起始时H2的物质的量为:______.
(4)某温度下在2L恒容密闭容器中加入CH3OH发生反应②,测得有关数据如下:
则此反应在该温度下的平衡常数为______,若再向容器分别加入甲醇0.02mol、CH3OCH3 1.0mol,此时该反应v正反应______v逆反应(填“>”、“<”或“=”).反应时间/min 0 1 2 3 4 c(CH3OH)/mol•L-1 0.51 0.2 0.1 0.01 0.01
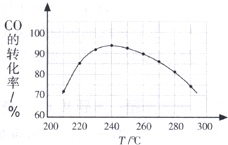
(5)为了寻找合适的反应温度,研究者进行了一系列试验,每次试验保持原料气组成、压强、反应时间等因素不变,试验结果CO转化率随温度变化的规律如图试解释原因是:______. cnlamar1年前1
cnlamar1年前1 -
 xddhh 共回答了7个问题
xddhh 共回答了7个问题 |采纳率85.7%解题思路:(1)根据盖斯定律计算△H;平衡常数指产物浓度系数次幂的乘积与反应物浓度系数次幂的乘积的比值;
(2)要提高CO的转化率,应该不条件平衡正向进行方向判断;
(3)依据化学平衡三段式列式计算,结合平衡常数计算 氢气起始量;
(4)根据表中数据,3分钟后达到平衡状态,计算出该反应的平衡常数;向容器分别加入甲醇0.02mol、CH3OCH31.0mol,重新计算出浓度商,与化学平衡常数对比,判断平衡移动方向;
(5)由图表可知,在较低温时,反应体系均未达到平衡,CO的转化率主要受反应速率影响,随着温度的升高反应速率增大,CO的转化率也增大;在较高温时,反应体系均已达到平衡,随着温度的升高平衡向逆反应方向移动,CO的转化率减小.(1)已知①CO( g)+2H2(g)⇌CH3OH( g)△H1=-91kJ•mol-1,
②2CH30H(g)⇌CH30CH3(g)+H20(g)△H2=-24kJ•mol-1,
③CO(g)+H2O(g)⇌CO2(g)+H2(g)△H3=-41kJ•mol-1,
根据盖斯定律,①×2+②+③得3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g)△H=-247kJ•mol-1,
平衡常数指产物浓度系数次幂的乘积与反应物浓度系数次幂的乘积的比值,所以K=
c(CH3OCH3)c(CO2)
c3(CO)c3(H2);
故答案为:3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g)△H=-247KJ•mol-1,
c(CH3OCH3)c(CO2)
c3(CO)c3(H2);
(2)一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施应使平衡正向进行,3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g)△H=-247KJ•mol-1;
a.反应是气体体积减小的放热反应,低温高压平衡正向进行,一氧化碳转化率增大,故a正确;
b.加入催化剂 改变反应速率不改变化学平衡,一氧化碳转化率不变,故b错误;
c.减少CO2的浓度,平衡正向进行,一氧化碳转化率增大,故c正确;
d.增加CO的浓度,平衡正向进行,一氧化碳转化率减小,故d错误;
故答案为:ac;
(3)在某温度下,2L密闭容器中发生反应①,起始时CO、H2的物质的量分别为2mol和6mol,3min后达到平衡,测得CO的转化率为60%,依据化学平衡三段式列式计算:
CO(g)+2H2(g)⇌CH3OH(g)
起始量(mol/L) 1 3 0
变化量(mol/L) 0.6 0.6 0.2
平衡量(mol/L) 0.4 2.4 0.2
则3min内CO的平均反应速率=[0.6mol/L/3min]=0.2mol/L•min;
若同样条件下起始时CO的物质的量为4mol,达到平衡后CH3OH为2.4mol,设氢气起始量ymol/L
CO(g)+2H2(g)⇌CH3OH(g)
起始量(mol/L)2y 0
变化量(mol/L)1.2 2.4 1.2
平衡量(mol/L) 0.8 y-2.41.2
依据化学平衡常数不变计算得到
1.2
0.8×(y−2.4)2=
0.2
0.4×2.42
y=4.2mol/L;
氢气物质的量为8.4mol
故答案为:0.2 mol•L-1•min-1,8.4 mol;
(4)根据反应方程式:2CH3OH(g)⇌CH3OCH3(g)+H2O(g),
反应前c(CH3OH)/mol•L-1:0.51 0 0
3分钟后达到平衡状态浓度:0.01 0.25 0.25
平衡常数为:
0.25×0.25
0.012=625,
再向容器分别加入甲醇0.02mol、CH3OCH31.0mol反应的浓度商为:
(1.0+0.25)×0.25
0.032≈347.2<625,平衡向着正向移动,正反应速率大于逆反应速率,
故答案为:625;>;
(5)由图表可知,温度低于240℃时,CO的转化率随着温度的升高而增大;温度高于240℃时,CO的转化率随着温度的升高而减小,
在较低温时,各反应体系均未达到平衡,CO的转化率主要受反应速率影响,随着温度的升高反应点评:
本题考点: 化学平衡的计算;热化学方程式;化学平衡的影响因素;化学平衡的调控作用.
考点点评: 本题考查反应热的计算、平衡移动、化学平衡常数等,难度中等,难点在于读图明白温度为240℃时反应体系均已达到平衡.1年前查看全部
- 太阳能是一种清洁、无污染的理想能源,太阳能热水器内盛有200kg的水,在阳光的照射下,温度上升40℃.[c水=4.2×l
太阳能是一种清洁、无污染的理想能源,太阳能热水器内盛有200kg的水,在阳光的照射下,温度上升40℃.[c水=4.2×lO3J/(kg•℃),q液化石油气=4.9×lO7J/kg]求:
(1)水吸收了多少的热量?
(2)这些热量相当于完全燃烧多少千克的液化石油气? xx新手1年前1
xx新手1年前1 -
 天使潘多拉 共回答了13个问题
天使潘多拉 共回答了13个问题 |采纳率84.6%解题思路:(1)已知水的比热容、质量和温度变化,可利用公式Q吸=cm△t计算热量.(2)已知热量和液化石油气热值,可利用公式m=Q放q计算质量.(1)水吸收的热量:
Q吸=c水m△t=4.2×103J/(kg•℃)×200kg×40℃=3.36×1O7J.
(2)∵Q放=Q吸=3.36×1O7J,q=4.9×107J/kg
∴由q=
Q放
m得:
m′=
Q放
q=
3.36×107J
4.9×107J/kg≈0.69kg.
答:(1)水吸收了3.36×1O7J的热量.
(2)这些热量相当于完全燃烧0.69kg的液化石油气.点评:
本题考点: 热平衡方程的应用.
考点点评: 本题考查了利用热量的公式Q=Cm△t进行分析和计算,并可利用热量的公式变形m=Q放q计算质量,同时培养了学生一种节约能源的意识.1年前查看全部
- A、B可发生中和反应,D是生活中最常见的液体.通常情况下,F、G、I为气体,且F是一种清洁能源.x是目前应用最广泛的金属
A、B可发生中和反应,D是生活中最常见的液体.通常情况下,F、G、I为气体,且F是一种清洁能源.x是目前应用最广泛的金属,y常用作食品干燥剂.各物质间的转化关系如图所示(个别产物略去).

(1)Y俗称______,它常用作食品干燥剂,是因为______.(用化学方程式表示)
(2)反应⑤的化学方程式为______,该反应说明在农业生产中,铵盐氮肥不能与______性物质混合施用.
(3)金属X的化学式______.
(4)金属x也能与硫酸铜溶液反应,其化学方程式为______. 猫小侠1年前1
猫小侠1年前1 -
 woyao48 共回答了14个问题
woyao48 共回答了14个问题 |采纳率100%解题思路:根据F是一种清洁能源,所以F是氢气,x是目前应用最广泛的金属,所以x是铁,铁和盐酸反应生成氯化亚铁和氢气,所以A是盐酸,D是生活中最常见的液体,通电会生成氢气和G,所以D是水,G是氧气,氧气和铁反应会生成四氧化三铁,所以H是四氧化三铁,y常用作食品干燥剂,y和水反应会生成B,B和盐酸会发生中和反应,所以y是氧化钙,B是氢氧化钙,氢氧化钙和硫酸铵反应会生成硫酸钙、水和氨气,所以I是氨气,盐酸和氢氧化钙反应生成氯化钙和水,所以C是氯化钙,氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,所以E是碳酸钙,然后将推出的各种物质代入转化关系中验证即可.(1)F是一种清洁能源,所以F是氢气,x是目前应用最广泛的金属,所以x是铁,铁和盐酸反应生成氯化亚铁和氢气,所以A是盐酸,D是生活中最常见的液体,通电会生成氢气和G,所以D是水,G是氧气,氧气和铁反应会生成四氧化三铁,所以H是四氧化三铁,y常用作食品干燥剂,y和水反应会生成B,B和盐酸会发生中和反应,所以y是氧化钙,B是氢氧化钙,氢氧化钙和硫酸铵反应会生成硫酸钙、水和氨气,所以I是氨气,盐酸和氢氧化钙反应生成氯化钙和水,所以C是氯化钙,氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,所以E是碳酸钙,经过验证,推出的各种物质均满足题中的转化关系,推导正确,所以Y是氧化钙,俗称生石灰,氧化钙和水反应会生成氢氧化钙,所以常用作食品干燥剂,化学方程式为:CaO+H2O=Ca(OH)2;
(2)反应⑤是氢氧化钙和硫酸铵反应生成硫酸钙、水和氨气,化学方程式为:Ca(OH)2+(NH4)2SO4=CaSO4+2H2O+2NH3↑,该反应说明在农业生产中,铵盐氮肥不能与碱性物质混合施用;
(3)通过推导可知,x是Fe;
(4)铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=FeSO4+Cu.
故答案为:(1)生石灰,CaO+H2O=Ca(OH)2;
(2)Ca(OH)2+(NH4)2SO4=CaSO4+2H2O+2NH3↑,碱;
(3)Fe;
(4)Fe+CuSO4=FeSO4+Cu.点评:
本题考点: 物质的鉴别、推断;书写化学方程式、文字表达式、电离方程式.
考点点评: 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.1年前查看全部
- 据报导,我国某些城市的酸雨严重,为改变这一状况,某市正准备推广使用的清洁能源,下列所列能源不是清洁能源的是( )
据报导,我国某些城市的酸雨严重,为改变这一状况,某市正准备推广使用的清洁能源,下列所列能源不是清洁能源的是( )
A. 太阳能
B. 石油
C. 天然气
D. 酒精 qdlqdl19591年前1
qdlqdl19591年前1 -
 suntao207 共回答了24个问题
suntao207 共回答了24个问题 |采纳率95.8%解题思路:石油属于化石燃料成分比较复杂,燃烧时生成的有害物质较多,不是清洁能源;而天然气和酒精燃烧后,只生成水和二氧化碳,没有硫的氧化物(煤的燃烧),没有氮氧化物、一氧化碳等有害物质,太阳能没有污染物,所以都属于清洁能源.A、太阳能无污染,属于清洁能源,故A不选;
B、石油成分比较复杂,燃烧时生成的有害物质较多,不是清洁能源,故B选;
C、天然气燃烧后,只生成水和二氧化碳,没有硫的氧化物(煤的燃烧),没有氮的氧化物等有害物质,属于清洁能源,故C不选;
D、酒精燃烧后,只生成水和二氧化碳,没有硫的氧化物(煤的燃烧),没有氮氧化物等有害物质,属于清洁能源,故D不选.
故选B.点评:
本题考点: 清洁能源.
考点点评: 本题考查了清洁能源的使用,题目难度不大,注意能源的开发、利用以及燃烧产物对环境的影响等问题.1年前查看全部
- 石油价格的不断上调,引起了消费者对未来能源的关注.下列燃料中被认为是最清洁能源的是( ) A.煤 B.液化石油气 C.
石油价格的不断上调,引起了消费者对未来能源的关注.下列燃料中被认为是最清洁能源的是( ) A.煤 B.液化石油气 C.甲烷 D.氢气  风中黄叶1年前1
风中黄叶1年前1 -
 沧海遗玉 共回答了13个问题
沧海遗玉 共回答了13个问题 |采纳率84.6%A、煤是古代植物经若干年复杂的变化形成的,不可再生,且燃烧可产生大量空气污染物,所以错误.
B、石油是古代的海洋生物经若干年复杂的变化形成的,不可再生,且燃烧可产生大量空气污染物,所以错误.
C、天然气是古代的海洋生物经若干年复杂的变化形成的,不可再生,且燃烧可产生少量空气污染物,所以错误.
D、氢气作为燃料有三大优点:①热值高,②可再生,③产物是无污染的水,所以正确.
故选D.1年前查看全部
- 甲烷是一种清洁燃料.某密闭的容器有甲烷(CH4)、氧气、二氧化碳三种物质,在一定条件下,它们充分发生化学反应.测得反应前
甲烷是一种清洁燃料.某密闭的容器有甲烷(CH4)、氧气、二氧化碳三种物质,在一定条件下,它们充分发生化学反应.测得反应前后各物质的质量如下表:
请根据表中的信息,判断下列说法正确的是( )物质 甲烷 氧气 二氧化碳 水 反应前物质的质量(g) 16 70 1 0 反应后物质的质量(g) 0 x 45 36
A.甲烷燃烧不会产生温室气体
B.表中“x”的值为6
C.该反应为分解反应
D.10g甲烷在50g氧气中燃烧生成60g生成物 Just-a-Joke1年前1
Just-a-Joke1年前1 -
 bb269 共回答了15个问题
bb269 共回答了15个问题 |采纳率80%解题思路:根据质量守恒定律得出x的值,由物质质量的增减量可确定反应物和生成物的质量,反应后质量增加属于生成物,质量增加了多少,就是生成了多少,反应后质量减小,说明是反应物,减少的质量就是参加反应的质量,再根据反应物和生成物的种类判断反应类型.A、甲烷燃烧生成二氧化碳和水,二氧化碳属于温室效应的主要气体,故A说法错误;
B、根据质量守恒定律可以知道,X=16+70+1+0-0-45-36=6,故B说法正确;
C、甲烷反应后质量减少属于反应物,反应后氧气质量减少,属于反应物,二氧化碳反应后质量增加,属于生成物,开始没有水,最后有水了,说明水是生成物,反应物是两种,生成物是两种,所以该反应不是分解反应,故C说法错误;
D、设10g甲烷完全燃烧需要氧气的质量为x,则
CH4+2O2
点燃
.
CO2+2H20
1664
10g x
[16/64]=[10g/x],解得x=40g,因此10g甲烷在50g氧气中燃烧,氧气有剩余,所以不会生成60g生成物,故D说法错误.
故选:B.点评:
本题考点: 质量守恒定律及其应用;反应类型的判定.
考点点评: 掌握质量守恒定律的内容:在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,能够根据反应前后质量的变化来判断反应物和生成物,并能够根据反应特点来判断反应类型.1年前查看全部
- 下列各句中,加粗成语 下列各句中,加粗成语使用正确的一项是 [ ] A.卫生值日时,清洁区相邻的两个班各自为战,
下列各句中,加粗成语
下列各句中,加粗成语使用正确的一项是 [ ] a.卫生值日时,清洁区相邻的两个班各自为战,互相之间简直是 秋毫无犯 .
b.军事专家认为极超音速导弹是反恐战争中非常有价值的“猎杀者”,一旦锁定目标,***就 无地自容 了.
c.上清寺是最具传奇色彩的地方,周公馆、桂园、人民大礼堂、三峡博物馆……,举手投足 都可以窥见历史的遗踪和时代的发展.
d.在积极应对***的同时,人们强烈感受到吸取经验教训的重要性,希望在未来的日子里能 防患于未然 . 云天宝贝1年前1
云天宝贝1年前1 -
 pao1999 共回答了19个问题
pao1999 共回答了19个问题 |采纳率89.5%D1年前查看全部
- (2008•海南)构建和谐社会,建设社会主义新农村的目标之一是让农民饮用清洁的自来水.ClO2是新一代饮用水的消毒剂,我
(2008•海南)构建和谐社会,建设社会主义新农村的目标之一是让农民饮用清洁的自来水.ClO2是新一代饮用水的消毒剂,我国成功研制出制取ClO2的新方法,其反应的微观过程图如图:

试回答:
(1)ClO2叫做______,其中氯元素的化合价为______;
(2)根据反应的微观过程图写出反应的化学方程式______. zhongwelfp1年前1
zhongwelfp1年前1 -
 7oo了 共回答了16个问题
7oo了 共回答了16个问题 |采纳率87.5%解题思路:(1)物质化学式的读法,由两种元素物质,一般从右向左依次读出各元素的名称,并在两种元素间加上“化”字,当原子个数不是一个时一般要读出原子个数;利用物质的化学式,根据化合物中元素化合价代数和为零,可计算其中氯元素的化合价;
(2)根据反应微观图中各物质的分子构成模型图,判断分子的构成,利用分子构成写出物质的化学式,然后完成反应的化学方程式.(1)化学式ClO2中有氯、氧两种元素,且每个分子中含有两个氯原子和一个氧原子,因此,物质的化学式读为二氧化氯;
其中O为-2价,设Cl元素化合价为x,则x+(-2)×2=0,解得x=+4;
故答案为:二氧化氯;+4;
(2)该反应的反应物分子为:由两个氯原子构成的一个氯气Cl2分子,由一个钠原子、一个氯原子、两个氧原子构成的NaClO2分子;生成物的分子为:由一个氯原子、两个氧原子构成的ClO2分子,一个钠原子、一个氯原子构成的NaCl分子;因此,该反应的化学方程式可写为Cl2+2NaClO2=2ClO2+2NaCl;
故答案为:Cl2+2NaClO2═2ClO2+2NaCl.点评:
本题考点: 微粒观点及模型图的应用;化学式的书写及意义;有关元素化合价的计算;书写化学方程式、文字表达式、电离方程式.
考点点评: 根据构成物质的分子的微观模型图,可判断分子的构成,由分子的构成可确定物质的组成及物质的化学式.1年前查看全部
- (2014•娄底)随着生活品味的提升,玻璃房逐渐受到人们的青眯,这大玻璃窗户的清洁可由如图所示的“自动擦窗机器人”完成.
 (2014•娄底)随着生活品味的提升,玻璃房逐渐受到人们的青眯,这大玻璃窗户的清洁可由如图所示的“自动擦窗机器人”完成.某“自动擦窗机器人”的质量为2kg,它的“腹部”有吸盘.当自动擦窗机器人的真空泵将吸盘内的空气向外抽出时,它能牢牢地吸在竖直玻璃上.(g取10N/kg)
(2014•娄底)随着生活品味的提升,玻璃房逐渐受到人们的青眯,这大玻璃窗户的清洁可由如图所示的“自动擦窗机器人”完成.某“自动擦窗机器人”的质量为2kg,它的“腹部”有吸盘.当自动擦窗机器人的真空泵将吸盘内的空气向外抽出时,它能牢牢地吸在竖直玻璃上.(g取10N/kg)
(1)当自动擦窗机器人在竖直玻璃板上静止时,摩擦力为______N.此时若真空泵继续向外抽气,则自动擦窗机器人受到的摩擦力______(选填“变大”、“变小”或“不变”).
(2)吸盘与玻璃的接触面积为1.2×10-3m2,若吸盘在此面积上对玻璃的压强为1.5×105Pa,则吸盘对玻璃的压力是多大?
(3)自动擦窗机器人竖直向下运动时,若真空泵继续向外抽气,则自动擦窗机器人受到的摩擦力______(选填“变大”、“变小”或“不变”).
(4)自动擦窗机器人在6s内匀速竖直向下运动了0.6m,重力做功的功率是多大? 米_饭1年前1
米_饭1年前1 -
 臭臭臭 共回答了27个问题
臭臭臭 共回答了27个问题 |采纳率88.9%解题思路:(1)首先要明确静止和匀速下滑时,物体都处于平衡状态,受平衡力,只要找出哪两个力是平衡力,然后根据平衡力的特点解题就可.(2)根据压强定义式的变形公式F=pS可求压力.(3)利用速度公式求出下降高度,用公式W=Gh求出重力做的功,用公式P=Wt(或P=Fv)求出功率.(1)“擦窗机器人”的重力G=mg=2kg×10N/kg=20N,“擦窗机器人”静止时处于平衡状态,即受力平衡,在竖直方向上摩擦力和重力平衡,则摩擦力大小等于重力大小20N,只要“擦窗机器人”在竖直玻璃上静止,重力不变,摩擦力就不变;
(2)由p=[F/S]得,吸盘对玻璃的压力F=pS=1.5×105Pa×1.2×10-3m2=180N.
(3)自动擦窗机器人竖直向下运动时,若真空泵继续向外抽气,墙对自动擦窗机器人的支持力增大,则自动擦窗机器人受到的摩擦力变大;
(4)擦窗机器人6s下降的高度h=s=0.6m,
重力做功W=Gh=20N×0.6m=12J,
重力做功功率P=[W/t]=[12W/6s]=2W.
答:(1)20;不变;(2)吸盘对玻璃的压力为180N;
(3)变大;(4)重力做功12J,重力做功功率2W.点评:
本题考点: 摩擦力的大小;压强的大小及其计算;功率的计算.
考点点评: 本题考查了二力平衡的特点及对压强公式、重力公式、功、功率公式的应用.物体在平衡状态下受平衡力,找出平衡力是解题关键.1年前查看全部
- 怎样做猪舍水泥地面才不会有积水积尿,保持猪舍干燥,清洁…
 ff浪子dyl1年前1
ff浪子dyl1年前1 -
 miceson 共回答了16个问题
miceson 共回答了16个问题 |采纳率81.3%在猪舍地面施工前要用砖砌筑好输气管路通道,砌筑时首先砌导气管周围的暗槽,导气管上端留两块活动砖,使砖的平面同水泥地面在一个平面上.通道宽12厘米,以2%的坡度通向猪舍外.猪舍地面用混凝土抹成,要高出自然地面20厘米.1年前查看全部
- 甲醇 乙醇 硝酸 硫酸 双氧水可以用来清洁什么
甲醇 乙醇 硝酸 硫酸 双氧水可以用来清洁什么
清洗什么物品 不把斋的和尚被封1年前2
不把斋的和尚被封1年前2 -
 vampire32167 共回答了17个问题
vampire32167 共回答了17个问题 |采纳率70.6%甲醇 乙醇清洗油污及其他有机物
硝酸洗可除去银镜、铜镜等物质
硫酸洗可除去金属、金属氧化物
双氧水可以除去带有还原性的物质,1年前查看全部
- 活动课后,班长派全班的五分之一去打扫清洁区,后又有两人参加,这时,参加扫除人数是没参加的三分之一,
 9萧萧91年前1
9萧萧91年前1 -
 angelanolove 共回答了16个问题
angelanolove 共回答了16个问题 |采纳率100%本题抓住“全班总人数不变”始终是单位“1”
因为“参加扫除人数是没参加的三分之一”所以得到:参加扫除人数是全班的1/4,
利用量率对应,得到:
1、全班人数: 2/(1/4-1/5)=40(人)1年前查看全部
- 为了减少大气污染,许多城市推广汽车使用清洁燃料.目前使用的清洁燃料主要有两类,一类是压缩天然气(CNG),另一类是液化石
为了减少大气污染,许多城市推广汽车使用清洁燃料.目前使用的清洁燃料主要有两类,一类是压缩天然气(CNG),另一类是液化石油气(LPG).这两类燃料的主要成份都是( )
A.碳水化合物
B.烃类
C.氢气
D.醇类 小兔撞墙晕晕1年前1
小兔撞墙晕晕1年前1 -
 想要只苏牧的兰寇 共回答了18个问题
想要只苏牧的兰寇 共回答了18个问题 |采纳率94.4%解题思路:天然气的主要成分是甲烷,液化石油气的主要成分是乙烯、乙烷、丙烷、丙烯、丁烷、丁烯等,都属于烃类物质.A、天然气和液化石油气都属于烃类物质,只含碳和氢两种元素,碳水化合物含C、H、O三种元素,故A错误;
B、烃类物质属于碳氢化合物,故B正确;
C、天然气和液化石油气中不含氢气,故C错误;
D、天然气和液化石油气都属于烃类物质,不含氧元素,而醇类物质一定含有氧元素,故D错误;
故选B.点评:
本题考点: 饱和烃与不饱和烃.
考点点评: 本题考查有机物的组成,较为简单,注意天然气和液化石油气的区别.1年前查看全部
- “我最崇拜的人”用英文怎么写“辛苦”、“清洁工人”、“我非常感动,我很崇拜她。”用英文怎么说
 影子zhl1年前1
影子zhl1年前1 -
 jh5111737 共回答了16个问题
jh5111737 共回答了16个问题 |采纳率93.8%The person I admire most
painstaking 辛苦 cleaner 清洁工人
"I am very moved .
I admire her so much,1年前查看全部
- (5分) A、B、C、D四种元素,A元素的单质是最清洁的燃料,B元素的单质是空气中最多的气体,C是地壳中含量最多的元素,
(5分) A、B、C、D四种元素,A元素的单质是最清洁的燃料,B元素的单质是空气中最多的气体,C是地壳中含量最多的元素,C元素和D元素组成的化合物能使澄清石灰水变浑浊。则元素A为 、元素B的单质为 、元素C为 、元素D为 、C和地壳中含量居的金属元素形成的化合物的化学式是 。(填符号)
 喜欢听故事的人1年前1
喜欢听故事的人1年前1 -
 爱的小虫虫 共回答了18个问题
爱的小虫虫 共回答了18个问题 |采纳率100%H 、 N 2 、O、C、Al 2 O 3 .
由于氢气燃烧后产物是水,不污染环境,燃烧放出的热量多所以最清洁的燃料是氢气,A是氢元素;空气中各成分及体积分数为:氮气:78%、氧气:21%、稀有气体:0.94%、二氧化碳0.03%、水蒸气和杂质:0.03%.所以空气里最多的气体单质是氮气,元素B的单质为 N 2 ;地壳中含量最多的前五种元素有:氧、硅、铝、铁、钙,所以地壳中最多的元素是氧元素,所以C元素是氧元素;使澄清的石灰水变浑浊的气体是二氧化碳,因为C是氧元素,所以D是碳元素;氧元素和地壳中含量最多的金属元素铝形成的化合物的化学式是 Al 2 O 3 .1年前查看全部
- 苍蝇飞落在某处就匆忙搓脚,它是在:.A清洁污物,准备开饭.B发射生物雷达波,探测
苍蝇飞落在某处就匆忙搓脚,它是在:.A清洁污物,准备开饭.B发射生物雷达波,探测
苍蝇飞落在某处就匆忙搓脚,它是在:.A清洁污物,准备开饭.B发射生物雷达波,探测食物.C辨别同类气味.D品尝味道.会的请火速回答. bjzhgjs1年前3
bjzhgjs1年前3 -
 明心2 共回答了14个问题
明心2 共回答了14个问题 |采纳率92.9%B .1年前查看全部
- 我帮助饲养员给动物喂食,做清洁.英语
 夏日悠扬1年前1
夏日悠扬1年前1 -
 伤心小雪 共回答了20个问题
伤心小雪 共回答了20个问题 |采纳率100%你好:
【翻译】:I helped the feeder feed animals and did some cleaning .
希望对你有帮助!满意请采纳!1年前查看全部
大家在问
- 1一道数学题求证直线与圆相切!如图,圆Q和圆Q'相交于AB两点,PQ是圆Q'的直径,求证PA、PB是圆Q的
- 2下列说法中,哪个句子是不正确的? [ ] A. 英语中共有21个辅音字母
- 3在下列各化学反应中,不属于放热反应的是( )
- 4小明在上学的路上要经过一段山路,上坡的路程是下坡路程的2/3,若他上坡的速度是0.8m/s,下坡的速度是1.2m/s,则
- 5梦到动物预示着什么
- 6梯形面积是48平方厘米,阴影部分比空白部分少12平方厘米,求阴影部分面积.
- 71 The headmaster showed us around the school __ (person)
- 8i have two skirt .one is yellow,_______is black.
- 92012一建讲座李佳升课件35中调值公式最后的例题式子中有个减1是什么?
- 10怎样才能宽容他人?拜托各位大神
- 11设奇函数f(x)的定义域为R,最小正周期T=3,若f(1)≥1,f(2)=2a−3a+1,则a的取值范围是( )
- 12长方形的面积为S,长为a,则宽为( )
- 13在青山不老中为什么作者要描写当时环境的恶劣?
- 14已知函数f(x)=Asin(x+π/4),x属于R,且f(5π/12)=3/2
- 15配置A.B两种药剂,需要甲乙两种原料,已知配一剂A种药需要甲料3mg,乙料5mg;配一剂B种药需要甲5mg,乙4mg.

