无色有刺激性气味的气体,能使紫色石蕊变蓝 是什么?
 zhchdyx2022-10-04 11:39:544条回答
zhchdyx2022-10-04 11:39:544条回答
已提交,审核后显示!提交回复
共4条回复
 黑色眼睛007 共回答了18个问题
黑色眼睛007 共回答了18个问题 |采纳率88.9%- 氨气
二氧化硫是酸性气体,变红 - 1年前
 xie830709 共回答了1个问题
xie830709 共回答了1个问题 |采纳率- 碱性气体,氨就行.二氧化硫不可以
- 1年前
 waing02 共回答了1个问题
waing02 共回答了1个问题 |采纳率- 使紫色石蕊变蓝,故气体为碱性,最常见的就是氨气了,有机黄鸣龙还原中有用到的肼(H2NNH2),这两种都是有刺激性气味的。
- 1年前
 风吹两面都不倒 共回答了20个问题
风吹两面都不倒 共回答了20个问题 |采纳率90%- 二氧化硫啊
- 1年前
相关推荐
- A-I为初中化学中常见的物质.已知B可以改良酸性土壤,C为大理石的主要成分,D为无色有刺激性气味的气体,E是一种氮肥,F
A-I为初中化学中常见的物质.已知B可以改良酸性土壤,C为大理石的主要成分,D为无色有刺激性气味的气体,E是一种氮肥,F是一种白色沉淀,H是钡盐的溶液.“→”表示物质间存在着相互转化的关系(部分生成物未标出),如图所示.请回答下列问题:

(1)写出化学式:F______,G______.
(2)写出A→B的化学方程式:______.基本反应类型______.
(3)写出B与I反应的化学方程式:______. ppcfan1年前1
ppcfan1年前1 -
 千手观音 共回答了14个问题
千手观音 共回答了14个问题 |采纳率85.7%解题思路:找出解答本题的突破口:C为大理石的主要成分,所以C为碳酸钙,根据B与I反应能生成碳酸钙和氢氧化钠,来反推出B和I,还需结合B为改良酸性土壤的碱,A与水反应生成B,确定出B和I的具体物质;E是一种氮肥,H是钡盐溶液,所以G含有铵根离子,D是氢氧化钠和G反应产生的具有刺激性气味的氨气,再进一步进行分析即可.(1)E是氮肥,H是钡盐溶液,F应该是常见的钡离子沉淀形成的硫酸钡,所以G是含有铵根离子的硫酸铵,才能与氢氧化钠生成刺激性气味的氨气;
故:F是BaSO4;G是(NH4)2SO4;
(2)C为大理石的主要成分,所以C为碳酸钙,根据B与I反应能生成碳酸钙和氢氧化钠,是B与I交换成分生成的碳酸钙和氢氧化钠,所以将碳酸钙和氢氧化钠相互交换成分为:碳酸钠和氢氧化钙,因此B应该是改良酸性土壤的氢氧化钙,则A是氧化钙,I是碳酸钠;
所以氧化钙和水生成氢氧化钙,属于化合反应,方程式为:CaO+H2O=Ca(OH)2
(3)B与I反应的反应物是氢氧化钙和碳酸钠,生成物是碳酸钙沉淀和氢氧化钠,反应的化学方程式是:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
故答案为:(1)BaSO4 (NH4)2SO4 (2)CaO+H2O=Ca(OH)2 化合反应 (3)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH点评:
本题考点: 物质的鉴别、推断;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题的关键是知道大理石的主要成分为碳酸钙,然后结合实验现象逐渐确定物质,是解决此类实验推断题的最基本方法.1年前查看全部
- (7分)A—I为初中化学中常见的物质。已知B可以改良酸性土壤,C为大理石的主要成分,D为无色有刺激性气味的气体,E是一种
(7分)A—I为初中化学中常见的物质。已知B可以改良酸性土壤,C为大理石的主要成分,D为无色有刺激性气味的气体,E是一种氮肥,F是一种白色沉淀,H是钡盐的溶液。“→”表示物质间存在着相互转化的关系(部分生成物未标出),如下图所示。请回答下列问题:
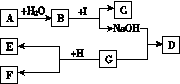
(1)写出化学式:F________,G________。
(2)写出A→B的化学方程式:______________________________________。基本反应类型________。
(3)写出B与I反应的化学方程式:________________________________。 jingmei19841年前1
jingmei19841年前1 -
 yang300_0 共回答了19个问题
yang300_0 共回答了19个问题 |采纳率94.7%(1) BaSO 4 (NH 4 ) 2 SO 4 (2)CaO+H 2 O=Ca(OH) 2 化合反应
(3)Ca(OH) 2 + Na 2 CO 3 =CaCO 3 ↓+ 2NaOH
(1)E是氮肥,H是钡盐溶液,F应该是常见的钡离子沉淀形成的硫酸钡,所以G是含有铵根离子的硫酸铵,才能与氢氧化钠生成刺激性气味的氨气;故:F是BaSO 4 ;G是(NH 4 ) 2 SO 4 ;
(2)C为大理石的主要成分,所以C为碳酸钙,根据B与I反应能生成碳酸钙和氢氧化钠,是B与I交换成分生成的碳酸钙和氢氧化钠,所以将碳酸钙和氢氧化钠相互交换成分为:碳酸钠和氢氧化钙,因此B应该是改良酸性土壤的氢氧化钙,则A是氧化钙,I是碳酸钠;
所以氧化钙和水生成氢氧化钙,属于化合反应,方程式为:CaO+H 2 O=Ca(OH) 2
(3)B与I反应的反应物是氢氧化钙和碳酸钠,生成物是碳酸钙沉淀和氢氧化钠,反应的化学方程式是:Ca(OH) 2 +Na 2 CO 3 =CaCO 3 ↓+2NaOH.1年前查看全部
- 化学无机推断有一种钠盐,共由三种短周期元素组成,它与稀硫酸溶液反应,产生乳白色沉淀和无色有刺激性气味的气体.问,这种钠盐
化学无机推断
有一种钠盐,共由三种短周期元素组成,它与稀硫酸溶液反应,产生乳白色沉淀和无色有刺激性气味的气体.问,这种钠盐是什么?
还有一种物质,也是由这三种元素组成的,摩尔质量比它大80,那那种化合物是什么呢?
(这是一个推断题) 狂煞1年前3
狂煞1年前3 -
 emmawang000 共回答了20个问题
emmawang000 共回答了20个问题 |采纳率90%钠盐是Na2S2O3硫代硫酸钠
高中选修实验化学中的重点内容
Na2S2O3+H2SO4=Na2SO4+H2O+S↓+SO2↑
S在没有大量析出的时候呈现乳白色,当析出的量多了便成淡黄色
这里乳白色可以解释
SO2是无色有刺激性气味的气体
钠盐是Na2S2O3硫代硫酸钠
高中选修实验化学中的重点内容
Na2S2O3+H2SO4=Na2SO4+H2O+S↓+SO2↑
S在没有大量析出的时候呈现乳白色,当析出的量多了便成淡黄色
这里乳白色可以解释
SO2是无色有刺激性气味的气体
Na和S和O
硫代硫酸钠的摩尔质量是158g/mol
而我们要推理的是158+80=238g/mol
可以意识到Na2SO3和Na2SO4是不可能的
只能是复杂的酸根离子
Na2S3O6
连三硫酸钠
我是原来的一楼1年前查看全部
- 各物质位1-20号元素 C H为无色有刺激性气味气体.D是一种黄绿色气体单质.物质I可用于饮水消毒.反应2 4是化工的重
各物质位1-20号元素 C H为无色有刺激性气味气体.D是一种黄绿色气体单质.物质I可用于饮水消毒.反应2 4是化工的重要反应.(部分反应条件未列出)
1 A+H2O=B+C
2 B(高温)=E+F F+H2O=I
4 D+I=J+K+H2O
3 C+H=G
5 I+G=K+C+H2O
各物质是什么?
(A由三种元素组成)
各物质为1-20号元素组成的单质或化合物
我也觉得这题好像有点问题,如果把I何J换一下就就完美的解决了。 yyhcool1年前5
yyhcool1年前5 -
 立木新东 共回答了23个问题
立木新东 共回答了23个问题 |采纳率87%A CaCN2
B CaCO3
C NH3
D Cl2
E CO2
F CaO
G NH4Cl
H HCl
I Ca(ClO)2
J Ca(OH)2
K CaCl2
还不懂的话 给我留言1年前查看全部
- 某实验小组的同学在加热铜与浓硫酸的混合物实验时,发现生成了一种无色有刺激性气味的气体和蓝色溶液,进行如下探究活动.
某实验小组的同学在加热铜与浓硫酸的混合物实验时,发现生成了一种无色有刺激性气味的气体和蓝色溶液,进行如下探究活动.
[查阅资料]①某些不活泼的金属(如铜)能与一些强氧化性的酸(如浓硫酸)发生反应,生成水而不生成氢气,同时生成二氧化硫和铜盐.
②硫酸铜溶于水后,溶液呈酸性.
[知识回顾]铜、银_______(能、不能)与稀硫酸、盐酸反应产生氢气.
[分析讨论]⑴对于生成的蓝色溶液,小东认为可能是Cu(NO 3 ) 2 溶液,小楠认为不可能是Cu(NO 3 ) 2 溶液,而可能是硫酸铜溶液,小楠的理由是 .
⑵写出铜与浓硫酸共热的化学方程式 .
⑶小东根据化学方程式说,该方法适用于以铜为原料大量制取硫酸铜,小田认为不适宜,你能说出小田的一个理由吗 .
[提出问题]上述蓝色溶液中有无硫酸剩余?
[实验论证]小坤认为可向蓝色溶液中滴加氯化钡溶液,观察有无沉淀产生,经大家讨论后,该方案被否定,你觉得否定该方案的理由是 .
[反思评价]⑴有同学提问:为什么不可以用石蕊试液来进行检验?你的回答是 .
⑵同学们发现:将足量的铜和足量的浓硫酸置于容器中加热,一段时间后,反应会逐渐变慢,最后反应停止,你能说出反应停止的原因吗? . 耒197309071年前1
耒197309071年前1 -
 流苏如雨 共回答了19个问题
流苏如雨 共回答了19个问题 |采纳率94.7%不能反应前后元素种类不变 Cu+2H 2 SO 4 =CuSO 4 +2H 2 O+SO 2 ↑ 生成的二氧化硫会污染环境(合理答案均给分)只能说明存在SO 4 2- ,不能确认硫酸有剩余(合理答案均给分) ...1年前查看全部
大家在问
- 1这个怎么读(单词,字母,读音)
- 2一瓶油,第一次用去五分之二,第二次用去五分之二千克,还剩这瓶油的百分之二十.这瓶油共重多少千克?
- 3如图所示,为一个质量为2千克的木块A夹在甲、乙两个固定的木块之间···
- 4在对角线有相同的所有矩形中,怎样的矩形周长最长,怎样的矩形面积最大
- 5给单词英语造句?如题 tall 、 control、computer、know 、important 、master 、
- 6小明把一根底面积为12.56平方分米的圆柱朩料削成一个圆锥,高是6分米.削成的圆锥的最大体积是所少?
- 7If Joe’s wife does·ttgo to the party,____.
- 8过氧乙酸能使紫色石蕊溶液变蓝吗?
- 9直角三角形两直角边分别为a,b,斜边为c,已知:a=40,b=9,则c=______.
- 10每样东西都将会免费吗?英语,用will
- 11金太阳2010届第二次联考英语答案
- 12每当想起这些食物时我都会流下口水用英文怎么说
- 13这句话怎么翻译成英语:这不难理解,任何东西在买后都会贬值.
- 14英语翻译All forecasting methods involve tedious repetitive calcu
- 15弦歌旧时闻 什么意思
