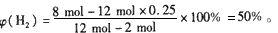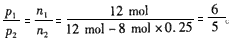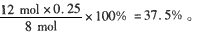把4 mol N 2 和8mol H 2 置于5L密闭容器中合成氨,达到平衡时测得混合气体中NH 3 的体积分数为20%
 softsdown2022-10-04 11:39:541条回答
softsdown2022-10-04 11:39:541条回答| 把4 mol N 2 和8mol H 2 置于5L密闭容器中合成氨,达到平衡时测得混合气体中NH 3 的体积分数为20%, 求: (1)混合气体中H 2 的体积分数; (2)反应前后容器内的压强比; (3)N 2 和H 2 的转化率。 |

已提交,审核后显示!提交回复
共1条回复
相关推荐
大家在问
- 1化学元素1到18号元素周期有什么规律!有多少说多少!
- 2已知,a、b、c在数轴上的位置如图.
- 3英语翻译kləuz'ɔrindʒ'zebrə'fɔ:tikli:nswi:pflɔ:spi:k'teibl 'swetə
- 4Half of the class ________ done most of the work. The left _
- 5《与朱元思书》中"与"读第几声
- 6二分之一比五分之一=四分之一比X解这个比例
- 7一个底面直径是8厘米.高8厘米的圆柱玻璃容器,里面装满水,把水倒入一个棱长8厘米的正方体玻璃容器中,水深
- 8三个互不相等的有理数,即可表示1,a+b,a的形式,又可表示为0,a/b.b的形式,则a的指数2000+b的指数2001
- 9按要求连接下列实物图,并在方框内画出对应的电路图
- 10心在沉淀灵魂的升华是什么意思
- 11三个同样大的等边三角形,组成一个梯形,(图如下)将这个梯形分成4个相同的梯形.
- 12函数f(x)=4x-4(x小于等于1)
- 13X-20%-(2/7X+2)=3/5X+5的解
- 14高中数列,1题,急求解答啊!已知数列a1=1,√a(n-1)-√an=√ana(n-1),求an.ps:√为根号.√a(
- 15在一个长16厘米,宽10厘米,高20厘米长方体玻璃缸中装一个棱长为8厘米的正方体铅块,然后往缸中放一些水,使它完全淹没这

 lailingzhi
lailingzhi