CO2与Ca(HCO3)2溶液为什么不能反应?
 pinky262022-10-04 11:39:542条回答
pinky262022-10-04 11:39:542条回答
已提交,审核后显示!提交回复
共2条回复
 彬子 共回答了20个问题
彬子 共回答了20个问题 |采纳率80%- 碳酸氢钙中碳酸氢根离子水解程度大于碳酸电离程度,所以碳酸酸性更强,根据强酸制弱酸,所以不反应.
- 1年前
 城中游地 共回答了57个问题
城中游地 共回答了57个问题 |采纳率- 因为CO2溶于水后,生成H2CO3
这样:H2CO3===H[+] + HCO3[-]
等号应该是可逆号
而Ca(HCO3)2在溶液里离子是Ca[2+]与HCO3[-],这两个离子与上述的物质均不反应
所以CO2不能与Ca(HCO3)2发生反应 - 1年前
相关推荐
- 澄清石灰水分别与少量,足量Ca(HCO3)2溶液混合的离子方程式,
 stcong1年前3
stcong1年前3 -
 生日烛光 共回答了10个问题
生日烛光 共回答了10个问题 |采纳率90%CA2++HCO3-+OH-=CACO3+H2O
碳酸氢钙的浓度不影响产物1年前查看全部
- 【化学】关于硬水的几个问题1、硬水对人体的危害主要是什么?硬水的Ca(HCO3)2和Mg(HCO3)2会因为人体温度而转
【化学】关于硬水的几个问题
1、硬水对人体的危害主要是什么?硬水的Ca(HCO3)2和Mg(HCO3)2会因为人体温度而转化为CaCO3和Mg(OH)2沉积导致结石吗?
2、如何去除水垢[可以用CaCO3+H2O+CO2====Ca(HCO3)2这个式子去除吗?] wushong出其西门1年前2
wushong出其西门1年前2 -
 凉地瓜 共回答了26个问题
凉地瓜 共回答了26个问题 |采纳率88.5%1.危害 形成结实
可能 设入过多钙离子容易患结实
不过结实的主要成分是草酸钙 不是碳酸钙
2.不好 因为二氧化碳在水中溶解度不大 要加压降温才能增大溶解度
而除水垢这样做太麻烦 而且碳酸氢钙受热易分解
用盐酸来除比较好1年前查看全部
- Ca(HCO3)2+NaOH的离子方程式,
Ca(HCO3)2+NaOH的离子方程式,
Ca(HCO3)2+NaOH=CaCO3+NaHCO3+H2O
离子方程式怎么写? sunhuainan591年前1
sunhuainan591年前1 -
 zhilcc 共回答了11个问题
zhilcc 共回答了11个问题 |采纳率100%Ca(HCO3)2+NaOH=CaCO3+NaHCO3+H2O
Ca(2+)+HCO3(-)+OH(-) === CaCO3(沉淀)+H2O
能拆开的全部拆开,沉淀和气体以及水是不能拆开的,两边在同时划掉重复的离子表达式,自己要学着做1年前查看全部
- NaOH与Ca(HCO3)2的反应
NaOH与Ca(HCO3)2的反应
Ca(HCO3)2少量时:2OH- +2HCO3-+CA2+=2H2O+CACO3+(CO3)2-Ca(HCO3)2过量时:OH- +HCO3- +CA2+ =H2O 不管少量或过量 OH-都是和HCO3-反应 为什么一个有(CO3)2- 另一个没有呢 白烨1年前2
白烨1年前2 -
 滢滢的美丽心情 共回答了17个问题
滢滢的美丽心情 共回答了17个问题 |采纳率100%NaOH少量:
NaOH + Ca(HCO3)2 = CaCO3↓ + NaHCO3 + H2O
OH- + Ca2+ + HCO3- = CaCO3↓ + H2O
NaOH过量:
2 NaOH + Ca(HCO3)2 = CaCO3↓ + Na2CO3 + 2 H2O
2 OH- + Ca2+ + 2 HCO3- = CaCO3↓ + CO32- + 2 H2O
其实很简单,就是中和一个HCO3-和中和2个HCO3-的差别.
因为Ca(HCO3)2 有2个HCO3-,只要中和1个HCO3-,就能形成CaCO3沉淀.
另一个HCO3-,
如果没有被中和,则产物就是NaHCO3.
如果被中和了,产物就是 Na2CO31年前查看全部
- Ca(HCO3)2溶液中滴入过量NaOH溶液的化学方程式和离子方程式怎么写?
 xiaxiaoyu11年前2
xiaxiaoyu11年前2 -
 果果2007 共回答了15个问题
果果2007 共回答了15个问题 |采纳率93.3%Ca(HCO3)2+2NaOH=Na2CO3+CaCO3(沉淀)+2H2O1年前查看全部
- 物质X可能由Ca(HCO3)2,Mg(HCO3)2,Mg(OH)2、CaCO3、BaCO3十万火急
物质X可能由Ca(HCO3)2,Mg(HCO3)2,Mg(OH)2、CaCO3、BaCO3十万火急
. xuanlv2581年前1
xuanlv2581年前1 -
 dingle27 共回答了24个问题
dingle27 共回答了24个问题 |采纳率100%氢氧化钙,增大,Mg(OH)2、CaCO3、BaCO3,三个孔最好应该呈等边三角形.
解析:有氢氧化钙会产生成沉淀,增大是因为空气中二氧化碳的原因.确定物质可用极限思维,如果只有碳酸钙产生的气体为22g,只有碳酸钡11.168g,所以必然为两者混合才可能产生20g,而无法判断是否有Mg(OH)2.所以可能有.成三角形,彼此距离较大,更坚固.1年前查看全部
- CaCO3+H2O+CO2===Ca(HCO3)2,书上说,此反应能够进行的原因,是因为难电离的碳酸和难溶的碳酸钙反应生
CaCO3+H2O+CO2===Ca(HCO3)2,书上说,此反应能够进行的原因,是因为难电离的碳酸和难溶的碳酸钙反应生成了更难电离的含碳酸氢根离子的化合物.
这句话我还是不能完全理解...他这句话的意思是不是只要产生了碳酸氢根,那就可以反应了?哪怕是生成可溶物? 212121年前3
212121年前3 -
 ice_gg2008 共回答了17个问题
ice_gg2008 共回答了17个问题 |采纳率82.4%这个要从化学平衡的角度来理
CO3(2-)+H2O=HCO3(-)+OH(-),这是碳酸根离子水解的方程式.虽然CaCO3是沉淀,但是沉淀并不是代表一丁点都不能溶于水,恰恰相反的是,溶于水的那一部分CaCO3却是全部电离的.CO2溶于水生成H2CO3,呈酸性,打破了旧的化学平衡,而HCO3(-)是不容易电离的离子,因此反应朝着HCO3(-)反应.
我记得复分解反应发生的三大条件:
1、生成水
2、生成气体
3、生成更难溶的物质
而上述反应恰恰满足第三条,因此可以反应.1年前查看全部
- 为什么NAOH和NAHCO3反应的离子方程式中 NAHCO3不可以拆.而CA(HCO3)2的加热反应就可以啊.
 yeph211年前2
yeph211年前2 -
 sunnylee77 共回答了12个问题
sunnylee77 共回答了12个问题 |采纳率91.7%NAHCO3在呈弱碱性,在水中只能游离出一个NA离子和一个HCO3离子,如果能游离出H离子就呈酸性了.碳酸氢钙加热就生成另外三种物质了,物质本身起了化学变化.1年前查看全部
- Ca(HCO3)2的物料守恒RT
 phxjw1年前1
phxjw1年前1 -
 tsstss 共回答了16个问题
tsstss 共回答了16个问题 |采纳率81.3%Ca2+=2(HCO3-+H2CO3+CO32-)1年前查看全部
- Ca(HCO3)2和Na2CO3能否反应
 Nesich1年前3
Nesich1年前3 -
 我要问问题 共回答了18个问题
我要问问题 共回答了18个问题 |采纳率72.2%Ca(HCO3)2+Na2CO3——〉2NaHCO3+CaCO3沉淀1年前查看全部
- CaCO3和什么反应生成Ca(HCO3)2?
CaCO3和什么反应生成Ca(HCO3)2?
CaCO3和什么反应生成Ca(HCO3)2
Ca(HCO3)2又能和什么反应生成CaCO3 WOLAINIAO1年前4
WOLAINIAO1年前4 -
 colin839 共回答了16个问题
colin839 共回答了16个问题 |采纳率100%Ca(HCO3)2是CaCO3的酸式盐,前者可溶,后者不可溶
一般可以在含有CaCO3沉淀的溶液里面,继续通入CO2,可以生成Ca(HCO3)2
CaCO3+CO2+H2O==Ca(HCO3)2
但是Ca(HCO3)2的固体不稳定,如果稍稍加热,就发生分解,生成CaCO3
Ca(HCO3)2==(加热)CaCO3+CO2(气体箭头)+H2O
Ca(HCO3)2和碱反应可以得到CaCO3.
例如和NaOH反应
Ca(HCO3)2+2NaOH==CaCO3(沉淀箭头)+2H20+Na2CO31年前查看全部
- Ca(HCO3)2和NaOH怎么反应得啊谢谢了,
Ca(HCO3)2和NaOH怎么反应得啊谢谢了,
2种可能得 吟狮作对1年前5
吟狮作对1年前5 -
 quanlong19864 共回答了20个问题
quanlong19864 共回答了20个问题 |采纳率70%两种,考虑NaOH足量与不足量~Ca(HCO3)2+2NaOH==Na2CO3+CaCO3!+2H2O NaOH不足量 Ca(HCO3)2+NaOH==Na+H2O+CaCO3!NaOH足量 其原理其实是HCO3-(碳酸氢根离子)和OH-(氢氧根离子的)反应,足量OH-的话就都生成CO3 2-(碳酸根离子) 不够的话除了生成碳酸根离子外还有碳酸氢根离子 =你们以后学了离子方程式就明白列1年前查看全部
- Ca(HCO3)2溶液中的物料守恒和电子守恒?
 slaveofsuede1年前1
slaveofsuede1年前1 -
 apl10 共回答了15个问题
apl10 共回答了15个问题 |采纳率100%c(Ca2+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
c(Ca2+)=2(c(HCO3-)+c(CO32-)+c(H2CO3))1年前查看全部
- 碳酸氢钠与澄清石灰水反应过量时为什么不像二氧化碳过量时生成Ca(HCO3)2而是怎样都生成碳酸钙沉淀?
 shuilou31年前3
shuilou31年前3 -
 hh119 共回答了24个问题
hh119 共回答了24个问题 |采纳率83.3%碳酸氢根离子与氢氧根离子不能共存,故只能生成碳酸钙沉淀.1年前查看全部
- CA(HCO3)2和NA2CO3反应有沉淀吗
 gaominju1年前1
gaominju1年前1 -
 254769783 共回答了14个问题
254769783 共回答了14个问题 |采纳率85.7%有,Ca2CO3沉淀1年前查看全部
- 4.分别将下列物质:①矾②Na2O2③NaCl④Ca(HCO3)2⑤FeCl3投入水中,对其溶液加热蒸干,仍能得到原物质
4.分别将下列物质:①矾②Na2O2③NaCl④Ca(HCO3)2⑤FeCl3投入水中,对其溶液加热蒸干,仍能得到原物质的
矾是含结晶水的硫酸盐。比如明矾,加热蒸干后还能得到原物质吗?还没有转过弯来, 天外飞泥巴1年前1
天外飞泥巴1年前1 -
 luozhyan1010 共回答了16个问题
luozhyan1010 共回答了16个问题 |采纳率100%①矾 矾是硫酸盐,加热蒸干后依然是矾
一般情况下易挥发酸的盐加热易分解,而硫酸不是挥发性酸,则硫酸盐加热蒸干后依然是硫酸盐.
②Na2O2 过氧化钠于水反应得到氢氧化钠和氧气,溶液蒸干得氢氧化钠
③NaCl 还是得到氯化钠
④Ca(HCO3)2 加热分解为碳酸钙二氧化碳和水,留下碳酸钙
⑤FeCl3 水解得到氢氧化铁,加热得到三氧化二铁1年前查看全部
- 溶液加热蒸干,仍能得到原物质好像是什么强碱,记不清了原题:1.矾 2.Na2O2 3.NaCl 4.Ca(HCO3)2
溶液加热蒸干,仍能得到原物质
好像是什么强碱,记不清了
原题:1.矾 2.Na2O2 3.NaCl 4.Ca(HCO3)2 5.FeCl3我是说 什么类物质加热蒸干,仍能得到原物质
A.123 B.13 C.34 D.3 liquidwater1年前6
liquidwater1年前6 -
 gladiator 共回答了15个问题
gladiator 共回答了15个问题 |采纳率93.3%B是对的,矾都是硫酸盐,不能水解生成其他物质,小心蒸干不会失去结晶水;Na2O2变成NaOH;Ca(HCO3)2加热分解成碳酸钙;FeCl3水解成Fe(OH)3,加热后可变成Fe2O3.1年前查看全部
- 物质溶解度大小怎样判断?判断下列物质溶解度大小A,Na2CO3 B,NaHCO3 C,Ca(HCO3)2 D,KHCO3
物质溶解度大小怎样判断?
判断下列物质溶解度大小
A,Na2CO3 B,NaHCO3 C,Ca(HCO3)2 D,KHCO3
要详解 cn_lato1年前1
cn_lato1年前1 -
 buttypan 共回答了15个问题
buttypan 共回答了15个问题 |采纳率80%大部分固体溶解度随温度的上升而上升,A在30摄氏度时溶解度大于20,B在30摄氏度时溶解度小于10,所以此时A的溶解度大于B;少部分固体溶解度随温度的上升而1年前查看全部
- 高温,CA(HCO3)2 分解为 CACO3 分解为 CAO ,会不会三者同时存在在一个体系中?
 MiamiCold1年前3
MiamiCold1年前3 -
 zqf168888 共回答了18个问题
zqf168888 共回答了18个问题 |采纳率88.9%Ca(HCO3)2是一种极易溶于水的无机酸式盐,只存在溶液中;将Ca(HCO3)2溶液蒸发则得到CaCO3 固体.也就是说碳酸氢钙加热得到碳酸钙温度不会特别的高,而碳酸钙固体要高温才能分解,所以说很难让两者同时分解反应.故三者共存的概率很小.
你如果能想方设法的弄到大型的Ca(HCO3)2固体,很坚硬的那种,然后让他在一个加热很不均匀的容器中加热,有可能外部的Ca(HCO3)2 分解为CaCO3 ,因为导热的原因最内部的Ca(HCO3)2 还没有开始分解,而外部生成的CaCO3已经开始分解为CaO,当然了,这只是有点钻牛角尖的可能罢了,从数学概率的角度讲,有这个概率;但是物理学上有言“小概率事件不可能发生”.
并且,Ca(HCO3)2是酸式盐,而CaO是碱式盐,两者共存肯定要发生反应的啦1年前查看全部
- 加热Ca(HCO3)2后生成Caco3+h2o+co2然后再怎么反应
 lys83691年前1
lys83691年前1 -
 sisyfox 共回答了13个问题
sisyfox 共回答了13个问题 |采纳率100%看最终的环境,如果是碱性的,碳酸钙会成为氢氧化钙.若果是酸性的,可能变回碳酸氢钙,甚至成为氢氧化钙.1年前查看全部
- Ca(HCO3)2是沉淀吗
 点点的微笑1年前1
点点的微笑1年前1 -
 killet_011 共回答了25个问题
killet_011 共回答了25个问题 |采纳率100%一般情况下,碳酸氢盐都不会出现沉淀情况,向澄清石灰水中通入过量的二氧化碳气体,澄清石灰水先变浑浊后又变澄清,即最后碳酸钙沉淀转化成碳酸氢钙,易溶.当然也有特殊情况,如饱和的碳酸钠溶液通入足量的二氧化碳,溶液会析出碳酸氢钠,当做沉淀处理.1年前查看全部
- Ca(HCO3)2====CaCO3+CO2+H2O现象
 lxw19701年前1
lxw19701年前1 -
 蓝色尘AI 共回答了19个问题
蓝色尘AI 共回答了19个问题 |采纳率94.7%煅烧时产生水汽1年前查看全部
- 过量的CO2通进CACI2溶液中生成可溶性的CA(HCO3)2,是否正确,原因.
 恨水东逝1年前1
恨水东逝1年前1 -
 清江秋 共回答了21个问题
清江秋 共回答了21个问题 |采纳率85.7%正确
cacl2在水中是离子分布 过量co2进入水里 会生成h2co3 可分解成 hco3 - 离子 可以生成 hco3-和ca2+的可溶物1年前查看全部
- 向澄清石灰水中通入足量的CO2,为什么会生成Ca(HCO3)2?
 rosieyang1年前4
rosieyang1年前4 -
 f2b2v 共回答了18个问题
f2b2v 共回答了18个问题 |采纳率100%CO2刚通入澄清石灰水中去:
CO2 + Ca(OH)2 = CaCO3↓ + H2O
过量的CO2通入澄清石灰水中或者说通入一段时间以后:
CaCO3 + CO2 + H2O = Ca(HCO3)2
因此,常常我们都会运用这种原理来检验CO2相关鉴定性问题.
同时与此类似的还有提纯NaHCO31年前查看全部
- 分离括号内杂质:CACO3【Ca(HCO3)2】置于坩埚加强热为什么是错的
 东南西北瓜1年前2
东南西北瓜1年前2 -
 我要讨厌XQS 共回答了16个问题
我要讨厌XQS 共回答了16个问题 |采纳率93.8%因为CaCO3受热会分解.
正确的方法是加水后过滤.
因为Ca(HCO3)2溶于水,CaCO3不溶于水.1年前查看全部
- ca(hco3)2与过量的ca(oh)2
ca(hco3)2与过量的ca(oh)2
离子方程式是不是Ca2++2HCO3-+2OH-→CaCO3↓+ CO32-+2H2O huang锦明1年前2
huang锦明1年前2 -
 时晨zzll 共回答了20个问题
时晨zzll 共回答了20个问题 |采纳率100%2Ca2+ + 2HCO3- + 2HO- = 2CaCO3↓+2H2O1年前查看全部
- Ca(HCO3)2与NaOH在量不同的情况下具体的反应方程式怎么写?
 luapafei1年前1
luapafei1年前1 -
 little4l 共回答了9个问题
little4l 共回答了9个问题 |采纳率88.9%如果NaOH过量,则Ca(HCO3)2+2NaOH=CaCO3+Na2CO3+2H2O;
如果 NaOH不足,则则Ca(HCO3)2+NaOH=CaCO3+NaHCO3+H2O.
离子方程式的书写以量少者为依据.1年前查看全部
- CaCO3 + CO2 + H2O =Ca(HCO3)2 的离子方程式
CaCO3 + CO2 + H2O =Ca(HCO3)2 的离子方程式
注:CaCO3 ,CO2 ,H2O 都不能拆 偷西瓜的小贼1年前2
偷西瓜的小贼1年前2 -
 bofu125 共回答了21个问题
bofu125 共回答了21个问题 |采纳率81%CaCO3(s) + CO2(g) + H2O(l) = Ca2+(aq) 2(HCO3)-(aq)1年前查看全部
- 向澄清石灰水中加入过量的Ca(HCO3)2 的离子反应方程式怎么写?
向澄清石灰水中加入过量的Ca(HCO3)2 的离子反应方程式怎么写?
也可以说是:Ca(HCO3)2与过量Ca(OH)2溶液反应的离子反应方程式 lxmlf15671年前1
lxmlf15671年前1 -
 大唐龙椅 共回答了13个问题
大唐龙椅 共回答了13个问题 |采纳率100%Ca(2+)+HCO3(-)+OH(-)=CaCO3(沉淀)+H2O1年前查看全部
- Ca(HCO3)2的电离方程式: NaHS的电离方程式: (NH4)2Fe(SO4)2的电离方程式
Ca(HCO3)2的电离方程式: NaHS的电离方程式: (NH4)2Fe(SO4)2的电离方程式
PS:表明用等号还是互逆符号
O(∩_∩)O谢谢 hare8301241年前5
hare8301241年前5 -
 hnzxzx 共回答了15个问题
hnzxzx 共回答了15个问题 |采纳率100%上述三种盐都是强电解质,所以第一步电离都是完全电离,写等号,弱酸的酸式根部分电离,所以写可逆号.
Ca(HCO3)2=Ca^2+ +2HCO3^-
HCO3^-﹤=﹥H^++CO3^2-
NaHS=Na^+ +HS^-
HS^-﹤=﹥H^+ +S^2-
(NH4)2Fe(SO4)2=2NH4^+ +Fe^2+ +2SO4^2+1年前查看全部
- 高一化学书写离子方程式1:SO2+KOH(少)2:SO2+KOH(过)3:Ca(HCO3)2+NaOH(少)4:Ca(H
高一化学书写离子方程式
1:SO2+KOH(少)
2:SO2+KOH(过)
3:Ca(HCO3)2+NaOH(少)
4:Ca(HCO3)2+NaOH(过) 我爱君君啊1年前3
我爱君君啊1年前3 -
 geminijudy 共回答了22个问题
geminijudy 共回答了22个问题 |采纳率90.9%1)SO2 + OH- ===HSO3-
2)SO2 + 2OH- === SO32- + H2O
3)Ca2+ + HCO3- + OH- === CaCO3(沉淀)+ H2O
4)Ca2+ + 2HCO3- +2OH- === CaCO3(沉淀)+ CO3^2- + 2H2O1年前查看全部
- 把二氧化碳通入澄清石灰水中 ca(hco3)2和ca(oh)2能共存吗?
 gelihua1年前2
gelihua1年前2 -
 tianya有泪 共回答了25个问题
tianya有泪 共回答了25个问题 |采纳率92%Ca(HCO3)2+Ca(OH)2=2CaCO3↓+2H2O所以不能,换一种方法想,碳酸氢钙是将过量二氧化碳通入澄清石灰水中,石灰水中就自然不会有氢氧化钙了(因为氢氧化钙与二氧化碳反应转化为碳酸氢钙和碳酸钙了),望给你启发1年前查看全部
- 漂白粉的有关化学式问题Ca(ClO)2+2H2O+2CO2 = Ca(HCO3)2+2HClO 这个是漂白粉多了还是什么
漂白粉的有关化学式问题
Ca(ClO)2+2H2O+2CO2 = Ca(HCO3)2+2HClO 这个是漂白粉多了还是什么?
Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO 这个是碳酸多了吗? 小小神仙0001年前2
小小神仙0001年前2 -
 wangzhaogang 共回答了20个问题
wangzhaogang 共回答了20个问题 |采纳率95%1.第一个是漂白粉起作用时的方程式.
2.第二个是是漂白粉在空气中变质的方程式,如果是固体漂白粉在空气中变质,那么不用写沉淀符号;如果是漂白粉的溶液在空气中变质,由于空气中CO2含量很少,生成的CaCO3也很少,不足以形成沉淀,也就不用写沉淀符号.1年前查看全部
- CaCo3 + CO2 + H2O = Ca(HCO3)2 到底怎么算出来的?
 vinto1年前1
vinto1年前1 -
 qcendc1qx5f44 共回答了16个问题
qcendc1qx5f44 共回答了16个问题 |采纳率81.3%CO2 + H2O = H2CO3
CO32- + H2CO3 = 2HCO3-
Ca2+ + 2HCO3- =Ca(HCO3)21年前查看全部
- 石灰水与足量Ca(HCO3)2溶液反应
石灰水与足量Ca(HCO3)2溶液反应
写出离子反应方程式、在线等 yst_1999_01年前1
yst_1999_01年前1 -
 lawyer1 共回答了23个问题
lawyer1 共回答了23个问题 |采纳率78.3%Ca(HCO3)2 + Ca(OH)2==CaCO3↓+2H2O1年前查看全部
- 求两个离子方程式Ca(HCO3)2+NaOH= 注意两种物质量不同会有两个方程式哦!
 我爱梅园梅1年前1
我爱梅园梅1年前1 -
 荷间清梦 共回答了18个问题
荷间清梦 共回答了18个问题 |采纳率94.4%Ca(HCO3)2+2NaOH==CaCO3↓+Na2CO3+2H2O
Ca(HCO3)2+NaOH==CaCO3↓+NaHCO3+H2O1年前查看全部
- 这个化学式怎样配平?Ca(OH)2 + CO2 →Ca(HCO3)2谢咯哈`!
 avl11111年前1
avl11111年前1 -
 大丰视眼 共回答了19个问题
大丰视眼 共回答了19个问题 |采纳率84.2%Ca(OH)2 + 2CO2 ==Ca(HCO3)21年前查看全部
- Ca(HCO3)2的电离方程式
 erickson0201年前1
erickson0201年前1 -
 shuiciwawa 共回答了17个问题
shuiciwawa 共回答了17个问题 |采纳率100%Ca(HCO3)2==Ca2+ + 2HCO3-
HCO3-=可逆符号=H+ + CO3(2-)
()内是上角标1年前查看全部
- 这个化学式怎样配平?Ca(OH)2 + CO2 →Ca(HCO3)2 谢咯哈`!
 鼠标点点1年前1
鼠标点点1年前1 -
 老老头子 共回答了17个问题
老老头子 共回答了17个问题 |采纳率94.1%二氧化碳两个就平了.1年前查看全部
- 碳酸氢盐的溶解度是怎样的?比如Ca2+,Al3+,Cl-,HCO3-能否大量共存这个问题,Ca(HCO3)2既然是澄清溶
碳酸氢盐的溶解度是怎样的?
比如Ca2+,Al3+,Cl-,HCO3-能否大量共存这个问题,Ca(HCO3)2既然是澄清溶液是不是就认为可以大量共存?那Al(HCO3)3的溶解度呢?
跟我说下碳酸氢盐中的溶解度情况, swjsyh51年前2
swjsyh51年前2 -
 透明朋友 共回答了21个问题
透明朋友 共回答了21个问题 |采纳率95.2%铝离子会与碳酸氢根离子发生水解反应:
Al3+ +3HCO3-==Al(OH)3↓+3CO2↑ 所以溶液中根本没有Al(HCO3)3的存在.
故Ca2+,Al3+,Cl-,HCO3-不能大量共存.
Ca(HCO3)2是澄清溶液,但溶液很不稳定,易分解成CaCO3、H2O和CO2:
Ca(HCO3)2==CaCO3↓+CO2↑+H2O
各种离子的化合物的溶解度可参考:
http://www.***.com/s?sr=052BBA7ED934315CF9B6BB93E4712A187D649D4E&tn=webxunlei_1_cb&cb=baiducb&word=%C8%DC%BD%E2%B6%C8%B1%ED&bar=71年前查看全部
- 6.下列解释不科学的是( ) A.在溶洞中,当溶有Ca(HCO3)2的水液发生分解,析出固体(在洞顶或洞底)
6.下列解释不科学的是( ) A.在溶洞中,当溶有Ca(HCO3)2的水液发生分解,析出固体(在洞顶或洞底)
6.下列解释不科学的是( )
A.在溶洞中,当溶有Ca(HCO3)2的水液发生分解,析出固体(在洞顶或洞底),日久天长便形成了钟乳石
B.长期盛放NaOH溶液的试剂瓶不易打开,是因为NaOH与瓶中的CO2反应导致瓶内气压小于瓶外大气压的缘故
C.“通风橱”是利用排风扇将橱内废气直接排放到室外的装置,它是一种不完善的防污设施
D.高压氧舱可治疗煤气中毒,原因是和血红蛋白结合的CO跟氧气反应生成无毒的CO2
7.在a、b两支试管中加入体积相同的同种生铁块.在a中加入食盐水,塞上橡皮塞,如右图.U型玻璃管内为红墨水(开始时两端液面等高).放置一段时间后,下列有关叙述错误的是( )
A.生铁块中的主要成分是铁,也含有少量的碳
B.红墨水柱两边的液面变为左低右高
C.两试管中铁均被锈蚀
D.a试管中发生的反应是:2C+2Fe+3O2=2FeCO3
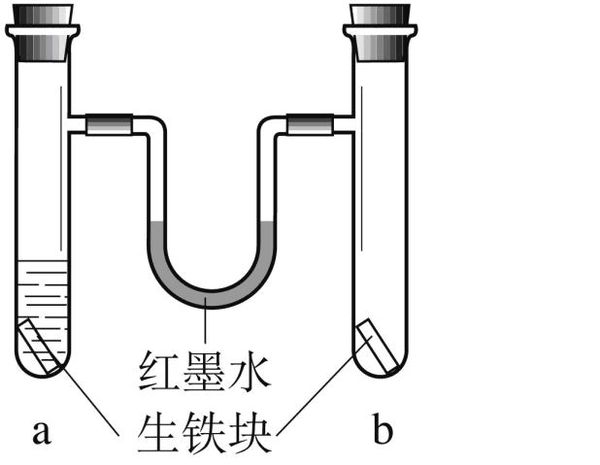
 Nancylu83161年前2
Nancylu83161年前2 -
 ublnz 共回答了16个问题
ublnz 共回答了16个问题 |采纳率93.8%第一题我认为选D.A选项没的说,高中化学书在讲碳酸钙的那一部分应该有过这个例子.B选项氢氧化钠能和二氧化碳反应.C选项也是正确的,因为排气扇只是把废气排到了大气中,实验室内没有废气了,所以说是不完善的.D选项一氧化碳和氧气在常温下很难反应,当然也不会生成二氧化碳了.
第二题我认为选D.A选项没的说,生铁中含有一定量的碳.B选项也正确,因为右边试管的铁片会与氧气发生反应,右边试管的气压降低.C选项两个铁片都会被腐蚀 左边的为电化学腐蚀,右边的为氧腐蚀.至于D选项,铁在食盐水中发生的应该是电化学腐蚀,反应式没有题中写的那么简单.因为好几年没看高中的化学,有些地方难免有不足,1年前查看全部
- Ca(HCO3)2 与HCl 或者NAOH反应生成什么?
 qiuyifei11年前1
qiuyifei11年前1 -
 芭拉嘎拉 共回答了20个问题
芭拉嘎拉 共回答了20个问题 |采纳率90%前者:CaCl2、H2O和CO2
后者:CaCO3、Na2CO3和H2O1年前查看全部
- Ca(HCO3)2与盐酸反应的化学方程式
 xishi20071年前6
xishi20071年前6 -
 果敢1 共回答了18个问题
果敢1 共回答了18个问题 |采纳率83.3%离子方程式都是:HCO3- + H+ = H2O + CO2↑
化学方程式都写成 :Ca(HCO3)2+2HCl==CaCl2+ 2H2O+ 2CO2↑1年前查看全部
- 写出 向Ca(HCo3)2中加入过量或少量 NaOH 的离子方程式 顺便把化学方程式也写出来
 压海棠的小梨花1年前1
压海棠的小梨花1年前1 -
 温和府库 共回答了16个问题
温和府库 共回答了16个问题 |采纳率106.3%Ca(HCo3)2+2NaOH= CaCo3(沉淀)+2H2O
氢氧根先跟碳酸氢跟反应生成碳酸根和水,然后碳酸根跟钙离子结合生成碳酸钙沉淀1年前查看全部
- 定量离子方程式书写技巧 例题:过量Ca(HCO3)2与NaOH离子方程式与Ca(HCO3
定量离子方程式书写技巧 例题:过量Ca(HCO3)2与NaOH离子方程式与Ca(HCO3
定量离子方程式书写技巧
例题:过量Ca(HCO3)2与NaOH离子方程式与Ca(HCO3)2与过量NaOH离子方程式,知道的大神说下,感激不尽 我是小烦1年前1
我是小烦1年前1 -
 陆回 共回答了21个问题
陆回 共回答了21个问题 |采纳率95.2%对这种非氧化还原的复分解反应型的离子反应来讲,要从离子的角度看物质间反应及量的关系.
如:过量Ca(HCO3)2与NaOH(NaOH少量)与Ca(HCO3)2与过量NaOH
在Ca(HCO3)2与NaOH反应时,反应实质是Ca2+、HCO3-、OH-三种离子间的反应:
HCO3-+OH-=CO32-+H2O
反应生成的CO32-与Ca2+继续反应:Ca2++CO32-=CaCO3(沉淀)
当提供少量OH-时(NaOH少量),OH-只能与一个HCO3-反应,生成1分子水和1个CO32-, 生成的1个CO32-与1个Ca2+结合成CaCO3沉淀(若写化学方程式,则生成NaOH):
Ca2++HCO3-+OH-=CaCO3(沉淀)+H2O (Ca(HCO3)2与少量NaOH反应)
当提供过量OH-时(NaOH过量),2个OH-就能与全部的HCO3-反应,生成2分子水和2个CO32-, 生成的2个CO32-中,其中一个与Ca2+结合成CaCO3沉淀,剩余一个CO32-(若写化学方程式,则生成Na2CO3):
Ca2++2HCO3-+2OH-=CaCO3(沉淀)+CO32-+2H2O (Ca(HCO3)2与过量NaOH反应)
在判断离子方程式书写正误时,关键看水的量和有无碳酸根离子的生成
当碳酸氢钙少量过量时,可以折算成氢氧化钠的问题:碳酸氢钙少量时,氢氧化钠过量; 碳酸氢钙过量时,氢氧化钠少量.
有疑问,请追问,希望能帮到你哦1年前查看全部
- NaHSO4+Ca(HCO3)2= NaHSO3+NaHSO4= HAC(醋酸)+Ba(OH)2=
NaHSO4+Ca(HCO3)2= NaHSO3+NaHSO4= HAC(醋酸)+Ba(OH)2=
顺便帮我总结一下写方程式反应物的规律!
急用!
NaHSO4+Ca(HCO3)2=?
NaHSO3+NaHSO4=?
HAC(醋酸)+Ba(OH)2=?
帮我总结一下写方程式反应物的规律! 哈药六厂11年前1
哈药六厂11年前1 -
 蓝色轩冰 共回答了25个问题
蓝色轩冰 共回答了25个问题 |采纳率96%2NaHSO4+Ca(HCO3)2=Na2SO4+CaSO4+2H2O+2C02↑
NaHSO3+NaHSO4=Na2SO4+H2O+SO2↑
HAC(醋酸)+Ba(OH)2=Ba(AC)2+2H20
先多背点方程,然后找规律,因为同一类型离子方程是一样的1年前查看全部
- Ca(HCO3)2的读法我刚学化学,所以不要说我哦~另外顺便问一下,什么时候读 数字+名称 化 数字+名称什么时候读 名
Ca(HCO3)2的读法
我刚学化学,所以不要说我哦~
另外顺便问一下,什么时候读 数字+名称 化 数字+名称
什么时候读 名称 化 名称 萧龙儿1年前6
萧龙儿1年前6 -
 Friendlies2008 共回答了15个问题
Friendlies2008 共回答了15个问题 |采纳率80%碳酸氢钙
当具有相同元素组成,一种名字无法区分的时候,加数字,例如Na2HPO3和NaH2PO3,前者叫磷酸氢二钠,后者叫磷酸二氢钠;又如CO与CO2,就必须加数字了,一氧化碳与二氧化碳
有相同元素组成,且一般只有一种组合的时候或者最常见的,就不加数字了,例如CaO,氧化钙
有些是经验的,见了多了就记住了,像氧化铁是Fe2O3,而Fe3O4就叫做四氧化三铁1年前查看全部
- 将Ca(HCO3)2和SiO2的混合物高温下加热,充分反应后,所得固体的质量为原混合物质量的一半,则原混合物中Ca(HC
将Ca(HCO3)2和SiO2的混合物高温下加热,充分反应后,所得固体的质量为原混合物质量的一半,则原混合物中Ca(HCO3)2与SiO2
物质的量之比及所得固体的成分分别是(我不要答案,求各位给我一个思路) 小哲子1年前3
小哲子1年前3 -
 戚戚 共回答了13个问题
戚戚 共回答了13个问题 |采纳率84.6%思想很好!肯定是不能因为答案而去做题,而是通过做题培养我们的思维方式!
下面我给你讲一下思路.
1.你必须知道这两种物质加热为什么会有质量减小,其减小的原因就是因为Ca(HCO3)2受热分解!
Ca(HCO3)2==高温==CaO+H2O+CO2(知道这个最好用差量法做!质量变化,这里我们就能分析出示水蒸气和二氧化塘跑掉了,导致物质质量的减少!)
2.你又要考虑产生的物质会不会继续反应,会反应会不会引起质量的变换
CaO+SiO2==高温==CaSiO3(高炉炼铁的造渣反应,在讲Fe,Cu性质有讲到),但是这个反应不再引起质量变化,所以不需要考虑了~.
知道这些之后如何计算,我相信你肯定轻车熟路!
总结:其实每个反应,现象不是一下子能够全部掌握的,需要通过积累,高中三年积累下来的知识量还是很多的!当积累多了,你能解决的问题也会多!就像人生阅历!阅历丰富你才能去通过自己的思路去分析问题.这样就有了创新!所以积累创新不无道理!
希望我的回答对你有所帮助1年前查看全部
- 化学过量少量的反应 比如Ca(HCO3)2 与 NaOH的反应,为什么过量的NaOH和少量的NaOH与Ca(HCO3)2
化学过量少量的反应 比如Ca(HCO3)2 与 NaOH的反应,为什么过量的NaOH和少量的NaOH与Ca(HCO3)2反应都会生成
碳酸钙,足量的NaOH与其反应后为什么不能生成氢氧化钙呢? 异言20071年前4
异言20071年前4 -
 朵朵147 共回答了17个问题
朵朵147 共回答了17个问题 |采纳率88.2%Ca(HCO3)2+ NaOH(少)=CaCO3+H20+NaHCO3
Ca(HCO3)2+2 NaOH(多)=CaCO3+Na2CO3+H2O
因为CaCO3 比Ca(OH)2稳定,如果生成Ca(OH)2,Ca(OH)2也会与HCO3-反应,也会转为CaCO3 ,1年前查看全部
大家在问
- 1设地面温度为20℃,如果每升高1㎞,气温下降6℃.
- 2虚拟机安装,如下图,接下来要做什么
- 3It’s not polite to ask people what the weather is like in En
- 4地球在呻吟的阅读答案①忧天,人类才可自救.②不必援引枯躁的数据,不必借用古老的格言,我们只须用肉眼仰望一下头顶的天空,就
- 5y=x+4与y=-2x+1的图像与y轴围成的面积是?
- 6下列金属中,金属活动性最强的是( )
- 7当飞机起飞时我正在写作业用英语怎摸说
- 8Y=18/X的积分怎么求?若不能求 其图像与X轴3到6之间的面积怎么求?
- 9已知角a的终边经过点(4,-3),则tana的值为
- 10石灰吟 古诗
- 11作文 MY VACATION八上第一课作文 MY VACATION不少于80字急
- 12a(1,0),b(4,3),c(2,4),d(m,n)当m,n满足什么条件,abcd为菱形矩形正方形梯形
- 13地球和太阳有多远?
- 14地球距离太阳有多远的距离?
- 15质量为m1,m2的两个质点,相距L,求整体重心的位置
