(2014•太原一模)教学楼的走廊里挂着一块平面镜,当同学们走近镜子时,他们在镜中所成像的大小______(选填“变大”
 peterlynn2022-10-04 11:39:541条回答
peterlynn2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 lixiangtong 共回答了19个问题
lixiangtong 共回答了19个问题 |采纳率89.5%- 解题思路:(1)物体在平面镜中成虚像,虚像和物体大小相等,跟物体到平面镜的距离无关.
(2)光的反射中,光路是可逆的.某同学在平面镜中成虚像,虚像大小和该同学大小相等,当该同学走进平面镜时,该同学本身大小不变,所以该同学的像大小不变;
同学间可以通过镜子互相看到对方,表明了反射时光路是可逆的.
故答案为:不变;可逆.点评:
本题考点: 平面镜成像的特点、原理、现象及其实验方案;光反射的可逆性.
考点点评: (1)人离平面镜越近感觉像越大,像的大小实际上是没有发生变化的,只是眼睛看像的视角变大,是眼睛的一种错觉.
(2)光的反射和光的折射中,光路都是可逆的. - 1年前
相关推荐
- (2013•太原二模)如图是某同学家里的电能表,将电饭锅单独接在电路中,发现电能表的转盘10min内转了600圈,这段时
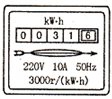 (2013•太原二模)如图是某同学家里的电能表,将电饭锅单独接在电路中,发现电能表的转盘10min内转了600圈,这段时间电饭锅实际消耗的电能是______J;电饭锅的电功率是______W.
(2013•太原二模)如图是某同学家里的电能表,将电饭锅单独接在电路中,发现电能表的转盘10min内转了600圈,这段时间电饭锅实际消耗的电能是______J;电饭锅的电功率是______W.  709060351年前1
709060351年前1 -
 网虫的kk体 共回答了19个问题
网虫的kk体 共回答了19个问题 |采纳率78.9%解题思路:从电能表的铭牌上可以看出每消耗1kW•h的电能,电能表的表盘转动3000转,可求转动60转消耗的电能,根据公式P=[W/t]可求电饭锅的电功率.电能表的转盘转动600转消耗的电能为W=[600/3000]kw•h=0.2kW•h=7.2×105J,
电饭锅的电功率是P=[W/t]=[0.2kw•h
10/60h]=1.2kW=1200W.
故答案为:7.2×105;1200.点评:
本题考点: 电功的计算;电功率的计算.
考点点评: 本题考查消耗电能和电功率的计算,关键是公式及其变形的灵活运用,重点是理解电能表的各个参数的物理意义,解题过程中还要注意单位的换算.1年前查看全部
- (2013•太原一模)如图是甲、乙、丙三种物质质量与体积的关系图象,期中甲、丙为固体,乙为足够多的液体,现用甲物质制成实
 (2013•太原一模)如图是甲、乙、丙三种物质质量与体积的关系图象,期中甲、丙为固体,乙为足够多的液体,现用甲物质制成实心小球A,用丙物质制成实心小球B,则下列说法正确的是( )
(2013•太原一模)如图是甲、乙、丙三种物质质量与体积的关系图象,期中甲、丙为固体,乙为足够多的液体,现用甲物质制成实心小球A,用丙物质制成实心小球B,则下列说法正确的是( )
A.若A、B两球质量相等,则B球的体积小
B.若将B球放入乙液体中静止后一定沉底
C.把A小球放在装入乙液体的杯中静止后,乙液体对杯底的压强一定不变
D.若A、B两球的体积相等,把两球放入乙液体中静止后,A球受到的浮力大 lauraluna1年前1
lauraluna1年前1 -
 txcw 共回答了23个问题
txcw 共回答了23个问题 |采纳率87%解题思路:A从图象上取一点,使甲、乙、丙质量相同,然后比较体积的大小.
BC根据m-v图象比较出的甲、乙、丙三种物质的密度大小,利用物体的浮沉条件逐一分析即可.
D根据图示得出两个小球排开水的体积的大小关系,根据阿基米德原理得出受到的浮力的大小关系.A、当质量相同时,甲的体积小于丙的体积,即若A、B两球质量相等,则B球的体积大,故A错误;B、据m-v图象可知甲、乙、丙三种物质的密度大小,即ρ甲>ρ乙>ρ丙,实心物体丙放入乙液体静止后,因为ρ丙<ρ乙,所以...
点评:
本题考点: 密度及其特性;物体的浮沉条件及其应用.
考点点评: 本题利用图象法求得物体的密度,根据密度公式及物体的浮沉条件进行分析求解;图象法是物理学中常用方法,在学习中应注意如何读出图象中告诉的有用信息并能加以利用.1年前查看全部
- (2011•太原模拟)下列化学用语正确的是( )
(2011•太原模拟)下列化学用语正确的是( )
A.乙烯的结构简式:CH2CH2
B.葡萄糖的结构式:C6H12O6
C.Ca2+的结构示意图:
D.NH4Cl的电子式:
 shan07181年前1
shan07181年前1 -
 心蓝331 共回答了12个问题
心蓝331 共回答了12个问题 |采纳率100%解题思路:A.乙烯中的C=C不能省略;
B.C6H12O6是葡萄糖的分子式;
C.钙是20号元素,Ca2+的核外有18个电子;
D.NH4Cl的电子式中氯离子周围8个电子.A.乙烯中的C=C不能省略,乙烯的结构简式为CH2=CH2;故A错误;
B.C6H12O6是葡萄糖的分子式,其结构简式为CH2OH(CHOH)4CHO;故B错误;
C.钙是20号元素,Ca2+的核外有18个电子,其离子结构示意图: ,故C正确;
,故C正确;
D.NH4Cl的电子式中氯离子周围8个电子,其电子式为: ,故D错误;
,故D错误;
故选C.点评:
本题考点: 电子式、化学式或化学符号及名称的综合.
考点点评: 本题考查化学用语,涉及电子式、离子结构示意图、结构简式等,注意化学用语使用的规范性即可解答,题目难度不大.1年前查看全部
- (2009•太原)A、B两座城市之间有一条高速公路,甲、乙两辆汽车同时分别从这条路两端的入口处驶入,并始终在高速公路上正
(2009•太原)A、B两座城市之间有一条高速公路,甲、乙两辆汽车同时分别从这条路两端的入口处驶入,并始终在高速公路上正常行驶.甲车驶往B城,乙车驶往A城,甲车在行驶过程中速度始终不变.甲车距B城高速公路入口处的距离y(千米)与行驶时间x(时)之间的关系如图.
(1)求y关于x的表达式;
(2)已知乙车以60千米/时的速度匀速行驶,设行驶过程中,两车相距的路程为s(千米).请直接写出s关于x的表达式;
(3)当乙车按(2)中的状态行驶与甲车相遇后,速度随即改为a(千米/时)并保持匀速行驶,结果比甲车晚40分钟到达终点,求乙车变化后的速度a.在下图中 画出乙车离开B城高速公路入口处的距离y(千米)与行驶时间x(时)之间的函数图象.
画出乙车离开B城高速公路入口处的距离y(千米)与行驶时间x(时)之间的函数图象.  水沉汀1年前0
水沉汀1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2013•太原)同学们在实验室用5%的H2O2溶液制取氧气并进行氧气性质实验.
(2013•太原)同学们在实验室用5%的H2O2溶液制取氧气并进行氧气性质实验.
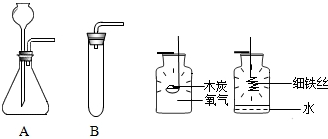
溶液配制:用50g30%的H2O2溶液(密度为1.13/cm3)配制5%的H2O2溶液(密度约为1g/cm3).溶液配制过程中,除用到玻璃棒外,还需用到下列仪器中的______.
A、托盘天平B、烧杯C、漏斗D、量筒E、胶头滴管
气体制备:用配制好的5%H2O2溶液和MnO2制取O2.请你在“A”、“B”两套装置中选择其中一套,并说明选择的理由______(合理即可),该反应的化学方程式为2H2O2
2H2O+O2↑MnO2 .2H2O2.待反应结束后同学们回收了混合物中的MnO2,实验操作为______.
2H2O+O2↑MnO2 .
性质实验:小明用收集好的氧气,进行了下面的实验:
把点燃的木条伸入集气瓶中,实验现象是______;为使铁丝在氧气中持续燃烧,他把光亮的细铁丝盘成螺丝状,______,缓慢插入集气瓶中,观察到持续剧烈燃烧.通过实验得出,氧气可以支持燃烧,并且可燃物燃烧更剧烈. taihuasong1年前1
taihuasong1年前1 -
 5965936 共回答了24个问题
5965936 共回答了24个问题 |采纳率87.5%解题思路:溶液配制:根据配制的步骤结合需要的仪器回答:计算、量取、溶解;
气体制备:根据A、B装置的特点进行分析;用过氧化氢溶液在二氧化锰做催化的条件下产生氧气和水,写出反应的方程式;根据二氧化锰难溶于水进行分离;
性质实验:根据木炭燃烧的现象及铁丝燃烧的注意事项:绕城螺旋状、用火柴引燃等分析.溶液配制:用50g30%的H2O2溶液(密度为1.13/cm3)配制5%的H2O2溶液(密度约为1g/cm3),步骤为;计算、量取、溶解,因此需要的仪器有:量筒、胶头滴管、烧杯、玻璃棒,故除用到玻璃棒外,还需用到下列仪器中的BDE;
气体制备:A装置的长颈漏斗便于添加液体药品制得较多的气体(或B装置简单);用过氧化氢溶液在二氧化锰做催化的条件下产生氧气和水,反应的方程式为:2H2O2
MnO2
.
2H2O+O2↑;因为二氧化锰难溶于水,故采用过滤、洗涤、干燥进行回收;
性质实验:木炭在纯净的氧气中燃烧,发出白光,放出热量;为使铁丝在氧气中持续燃烧,他把光亮的细铁丝盘成螺丝状,下端系一根火柴,点燃火柴,待火柴快燃尽时,缓慢插入集气瓶中,观察到持续剧烈燃烧;
故答案为:BDE;A,便于添加液体药品制得较多的气体(或B,装置简单);2H2O2
MnO2
.
2H2O+O2↑;过滤、洗涤、干燥;发出白光,放出热量;下端系一根火柴,点燃火柴,待火柴快燃尽时.点评:
本题考点: 氧气的制取装置;一定溶质质量分数的溶液的配制;混合物的分离方法;氧气的化学性质;氧气的检验和验满.
考点点评: 本题考查了溶液的配制、气体的制取、混合物的分离及氧气性质的探究,综合性较强,根据氧气相关的性质逐一分析即可.1年前查看全部
- (2013•太原)中学生应有一定的安全常识.下列做法不正确的是( )
(2013•太原)中学生应有一定的安全常识.下列做法不正确的是( )
A.室内起火时,立即打开门窗通风
B.炒菜时,油锅内以外着火,立即加入青菜灭火
C.液化气、煤气泄露起火时,首先关闭气体阀门
D.被围困在火灾区时,用湿毛巾捂住口鼻低下身子逃生 limulin20051年前1
limulin20051年前1 -
 七月神仙 共回答了22个问题
七月神仙 共回答了22个问题 |采纳率90.9%解题思路:A、根据促进燃烧的方法判断.
B、根据灭火的原理判断.
C、根据液化气、煤气泄露起火时的处理方法分析,要立即关闭阀门打开门窗,不能见明火.
D、根据湿毛巾有类似防毒面具的功能和有毒气体的密度受热会变小判断.A、室内着火时,立即打开门窗通风,会使室内空气对流,反而为燃烧提供了大量的氧气,故室内起火时,不能急于打开门窗,故说法错误.
B、炒菜时油锅着火,迅速加入大量青菜,可以降低油的温度到着火点以下,从而达到灭火的目的,故说法正确.
C、液化气、煤气具有可燃性,液化气、煤气泄露起火时,要立即关闭阀门打开门窗,降低其浓度,千万不能见明火,故说法正确.
D、湿毛巾有类似防毒面具的功能,可防止吸入有毒气体或烟尘;有毒气体的密度受热会变小,会聚集在上方,故逃生时应底下身子,故说法正确.
故选:A.点评:
本题考点: 灭火的原理和方法;防范爆炸的措施.
考点点评: “安全重于泰山”,防火、防爆问题事关人民生命财产安全,故易燃易爆物的安全知识就成了化学考查热点,了解燃烧的条件和灭火的原理、防火防爆的措施、逃生的方法等是解题的前提.1年前查看全部
- (2010•太原模拟)下列实验设计和结论相符的是( )
(2010•太原模拟)下列实验设计和结论相符的是( )
A.某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性
B.将碘水倒入分液漏斗加适量乙醇,振荡后静置,可将碘萃取到乙醇中
C.某溶液中加Ba(NO3)2溶液,再加稀盐酸,沉淀不溶解,原溶液中一定含有SO42-
D.将某气体通入品红溶液中,品红溶液褪色,该气体一定是SO2 绿色uu1年前1
绿色uu1年前1 -
 杜寒蟾 共回答了18个问题
杜寒蟾 共回答了18个问题 |采纳率88.9%解题思路:A.氨气能使湿润的红色石蕊试纸变蓝;
B.乙醇和水是互溶的;
C.硫酸钡和亚硫酸钡是不溶于硝酸的白色沉淀;
D.强氧化性的物质能使品红褪色.A.氨气能使湿润的红色石蕊试纸变蓝,则其水溶液为氨水,显碱性,故A正确;
B.乙醇和水是互溶的,不能用乙醇做碘水分离的萃取剂,故B错误;
C.某无色溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中有SO42-或SO32-中的至少一种,故C错误;
D.强氧化性的物质能使品红褪色,如氯气,不一定是二氧化硫,故D错误.
故选A.点评:
本题考点: 化学实验方案的评价.
考点点评: 本题考查物质及分离提纯,注意物质的性质及检验中排除物质之间的相互干扰是解答的关键,选项D为易错点,题目难度不大.1年前查看全部
- (2013•太原模拟)化学反应原理在工业生产中具有十分重要的意义.
(2013•太原模拟)化学反应原理在工业生产中具有十分重要的意义.
(1)工业生产可以用NH3(g)与CO2(g)经过两步反应生成尿素,两步反应的能量变化示意图如图:
则NH3(g)与CO2(g)反应生成尿素的热化学方程式为______.
(2)已知反应Fe(s)+CO2(g)⇌FeO(s)+CO(g)△H=akJ.mol-1.测得在不同温度下,该反应的平衡常数K随温度的变化如下:
①该反应的化学平衡常数表达式K=温度/ 500 700 900 K 1.00 1.47 2.40 c(CO) c(CO2) ,a______0(填“>”、“<”或“=”).在500℃2L密闭容器中进行反应,Fe和CO2的起始量均为4mol,则5min后达到平衡时CO2的转化率为c(CO) c(CO2)
______,生成CO的平均速率v(CO)为______.
②700℃反应达到平衡后,要使该平衡向右移动,其他条件不变时,可以采取的措施有______(填字母).
A.缩小反应器容积B.增加Fe的物质的量
C.升高温度到900℃D.使用合适的催化剂
(3)硫酸厂常用NaOH溶液吸收SO2废气.当吸收液呈中性时,溶液中离子浓度关系正确的是[已知n(SO
):n(HSO2−3
)=1:1时,pH=7.2](填字母)______.−3
A、c(Na+)=2c(SO
)+c(HSO2−3
)−3
B、c(Na+)>c(HSO
)>c(SO−3
)>c(H+)=c(OH-)2−3
C、c(Na+)+c(H+)=c(SO
)+c(HSO2−3
)+c(OH-)−3 哥哥的龙儿1年前1
哥哥的龙儿1年前1 -
 zzx152185 共回答了20个问题
zzx152185 共回答了20个问题 |采纳率75%解题思路:(1)由图示可知,两步反应的完成的热效应与一步完成的热效应是相同的;
(2)①化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,据此书写反应①的平衡常数,注意固体不需要写出;由表中数据可知,对于反应①,温度越高平衡常数越大,说明升高温度平衡向正反应移动,据此判断a值的符号;
令平衡时参加反应的二氧化碳的物质的量为xmol,利用三段式表示出平衡时各组分的物质的量,气体的化学计量数都为1,前后气体的物质的量相等,用物质的量代替浓度代入平衡常数计算x的值,再利用转化率定义计算二氧化碳的转化率;根据参加反应的二氧化碳的物质的量计算生成的CO的物质的量,再根据v=
计算v(CO);△n V △t
②根据平衡移动原理进行分析解答;
(3)吸收液呈中性时,溶质为亚硫酸钠和亚硫酸氢钠,电离与水解的程度相等,结合电荷守恒解答.(1)由图示可知,两步反应的完成的热效应与一步完成的热效应是相同的,将两个反应相加可得2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(l)△H=-134 kJ/mol,
故答案为:2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(l)△H=-134 kJ/mol;
(2)①反应Fe(s)+CO2(g)═FeO(s)+CO(g)的平衡常数k=
c(CO)
c(CO2),
由表中数据可知,对于反应①,温度越高平衡常数越大,说明升高温度平衡向正反应移动,升高温度平衡向吸热反应进行,故a>0,
令平衡时参加反应的二氧化碳的物质的量为xmol,则:
Fe(s)+CO2(g)═FeO(s)+CO(g)
开始(mol):4 0
变化(mol):x x
平衡(mol):4-x x
所以[x/4−x]=1,解得x=2,
故二氧化碳的转化率为[2mol/4mol]×100%=50%,
故CO表示的平均速率v(CO)=
2mol
2L
5min=0.2mol/(L•min)
故答案为:
c(CO)
c(CO2);>;50%;0.2mol/(Lmin);
②A.该反应前后气体的物质的量不变,缩小反应器体积,压强增大,平衡不移动,故A不符合;
B.铁是固体,增加铁的量,对平衡无影响,故B不符合;
C.该反应正反应是吸热反应,升高温度到900℃,平衡向正反应移动,故C符合;
D.使用合适的催化剂,加快反应速率,平衡不移动,故D不符合;
故答案为:C;
(3)吸收液呈中性时,溶质为亚硫酸钠和亚硫酸氢钠,电离与水解的程度相等,
A.由电荷守恒可知,cC(H+)+c(Na+)═2c(SO32-)+c(HSO3-)+c(OH-),中性溶液则c(H+)═c(OH-),则c(Na+)═2c(SO32-)+c(HSO3-),故A正确;
B.SO32-+H2O⇌HSO3-+OH-,HSO3-⇌H++SO32-,亚硫酸两步水解,则离子浓度为c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-),故B正确;
C.电荷守恒c(Na+)+c(H+)═2c(SO32-)+c(HSO3-)+c(OH-),选项中不遵循电荷守恒,故C错误;
故答案为:AB.点评:
本题考点: 热化学方程式;化学平衡常数的含义;化学平衡的影响因素;化学反应速率和化学计量数的关系;离子浓度大小的比较.
考点点评: 本题考查反应速率计算、平衡常数、化学平衡计算、影响反应速率与化学平衡移动的因素、盖斯定律与反应热的计算等,注意(5)中溶液中电荷守恒,物料守恒的分析判断,难度中等.1年前查看全部
- [2012·太原二模]在 T ℃时,将 a g NH 3 完全溶于水,得到 V mL溶液,假设该溶液的密度为 ρ g·c
[2012·太原二模]在 T ℃时,将 a g NH 3 完全溶于水,得到 V mL溶液,假设该溶液的密度为 ρ g·cm - 3 ,溶质的质量分数为 w ,其中含NH的物质的量为 b mol。下列叙述中正确的是( )
A.溶质的质量分数为 w =×100% B.溶质的物质的量浓度 c = mol·L - 1 C.溶液中 c (OH - )= mol·L - 1 D.上述溶液中再加入 V mL水后,所得溶液溶质的质量分数大于0.5 w  gogoqo1年前1
gogoqo1年前1 -
 xyn123 共回答了23个问题
xyn123 共回答了23个问题 |采纳率87%B
根据题中给出的已知量及各选项的要求,利用待求量的最基本计算关系代入求解即可。A不正确, w 应为×100%;根据公式 c =进行计算知B正确;由溶液中的电荷守恒可知 c (OH - )= mol·L - 1 + c (H + ),C错误;因为氨水的密度小于水的密度,故上述溶液再加 V mL水后,所得溶液溶质的质量分数小于0.5 w ,故D不正确。1年前查看全部
- 用一段话,写写家乡的某处景或某个物,要突出特点来.(200字,写山西太原的某个物)跪求!
 fasfasfasge1年前1
fasfasfasge1年前1 -
 21世纪末的ll 共回答了16个问题
21世纪末的ll 共回答了16个问题 |采纳率93.8%家乡的院子可真美啊!那一朵朵盛开的花儿可是很特别.她们不用谁去照顾,哪像城市里的花朵那样,需要人去照顾它们.院子里的葡萄更让人喜爱.那一颗颗透明的紫色的像没穿线的珠子那样,纵横交错像威尼斯的河道一般.我真想找上一双翅膀飞过去,再去享受院子的美.1年前查看全部
- 太原双星奥数题题:三角形ABC的面积是36平方厘米,点E为BC上一点,点F为AB上一点,且EF与AB垂直.三角形ABE与
太原双星奥数题
题:三角形ABC的面积是36平方厘米,点E为BC上一点,点F为AB上一点,且EF与AB垂直.三角形ABE与三角形AEC的面积相等,如果AB=9厘米,FB=FE,求三角形AFE的面积. 313281年前2
313281年前2 -
 fy360520 共回答了18个问题
fy360520 共回答了18个问题 |采纳率94.4%因:ABE=AEC,所以:ABE=AEC=18
且:AB=9,所以;EF=4,
因FE=FB,所以:AF=9-4=5
又因EF垂直AB,所以AFE=5
先画出图来就容易多了……1年前查看全部
- 太原与普中两地相距40千米,一辆汽车从太原出发,速度为45千米/时,一辆货车从普中出发,速度为35千米/时,若两车分别从
太原与普中两地相距40千米,一辆汽车从太原出发,速度为45千米/时,一辆货车从普中出发,速度为35千米/时,若两车分别从两地同时出发,经过几小时,两车相距20千米
 snowy_zxf1年前1
snowy_zxf1年前1 -
 hua0hero 共回答了16个问题
hua0hero 共回答了16个问题 |采纳率87.5%设经过x小时
(45+35)x+20=40
80x=40-20
80x=20
x=1/41年前查看全部
- 太原哪买九年级下册数学书
 zfb5241年前1
zfb5241年前1 -
 牙上有片菜 共回答了21个问题
牙上有片菜 共回答了21个问题 |采纳率90.5%省实验中学即十中旁边有个书店 满满的教科书 什么版本都有1年前查看全部
- (2014•太原二模)2013年6月20日,我国航天员王亚平在“天宫一号”中进行太空授课时,完成了制作水膜与水球的实验.
(2014•太原二模)2013年6月20日,我国航天员王亚平在“天宫一号”中进行太空授课时,完成了制作水膜与水球的实验.一个金属圆插入饮用水袋抽出,形成了一个水膜,轻晃金属圈,水膜并未破裂,而是甩出了一个小水滴.向水膜继续注水,水膜很快长成一个晶莹剔透的打水球.水球内有连串的空气泡,将针尖扎入用针筒抽出空气,水球却不受任何破坏.注入红色液体,红色慢慢扩张,水球变成一枚美丽的“红宝石”.下列说法正确的是( )
A.失重条件下水滴呈现球形是由于液体的表面张力作用
B.失重条件下能形成大水球是由于液体表面分子间只存在引力
C.空气泡内气体的压强大于气泡外气休的压强
D.当针尖戳入水球时,水的表面张力就会消失 太空肥鱼1年前1
太空肥鱼1年前1 -
 okala 共回答了21个问题
okala 共回答了21个问题 |采纳率95.2%解题思路:表面张力,是液体表面层由于分子引力不均衡而产生的沿表面作用于任一界线上的张力.将水分散成雾滴,即扩大其表面,有许多内部水分子移到表面,就必须克服这种力对体系做功;
失重条件下水滴呈现球形是由于液体的表面张力作用;空气泡内气体的压强大于气泡外气休的压强;当针尖戳入水球时,水的表面张力就会消失;水珠变成“红宝石”是因为红色液体分子在水中扩散形应的;A、失重条件下水滴呈现球形是由于失重状态下液体的重力全部用来提供向心加速度,液体的表面张力作用使液体的表面积最小化.故A正确;
B、液体表面分子间既有引力,又有斥力,整体表现为引力.故B错误;
C、由于表面张力的收缩作用,使得空气泡内气体的压强大于气泡外气休的压强.故C正确;
D、当针尖戳入水球时,水的表面张力就不会消失.故D错误;
E、水珠变成“红宝石”是因为红色液体分子在水中扩散形应的;故E正确.
故选:ACE点评:
本题考点: 超重和失重;分子间的相互作用力.
考点点评: 本题考查了液体的表面张力理论的应用,是一道基础题,掌握基础知识即可正确解题.1年前查看全部
- (2013•太原二模)顺次连接有一个内角为锐角的菱形各边中点,得到一个新的矩形,如图1,然后顺次连接新矩形各边中点,得到
(2013•太原二模)顺次连接有一个内角为锐角的菱形各边中点,得到一个新的矩形,如图1,然后顺次连接新矩形各边中点,得到一个新的菱形,如图2,再顺次连接新菱形各边中点,又得到一个新的矩形,如图3,…如此反复操作下去,则第2013个图形中等腰三角形共有______个.

 英雄本色之1年前1
英雄本色之1年前1 -
 易寒之 共回答了10个问题
易寒之 共回答了10个问题 |采纳率90%解题思路:写出前几个图形中的等腰三角形的个数,并找出规律,当n为奇数时,等腰三角形的个数是2(n+1),当n为偶数时,等腰三角形的个数是2n,根据此规律求解即可.第1个图形,有4个等腰三角形,
第2个图形,有4个等腰三角形,
第3个图形,有8个等腰三角形,
第4个图形,有8个等腰三角形,
…,
依此类推,当n为奇数时,等腰三角形的个数是2(n+1),当n为偶数时,等腰三角形的个数是2n个,
所以,第2013个图形中等腰三角形的个数是2×(2013+1)=4028.
故答案为:4028.点评:
本题考点: 规律型:图形的变化类;中点四边形.
考点点评: 本题主要考查了图形的变化,根据前几个图形的三角形的个数,观察出与序号的关系式解题的关键.1年前查看全部
- 我是太原的,怎样写《家乡美》的作文,
 落花西皮流水1年前1
落花西皮流水1年前1 -
 ainijiuri 共回答了21个问题
ainijiuri 共回答了21个问题 |采纳率90.5%太原是龙城,历史文化源远流长,先从过去的名人名物开始写起,再写如今龙城的繁荣风貌,再由表及里的写太原人流传下来的一种朴素,勤劳的精神.1年前查看全部
- (2014•太原二模)如图,平面直角坐标系中,点A,B的坐标分别为(6,0),(4,-6),△A′B′O△ABO是以原点
 (2014•太原二模)如图,平面直角坐标系中,点A,B的坐标分别为(6,0),(4,-6),△A′B′O△ABO是以原点O为位似中心的位似图形,且△A′B′O与△ABO的位似比为1:2,则B′的坐标为______.
(2014•太原二模)如图,平面直角坐标系中,点A,B的坐标分别为(6,0),(4,-6),△A′B′O△ABO是以原点O为位似中心的位似图形,且△A′B′O与△ABO的位似比为1:2,则B′的坐标为______.  zxzhuo1年前1
zxzhuo1年前1 -
 zz爱起轩 共回答了14个问题
zz爱起轩 共回答了14个问题 |采纳率85.7%解题思路:根据在平面直角坐标系中,如果位似变换是以原点为位似中心,相似比为k,那么位似图形对应点的坐标的比等于k或-k,即可求得答案.∵点A,B的坐标分别为(6,0),(4,-6),△A′B′O△ABO是以原点O为位似中心的位似图形,且△A′B′O与△ABO的位似比为1:2,
则B′的坐标为:(2,-3)或(-2,3).
故答案为:(2,-3)或(-2,3).点评:
本题考点: 位似变换;坐标与图形性质.
考点点评: 此题考查了位似图形与坐标的关系.此题比较简单,注意在平面直角坐标系中,如果位似变换是以原点为位似中心,相似比为k,那么位似图形对应点的坐标比等于±k.1年前查看全部
- (2011•太原二模)甲、乙两上实验小组分别进行测定Na2CO3和NaC1混合物中Na2CO3含量的实验.
(2011•太原二模)甲、乙两上实验小组分别进行测定Na2CO3和NaC1混合物中Na2CO3含量的实验.
甲组:沉淀分析法(相对分子质量:Na2CO3为106; BaCO3为197; BaCl2为208)
(1)配制一定物质的量浓度的BaC12溶液:用已经称量好的______gBaC12固体配制0.4mol•L-lBaCl2溶液250mL,所需要的仪器为量筒和______.
(2)把m g混合物溶解后加入过量BaC12溶液,然后将所得沉淀过滤、洗涤、烘干、称量,固体质量为wg,根据沉淀质量计算原混合物中Na2CO3的质分数为[106wg /197mg]×100%[106wg /197mg]×100%(用含m、w的代数式表示).如果原溶液中过量的Ba2+浓度达到0.01mol/L,则溶液中残留的CO32-的物质的量浓度是______.[Ksp(BaCO3)=2.58×10-9]
乙组:气体分析法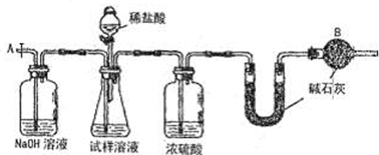
(3)实验中待锥形瓶中不再产生气体后,打开活塞从导管A端缓缓鼓入一定量的空气,这样做的目的是______.
(4)装置中干燥管B的作用是______.
(5)除已理的agNa2CO3样品外,实验中还应测定的数据是______处(填图中仪器的名称)装置实验前后的质量差.
(6)该实验还存在的明显缺陷是______. gg何在a1年前1
gg何在a1年前1 -
 偶就那浮云 共回答了28个问题
偶就那浮云 共回答了28个问题 |采纳率89.3%解题思路:(1)根据m=cVM计算gBaC12固体的质量;根据实验操作的步骤以及每步操作需要仪器确定反应所需仪器;
(2)根据化学方程式求出碳酸钠的质量进而可以表示出碳酸钠的质量分数;根据沉淀的溶度积来计算;
(3)根据实验中待锥形瓶中不再产生气体后,二氧化碳会滞留在装置中影响测定的结果;
(4)根据空气中的二氧化碳和水可以进入U型管影响测定的结果;
(5)根据实验的原理通过测定二氧化碳的质量来求出碳酸钠的质量,最后求出碳酸钠的质量分数;
(6)根据盐酸具有挥发性,制得的二氧化碳中混有氯化氢;(1)BaC12固体的质量m=cVM=0.4mol•L-l×0.25L×208g/mol=20.8g,故答案为:20.8;
溶液配制步骤为:一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水),用玻璃棒搅拌,冷却后转移到250mL容量瓶中,并用玻璃棒引流,洗涤并将洗涤液移入容量瓶中,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹面与刻度线水平相切,盖好瓶塞,摇匀,所以需要的仪器为:托盘天平、药匙、烧杯、筒量(可用、也可不用)、玻璃棒、250ml容量瓶、胶头滴管,故答案为:烧杯、玻璃棒、250ml容量瓶、胶头滴管;
(2)根据题意可知发生的反应为碳酸钠和氯化钡的反应,同时生成碳酸钡的质量为wg,所以可以据此求出碳酸钠的质量,然后得出样品中碳酸钠的质量分数;
设碳酸钠的质量为x
BaCl2+Na2CO3═2NaCl+BaCO3↓
106197
x wg
[106/ x =
197
wg ]
解得:x=[106wg /197]
所以碳酸钠的质量分数可以表示为:[106wg /197mg]×100%,
碳酸钡沉淀的溶度积为Ksp(BaCO3)=2.58×10-9,原溶液中过量的Ba2+浓度达到0.01 mol/L,则溶液中残留的CO32-的物质的量浓度为
Ksp(BaCO3)
C(Ba 2+)=
2.58×10 −9
0.01mol/L=2.58×10-7mol/L,
故答案为::[106wg /197mg]×100%;2.58×10-7mol/L;
(3)实验中待锥形瓶中不再产生气体后,二氧化碳会滞留在装置中,所以通入空气使产生的二氧化碳全部进入后续的装置,故答案为:使产生的二氧化碳全部进入后续的装置;
(4)空气中的二氧化碳和水可以进入U型管,所以装置中干燥管B的作用是吸收空气中的二氧化碳和水,故答案为:吸收空气中的二氧化碳和水;
(5)实验的原理通过测定二氧化碳的质量来求出碳酸钠的质量,二氧化碳的质量也就是U型管增重的质量,故答案为:U型管;
(6)盐酸具有挥发性,制得的二氧化碳中混有氯化氢,也能被碱石灰吸收,使得二氧化碳的质量偏大,最后结果偏大,故答案为:盐酸具有挥发性,制得的二氧化碳中混有氯化氢,U型管增重的质量偏大,最后结果偏大.点评:
本题考点: 探究物质的组成或测量物质的含量;难溶电解质的溶解平衡及沉淀转化的本质;钠的重要化合物;配制一定物质的量浓度的溶液.
考点点评: 本题主要考查了物质含量的测定,抓住测定的原理是解题的关键,难度不大.1年前查看全部
- (2011•太原模拟)下表是部分短周期元素的原子半径及主要化合价,以下叙述正确的是( )
(2011•太原模拟)下表是部分短周期元素的原子半径及主要化合价,以下叙述正确的是( )
元素代号 L M Q R T 原子半径/nm 0.160 0.143 0.112 0.104 0.066 主要化合价 +2 +3 +2 +6、-2 -2
A.气态氢化物的稳定性为H2T<H2R
B.单质与稀盐酸反应的速率为L<Q
C.M与T形成的化合物具有两性
D.L2+与R2-的核外电子数相等 lhx_2589511年前1
lhx_2589511年前1 -
 dvueiyav 共回答了17个问题
dvueiyav 共回答了17个问题 |采纳率94.1%解题思路:短周期元素,由元素的化合价可知,R、T都有-2价、处于ⅥA族,T只有-2价、R有+6价,结合原子半径,则T为O元素、R为S元素,L、Q只有+2价,处于ⅡA族,原子半径L>Q,则L为Mg元素,Q为Be元素;M有+3价,处于ⅢA族,原子半径M的介于L、Q之间,则M为Al元素,据此解答.短周期元素,由元素的化合价可知,R、T都有-2价、处于ⅥA族,T只有-2价、R有+6价,结合原子半径,则T为O元素、R为S元素,L、Q只有+2价,处于ⅡA族,原子半径L>Q,则L为Mg元素,Q为Be元素;M有+3价,处于ⅢA族,原子半径M的介于L、Q之间,则M为Al元素,
A、非金属性O>S,则氢化物稳定性H2O>H2S,故A错误;
B、金属性Mg比Be强,则Mg与酸反应越剧烈,则相同条件下单质与稀盐酸反应速率为L>Q,故B错误;
C、M与T形成的化合物是氧化铝,是两性氧化物,故C正确;
D、L2+的核外电子数为12-2=10,R2-的核外电子数为16+2=18,核外电子数不相等,故D错误.
故选:C.点评:
本题考点: 原子结构与元素周期律的关系.
考点点评: 本题考查结构性质物质关系应用,利用原子半径及化合价来推断出元素是解答本题的关键,难度不大.1年前查看全部
- (2006•太原)化学影响着社会的发展和我们的生活质量.以下认识正确的是( )
(2006•太原)化学影响着社会的发展和我们的生活质量.以下认识正确的是( )
A.硬水过滤后变为软水
B.废旧塑料可采用焚烧的方法处理
C.农药、化肥会给环境带来污染,因此禁止使用
D.回收废旧金属既节约金属资源,又减少环境污染 alh8888ld1年前1
alh8888ld1年前1 -
 talangshan 共回答了29个问题
talangshan 共回答了29个问题 |采纳率93.1%解题思路:由过滤的原理分析;焚烧废旧塑料会产生大量的空气污染物;要合理使用农药和化肥;由回收利用废旧金属得意义分析.A、过滤只能除去水中颗粒较大的不溶性物质,不能使硬水转化为软水,故说法错误;
B、焚烧废旧塑料会生成二氧化碳和有毒物质,故说法错误;
C、尽管使用化肥和农药都会造成水体的污染,而农作物的生长离不开化肥农药,所以只能合理使用,不能禁止;故说法错误;
D、回收利用废旧金属不仅可以节约资源,而且可以减少对环境的污染.故说法正确.
故选D.点评:
本题考点: 硬水与软水;金属的回收利用及其重要性;白色污染与防治;合理使用化肥、农药对保护环境的重要意义.
考点点评: 本题联系生活,难度不大,考查了化学在实际生活中的应用,体现了生活中处处有化学,要求同学们在日常生活中注意运用所学化学知识来处理问题.1年前查看全部
- (2014•太原二模)下列函数中,既是偶函数又在(0,+∞)单调递增的函数是( )
(2014•太原二模)下列函数中,既是偶函数又在(0,+∞)单调递增的函数是( )
A.y=x3
B.y=|x|+1
C.y=-x2+1
D.y=2-|x| 牛奶娃娃1年前1
牛奶娃娃1年前1 -
 所罗门海盗 共回答了11个问题
所罗门海盗 共回答了11个问题 |采纳率100%因为y=x3是奇函数,y=|x|+1、y=-x2+1、y=2-|x|均为偶函数,
所以选项A错误;
又因为y=-x2+1、y=2-|x|=(
1
2)|x|在(0,+∞)上均为减函数,只有y=|x|+1在(0,+∞)上为增函数,
所以选项C、D错误,只有选项B正确.
故选B.1年前查看全部
- (2011•太原模拟)如图,PAB,PCD是圆的两条割线,BC交AD于E,连接BD、AC,则图中的相似三角形有( )
(2011•太原模拟)如图,PAB,PCD是圆的两条割线,BC交AD于E,连接BD、AC,则图中的相似三角形有( )

A.2对
B.3对
C.4对
D.5对 小陈00071年前0
小陈00071年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2013•太原一模)下列实验操作错误的是( )
(2013•太原一模)下列实验操作错误的是( )
A.
检查气密性
B.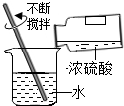
稀释浓硫酸
C.
称取氯化钠
D.
过滤粗盐水 ssii1年前1
ssii1年前1 -
 zhang83928 共回答了16个问题
zhang83928 共回答了16个问题 |采纳率93.8%解题思路:A、根据检查装置气密性的方法进行分析判断.
B、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中.
C、根据托盘天平的使用要遵循“左物右码”的原则进行分析判断.
D、过滤液体时,要注意“一贴、二低、三靠”的原则.A、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气;图中所示操作正确.
B、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;图中所示操作正确.
C、托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,图中所示操作错误.
D、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流,图中所示操作正确.
故选C.点评:
本题考点: 检查装置的气密性;称量器-托盘天平;浓硫酸的性质及浓硫酸的稀释;过滤的原理、方法及其应用.
考点点评: 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.1年前查看全部
- (2011•太原模拟)已知函数f(x)=|x-2|,g(x)=-|x+3|+m.
(2011•太原模拟)已知函数f(x)=|x-2|,g(x)=-|x+3|+m.
(1)解关于x的不等式f(x)+a-1>0(a∈R);
(2)若函数f(x)的图象恒在函数g(x)图象的上方,求m的取值范围. lymhx1年前1
lymhx1年前1 -
 9512114 共回答了18个问题
9512114 共回答了18个问题 |采纳率88.9%(Ⅰ)不等式f(x)+a-1>0即为|x-2|+a-1>0,
当a=1时,解集为x≠2,即(-∞,2)∪(2,+∞);
当a>1时,解集为全体实数R;
当a<1时,解集为(-∞,a+1)∪(3-a,+∞).
(Ⅱ)f(x)的图象恒在函数g(x)图象的上方,即为|x-2|>-|x+3|+m对任意实数x恒成立,
即|x-2|+|x+3|>m恒成立,(7分)
又由不等式的性质,对任意实数x恒有|x-2|+|x+3|≥|(x-2)-(x+3)|=5,于是得m<5,
故m的取值范围是(-∞,5).1年前查看全部
- 山西太原的那个解析英语靠谱吗,说得是会中文就会英文,有没有人听过?
 water75731年前1
water75731年前1 -
 guhe2323 共回答了13个问题
guhe2323 共回答了13个问题 |采纳率76.9%广告宣传不可尽信,每个培育班都差不多关键在于你自己又没用心学1年前查看全部
- 一支队伍从西安出发,前往太原,每小时前进30千米,2小时后,通信员因故必须返回西安,然后追上部队,每小时
一支队伍从西安出发,前往太原,每小时前进30千米,2小时后,通信员因故必须返回西安,然后追上部队,每小时
速度为80千米,求几小时后通信员能够追上队伍?追上时距西安多少千米? wszx55551年前1
wszx55551年前1 -
 需要建议的小猪1 共回答了14个问题
需要建议的小猪1 共回答了14个问题 |采纳率100%30x+120=80x
x=2.4小时
距西安的距离为2.4*30+60=132km1年前查看全部
- 关于数列的应用题 一列火车自太原驶往北京,沿途有n个车站(包括起点站太原和终点站北京)车上有一邮政厢,每停靠一站便要卸下
关于数列的应用题
一列火车自太原驶往北京,沿途有n个车站(包括起点站太原和终点站北京)车上有一邮政厢,每停靠一站便要卸下前面各站发往该站的邮袋各一个,同时又要装上该站发往后面各站的邮袋各一个,设从第k站出发时,邮政厢共有邮袋ak个(k=1,2,3,4,5,.,n)求数列{ak}的通项公式?当k为何值时,ak最大?最大值是? dxmcfte1年前1
dxmcfte1年前1 -
 Jackinghan 共回答了20个问题
Jackinghan 共回答了20个问题 |采纳率90%这列火车每到1站(包括第一站),都会获得n-k个邮袋
获得邮包总数=(n-1)+(n-2)+(n-3)+(n-4)+..+(n-k)
=(2n-k-1)k/2=(2nk-k^2-k)/2
每一站都会失去k-1个邮袋
失去邮袋总数=(1-1)+(2-1)+(3-1)+(4-1)+(5-1)+..+(n-1)
=(k-1)k/2=(k^2-k)/2
带走的邮袋=获得总数-失去总数
=(2nk-k^2-k)/2-(k^2-k)/2
=kn-k^2
{ak}=kn-k^2
根据二次函数性质:
若n为奇数,k=n/2时ak最大,为(n^2)/4
若n为偶数,k=(n-1)/2与k=(n+1)/2时同样大
为(n^2-1)/41年前查看全部
- (2012•太原模拟)甲、乙两车分别同时从A、B两地出发,相向而行,在距A地40千米处第一次相遇,到达目的地后立即返回,
(2012•太原模拟)甲、乙两车分别同时从A、B两地出发,相向而行,在距A地40千米处第一次相遇,到达目的地后立即返回,在距B地20千米处第二次相遇,A、B两地距离多少?照这样走法,两辆车第三次相遇在什么地方.
 yizhizzza1年前1
yizhizzza1年前1 -
 重要环节 共回答了16个问题
重要环节 共回答了16个问题 |采纳率93.8%解题思路:甲和乙第一次相遇时,两个合走一个全程,第二次相遇时,两人合走三个全程,两人合走一个全程时,甲走了40千米,合走三个全程时,甲应该走40×3=120千米,又因为第二次相遇时,距B地20千米,那么减去这20千米,就正好是1个全程了.照这样计算,两辆车第三次相遇时,甲又行了2个40千米即80千米,正好回到A点.40×3-20,
=120-20,
=100(千米);
20+80=100(千米);
答:A、B两地的距离是100千米,照这样的走法,两辆车第三次相遇时甲车回到A点.点评:
本题考点: 多次相遇问题.
考点点评: 解答这类题目,可以根据第一次相遇甲走的路程来进行推算,以后的每次相遇都是第一次相遇时所走路程的2倍,这样计算就简便了.1年前查看全部
- (2014•太原二模)小明使用电饭煲做饭时,发现插头有些松动且较热,仔细观察发现,插座已被烧焦,如图所示,他查阅资料后得
 (2014•太原二模)小明使用电饭煲做饭时,发现插头有些松动且较热,仔细观察发现,插座已被烧焦,如图所示,他查阅资料后得知,插头松动后,会使插头与插座间的接触难度变大.请你从物理学角度分析插座烧焦的原理.
(2014•太原二模)小明使用电饭煲做饭时,发现插头有些松动且较热,仔细观察发现,插座已被烧焦,如图所示,他查阅资料后得知,插头松动后,会使插头与插座间的接触难度变大.请你从物理学角度分析插座烧焦的原理.  polk123go1年前1
polk123go1年前1 -
 缤纷之雪 共回答了15个问题
缤纷之雪 共回答了15个问题 |采纳率93.3%解题思路:(1)插头松动后,插头与插孔接触面积减小;
(2)导体在材料、长度一定的情况下,横截面积越小,电阻越大;
(3)由Q=I2Rt可知,电流I与时间t相同时,R越大,导体电阻产生的热量越多.答:由焦耳定律Q=I2Rt可知,在电流相等的条件下,由于插头处的电阻变大,所以短时间内会产生很多热量,使插头处温度急剧升高,所以将插座烧焦.
点评:
本题考点: 焦耳定律.
考点点评: 本题考查了焦耳定律在生活中的应用,学以致用,体现了物理知识来源于生活,又服务于生活的理念,仔细审题、认真分析图示现象,灵活应用焦耳定律是解题的关键.1年前查看全部
- (2004•太原)小萍要在一幅长是90厘米、宽是40厘米的风景画四周外围,镶上一条宽度相同的金色纸边,制成一幅挂图,使风
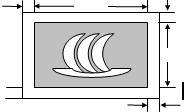 (2004•太原)小萍要在一幅长是90厘米、宽是40厘米的风景画四周外围,镶上一条宽度相同的金色纸边,制成一幅挂图,使风景画的面积是整个挂图面积的54%,设金色纸边的宽度是x厘米,根据题意所列方程是( )
(2004•太原)小萍要在一幅长是90厘米、宽是40厘米的风景画四周外围,镶上一条宽度相同的金色纸边,制成一幅挂图,使风景画的面积是整个挂图面积的54%,设金色纸边的宽度是x厘米,根据题意所列方程是( )
A.(90+x)(40+x)54%=90×40
B.(90+2x)(40+2x)54%=90×40
C.(90+x)(40+2x)54%=90×40
D.(90+2x)(40+x)54%=90×40 醉在清风1年前1
醉在清风1年前1 -
 四川广汉 共回答了19个问题
四川广汉 共回答了19个问题 |采纳率84.2%解题思路:本题可根据题意运用面积公式列出方程,再进行化简即可得出本题的答案.依题意得:
(2x+90)(2x+40)×54%=90×40.
故本题选B.点评:
本题考点: 由实际问题抽象出一元二次方程.
考点点评: 本题考查一元二次方程的运用,此类题是看准题型列出方程,题目不难,重在看准题.1年前查看全部
- (2011•太原模拟)金属钛对人体无毒且惰性,能与肌肉和骨骼生长在一起,有“生物金属”之称.下列有关 4822
(2011•太原模拟)金属钛对人体无毒且惰性,能与肌肉和骨骼生长在一起,有“生物金属”之称.下列有关
Ti和4822
Ti的说法中正确的是( )5022
A.
Ti和4822
Ti原子中均含有22个中子5022
B.
Ti和4822
Ti在周期表中位置相同,都在第4纵行5022
C.分别由
Ti和4822
Ti组成的金属钛单质物理性质相同5022
D.
Ti与4822
Ti为同一核素5022 一天到晚闲逛的猪1年前1
一天到晚闲逛的猪1年前1 -
 xiexin19821110 共回答了15个问题
xiexin19821110 共回答了15个问题 |采纳率86.7%A、
4822Ti和
5022Ti的质子数相同都是22,中子数分别为48-22=26,50-22=28,故A错误;
B、
4822Ti和
5022Ti属于同种元素,质子数为22,属于22-2-8-8=4,处于周期表第四周期,第4列,故B正确;
C、
4822Ti和
5022Ti互为同位素,组成的金属钛单质物理性质不相同,化学性质几乎相同,故C错误;
D、
4822Ti和
5022Ti质子数相同中子数不同,互为同位素,是Ti元素不同的核素,故D错误.
故选B.1年前查看全部
- (2013•太原二模)造船厂的船台是一座设在江边的水泥斜坡,在斜坡上装有木制的滑道,船体就放在船台上,船体与滑道之间还放
 (2013•太原二模)造船厂的船台是一座设在江边的水泥斜坡,在斜坡上装有木制的滑道,船体就放在船台上,船体与滑道之间还放有木板--滑板,滑板和船体用“止滑器”平行滑道向上拉住.船体造好后,打开“止滑器”,整个船体连同滑板从涂满润滑油脂的滑道上滑下去,这就是传统的“下水”方式.
(2013•太原二模)造船厂的船台是一座设在江边的水泥斜坡,在斜坡上装有木制的滑道,船体就放在船台上,船体与滑道之间还放有木板--滑板,滑板和船体用“止滑器”平行滑道向上拉住.船体造好后,打开“止滑器”,整个船体连同滑板从涂满润滑油脂的滑道上滑下去,这就是传统的“下水”方式.
已知某船台水泥斜坡的坡度[h/d=1 20],船体质量为M=4.2×106kg,滑板的质量m=1.0×104kg,滑板与滑道间的动摩擦因数为μ1=0.03.设最大静摩擦力等于滑动摩擦力,取sina≈tana,cosa=1,g=10m/s2,问:
(1)在制造过程中为保证船体和滑板不向下滑动,“止滑器”在与滑道平行的方向上至少要施加多大的力?
(2)船体“下水”时,为保证船体与滑板不会相对滑动,船体与滑板间的动摩擦因数μ2应满足什么关系?赞
funster 幼苗
共回答了24个问题采纳率:87.5% 举报
(1)船体滑板整体处于静止,合力为零,故:
(M+m)gsinα-Ff-FT=0
FN-(M+m)gcosθ=0
而,Ff=μ1FN
解得:FT=8.42×105N
(2)为保证船体与滑板不会相对滑动,两者应具有共同的加速度,由牛顿第二定律得:
(M+m)gsinα-Ff=(M+m)a
所以,a=gsinα-μ1gcosα
隔离船体,分析船体受力
Mgsinα-Ff′=Ma
FN′-Mgcosα=0
Ff≤μ2FN′
故,μ2≥μ1=0.03
答:(1)止滑器在与滑道平行的方向上至少要施加8.42×105N的力
(2)船体与滑板间的动摩擦因数μ2应满足故,μ2≥μ1=0.031年前
2可能相似的问题-
1年前1个回答
-
1年前1个回答
你能帮帮他们吗
Copyright © 2022 YULUCN.COM - 雨露学习互助 - 17 q. 0.049 s. - webmaster@yulucn.com huzc911111年前1
huzc911111年前1 -
 funster 共回答了24个问题
funster 共回答了24个问题 |采纳率87.5%(1)船体滑板整体处于静止,合力为零,故:
(M+m)gsinα-Ff-FT=0
FN-(M+m)gcosθ=0
而,Ff=μ1FN
解得:FT=8.42×105N
(2)为保证船体与滑板不会相对滑动,两者应具有共同的加速度,由牛顿第二定律得:
(M+m)gsinα-Ff=(M+m)a
所以,a=gsinα-μ1gcosα
隔离船体,分析船体受力
Mgsinα-Ff′=Ma
FN′-Mgcosα=0
Ff≤μ2FN′
故,μ2≥μ1=0.03
答:(1)止滑器在与滑道平行的方向上至少要施加8.42×105N的力
(2)船体与滑板间的动摩擦因数μ2应满足故,μ2≥μ1=0.031年前查看全部
- 最近几天太原夜空中正东方向非常亮的那颗星星是什么啊?是人造卫星还是太阳系行星?
 asd9816181年前3
asd9816181年前3 -
 三棱镜假发 共回答了18个问题
三棱镜假发 共回答了18个问题 |采纳率77.8%人造飞行器除了同步卫星以外位置都不是固定的,亮度也不高.一般可以认为是行星,当然也可能是天狼、大角等恒星.
内地行星(水星和金星)离太阳的距离不会太远,晚上不会出现在东方.
火星的亮度不低,但一般可以看出略带火红色.
天狼等特殊恒星现在要到后半夜才可以看到(大角要到春季找牧夫座了o(╯□╰)o)
另外,土星10月星等只有0.7,亮度一般.
而木星10月星等约为-2.9,所以“夜空中正东方向非常亮的那颗星星”应该是木星^_^1年前查看全部
- (2014•太原二模)如图所示的玻璃装置内放入适量的水,在阀门E、F关闭的情况下,此装置相当于一个______,将此装置
 (2014•太原二模)如图所示的玻璃装置内放入适量的水,在阀门E、F关闭的情况下,此装置相当于一个______,将此装置的阀门E打开,接到水流速度稳定的自来水管上,同时打开阀门F,水在流动的过程中,两竖直管中的高度关系是______(选填“C的高”、“D的高”或“一样高”)
(2014•太原二模)如图所示的玻璃装置内放入适量的水,在阀门E、F关闭的情况下,此装置相当于一个______,将此装置的阀门E打开,接到水流速度稳定的自来水管上,同时打开阀门F,水在流动的过程中,两竖直管中的高度关系是______(选填“C的高”、“D的高”或“一样高”)  5lk9ec1年前1
5lk9ec1年前1 -
 suki520001 共回答了25个问题
suki520001 共回答了25个问题 |采纳率96%解题思路:(1)上端开口,底部连通的容器构成连通器,在水不流动时,其水面应该是相平的;
(2)当水流时,分析A和B管水流速度大小,根据流体流速越大,压强越小,判断A和B管内水的压强,来分析C和D管水面高低.(1)如图所示的玻璃装置内放入适量的水,在阀门E、F关闭的情况下,此装置上端开口,底部连通,相当于一个连通器,其液面相平;
(2)水流流过AB管,由于A管横截面积大,水流速度小,水的压强大,C管水面高;B管横截面积小,水流速度大,水的压强小,D管水面低.
故答案为:连通器; C的高.点评:
本题考点: 流体压强与流速关系的探究实验;连通器原理.
考点点评: 对于流体压强跟流速关系的问题,一般要分析两处的流体流速,根据流体压强跟流速的关系,判断压强,判断物体的运动情况.1年前查看全部
- (2012•太原模拟)已知命题p:若x2+y2=0,则x、y全为0;命题q:∃x∈R,使sinx+cosx=32.则下列
(2012•太原模拟)已知命题p:若x2+y2=0,则x、y全为0;命题q:∃x∈R,使sinx+cosx=
.则下列命题是真命题的是( )3 2
A.p∧q
B.(¬p)∨q
C.p∧(¬q)
D.(¬p)∧q tzds881年前0
tzds881年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2008•太原)人的视觉机能受运动速度的影响很大,行驶中司机在驾驶室内观察前方物体时是动态的,车速增加,视野变窄.当车
(2008•太原)人的视觉机能受运动速度的影响很大,行驶中司机在驾驶室内观察前方物体时是动态的,车速增加,视野变窄.当车速为50km/h时,视野为80度.如果视野f(度)是车速v(km/h)的反比例函数,求f,v之间的关系式,并计算当车速为100km/h时视野的度数.
 worldcitizen1年前2
worldcitizen1年前2 -
 yzzzz 共回答了22个问题
yzzzz 共回答了22个问题 |采纳率100%设f、v的关系式为f=k/v,(50,80 )代入得k=4000∴f=4000/v
当v=100时f=4000/100=401年前查看全部
- 阅读下面的文言文,完成问题。 杨业,并州太原人。父信,为汉麟州刺史。业幼倜傥任侠,善骑射,好畋猎,所获倍于人。弱冠事刘
阅读下面的文言文,完成问题。
杨业,并州太原人。父信,为汉麟州刺史。业幼倜傥任侠,善骑射,好畋猎,所获倍于人。弱冠事刘崇 ① ,为保卫指挥使,以骁勇闻。累迁至建雄军节度使,屡立战功,所向克捷,***号为“无敌”。
太宗征太原,尝购求之。既而孤垒甚危,业劝其主刘继元降,以保生聚。继元既降,帝遣中使召见业,大喜,以为右领军卫大将军。师还,授郑州刺史。帝以业老于边事,复迁代州兼三交驻泊兵马都部署。会契丹入雁门,业领麾下数千骑自西陉而出,由小陉至雁门北口,南向背击之,契丹大败。以功迁云州观察使,仍判郑州、代州。自是,契丹望见业旌旗即引去。 主将戍边者多忌之,有潜上谤书斥言其短,帝览之皆不问,封其奏以付业 。
雍熙三年,大兵北征,以忠武军节度使潘美为云、应路行营都部署,命业副之。诸军连拔云、应、寰、朔四州,师次桑乾河,会曹彬之师不利,诸路班师,美等归代州。
未几,诏迁四州之民于内地,令美等以所部之兵护之。时契丹***萧氏与其大臣耶律汉宁等领众十余万,复陷寰州。业谓美等曰:“今辽兵益盛,不可与战。先遣人密告云、朔州守将,俟大军离代州日,令云州之众先出。我师次应州,契丹必来拒,即令朔州民出城,直入石碣谷。”护军王侁 ② 沮其议曰:“领数万精兵而畏懦如此。但趋雁门北川中,鼓行而往。”护军刘文裕亦赞成之。业曰:“不可,此必败之势也。”侁曰:“君侯素号无敌,今见敌逗挠不战,得非有他志乎?”业曰:“业非避死,盖时有未利,徒令杀伤士卒而功不立。今君责业以不死,当为诸公先。”将行,泣谓美曰:“此行必不利。非纵敌不击,盖伺其便,将立尺寸功以报国恩。今诸君责业以避敌,业当先死于敌。”因指陈家谷口曰:“诸君于此张步兵强弩,为左右翼以援,不然,无遗类矣。”美即与侁领麾下兵阵于谷口。
自寅至巳,侁使人登托逻台 ③ 望之,以为契丹败走,欲争其功,即领兵离谷口。 美不能制,乃缘交河西南行二十里。俄闻业败,即麾兵却走 。业力战,自午至暮,果至谷口。望见无人,再率帐下士力战,身被数十创,士卒殆尽,业犹手刃数十百人。马重伤不能进,遂为契丹所擒,其子延玉亦没焉。业不食,三日死。
(节选自《宋史·杨业传》)
注:①刘崇、刘继元,为后汉的开国、末代帝王。 ②侁,古国名。③托逻台:在山西朔州宁武山处。
1.对下列加点字的解释错误的一项是( )
a.太宗征太原,尝 购 求之 购求:重金以求
b.帝以业 老 于边事 老:老练,有经验
c.护军王侁 沮 其议曰 沮:沮丧
d.今见敌 逗挠 不战 逗挠:曲行避敌以观望
2.下列各组中全都能表现杨业骁勇善战的一项是( )
①善骑射,好畋猎,所获倍于人
②屡立战功,所向克捷
③南向背击之,契丹大败
④今君责业以不死,当为诸公先
⑤业犹手刃数十百人
⑥业不食,三日死
a.①②④
b.②③⑤
c.③④⑤
d.④⑤⑥
3.下列对原文内容的理解和分析错误的一项是( )
a.杨业年幼时就洒脱豪爽、见义勇为。杨业在二十岁左右的时候在后汉帝王刘崇朝中做了保卫指挥使,后升迁至节度使一职,被人誉为“杨无敌”。
b.宋太宗征讨并围困太原城,使得太原城成为危险的孤城,此时“杨无敌”为了保全城中的生灵,劝服他的主子刘继元向宋太祖投降。
c.***命令迁徙四个州府的百姓到内地,杨业向潘美提出的避开强敌、秘密撤出四个州府之民的策略,被护军王侁讥讽为畏惧、懦弱、退缩之举。
d.杨业虽是无敌将军,但在陈家谷口因无援军而被契丹军队所擒,而且他的儿子杨延玉也在战斗中死去。
4.将文中画线句子翻译成现代汉语。
(1)主将戍边者多忌之,有潜上谤书斥言其短,帝览之皆不问,封其奏以付业。
__________________________________________________________
(2)美不能制,乃缘交河西南行二十里。俄闻业败,即麾兵却走。
__________________________________________________________ 沽名求沧桑1年前1
沽名求沧桑1年前1 -
 牛雅的妹妹 共回答了19个问题
牛雅的妹妹 共回答了19个问题 |采纳率94.7%1.C
2.B
3.C
4.(1)戍守边关的主将大多嫉妒杨业,有人暗中上奏诽谤书信指责说杨业的短处,皇帝看后都不追问(责问),封上奏折来交给杨业。
(2)潘美不能够制止住,于是沿着交河向西南行进二十里地。不久听说杨业兵败,就率兵退走。1年前查看全部
- 太原的冬天是冷的用英语怎么说
 Holly_琳儿1年前3
Holly_琳儿1年前3 -
 samwallace 共回答了19个问题
samwallace 共回答了19个问题 |采纳率84.2%1.It's cold in winter at Taiyuan
2.During the winter,it's cold at Taiyuan.1年前查看全部
- (2013•太原模拟)用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是( )
 (2013•太原模拟)用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是( )
(2013•太原模拟)用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是( )
A.若A为浓盐酸,B为KMnO4晶体,C中盛有紫色石蕊溶液,则C中溶液最终是红包
B.实验仪器D可以起到防止溶液倒吸的作用
C.若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,则C中溶液先产生白色沉淀后沉淀又溶解
D.若A为浓H2SO4,B为Cu,C中盛有澄清石灰水,则C中溶液变浑浊 qq06261年前1
qq06261年前1 -
 xbamboo 共回答了16个问题
xbamboo 共回答了16个问题 |采纳率93.8%解题思路:A.氯气通到紫色石蕊溶液中,溶液先变红,后褪色;
B.D装置上部容积较大,倒吸的液体靠自身重量回落;
C.氢氧化铝能溶于强酸和强碱,但不溶于弱碱;
D.浓硫酸和Cu的反应需要加热.A.若A为浓盐酸,B为KMnO4晶体,二者反应生成氯气,把氯气通到紫色石蕊溶液中,氯气与水反应生成HCl和HClO,HCl使紫色石蕊溶液变红,HClO具有漂白性,使溶液褪色,故A错误;
B、导气管下端连接球形干燥管时,由于球形干燥管中间部分较粗,盛放的液体的量较多,倒吸的液体靠自身重量回落,因此可以防止液体倒吸,故B正确;
C、若A为浓氨水,B为生石灰,滴入后反应生成氨气,氨气和铝离子反应生成氢氧化铝,但氢氧化铝不溶于氨水,所以C中产生白色沉淀不溶解,故C错误;
D、若A为浓硫酸,B为Cu,反应需要加热才能反应,如果不加热,则没有二氧化硫产生,所以C中溶液无变化,故D错误;
故选B.点评:
本题考点: 实验装置综合.
考点点评: 本题考查了氯气、氨气、浓硫酸等性质的分析判断,明确反应条件是解题关键,题目难度中等.1年前查看全部
- 在比例尺为1:8000000的地图上,量得太原到北京的距离为6.4厘米,将实际距离用科学记数法表示为______千米(保
在比例尺为1:8000000的地图上,量得太原到北京的距离为6.4厘米,将实际距离用科学记数法表示为______千米(保留两个有效数字).
 雄师1年前4
雄师1年前4 -
 ruidancin 共回答了15个问题
ruidancin 共回答了15个问题 |采纳率86.7%解题思路:先根据比例尺求出太原到北京的实际距离,然后用科学记数法保留两个有效数字得出结果.6.4厘米×8 000 000=51 200 000厘米=512千米≈5.1×102千米.
点评:
本题考点: 科学记数法与有效数字.
考点点评: 将一个绝对值较大的数写成科学记数法a×10n的形式时,其中1≤|a|<10,n为比整数位数少1的数.
用科学记数法保留有效数字,要在标准形式a×10n中a的部分保留,从左边第一个不为0的数字数起,需要保留几位就数几位,然后根据四舍五入的原理进行取舍.1年前查看全部
- (2014•太原二模)若sin([π/3]+a)=[1/3],则cos([π/6]-a)=[1/3][1/3].
 不知道想知道1年前1
不知道想知道1年前1 -
 苏小毕 共回答了23个问题
苏小毕 共回答了23个问题 |采纳率73.9%解题思路:原式中的角度变形后,利用诱导公式化简,将已知等式代入计算即可求出值.∵sin([π/3]+α)=[1/3],
∴cos([π/6]-α)=cos[[π/2]-([π/3]+α)]=sin([π/3]+α)=[1/3].
故答案为:[1/3]点评:
本题考点: 运用诱导公式化简求值.
考点点评: 此题考查了运用诱导公式化简求值,熟练掌握诱导公式是解本题的关键.1年前查看全部
- (2011•太原)将一个矩形纸片依次按图(1)、图(2)的方式对折,然后沿图(3)中的虚线裁剪,最后将图(4)的纸再展开
(2011•太原)将一个矩形纸片依次按图(1)、图(2)的方式对折,然后沿图(3)中的虚线裁剪,最后将图(4)的纸再展开铺平,所得到的图案是( )

A.
B.
C.
D.
 江灵1年前1
江灵1年前1 -
 34499 共回答了13个问题
34499 共回答了13个问题 |采纳率92.3%解题思路:按照题意要求,动手操作一下,可得到正确的答案.严格按照图中的顺序先向上再向右对折,从左下方角剪去一个直角三角形,展开得到结论.
故选A.点评:
本题考点: 剪纸问题.
考点点评: 本题主要考查学生的动手能力及空间想象能力.对于此类问题,学生只要亲自动手操作,答案就会很直观地呈现.1年前查看全部
- 世界最高峰珠穆朗玛峰的海拔为8844.43米,太原平均海拔约800米,两地的相对高度是( )
世界最高峰珠穆朗玛峰的海拔为8844.43米,太原平均海拔约800米,两地的相对高度是( )
A.844.43米
B.8044.43米
C.9644.43米
D.44.43米 sunny花木兰1年前1
sunny花木兰1年前1 -
 sky860708 共回答了19个问题
sky860708 共回答了19个问题 |采纳率100%解题思路:海拔是地面某一个地点高出海平面的垂直距离,相对高度是指地面某个地点高出另一个地点的垂直距离,即两个地点之间的高度差.珠穆朗玛峰的海拔高度为8844.43米,太原平均海拔约800米,二者的相对高度就是二者海拔高度的差,即8844.43米-800米=8044.43米.
故选:B.点评:
本题考点: 海拔和相对高度及其估算.
考点点评: 这是一道典型的地理计算题型,要求在做题时一定要计算准确.1年前查看全部
- (2014•太原一模)如图为汽车油量表的工作原理图,当汽车发动机工作时,油箱内汽油的液面下降,则变阻器连入电路的电阻及电
 (2014•太原一模)如图为汽车油量表的工作原理图,当汽车发动机工作时,油箱内汽油的液面下降,则变阻器连入电路的电阻及电流表示数变化情况正确的是( )
(2014•太原一模)如图为汽车油量表的工作原理图,当汽车发动机工作时,油箱内汽油的液面下降,则变阻器连入电路的电阻及电流表示数变化情况正确的是( )
A.不变不变
B.变小变小
C.变大变大
D.变大变小 我爱璇璇1年前1
我爱璇璇1年前1 -
 robbin_dx 共回答了14个问题
robbin_dx 共回答了14个问题 |采纳率64.3%解题思路:根据汽油液面的变化判断滑动变阻器接入电路的阻值如何变化,应用欧姆定律判断电路电流如何变化,然后判断电流表示数如何变化.由图示可知,油箱内汽油的液面下降时,滑片向上移动,滑动变阻器连入电路的阻值变大,蓄电池电压不变,滑动变阻器接入电路的阻值变大,由欧姆定律可知,电路电流减小,电流表示数变小;
故选D.点评:
本题考点: 电路的动态分析.
考点点评: 本题的关键是滑动变阻器的变阻原理:通过改变连入电阻丝的长度,改变阻值的大小,从而改变电路中的电流.1年前查看全部
- (2011•太原二模)如图,点A1是▱ABCD对角线AC上的一点,将△ADC沿着AC方向平移,点A移到点A1后得到△A1
 (2011•太原二模)如图,点A1是▱ABCD对角线AC上的一点,将△ADC沿着AC方向平移,点A移到点A1后得到△A1D1C1.
(2011•太原二模)如图,点A1是▱ABCD对角线AC上的一点,将△ADC沿着AC方向平移,点A移到点A1后得到△A1D1C1.
(1)在图中画出平移后的△A1D1C1,并连接AD1、BC1;
(2)在(1)中画出的图中,除了△ABC≌△C1D1A1≌△CDA还有几对全等的三角形(不能另外添加辅助线或文字),请选择其中的一对加以证明. 时间剩一秒1年前1
时间剩一秒1年前1 -
 mijn 共回答了18个问题
mijn 共回答了18个问题 |采纳率88.9%1年前查看全部
- (2009•太原)医疗上,许多化学物质用于治疗疾病或辅助诊断疾病.
(2009•太原)医疗上,许多化学物质用于治疗疾病或辅助诊断疾病.
(1)用X射线检查胃肠疾病时,要让患者服用“钡餐”(主要成分是难溶于水和盐酸的硫酸钡).硫酸钡属于______(填“酸”、“碱”或“盐”),它是由钡离子和______(填离子符号)构成;
(2)硫酸钡可由Ba(OH)2和稀硫酸反应制得,反应的化学方程式为______;
(3)碳酸钡也难溶于水,但不能用BaCO3制“钡餐”,这是因为BaCO3能与胃液中的盐酸反应,化学方程式为______,反应生成的BaCl2是重金属盐,易溶于水,会使人中毒.,故有人误服BaCO3而造成BaCl2中毒,可饮用适量的硫酸钠溶液解毒,这是因为______. jiajia10721年前1
jiajia10721年前1 -
 春秋战nning 共回答了18个问题
春秋战nning 共回答了18个问题 |采纳率88.9%解题思路:(1)根据盐是由金属离子和酸根离子组成的分析即可.
(2)根据复分解反应的原理即可写出化学方程式.
(3)根据碳酸钡难溶于水,但是会溶于酸,即可写出方程式.要想解毒,应将可溶性钡盐转化为不溶性性钡盐.(1)根据盐是由金属离子和酸根离子组成,即可看出答案为:盐,SO42-(2)根据复分解反应的原理,可以得出氢氧化钡和硫酸互相交换成分生成硫酸钡和水,故选Ba(OH)2+H2SO4=BaSO4↓+2H2O(3)根据碳酸钡难溶于水,但...
点评:
本题考点: 常用盐的用途;酸的化学性质;常见的氧化物、酸、碱和盐的判别;分子、原子、离子、元素与物质之间的关系;书写化学方程式、文字表达式、电离方程式;常见中毒途径及预防方法.
考点点评: 本题重点考查了复分解反应的原理,盐的定义以及可溶性盐与不溶性盐之间的转换.1年前查看全部
- (2012•太原一模)A~J是中学化学中常见的几种物质,它们之间的转化关系如图所示(部分反应条件已略去).已知常温下A为
 (2012•太原一模)A~J是中学化学中常见的几种物质,它们之间的转化关系如图所示(部分反应条件已略去).已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,J可用作杀菌消毒剂.请回答下列问题:
(2012•太原一模)A~J是中学化学中常见的几种物质,它们之间的转化关系如图所示(部分反应条件已略去).已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,J可用作杀菌消毒剂.请回答下列问题:
(1)B的电子式是______.
(2)J的水溶液显______(填“酸性”、“碱性”或“中性”),其原因是______(用离子方程式表示).
(3)已知a g F在足量C中燃烧,恢复至室温时放出的热量是b kJ,请写出相应的热化学方程式:2H2(g)+O2(g)=2H2O(l)△H=-[4b/a]kJ/mol2H2(g)+O2(g)=2H2O(l)△H=-[4b/a]kJ/mol.
(4)若在1L 0.2mol•L-1 AlCl3溶液中逐滴加入等体积的0.7mol•L-1 D溶液,则此过程中将观察到:______.
(5)常温下,以Pt为电极电解滴加有少量酚酞的H的饱和溶液,则在______(填“阴”或“阳”)极附近溶液由无色变为红色,若在此极收集到标准状况下2.24L气体,则此时溶液的pH是______(假设溶液的体积为2L且不考虑电解后体积的变化).
(6)实验室可用不含E的乙醇处理少量残留的A,有关反应的化学方程式是______. liuweihong981年前1
liuweihong981年前1 -
 sdych12345 共回答了19个问题
sdych12345 共回答了19个问题 |采纳率94.7%解题思路:常温下A为固体单质,B为淡黄色粉末,C是气体,A和C反应生成B,则B是Na2O2,A是Na,C是O2;E在常温下为液体,E是H2O,钠和水反应生成NaOH和氢气,过氧化钠和水反应生成氢氧化钠和氧气,C是氧气,D是NaOH,F是H2;
H的水溶液通电生成氢气、I气体和氢氧化钠,且J可作杀菌消毒剂,为次氯酸盐,所以I是Cl2,电解饱和食盐水制取氯气,所以H是NaCl,氢气和氯气反应生成G,所以G是HCl;氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,所以J是NaClO,然后结合物质的性质及化学用语来解答.常温下A为固体单质,B为淡黄色粉末,C是气体,A和C反应生成B,则B是Na2O2,A是Na,C是O2;E在常温下为液体,E是H2O,钠和水反应生成NaOH和氢气,过氧化钠和水反应生成氢氧化钠和氧气,C是氧气,D是NaOH,F是H2;
H的水溶液通电生成氢气、I气体和氢氧化钠,且J可作杀菌消毒剂,为次氯酸盐,所以I是Cl2,电解饱和食盐水制取氯气,所以H是氯化钠,氢气和氯气反应生成G,所以G是HCl;氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,所以J是NaClO,
(1)通过以上分析知,B是Na2O2,电子式为 ,故答案为:
,故答案为: ;
;
(2)J是NaClO,发生水解离子反应为ClO-+H2O⇌HClO+OH-,溶液显碱性,故答案为:碱性;ClO-+H2O⇌HClO+OH-;
(3)F是H2,C是O2,a gF在足量C中燃烧,恢复至室温时放出的热量是bkJ,则 2molF燃烧生成液态水放出[4b/a]kJ热量,则热化学方程式为2H2(g)+O2(g)=2H2O(l)△H=-[4b/a]kJ/mol,故答案为:2H2(g)+O2(g)=2H2O(l)△H=-[4b/a]kJ/mol;
(4)D为NaOH,1L 0.2mol•L-1 AlCl3溶液中逐滴加入等体积的0.7mol•L-1 D溶液,先生成氢氧化铝,后氢氧化铝与NaOH反应而溶解,但二者物质的量之比为2:7,沉淀不能完全溶解,则观察到先有白色沉淀生成,后沉淀部分溶解,故答案为:先有白色沉淀生成,后沉淀部分溶解;
(5)H为NaCl,电解滴加有少量酚酞的H的饱和溶液发生2NaCl+2H2O
电解
.
2NaOH+Cl2↑+H2↑,氢离子在阴极放电同时生成氢氧根离子,则无色变为红色,在此极收集到标准状况下2.24L气体,n(H2)=0.1mol,由反应可知,n(NaOH)=0.2mol,则c(NaOH)=[0.2mol/2L]=0.1mol/L,所以pH=13,
故答案为:阴;13;
(6)实验室可用不含E的乙醇处理少量残留的A,发生的化学方程式为2Na+2C2H5OH→2C2H5ONa+H2↑,故答案为:2Na+2C2H5OH→2C2H5ONa+H2↑.点评:
本题考点: 无机物的推断.
考点点评: 本题考查无机物的推断,把握元素化合物的特性和反应,并用框图结合正向思维、逆向思维、发散和收敛思维,利用题眼正确判断物质是解本题的关键,本题的题眼为“B为淡黄色粉末,E在常温下为液体”,题目难度较大,综合性较强.1年前查看全部
- (2012•太原一模)下列对有关化学反应过程或实验现象的解释中,正确的是( )
(2012•太原一模)下列对有关化学反应过程或实验现象的解释中,正确的是( )
A.NH3的水溶液可以导电,说明NH3是电解质
B.在高温条件下,C能置换出SiO2中的Si,说明C的氧化性强于Si
C.在滴有酚酞的Na2CO3溶液中,加入CaCl2溶液,溶液褪色,说明CaCl2溶液有酸性
D.向淀粉碘化钾的溶液中加入溴水,溶液变为蓝色,说明Br2的氧化性强于I2 北方狼魂1年前1
北方狼魂1年前1 -
 taizhaoyang 共回答了16个问题
taizhaoyang 共回答了16个问题 |采纳率93.8%解题思路:A.NH3是非电解质,从氨气与水反应的角度分析;
B.C能置换出SiO2中的Si,表现为还原性;
C.从水解平衡移动的角度分析;
D.溶液变为蓝色,说明生成碘,根据氧化剂氧化性大于氧化产物氧化性判断.A.NH3的水溶液可以导电,是因为氨气和水反应生成一水合氨,一水合氨电离出自由移动的离子,NH3是非电解质,故A错误;
B.C能置换出SiO2中的Si,表现为还原性,故B错误;
C.Na2CO3水解呈碱性,加入CaCl2溶液,生成碳酸钙沉淀,碳酸根离子浓度减小,则红色褪去,故C错误;
D.溶液变为蓝色,说明生成碘,反应中溴为氧化剂,碘为还原剂,氧化剂氧化性大于氧化产物氧化性,故D正确.
故选D.点评:
本题考点: 化学实验方案的评价;氧化性、还原性强弱的比较;电解质与非电解质.
考点点评: 本题考查较为综合,涉及电解质、氧化还原反应、水解平衡等知识,侧重于学生的分析能力、实验能力和评价能力的考查为高考常见题型,注意把握相关实验方法和注意事项,难度不大.1年前查看全部
- 急需一篇介绍家乡的英文介绍 太原的
 优游悠悠3331年前1
优游悠悠3331年前1 -
 你好再見 共回答了20个问题
你好再見 共回答了20个问题 |采纳率85%Taiyuan,the capital of Shanxi Province,is bounded on three sides by mountains.It has a 2500-year history and in ancient times was an important military town.Now Taiyuan is one of China's heavy industrial cities and accounts for more than half the national coal mining output.
Taiyuan also has a wealth of tourist attractions and notably among these is the Jinci Temple.This is the city's most attractive temple although the Shuangta Si (Twin-Pagoda Temple) has become a symbol of Taiyuan on account of its unique architecture.Another major attraction is the Tianlong Shan Stone Caves where magnificent sculptures dating from the Tang Dynasty (618-907) may be seen.
Taiyuan benefits from convenient public transport systems as the city is the provincial transportation hub.Accommodation facilities have become more and more advanced over recent years and range from 5-star hotels to a selection of comfortable guest houses.
The gourmand should be aware that Shanxi noodles are highly reputed all over China,as well as the local vinegar.Other local delicacies are the Tou Nao,the Steamed Dumpling,Sausages and Mutton Soup.To accompany these wholesome foods there are Fen Jiu (Fen Wine) and Zhuye Qing (Zhuye Qing Wine).As well as its cuisine the city is noted for products such as finely crafted lacquer ware.
太原,山西省省会,三面环山为界.它有2500年的历史,在古代是一个重要的军事重镇.现在太原是中国重工业城市,占全国一半以上的煤矿产量之一.
太原也具有丰富的旅游景点,特别是其中的晋祠.这是这个城市最具吸引力的寺庙,因其独特的太原市建筑,已经变成了一种象征,.另一个主要景点是天龙山石窟的宏伟雕塑,在自唐朝(公元618—907年)天龙山石窟.
太原得益于方便快捷的公交系统为省级交通枢纽城市.住宿设施也变得越来越先进,近年来,范围从五星级酒店客人选择舒适的房子.
美食家应该知道的山西面条在中国非常有名,以及当地的醋.其他地方风味小吃是头垴,蒸饺,香肠和羊肉汤.伴随这些有益健康的食品有有汾酒(汾酒)和竹叶清(竹叶清酒).以及它的美食城市和精雕细琢的漆器产品.1年前查看全部
大家在问
- 1笑笑看一本故事书,第一天看了全书的四分之一,第二天看了全书的20%多两页,这时正好还剩下全书的64
- 2一个额度功率1w.阻值100欧的电阻 额度电流多大?
- 3某地出租车收费方法如下:乘车路程不超过3千米时,收费4元(起步价);超过3千米时,超过部分按每千米1.2元加收车费.某乘
- 4若线段x,x-1,x+4的第四比例项是3,则x=______.
- 5关于仿生学的故事不要太多,也不要太少.一条就够了.
- 6一架飞机在两城市之间飞行,顺风去要4小时,逆风返回时要5小时,飞机在无风时候速度为360千米/1时,求风速及两城市之间的
- 73600除以450的简便运算(脱式计算)
- 8若<A=1/5<B=1/6<C,则<A等于几
- 917+19+21+23+25+26+27=()*()=()
- 10听越狱学英语怎么样
- 11朱自清《春》中的“‘一年之计在于春’,刚起头儿,有的是工夫,有的是希望.”中的“工夫”是什么意思?
- 12hard,healthy,should,study,and,we,stay(.)
- 13我心中的那一轮太阳
- 14我明天要英语考试,哪位同学能向我提供一些语法知识和考试要点?
- 15贯chuan全文的chuan是哪个chuan?




