铝与浓氢氧化钠反应离子方程式
 剑浪客2022-10-04 11:39:541条回答
剑浪客2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 微笑袭人YOU 共回答了16个问题
微笑袭人YOU 共回答了16个问题 |采纳率93.8%- 正解是,3个铝离子+4个氢氧根离子+1个水生成1个偏铝酸根离子+3个水
- 1年前
相关推荐
- 浓硫酸使纸成什么样?浓氢氧化钠使纸成什么样?
 孱头左派1年前1
孱头左派1年前1 -
 钱淮 共回答了18个问题
钱淮 共回答了18个问题 |采纳率88.9%浓硫酸使纸成 黑色 ;
浓氢氧化钠使纸 变成黄色.1年前查看全部
- 为什么吸收二氧化碳用浓氢氧化钠溶液而不用饱和石灰水
 52503391年前1
52503391年前1 -
 abs321 共回答了12个问题
abs321 共回答了12个问题 |采纳率91.7%氢氧化钠溶解度高,因为ca(oh)2吸收大量co2以后生成caco3后又会反应,caco3的含量又会变少,所以只能用ca(oH)2来检验co2的存在,用naoh来吸收co2同样100克的水,氢氧化钠的溶解度可以达到53克,但是20度时氢氧化钙才0.74,吸收1摩尔的二氧化碳,需要体积相当大的氢氧化钙,所以不合理,而氢氧化钠只需1瓶就可以吸收很多1年前查看全部
- 关于溶液稀释或浓缩计算的问题如题:用溶质质量分数为40﹪的浓氢氧化钠溶液(密度为1.43克每立方厘米)配制143克溶质质
关于溶液稀释或浓缩计算的问题
如题:用溶质质量分数为40﹪的浓氢氧化钠溶液(密度为1.43克每立方厘米)配制143克溶质质量分数为10﹪的氢氧化钠溶液,需量取40﹪氢氧化钠溶液25ml与水(密度1克每立方厘米)107.25ml.
答案上和我说,水的体积为143克×(1-10﹪)-25立方厘米×1.43克每立方厘米×(1-40%)= 107.25 只爱无赖1年前1
只爱无赖1年前1 -
 LotosHH 共回答了22个问题
LotosHH 共回答了22个问题 |采纳率95.5%其实就是在算所需的水的质量.
143克×(1-10﹪)是最后溶液里水的总质量
25立方厘米×1.43克每立方厘米 是量取的氢氧化钠的质量,再乘以(1-40%)是这其中的水的质量
两个质量一减就是我们还需要加的水的质量
水毫升数与克数一样,所以答案就是107.25ml
希望我的回答能帮到你~不懂可以再问我哈~1年前查看全部
- 蛋白质在一定条件下与浓硫酸反应可转化为硫酸铵,后者在浓氢氧化钠溶液和水蒸气作用下,其中氮元素可转化为氨析出.现用30.0
蛋白质在一定条件下与浓硫酸反应可转化为硫酸铵,后者在浓氢氧化钠溶液和水蒸气作用下,其中氮元素可转化为氨析出.现用30.0mL的牛奶进行上述实验,将牛奶中的蛋白质里的氮元素完全转化为氨,再用50.0ml0.500mol•L-1硫酸溶液吸收析出的氨,剩余的酸用38.0ml1.00mol•L-1氢氧化钠溶液可恰好完全中和.问:
(1)30.0mL牛奶中含有多少g氮?
(2)如果蛋白质中含氮16%(质量分数),则牛奶中蛋白质的质量分数是多少?(已知牛奶密度是1.03g•mL-1) 徐静蕾妹1年前1
徐静蕾妹1年前1 -
 echo58 共回答了18个问题
echo58 共回答了18个问题 |采纳率94.4%解题思路:(1)根据氢氧化钠计算剩余的硫酸,进而计算与氨气反应的硫酸的物质的量,再根据关系式2N~2NH3~H2SO4计算氮元素的质量;
(2)根据m=ρV计算30mL牛奶的质量,m(牛奶)×ω(蛋白质)×ω(蛋白质中N元素)=m(牛奶中N元素),据此计算蛋白质质量分数.(1)令38mL1.00mol•L-1的 NaOH溶液中和硫酸的物质的量为n,则:
2NaOH+H2SO4=Na2SO4+2H2O
2 1
0.038L×1mol/Ln
解得:n=0.038L×1mol/L×[1/2]=0.019mol
故吸收氨气的硫酸的物质的量为:0.500mol•L-1×0.05mL-0.019mol=0.006mol
令30.0mL牛奶中氮元素的质量是m,则:
2N~2NH3~H2SO4
28g 1mol
m 0.006mol
所以m=28g×[0.006mol/1mol]=0.168g
答:30.0mL牛奶中氮元素的质量是0.168g;
(2)30mL牛奶的质量为:30mL×1.03g•mL-1=30.9g
所以30.9g×ω(蛋白质)×16.0%=0.168g
解得:ω(蛋白质)=3.4%
答:该牛奶中蛋白质的质量分数为3.4%.点评:
本题考点: 化学方程式的有关计算.
考点点评: 本题考查根据方程式的计算、质量分数的有关计算,难度不大,根据N元素守恒确定蛋白质中氮元素与硫酸反应的关系式是解题关键.1年前查看全部
- 氯化镁,氯化铝,氯化铜,氯化铁,碳酸钠五种溶液只用一种试剂把他们区别是 A氨水 B硝酸银 C浓氢氧化钠D氯化钠
 默思语1年前3
默思语1年前3 -
 atp_000 共回答了15个问题
atp_000 共回答了15个问题 |采纳率86.7%C 第一个白色沉淀,第二个先沉淀后溶解,第三个蓝色沉淀,第四个红色沉淀吧应该1年前查看全部
- 高一化学 必修二 有机物计算题在纯氧中完全燃烧0.2mol某烃,燃烧产物依次缓缓通过浓硫酸,浓氢氧化钠溶液.实验结束后,
高一化学 必修二 有机物计算题
在纯氧中完全燃烧0.2mol某烃,燃烧产物依次缓缓通过浓硫酸,浓氢氧化钠溶液.实验结束后,测得浓硫酸增重21.6g,氢氧化钠增重44g.求该烃的分子式,并写出其所有可能的结构简式. rachle20041年前4
rachle20041年前4 -
 twtguang 共回答了18个问题
twtguang 共回答了18个问题 |采纳率88.9%浓硫酸增重---吸水21.6g.则n(H2O)=21.6/18mol=1.2mol 即n(H)=2.4mol
氢氧化钠溶液增重---吸收二氧化碳44g.则n(CO2)=44/44mol=1.0mol 即 n(C)=1.0mol
则n(C):n(H)=1:2.4=5:12
则设化学式为CxHy
有:0.2x=1
y=12
得化学式C5H12 同分异构体就不用我帮你找了吧、 楼上几位找的很对.
准高二了吧 加油 (岁月催人老,我也准高三了、5555)1年前查看全部
- 浓硫酸和浓氢氧化钠同样具有强腐蚀性
浓硫酸和浓氢氧化钠同样具有强腐蚀性
那为什么电视剧和小说里人常说的泼硫酸***而不是泼氢氧化钠呢? andycloud1年前1
andycloud1年前1 -
 哈拉拉 共回答了12个问题
哈拉拉 共回答了12个问题 |采纳率83.3%对人体的腐蚀浓硫酸更明显最主要是其强的吸水性,浓硫酸好弄,很多人不知道氢氧化钠,硫酸铅蓄电池里就有知道的人多1年前查看全部
- 浓硫酸和浓氢氧化钠哪个腐蚀性强再说为什么呀?
 枫叶孤城1年前1
枫叶孤城1年前1 -
 atang00000 共回答了20个问题
atang00000 共回答了20个问题 |采纳率90%浓硫酸
由于其强氧化性产生的脱水性,有极强的腐蚀性
并不是所有强酸都有腐蚀性,如酸性最强的高氯酸并不是氧化性酸.而强氧化性导致强腐蚀性,如氢氟酸(弱酸,但能腐蚀玻璃,人接触后会渗入骨头,腐蚀骨头,产生剧痛).
刘海洋泼熊事件他也得出一结论就是浓硫酸腐蚀性强.1年前查看全部
- (2013•重庆三模)铝能与浓氢氧化钠反应,生成一种无色无味的气体.
(2013•重庆三模)铝能与浓氢氧化钠反应,生成一种无色无味的气体.
(1)请完成该反应的化学方程式:2Al+2NaOH+2H20=2NaAlO2+______;
(2)用10.0g氢氧化钠固体配制20%的氢氧化钠溶液,需加水______mL;
(3)若用上述溶液与铝反应(假设NaOH全部反应).计算反应后所得溶液中NaAlO2的质量分数.(计算结果准确至0.1%) heiseeyes1年前1
heiseeyes1年前1 -
 purewaterty 共回答了17个问题
purewaterty 共回答了17个问题 |采纳率76.5%解题思路:(1)根据化学变化前后原子的种类、数目不变,可完成反应化学方程式的填写;
(2)根据溶液质量=溶质质量÷溶质的质量分数,溶剂质量=溶液质量-溶质质量以及水的密度=1.1g/cm3,进行分析解答.
(3)根据化学反应方程式利用氢氧化钠的质量分别计算出生成的NaAlO2和H2的质量以及参加反应的铝的质量,然后利用质量分数公式计算即可.(1)根据质量守恒定律可知:元素种类不变、原子个数不变.由题干中化学方程式的左边有2个铝原子、2个钠原子、4个氧原子和6个氢原子,右边偏铝酸钠中只有2个钠原子、2个铝原子和4个氧原子,因此还缺少6个氢原子,所以横线上应填3H2↑;
故答案为:3H2↑;
(2)用10.0g氢氧化钠固体配制20%的氢氧化钠溶液的质量为:10g÷20%=50g,需加入水的质量为50g-10g=40g,因此加入水的体积是40g÷1.1g/cm3=40mL;
故答案为:40;
(3)设生成NaAlO2的质量为x,氢气的质量是y,参加反应的铝的质量为z,则
2Al+2NaOH+2H20=2NaAlO2+3H2↑
5480164 6
z 10g x y
[80/164]=[10g/x],解得x=20.5g;
[80/6]=[10g/y],解得y=0.75g;
[54/80]=[z/10g],解得z=6.75g;
反应后所得溶液的质量为6.75g+50g-0.75g=56g,反应后所得溶液中NaAlO2的质量分数为[20.5g/56g]×100%≈36.6%;
答:反应后所得溶液中NaAlO2的质量分数为36.6%.点评:
本题考点: 质量守恒定律及其应用;有关溶质质量分数的简单计算;根据化学反应方程式的计算.
考点点评: 根据化学变化前后原子的种类、数目不变可以将反应的化学方程式补充完整,掌握根据化学方程式与溶液质量分数结合的计算,难度较大.1年前查看全部
- 浓氢氧化钠溅到皮肤上,可否用水冲洗,然后涂上稀醋酸?
 ggvvgg1年前3
ggvvgg1年前3 -
 月映残阳 共回答了13个问题
月映残阳 共回答了13个问题 |采纳率100%标准方法.浓酸浓碱流到试验台上或者滴到皮肤上时先用抹布擦去,然后用水冲洗,最后涂上碳酸氢钠溶液(浓酸)或者硼酸溶液(浓碱).
用稀醋酸也可以但是大部分高中实验室都不会有醋酸.1年前查看全部
- 两道化学选择题1.常温下,下列溶液不能用铁制容器盛装的是( )A.浓硫酸 B.浓硝酸 C.浓氢氧化钠溶液 D.浓盐酸2.
两道化学选择题
1.常温下,下列溶液不能用铁制容器盛装的是( )
A.浓硫酸 B.浓硝酸 C.浓氢氧化钠溶液 D.浓盐酸
2.对氯化铁溶液和氢氧化铁胶体的说法正确的是( )
A.分散系颗粒直径都在1~100nm之间 B.能透过半透膜
C.都呈红褐色 D.用丁达尔效应可以鉴别
单项选择题 cg3031年前2
cg3031年前2 -
 静静地kk去 共回答了25个问题
静静地kk去 共回答了25个问题 |采纳率88%D D1年前查看全部
- 现实验室要用质量分数为40%浓氢氧化钠溶液(密度为1.2g/mL)来配制浓度为0.6mol/L的稀氢氧化钠100mL,问
现实验室要用质量分数为40%浓氢氧化钠溶液(密度为1.2g/mL)来配制浓度为0.6mol/L的稀氢氧化钠100mL,问需要这种浓碱的体积为______mL.
 story_er_01191年前1
story_er_01191年前1 -
 sunweihotlive 共回答了18个问题
sunweihotlive 共回答了18个问题 |采纳率88.9%解题思路:根据物质的量浓度与密度、质量分数、摩尔质量之间的关系式:C=[1000ρω/M]计算浓溶液的物质的量浓度,
再根据溶液稀释前后溶质的物质的量不变计算所需浓碱的体积.C=[1000ρω/M]=[1000×1.2×40%/40]=12(mol/L)
所以浓氢氧化钠的浓度为12mol/L;
溶液稀释前后溶质的物质的量不变,所以C1V1=C2V2,12mol/L×V1=0.6mol/L×0.1L,V1=0.005L=5.0mL
所以配置时需要浓氢氧化钠体积为5.0 mL.
故答案为:5.0.点评:
本题考点: 溶液的配制.
考点点评: 本题考查了物质的量浓度的有关计算,理清各物理量间的关系是解本题的关键.1年前查看全部
- 如图所示,在烧瓶里收集满某种气体,烧瓶用带导管(导管一端事先已经绑好一个气球)的胶塞塞紧.当拔开胶塞迅速倒入浓氢氧化钠溶
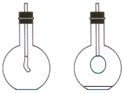 如图所示,在烧瓶里收集满某种气体,烧瓶用带导管(导管一端事先已经绑好一个气球)的胶塞塞紧.当拔开胶塞迅速倒入浓氢氧化钠溶液,立即塞紧振荡,可以看到气球逐渐膨大.瓶中气体可能是( )
如图所示,在烧瓶里收集满某种气体,烧瓶用带导管(导管一端事先已经绑好一个气球)的胶塞塞紧.当拔开胶塞迅速倒入浓氢氧化钠溶液,立即塞紧振荡,可以看到气球逐渐膨大.瓶中气体可能是( )
A.二氧化硫
B.一氧化碳
C.二氧化碳
D.氧气 VenSon程1年前1
VenSon程1年前1 -
 shiquan18 共回答了20个问题
shiquan18 共回答了20个问题 |采纳率95%解题思路:A、根据酸性气体会与碱反应进行分析;
B、根据一氧化碳不会与碱反应进行分析;
C、根据二氧化碳会与氢氧化钠反应进行分析;
D、根据氧气不会与氢氧化钠反应进行分析.倒入浓氢氧化钠溶液,立即塞紧振荡,可以看到气球逐渐膨大,说明烧瓶中的气压减小,
A、二氧化硫和氢氧化钠反应生成亚硫酸钠和水,使瓶内的气压减小,故A正确;
B、一氧化碳不会与氢氧化钠反应,瓶内气压不变,故B错误;
C、二氧化碳和氢氧化钠反应生成碳酸钠和水,瓶内气压减小,故C正确;
D、氧气不会与氢氧化钠反应,瓶内气压不变,故D错误;
故选AC.点评:
本题考点: 碱的化学性质;反应现象和本质的联系.
考点点评: 在解此类题时,首先分析气球胀大的原因,然后结合各气体的性质进行分析解答.1年前查看全部
- 用干燥的pH试纸测定浓氢氧化钠的pH
用干燥的pH试纸测定浓氢氧化钠的pH
用干燥的pH试纸测定浓氢氧化钠溶液的pH可以吗
如果不行请说明理由, yinxiaorui1年前6
yinxiaorui1年前6 -
 岩石2003 共回答了19个问题
岩石2003 共回答了19个问题 |采纳率89.5%不可以.因为用干燥的pH试纸所测得的pH值是在1-14的范围内的正整数,对于有小数的pH值是测定不出的.而且,1mol/l的氢氧化钠,ph值是在14左右,所以不可以.1年前查看全部
- 硫酸铵溶液中加入浓氢氧化钠溶液并加热的化学反应方程式
 梦小朵1年前1
梦小朵1年前1 -
 KGGB 共回答了21个问题
KGGB 共回答了21个问题 |采纳率95.2%(NH4)2SO4+2NaOH===加热===2NH3(箭头) +2H20+Na2SO41年前查看全部
- 浓氢氧化钠溶液置于空气中浓度变怎么样
 磐石石磊1年前1
磐石石磊1年前1 -
 feng2928 共回答了15个问题
feng2928 共回答了15个问题 |采纳率93.3%浓的氢氧化钠溶液至于空气中浓度会变小,因为浓度较高的氢氧化钠溶液里面氢氧化钠的含量相对较多,而氢氧化钠有两个重要的特性,第一是具有极大的吸水性;第二是易于与空气中的二氧化碳发生反应生成碳酸钙,碳酸钙溶水性极好,因此以上两点导致暴露在空气中的浓氢氧化钠溶液浓度会降低.以上是个人的一点分析,希望对你有所帮助,祝周末愉快!1年前查看全部
- 为什么浓氢氧化钠吸收氯气回倒吸,而稀氢氧化钠不会?
 e12341年前1
e12341年前1 -
 jinxiudong 共回答了19个问题
jinxiudong 共回答了19个问题 |采纳率89.5%能不能产生倒吸,主要看此物质的溶解情况,氯气在水中的溶解度不足以产生倒吸.
随着氢氧化钠浓度的逐渐增加,氯气的单位体积内溶解的量也在增加.所以当氢氧化钠的浓度达到一定数值时也会产生倒吸.1年前查看全部
- 高锰酸钾与浓氢氧化钠反应反应现象为溶液变墨绿色,有少量气泡然后我加了一点硫酸氢钾,溶液变血红色,这明显不是锰酸根离子的反
高锰酸钾与浓氢氧化钠反应
反应现象为溶液变墨绿色,有少量气泡
然后我加了一点硫酸氢钾,溶液变血红色,这明显不是锰酸根离子的反应
那绿色物质是什么
反应方程式是什么 倒戈拉hh1年前1
倒戈拉hh1年前1 -
 ni8hyvlhv44 共回答了17个问题
ni8hyvlhv44 共回答了17个问题 |采纳率100%4KMnO4+4NaOH(浓)==加热===2K2MnO4+2Na2MnO4+O2(气体)+2H2O这个实验可以观察出,高锰酸钾的紫红色渐渐变为墨绿色!1年前查看全部
- 用溶质的质量分数为40%的浓氢氧化钠溶液(密度1.43克/cm²)
用溶质的质量分数为40%的浓氢氧化钠溶液(密度1.43克/cm²)
用溶质质量分数为40%的氢氧化钠溶液配制,143克溶质的质量分数为10%的氢氧化纳溶液,需要取40%的氢氧化钠溶液多少毫升和水多少毫升混合而成 亲爱的ミ1年前1
亲爱的ミ1年前1 -
 kka9 共回答了19个问题
kka9 共回答了19个问题 |采纳率94.7%设各需要a,b毫升
那么配好之后含有NaOH 1.43a*40%g,水(1.43a*60%+b)g,质量分数为1.43a*40%/(1.43a+b)=10%
另外这种溶液要有143g,即1.43a+b=143.解方程即可
这个解下 看下对吗?1年前查看全部
- 在制乙酸乙酯实验中,在除酸操作中,若用浓氢氧化钠溶液,可能出现什么情况
 ffwkbds91年前1
ffwkbds91年前1 -
 jinqing 共回答了25个问题
jinqing 共回答了25个问题 |采纳率96%若用浓氢氧化钠溶液,由于浓氢氧化钠溶液的碱性太强,很容易使乙酸乙酯在其中发生水解反应1年前查看全部
- 苯甲醛在稀氢氧化钠溶液中为什么比浓氢氧化钠反应慢
 hansonlee8881年前1
hansonlee8881年前1 -
 买二手内库 共回答了11个问题
买二手内库 共回答了11个问题 |采纳率90.9%反应物浓度问题吧.1年前查看全部
- 为什么二氧化碳和浓氢氧化钠溶液反应能使平底烧瓶里的小气球膨胀?
 jenniferzhu91年前1
jenniferzhu91年前1 -
 小病孩儿 共回答了21个问题
小病孩儿 共回答了21个问题 |采纳率95.2%浓氢氧化钠溶液吸收二氧化碳,平底烧瓶里的压强减小,小气球的内压强相对变大 ,膨胀!1年前查看全部
- 硫和浓氢氧化钠怎么反应?(分是否加热两种情况吗?请给出方程式)
 我指着太阳说—日1年前2
我指着太阳说—日1年前2 -
 jiahua913 共回答了20个问题
jiahua913 共回答了20个问题 |采纳率100%冷:6NaOH+2S===2Na2S+Na2SO3+3H2O
热:6NaOH+2S===△2Na2S+Na2SO3+3H2O
其中当硫较多时:Na2S+S=△Na2s2
Na2S+2S=△Na2S3(更多)
Na2S+3S=△Na2S4(更更多)
Na2S+4S=△Na2S5(过量)
而:Na2SO3+S=△Na2S2O3(硫代硫酸钠)
其溶液会因为Na2Sx,x不断增大溶液由黄变成橙红.
S+6HNO3(浓)====H2SO4+6NO2↑+H2O
S+2H2SO4(浓)====3SO2↑+2H2O(须加热,若不加热则反应相当缓慢)1年前查看全部
- 浓氢氧化钠溶液有挥发性么?说是实验装置有缺点
 twwumin1年前1
twwumin1年前1 -
 blueporcelain 共回答了20个问题
blueporcelain 共回答了20个问题 |采纳率85%但是会吸水潮解,吸收二氧化碳变质.
再浓的也不会挥发.1年前查看全部
- 氯化铵和浓氢氧化钠反应不加热能不能制氨气?
 ee洋娃娃1年前1
ee洋娃娃1年前1 -
 林若子 共回答了12个问题
林若子 共回答了12个问题 |采纳率91.7%应该是可以的,不过氢氧化铵存在可逆反应过程,不加热的话差生的氨气会少很多,加热只是让可逆反应向着产生氨气的方向进行,产生更多的氨气.1年前查看全部
- 将一块带有氧化膜的铝片与过量浓氢氧化钠反应,取澄清溶液并且蒸干,得到纯净偏铝酸钠固体.
 iliris1年前1
iliris1年前1 -
 看了就烦 共回答了16个问题
看了就烦 共回答了16个问题 |采纳率87.5%还有氢氧化钠固体,因为刚开始是过量的1年前查看全部
- 氢氧化铜溶于浓氢氧化钠溶液中的化学方程式
 lzzzhen1年前2
lzzzhen1年前2 -
 1发发 共回答了10个问题
1发发 共回答了10个问题 |采纳率80%Cu(OH)2+2NaOH===Na2[Cu(OH)4](四羟基铜酸钠,蓝色)
刚查的,保证对1年前查看全部
- 质量相同的两杯浓氢氧化钠固体和浓硫酸,放在空气中,这一过程中两者的相同的变化是什么?
 dengqiong1年前2
dengqiong1年前2 -
 曹三割卵弃毛 共回答了17个问题
曹三割卵弃毛 共回答了17个问题 |采纳率88.2%楼上的:氢氧化钠溶液不会吸水,
你问的是氢氧化钠固体和浓硫酸吧?是都能吸水质量增加.1年前查看全部
- 某同学用石灰石、稀盐酸浓氢氧化钠溶液等化学试剂和试管、单孔橡皮塞、玻璃导管、可乐瓶、注射器等实验仪
某同学用石灰石、稀盐酸浓氢氧化钠溶液等化学试剂和试管、单孔橡皮塞、玻璃导管、可乐瓶、注射器等实验仪
同学用石灰石、稀盐酸浓氢氧化钠溶液等化学试剂和试管、单孔橡皮塞、玻璃导管、可乐瓶、注射器等实验仪器,做了如下试验,用可乐瓶收集满一种气体所用试剂是什么 —— ,仪器为——
像瓶内注射一种试剂,震荡后可乐瓶变瘪了,所用试剂为——
再向瓶内注射一种试剂,震荡后可乐瓶又鼓起来 所用试剂为——
写出有关反应的方程式 Oo天山莲花oO1年前1
Oo天山莲花oO1年前1 -
 caicaipei 共回答了16个问题
caicaipei 共回答了16个问题 |采纳率87.5%收集气体 所用试剂为石灰石,稀盐酸,仪器为试管,弹孔橡皮塞,玻璃导管,可乐瓶;CaCO3+2HCl==CaCl2+H2O+CO2
先注射试剂为浓NaOH CO2+2NaOH==Na2CO3+H2O
后注射为稀盐酸 Na2CO3+2HCl==2NaCl+H2O+CO21年前查看全部
- 现实验室要用质量分数为40%浓氢氧化钠溶液(密度为1.2g/mL)来配制浓度为0.6mol/L的稀氢氧化钠100mL,问
现实验室要用质量分数为40%浓氢氧化钠溶液(密度为1.2g/mL)来配制浓度为0.6mol/L的稀氢氧化钠100mL,问需要这种浓碱的体积为______mL.
 荒野伶仃1年前1
荒野伶仃1年前1 -
 天天想你sh 共回答了21个问题
天天想你sh 共回答了21个问题 |采纳率100%解题思路:根据物质的量浓度与密度、质量分数、摩尔质量之间的关系式:C=[1000ρω/M]计算浓溶液的物质的量浓度,
再根据溶液稀释前后溶质的物质的量不变计算所需浓碱的体积.C=[1000ρω/M]=[1000×1.2×40%/40]=12(mol/L)
所以浓氢氧化钠的浓度为12mol/L;
溶液稀释前后溶质的物质的量不变,所以C1V1=C2V2,12mol/L×V1=0.6mol/L×0.1L,V1=0.005L=5.0mL
所以配置时需要浓氢氧化钠体积为5.0 mL.
故答案为:5.0.点评:
本题考点: 溶液的配制.
考点点评: 本题考查了物质的量浓度的有关计算,理清各物理量间的关系是解本题的关键.1年前查看全部
- 往二氧化碳集气瓶中倒入浓氢氧化钠溶液,用小气球的胶塞塞紧,震荡后观察到小气球逐步膨大,这说明
 做梦去吧1年前1
做梦去吧1年前1 -
 lilyxpp 共回答了16个问题
lilyxpp 共回答了16个问题 |采纳率100%集气瓶壁与气球间气体减少,导致气球外压强小于内压强,所以气球膨胀.要用微元法来看,1年前查看全部
- 为什么氯气和浓氢氧化钠生成氯酸钠
为什么氯气和浓氢氧化钠生成氯酸钠
如题为什么不是生成次氯酸钠,原因是什么 孤单的夜灯1年前1
孤单的夜灯1年前1 -
 帅帅男子 共回答了23个问题
帅帅男子 共回答了23个问题 |采纳率87%应该还要加热吧?这个没具体分析过,不过既然是浓的不加热大概也会放热的,应该也可以,但最好还是要加热
氯气在碱性条件下歧化,温度高,氯气活泼性增强,被氧化成高价态的氯,同时氯酸钠也要比次氯酸钠稳定1年前查看全部
- NaOH溅到皮肤后怎么办为什么在做化学实验时,浓氢氧化钠溶液不慎溅到皮肤上,不能先用水冲洗,再涂上稀盐酸,而是要先涂稀盐
NaOH溅到皮肤后怎么办
为什么在做化学实验时,浓氢氧化钠溶液不慎溅到皮肤上,不能先用水冲洗,再涂上稀盐酸,而是要先涂稀盐酸再冲洗 薄荷-凌1年前1
薄荷-凌1年前1 -
 殇歆 共回答了16个问题
殇歆 共回答了16个问题 |采纳率75%因为氢氧化钠遇水放热 会烫伤1年前查看全部
- 甲醛与浓氢氧化钠反应是什么颜色产物
 hanzeliang1年前3
hanzeliang1年前3 -
 榆叶梅 共回答了17个问题
榆叶梅 共回答了17个问题 |采纳率88.2%2HCHO + NaOH ==== HCOONa + CH3OH.是个氧化还原反应生成甲醇无色1年前查看全部
- 铝瓶中加入二氧化碳 再加浓氢氧化钠 盖住盖子变瘪又鼓 和离子方程式
铝瓶中加入二氧化碳 再加浓氢氧化钠 盖住盖子变瘪又鼓 和离子方程式
铝瓶中加入二氧化碳 再加浓氢氧化钠 盖住盖子变瘪又鼓 和离子方程式 dreamfantasy1年前1
dreamfantasy1年前1 -
 小积木 共回答了14个问题
小积木 共回答了14个问题 |采纳率85.7%变瘪是因为氢氧化钠吸收了二氧化碳是瓶内大气压小于瓶外大气压,
所以在大气压作用下瓶子辨瘪.
而后,再强碱性环境下氢氧化钠由于铝反应,生成氢气使瓶子又变胀.
CO2+2OH-=CO3(2-)+H20
2Al+2OH-+2H2O=2AlO2-+3H21年前查看全部
- 熟石灰的悬浊液、澄清石灰水、浓氢氧化钠吸收二氧化硫
熟石灰的悬浊液、澄清石灰水、浓氢氧化钠吸收二氧化硫
从净化效果、经济等方面综合考虑,哪种试剂比较合理?为什么? yuershuang1年前1
yuershuang1年前1 -
 浪漫圣诞夜 共回答了23个问题
浪漫圣诞夜 共回答了23个问题 |采纳率95.7%熟石灰的悬浊液.
比较来源:熟石灰的悬浊液由石灰石加热后加水即可,澄清石灰水还要再过滤一下,氢氧化钠由氯碱工业制得,更麻烦,所以来源上熟石灰的悬浊液最方便.
比较经济:熟石灰的悬浊液和澄清石灰水的吸收产物都是亚硫酸钙,进一步氧化可得另一重要工业原料--石膏,但是熟石灰的悬浊液吸收更充分.氢氧化钠是工业原料,吸收产物是亚硫酸钠,没什么工业利用价值,显然最不合算.所以经济上熟石灰的悬浊液最便宜.
比较净化效果:熟石灰的悬浊液反应平衡不断右移,效果最佳,氢氧化钠其次,澄清石灰水么,那么稀的东西效果最差.所以净化效果上熟石灰的悬浊液最好.
综上:用熟石灰的悬浊液.1年前查看全部
- 高锰酸钾和浓氢氧化钠放在一起加热会有什么现象?
 地噢的1年前2
地噢的1年前2 -
 teresafang 共回答了17个问题
teresafang 共回答了17个问题 |采纳率88.2%高锰酸钾是一种中性无机盐,应该不会和氢氧化钠反应,最多加热了产生氧气.而且它的分解产物氧气和二氧化锰也是不和碱反应,所以呢加热时最多产生氧气1年前查看全部
- 检验铵根离子,必须用浓氢氧化钠溶液并加热吗?必须强调浓吗?只写用氢氧化钠溶液并加热对不对啊?
 avenewh1年前3
avenewh1年前3 -
 ldmz 共回答了15个问题
ldmz 共回答了15个问题 |采纳率73.3%加热是必要的,因为氨气在水中会有一定的溶解度.强调浓氢氧化钠就没必要了1年前查看全部
- 下列物质那种加入热浓氢氧化钠溶液碱性最弱
下列物质那种加入热浓氢氧化钠溶液碱性最弱
A P4 B F2 C BrN3 D (SeCN)2
我想知道都什么反应,按碱性强弱排列下
次磷酸不是极弱酸么?正价溴不氧化叠氮根么? 辛勤qq1年前5
辛勤qq1年前5 -
 Liyangsoft 共回答了15个问题
Liyangsoft 共回答了15个问题 |采纳率73.3%A:P4(固) + 3NaOH(浓) + 3H2O =加热= PH3↑ + 3NaH2PO2,次磷酸钠溶液为中性.
B:2F2 + 2NaOH = 2NaF + OF2↑ + H2O,氟化钠溶液为弱碱性.
C:BrN3 + 2NaOH = NaBrO + NaN3 + H2O,之后次溴酸钠歧化生成溴化钠和溴酸钠,两者溶液都为中性,而叠氮化钠溶液为碱性,所以反应后溶液呈碱性,但强弱我不知道.
D:没听说过,我猜也是(SeCN)2 + 2NaOH = NaSeCN + NaSeCNO + H2O
但我对产物NaSeCNO表示怀疑.但溶液应该呈强碱性.
总之碱性最弱的是A .1年前查看全部
- 处理铝锅锅垢应采用A.浓硝酸的人 B.浓盐酸 C.浓乙酸 D.浓氢氧化钠
 bmnct1年前1
bmnct1年前1 -
 子曰親親蘋菓 共回答了17个问题
子曰親親蘋菓 共回答了17个问题 |采纳率100%C1年前查看全部
- 将4.24g硫酸铵和硝酸铵的混合物溶于水后,加入足量浓氢氧化钠溶液,加热使反应充分
将4.24g硫酸铵和硝酸铵的混合物溶于水后,加入足量浓氢氧化钠溶液,加热使反应充分
将4.24g硫酸铵和硝酸铵的混合物溶于水后,加入足量浓氢氧化钠溶液,加热使反应充分进行,生成的氨气与30mol 1mol/L硫酸铵恰好反应生成正盐,求混合物中氮的质量分数 fancinate1年前2
fancinate1年前2 -
 yanpinga 共回答了15个问题
yanpinga 共回答了15个问题 |采纳率73.3%生成硝酸铵30ml*1mol/L=0.03mol,
铵根离子为0.06摩尔,氨气为0.06摩尔
氮为0.06摩尔,质量为0.06*14=0.84克
氮质量分数为0.84/4.24=0.1981=19.81%1年前查看全部
- 关于电解氢氧化钠溶液的问题.我们知道电解稀氢氧化钠溶液其实是一个电解水的过程,但是当水电解的差不多了得到浓氢氧化钠溶液后
关于电解氢氧化钠溶液的问题.
我们知道电解稀氢氧化钠溶液其实是一个电解水的过程,但是当水电解的差不多了得到浓氢氧化钠溶液后就开始电解氢氧化钠了.
问:开始电解氢氧化钠时,氢氧化钠溶液的浓度也该是多少? 江采苹1年前3
江采苹1年前3 -
 benbenaimengmeng 共回答了16个问题
benbenaimengmeng 共回答了16个问题 |采纳率87.5%这种情形是不会出现的.
正象rocket004 所说,水逐渐分解后,溶液中氢氧化钠浓度会越来越高,达到饱和程度后就开始有固体氢氧化钠析出,那么溶液开始保持饱和溶液的浓度,当水全部分解后,反应就结束了.因为固体氢氧化钠是不导电的.
要想电解氢氧化钠,必须要将纯氢氧化钠加热到熔融状态才可以进行.1年前查看全部
- 为什么水的离子积不适用于浓的酸碱溶液,比如浓盐酸,浓硝酸,浓氢氧化钠.
 liuyijun1年前1
liuyijun1年前1 -
 liuvvok 共回答了27个问题
liuvvok 共回答了27个问题 |采纳率88.9%因为浓的酸碱会抑制水的氢离子或者氢氧根离子的电离1年前查看全部
- 二氧化碳通入浓氢氧化钠溶液中的现象如题
 firstgu1年前1
firstgu1年前1 -
 shelly213089 共回答了23个问题
shelly213089 共回答了23个问题 |采纳率87%生成NaHCO3沉淀,一是因为NaHCO3溶解度比Na2CO3低,二是因为反应消耗水1年前查看全部
- 衣服沾有氢氧化钠衣服上如果沾有大量浓氢氧化钠溶液须将此衣服浸泡在盛水盆中这句话为什么答案给的是不对?难道要泡在酸中?岂不
衣服沾有氢氧化钠
衣服上如果沾有大量浓氢氧化钠溶液须将此衣服浸泡在盛水盆中
这句话为什么答案给的是不对?难道要泡在酸中?岂不是更没救了? happwer1年前2
happwer1年前2 -
 Rogers54 共回答了17个问题
Rogers54 共回答了17个问题 |采纳率94.1%泡在水里除不了,应泡在5~10%硫酸镁溶液或硼酸溶液中,大量醋酸也可以1年前查看全部
- Zn与氢氧化钠反应37、Zn在浓氢氧化钠溶液中与硝酸根作用主要生成 .(A) NO2 (B) NO (C) N2 (D)
Zn与氢氧化钠反应
37、Zn在浓氢氧化钠溶液中与硝酸根作用主要生成 .
(A) NO2 (B) NO (C) N2 (D) H2 (E) NH3 生在杭州1年前2
生在杭州1年前2 -
 追年 共回答了27个问题
追年 共回答了27个问题 |采纳率77.8%氢气,因为锌是中性,而在浓碱环境中硝酸根没有氧化性,这里Zn只能与氢氧根反应而生成氢气1年前查看全部
- 氯化镁与浓氢氧化钠反应为什么现黄色?
 佛也动心1年前2
佛也动心1年前2 -
 桀宿 共回答了23个问题
桀宿 共回答了23个问题 |采纳率95.7%可能是你所用的反应仪器中有较少的Fe3+离子,形成了FeCl3,一般浓度的FeCl3溶液是黄色的.1年前查看全部
- 下列离子方程式的书写正确的是( ) A.硅和浓氢氧化钠溶液反应:2Si+6OH - =2SiO 3 2- +3H 2
下列离子方程式的书写正确的是( ) A.硅和浓氢氧化钠溶液反应:2Si+6OH - =2SiO 3 2- +3H 2 ↑ B.铁和稀硫酸反应:2Fe+6H + =2Fe 3+ +3H 2 ↑ C.向氯化铝溶液中加入过量的氨水:Al 3+ +3NH 3 •H 2 O=Al(OH) 3 ↓+3NH 4 + D.铜片插入氯化铁溶液中:Cu+Fe 3+ =Cu 2+ +Fe 2+  2337445921年前1
2337445921年前1 -
 fei406 共回答了16个问题
fei406 共回答了16个问题 |采纳率87.5%A、硅和浓氢氧化钠溶液反应,正确的离子方程式为:Si+H 2 O+2OH - =SiO 3 2- +2H 2 ↑,故A错误;
B、铁和稀硫酸反应生成了亚铁离子和氢气,反应的离子方程式为:Fe+2H + =Fe 2+ +H 2 ↑,故B错误;
C、向氯化铝溶液中加入过量的氨水,反应生成了氢氧化铝沉淀,反应的离子方程式为:Al 3+ +3NH 3 •H 2 O=Al(OH) 3 ↓+3NH 4 + ,故C正确;
D、铜片插入氯化铁溶液中,离子方程式两边电荷不相等,正确的离子方程式为:Cu+2Fe 3+ =Cu 2+ +2Fe 2+ ,故D错误;
故选C.1年前查看全部
- 在一个试管中放入一些鸡毛,再倒入适量的浓氢氧化钠溶液,然后加热,现象是
在一个试管中放入一些鸡毛,再倒入适量的浓氢氧化钠溶液,然后加热,现象是
如果不慎将碱液沾到皮肤上应如何处理 vivianok1年前3
vivianok1年前3 -
 吉祥之旅 共回答了14个问题
吉祥之旅 共回答了14个问题 |采纳率92.9%蛋白质水解
干布擦去后用大量清水冲洗1年前查看全部
大家在问
- 1(阳光遗忘的角落)这句话译成英文要怎么拼,不要在线快译的,请英语水平有深度的朋友帮忙译一下,
- 2“过去式”译成英文怎么拼?
- 3求翻译三十五万英文,顺便拼出来谢谢!
- 4怎样用化学方法鉴别蒸馏水还是硝酸银溶液
- 5酒精灯的火焰分为哪三个部分,其中什么部分温度最高,熄灭酒精灯要用什么,不能用什么灭火
- 6怎样用化学方法鉴定蒸馏水和硝酸银溶液?
- 7已知冰的密度为0.9乘10的三次方kg/m一块全部化成水,质量为多少?
- 8为什么地球会围着太阳转?
- 9单细胞生物怎么分裂,有丝分裂?无丝分裂?会进行减数分裂吗?(是有性生殖还是其他什么的)
- 10单细胞生物通过细胞增殖繁殖后代,这里的细胞增殖是有死 无私 还是减数分裂?
- 11真核生物、原核生物的概念?
- 12分子式C4H8的径被高锰酸钾酸性溶液氧化得乙酸.推出结构式 和反应式
- 1390dm2等于多少cm2
- 14《繁星春水》的十道填空题,
- 15溴单质可以和哪些气体反应
