2012 上海化学高考9.工业生产水煤气的反应为:C(s)+H2O(g)→CO(g)+H2(g)-131.4 kJ,下列
 pkorsh2022-10-04 11:39:541条回答
pkorsh2022-10-04 11:39:541条回答
2012 上海化学高考
9.工业生产水煤气的反应为:C(s)+H2O(g)→CO(g)+H2(g)-131.4 kJ,下列判断正确的是
A.反应物能量总和大于生成物能量总和
B.CO(g)+H2(g)→C(s)+H2O(g)+131.4kJ
C.水煤气反应中生成1 mol H2(g)吸收131.4 KJ热量
D.水煤气反应中生成1体积CO(g)吸收131.4 KJ热量
【解析】本题考查热化学知识,意在考查考生对概念的理解.由题中信息知合成水煤气反应为吸热反应,故可判知知反应物总能量小于生成物总能量,同时知生成1molH2时需吸收131.4KJ的热量,故A项错、C项正确、D项错;B项中H2O为液态,故B项错.
C(s)+H2O(g)→CO(g)+H2(g)-131.4 kJ是吸热还是放热.按说是吸热,这样表示是Q的表示方法?
9.工业生产水煤气的反应为:C(s)+H2O(g)→CO(g)+H2(g)-131.4 kJ,下列判断正确的是
A.反应物能量总和大于生成物能量总和
B.CO(g)+H2(g)→C(s)+H2O(g)+131.4kJ
C.水煤气反应中生成1 mol H2(g)吸收131.4 KJ热量
D.水煤气反应中生成1体积CO(g)吸收131.4 KJ热量
【解析】本题考查热化学知识,意在考查考生对概念的理解.由题中信息知合成水煤气反应为吸热反应,故可判知知反应物总能量小于生成物总能量,同时知生成1molH2时需吸收131.4KJ的热量,故A项错、C项正确、D项错;B项中H2O为液态,故B项错.
C(s)+H2O(g)→CO(g)+H2(g)-131.4 kJ是吸热还是放热.按说是吸热,这样表示是Q的表示方法?

已提交,审核后显示!提交回复
共1条回复
 youkaicheng 共回答了26个问题
youkaicheng 共回答了26个问题 |采纳率92.3%- 现在很少采用这种表达式了,因为这个书写是不规范的了,+Q,如果Q是正数,则表示放热,-Q表示吸热.现在通用的正确的表达应该是:在化学方程式后加分号; 然后 ΔH= kJ/mol .+表示吸热,-表示放热
- 1年前
相关推荐
- 上海化学拓展型课程练习部分答案蓝色封面
 womenzhenbang1年前2
womenzhenbang1年前2 -
 我的他 共回答了17个问题
我的他 共回答了17个问题 |采纳率82.4%有没有关于上海高中化学拓展型课程练习部分的答案啊!就是高三的那本.问题问下邱老师,他肯定有的,在网上搜下“高中化学邱老师”,他带高三蛮多届1年前查看全部
- 上海化学高一第二学期第一章有关硫的化学方程式
 闲来扯淡1年前1
闲来扯淡1年前1 -
 g21496 共回答了13个问题
g21496 共回答了13个问题 |采纳率100%S+O2=SO2
2H2S+SO2=3S↓+2H2O
S+O2=点燃=SO2
SO3 + H2O ==== H2SO4
H2SO4 + Cu(OH)2 = CuSO4 + 2H2O
H2SO4 + BaCl2 = BaSO4 ↓+ 2HCl
Fe + CuSO4 === FeSO4 + Cu
2Al + 3H2SO4 === Al2(SO4)3 + 3H2↑1年前查看全部
- 2007年上海化学调研卷上的问题
2007年上海化学调研卷上的问题
9.以下物质的制备原理错误的是( A )
A.无水氯化镁的制备 :MgCl2•6H2O MgCl2+ 6H2O
B.钴的制备:3Co3O4+8Al 9Co+4Al2O3
C.烧碱的制备:2NaCl+2H2O 2NaOH +H2↑+ Cl2↑
D.漂粉精的制备:2Ca(OH)2+ 2Cl2→Ca(ClO)2 +CaCl2+2H2O
我选B的...为什么是A啊?
12.在含氧酸中有一种称为原某酸的,它们的性质都不稳定.例如,原硅 酸的化学式为H4SiO4;原碳酸的化学式为H4CO4,据此可推知,下列结构简式中属于原甲酸乙酯酯类的是( D )
A.C(COC2H5)4 B.CO(OC2H5)2 C.H2C(COC2H5)2 D.HC(OC2H5)3
21.以下决定物质性质的因素全面、正确的是( BD )
A.元素的化学性质:元素原子的最外层电子数 B.KNO3的溶解度:温度
C.分子间作用力:相对分子质量 D.气体摩尔体积:温度、压强
A为什么不对啊? nomanhou1年前4
nomanhou1年前4 -
 江舰 共回答了21个问题
江舰 共回答了21个问题 |采纳率85.7%9 MgCl2极易水解,而该方程产物为MgCl2和H2O ,故错误
12 H4SiO4经过脱水得到硅酸H2SiO3,所以原甲酸经过脱水得到甲酸,
猜测它的分子式为HC(OH)3,与乙酸酯化就得到HC(OC2H5)3
21 A元素的化学性质不仅与元素原子的最外层电子数有关,还与电子层数有关,而题目要求--决定物质性质的因素全面、正确的是--,该项不全面1年前查看全部
- 2011年高考上海化学实验题A试管中三层物质分别是什么
 幽谷空兰心若1年前1
幽谷空兰心若1年前1 -
 sharklion_hua 共回答了18个问题
sharklion_hua 共回答了18个问题 |采纳率94.4%第一层:冰水混合物;第二层:HBr、CH3CH2OH;第三层:产品溴乙烷.1年前查看全部
- 2014上海化学高考 六 疑惑在精制饱和食盐水中加入碳酸氢铵可制备小苏打(NaHCO3),并提取氯化铵作为肥料或进一步提
2014上海化学高考 六 疑惑
在精制饱和食盐水中加入碳酸氢铵可制备小苏打(NaHCO3),并提取氯化铵作为肥料或进一步提纯为工业氯化铵.写出上述制备小苏打的化学方程式______
NH4HCO3+NaCl→NaHCO3↓+NH4Cl
答案是箭头,不能理解 不是有机采用箭头吗?
 yansoul1年前1
yansoul1年前1 -
 savaga666 共回答了16个问题
savaga666 共回答了16个问题 |采纳率93.8%在无机化学工业上制备小苏打时,不是一步反应就能得到的;而是需要多步反应依次进行,其实中间反应被忽略了,因为那是个复杂的过程,上式是总反应方程式,所以书写化学方程式时不能用等号,而是用箭头表示反应的过程。1年前查看全部
- 上海化学2010的题目,关于KI的
上海化学2010的题目,关于KI的
向盛有KI的试管中加入少许的CCL4后滴加氯水,CCL4变紫.如果继续向试管中滴加氯水,震荡,CCL4颜色会慢慢变浅最后无色.
(1)写出CCL4有紫色变无色的化学反应方程式
(2)整个过程中的还原剂
(3)把KI换成KBr,则CCL4会变成什么颜色,滴加氯水,CCL4的颜色没有变化.那么CL2、HIO3、HBr 是氧化性由强到弱的顺序是 zhaoyanguo1年前1
zhaoyanguo1年前1 -
 ce9b 共回答了20个问题
ce9b 共回答了20个问题 |采纳率90%(1)2I-+Cl2=I2(使得CCL4变紫)+2Cl-
Cl2+H2O=HClO+HCl 5HCLO+I2+H20=5HCL+2HIO3 (CCL4颜色会慢慢变浅最后无色)
所以化学方程式为5Cl2+6H2O+I2=10HCl+2HIO3
(2)KI和I2
(3)把KI换成KBr,则CCL4会变成橙色 Cl2+2KBr=2KCl+Br2(使得CCL4变橙色)
滴加氯水,CCL4的颜色没有变化,
则氧化性由强到弱的顺序是Cl2>HBr>HIO31年前查看全部
- 1.SO2可以作为食品防腐剂吗2,NO可以用来诊断一些疾病吗个人感觉SO2 NO都有毒1.是2010上海化学高考题的一个
1.SO2可以作为食品防腐剂吗
2,NO可以用来诊断一些疾病吗
个人感觉SO2 NO都有毒
1.是2010上海化学高考题的一个选项,它是对的 共同ww过娼1年前4
共同ww过娼1年前4 -
 MS上网的青蛙 共回答了21个问题
MS上网的青蛙 共回答了21个问题 |采纳率95.2%SO2的确可以,凡是防腐剂、消毒剂都是都是有毒性的,只是食品的话有严格的量的控制,一般不会出问题,但还是少吃为好1年前查看全部
- 2010上海化学第二十二题2010上海市高考化学第22题如何解?22.由5mol Fe2O3 、4mol Fe3O4和3
2010上海化学第二十二题
2010上海市高考化学第22题如何解?22.由5mol Fe2O3 、4mol Fe3O4和3mol Fe0组成的混合物,加入纯铁1mol并在高温下和Fe2O3反应.若纯铁完全反应,则反应后混合物中Fe0与Fe2O3的物质的量之比可能是 A 4:3 B.3:2 C.3:1 D.2:l C 我弄不清楚为什么不能选D.若两反应同时存在,那么就可以选择介于3:1于3:2的2:1
我就是想知道为什么不远D!当年的化学答案解析并没有D abbc00001年前1
abbc00001年前1 -
 千山雪183 共回答了24个问题
千山雪183 共回答了24个问题 |采纳率87.5%反应方程式可以根据
这两个式子推导
Fe2O3+Fe=3FeO (1)
FeO+Fe2O3=Fe3O4 (2)
可以推出几个公式
Fe2O3+Fe=3FeO (1)+(2)X0 3:2 最小
2Fe2O3+Fe=Fe3O4+2FeO (1)+(2)X1 5:3
3Fe2O3+Fe=2Fe3O4+FeO (1)+(2)X2 2:1
4Fe2O3+Fe=3Fe3O4 (1)+(2)X3 3:1
5Fe2O3+Fe+FeO=4Fe3O4 (1)+(2)X4 2:0
6Fe2O3+Fe+2FeO=5Fe3O4 (1)+(2)X5 没有那么多Fe2O3
2:1也是可以的1年前查看全部
- 上海化学竞赛的几个问题粗食盐中常含有CaCl2,MgCl2,Na2SO4杂质,须按一定顺序加入NaOH,Na2CO3,B
上海化学竞赛的几个问题
粗食盐中常含有CaCl2,MgCl2,Na2SO4杂质,须按一定顺序加入NaOH,Na2CO3,BaCl2溶液和盐酸(均过量),通过过滤蒸发等操作,可制得精盐.所加四种溶液的顺序正确的是什么? 木林森zly1年前1
木林森zly1年前1 -
 _一个人的精彩_ 共回答了16个问题
_一个人的精彩_ 共回答了16个问题 |采纳率93.8%这是高一的必修课吧?
先加过量BaCl2溶液,得到BaCl2、CaCl2、MgCl2、NaCl,过滤掉BaSO4.
然后加过量NaOH溶液和过量Na2CO3溶液,得到NaOH、Na2CO3、NaCl,过滤掉BaCO3、CaCO3、MgCO3
最后加过量HCl溶液,得到HCl、NaCl溶液.加热,HCl挥发掉,于是得到纯净的NaCl.1年前查看全部
- 06高考上海化学题 有两道上海高考题寻求解释:
06高考上海化学题 有两道上海高考题寻求解释:
22.已知Ba(AlO2)2可溶于水.右图表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加人Ba(OH)2的物质的量x的关系.下列有关叙述正确的是
A.a—b时沉淀的物质的量:A1(OH)3比BaSO4多
B.c—d时溶液中离子的物质的量:AlO2-比Ba2+多
C.a—d时沉淀的物质的量: BaSO4可能小于A1(OH)3
D.d—e时溶液中离子的物质的量:Ba2+可能等于OH-
26.某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
③收集产品时,控制的温度应在_________左右,实验制得的环己烯精品质量低于理论产量,可能的原因是( )
a.蒸馏时从70℃开始收集产品 b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是_________.
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点 各位高手,我需要请大家帮忙解释为什么选择这个答案? 水月木木1年前1
水月木木1年前1 -
 平正天 共回答了13个问题
平正天 共回答了13个问题 |采纳率92.3%[06上海高考22题] 已知Ba(AlO2)2可溶于水.右图表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加人Ba(OH)2的物质的量x的关系.下列有关叙述正确的是
A.a—b时沉淀的物质的量:A1(OH)3比BaSO4多
B.c—d时溶液中离子的物质的量:AlO2-比Ba2+多
C.a—d时沉淀的物质的量: BaSO4可能小于A1(OH)3
D.d—e时溶液中离子的物质的量:Ba2+可能等于OH-
[解析] 设A12(SO4)3溶液中含1mol A12(SO4)3,既含2molAl3+和3molSO42-.
[o-a-b] 离子反应:2molAl3+ + 3molSO42- + 3Ba2+ + 6OH- = 3BaSO4↓+2Al(OH)3↓
沉淀为BaSO4 和Al(OH)3 其物质的量之比为 3:2 .b点达最大值,为5mol,此时加入的Ba(OH)2为3mol
(b-c-d )加入的Ba(OH)2,仅OH- 参与离子反应: 2Al(OH)3 + 2OH- = 2AlO2- + 4H2O 每消耗2mol OH—则生成2AlO2-,是留在溶液中Ba2+的两倍.沉淀混合物中Al(OH)3随加入的Ba(OH)2不断溶解.当加入的Ba(OH)2为4mol时, Al(OH)3沉淀恰好溶解完.d点沉淀达最小值组成全为BaSO4, 既y=3mol ,x=4mol. 此时,若不考虑AlO2-的水解,反应后溶液中溶质仅为1mol Ba(AlO2)2, 既 1mol Ba2+ 和 2molAlO2-
[d-e---] 再加入的Ba(OH)2 不发生离子反应,沉淀量不变,只是增加了溶液中的Ba2+和OH- 离子.显然,当再加入1mol Ba(OH)2 ,既x=5mol ,此时溶液中的n(Ba2+)=1mol+1mol=2mol, n(OH-)=2mol , 两种离子的物质的量相等.
由上分析,答案B是背定的,而D项也可入选.
可是,在所见到的标准答案中D项却落选了,为什么,可能命题者要求考生考虑水解问题,或要求考虑溶液中水会电离产生OH—吧.若这样,也太难为我们的考生了!而且,这里有必要考虑水解吗?笔者认为这里不考虑水解才是合理的.水解产生的OH—在量上能与加入Ba(OH)2电离产生的OH-相比吗?这里应该忽略水解产生的OH—才符合处理实际问题的方法.有绝对相等的吗? 不可能!要求绝对相等合理吗?不合理!这道题多选上D应该算正确的,不能扣分!
26(B)(1)①防暴沸 冷凝 ②防止环己烯挥发
(2)①上层 C ②g 冷却水与气体形成逆流 ③83 oC b (3)C1年前查看全部
- 2014上海化学高考 结构为…-CH=CH-CH=CH-CH=CH-CH=CH-…的高分子化合物用碘蒸气处理后,其导电能
2014上海化学高考
结构为…-CH=CH-CH=CH-CH=CH-CH=CH-…的高分子化合物用碘蒸气处理后,其导电能力大幅度提高.上述高分子化合物的单体是( )
A.乙炔 B.乙烯 C.丙烯 D.1,3-丁二烯
求解为什么不是D?D的话1,4打开 然后加聚不是也这个效果吗 耨子1年前1
耨子1年前1 -
 焊人兄de知音 共回答了18个问题
焊人兄de知音 共回答了18个问题 |采纳率100%1,3-丁二烯是CH2=CH-CH=CH2 形成的聚合物应该是 -CH2-CH-CH-CH2-CH2-CH-CH-CH2- 这样的聚合只是键断裂,氢不会少1年前查看全部
- 2010上海化学高考题22.由5mol 、4mol 和3mol Fe0组成的混合物,加入纯铁1mol并在高温
2010上海化学高考题
22.由5mol 、4mol 和3mol Fe0组成的混合物,加入纯铁1mol并在高温下和 反应.若纯铁完全反应,则反应后混合物中Fe0与 的物质的量之比可能是 A 4:3 R.3:2 C,3:1 D.2:l 解题思路 swhkkkfox1年前1
swhkkkfox1年前1 -
 粉红色郎 共回答了15个问题
粉红色郎 共回答了15个问题 |采纳率86.7%可用极限思维法:
(1)若Fe2O3+Fe=3FeO时, 反应混合物中含有6molFeO 4molFe2O3则:FeO和Fe2O3的物质的量之比为3:2 ;
(2)若Fe2O3+Fe+FeO=Fe3O4时,反应混合物中含有2molFeO 、4molFe2O3则:FeO和Fe2O3的物质的量之比为1:2 .
(3)当这两个反应都存在时FeO和Fe2O3的物质的量之比处于两者之间.
故答案为:BC1年前查看全部
- 2014上海化学高考选择题最后一题.想问怎么得出离子反应的先后顺序.可以就题论题,也可以把这方面的方法告诉我.好回答必采
2014上海化学高考选择题最后一题.想问怎么得出离子反应的先后顺序.可以就题论题,也可以把这方面的方法告诉我.好回答必采纳.题干:
22.已知:2Na[Al(OH)4]+CO2→2Al(OH)3↓+Na2CO3+H2O,向含2 mol NaOH、
1 mol Ba(OH)2、2 mol Na[Al(OH)4]的混合溶液中慢慢通入CO
,则通入CO的量和生成沉淀的量的关系正确的是?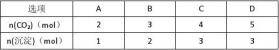
 nn青蛙1年前1
nn青蛙1年前1 -
 小理废叨 共回答了23个问题
小理废叨 共回答了23个问题 |采纳率91.3%原溶液中能和CO2反应的有:OH-、 AlO2-(题中是 Na[Al(OH)4])、以及CO2的开始产物CO32-
先和OH-反应,再和AlO2-反应,最后和CO32-反应,你从离子反应的角度来分析这个问题就好办了.
第一步又分为两个阶段(先沉淀增加后不变),第三步也分两个阶段(先沉淀不变,后沉淀减少),1年前查看全部
- 2011上海化学有机求解β—月桂烯的结构如下图所示,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多
2011上海化学有机求解
β—月桂烯的结构如下图所示,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有( )
A、2种 B、3种 C、4种 D、6种 为什么我觉得有五种,一四加成有两个,双键加成三个啊
 玫瑰清香1年前0
玫瑰清香1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 求2013上海化学的18题答案 2013上海化学的全部答案更好.
求2013上海化学的18题答案 2013上海化学的全部答案更好.
为什么找不到上海的答案?
(2013上海18)汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3==K2O+5Na2O+16N2↑.若氧化物比还原物多1.75mol,则下列判断正确的是
A.生成42.0LN2(标准状况)
B.有0.250molKNO3被氧化
C.转移电子的物质的量为1.25mol
D.被氧化的N原子的物质的量为3.75mol 无病无灾1年前1
无病无灾1年前1 -
 kane81 共回答了16个问题
kane81 共回答了16个问题 |采纳率93.8%反应中,叠氮酸的氮被复原,由于全部是变成0价,所以1mol叠氮酸根得到1mol电子,失掉3/2mol氧化产物;而1mol硝酸根将得到5mol电子,失掉1/2mol复原产物,
设有xmol硝酸钾参与反响,那么依据得失电子守恒,就有5xmol叠氮酸钠参与反响,失掉复原产物x/2mol,失掉氧化产物是15x/2mol,由于氮气即是复原产物,又是氧化产物,所以失掉氮气是8xmol
由于氧化产物比复原产物多1.75mol,所以15x/2-x/2=1.75
所以x=0.25mol
A,失掉2molN2,即44.8L,所以A错误;
B,KNO3应该被复原,所以B错误;
C,转移电子数等于0.25×5=1.25,所以C正确;
D,由于氧化产物中N2含有2个N,所以被氧化的N的物质的量是15/2×0.25×2=3.75mol,所以D正确.
【答案】:CD1年前查看全部
- 2013上海化学第20题解析是否有错?
2013上海化学第20题解析是否有错?
假如B为气体,刚好平衡时B和C的浓度相等,则K=c(B)·c(C),平衡移动后,C浓度回到原来值,B也回到原来值,K不变.这种可能不是没有啊.所以我觉得答案是BC,而不是AB. 秀场kk1年前1
秀场kk1年前1 -
 远方abcde 共回答了15个问题
远方abcde 共回答了15个问题 |采纳率86.7%你先附图!没题,我们怎么解答!1年前查看全部
- 09上海化学会考答案谢谢~~~
 shenqunxi80461年前1
shenqunxi80461年前1 -
 成都枫总 共回答了17个问题
成都枫总 共回答了17个问题 |采纳率100%2009年上海市高中结业文化考试
化学试卷
参考答案及评分标准
一、单项选择题(每小题2分,共50分)
题号x051x052x053x054x055x056x057x058x059x0510x0511x0512x0513
答案x05Dx05Cx05Cx05Dx05Dx05Ax05Cx05Ax05Ax05A x05Cx05B x05A
题号x0514x0515x0516x0517x0518x0519x0520x0521x0522x0523x0524x0525x05
答案x05Dx05Bx05Dx05Dx05Cx05Ax05Bx05Cx05Bx05Bx05C x05Bx05
二、填空题(共40分)
题号x05答案x05分值x05说明
26x05(1)x05元素符号、元素名称、质子数(或原子序数、核电核数)、相对原子质量、外层电子排布(最外层电子数)x052分x05合理即可,每答出一点得1分,多答如有错误每答错一点扣一分,扣完2分即止
x05(2)x05原子核外电子层数x051分x05
x05x05VAx051分x05
x05(3)x05①x05-3x051分x05
x05x05x05
1分x05
x05x05②x05>x051分x05
x05x05③x05HClO4x051分x05
x05x05x05HNO3→H++NO3-x051分x05
x05x05④x05强于x051分x05
x05x05x05 x052分x05化学方程式1分,电子转移1分
x05x05x05NaBrx051分x05
x05x05⑤x05bx051分x05
27x05(1)x05①x05cx051分x05
x05x05②x05酒精x051分x05
x05x05x05羟基x051分x05
x05x05x05170x051分x05
x05x05③x05CH3COOH+C2H5OH CH3COOC2H5+H2O
2分x05
x05x05x05酯化反应(或取代反应)x051分x05
x05(2)x05①x05CaC2+2H2O→2Ca(OH)2+CH≡CH↑x051分x05
x05x05x05
1分x05
x05x05x05白色污染(或环境污染等)x051分x05合理即可
x05x05x05一样多x051分x05
x05x05x05银氨溶液(或新制氢氧化铜)x051分x05任答一种即可
x05x05②x05 +Br2 +HBr
1分x05
x05x05x05液溴x051分x05
x05x05③x05甲烷(或CH4)x051分x05
28x05(1)x05NH4+x051分x05
x05x05血红x051分x05
x05x05盐酸x051分x05
x05(2)x05①x05坩埚x051分x05
x05x05x05电子天平x051分x05
x05x05②x051.600x051分x05
x05x05③x05化学式中各元素(原子团)的化合价的代数和为0(或化合物中正、负电荷总数相等;或化合物呈电中性)x051分x05
x05x05④x05是x051分x05
x05x05x05M的质量:9.640g;Fe2O3的质量:1.600g;BaSO4的质量:9.320gx051分x05若前面答“否”,此题不得分
x05(3)x05铝热x051分x05
x05x052Al+Fe2O3→2Fe+Al2O3x051分x05
三、计算题(共10分)
题号x05答案x05分值
29x05(1)x05M=2×28=56x052分
x05(2)x05
设该烃分子式为CxH2x,12x + 2x=58,x=4,则分子式为C4H8.x052分
30x05(1)x05n(Na2CO3)= =0.02(mol)
2分
x05(2)x05w(Na2SO4)%= =57.26%
2分
x05(3)x05c(HCl)= =1.34(mol/L)
2分1年前查看全部
- (2008•上海化学,3)植物及其废弃物可制成乙醇燃料,下列关于乙醇燃料的说法错误的是( ) A.它是一种再生能源 B
(2008•上海化学,3)植物及其废弃物可制成乙醇燃料,下列关于乙醇燃料的说法错误的是( ) A.它是一种再生能源 B.乙醇易燃烧,污染小 C.乙醇只能在实验室内作燃料 D.粮食作物是制乙醇的重要原料  zzz3s19841年前1
zzz3s19841年前1 -
 ymar1313 共回答了19个问题
ymar1313 共回答了19个问题 |采纳率94.7%A、因乙醇我们可以通过生物方法制取,例如发酵淀粉,纤维素等方法制取,而淀粉源源不断,只要光合作用能进行,就有取之不尽的来源,因此乙醇是可再生能源,故A正确;
B、因乙醇是一种燃料,易燃烧,产生二氧化碳和水,污染小,故B正确;
C、因乙醇除了在实验室内作燃料外,可以用于乙醇汽油,故C错误;
D、因乙醇可由含淀粉、纤维素丰富的粮食作物水解制取,故D正确;
故选:C.1年前查看全部
大家在问
- 1《墨子·兼爱中》里的:“越王亲自鼓其士而进之”一句中“而”字怎么翻译?是表递进还是承接?如果从“...
- 2将3.9g镁铝合金投入到500ml 2mol.-1 的盐酸中,
- 3人多力量大用英语怎么说如题
- 4必修一 牛顿运动定律质量为m=2kg的物体在水平桌面上运动时,受到与运动方向相同的水平拉力F的作用,物体与桌面间的动摩擦
- 5已知图1,折叠矩形ABCD,先沿对角线BD折叠,压出折痕,在折叠,使AD落在折痕BD上,得另一折痕DG,若AB=2,BC
- 6一杯果汁,喝去三分之一后用水加满,又喝去四分之一,再用水加满,全部喝完,喝的水和果汁的比是(:)【要解题过程】
- 7Mr wang offered_____ me some books
- 8小红和小明设计了如图甲所示的实验研究电和磁现象,当他们闭合开关S后,发现小磁针发生了偏转,这说明____________
- 9一群群的鸟在树上()地唱歌 括号里填自字组的词
- 10请帮忙找苏教版八年级下学期数学计算题100道以上!谢谢!请快速!在线等!
- 11英语翻译1.____is announced in the papers,our country has launche
- 12求外研版八年级上英语书上的过去分词表,(irregular verbs )
- 13建图纸KL1-1(1) 240X550,Φ8@100/150(2),2Φ下一横18;2Φ下一横16/3Φ下一横18,G4
- 141,A___w___and p__are fruits.2,C___,o___and p___are all veget
- 15(1)never,for,late,work,we,been,have (2)he,died,since,years,i
