硬水软化的方法:最常用的方法(),软化程度最高的方法()
 毛西毛2022-10-04 11:39:541条回答
毛西毛2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 wrhyl 共回答了14个问题
wrhyl 共回答了14个问题 |采纳率92.9%- 硬水软化的方法:最常用的方法(煮沸),软化程度最高的方法(蒸馏)
- 1年前
相关推荐
- 我们物理练习册的一道题物体溶解于水时都会放出热量 利用活性炭吸附水中的杂志可以使硬水软化 这两句话都是错的,为什么?
 蓝若求球1年前1
蓝若求球1年前1 -
 我是尼姑带两秃子 共回答了12个问题
我是尼姑带两秃子 共回答了12个问题 |采纳率83.3%Ca(OH)2
h2so4
溶于水等都会放热
活性炭只能吸附杂质,
硬水是指含有较多可以溶解的钙盐、镁盐的水,其中含碳酸氢钙,碳酸氢镁较多的水叫暂时硬水,这种水被煮沸后,可溶性钙、镁盐就变成碳酸盐(石头的主要成分之一),大部分析出,井水就是暂时硬水;而含硫酸钙(石膏的主要成分)、硫酸镁较多的水叫永久硬水,这种水煮沸时,所含盐不能析出,海水就是永久硬水.
和硬水不同,软水是只含少量或不含可溶性钙盐、镁盐的水,煮沸时不发生明显的变化.
所以活性炭无法软化硬水1年前查看全部
- 水是生命之源.将浑浊的水变澄清的简单方法是______.区分硬水和软水的试剂是______,生活中硬水软化的方法是___
水是生命之源.将浑浊的水变澄清的简单方法是______.区分硬水和软水的试剂是______,生活中硬水软化的方法是______.常见的水污染的原因有______(写一条即可).
 wsss22222221年前1
wsss22222221年前1 -
 lengxiufeng 共回答了22个问题
lengxiufeng 共回答了22个问题 |采纳率72.7%解题思路:过滤能除去不溶于液体的固体.根据硬水软化的方法和区分方法解答.常见的水污染的原因有工业废水未处理就排放、生活污水未处理就排放.浑浊的水中含有不溶于水的固体杂质,可用过滤法除去;硬水中含有较多不溶性钙镁离子化合物,煮沸时分解产生水垢多,硬水中加入肥皂水,产生的泡沫少,浮渣多;常见的水污染的原因有工业废水未处理就排放、生活污水未处理就排放.
故答案为:过滤;肥皂水;煮沸;工业废水未处理就排放.点评:
本题考点: 水的净化;硬水与软水;水资源的污染与防治.
考点点评: 本题以净化水为中心,同时考查了过滤操作的相关知识、硬水和软水的区别、转化方法,结合所学习知识,仔细分析后再作回答.1年前查看全部
- 下列叙述中,不正确着是( )A.用食盐溶液可以将硬水软化B.釜底抽薪蕴含的灭火原理是撤离可燃物C.工业废水处理后可以循
下列叙述中,不正确着是( )
A.用食盐溶液可以将硬水软化
B.釜底抽薪蕴含的灭火原理是撤离可燃物
C.工业废水处理后可以循环使用
D.水是能溶解多种物质的常用溶剂 昨天夜又春雨1年前1
昨天夜又春雨1年前1 -
 lly0025 共回答了28个问题
lly0025 共回答了28个问题 |采纳率78.6%解题思路:A、根据食盐的性质和硬水的定义判断.
B、根据灭火的原理判断.
C、根据水污染的防治和用途判断.
D、根据水的用途判断.A、食盐的主要成分是氯化钠,氯化钠与可溶的钙、镁化合物不反应,也不影响其溶解性,不能将硬水软化,所以错误.
B、薪是可燃物,釜底抽薪蕴含的灭火原理是清除可燃物,所以正确.
C、工业废水处理后,成为中水,不能饮用,但工业上可以循环使用,所以正确.
D、水是最常用溶剂,能溶解多种物质,所以正确.
故选A.点评:
本题考点: 硬水与软水;水资源的污染与防治;常见的溶剂;灭火的原理和方法.
考点点评: 水是人类宝贵的自然资源,与水相关的化学知识是化学考查热点之一,如水的组成及水电解实验、性质、用途、硬水和软水、节约水资源、水污染及防治等内容,在中考中出现机率很高.1年前查看全部
- 硬水软化时为什么要用饱和的碳酸钠溶液
硬水软化时为什么要用饱和的碳酸钠溶液
有一杯主要含有氯化镁和氯化钙的硬水,欲将其软化.
1、取少量水样于试管中,向其中滴加氢氧化钙溶液,直到不再产生沉淀
2、继续向上述试管中滴加饱和的碳酸钠溶液,直到不再产生沉淀
请问为什么要滴加饱和的碳酸钠溶液,不是饱和的会怎么样 化作雨的泪1年前3
化作雨的泪1年前3 -
 asdhfwakejh 共回答了19个问题
asdhfwakejh 共回答了19个问题 |采纳率78.9%饱和的浓度最高,溶液里的水最少,不饱和也没关系;;;1年前查看全部
- 下列叙述正确的是( ) A.炼铁的原理是利用一氧化碳将氧化铁中的铁还原出来 B.用消毒的方法可将硬水软化 C.加入适量
下列叙述正确的是( )
A.炼铁的原理是利用一氧化碳将氧化铁中的铁还原出来
B.用消毒的方法可将硬水软化
C.加入适量H 2 SO 4 溶液除去NaCl溶液中少量的Na 2 CO 3
D.过滤时滤纸的边缘应高于漏斗口 79LA1年前1
79LA1年前1 -
 zcsea 共回答了20个问题
zcsea 共回答了20个问题 |采纳率100%A、炼铁的原理是利用还原剂把氧化铁中的铁还原出来,一般是利用一氧化碳进行,故此选项正确.
B、消毒只是对水进行杀菌的过程,与硬水软化的过程无直接关系,故此选项错误.
C、加入适量H 2 SO 4 溶液除去NaCl溶液中少量的Na 2 CO 3 ,会因硫酸与碳酸钠反应而消耗掉碳酸钠,但也会引入了硫酸钠的杂质,故此选项错误.
D、过滤时滤纸的边缘应低于漏斗口,故此选项错误.
故选A1年前查看全部
- 下列有关水的认识中不正确的是( ) A.自然界中的水都是混合物 B.过滤可使硬水软化 C.水是一种重要的溶剂 D.电解
下列有关水的认识中不正确的是( )
A.自然界中的水都是混合物 B.过滤可使硬水软化 C.水是一种重要的溶剂 D.电解水时,负极上产生的气体是氢气  百事K乐1年前1
百事K乐1年前1 -
 sunleilei1986 共回答了22个问题
sunleilei1986 共回答了22个问题 |采纳率86.4%B
1年前查看全部
- 这样节不节约(化学)X做硬水软化实验时,先点燃酒精灯,再倒取硬水于试管内进行加热
 没事我就偷乐1年前2
没事我就偷乐1年前2 -
 G14之利物浦 共回答了15个问题
G14之利物浦 共回答了15个问题 |采纳率73.3%先倒取硬水于试管内 后点燃酒精灯1年前查看全部
- 在工业上如何把硬水软化
 来看热闹地1年前1
来看热闹地1年前1 -
 mp4368 共回答了11个问题
mp4368 共回答了11个问题 |采纳率81.8%石灰纯碱法
在锅炉里加入石灰(CaO)和纯碱(Na2CO3)
发生反应 CaO+H2O===Ca(OH)2
Ca(OH)2+ Mg2+=== Mg(OH)2↓+Ca2+
Na2CO3+ Ca2+=== CaCO3↓+ 2Na+1年前查看全部
- (2013•泰安二模)处理主要包括水的净化、污水处理、硬水软化和海水淡化等.
 (2013•泰安二模)处理主要包括水的净化、污水处理、硬水软化和海水淡化等.
(2013•泰安二模)处理主要包括水的净化、污水处理、硬水软化和海水淡化等.
(1)水处理技术的核心是减少或除去水中的各种杂质离子.目前,______和______是主要的去离子方法.
(2)ClO2是一种性能优良的消毒剂,可将废水中少量的S2-,NO2-和CN-等有毒有害的还原性离子氧化除去.请写出ClO2将废水中剧毒的CN-氧化成无毒气体的离子方程式:______
(3)地下水往往含有钙、镁的碳酸盐,自来水厂需要对地下水进行______处理.把进行过离子交換的CaR2 (或MgR2 )型树脂置于______中浸泡一段时间后便可再生.
(4)海水的淡化是除去海水中所含的盐分,如图是海水利用电渗析法获得淡水的原理图,已知海水中含有Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.请回答:
①阳离子交换膜是指______(填“A”或“B”)o
②写出通电后阳极区的电极反应式______. oo狼1年前1
oo狼1年前1 -
 monicafu 共回答了13个问题
monicafu 共回答了13个问题 |采纳率76.9%解题思路:(1)水处理技术的核心是减少或除去水中的各种杂质离子,主要的去离子方法是离子交换法和膜分离法;
(2)二氧化氯中氯为+4价,CN-中氮为-3价,碳为+2价;
(3)根据地下水硬度较大,需要软化;用磺化煤(NaR)作离子交换剂:2NaR+Ca2+=CaR2+2Na+,2NaR+Mg2+=MgR2+2Na+,用5%-8%的食盐水浸泡可使失去软化能力的磺化煤再生:CaR2+2Na+=2NaR+Ca2+,MgR2+2Na+=2NaR+Mg2+;
(4)①阴离子交换膜只允许阴离子自由通过,阳离子交换膜只允许阳离子自由通过;
②根据阳极是氯离子放电.(1)水处理技术的核心是减少或除去水中的各种杂质离子,主要的去离子方法是离子交换法和膜分离法,故答案为:离子交换法;膜分离法;
(2)ClO2氧化性较强,是常用的氧化剂,其中+4价氯元素通常被还原为-1价,在该反应中而CN-中+2价碳元素通常被氧化成+4价,而氮元素则容易被还原成0价形成氮气:
2CN-+2ClO2=2CO2↑+N2↑+2Cl-;故答案为:2CN-+2ClO2=2CO2↑+N2↑+2Cl-;
(3)地下水硬度较大,需要软化,所以自来水厂需要对地下水进行软化;
用磺化煤(NaR)作离子交换剂:2NaR+Ca2+=CaR2+2Na+,2NaR+Mg2+=MgR2+2Na+,用5%-8%的食盐水浸泡可使失去软化能力的磺化煤再生:CaR2+2Na+=2NaR+Ca2+,MgR2+2Na+=2NaR+Mg2+;
故答案为:软化;5%-8%的食盐水;
(4)①阴离子交换膜只允许阴离子自由通过,阳离子交换膜只允许阳离子自由通过,隔膜B和阴极相连,阴极是阳离子放电,所以隔膜B是阳离子交换膜,故答案为:B;
②根据阳极是氯离子放电:2Cl--2e-=Cl2↑,故答案为:2Cl--2e-=Cl2↑.点评:
本题考点: "三废"处理与环境保护.
考点点评: 本题是一道化学和生活相结合的题目,注重知识的迁移应用,难度不大,能较好的考查学生分析和解决问题的能力.1年前查看全部
- 硬水软化?我家新打了一口井 井水硬度巨高 用洗衣粉洗衣时基本上不会产生泡沫 每烧一次水,炊具都会结上严重的白色水垢 开水
硬水软化?
我家新打了一口井 井水硬度巨高 用洗衣粉洗衣时基本上不会产生泡沫 每烧一次水,炊具都会结上严重的白色水垢 开水倒在杯中,下半杯有悬浮物,非常浑浊
(1)有没有办法对井做一些处理?村里的老人说可以扔几块石头下去,有没有道理?
(2)能不能在抽入水池的水中下一些药?比如石灰[对付暂时硬水],苏打[对付非碳酸盐硬水],明磺[沉淀作用].如何掌握用药量?长期喝下过药的水有没有坏处? 劳运明1年前1
劳运明1年前1 -
 baoweisa 共回答了19个问题
baoweisa 共回答了19个问题 |采纳率94.7%将水抽入水池 让其自然沉淀 然后食用1年前查看全部
- 在水的净化过程中,可以将硬水软化的操作是( ) A.蒸馏 B.过滤 C.沉淀 D.吸附
 hanxiao5551年前1
hanxiao5551年前1 -
 陨石的守望 共回答了21个问题
陨石的守望 共回答了21个问题 |采纳率100%A、蒸馏能除去水中可溶性钙镁离子,实现硬水软化,故A正确;
B、过滤不能减少可溶性钙镁离子的含量,故B错误;
C、沉淀不能减少可溶性钙镁离子的含量,故C错误;
D、吸附不能减少可溶性钙镁离子的含量,故D错误;
故答案为:A1年前查看全部
- 下列说法正确的是______A.蒸馏与过滤都可以将硬水软化 &
下列说法正确的是______
A.蒸馏与过滤都可以将硬水软化B.活性炭可以吸附一些溶解的杂质,除去臭味
C.软水一定不含有可溶性钙镁化合物D.长期使用硬水对生产和生活有益. yekong2001年前1
yekong2001年前1 -
 wangilygily 共回答了15个问题
wangilygily 共回答了15个问题 |采纳率80%A、过滤除去的是水中的不溶性的固体杂质,不能减少钙镁离子的化合物,不能使硬水软化;蒸馏得到的蒸馏水是净化程度较高的水.不含钙镁离子的化合物,能将硬水软化,故A说法错误;
B、活性炭具有疏松多孔的结构,所以可以吸附一些溶解的杂质,并能出去臭味,故B说法正确;
C、软水是指含有较少或不含可溶性钙镁化合物的水,而不是一定不含可溶性钙镁化合物,故C说法错误;
D、硬水中含有较多的钙镁化合物,长期饮用对身体有害,故D说法错误.
故选B.1年前查看全部
- 常用的净化水的方法有______、______、______、______等,实验室里常用______方法使硬水软化,在
常用的净化水的方法有______、______、______、______等,实验室里常用______方法使硬水软化,在操作过程中常在水中加入几粒沸石(碎瓷片),其作用是______.  竹 萧1年前1
竹 萧1年前1 -
 shijl 共回答了22个问题
shijl 共回答了22个问题 |采纳率72.7%常用的净化水的方法有沉淀、过滤、吸附、蒸馏等.蒸馏之后得到的水是纯水,净化程度最高,实验室里常用蒸馏方法使硬水软化,在操作过程中常在水中加入几粒沸石(碎瓷片),其作用是防止爆沸.
故答为:沉淀、过滤、吸附、蒸馏. 蒸馏;防止爆沸.1年前查看全部
- (2008•苏州)纯碱在日常生活和化学工业中用途很广,如用于硬水软化、洗涤剂生产、食品加工、石油精炼、粗盐精制、玻璃制造
(2008•苏州)纯碱在日常生活和化学工业中用途很广,如用于硬水软化、洗涤剂生产、食品加工、石油精炼、粗盐精制、玻璃制造等领域.工业上以食盐、氨气(主要由合成氨厂提供)和二氧化碳为主要原料生产纯碱.其流程如下:
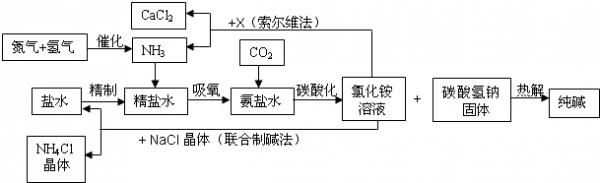
已知有关物质重要反应的化学方程式如下:
①NaCl+NH3+H2O+CO2
NaHCO3↓+NH4Cl△ .
②2NaHCO3
Na2CO3+H2O+CO2↑△ .
③2NH4Cl+X
2NH3↑+CaCl2+2H2O△ .
④NH4Cl═NH3↑+HCl↑
根据以上信息回答下列问题.
(1)盐水精制的过程是除去溶液中各种杂质的过程.为将盐水中含有的Ca2+、Mg2+等沉积,可以向其一和加入过量纯碱.此时将混合液中不溶物除去的方法是______;溶液中多余的纯碱可以加______试剂来除去.
(2)氨碱工业最关键的一步是:在加压的条件下不断向饱和的氨盐水中通人二氧化碳气体,溶液中会有碳酸氢钠晶体析出.试分析该流程需要加压条件的原因是:______.
(3)在氨碱工业的历史上.如何处理流程中剩余的氯化铵溶液,出现了两种工艺:一是“索尔维法”.即在氯化铵溶液中加入物质X______(填化学式),产生了可循环使用的氨气,和大量固体废弃物氯化钙;二是我国化学家侯德榜发明的“联合制碱法”,即在氯化铵溶液中加入适量氯化钠晶体.降低了氯化氨的______,使氯化铵晶体单独析出得到另一种产品--氮肥.氯化钠溶液则可以循环利用.
(4)在氨碱工业处理剩余的氯化铵溶液时.为何不直接蒸发结晶析出氯化铵固体?答:______. 神仙popo1年前1
神仙popo1年前1 -
 兰-心-慧 共回答了17个问题
兰-心-慧 共回答了17个问题 |采纳率82.4%解题思路:(1)根据过滤的原理回答前一空;根据碳酸钠的化学性质和除杂的原理回答后一空.
(2)根据气体的溶解度随压强的增大而增大回答.
(3)根据铵盐与碱性物质反应生成氨气的性质回答前一空;根据氯化钠溶液和氯化铵溶液中都含氯离子,氯化钠是制纯碱的原料回答.
(4)根据氯化铵的化学性质回答.(1)过滤是把不溶于液体的固体与液体分开的操作,所以除去液体混合物中的不溶性杂质用过滤的方法;碳酸钠能和盐酸反应生成氯化钠、水、二氧化碳,用盐酸除去多余的碳酸钠不会产生新杂质.
(2)二氧化碳能溶于水,但溶解性较差,气体的溶解度随压强的增大而增大,为了促进更多二氧化碳溶解,使反应更充分,所以需加压条件.
(3)铵盐与碱性物质反应生成氨气,在氯化铵溶液中加入物质X产生了可循环使用的氨气,定是加入的碱性物质,最廉价的碱是熟石灰,所以加入的物质是熟石灰;氯化钠溶液和氯化铵溶液中都含氯离子,在氯化铵溶液中加入适量氯化钠晶体可降低氯化铵的溶解度,使氯化铵晶体单独析出.
(4)不直接蒸发结晶析出氯化铵固体,是因氯化铵受热易分解.
故答案为:(1)过滤;盐酸;
(2)促进更多二氧化碳溶解,使反应更充分;
(3)Ca(OH)2;溶解度;
(4)因氯化铵受热易分解.点评:
本题考点: 过滤的原理、方法及其应用;物质除杂或净化的探究;纯碱的制取.
考点点评: 化学来源于生产、生活,又服务于生产、生活,氨碱工业是初中化学重要的应用之一,是考查重点,常涉及化学方程式的书写,二氧化碳和氨气通入的顺序及原因,反应时析出碳酸氢钠的原因与物质溶解度的关系.1年前查看全部
- 下列叙述正确的是( )A. 炼铁的原理是利用一氧化碳将氧化铁中的铁还原出来B. 用消毒的方法可将硬水软化C. 加入适量
下列叙述正确的是( )
A. 炼铁的原理是利用一氧化碳将氧化铁中的铁还原出来
B. 用消毒的方法可将硬水软化
C. 加入适量H2SO4溶液除去NaCl溶液中少量的Na2CO3
D. 过滤时滤纸的边缘应高于漏斗口 yy_mikelee1年前1
yy_mikelee1年前1 -
 自由的风0 共回答了22个问题
自由的风0 共回答了22个问题 |采纳率86.4%解题思路:A、炼铁的原理是利用还原剂把氧化铁中的铁还原出来.
B、消毒只是对水进行杀菌的过程,与硬水软化无直接关系.
C、加入适量H2SO4溶液除去NaCl溶液中少量的Na2CO3,会消耗掉杂质,但也引入了硫酸钠的杂质.
D、过滤时滤纸的边缘应低于漏斗口.A、炼铁的原理是利用还原剂把氧化铁中的铁还原出来,一般是利用一氧化碳进行,故此选项正确.
B、消毒只是对水进行杀菌的过程,与硬水软化的过程无直接关系,故此选项错误.
C、加入适量H2SO4溶液除去NaCl溶液中少量的Na2CO3,会因硫酸与碳酸钠反应而消耗掉碳酸钠,但也会引入了硫酸钠的杂质,故此选项错误.
D、过滤时滤纸的边缘应低于漏斗口,故此选项错误.
故选A点评:
本题考点: 铁的冶炼;物质除杂或净化的探究;过滤的原理、方法及其应用;硬水与软水.
考点点评: 此题是一道多点知识考查题,解题的关键是对这些相关知识的掌握,特别是除杂这道题目一定要坚持不能引入杂质的原则完成相关的分析.1年前查看全部
- 硬水软化是不是就是把钙离子转化为沉淀就可以了?
 太阳熊sunbear1年前1
太阳熊sunbear1年前1 -
 没有鱼的尾巴 共回答了30个问题
没有鱼的尾巴 共回答了30个问题 |采纳率96.7%如果水的硬度是由碳酸氢钙或碳酸氢镁引起的,这种硬度叫作暂时硬度.这种水经过煮沸以后,水里所含的碳酸氢钙就分解成不溶于水的碳酸钙,水里所含的碳酸氢镁就生成难溶于水的碳酸镁沉淀.这些沉淀物析出,水的硬度就可以降低,从而使硬度较高的水得到软化.如果水的硬度是由钙和镁的硫酸盐或氯化物引起的,这种硬度就叫作永久硬度.永久硬度不能用加热的方法软化.天然水大多同时具有暂时硬度和永久硬度,因此,一般所说水的硬度是指上述两种硬度的总和.矿泉水是富含对人体有益的矿物质的饮用水,而蒸馏水则是用蒸发冷凝的方法制成的纯水.1年前查看全部
- 利用活性炭吸附水中的杂质可以使硬水软化吗?
 早睡早起身体好_1年前1
早睡早起身体好_1年前1 -
 wxfwll 共回答了15个问题
wxfwll 共回答了15个问题 |采纳率100%这个是不可以的.1年前查看全部
- (2014•焦作一模)硬水的危害较多,生活中将硬水软化的方法是______;检验自来水是硬水的方法是______.
 一湖月光1年前1
一湖月光1年前1 -
 源若 共回答了18个问题
源若 共回答了18个问题 |采纳率88.9%解题思路:降低水的硬度的方法是:加热煮沸、蒸馏,生活中常用加热煮沸的方法来降低水的硬度;
区分硬水和软水的方法是:用肥皂水.加入肥皂水,泡沫多的是软水,泡沫少的是硬水.降低水的硬度的方法是:加热煮沸、蒸馏,生活中常用加热煮沸的方法来降低水的硬度;
区分硬水和软水的方法是:用肥皂水.加入肥皂水,泡沫多的是软水,泡沫少的是硬水.
故答案为:煮沸;加肥皂水,泡沫少则是硬水.点评:
本题考点: 硬水与软水.
考点点评: 本题结合了新课标中的一个新的考点硬水与软水的区分,一定要加强记忆,综合应用.1年前查看全部
- 煮沸为什么可以使硬水软化
 雪人晒太阳1年前2
雪人晒太阳1年前2 -
 libabuluo 共回答了12个问题
libabuluo 共回答了12个问题 |采纳率83.3%若水的硬度是暂时硬度,这种水经过煮沸以后,水里所含的碳酸氢钙或碳酸氢镁就会分解成不溶于水的碳酸钙和难溶于水的氢氧化镁沉淀.这些沉淀物析出,水的硬度就可以降低,从而使硬度较高的水得到软化.1年前查看全部
- 下列说法正确的是______A.蒸馏与过滤都可以将硬水软化 &
下列说法正确的是______
A.蒸馏与过滤都可以将硬水软化B.活性炭可以吸附一些溶解的杂质,除去臭味
C.软水一定不含有可溶性钙镁化合物D.长期使用硬水对生产和生活有益. galax20001年前1
galax20001年前1 -
 zjz8988190 共回答了26个问题
zjz8988190 共回答了26个问题 |采纳率92.3%解题思路:A、根据过滤、蒸馏的原理分析;B、根据活性炭的结构来解答该题;C、根据软水的定义来完成解答;D、根据硬水对生产和生活的影响来完成解答.A、过滤除去的是水中的不溶性的固体杂质,不能减少钙镁离子的化合物,不能使硬水软化;蒸馏得到的蒸馏水是净化程度较高的水.不含钙镁离子的化合物,能将硬水软化,故A说法错误;
B、活性炭具有疏松多孔的结构,所以可以吸附一些溶解的杂质,并能出去臭味,故B说法正确;
C、软水是指含有较少或不含可溶性钙镁化合物的水,而不是一定不含可溶性钙镁化合物,故C说法错误;
D、硬水中含有较多的钙镁化合物,长期饮用对身体有害,故D说法错误.
故选B.点评:
本题考点: 硬水与软水;碳单质的物理性质及用途.
考点点评: 解答本题要熟悉硬水和软水的鉴别方法和转化方法,知道蒸馏得到的水是净化程度最高的水.1年前查看全部
- 一道化学题纯碱在日常生活和化学工业中用途很广,如用于硬水软化,洗涤剂生产,食品加工,石油精炼,粗盐精制,玻璃制造等领域.
一道化学题
纯碱在日常生活和化学工业中用途很广,如用于硬水软化,洗涤剂生产,食品加工,石油精炼,粗盐精制,玻璃制造等领域.工业上以食盐,氨气(主要由合成氨厂提供)和二氧化碳为主要原料生产纯碱.其流程如下:
已知有关物质重要反应的化学方程式如下:
①NaCl+NH3+H2O+CO2====NaHCO3↓+NH4Cl
②2NaHCO3==== Na2CO3+ H2O+CO2↑
③2NH4Cl +X====2NH3↑+CaCl2+2H2O
④NH4Cl ==== NH3↑+HCl↑
根据以上信息回答下列问题.
(1)盐水精制的过程是除去溶液中各种杂质的过程.为将盐水中含有的Ca2+,Mg2+等沉积,可以向其一和加入过量纯碱.此时将混合液中不溶物除去的方法是 ________;溶液中多余的纯碱可以加 _______试剂来除去.
(2)氨碱工业最关键的一步是:在加压的条件下不断向饱和的氨盐水中通人二氧化碳气体,溶液中会有碳酸氢钠晶体析出.试分析该流程需要加压条件的原因是:__________ .
(3)在氨碱工业的历史上.如何处理流程中剩余的氯化铵溶液,出现了两种工艺:一是"索尔维法".即在氯化镀溶液中加入物质X _______(填化学式),产生了可循环使用的氢气和大量固体废弃物氯化钙;二是我国化学家侯德榜发明的"联合制碱法",即在氯化铵溶液中加入适量氯化钠晶体.降低了氯化氨的______,使氯化铵晶体单独析出得到另一种产品——氮肥.氯化钠溶液则可以循环利用.
 fuming7612111年前6
fuming7612111年前6 -
 4567535 共回答了19个问题
4567535 共回答了19个问题 |采纳率84.2%1)盐水精制的过程是除去溶液中各种杂质的过程.为将盐水中含有的Ca2+,Mg2+等沉积,可以向其一和加入过量纯碱.此时将混合液中不溶物除去的方法是 (过滤);溶液中多余的纯碱可以加 (盐酸)试剂来除去.
(2)氨碱工业最关键的一步是:在加压的条件下不断向饱和的氨盐水中通人二氧化碳气体,溶液中会有碳酸氢钠晶体析出.试分析该流程需要加压条件的原因是:(增大CO2在水中的溶解度).
(3...1年前查看全部
- 某地下水是硬水,含有Ca2+,和大量Mg2+,用Ca{OH}2,和Na2CO3,使硬水软化,先加哪一个
 小天出来玩吧1年前6
小天出来玩吧1年前6 -
 urwell 共回答了20个问题
urwell 共回答了20个问题 |采纳率95%Ca{OH}2然后Na2CO3
因为你要加过量Ca{OH}2会有好多Ca2+,然后统一用Na2CO3来除
如果你先加Na2CO3,那你的目的是除去水里的Ca2+,然后你之后又加Ca(OH)2,肯定是过量的,就不能保证Ca2+的完全沉淀了.1年前查看全部
- 用肥皂水可以检验硬水和软水,生活中常用的硬水软化的方法是______,爱护水资源的途径是______和防治水体污染,其中
用肥皂水可以检验硬水和软水,生活中常用的硬水软化的方法是______,爱护水资源的途径是______和防治水体污染,其中防治水体污染的方法有:①工业污水达标处理后排放;②______③生活污水集中处理后再排放等.
 zw1161年前1
zw1161年前1 -
 hornetbee 共回答了15个问题
hornetbee 共回答了15个问题 |采纳率93.3%解题思路:根据硬水软化的方法、爱护水资源的途径、防治水体污染的方法分析回答.加热煮沸能减少水中钙、镁离子的化合物的含量.所以,生活中常用的硬水软化的方法是煮沸;爱护水资源的途径是节约用水和防治水体污染.其中防治水体污染的方法有:①工业污水达标处理后排放;②农业上合理使用化肥与农药;③生活污水集中处理后再排放等.
故答为:煮沸;节约用水;农业上合理使用化肥与农药.点评:
本题考点: 硬水与软水;水资源的污染与防治;保护水资源和节约用水.
考点点评: 水资源的利用和保护是现代社会面临的重要问题,同时也就成为中考的重要内容之一,应加强学习.1年前查看全部
- 下列说法中正确的是( ) A.青少年长期饮用纯净水有益健康 B.家里烧开水的目的之一是使硬水软化 C.人体内含量最多的
下列说法中正确的是( ) A.青少年长期饮用纯净水有益健康 B.家里烧开水的目的之一是使硬水软化 C.人体内含量最多的物质是蛋白质 D.无色透明的液体一定是纯净水  xianliu**1年前1
xianliu**1年前1 -
 思路华语 共回答了16个问题
思路华语 共回答了16个问题 |采纳率81.3%A、因为纯净水中不含有人体需要的矿物质,青少年长期饮用纯净水对健康不利.故选项错误;
B、家里烧开水的目的之一是使硬水软化,因为这样可以使水中的钙离子和镁离子以沉淀的形式从水中析出.故选项正确;
C、人体内含量最多的物质是水.故选项错误;
D、无色透明的液体不一定是纯净水,例如氯化钠溶液是无色透明的液体.故选项错误.
故选B.1年前查看全部
- 水的净化效果最好的操作是______,可用______和______的方法使硬水软化.
 langrenjjk1年前1
langrenjjk1年前1 -
 又土又骚又丑 共回答了19个问题
又土又骚又丑 共回答了19个问题 |采纳率94.7%解题思路:根据已有的知识进行分析,净化水得到蒸馏水是最好的净水方法,硬水软化就是减少水中可溶性钙镁化合物的含量,据此解答.净化水得到蒸馏水是最好的净水方法,硬水软化就是减少水中可溶性钙镁化合物的含量,可溶性钙镁化合物受热易转化为不溶性钙镁化合物,故可以使用蒸馏或煮沸的方法降低水的硬度,故填:蒸馏,蒸馏,煮沸.
点评:
本题考点: 水的净化;硬水与软水.
考点点评: 本题考查了水净化的知识,完成此题,可以依据已有的知识进行.1年前查看全部
- 下列叙述正确的是( ) A.非金属单质都不导电 B.海水淡化、湖水净化和硬水软化都可用蒸馏法 C.物质在空气中变质都是
下列叙述正确的是( ) A.非金属单质都不导电 B.海水淡化、湖水净化和硬水软化都可用蒸馏法 C.物质在空气中变质都是与氧气有关 D.奥运火炬在没有氧气情况下也可以燃烧  仙sohyo1年前1
仙sohyo1年前1 -
 5ds54fds544 共回答了19个问题
5ds54fds544 共回答了19个问题 |采纳率89.5%A、石墨可以导电,可以作干电池的电极,所以非金属单质也可以导电,故A错误,
B、蒸馏是一种热力学的分离工艺,它利用混合液体或液-固体系中各组分沸点不同,使低沸点组分蒸发,再冷凝以分离整个组分的单元操作过程,是蒸发和冷凝两种单元操作的联合,分离液态混合物,三种水都可以利用蒸馏法将水净化,故B正确,
C、石灰水和氢氧化钠的变质和空气中的二氧化碳有关,不与空气中的氧气有关,故C错误,
D、可燃物必须和氧气接触,温度达到着火点才能燃烧,故D错误,
故选B.1年前查看全部
- (2012•阜新)在水的净化过程中,可以将硬水软化的操作是( )
(2012•阜新)在水的净化过程中,可以将硬水软化的操作是( )
A.蒸馏
B.过滤
C.沉淀
D.吸附 苏小莲eeww1年前1
苏小莲eeww1年前1 -
 懒人两个 共回答了16个问题
懒人两个 共回答了16个问题 |采纳率75%解题思路:根据已有的知识进行分析,硬水是指含有较多可溶性钙、镁离子的水,软水是指含有较少可溶性钙、镁离子的水,硬水软化就是减少水中的可溶性钙、镁离子的含量.A、蒸馏能除去水中可溶性钙镁离子,实现硬水软化,故A正确;
B、过滤不能减少可溶性钙镁离子的含量,故B错误;
C、沉淀不能减少可溶性钙镁离子的含量,故C错误;
D、吸附不能减少可溶性钙镁离子的含量,故D错误;
故答案为:A点评:
本题考点: 硬水与软水.
考点点评: 本题考查了硬水软化的方法,较容易,可以依据已有的净水知识完成1年前查看全部
- 硬水软化中,不能使液体剧烈沸腾为什么
 心静无雨1年前1
心静无雨1年前1 -
 荆棘森林 共回答了14个问题
荆棘森林 共回答了14个问题 |采纳率85.7%你要软化硬水,使用的方法是蒸馏,你想得到的是软水,如果剧烈沸腾了,蒸馏烧瓶内的硬水可能会溅入导管中,留入收集软水的容器中,得到的就不是你想要的纯软水了.蒸馏时加几块沸石或碎瓷片就不会暴沸了1年前查看全部
- 怎样使硬水软化?
 3622033711年前1
3622033711年前1 -
 1kcs0 共回答了13个问题
1kcs0 共回答了13个问题 |采纳率92.3%硬水软化的方法主要有:石灰软化法、离子交换法、电渗析法和反渗透法.
在水中加入石灰等化学药剂,在不加热的条件下除去Ca2+、Mg2+,降低水的硬度,达到水质软化的目的,这种方法称之为石灰软化法.
离子交换法是利用离子交换树脂交换离子的能力,按水处理的要求将原水中所不需要的离子通过交换而暂时占有,然后再将它释放到再生液中,使水得到软化的水处理方法.
反渗透法是从二十世纪五十年代发展起来的一项新型膜分离技术.
电渗析是利用离子交换膜和直流电场的作用,从水溶液和其他不带电组分中分离带电离子组分的一种电化学分离过程.1年前查看全部
- (2014•河南模拟)水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水的处理主要包括水的净化、污水处理、硬水软化
 (2014•河南模拟)水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水的处理主要包括水的净化、污水处理、硬水软化和海水的淡化等.
(2014•河南模拟)水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水的处理主要包括水的净化、污水处理、硬水软化和海水的淡化等.
(1)海水的淡化常用的方法有______、______、电渗析法等.
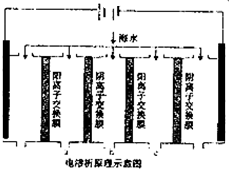
(2)电渗析法是近年来发展起来的一种较好的海水淡化技术,其原理如图所示.
①阳极(惰性电极)的电极反应式为______.
②淡水的出口为a、b、c中的______ 出口.
③某出口排出的浓海水中溴元素的含量为0.68g/L,现用氯气将其中的溴离子氧化为溴单质,则处理1.O×105L该浓海水需标况下的氯气的体积为______m3.
(3)K2FeO4是自来水厂常用的消毒、净化剂.工业上常用Fe(NO3)3溶液与浓KCIO溶液在强碱性环境中生成K2FeO4,该反应的离子方程式为______.
(4)氯碱工业常用______(填“阴”或“阳”)离子交换膜电解槽电解精制的饱和食盐水,若食盐水中含有杂质MgCl2则会对离子交换膜电解槽造成损害,其原因是Mg2++2Cl-+2H2O
Cl2↑+H2↑+Mg(OH)2↓电解 .Mg2++2Cl-+2H2O(用离子方程式表示).
Cl2↑+H2↑+Mg(OH)2↓电解 .
(5)工程塑料ABS合成时,用了以下三种单体:CH2═CH-CN、CH2═CH-CH═CH2、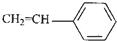 ,请写出ABS的结构简式______.
,请写出ABS的结构简式______.  程智怡1年前1
程智怡1年前1 -
 梁梁ma 共回答了21个问题
梁梁ma 共回答了21个问题 |采纳率90.5%解题思路:(1)海水淡化海水就是将海水中的可溶性杂质除去的过程;(2)①阳极是氢氧根离子失电子生成氧气和水;②在电渗析法淡化海水示意图中阴离子移向阳极,阳离子移向阴极,所以水在b处流出;③先求出溴元素的总质量和总物质的量,再求出消耗的氯气的量;(3)Fe(NO3)3溶液与浓KCIO溶液在强碱性环境中生成K2FeO4、氯化钾和水;(4)阳离子交换膜只允许阳离子通过,而阴离子不能通过;电解MgCl2会生成氢氧化镁沉淀、氯气和氢气;(5)单体之间发生加聚反应,单体中的双键断裂相互连接生成高分子化合物.(1)蒸馏法是把水从水的混合物中分离出来,得到纯净的水,利用离子交换法可以除去海水中的多种离子以达到硬水软化的效果,
故答案为:蒸馏法;离子交换法;
(2)①阳极是氢氧根离子失电子生成氧气和水,所以电极反应为:4OH--4e-=2H2O+O2↑,
故答案为:4OH--4e-=2H2O+O2↑;
②在电渗析法淡化海水示意图中阴离子移向阳极,阳离子移向阴极,通过用一段时间海水中的 阴阳离子在两个电极放电,所以水在b处流出,
故答案为:b;
③1.O×105L该浓海水中溴元素的质量为0.68g/L×1.O×105L=6.8×104g,则n(Br-)=
6.8×104g
80g/mol=8.5×102mol,由Cl2+2Br-=2Cl-+Br2可知处理1.O×105L该浓海水需标况下的氯气为4.25×102mol,则氯气的体积为4.25×102mol×22.4L/mol=9.52×103L=9.52m3;
故答案为:9.52;
(3)Fe(NO3)3溶液与浓KCIO溶液在强碱性环境中生成K2FeO4、氯化钾和水,该反应的离子方程式为2Fe3++3ClO-+10 OH-=2 FeO42-+3Cl-+5H2O;
故答案为:2Fe3++3ClO-+10 OH-=2 FeO42-+3Cl-+5H2O;
(4)使用阳离子交换膜,生成的氯气在阳极,生产的氢氧化钠在阴极,可避免Cl2和NaOH溶液,电解MgCl2会生成氢氧化镁沉淀、氯气和氢气,其电解反应为:Mg2++2Cl-+2H2O
电解
.
Cl2↑+H2↑+Mg(OH)2↓;
故答案为:阳;Mg2++2Cl-+2H2O
电解
.
Cl2↑+H2↑+Mg(OH)2↓;
(5)单体之间发生加聚反应,单体中的双键断裂相互连接生成高分子化合物,已知:CH2═CH-CN、CH2═CH-CH═CH2、 ,则反应生成的高分子化合物为:
,则反应生成的高分子化合物为: .
.点评:
本题考点: 氯碱工业;电解原理;常用合成高分子材料的化学成分及其性能.
考点点评: 本题考查了海水淡化的电渗析原理的分析判断、氯气的性质及计算、加聚反应等,题目难度中等,掌握电解原理是解题的关键.1年前查看全部
- (1)长期饮用硬水对身体健康不利,区分软水还是硬水可以用______来检验.日常生活中可以用______方法来硬水软化;
(1)长期饮用硬水对身体健康不利,区分软水还是硬水可以用______来检验.日常生活中可以用______方法来硬水软化;
(2)就如何处理好经济发展与水资源保护的关系,下列观点你认为不正确的有______
A水资源取之不尽,只要经济发展了,不怕污染和浪费
B在经济发展过程中,造成环境污染使不可避免的,对此不必大惊小怪
C先发展后治理. goodwing151年前1
goodwing151年前1 -
 gabyaijunji14 共回答了15个问题
gabyaijunji14 共回答了15个问题 |采纳率100%解题思路:(1)常用肥皂水来检验水是软水还是硬水;煮沸可以降低水的硬度;
(2)根据水资源的状况及防止水的污染的措施分析.(1)为检验净化后的水是软水还是硬水,可以加入肥皂水,浮渣多的是硬水,泡沫多的是软水.加热煮沸能够将水中可溶性的钙镁化合物转化成不溶性的,从而降低水的硬度;
(4)正确处理好经济发展与水资源保护的关系.水资源是有限的,不是取之不尽的,在经济发展过程中,应节约用水,保护水资源,防止水污染.故A、B、C的观点都是错误的.
故答为:(1)肥皂水;煮沸;(2)ABC.点评:
本题考点: 硬水与软水;保护水资源和节约用水.
考点点评: 解答本题要充分理解净化水的方法、防止水的污染等方面的知识,只有这样才能对相关方面的问题做出正确的判断.1年前查看全部
- 水是生命之源.将浑浊的水变澄清的简单方法是______.区分硬水和软水的试剂是______,生活中硬水软化的方法是___
水是生命之源.将浑浊的水变澄清的简单方法是______.区分硬水和软水的试剂是______,生活中硬水软化的方法是______.常见的水污染的原因有______(写一条即可).  老隼1年前1
老隼1年前1 -
 接地线 共回答了19个问题
接地线 共回答了19个问题 |采纳率89.5%浑浊的水中含有不溶于水的固体杂质,可用过滤法除去;硬水中含有较多不溶性钙镁离子化合物,煮沸时分解产生水垢多,硬水中加入肥皂水,产生的泡沫少,浮渣多;常见的水污染的原因有工业废水未处理就排放、生活污水未处理就排放.
故答案为:过滤;肥皂水;煮沸;工业废水未处理就排放.1年前查看全部
- 下列说法中有错误的是( )A.区分硬水和软水--加肥皂水振荡B.生活中将硬水软化--煮沸水C.净化水程度最高的方法--
下列说法中有错误的是( )
A.区分硬水和软水--加肥皂水振荡
B.生活中将硬水软化--煮沸水
C.净化水程度最高的方法--吸附
D.食盐和纯碱--都是盐 罗开1年前1
罗开1年前1 -
 美的12345 共回答了17个问题
美的12345 共回答了17个问题 |采纳率94.1%解题思路:A、肥皂水可以区分软水和硬水;
B、煮沸的方法可以将硬水软化;
C、吸附会除去异味和杂质;
D、盐是指由金属离子和酸根离子构成的化合物.A、软水加肥皂水可生成较多的泡沫,硬水加肥皂水生成的泡沫少,所以区分硬水和软水加肥皂水振荡,故A正确;
B、硬水在加热煮沸的条件下能生成不溶于水的碳酸钙和氢氧化镁沉降下来,能将硬水软化,故B正确;
C、吸附只会除去水中的异味和色素,不会除去其他可溶性的杂质,所以净化程度不高,故C错误;
D、盐是指由金属离子和酸根离子构成的化合物,所以食盐和纯碱都是盐,故D正确.
故选C.点评:
本题考点: 硬水与软水;常见的氧化物、酸、碱和盐的判别.
考点点评: 蒸馏可以将水转化成水蒸气,然后再液化的一种操作,得到的水中几乎不含杂质,是净化水程度最高的方法.1年前查看全部
- (2010•柳州)硬水洗衣服既浪费肥皂又洗不干净,生活中要使硬水软化,可采用的方法是( )
(2010•柳州)硬水洗衣服既浪费肥皂又洗不干净,生活中要使硬水软化,可采用的方法是( )
A.煮沸
B.搅拌
C.吸附
D.过滤 redruik1年前1
redruik1年前1 -
 天海散人 共回答了13个问题
天海散人 共回答了13个问题 |采纳率100%解题思路:过滤只能除去颗粒较大的不溶性杂质,吸附只会除去色素和异味,搅拌会使溶解的物质更加均匀,煮沸可以降低水的硬度,通过分析可以解答.A、煮沸可以使水中的可溶性钙镁化合物分解,而降低水的硬度,故A正确.
B、搅拌只会使溶解的物质更加均匀,不能改变水硬度,故B错误.
C、吸附只能吸附色素和异味,不能改变水的硬度,故C错误.
D、过滤只能除去水中颗粒较大的不溶性物质,不能改变水的硬度,故D错误.
故选A.点评:
本题考点: 硬水与软水.
考点点评: 本题主要考查了可以降低水硬度的方法,比较简单,便于解答.1年前查看全部
- 下列关于水的说法正确的是?A.活性炭可以吸附水中不溶性杂质 B.沉降方法可以使硬水软化为软水C.过滤能除去天然水中所有杂
下列关于水的说法正确的是?
A.活性炭可以吸附水中不溶性杂质 B.沉降方法可以使硬水软化为软水
C.过滤能除去天然水中所有杂质 D.日常生活中的水大多是混合物 hao_无赖1年前1
hao_无赖1年前1 -
 coffee1981825 共回答了12个问题
coffee1981825 共回答了12个问题 |采纳率91.7%选择D项.
活性炭吸附可溶性杂质.
煮沸才能是硬水变为软水.
过滤只能过滤掉固体颗粒物,不能去掉可溶性杂质.1年前查看全部
- 使用硬水会给生活和生产带来许多麻烦,设法除去硬水中的_____,可以使硬水软化成软水.
 xj05311年前1
xj05311年前1 -
 kaka0625 共回答了14个问题
kaka0625 共回答了14个问题 |采纳率78.6%硬水是指含有较多、可溶性、钙镁化合物的水.设法除去硬水中的钙、镁化合物,可以使硬水软化成软水..1年前查看全部
- 纯碱在日常生活和化学工业中用途很广,如用于硬水软化、洗涤剂生产、食品加工、石油精炼、粗盐精制、玻璃制造等领域.工业上以食
纯碱在日常生活和化学工业中用途很广,如用于硬水软化、洗涤剂生产、食品加工、石油精炼、粗盐精制、玻璃制造等领域.工业上以食盐、氨气(主要由合成氨厂提供)和二氧化碳为主要原料生产纯碱.其流程如下:

已知有关物质重要反应的化学方程式如下:
①NaCl+NH3+H2O+CO2
NaHCO3↓+NH4Cl△ .
②2NaHCO3
Na2CO3+H2O+CO2↑△ .
③2NH4Cl+X
2NH3↑+CaCl2+2H2O△ .
④NH4Cl═NH3↑+HCl↑
根据以上信息回答下列问题.
(1)盐水精制的过程是除去溶液中各种杂质的过程.为将盐水中含有的Ca2+、Mg2+等沉积,可以向其一和加入过量纯碱.此时将混合液中不溶物除去的方法是______;溶液中多余的纯碱可以加______试剂来除去.
(2)氨碱工业最关键的一步是:在加压的条件下不断向饱和的氨盐水中通人二氧化碳气体,溶液中会有碳酸氢钠晶体析出.试分析该流程需要加压条件的原因是:______.
(3)在氨碱工业的历史上.如何处理流程中剩余的氯化铵溶液,出现了两种工艺:一是“索尔维法”.即在氯化铵溶液中加入物质X______(填化学式),产生了可循环使用的氨气,和大量固体废弃物氯化钙;二是我国化学家侯德榜发明的“联合制碱法”,即在氯化铵溶液中加入适量氯化钠晶体.降低了氯化氨的______,使氯化铵晶体单独析出得到另一种产品--氮肥.氯化钠溶液则可以循环利用.
(4)在氨碱工业处理剩余的氯化铵溶液时.为何不直接蒸发结晶析出氯化铵固体?答:______. gxb0031年前1
gxb0031年前1 -
 雾海碧竹 共回答了21个问题
雾海碧竹 共回答了21个问题 |采纳率81%解题思路:(1)根据过滤的原理回答前一空;根据碳酸钠的化学性质和除杂的原理回答后一空.
(2)根据气体的溶解度随压强的增大而增大回答.
(3)根据铵盐与碱性物质反应生成氨气的性质回答前一空;根据氯化钠溶液和氯化铵溶液中都含氯离子,氯化钠是制纯碱的原料回答.
(4)根据氯化铵的化学性质回答.(1)过滤是把不溶于液体的固体与液体分开的操作,所以除去液体混合物中的不溶性杂质用过滤的方法;碳酸钠能和盐酸反应生成氯化钠、水、二氧化碳,用盐酸除去多余的碳酸钠不会产生新杂质.
(2)二氧化碳能溶于水,但溶解性较差,气体的溶解度随压强的增大而增大,为了促进更多二氧化碳溶解,使反应更充分,所以需加压条件.
(3)铵盐与碱性物质反应生成氨气,在氯化铵溶液中加入物质X产生了可循环使用的氨气,定是加入的碱性物质,最廉价的碱是熟石灰,所以加入的物质是熟石灰;氯化钠溶液和氯化铵溶液中都含氯离子,在氯化铵溶液中加入适量氯化钠晶体可降低氯化铵的溶解度,使氯化铵晶体单独析出.
(4)不直接蒸发结晶析出氯化铵固体,是因氯化铵受热易分解.
故答案为:(1)过滤;盐酸;
(2)促进更多二氧化碳溶解,使反应更充分;
(3)Ca(OH)2;溶解度;
(4)因氯化铵受热易分解.点评:
本题考点: 过滤的原理、方法及其应用;物质除杂或净化的探究;纯碱的制取.
考点点评: 化学来源于生产、生活,又服务于生产、生活,氨碱工业是初中化学重要的应用之一,是考查重点,常涉及化学方程式的书写,二氧化碳和氨气通入的顺序及原因,反应时析出碳酸氢钠的原因与物质溶解度的关系.1年前查看全部
- 常用的净化水的方法有______、______、______、______等,实验室里常用______方法使硬水软化,在
常用的净化水的方法有______、______、______、______等,实验室里常用______方法使硬水软化,在操作过程中常在水中加入几粒沸石(碎瓷片),其作用是______.
 dior08291年前1
dior08291年前1 -
 磬龙 共回答了20个问题
磬龙 共回答了20个问题 |采纳率95%解题思路:根据净化水常用的方法分析填空.蒸馏之后得到的水是纯水,净化程度最高,在蒸馏操作中常在水中加入几粒沸石以防止爆沸.常用的净化水的方法有沉淀、过滤、吸附、蒸馏等.蒸馏之后得到的水是纯水,净化程度最高,实验室里常用蒸馏方法使硬水软化,在操作过程中常在水中加入几粒沸石(碎瓷片),其作用是防止爆沸.
故答为:沉淀、过滤、吸附、蒸馏. 蒸馏;防止爆沸.点评:
本题考点: 水的净化;蒸发与蒸馏操作;硬水与软水.
考点点评: 本题主要考查了水的净化方法.熟练掌握净水的几种方法,知道蒸馏可以得到纯水.1年前查看全部
- 硬水软化时发生的化学方程式?如没有 请解释为何硬水的软化是化学变化以及为何钙镁离子可以转为沉淀
 wuhualin55661年前2
wuhualin55661年前2 -
 cyberthug 共回答了21个问题
cyberthug 共回答了21个问题 |采纳率85.7%Ca(HCO3)2=△=CaCO3↓+CO2↑+H2O↑(水已变成水蒸气)
Mg(HCO3)2=△=MgCO3↓+CO2↑+H2O↑
相信我,没错的!1年前查看全部
- 回答下列与水有关的问题:(1)日常生活中,常利用______的方法使硬水软化;(2)在水的净化过程中,常利用______
回答下列与水有关的问题:
(1)日常生活中,常利用______的方法使硬水软化;
(2)在水的净化过程中,常利用______的吸附性除去异味和有色物质;
(3)通电分解水时,与电源的______极相连的玻璃管中产生的气体能使带火星的木条复燃. 高山1流水1年前1
高山1流水1年前1 -
 爱mm杀生丸 共回答了13个问题
爱mm杀生丸 共回答了13个问题 |采纳率92.3%解题思路:(1)根据硬水软化法分析;
(2)根据活性炭具有吸附性分析;
(3)根据电解水的现象分析(1)日常生活中,常利用煮沸的方法使硬水软化;
(2)活性炭具有吸附性,在水的净化过程中,常利用活性炭的吸附性除去异味和有色物质;
(3)电解水时,“正氧负氢,氢二氧一”,与电源的正极相连的玻璃管中产生的气体是氧气,能使带火星的木条复燃.
故答案为:(1)煮沸;
(2)活性炭;
(3)正.点评:
本题考点: 硬水与软水;电解水实验;碳单质的物理性质及用途.
考点点评: 本题主要考查基础知识,难度不大.1年前查看全部
- (2006•张家界)长期饮用硬水可能会引起体内结石.生活中要使硬水软化可采用的方法是( )
(2006•张家界)长期饮用硬水可能会引起体内结石.生活中要使硬水软化可采用的方法是( )
A.煮沸
B.吸附
C.过滤
D.搅拌 开始懂了22221年前1
开始懂了22221年前1 -
 压丫 共回答了16个问题
压丫 共回答了16个问题 |采纳率100%解题思路:从硬水的成分和如何简单有效的消除硬水成分进行考虑.硬水是指含有较多钙、镁离子的水,煮沸能使钙、镁离子形成沉淀析出,这是生活中最常用的最简单的降低水硬度的方法.
故选A点评:
本题考点: 硬水与软水.
考点点评: 该题能帮助学生了解化学在生活中的应用,体会学以致用的快乐.1年前查看全部
大家在问
- 1I -----go to bed -----12 o'clock last night?
- 2杂志 作文
- 3(2010•海淀区二模)生态系统的自我调节能力,对于维持生态系统的稳定起着关键作用.这是通过( )
- 4一批水果,第一天卖出5/4,第二天比第一天少卖7/6,第一天比第二天多卖120千克,这批水果有多少千克?
- 5Eric ___________ (not play) soccer after class.
- 6等腰三角形的两个底角的平分线相等.写出逆定理并证明.
- 7解方程8又七分之二-x=三又三分之一-3.5
- 8(m55五•西城区三模)在研究性学习中,某同学设计了一个测定带电粒子 比荷的实验,其实验装置如k所示.
- 9还要写公式.急.(1)小东有一辆自行车,车轮的直径大约是66cm,如果平均每周转100周,从家到学校的路程是2000m,
- 10The Life of Mark Twain的英语课文翻译
- 11(2014•奉贤区一模)互为同素异形体的一组物质是( )
- 12把“人们把‘有知识’说成‘有学问’,这不是没有道理的.”这句话换个说法,但句意不变
- 13y=1/2x的平方-2/3x-2化为顶点式怎么化?
- 14My cunt's daughter is my ______.
- 15In fact,IIn fact,I miss you too much miss you
