直接甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。
 不能三言两语2022-10-04 11:39:541条回答
不能三言两语2022-10-04 11:39:541条回答| 直接甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。  (1)101 kPa时,1 mol CH 3 OH完全燃烧生成稳定的氧化物放出热量726.51 kJ/mol,则甲醇燃烧的热化学方程式为 。 (2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是: ①CH 3 OH(g)+H 2 O(g)=CO 2 (g)+3H 2 (g) △H 1 ="+49.0" kJ·mol -1 ②CH 3 OH(g)+ 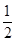 O 2 (g)= CO 2 (g)+2H 2 (g) △H 2 O 2 (g)= CO 2 (g)+2H 2 (g) △H 2 已知H 2 (g)+ 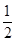 O 2 (g)=H 2 O(g) △H ="-241.8" kJ·mol -1 O 2 (g)=H 2 O(g) △H ="-241.8" kJ·mol -1 则反应②的△H 2 = kJ·mol -1 。 (3)甲醇燃料电池的结构示意图如右。甲醇进入 极(填“正”或“负”),正极发生的电极反应式为 。负极发生的电极反应式为 。 |

已提交,审核后显示!提交回复
共1条回复
 啊啊72 共回答了23个问题
啊啊72 共回答了23个问题 |采纳率87%- (1)CH 3 OH(g)+3/2O 2 (g)=CO 2 (g)+2H 2 O(l) △H=-726.51kJ/mol (2)-192.8
(3)负 O 2 +4H + +4e - =2H 2 O CH 3 OH+H 2 O-6e - =CO 2 ↑+6H +
- 1年前
相关推荐
- (2011•连云港模拟)直接甲醇燃料电池(DMFC),它属于质子交换膜燃料电池(PEMFC)中之一类,系直接使用水溶液以
 (2011•连云港模拟)直接甲醇燃料电池(DMFC),它属于质子交换膜燃料电池(PEMFC)中之一类,系直接使用水溶液以及蒸汽甲醇为燃料供给能源,而不需通过重组器高温重组甲醇、汽油及天然气等再取出氢以供发电.下列对于该电池的说法不正确的是( )
(2011•连云港模拟)直接甲醇燃料电池(DMFC),它属于质子交换膜燃料电池(PEMFC)中之一类,系直接使用水溶液以及蒸汽甲醇为燃料供给能源,而不需通过重组器高温重组甲醇、汽油及天然气等再取出氢以供发电.下列对于该电池的说法不正确的是( )
A.直接甲醇燃料电池低温生电、燃料成分危险性低与电池结构简单等特性
B.电池工作时,电解质溶液pH值保持不变
C.电池的负极反应式为3O2+12e-+12H+═6H2O
D.电池工作时,1molCH3OH被氧化时就有6NA个氢离子在正极消耗 凸-_-凸o觜1年前1
凸-_-凸o觜1年前1 -
 小云儿宝贝 共回答了21个问题
小云儿宝贝 共回答了21个问题 |采纳率95.2%解题思路:A.直接甲醇燃料电池低温生电、燃料成分危险性低、电池结构简单;
B.电池工作的原理是氢气与氧气反应生成水的过程,水增多,使硫酸溶液pH增大;
C.原电池负极失电子;
D.根据在闭合回路中正极和负极流过的电子数相等解题.A.直接甲醇燃料电池低温生电、燃料成分危险性低、电池结构简单等,故A正确;
B.该装置中由于水的生成而使硫酸溶液的浓度变小,因此pH值增大,故B错误;
C.原电池负极失电子,应为甲醇失电子,负极反应式为:2CH3OH+2H2O-12e-═12H++2CO2,故C错误;
D.正极发生的电极反应式是:3O2+12H++12e-═6H2O,负极发生的电极反应式是:2CH3OH+2H2O-12e-═12H++2CO2,当1molCH3OH被氧化时,负极失去6mol电子,在正极正极得到6mol电子,消耗的氢离子是6mol,即1molCH3OH被氧化时就有6NA个氢离子在正极消耗,故D正确;
故选:BC.点评:
本题考点: 化学电源新型电池.
考点点评: 本题考查学生燃料电池的工作原理知识,题干信息和图示转化关系是分析的关键,可以根据所学知识进行回答,难度适中.1年前查看全部
- (13分)直接甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。
(13分)直接甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。
(1)101 kPa时,1 mol CH 3 OH完全燃烧生成稳定的氧化物放出热量726.51 kJ/mol,则甲醇燃烧的热化学方程式为 。
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是:
①CH 3 OH(g)+H 2 O(g)=CO 2 (g)+3H 2 (g) △H 1 ="+49.0" kJ·mol -1
②CH 3 OH(g)+ O 2 (g)= CO 2 (g)+2H 2 (g) △H 2
O 2 (g)= CO 2 (g)+2H 2 (g) △H 2
已知H 2 (g)+ O 2 (g)===H 2 O(g) △H ="-241.8" kJ·mol -1
O 2 (g)===H 2 O(g) △H ="-241.8" kJ·mol -1
则反应②的△H 2 = 。
(3)甲醇燃料电池的结构示意图如右。甲醇进入 极(填“正”或“负”),该极发生的电极反应为 。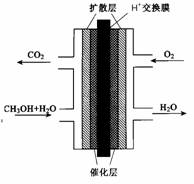
(4)已知H—H键能为436 KJ/mol,H—N键能为391KJ/mol,根据化学方程式:
N 2 ( g ) + 3H 2 ( g ) = 2NH 3 ( g ) ΔH=" —92.4" KJ/mol,则N≡N键的键能是 。 鲸鲸的小梳子1年前1
鲸鲸的小梳子1年前1 -
 ly591405798 共回答了21个问题
ly591405798 共回答了21个问题 |采纳率90.5%(13分)(1)CH 3 OH(l) + 3/2 O 2 (g) = CO 2 (g) + 2H 2 O(l) △H =-726.51 kJ/mol (3分)
(2)-192.8 kJ·mol -1 (3分)
(3)负 (2分) CH 3 OH+ H 2 O-6e - =CO 2 + 6H + (2分) (4)945.6KJ/mol (3分)
1年前查看全部
- 直接甲醇燃料电池被认为是21世纪电动汽车最佳候选动力源.
 直接甲醇燃料电池被认为是21世纪电动汽车最佳候选动力源.
直接甲醇燃料电池被认为是21世纪电动汽车最佳候选动力源.
(1)101KPa时,1mol气态CH3OH完全燃烧生成CO2气体和液态水时,放出726.51kJ的热量,则甲醇燃烧的热化学方程式是CH3OH(l)+[3/2]O2(g)=CO2(g)+2H2O(l)△H=-726.51kJ/molCH3OH(l)+[3/2]O2(g)=CO2(g)+2H2O(l)△H=-726.51kJ/mol_.
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是:
①CH3OH(g)+H2O (g)═CO2(g)+3H2(g);△H1═+49.0KJ•mol-1
②CH3OH(g)+[1/2] O2 (g)═CO2(g)+2H2(g);△H2═?
已知H2(g)+[1/2] O2 (g)═H2O (g)△H═-241.8KJ•mol-1,则反应②的△H2=______.
(3)一种甲醇燃料电池是采用铂或碳化钨作电极,稀硫酸作电解液,一极直接加入纯化后的甲醇,同时向另一个电极通人空气.则甲醇进入______极,正极发生的电极反应方程式为______. iszero1年前1
iszero1年前1 -
 微雨嫣火 共回答了24个问题
微雨嫣火 共回答了24个问题 |采纳率100%解题思路:(1)1molCH3OH完全燃烧生成稳定的氧化物为气态二氧化碳和液态水,放出热量726.51kJ/mol,以此书写热化学方程式;
(2)由盖斯定律可知,①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H1=+49.0kJ•mol-1、③H2(g)+[1/2]O2(g)═H2O(g)△H=-241.8kJ•mol-1,①+③得到反应②;
(3)甲醇燃料电池中,甲醇为负极,电解质为酸,甲醇失去电子生成二氧化碳;(1)1molCH3OH完全燃烧生成稳定的氧化物为气态二氧化碳和液态水,放出热量726.51kJ/mol,则燃烧的热化学方程式为CH3OH(l)+[1/2]O2(g)=CO2(g)+2H2O(l)△H=-726.51kJ/mol,
故答案为:CH3OH(l)+[3/2]O2(g)=CO2(g)+2H2O(l)△H=-726.51kJ/mol;
(2)由盖斯定律可知,①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H1=+49.0kJ•mol-1、③H2(g)+[1/2]O2(g)═H2O(g)△H=-241.8kJ•mol-1,①+③得到反应②,
则△H2=+49.0kJ•mol-1+(-241.8kJ•mol-1)=-192.8kJ•mol-1,故答案为:-192.8kJ•mol-1;
(3)甲醇燃料电池中,甲醇中C元素的化合价升高,则甲醇为负极,电解质为酸,甲醇失去电子生成二氧化碳,正极电极反应为O2+4H++4e-=2H2O,
故答案为:负;O2+4H++4e-=2H2O.点评:
本题考点: 用盖斯定律进行有关反应热的计算;热化学方程式;原电池和电解池的工作原理.
考点点评: 本题为综合题,涉及反应热的计算、热化学反应方程式的书写、燃料电池等知识点,注重高考常考考点的考查,题目难度中等.1年前查看全部
- 能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。直接甲醇燃料电池(DNFC)被认为是2
能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。直接甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。
(1)工业上一般采用下列两种反应合成甲醇:
反应I:CO(g)+2H 2 (g)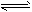 CH 3 OH(g) △H1
CH 3 OH(g) △H1
反应Ⅱ:CO 2 (g)+3H 2 (g)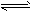 CH 3 OH(g)+H 2 O(g) △H2
CH 3 OH(g)+H 2 O(g) △H2
①上述反应符合“原子经济”原则的是____(填“I”或“Ⅱ”);
②用反应I生产燃料甲醇,该反应的化学平衡常数表达式为K=_________,下表所列数据是反应I在不同温度下的化学平衡常数(K)。
由表中数据判断△H1___0(填“>”“=”或“<”);
③某温度下,将2 mol CO和6 mol H 2 充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO) =0.2
mol/L,则CO的转化率为_____,此时的温度为____(从上表中选择)。
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH 3 OH(g) +H 2 O(g) =CO 2 (g)+3H 2 (g) △H1 =+49. 0 kJ/mol
②CH 3 OH(g)+O 2 (g)=CO 2 (g)+2H 2 (g) △H2
已知H 2 (g)+O 2 (g)=H 2 O(g) △H=-241.8 kJ/mol
则反应②的△H2=____kJ/mol;
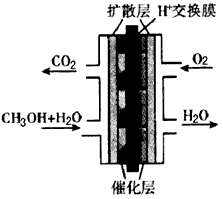
(3)下图是甲醇燃料电池的结构示意图。甲醇进入____极(填“正”或“负”),正极发生的电极反应为
___________________。
 一呀么yi1年前1
一呀么yi1年前1 -
 洪波涌起 共回答了18个问题
洪波涌起 共回答了18个问题 |采纳率100%1年前查看全部
大家在问
- 1如何从硝酸钡和硝酸银中制取银和碳酸钡
- 2家人,的英文怎么写
- 3福尔摩斯中“ 艾琳艾德勒”的英文原名是什么?(音译之前)
- 4他打算和朋友一起过,译英
- 5设集合U={y|y=3-x^2﹜,N={y|y=2x^2-1},则M∩N=——
- 6未完成(二) 作文
- 7地球孕育生命,但也破坏生命?给个例子
- 8我一直觉得我们人类其实就和其他未知生物一样的 看不到大的方向 一直以我们地球 我们人类就是宇宙中唯一 其实宇宙理论上 无
- 9妈妈买了一些桃子,如果2个放一盘,多出1个;如果3个放一盘,也多出一1给个;如果5个放一盘,还多出一个.妈妈最少买了多少
- 10小学和初中语文教师应聘笔试面试内容是什么
- 11六年级英语选择填空
- 12请教色环电阻棕1,红2,橙3,黄4,绿5,蓝6,紫7,灰8,白9,黑0怎样算?
- 13如图1,已知等边△ABC的边长为1,D、E、F分别是AB、BC、AC边上的点(均不与点A、B、C重合),记△DEF的周长
- 14I sincerely hope you can return my sentence是什么意思
- 15researchers believe that the tendency for diabetes is presen

