漂白性的概念,且说明为什么二氧化硫把品红溶液褪色了,算漂白,有些氧化还原反应把有色溶液变成无色不算
 swexbf2022-10-04 11:39:543条回答
swexbf2022-10-04 11:39:543条回答那么次氯酸也有漂白性,也和其他物质反应了,为什么

已提交,审核后显示!提交回复
共3条回复
 you007long 共回答了16个问题
you007long 共回答了16个问题 |采纳率93.8%- SO2使品红褪色是它的性质
氧化还原反应是把有色物质反应生成了其他没有颜色的物质 所以不是漂白 - 1年前
 利箭1 共回答了4个问题
利箭1 共回答了4个问题 |采纳率- 发生反应生成了物质就不算
- 1年前
 ISTARchen 共回答了5个问题
ISTARchen 共回答了5个问题 |采纳率- 因为二氧化硫使品红褪色没有生成新的物质,而有些氧化还原反应使有色溶液变成无色是生成了新的物质
- 1年前
相关推荐
- 自来水用氯气消毒,为什么说是次氯酸的强氧化性和漂白性.氯气不是也有强氧化性可以杀菌?
 chase_soulmate1年前1
chase_soulmate1年前1 -
 koushuiji 共回答了17个问题
koushuiji 共回答了17个问题 |采纳率88.2%氯气确为强氧化剂,但氯气遇水会会更倾向于生成次氯酸,进而借由具有更强的氧化性的次氯酸发挥消毒作用.查看更多答案1年前查看全部
- 二氧化硫加入酚酞中,溶液褪色,能否证明二氧化硫具有漂白性
 天外来客881年前3
天外来客881年前3 -
 ao_1 共回答了12个问题
ao_1 共回答了12个问题 |采纳率83.3%不可以,因为二氧化硫溶于水显酸性,酚酞遇酸呈无色,且漂白性表现为使液体褪色,酚酞本身无色,加入二氧化硫当然不能说明二氧化硫有漂白性1年前查看全部
- 1 次氯酸钠和次氯酸钙都有漂白性吗?
1 次氯酸钠和次氯酸钙都有漂白性吗?
2 氯水的成分有什么,它和液氯有什么区别? fhh5it1年前1
fhh5it1年前1 -
 伊人微微 共回答了13个问题
伊人微微 共回答了13个问题 |采纳率92.3%1.都有吧
2.氯水是氯气溶于水,生成了HCL和HCLO,并且还有一部分以CL2存在于水中.液氯是氯气在高压低温下液化形成的1年前查看全部
- 二氧化硫的还原性与漂白性都是化学性质吗?
 hotice3211年前2
hotice3211年前2 -
 啤酒沫 共回答了16个问题
啤酒沫 共回答了16个问题 |采纳率81.3%都是
漂白性体现在与品红溶液反应,
还原性体现在S的+4价被氧化成+6价,即2SO2+O2=2SO31年前查看全部
- 次氯酸的漂白性和氧化性有什么区别
 族一梦做1年前2
族一梦做1年前2 -
 zb226 共回答了24个问题
zb226 共回答了24个问题 |采纳率95.8%没有区别,次氯酸的漂白性就是它的强氧化性,将有色物质氧化漂白.氧化性物质不一定具有漂白性.如O2就没有漂白性.1年前查看全部
- 强氧化性 漂白性 酸性他们之间有什么关系尤其是强氧化性和漂白性,他们之间不是没有必然的联系吗 为什么 次氯酸是弱酸,比碳
强氧化性 漂白性 酸性
他们之间有什么关系
尤其是强氧化性和漂白性,他们之间不是没有必然的联系吗 为什么 次氯酸是弱酸,比碳酸弱,但有强氧化性和漂白性?
囊 氯水让有色布条退色是用了什么原理?为什么不是漂白性? woyao20091年前4
woyao20091年前4 -
 彭转转171 共回答了12个问题
彭转转171 共回答了12个问题 |采纳率83.3%氯水让有色布条退色是用了HCLO有强氧化性的原理
氯水让有色布条退色是用了HCLO有强氧化性的原理,体现了HCLO的漂白性
(这里,强氧化性是前提,是条件,而漂白性是现象、是结果.能体会么?)
.
1.有强氧化性 一般都是高价态的物质
且有强氧化性一般都有漂白性
2.物质具有漂白性的原因却各不相同.
大致分为两大类:物理原因(活性炭)
化学原因(强氧化性或与有色物质结合)
3总之,强氧化性 漂白性 酸性 三者都没有必然联系1年前查看全部
- 过氧化钠,次氯酸,臭氧的漂白性都是利用其强氧化型 活性炭利用吸附作用 二氧化硫应能与有色物质结合而漂白]以上的表白那些在
过氧化钠,次氯酸,臭氧的漂白性都是利用其强氧化型 活性炭利用吸附作用 二氧化硫应能与有色物质结合而漂白]以上的表白那些在加热或什么情况下可以是有色物质复原呢呢?还是说他们的漂白都是永久的?还有比如次氯酸他可以表白任何有颜色的物质么?都体现强氧化型么?都可以永久漂白么?加热都不复原的么?3.次氯酸可以漂白含碘使淀粉变蓝的溶液么?
 zz有音乐吗1年前2
zz有音乐吗1年前2 -
 超级无敌宝贝猪 共回答了17个问题
超级无敌宝贝猪 共回答了17个问题 |采纳率76.5%二氧化硫漂白是通过与有色物质结合变为无色,有色物质并未被破坏,所以一但其中的二氧化硫流失就会再显色.
强氧化剂漂白是通过破坏有色物质的分子结构来脱色,并且通常将有色物质分解为小分子,此过程是不可逆的,所以能永久漂白.1年前查看全部
- SO2漂白性SO2与品红褪色,你们怎么知道是SO2的漂白性呢,可能是其于品红发生氧化还原反应呢?
 4960354201年前2
4960354201年前2 -
 manys 共回答了13个问题
manys 共回答了13个问题 |采纳率84.6%哈哈,我来吧.跟我以前一样
漂白性和氧化还原性不是一个系统的,是一个互相包容的性质.
可以氧化漂白,可以反应生成白色物质,还有还原,物理漂白.
SO2具有还原性和氧化性,还具有漂白性
漂白是结果,反应是过程,不矛盾1年前查看全部
- 氯气可以说有漂白性吗
 关西道口1年前1
关西道口1年前1 -
 好想摆脱 共回答了20个问题
好想摆脱 共回答了20个问题 |采纳率100%氯水有漂白性 干燥氯气无漂白性1年前查看全部
- 次氯酸钠为什么会有漂白性?
 亡美dd1年前2
亡美dd1年前2 -
 游离的海 共回答了20个问题
游离的海 共回答了20个问题 |采纳率90%NaClO中ClO-水解生成HClO,所以也有漂白性.
ClO- + H2O HClO + OH-
次氯酸钠具有强氧化性,可以用来用于水的净化,以及作消毒剂、纸浆漂白等.1年前查看全部
- 高中有机物中有什么物质有漂白性?
 冰冻千年1年前3
冰冻千年1年前3 -
 lilyplmm123 共回答了20个问题
lilyplmm123 共回答了20个问题 |采纳率90%高中里有机物常见的没有,
但是有时做题时会出过氧乙酸,
过氧乙酸就具有漂白性和强氧化性!1年前查看全部
- 次氯酸漂白性的实质...老师说是氧化还原反应.麻烦举几个例子说明一下原因.为什么HClo能漂白呢.就是...将它滴入紫色
次氯酸漂白性的实质...
老师说是氧化还原反应.麻烦举几个例子说明一下原因.
为什么HClo能漂白呢.就是...将它滴入紫色石蕊溶液中 是发生了什么反应 使溶液褪色了呢?这个问题我一直没有想明白. 999-xin1年前1
999-xin1年前1 -
 wz520jf 共回答了19个问题
wz520jf 共回答了19个问题 |采纳率89.5%次氯酸漂白性的实质是次氯酸被还原,发生了氧化反应
而次氯酸中的次氯酸根有强氧化性,会与有色物质反应,把有色物质氧化成白色
如果说例子的话跟有色物质反应也没法写方程式.HCLO中的cl是+1价氧化性极强.很容易被还原成0价或者是-1价,这就是它漂白的实质.
石蕊
蓝紫色粉末.是从植物中提取得到的蓝色色素,能部分地溶解于水而显蓝色.石蕊是一种常用的指示剂,变色范围是pH5.0—8.0之间.石蕊起指示剂作用是由于石蕊中含石蕊精(C7H7O4N)的原因.其原理是石蕊也是一种弱酸,在水溶液中存在如下平衡:HZ代表石蕊分子
关于石蕊试液和次氯酸的反应式我想应该不需要知道,反应式也特别复杂.只要知道石蕊试液是一种色素,能被次氯酸氧化即可.1年前查看全部
- 下列反应中能体现二氧化硫有漂白性的是( )
下列反应中能体现二氧化硫有漂白性的是( )
A.将SO2通入品红溶液中,溶液褪色
B.将SO2气体通入溴水中,溶液褪色
C.将SO2气体通入含有氢氧化钠的酚酞溶液中,溶液褪色
D.将SO2气体通入酸性高锰酸钾溶液中,溶液褪色 luckid1年前1
luckid1年前1 -
 oklawa 共回答了21个问题
oklawa 共回答了21个问题 |采纳率85.7%解题思路:A、红色褪去的原因是:二氧化硫和水反应生成的亚硫酸和有机色素品红结合成不稳定的无色物质,体现了二氧化硫的漂白性;
B、红棕色褪去的原因是:溴水是红棕色,SO2和Br2、H2O反应,是二氧化硫的还原性,不是二氧化硫的漂白性;
C、红色褪去的原因是:原溶液变红是氢氧化钠的原因,二氧化硫气体和氢氧化钠发生反应后生成了亚硫酸钠,在溶液中亚硫酸钠水解显碱性很弱,不会使酚酞变红,体现了酸性氧化物SO2的性质;
D、紫红色是高锰酸根离子的颜色,通入二氧化硫气体溶液褪色是二氧化硫把高锰酸根还原为无色的锰离子;A、二氧化硫的漂白性使有机色素褪色,品红是有机色素的溶液,所以A中褪色是二氧化硫的漂白性,故A正确;
B、二氧化硫气体通入溴水中发生氧化还原反应SO2+Br2+2H2O=H2SO4+2HBr,红棕色退去,体现了二氧化硫的还原性,故B错误;
C、氢氧化钠的酚酞混合溶液呈红色,SO2通入后发生反应SO2+2NaOH=Na2SO3+H2O,消耗掉氢氧化钠,红色退去,是酸性氧化物的性质,故C错误;
D、高锰酸钾溶液本身呈紫红色,通入二氧化硫气体,发生氧化还原反应,高锰酸钾把二氧化硫氧化,本身被还原为无色锰离子,体现二氧化硫的还原性,故D错误;
故选A.点评:
本题考点: 二氧化硫的化学性质.
考点点评: 本题考查了二氧化硫的还原性、漂白性、酸性氧化物的化学性质,注意利用物质或离子的颜色及发生的化学反应来分析判断.1年前查看全部
- 请问哪些物质具有漂白性(高中化学)
请问哪些物质具有漂白性(高中化学)
请问SO2使品红溶液褪色算是漂白性吗? 那村夫1年前3
那村夫1年前3 -
 cimbadboys 共回答了15个问题
cimbadboys 共回答了15个问题 |采纳率100%强氧化性的物质一般都具有漂白性,比如,氯气,次氯酸,二氧化硫,过氧化钠,双氧水等1年前查看全部
- 次氯酸钠为什么有漂白性?
 linnrainy71年前1
linnrainy71年前1 -
 匿名天使007 共回答了11个问题
匿名天使007 共回答了11个问题 |采纳率90.9%NaClO中ClO-水解生成HClO,所以也有漂白性.
ClO- + H2O <--> HClO + OH-
次氯酸钠具有强氧化性,可以用来用于水的净化,以及作消毒剂、纸浆漂白等.1年前查看全部
- 次氯酸钠与氧化钠是否具有漂白性
 vickyzzi1年前1
vickyzzi1年前1 -
 windlover 共回答了16个问题
windlover 共回答了16个问题 |采纳率81.3%氧化钠没有漂白性.
次氯酸钠本身也没有漂白性,但是溶于水后会生成次氯酸,次氯酸有漂白性.
其实真正起漂白作用的是新生态的氧,次氯酸可以分解成氧和氯化氢,所以具有漂白性1年前查看全部
- 为什么强氧化剂具有漂白性?
 要看流星雨1年前1
要看流星雨1年前1 -
 大大1101 共回答了21个问题
大大1101 共回答了21个问题 |采纳率85.7%只要是有强氧化性的物质就有一定的漂白性,原理是强氧化性的物质的氧化性远远大于有色物质,从而有色物质表现出还原性,被氧化成无色物质了.漂白有三种:(1)氧化 如氯气,高锰酸钾,双氧水 (2)化合 如二氧化硫 (3)吸附 如活性炭1年前查看全部
- 是否具有漂白性的物质都能杀菌消毒?如SO2和次氯酸
 jiacongjian1年前1
jiacongjian1年前1 -
 游客wang 共回答了15个问题
游客wang 共回答了15个问题 |采纳率80%漂白性有两种类型,一种是强氧化性,例如次氯酸,利用强氧化性可以杀菌,另一种是还原性,像二氧化硫,和有色物质生成无色的物质,是不能杀菌的.1年前查看全部
- 还原性 漂白性 氧化性有什么区别?
 hollow_man1年前1
hollow_man1年前1 -
 djp2093 共回答了16个问题
djp2093 共回答了16个问题 |采纳率93.8%还原性是相对于氧化性来说的,能还原别的物质 ,即具有还原性(物质失电子的能力,此时物质的中元素的化合价可以升高
氧化性是指物质得电子的能力.处于高价态的物质一般具有氧化性.
漂白性是可以使得物质的表面的颜色褪变成白色的性质,大多数的漂白性体现的是物质的氧化性,但是有部分的漂白性不是比如二氧化硫的漂白性是由于形成了新的复合物导致的.1年前查看全部
- SO2和Cl2都具有漂白性,若将等物质的量的这两种气体同时作用于潮湿的有色物质,可观察到有色物质( )
SO2和Cl2都具有漂白性,若将等物质的量的这两种气体同时作用于潮湿的有色物质,可观察到有色物质( )
A. 立刻褪色
B. 慢慢褪色
C. 先褪色,后复原
D. 颜色不褪 jinkio1年前1
jinkio1年前1 -
 匪公子 共回答了14个问题
匪公子 共回答了14个问题 |采纳率92.9%解题思路:SO2和Cl2等物质的量混合时,发生SO2+Cl2+2H2O═H2SO4+2HCl,生成物不具有漂白性,则不能使有色的物质褪色.虽SO2和Cl2都具有漂白性,
但等物质的量的这两种气体同时作用于潮湿的有色物质,
发生SO2+Cl2+2H2O═H2SO4+2HCl,
硫酸与盐酸都不具有漂白性,
则不能使有色的物质褪色,
故选D.点评:
本题考点: 二氧化硫的化学性质;氯气的化学性质.
考点点评: 本题考查SO2和Cl2的性质,熟悉物质的性质是解答本题的关键,明确二氧化硫和氯气的反应即可解答,难度不大.1年前查看全部
- 硝酸 NO2有无漂白性THANKS
 lwl98411年前1
lwl98411年前1 -
 afu2008 共回答了17个问题
afu2008 共回答了17个问题 |采纳率94.1%硝酸只有强氧化 ,而没有漂白性.
硝酸应有+5价的N而具有氧化性,那不叫漂白性,浓度越高,氧化性越强.要鉴别的话,通入水中,溴单质与水的混合物,溴单质微溶于水,部分溴会与水反应生成氢溴酸与次溴酸,但仍然会有少量溴单质溶解在水中,所以溴水呈橙黄色,而NO2不会,NO2溶于水,发生反应3NO2+H2O=2HNO3+NO,得到的是HNO3无色溶液.
NO2也无漂白作用,NO2能被氧化,和水反应生成硝酸,硝酸可以和蛋白质发生变色反应,人的手上有水分,遇到NO2就发生了化学反应,变为黄色.1年前查看全部
- 如何验证SO2漂白性?
 终极ll1年前1
终极ll1年前1 -
 linlin121 共回答了19个问题
linlin121 共回答了19个问题 |采纳率94.7%so2通入品红溶液,品红腿色!加热颜色消失!1年前查看全部
- 次氯酸根有漂白性吗?如果有那为什么次氯酸钙不说具有漂白性而是次氯酸?不是只要有次氯酸根就有漂白性吗
 闲云野荷1年前3
闲云野荷1年前3 -
 你能咋地了我 共回答了23个问题
你能咋地了我 共回答了23个问题 |采纳率87%是次氯酸有漂白性,而不是次氯酸根,但是次氯酸不稳定易分解,因此常以次氯酸钙保存.次氯酸钙是固体时没有漂白性,只有溶于水时才具有漂白性.1年前查看全部
- 次氯酸跟有漂白性吗
 老少1年前4
老少1年前4 -
 咣当六小婶儿 共回答了21个问题
咣当六小婶儿 共回答了21个问题 |采纳率90.5%有的.
次氯酸根具有强氧化性.在酸性条件下主要是次氯酸HClO表现强氧化性,氧化漂白;在碱性条件下次氯酸根仍然具有很强的氧化性,氧化漂白.
所以无论酸碱,次氯酸根都具有很强的漂白性.1年前查看全部
- 次氯酸根离子具有漂白性么1.到底是次氯酸根离子具有漂白性 还是次氯酸具有2.那么 次氯酸钠为什么可以使品红退色发生氧化还
次氯酸根离子具有漂白性么
1.到底是次氯酸根离子具有漂白性 还是次氯酸具有
2.那么 次氯酸钠为什么可以使品红退色
发生氧化还原反应为什么就具有漂白性? 快被烦mm了1年前5
快被烦mm了1年前5 -
 ww军 共回答了12个问题
ww军 共回答了12个问题 |采纳率100%1.到底是次氯酸根离子具有漂白性 还是次氯酸具有
---- 次氯酸有漂白性.
----次氯酸根只有转化为次氯酸时,才有漂白性.如,固体漂白粉不能漂白,只有溶于水,才能转化生成次氯酸,才有漂白性.
----判断能否漂白的标准:看有没有次氯酸存在.
2.那么 次氯酸钠为什么可以使品红退色
----次氯酸钠是一个强碱弱酸盐,其溶于水时会发生水解反应
----NaCLO + H2O ==(可逆)==NaOH + HClO
----生成了次氯酸,故能漂白1年前查看全部
- SO2不能使酸碱指示剂(石蕊)褪色?这有漂白性的吧…
SO2不能使酸碱指示剂(石蕊)褪色?这有漂白性的吧…
还有什么气体也不使石蕊褪色? pai1206966241年前1
pai1206966241年前1 -
 mike_chow 共回答了14个问题
mike_chow 共回答了14个问题 |采纳率85.7%二氧化硫的漂白性主要针对于品红,不同于氯气,这不是氧化褪色,而是络合反应,长时间的话品红会恢复原色,不能使石蕊褪色的气体多了,各种非氧化性的气体(氯化氢、氨气、二氧化碳)1年前查看全部
- 化学问题求救关于硫酸脱水性和吸水性,强氧化性.二氧化硫的漂白性,氧化还原性
化学问题求救关于硫酸脱水性和吸水性,强氧化性.二氧化硫的漂白性,氧化还原性
想找些关于浓硫酸硫酸脱水性和吸水性,强氧化性.二氧化硫的漂白性和氧化还原性在实际生活当中的案例!大家多多帮助,我实在没办法! huair_3211年前2
huair_3211年前2 -
 poorer_cdy 共回答了23个问题
poorer_cdy 共回答了23个问题 |采纳率95.7%浓硫酸脱水性:白糖放入其中,变黑,成碳.
浓硫酸吸水性:敞口放置,时间久了,溶液量变多,是因为吸收水蒸气;
此特性用于干燥器
浓硫酸强氧化性:与铜共煮,不发生置换反应,生成二氧化硫,和硫酸铜.
二氧化硫的漂白性:不法商贩用二氧化硫熏白面馒头,使之更白,很诱人的白.
二氧化硫的氧化还原性:与硫化氢反应产生浑浊;二氧化硫通入氯水中,浅黄绿色退去,容易表现强酸特性.1年前查看全部
- 氯水久置后漂白性是否增强
 伍丽云1年前4
伍丽云1年前4 -
 sue_7777 共回答了16个问题
sue_7777 共回答了16个问题 |采纳率87.5%氯水之所以有漂白性那是因为溶液中溶有次氯酸,次氯酸具有强氧化性,能使红色布条褪色,但在久置后会分解生成盐酸和氧气,因此漂白性自然会减弱,所以氯水要在阴凉干燥处保存或现用现配,明白了吗?不明白可以继续问.1年前查看全部
- 为什么氯水不是无色的? 氯水中有氯气和次氯酸,因为溶有氯气所以呈黄绿色,而次氯酸不是有漂白性,为什么氯水不是无色的?
 cfqtree1年前3
cfqtree1年前3 -
 LI3344 共回答了23个问题
LI3344 共回答了23个问题 |采纳率95.7%因为氯水中溶解了少量的氯气,氯气能溶于水,1:2溶解,氯气有黄绿色,氯水显浅黄绿色.
次氯酸的强氧化性漂白对本身就是强氧化性的cl2来说无影响.1年前查看全部
- 高中化学中哪些物质具有漂白性?(包括无机物和有机物)
高中化学中哪些物质具有漂白性?(包括无机物和有机物)
如题. 绽放的美1年前4
绽放的美1年前4 -
 tanhyl 共回答了18个问题
tanhyl 共回答了18个问题 |采纳率83.3%强氧化性漂白:原理将有色物质氧化成无色物质,所以漂白剂都是强氧化剂
如:H2O2,Na2O2,O3,HClO,NaClO,Ca(ClO)2(漂白粉的有效成分)
吸附型漂白:利用物理吸附的xingzhi,将色素吸附,而脱色,是物理变化
如:活性炭,氢氧化铝胶体
还有一种就是化合型漂白:只介绍了SO2,是将有色物质化合成无色的物质,同理该物质分解可以返回原色,如书本摆放的时间长,会变黄,就是这个原因.
高中的实验是 SO2漂白品红溶液,褪色后加热返回红色.
考点:SO2不能与氧化性的漂白剂混用,SO2中+4价硫有还原性,会氧化还原反应,都失去漂白性质.1年前查看全部
- 物质具有漂白性与强氧化性之间有什么关系?
 羯飞1年前1
羯飞1年前1 -
 kotralee 共回答了17个问题
kotralee 共回答了17个问题 |采纳率94.1%漂白有氧化漂白和吸附漂白,即化学和物理漂白,这样就知道了吧!1年前查看全部
- 高中化学漂白作用石蕊 酚酞 和品红都是有机色素吧,SO2具有漂白性,可以使品红褪色,但为什么不能使酚酞和石蕊褪色啊?只能
高中化学漂白作用
石蕊 酚酞 和品红都是有机色素吧,SO2具有漂白性,可以使品红褪色,但为什么不能使酚酞和石蕊褪色啊?只能使它们变色?
如果可以的话,希望能给我详细讲下,在次谢谢! Boyplunger1年前5
Boyplunger1年前5 -
 yygszhy 共回答了18个问题
yygszhy 共回答了18个问题 |采纳率100%二氧化硫的氧化性太弱了!只能品红氧化成一种不移定的显色基团!这种显色基团受热易分解!但由于其他两种显色其团稳定以二氧化硫的氧化性还未能将其显色1年前查看全部
- 过氧化钠具有漂白性是因为过氧化钠能与水反应生成的氢氧化钠为强碱.为什么这句话不正确?
过氧化钠具有漂白性是因为过氧化钠能与水反应生成的氢氧化钠为强碱.为什么这句话不正确?
过氧化钠具有漂白性是因为过氧化钠能与水反应生成的氢氧化钠为强碱.
为什么这句话不正确? 海英街1年前4
海英街1年前4 -
 爱猪一生 共回答了13个问题
爱猪一生 共回答了13个问题 |采纳率84.6%NaOH,没有漂白性,但是生成的H2O2具有比较强烈的氧化性,应该为H2O2的原因.但是现在的解释只要是说Na2O2具有氧化性的原因和H2O2具有氧化性的原因.这些都和NaOH 无关!1年前查看全部
- (2008•唐山二模)某学生课外活动小组为了证明和比较二氧化硫和氯气的漂白性,设计了如图所示的实验装置.
(2008•唐山二模)某学生课外活动小组为了证明和比较二氧化硫和氯气的漂白性,设计了如图所示的实验装置.
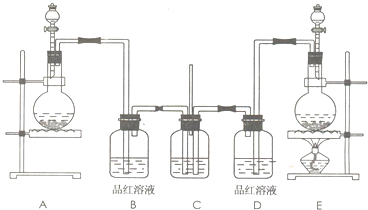
请回答下列问题:
(1)实验室制取氯气的化学方程式为MnO2+4HCl
MnCl2+Cl2↑+2H2O△ .MnO2+4HCl.
MnCl2+Cl2↑+2H2O△ .
(2)实验室常用浓硫酸与亚硫酸钠固体反应制取二氧化硫,则其反应装置为上图中的______(填写字母代号),不用稀硫酸与亚硫酸钠溶液制取二氧化硫的理由是______.
(3)装置C中试剂的名称及作用是______.
(4)反应开始后,发现B、D两个装置中的品红溶液都褪色.请设计一个简单实验,证明二氧化硫和氯气漂白品红溶液的原理不同,实验方法、预期的现象和结论为______.
(5)若将B、D装置中的品红溶液换为滴有酚酞的氢氧化钠溶液,反应一段时间后,B、D中的现象是______.
(6)实验结束后,经检验,发现装置C中的溶液呈碱性,并且含有SO42-.试写出C中生成的离子方程式(有多种可能,只写出一个即可)______. 风之子2161年前1
风之子2161年前1 -
 奇幻喵豆豆 共回答了19个问题
奇幻喵豆豆 共回答了19个问题 |采纳率68.4%解题思路:(1)实验室中用二氧化锰和浓盐酸加热来制取氯气;
(2)二氧化硫易溶于水,在制取过程中不能使用溶液,选择固体和液体不加热制气体的装置即可;
(3)二氧化硫有毒,要用氢氧化钠进行尾气处理;
(4)二氧化硫和氯气漂白品红溶液的原理不同:二氧化硫是因为和有机色质结合而褪色,氯气因为具有氧化性而使有色物质褪色;
(5)酚酞到碱性溶液便显示红色,根据物质的性质来回答;
(6)氯气以及次氯酸根离子都具有氧化性,能将还原性的离子氧化,据此书写方程式.(1)实验室中用二氧化锰和浓盐酸加热来制取氯气,反应原理为:MnO2+4HCl
△
.
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl
△
.
MnCl2+Cl2↑+2H2O;
(2)二氧化硫易溶于水,在制取过程中不能使用溶液,用浓硫酸与亚硫酸钠固体反应制取二氧化硫,应该选择固体和液体不加热制气体的装置即可,故答案为:A;二氧化硫易溶于水;
(3)二氧化硫、氯气都有毒,要用氢氧化钠进行尾气处理,所以装置C中试剂是氢氧化钠,作用是进行尾气处理,故答案为:氢氧化钠溶液,吸收尾气中的氯气和二氧化硫;
(4)二氧化硫和氯气漂白品红溶液的原理不同:二氧化硫是因为和有机色质结合而褪色,加热后会恢复原来的红色,但是氯气因为具有氧化性而使有色物质褪色,加热颜色不会复原,故答案为:分别取少量褪色后的溶液于试管中,用酒精灯加热,经二氧化硫漂白的品红溶液恢复红色,说明二氧化硫和品红结合成不稳定的物质,经氯气漂白的品红溶液不会变红,说明氯气将品红溶液氧化褪色;
(5)酚酞到碱性溶液便显示红色,将B、D装置中的品红溶液换为滴有酚酞的氢氧化钠溶液,因为氯气和二氧化硫都可以和氢氧化钠反应,所以B、D装置的红色都退去,故答案为:B、D装置的红色都退去;
(6)氯气和次氯酸根离子都具有氧化性,能够将还原性的离子亚硫酸根离子氧化为硫酸根离子,在碱性环境下,可能发生的方程式为:Cl2+SO2+4OH-=SO42-+2Cl-+2H2O、ClO-+SO32-=SO42-+Cl-,故答案为:Cl2+SO2+4OH-=SO42-+2Cl-+2H2O(或ClO-+SO32-=SO42-+Cl-).点评:
本题考点: 性质实验方案的设计.
考点点评: 本题是一道关于化学实验方案的设计题,考查学生分析和解决问题的能力,综合性强,难度大.1年前查看全部
- 化学 so2使品红溶液褪色,为什么说明它有漂白性,不是是因为亚硫酸跟品红结合么?
 zzb_hz1年前2
zzb_hz1年前2 -
 123872302 共回答了13个问题
123872302 共回答了13个问题 |采纳率84.6%这也是漂白性的一种1年前查看全部
- 证明KMNO4溶液褪色是因为SO2有还原性而不是漂白性
 狗屁不通1年前1
狗屁不通1年前1 -
 doneychow 共回答了25个问题
doneychow 共回答了25个问题 |采纳率88%加热后不恢复紫红色.因为SO2漂白性是生成不稳定的亚硫酸化合物,加热会分解1年前查看全部
- 二氧化硫的化学性质,用方程式说明,除漂白性以外,急,急·····
 zty03161年前2
zty03161年前2 -
 BiGtaiLfiSh 共回答了17个问题
BiGtaiLfiSh 共回答了17个问题 |采纳率100%化学性质
二氧化硫可以在硫磺燃烧的条件下生成
S(s) + O2(g) → SO2(g)
硫化氢可以燃烧生成二氧化硫
2H2S(g) + 3O2(g) → 2H2O(g) + 2SO2(g)
加热硫铁矿,闪锌矿,硫化汞,可以生成二氧化硫
4FeS2(s) + 11O2(g) → 2Fe2O3(s) + 8SO2(g)
2ZnS(s) + 3O2(g) → 2ZnO(s) + 2SO2(g)
HgS(s) + O2(g) → Hg(g) + SO2(g)1年前查看全部
- 下列物质都具有漂白性,其中一种与其它物质的漂白原理不相同,这种物质是 A. HClO B. H 2 O 2 C. O 3
下列物质都具有漂白性,其中一种与其它物质的漂白原理不相同,这种物质是
A. HClO B. H 2 O 2 C. O 3 D. SO 2  符熙敏1年前1
符熙敏1年前1 -
 有害书籍爱好者 共回答了13个问题
有害书籍爱好者 共回答了13个问题 |采纳率92.3%D
1年前查看全部
- 二氧化硫具有漂白性还是亚硫酸具有漂白性
二氧化硫具有漂白性还是亚硫酸具有漂白性
为什么书上都说是二氧化硫的漂白性,漂白的原理是二氧化硫和有色物质结合成不稳定的化合物,这个不稳定的物质是什么? king865501年前2
king865501年前2 -
 vivianfighting 共回答了16个问题
vivianfighting 共回答了16个问题 |采纳率87.5%高中教材上认为是SO2具有漂白性,殊不知本质是HSO3-/SO32-参与反应.诸多实验现象证明了这个观点.
不稳定物质是品红与H2SO3发生加成,再脱去一分子水得到的产物,加热条件下又水解成品红和H2SO3,并分解成SO2和H2O1年前查看全部
- 二氧化硫和氯气放在一起漂白性为什么会减弱?
二氧化硫和氯气放在一起漂白性为什么会减弱?
知道反应的方程式吗? csempty1年前3
csempty1年前3 -
 向左走向右走6 共回答了18个问题
向左走向右走6 共回答了18个问题 |采纳率100%因为他们反应,SO2 + Cl2 + 2H2O = H2SO4 + 2HCl1年前查看全部
- Cl2使蘸有Naoh的ph试纸退色的主要原因,具因为和NaOH发生了反应还是因为生成的HCLO具有漂白性?为什么?
 谜失的永恒1年前2
谜失的永恒1年前2 -
 kfyu_001 共回答了17个问题
kfyu_001 共回答了17个问题 |采纳率82.4%是漂白的作用,因为是褪色了,不是变色了
如果说是变色了,到可能是反应了NaOH,因为碱性变弱了嘛,但是褪色的话就是显色物质不见了,就是被氧化了1年前查看全部
- 等物质的量的SO2与Cl2气体与水反应,为什么会失去漂白性?请写出所有反应方程式及其合反应
等物质的量的SO2与Cl2气体与水反应,为什么会失去漂白性?请写出所有反应方程式及其合反应
我现在就是搞不懂他们是怎样反应的,请各位大大别只写个总反应方程式好不好?在此拜谢各位 kjjuventus1年前3
kjjuventus1年前3 -
 mfkihdx 共回答了16个问题
mfkihdx 共回答了16个问题 |采纳率100%SO2会和有机物结合而漂白,Cl2会氧化有色物质而漂白
如果1:1再加水混合.
SO2 + Cl2 + 2H2O = 2HCl + H2SO4
生成HCl和H2SO4都不具有漂白性
这并非总反应式,这就是一个单独的反应.SO2和氯气溶解在水中,SO2你可以把它看做亚硫酸,也可以就看做SO2,氯气将其氧化成硫酸,自己被还原成了HCl.1年前查看全部
- SO2有漂白性,那么湿润的SO2有没有漂白性?
SO2有漂白性,那么湿润的SO2有没有漂白性?
亚硫酸有没有漂白性?与HClO和SO2的有没有区别? reina_sun1年前2
reina_sun1年前2 -
 3232t 共回答了24个问题
3232t 共回答了24个问题 |采纳率87.5%二氧化硫主要是与反应物结合生成不稳定的化合物.而相对它的水溶液和亚硫酸盐主要是还原作用与氧化性物质反应而退色.比如和高锰酸钾反应.前一种是可逆的,后一种不可以.次氯酸是靠它的氧化作用来完成漂白的.与前面两种都不一样.1年前查看全部
- 浓硝酸或稀纸硝酸加到蓝色石蕊试纸上有什么现象?它们有漂白性吗
 爱你的腚1年前1
爱你的腚1年前1 -
 dsfasfasdfsdafsa 共回答了15个问题
dsfasfasdfsdafsa 共回答了15个问题 |采纳率80%浓硝酸加到蓝色石蕊试纸上,试纸先变红后褪色;
稀硝酸加到蓝色石蕊试纸上,试纸变红.
浓硝酸使试纸褪色,靠其强氧化性,也可称为漂白性,因腐蚀性强,不用作漂白剂1年前查看全部
- (共14分)某中学化学实验小组为了证明和比较SO 2 和氯水的漂白性,设计了如下装置:
(共14分)某中学化学实验小组为了证明和比较SO 2 和氯水的漂白性,设计了如下装置:

(1)实验室常用装置E制各Cl 2 ,写出该反应的离子方程式__________________________指出该反应中浓盐酸所表现出的性质
(2)反应开始后,发现B、D两个容器中的品红溶液都褪色,停止通气后,给B、D两个容器加热,两个容器中的现象分别为:B D
(3)装置C的作用是
(4)该实验小组的甲、乙两位同学利用上述两发生装置按下图装置继续进行实验:
通气一段时间后,甲同学实验过程中品红溶液几乎不褪色,而乙同学的实验现象是品红溶液随时间的推移变得越来越浅。试根据该实验装置和两名同学的实验结果回答问题。
①试分析甲同学实验过程中,品红溶液不褪色的原因是: 。(用离子方程式进行说明)
②你认为乙同学是怎样做到让品红溶液变得越来越浅的? 又圆又扁常德米粉1年前1
又圆又扁常德米粉1年前1 -
 feizi888 共回答了13个问题
feizi888 共回答了13个问题 |采纳率92.3%1年前查看全部
- 二氧化硫使品红褪色是利用的他漂白性还是还原性 说具体点.
 牧歌的薄荷糖1年前3
牧歌的薄荷糖1年前3 -
 神鼎周四阿 共回答了22个问题
神鼎周四阿 共回答了22个问题 |采纳率100%漂白性,二氧化硫和色素分子结合成分子间无色化合物,使得品红褪色,所以加热可以恢复品红的红色.1年前查看全部
- 下列变化中可以说明SO2具有漂白性的是( )
下列变化中可以说明SO2具有漂白性的是( )
A.SO2通入橙红色的溴水中(和氯水相似),红色褪去
B.SO2通入硫酸酸化的高锰酸钾溶液中,紫红色褪去
C.SO2通入品红溶液中,红色褪去;加热后红色恢复
D.SO2通入滴有酚酞的氢氧化钠溶液中,红色褪去 lihao198570161年前1
lihao198570161年前1 -
 Tspeng 共回答了16个问题
Tspeng 共回答了16个问题 |采纳率100%解题思路:A、红棕色褪去的原因是:溴水是红棕色,SO2和Br2、H2O反应,是二氧化硫的还原性,不是二氧化硫的漂白性;
B、紫红色是高锰酸根离子的颜色,通入二氧化硫气体溶液褪色是二氧化硫把高锰酸根还原为无色的锰离子;
C、红色褪去的原因是:二氧化硫和水反应生成的亚硫酸和有机色素品红结合成不稳定的无色物质,加热不稳定的物质分解恢复原来的眼神,体现了二氧化硫的漂白性;
D、红色褪去的原因是:原溶液变红是氢氧化钠的原因,二氧化硫气体和氢氧化钠发生反应后生成了亚硫酸钠,在溶液中亚硫酸钠水解显碱性很弱,不会使酚酞变红,体现了酸性氧化物SO2的性质.A、二氧化硫气体通入溴水中发生氧化还原反应SO2+Br2+2H2O=H2SO4+2HBr,红棕色退去,体现了二氧化硫的还原性,故A不选;
B、高锰酸钾溶液本身呈紫红色,通入二氧化硫气体,发生氧化还原反应,高锰酸钾把二氧化硫氧化,本身被还原为无色锰离子,体现二氧化硫的还原性,故B不选;
C、二氧化硫的漂白性使有机色素褪色,品红是有机色素的溶液,所以褪色是二氧化硫的漂白性,故C选;
D、氢氧化钠的酚酞混合溶液呈红色,SO2通入后发生反应SO2+2NaOH=Na2SO3+H2O,消耗掉氢氧化钠,红色退去,是酸性氧化物的性质,故D不选;
故选C.点评:
本题考点: 二氧化硫的化学性质.
考点点评: 本题考查了二氧化硫的还原性、漂白性、酸性氧化物的化学性质,注意利用物质或离子的颜色及发生的化学反应来分析解答.1年前查看全部
- 下列叙述正确的是( )A.将二氧化硫气体通入浅黄色的溴水中使其颜色褪去,说明二氧化硫具有漂白性B.SiO2为酸性氧化物
下列叙述正确的是( )
A.将二氧化硫气体通入浅黄色的溴水中使其颜色褪去,说明二氧化硫具有漂白性
B.SiO2为酸性氧化物,故不能与任何酸发生化学反应
C.用砂纸打磨过的铝箔放在酒精灯焰上不燃烧,说明铝不易与O2反应
D.FeCl2、SO2、NO、Fe(OH)3四种物质都可以直接通过化合反应制取 深圳孤独男孩1年前1
深圳孤独男孩1年前1 -
 回首一片风雨飘摇 共回答了21个问题
回首一片风雨飘摇 共回答了21个问题 |采纳率85.7%解题思路:A、二氧化硫和溴单质发生氧化还原反应,二氧化硫的漂白作用具有选择性;
B、二氧化硅和氢氟酸反应;
C、依据金属的活泼性分析判断,铝易于氧气发生反应;
D、依据在性质和特征反应分析判断.A、二氧化硫和溴单质发生氧化还原反应,二氧化硫的漂白作用具有选择性;将二氧化硫气体通入浅黄色的溴水中使其颜色褪去,说明二氧化硫具有还原性,故A错误;B、SiO2为酸性氧化物,和氢氟酸酸发生化学反应,SiO2+4HF=...
点评:
本题考点: 二氧化硫的化学性质;硅和二氧化硅;铝的化学性质.
考点点评: 本题是一道有关物质性质的综合题,考查角度广,难度不大,要求学生熟悉教材知识,学以致用.1年前查看全部
- 漂白粉溶液在空气中放置一段时间后漂白性增强的原因
 X女孩1年前2
X女孩1年前2 -
 8ddj 共回答了17个问题
8ddj 共回答了17个问题 |采纳率100%由于HCIO的酸性比H2CO3的酸性弱,根据强酸制弱酸原理,漂白粉溶液的ClO-可以结合H2CO3电离出来的H+形成HClO,方程式如下:
Ca(ClO)2 +CO2 +H20 ===CaCO3↓+2HClO1年前查看全部
大家在问
- 1在直角坐标系内,满足不等式x2-y2≥0的点(x,y)的集合(用阴影表示)是 2是平方
- 2已知直线L过点P(-3,4),若直线于X轴负半轴,Y轴正半轴分别交A,B两点,试求三角形OAB的最小值及此时L直线的方程
- 3先化简,再求值:5x²-[2xy-3(1/3xy+2)+4x²]求过程和答案,
- 4天黑了星星一定会有吗?..
- 5英文翻译:我是一个不回家的人
- 6用3个2,1个0和一个小数点,写出所有只读出一个零的小数
- 7已知集合A=﹛x│-1≤x<3﹜,B=﹛x│2x-4≥x-2﹜
- 8英语选择题求问题目:i've___heard of him,but i don'tknow who he is.a.so
- 9求一本训练高中语文基础知识的练习,改病句,拼音,改错,词语的运用啊,主要针对高考的前4道基础题
- 101-2+3-4+5-6+7...+99-100+101=多少
- 11指出下列句子中引号的作用.A.表引用 B表特殊称谓C.表强调D着重指出1:“修理”这个词怎么拼写?2:我拨通了“问讯处”
- 12Father likes fishing is his
- 13将72/45,48/40,44/12,12/16,15/18,24/56,化成最简分数(带分数)
- 14比较4a和-4a的大小.
- 15按题目要求作图. (1)在图1中的“O”内填上合适的电表,使合上开关两个小灯都能发光.(2)一个照明用的灯具如

