用量子数n,l和m对原子核外n=4的所有可能的原子轨道分别进行描述\x0c还有就是用四个量子数nlmms对原子核外n=3
 laikanba2022-10-04 11:39:541条回答
laikanba2022-10-04 11:39:541条回答表述的方法?

已提交,审核后显示!提交回复
共1条回复
 山东鸢都义工 共回答了26个问题
山东鸢都义工 共回答了26个问题 |采纳率84.6%- 楼主湖大的吧
- 1年前
相关推荐
- 一群氢原子处于量子数n=4能级状态,氢原子的能级示意图如图所示,那么
 一群氢原子处于量子数n=4能级状态,氢原子的能级示意图如图所示,那么
一群氢原子处于量子数n=4能级状态,氢原子的能级示意图如图所示,那么
①氢原子可能发射______种频率的光子.
②氢原子由量子数n=4的能级跃迁到n=2的能级时辐射光子的频率是______Hz,用这样的光子照射右表中,金属______能发生光电效应,发生光电效应时,发射光电子的最大初动能是______eV.(普朗克常量h=6.63×10-34J•s,1eV=1.6×10-19J)
几种金属的逸出功
金属 铯 钙 镁 钛 逸出功W/eV 1.9 2.7 3.7 4.1  那边岸芷汀兰1年前1
那边岸芷汀兰1年前1 -
 唯有泪干行 共回答了17个问题
唯有泪干行 共回答了17个问题 |采纳率94.1%解题思路:(1)根据数学组合公式
求出氢原子可能发射不同频率光子的种数;C 2n
(2)根据Em-En=hv求出辐射光子的频率,结合光电效应的条件,判断能使哪种金属发生光电效应,结合光电效应方程求出最大初动能.(1)根据
C24=6知,氢原子可能发射6种不同频率的光子.
(2)根据E4-E2=hv知,辐射的光子频率v=
E4−E2
h=
(3.40−0.85)×1.6×10−19
6.63×10−34Hz=6.15×1014Hz,
辐射的光子能量为2.55eV,可知可以使金属铯发生光电效应.根据光电效应方程知,最大初动能Ekm=hv-W0=2.55-1.9eV=0.65eV.
故答案为:(1)6,(2)6.15×1014Hz,铯,0.65.点评:
本题考点: 氢原子的能级公式和跃迁.
考点点评: 解决本题的关键知道能级间跃迁所满足的规律,以及知道光电效应的条件,掌握光电效应方程.1年前查看全部
- 根据玻尔理论,在氢原子中,量子数n越大,则( )
根据玻尔理论,在氢原子中,量子数n越大,则( )
A. 电子轨道半径越小
B. 核外电子运动速度越大
C. 原子能量越大
D. 电势能越小 pigu9111年前2
pigu9111年前2 -
 zhouxiang123 共回答了27个问题
zhouxiang123 共回答了27个问题 |采纳率88.9%解题思路:在氢原子中,量子数n越大,轨道半径越大,根据库仑引力提供向心力,判断核外电子运动的速度的变化,从而判断出电子动能的变化,根据能量的变化得出电势能的变化.在氢原子中,量子数n越大,电子的轨道半径越大,
根据
ke2
r2=m
v2
r知,r越大,v越小,则电子的动能减小.
因为量子数增大,原子能级的能量增大,动能减小,则电势能增大.故C正确,A、B、D错误.
故选C.点评:
本题考点: 玻尔模型和氢原子的能级结构.
考点点评: 解决本题的关键知道量子数越大,轨道半径越大,原子能级的能量越大,以及知道原子能量等于电子动能和势能的总和.1年前查看全部
- 在量子数为4的电子层中,能容纳的最多电子数是?A.18 B.24 C.32 D.36
 xingxing2qiqi1年前1
xingxing2qiqi1年前1 -
 283805051小山 共回答了16个问题
283805051小山 共回答了16个问题 |采纳率100%C1年前查看全部
- 已知氢原子基态的电子轨道为r1=0.528×10-10m,量子数为n的能级值为En=-[13.6n2ev
 已知氢原子基态的电子轨道为r1=0.528×10-10m,量子数为n的能级值为En=-[13.6
已知氢原子基态的电子轨道为r1=0.528×10-10m,量子数为n的能级值为En=-[13.6n2  又是细雨1年前0
又是细雨1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 量子数为n,l的支壳层中可容纳的电子数为多少
 熏色眼角1年前2
熏色眼角1年前2 -
 wcsnzy 共回答了17个问题
wcsnzy 共回答了17个问题 |采纳率94.1%n是主量子数,如n=1是K层
n层有n^2个电子轨道
l为角量子数如l=0是s轨道
有(l+1)^2-l^2个电子亚层
所以可容纳4l+2个电子1年前查看全部
- 四个量子数之间存在什么关系?
 chinsung1年前1
chinsung1年前1 -
 游走的鱼2007 共回答了15个问题
游走的鱼2007 共回答了15个问题 |采纳率93.3%量子力学在推导原子中电子的运动状况时会出现这四个量子数.
n是主量子数,它对电子能量的影响通常是最大的.它主要就表示电子距离原子核的“平均距离”的远近,越远,n越大,相应的能量也越大.n等于电子绕核一周所对应的物质波的波数——绕核一周有n个波长的电子的物质波.n可能的取值为所有正整数.
l是轨道量子数,它表示电子绕核运动时角动量的大小,它对电子的能量也有较大的影响.l可能的取值为小于n的所有非负整数——l=0、1……n-2、n-1.
m是磁量子数,在有外加磁场时,电子的轨道角动量在外磁场的方向上的分量不是连续的,也是量子化的,这个分量的大小就由m来表示.m可能的取值为所有绝对值不大于l的整数——m=-l、-l+1……0……l-1、l.
ms是自旋量子数,它对应着电子的自旋的角动量的大小和方向,它只有正负1/2这两个数值,这表示电子自旋的大小是固定不变的,且只有两个方向——每个m都对应2个ms值正负1/2.1年前查看全部
- 现有1500个氢原子被激发到量子数为4的能级上,若这些受激发的氢原子最后都回到基态,则在此过程中发出的光子总数是(假定处
现有1500个氢原子被激发到量子数为4的能级上,若这些受激发的氢原子最后都回到基态,则在此过程中发出的光子总数是(假定处在量子数为n的激发态的氢原子跃迁到各较低能级的原子数都是处在该激发态能级上的原子总数的[1/n−1])( )
A.2 200
B.2500
C.2750
D.2 400 bravechen771年前1
bravechen771年前1 -
 ll柄杀 共回答了13个问题
ll柄杀 共回答了13个问题 |采纳率100%解题思路:根据题意分别求出n=4跃迁到n=3、n=2、n=1的光子总数,以及n=3跃迁到n=2、n=1的光子总数、n=2跃迁到n=1的光子总数,从而求出所有的光子总数.根据题中所给信息,处在量子数为4的激发态的氢原子跃迁到各较低能级的原子数都是处在该激发态能级上的原子总数的[1/3],
即向量子数为2、3的激发态和基态各跃迁1500×[1/3]=500个,发出光子500×3=1500个;
同理,处在量子数为3的激发态的500个氢原子跃迁到量子数为2的激发态和基态的原子数都是500×[1/2]=250个,
发出光子250×2=500个;
处在量子数为2的激发态的500+250=750个氢原子跃迁到基态的原子数是750×1=750个,发出光子750个.
所以在此过程中发出的光子总数为n=1500+500+750=2750个.故C正确,A、B、D错误.
故选:C.点评:
本题考点: 氢原子的能级公式和跃迁.
考点点评: 本题属于信息题,关键能够从题目中挖出信息,抓住处在量子数为n的激发态的氢原子跃迁到各较低能级的原子数都是处在该激发态能级上的原子总数的[1/ n−1]进行求解.1年前查看全部
- 现有1200个氢原子被激发到量子数为4的能级上,若这些受激氢原子最后都回到基态,则在此过程中发出的光子总数是多少?假设处
现有1200个氢原子被激发到量子数为4的能级上,若这些受激氢原子最后都回到基态,则在此过程中发出的光子总数是多少?假设处在量子数为n的激发态的氢原子跃迁到各较低能级的原子数都是处在该激发态能级上的原子总数的
 。
。A.2200 B.2000 C.1200 D.2400  wandai20051年前1
wandai20051年前1 -
 版主的vv 共回答了9个问题
版主的vv 共回答了9个问题 |采纳率66.7%1年前查看全部
- (1)已知金属钙的逸出功为2.7eV,氢原子的能级图如图A所示,一群氢原子处于量子数n=4能级状态,则______
(1)已知金属钙的逸出功为2.7eV,氢原子的能级图如图A所示,一群氢原子处于量子数n=4能级状态,则______
A.氢原子可能辐射6种频率的光子
B.氢原子可能辐射5种频率的光子
C.有3种频率的辐射光子能使钙发生光电效应
D.有4种频率的辐射光子能使钙发生光电效应
(2)质量为m1=1.0kg和m2(未知)的两个物体在光滑的水平面上正碰,碰撞时间不计,其x~t (位移-时间) 图象如图B所示,试通过计算回答下列问题
①m2等于多少千克?
②碰撞过程是弹性碰撞还是非弹性碰撞?
 jamsjian1年前0
jamsjian1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 已知氢原子的电子轨道半径r1=5.3×10-9m,基态能量E1=-13.6eV,量子数n的能级值En=[1n2E1,静电
已知氢原子的电子轨道半径r1=5.3×10-9m,基态能量E1=-13.6eV,量子数n的能级值En=[1
n2  zhaoming821年前1
zhaoming821年前1 -
 想生的猫 共回答了23个问题
想生的猫 共回答了23个问题 |采纳率91.3%解题思路:1、根据库仑引力提供向心力求出电子在基态轨道上运动的速率,再求出动能
2、根据高能级跃迁到低能级画图
3、波长最短,即频率最大,能级间发生跃迁时吸收或辐射的光子能量等于两能级间的能级差.(1)根据库仑引力提供向心力得
ke2
r20=m
v2
r0,
则
1/2]mv2=[1/2]
ke2
r0=13.6ev
(2)氢原子最多能发出3种光谱线;画一能级图,
(3)根据λ=[c/γ],当λ最小,频率最大.
n=1到n=3,λ=
hc
E3−E1=1.03×10-7 m
答:(1)电子在基态轨道上运动的动能是13.6eV;
(2)氢原子最多能发出3种光谱线;
(3)波长最短的一条谱线波长是1.03×-7m.点评:
本题考点: 爱因斯坦质能方程.
考点点评: 解决本题的关键知道能级间跃迁所满足的规律,即Em-En=hv.1年前查看全部
- 玻尔氢原子理论应用题根据玻尔氢原子理论,试计算氢原子中电子在量子数为n的轨道上作圆周运动的频率.
 两月Y头1年前1
两月Y头1年前1 -
 262726 共回答了25个问题
262726 共回答了25个问题 |采纳率96%设电子在量子数为n轨道上作圆周运动的线速度为v,半径为r,则可知
mv^2/r=e^2/4πε0r^2
再应用玻尔角动量量子化条件
L=mvr=nh(h是约化普朗克常量不是普朗克常量)
联立两式,可解得
v=e^2/4πε0nh
r=4πε0n^2h^2/me^2
得ω=v/r=me^4/16π^2ε0^2n^3h^3
∴υ=ω/2π=me^4/32π^3ε0^2n^3h^31年前查看全部
- 基态K(Z = 19)原子最外层电子的四个量子数为
 bmom1年前1
bmom1年前1 -
 牛牛便利店 共回答了14个问题
牛牛便利店 共回答了14个问题 |采纳率92.9%4,0,0,(+/-)1/21年前查看全部
- 关于无机化学的四个量子数RT,我搞不清怎样用四个量子数描述原子轨道啊?(主量子数n,角量子数l,磁量数m,自旋量子数ms
关于无机化学的四个量子数
RT,我搞不清怎样用四个量子数描述原子轨道啊?(主量子数n,角量子数l,磁量数m,自旋量子数ms),望高手打救,最好有例子说明, ranfly1年前1
ranfly1年前1 -
 coffecat1119 共回答了20个问题
coffecat1119 共回答了20个问题 |采纳率90%你是学无机的吧,呵呵
量子数是由于要描述微观粒子波粒二象性运动规律的时候引入的概念.与此同时,量子力学诞生.它的基本方程式薛定谔方程,由于我的电脑不好编辑此公式,你可以在下面的链接中看一下,对它有个基本了解.http://baike.baidu.com/view/551078.html?wtp=tt
由薛定谔方程可以看出来,它很好的把体现微观例子的粒子性(m、E、V和坐标等)于波动性Ψ(r)融合在一起,从而能更真实的反映出微观粒子的运动状态.
在不同的条件下可以解出E(势能)和Ψ(波函数),由于薛定谔方程是一个二阶偏微分方程,我们没有那么高深的数学功底可以解出来,我学的时候老师只是把重点放在定性介绍和图示补充说明上面.
波函数是用不同量子数(n、l、m)来表征的,在解薛定谔方程的时候引入了这三种量子数,主量子数n、角量子数l、磁量子数m.或者说只有引入了这三种量子数,才能从薛定谔方程解出有意义的E解来.量子数与原子能量、原子轨道和电子云都有关系,这种关系是:
1、 主量子数n规定着电子出现最大概率区域离核的远近,以及原子能量的高低
代表不同电子层(离核远近、能量高低)
可取数值为n=1,2,3,.(任意非零正整数)
2、 角量子数l规定电子在空间角度分布情况,即与电子云形状有关(在多电子院子中也影 响原子能量)
代表在同一电子层不同电子亚层
可取数值为l=0,1,2,.n-1(n个从零开始的正整数)
3、 磁量子数m反映原子轨道在空间的不同伸展方向
代表在同一电子亚层不同的电子轨道
可取数值为m=+l,...0...-l(从+l经过零到-l的整数)
4、 自旋量子数决定着电子的自旋方式,表示电子两种不同的运动状态
可取数值为ms=+1/2或-1/2
例如:n=1,l可取的数值为0,m可取的数值为0,对应的波函数为Ψ1s
n=2,l可取的数值为0和1,m可取的数值为-1、0、1.
n=2,l=0,m=0时波函数为Ψ2s
n=2,l=1,m=0时波函数为Ψ2pz
n=3,l可取的数值为0、1和2,m可取的数值为-2、-1、0、1、2
在得到不同波函数的同事.可得到于这些状态相对应的能量E
不知道对你有没有帮助 ,有问题可以一起探讨,我的QQ是5409150261年前查看全部
- 对任何原子核外某一电子来说,只有四个量子数完全确定后,其能量才有一定值.这句话对吗?.为什么
 左耳的oo1年前1
左耳的oo1年前1 -
 qinyan520 共回答了18个问题
qinyan520 共回答了18个问题 |采纳率94.4%电子能量只取决于主量子数n和角量子数l,与磁量子数和自旋量子数无关.
也就是说,只要前两个量子数确定,电子能量就确定了.1年前查看全部
- 原子机构中电子的四个量子数四个量子书分别为:主量子数n,副量子数l,磁量子数m,自旋量子数ms.各自的意义是否可以这样理
原子机构中电子的四个量子数
四个量子书分别为:主量子数n,副量子数l,磁量子数m,自旋量子数ms.
各自的意义是否可以这样理解:
主量子数:表示电子距离原子核的远近,即在不同的电子层上;
副量子数:在该电子层上的角速度(角速度还不一样吗?)
磁量子数:在该层中,确定的角速度下,运行的方向(x,y,z)
自旋量子数:电子自旋速度.
请问可以这样理解吗? 骑yy上茅房1年前2
骑yy上茅房1年前2 -
 飞行的ee 共回答了19个问题
飞行的ee 共回答了19个问题 |采纳率94.7%主量子数可以说是表示电子离核的平均距离.楼主说得对.
角量子数表示电子轨道运动的角动量的大小,表示电子亚层.s亚层和p亚层的电子轨道运动的角动量是不同的.
磁量子表示电子轨道运动角动量在z轴方向的分量.亦可看成是电子云伸展的方向.
自旋量子数不是代表电子自旋运动角动量的大小.1年前查看全部
- 设在处于基态的氢原子中,电子绕核做匀速圆周运动形成的电流为I,当氢原子处于量子数n=2的激发态时
设在处于基态的氢原子中,电子绕核做匀速圆周运动形成的电流为I,当氢原子处于量子数n=2的激发态时
电子形成的电流为__________ 等待一七六1年前1
等待一七六1年前1 -
 花里八拉大樟树 共回答了20个问题
花里八拉大樟树 共回答了20个问题 |采纳率80%由EK=Ke^2/2r rn=n^2r1 v2=0.5v1 T=2πr/v T2=8T1
I=e/T
I2=I/81年前查看全部
- 关于玻尔理论的问题根据玻尔理论(1)计算氢原子中电子在量子数为n的轨道上作圆周运动的频率(2)计算当该电子跃迁到(n-1
关于玻尔理论的问题
根据玻尔理论
(1)计算氢原子中电子在量子数为n的轨道上作圆周运动的频率
(2)计算当该电子跃迁到(n-1)的轨道上时所发出的光子的频率
(3)证明当n很大时,上述(1)和(2)的结果近似相等 m7pjv1年前2
m7pjv1年前2 -
 二十4桥明月夜 共回答了9个问题
二十4桥明月夜 共回答了9个问题 |采纳率100%给你一个粗略的回答:(下式中 pi 即 3.1415...)
1.电磁吸引力等于向心力:
m*v^2/r = k/r^2 (电荷为1库仑)
=> 频率:v1 = [1/(2pi)]*[(k/m)^1/2]*r^(-3/2)
估计这你推导了,还要用公式:r = n^2* r0 (n---主量子数,r0---氢原子第一轨道半径,是个常量),将此式代入上式:
频率 v = R * n^(-3),R是前面一大堆常量,自己去算,意思是v 与主量子数的-3次方成正比.
2.n能级跃迁到n-1能级
经典理论:n能级总能量,电子动能加电子势能:
E = 1/2*m*v^2 - k/r = 1/2 k/r
又量子假设:E = hv
=> 跃迁频率 v2 = 1/2 k/h* [(n - 1)^(-2) - n^(-2)]
(简记) = C* [n^(-2) - (n-1)^(-2)] (C为上面的常量)
当n很大时,上式的 (n-1)^(-2) - n^(-2) 项
=(2n - 1)/ n^2*(n -1)^2
近似= 2n / n^2*(n -1)^2
近似= 2n / n^4 = n^(-3) (系数 2 提到前边常数项中)
这样当n 很大时
跃迁频率 v2 = S * n^(-3),即与n^(-3)成正比.同情况1.
证毕.
注:(1)过程大致如此,细节上自己去算.
(2)严格比较的话,大概可以得出r0即第一轨道半径公式,可以与标准公式比较一下看看是否一样,标准公式自己查,我记不清了,大概是:
r = n^2*[h(bar)]^2/e^2* me 自己试试1年前查看全部
- N原子中有7个电子,写出各电子的四个量子数.
N原子中有7个电子,写出各电子的四个量子数.
答案我有求讲解.```
`` naicha221年前3
naicha221年前3 -
 loveu365ayear 共回答了11个问题
loveu365ayear 共回答了11个问题 |采纳率90.9%n=1,l=0,m=0,ms=+1/2 ; n=1,l=0,m=0,ms=-1/2
n=2,l=0,m=0,ms=+1/2 ; n=2,l=0,m=0,ms=-1/2
n=2,l=1,m=0,ms=+1/2 ; n=2,l=1,m=-1,ms=+1/2 ; n=2,l=1,m=+1,ms=+1/2
规律:
n=1,2,3,4.
l=0,1,2,3.(n-1)
m=0,(+/-)1,(+/-)2,(+/-)3.(+/-)l
ms=(+/-)1/21年前查看全部
- 已知金属钙的逸出功为2.7eV,氢原子的能级图如图所示,一群氢原子处于量子数n=4能级状态,则( )
 已知金属钙的逸出功为2.7eV,氢原子的能级图如图所示,一群氢原子处于量子数n=4能级状态,则( )
已知金属钙的逸出功为2.7eV,氢原子的能级图如图所示,一群氢原子处于量子数n=4能级状态,则( )
A.使某个该种氢原子电离至少需要13.6 eV的能量
B.使某个该种氢原子电离至少需要0.85 eV的能量
C.只有1种频率的辐射光子能使钙发生光电效应
D.有4种频率的辐射光子能使钙发生光电效应 riverbig1年前1
riverbig1年前1 -
 天下无疆 共回答了16个问题
天下无疆 共回答了16个问题 |采纳率81.3%解题思路:能级间跃迁辐射的光子能量等于两能级间的能级差,可知电离需要的最小能量.当光子的能量大于逸出功时,可以发生光电效应.A、因为放出的光子能量满足hγ=Em-En,知,从n=4能级跃迁到无穷远需要的最小能量为:△E=0-(-0.85 )=0.85 eV.
所以使某个该种氢原子电离至少需要0.85 eV的能量,故A错误,B正确;
C、n=4跃迁到n=3辐射的光子能量为0.66eV,n=3跃迁到n=2辐射的光子能量为1.89eV,n=4跃迁到n=2辐射的光子能量为2.55eV,均小于逸出功,不能发生光电效应,其余3种光子能量均大于2.7eV,所以这群氢原子辐射的光中有3种频率的光子能使钙发生光电效应.故CD错误;
故选:B.点评:
本题考点: 玻尔模型和氢原子的能级结构;氢原子的能级公式和跃迁.
考点点评: 解决本题的关键知道能级间跃迁放出或吸收光子的能量满足hγ=Em-En,注意理解氢原子电离的含义.1年前查看全部
- A元素原子的最外电子层上有2个量子数n=4,l=0的电子,量子数n=3,l=2的轨道上无电
A元素原子的最外电子层上有2个量子数n=4,l=0的电子,量子数n=3,l=2的轨道上无电
A元素原子的最外电子层上有2个量子数n=4、l=0的电子,量子数n=3、l=2的轨道上无电子;B元素原子的最外电子层有2个量子数n=3、l=0的电子和5个量子数n=3、l=1的电子,试写出:
(1)A元素氧化物的化学式 CaO
(2)A元素氧化物与水的反应方程式 CaO+H2O=CaCO3
(3)B元素氢化物的分子式 HCl
(4)B元素氢化物的水溶液与A元素氧化物的反应方程式
HCl+ CaO=CaCl
是不是这样 竹露水波1年前1
竹露水波1年前1 -
 坦荡的鱼 共回答了16个问题
坦荡的鱼 共回答了16个问题 |采纳率100%A:价电子构型为:4s2,为Ca
B:价电子构型为:3s2 3p5,为Cl
(1)对
(2)错,CaO + H2O = Ca(OH)2
(3)对
(4)错,2HCl + CaO = CaCl2 + H2O1年前查看全部
- 根据玻尔理论,在氢原子中,量子数n越大,则( )
根据玻尔理论,在氢原子中,量子数n越大,则( )
A. 电子轨道半径越小
B. 核外电子速度越小
C. 原子能级的能量越小
D. 原子的电势能越小 无比期待1年前1
无比期待1年前1 -
 zj9831 共回答了19个问题
zj9831 共回答了19个问题 |采纳率100%解题思路:在氢原子中,量子数n越大,轨道半径越大,根据库仑引力提供向心力,判断核外电子运动的速度的变化,从而判断出电子动能的变化,根据能量的变化得出电势能的变化.在氢原子中,量子数n越大,电子的轨道半径越大,
根据
ke2
r2=m
v2
r 知,r越大,v越小,则电子的动能减小,即速度越小.
因为量子数增大,原子能级的能量增大,动能减小,则电势能增大.故B正确,A、C、D错误.
故选:B.点评:
本题考点: 玻尔模型和氢原子的能级结构;电势能.
考点点评: 解决本题的关键知道量子数越大,轨道半径越大,原子能级的能量越大,以及知道原子能量等于电子动能和势能的总和.1年前查看全部
- 已知氢原子基态能量为 13.6eV,要想氢原子由量子数为 n的激发态向 n-1的态跃迁时放出的能量,大於使电子由 n激发
已知氢原子基态能量为 13.6eV,要想氢原子由量子数为 n的激发态向 n-1的态跃迁时放出的能量,大於使电子由 n激发态脱离原子核的束缚变为自由电子所需的能量,则 n的最大值为?
Ans :3
为什麼会是3呢?请附上解释.
n^2-4n+2 = 0
n = 3 gg动力1年前1
gg动力1年前1 -
 HuguCapet 共回答了17个问题
HuguCapet 共回答了17个问题 |采纳率94.1%1/(n-1)^2-1/n^21年前查看全部
- 动能为12.5eV的电子通过碰撞使处于基态的氢原子激发,最高能跃迁到量子数n=______的能级.当氢原子从这个能级跃迁
动能为12.5eV的电子通过碰撞使处于基态的氢原子激发,最高能跃迁到量子数n=______的能级.当氢原子从这个能级跃迁回基态的过程中,辐射的光子的最长波长λ=______m.已知氢原子基态能量E1=-13.6eV,普朗克常量h=6.63×10-34J•S.(保留三位有效数字)
 zandyzhou1年前1
zandyzhou1年前1 -
 tsing121 共回答了25个问题
tsing121 共回答了25个问题 |采纳率92%解题思路:根据En=
求出第2能级,第3能级和第4能级能量,通过Em-En=h[C/λ]求出辐射光子的最长波长.E1 n2 氢原子基态能量E1=-13.6eV,根据En=E1n2得第2能级,第3能级和第4能级能量分别是-3.4eV,-1.51eV,-0.85eV.能级差值等于氢原子吸收的能量,所以动能为12.5eV的电子通过碰撞使处于基态的氢原子激发,最高能跃迁到量子...
点评:
本题考点: 氢原子的能级公式和跃迁.
考点点评: 解决本题的关键知道高能级向低能级跃迁,辐射光子,低能级向高能级跃迁,吸收能量,知道能级差与光子频率间的关系.1年前查看全部
- (1)已知金属钙的逸出功为2.7eV,氢原子的能级图如图A所示,一群氢原子处于量子数n=4能级状态,则______
(1)已知金属钙的逸出功为2.7eV,氢原子的能级图如图A所示,一群氢原子处于量子数n=4能级状态,则______
A.氢原子可能辐射6种频率的光子
B.氢原子可能辐射5种频率的光子
C.有3种频率的辐射光子能使钙发生光电效应
D.有4种频率的辐射光子能使钙发生光电效应
(2)质量为m 1 =1.0kg和m 2 (未知)的两个物体在光滑的水平面上正碰,碰撞时间不计,其x~t(位移-时间)图象如图B所示,试通过计算回答下列问题
①m 2 等于多少千克?
②碰撞过程是弹性碰撞还是非弹性碰撞?
 jufeng211年前1
jufeng211年前1 -
 BaBy默默 共回答了18个问题
BaBy默默 共回答了18个问题 |采纳率88.9%(1)A、B根据公式
C 2n =
C 24 =6知,这群氢原子可能辐射6种频率的光子.故A正确,B错误.
C、Dn=4跃迁到n=3辐射的光子能量为0.66eV,n=3跃迁到n=2辐射的光子能量为1.89eV,n=4跃迁到n=2辐射的光子能量为2.55eV,均小于逸出功,不能发生光电效应,其余3种光子能量均大于2.7eV,所以这群氢原子辐射的光中有3种频率的光子能使钙发生光电效应.故C正确、D错误.
故选AC
(2)①碰撞前m 2 是静止的,m 1 的速度为 v 1 =4m/s
碰后m 1 的速度为 v 1 ′=-2m/s
m 2 的速度 v 2 ′=2m/s
根据动量守恒定律有m 1 v 1 =m 1 v 1 ′+m 2 v 2 ′
1×4=1×(-2)+m 2 ×2
m 2 =3kg
②碰前总动能 E k1 +E k2 =
1
2 ×1× 4 2 +0=8J
碰后总动能 E′ k1 +E′ k2 =
1
2 ×1×(-2) 2 +
1
2 ×3× 2 2 =8J
碰撞前后机械能守恒故是弹性碰撞.
故答案为:(1)AC
(2)①m 2 等于3kg千克.
②碰撞过程是弹性碰撞.1年前查看全部
- (2013•江苏一模)已知原子基态电子轨道半径为r0=0.528×10-10m,量子数为n的激发态的能量EN=-[13.
 (2013•江苏一模)已知原子基态电子轨道半径为r0=0.528×10-10m,量子数为n的激发态的能量EN=-[13.6
(2013•江苏一模)已知原子基态电子轨道半径为r0=0.528×10-10m,量子数为n的激发态的能量EN=-[13.6n2  西畔数桃花1年前1
西畔数桃花1年前1 -
 wby61 共回答了25个问题
wby61 共回答了25个问题 |采纳率84%解题思路:根据库仑引力提供电子做圆周运动的向心力,求出电子在轨道上的速度和频率.(1)当氢原子从量子数n=3的能级跃迁到较低能级时,可以得到3条光谱线.如图所示.
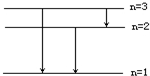 (2)波长最长的光对应处于n=3的激发态氢原子向n=2能级跃迁所发出的光谱线,
(2)波长最长的光对应处于n=3的激发态氢原子向n=2能级跃迁所发出的光谱线,
能量为:E=E3-E2=-1.51-(-3.4)=1.89eV;
由E=hγ,得:γ=
E/h]=
1.89×1.6×10−19
6.63×10−34=4.56×1014Hz>4.5×1014Hz;
由光电效应条件可知,能发生光电效应.
答:(1)当氢原子从量子数n=3的能级跃迁到较低能级时,可以得到3条光谱线.如图所示.
(2)能发生光电效应.点评:
本题考点: 氢原子的能级公式和跃迁.
考点点评: 本题考查对玻尔理论的理解和应用能力,关键抓住辐射的光子能量与能级差之间的关系.1年前查看全部
- 四个量子数指的是什么?
 白天梦游1年前1
白天梦游1年前1 -
 语过添情520 共回答了18个问题
语过添情520 共回答了18个问题 |采纳率61.1%n、l、ml、ms
主量子数,角量子数,磁量子数,自旋量子数1年前查看全部
- 已知金属钙的逸出功为2.7eV,氢原子的能级图如图所示.一群氢原子处于量子数n=4能级状态,则( )
已知金属钙的逸出功为2.7eV,氢原子的能级图如图所示.一群氢原子处于量子数n=4能级状态,则( )
 A. 氢原子可能辐射6种频率的光子
A. 氢原子可能辐射6种频率的光子
B. 氢原子可能辐射5种频率的光子
C. 有3种频率的辐射光子能使钙发生光电效应
D. 有4种频率的辐射光子能使钙发生光电效应 120812501年前2
120812501年前2 -
 严酷咯眼 共回答了18个问题
严酷咯眼 共回答了18个问题 |采纳率88.9%解题思路:根据数学组合公式求出氢原子可能辐射光子频率的种数,当光子的能量大于逸出功时,可以发生光电效应.A、根据
C24=6知,氢原子可能辐射6种频率的光子.故A正确,B错误.
C、金属钙的逸出功为2.7eV,只有n=4跃迁到n=1,n=3跃迁到n=1,n=2跃迁到n=1所辐射的光子能量大于逸出功,才能发生光电效应.故C正确,D错误.
故选AC.点评:
本题考点: 氢原子的能级公式和跃迁.
考点点评: 解决本题的关键知道能级间跃迁辐射的光子能量等于两能级间的能级差.1年前查看全部
- Cr正三价离子的3d轨道上的三个电子可能的运动状态的四个量子数
Cr正三价离子的3d轨道上的三个电子可能的运动状态的四个量子数
如果考虑到电子与电子之间的相互作用,根据“洪特原理”磁量子数就不能随便取了.Cr正三价离子的3d轨道上的三个电子可能的运动状态的四个量子数应该是:
3,2,2,1/2
3,2,1,1/2
3,2,0,1/2
这是我刚才看到的一道题,上面是答案.我想问问,为什么这里m只能取1/2而l不能取-2,-1呢? zml821年前1
zml821年前1 -
 6870010 共回答了18个问题
6870010 共回答了18个问题 |采纳率88.9%3d轨道,n=3,l=2.所以前两个量子数都是3,2.
第三个是磁量子数m,m=0,正负1,正负2,……,正负l.因为l=2,所以m可以取5个值,2,1,0,-1,-2.
根据洪特规则,三个电子应占三个d轨道且自旋平行,占的d轨道应使m尽可能大,故第三个量子数m分别为2,1,0.
三个电子自旋平行,所以自旋磁量子数都是1/2.对于电子来说,自旋磁量子数只能取正负二分之一两个值,一般自旋平等的电子都写成1/2.当然,都写成-1/2在原则上也没有错.1年前查看全部
- 原子结构原子中每个电子的运动状态由四个量子数n,l,m,ms确定.假设它的取值规则为:n=1,2,3,……;l=0,1,
原子结构
原子中每个电子的运动状态由四个量子数n,l,m,ms确定.假设它的取值规则为:n=1,2,3,……;l=0,1,2,…,(n-1);m=0,±1,±2,…,±l;ms=±1/2.
(1)每个n值一定的电子层包含多少原子轨道?
(2)每个l值一定的电子亚层可容纳多少个电子?
(3)前三个电子层***可容纳多少个电子? 你说叫个啥1年前1
你说叫个啥1年前1 -
 wunanrui 共回答了17个问题
wunanrui 共回答了17个问题 |采纳率94.1%n对应电子层,每个电子层有n个亚层(L的取值个数),每个亚层有(2L+1)个原子轨道(m的取值个数,m每取一个值对应一个原子轨道),每个原子轨道可容纳2个电子(自旋量子数不同).
1、每个n值包含n^2个原子轨道:1+3+5+7+...+[2(n-1)+1]
2、每个L值可容纳2(2L+1)个电子
3、前三个电子层最多容纳(2+8+32)=42个电子1年前查看全部
- (2013•滨州一模)氢原子的能级图如图所示,一群氢原子处于量子数n=4能量状态,则氢原子最多辐射______种频率的光
 (2013•滨州一模)氢原子的能级图如图所示,一群氢原子处于量子数n=4能量状态,则氢原子最多辐射______种频率的光子.辐射光子的最大能量为______.
(2013•滨州一模)氢原子的能级图如图所示,一群氢原子处于量子数n=4能量状态,则氢原子最多辐射______种频率的光子.辐射光子的最大能量为______.  一只mm1年前1
一只mm1年前1 -
 蝶舞0098 共回答了17个问题
蝶舞0098 共回答了17个问题 |采纳率100%解题思路:一群处于n=4能级的氢原子可能辐射C
种不同频率的光子;2 4
根据玻尔理论:辐射的光子能量hγ=hγ=Em-En(m>n),氢原子从n=4的激发态跃迁到n=1激发态时辐射的光子的能量最大.一群处于n=4能级的氢原子可能辐射C
2
4=6种不同频率的光子;
根据玻尔理论:辐射的光子能量hγ=hγ=Em-En(m>n),氢原子从n=4的激发态跃迁到n=1激发态时辐射的光子的能量最大.
所以辐射光子的最大能量为-0.85eV-(-13.6eV)=12.75eV
故答案为:6,12.75eV.点评:
本题考点: 氢原子的能级公式和跃迁.
考点点评: 本题考查对玻尔理论的理解和应用能力,关键抓住辐射的光子能量和公式c=λγ.1年前查看全部
- 原子核~动量题各一道1.现有1200个氢原子被激发到量子数为4的能级上,若这些受激氢原子最后都回到基态,则在此过程中发出
原子核~动量题各一道
1.现有1200个氢原子被激发到量子数为4的能级上,若这些受激氢原子最后都回到基态,则在此过程中发出的光子总数是多少?(假定处在量子数为n的激发态的氢原子跃迁到各较低能级的原子数都是处在该激发态的能级上的原子总数的1/n-1) ( A )
A.2200 B.2000 C.1200 D.2400
2.带有1/4光滑圆弧轨道,质量为M的滑车静止置于光滑水平面上,一质量为m的小球以速度Vo水平冲上滑车,当小球上行再返回并脱离滑车时,以下说法正确的是(B )
A.小球一定水平向左做平抛运动
B.小球可能水平向左做平抛运动
C.小球不可能做自由落体
D.小球不可能水平向右做平抛运动 xmlu3161年前1
xmlu3161年前1 -
 优车spa男 共回答了14个问题
优车spa男 共回答了14个问题 |采纳率85.7%1.第四轨道向第一、二、三轨道迁移各400个(共发出1200个光子).
第三轨道向第一、二轨道迁移各200个(共发出400个光子).
第二轨道向第一轨道迁移(第四轨道迁移)400+(第二轨道迁移)200=600个光 子.
1200+400+600=2200
2.系统水平方向动量守恒,故当小球上行再返回并脱离滑车时,二者均在水平方向上有速度.且速度方向是相同还是相反这取决于其质量的大小关系.当二者的质量相等时,最后小球水平速度将为0.
自己列一下动量守恒和机械能守恒的式子,分析一下1年前查看全部
- 有一群处于量子数n=4的激发态的氢原子,在它们发光的过程中,发出的光谱线共有几条?(最好能画图说明)
有一群处于量子数n=4的激发态的氢原子,在它们发光的过程中,发出的光谱线共有几条?(最好能画图说明)
本人对此甚感迷惑,希望各位能尽量说具体,清晰点,感激不尽! 卢玲玲1年前4
卢玲玲1年前4 -
 TDMG--SUMMER 共回答了16个问题
TDMG--SUMMER 共回答了16个问题 |采纳率75%我高三,正好学呢
由激发态的氢原子要发光,必定是放出光子,放出能量,所以要向低能级跃迁
由n=4可以到3,2,1.有三种
刚才说了,有的氢原子跃迁到第三能级,还可以继续跃迁至2,1,有两种.
同理,n=2处的会跃迁至1.有一种
一共六种!1年前查看全部
- 同一原子中存在一个电子的四个量子数完全相同吗
 潘青1年前2
潘青1年前2 -
 胖子999 共回答了15个问题
胖子999 共回答了15个问题 |采纳率80%K层磁量子数为21年前查看全部
- 用某频率光照氢原子,使他从基态跃迁到量子数为4的激发态,该光在真空中频率为多少?
 爱芙蓉vv1年前1
爱芙蓉vv1年前1 -
 oldfull 共回答了13个问题
oldfull 共回答了13个问题 |采纳率92.3%直接代入公式E4-E1=hν1年前查看全部
- 写出23V的核外电子排布式,并写出5个价电子四个量子数
 yan01011年前2
yan01011年前2 -
 流泪的洋狗狗 共回答了16个问题
流泪的洋狗狗 共回答了16个问题 |采纳率75%V
1s2 2s2 2p6 3s2 3p6 3d3 4s2
①n=3,l=2,m=0,ms = 1/2
②n=3,l=2,m=0,ms = -1/2
③n=3,l=2,m=1,ms = 1/2
④n=4,l=0,m=0,ms = 1/2
⑤n=4,l=0,m=0,ms = -1/21年前查看全部
- 填写下表中合理的量子数还要解释一下什么基态原子,不要太理论性的,简单易懂,最好举例子一下.还有还有,那个就是L=2,代表
填写下表中合理的量子数
还要解释一下什么基态原子,不要太理论性的,简单易懂,最好举例子一下.
还有还有,那个就是L=2,代表什么意思啊?
 xiangtui1年前1
xiangtui1年前1 -
 rrrr家 共回答了21个问题
rrrr家 共回答了21个问题 |采纳率90.5%1,n=3
2,l=1
3,ms=+1/2
4,m=0
l=2代表的是d亚层
在正常状态下,电子尽可能处于离核较近、能量较低的轨道上,这时原子所处的状态称为基态,此时的原子称为基态原子.1年前查看全部
- 已知金属钙的逸出功为2.7eV,氢原子的能级图如图所示,一群氢原子处于量子数n=4的能量状态,则( )
 已知金属钙的逸出功为2.7eV,氢原子的能级图如图所示,一群氢原子处于量子数n=4的能量状态,则( )
已知金属钙的逸出功为2.7eV,氢原子的能级图如图所示,一群氢原子处于量子数n=4的能量状态,则( )
A.氢原子可能辐射3种频率的光子
B.氢原子可能辐射5种频率的种子
C.有3种频率的辐射光子能使钙发生光电效应
D.有4种频率的辐射光子能使钙发生光电效应 吵翻1年前1
吵翻1年前1 -
 ture03910371 共回答了18个问题
ture03910371 共回答了18个问题 |采纳率83.3%解题思路:根据数学的组合公式
求出这群氢原子可能辐射光子频率的种数.发生光电效应的条件是光子能量大于逸出功.C 2nA、根据
C24=6知,这群氢原子可能辐射6种频率的光子.故A错误,B错误.
C、n=4跃迁到n=3辐射的光子能量为0.66eV,n=3跃迁到n=2辐射的光子能量为1.89eV,n=4跃迁到n=2辐射的光子能量为2.55eV,均小于逸出功,不能发生光电效应,其余3种光子能量均大于2.7eV,所以这群氢原子辐射的光中有3种频率的光子能使钙发生光电效应.故C正确,D错误.
故选:C.点评:
本题考点: 氢原子的能级公式和跃迁.
考点点评: 解决本题的关键掌握光电效应的条件,以及知道能极差与辐射的光子能量的关系.1年前查看全部
- 量子数为n=3,l=2,m=2的能级可允许的最多电子数为多少个
量子数为n=3,l=2,m=2的能级可允许的最多电子数为多少个
是不是两个? shimang1年前1
shimang1年前1 -
 憨豆2003 共回答了10个问题
憨豆2003 共回答了10个问题 |采纳率90%是两个.根据Pauli不相容原理,系统中没有两个四个量子数都相同的电子.现在已经有3个量子数(n,l,m)都相同,只能在第四个量子数上不同.第四个量子数自旋磁量子数只能取正二分之一或负二分之一两个值,故最多可以有两个电子.
更直观地说,n=3,l=2指的是3d轨道,5个3d轨道m的值分别为2,1,0,-1,-2.m=2其实指的是其中的一个3d轨道.一个轨道上只能容纳两个自旋相反的电子.1年前查看全部
- 四个量子数与各原子核外电子排布的关系,请举例子说明
 故人舒眉1年前1
故人舒眉1年前1 -
 销户 共回答了13个问题
销户 共回答了13个问题 |采纳率100%四个量子数与原子核外电子排布没有太大的关系.只是原子核外每个电子都有自己特定的四个量子数定制的波函数而已.
如钠原子的最外层的3s1电子,可用四个量子数:3,0,0,1/2或-1/2;而当其中的某个电子激发到3d轨道上时,该轨道上的电子描述为:3,2,m,ms,其中,m = 2,1,0,-1,-2中的任意一个数;而 ms = 1/2,-1/2中的任意一值.1年前查看全部
- 为什么在天文上才容易观测到量子数n较大的里德堡原子?
 luchong1年前1
luchong1年前1 -
 喀丘莎 共回答了20个问题
喀丘莎 共回答了20个问题 |采纳率100%里德伯原子是高激发态的,非常容易受到其他粒子影响而改变形态,所以现在只有在极低密度的宇宙空间才能观察到.补充一点,宇宙空间的密度是远低于人造真空的.
参考里德伯原子的百科,还是比较详细的,再多的知识就参考原子物理学的课本1年前查看全部
- 刚学到能级,不理解什么是量子数,不用讲太深.相关练习,氢原子中,量子书N越大,则下列说法正确的是?A电子轨道半径越大 B
刚学到能级,不理解什么是量子数,不用讲太深.相关练习,氢原子中,量子书N越大,则下列说法正确的是?A电子轨道半径越大 B核外电子的速率越大
C氢原子能级能量越大 D核外电子的速率越大.请给出解释,不要转载的那种,要自己回答 娃哈哈ch21年前1
娃哈哈ch21年前1 -
 新兵0358 共回答了16个问题
新兵0358 共回答了16个问题 |采纳率93.8%你说的n叫做主量子数,其实就是过去讲的第几电子层.
还有副量子数l、磁量子数m和自旋量子数ms.
A是对的,量子数大就是外层,半径大.
BD怎么一样?是错的,半径大速率低,这个用高中的圆周运动公式可以得到,v=根号下[k*E*E/(MR)].
C对,能级高,能量大.1年前查看全部
- 若电子自旋量子数由两种变成三种,每个轨道上所能容纳的电子数是不是也变成三个?为什么?同学说还是两个…
若电子自旋量子数由两种变成三种,每个轨道上所能容纳的电子数是不是也变成三个?为什么?同学说还是两个…
对哦,在保证费米子的情况下,怎么会是三种可能?应该是偶数种吧…题目不严密… 有种你tt我1年前1
有种你tt我1年前1 -
 贝帆 共回答了22个问题
贝帆 共回答了22个问题 |采纳率95.5%对哦.题目不严密嘛.1年前查看全部
- 描述每个原子轨道时需要3个量子数这个3个量子数是( )
描述每个原子轨道时需要3个量子数这个3个量子数是( )
描述每个电子的运动状态时除了电子所占据的轨道的量子数外还要再加一个( )量子数 q_____t1年前1
q_____t1年前1 -
 白蛤蟆 共回答了20个问题
白蛤蟆 共回答了20个问题 |采纳率90%量子数是量子力学中表述原子核外电子运动的一组整数或半整数.因为核外电子运动状态的变化不是连续的,而是量子化的,所以量子数的取值也不是连续的,而只能取一组整数或半整数.量子数包括主量子数n、角量子数l、磁量子数m和自旋量子数ms四种,前三种是在数学解析薛定谔方程过程中引出的,而最后一种则是为了表述电子的自旋运动提出的1年前查看全部
- 根据玻尔理论,在氢原子中,量子数n越大,则( )
根据玻尔理论,在氢原子中,量子数n越大,则( )
A. 电子轨道半径越小
B. 核外电子运动速度越小
C. 原子能级的能量越小
D. 电子的电势能越大 lxcql3121年前1
lxcql3121年前1 -
 loveme821 共回答了22个问题
loveme821 共回答了22个问题 |采纳率86.4%解题思路:在氢原子中,量子数n越大,原子的能量越大,根据库仑引力提供向心力,根据轨道半径的变化,判断电子动能的变化.原子能量等于电子动能和势能的总和,从而确定电子势能的变化.n越大,轨道半径越大,原子能量越大,根据k
e2
r2=m
v2
r,知电子的动能越小,原子能量等于电子动能和势能的总和,知电阻的电势能越大.故B、D正确,A、C错误.
故选BD.点评:
本题考点: 玻尔模型和氢原子的能级结构.
考点点评: 解决本题的关键知道量子数越大,轨道半径越大,电子动能越小,原子能量越大,电子电势能越大.1年前查看全部
- 现有1200个氢原子被激发到量子数为4的能级上,若这些受激氢原子最后都回到基态,已知金属钾的逸出功为2.22eV。在这些
现有1200个氢原子被激发到量子数为4的能级上,若这些受激氢原子最后都回到基态,已知金属钾的逸出功为2.22eV。在这些光波中,能够从金属钾的表面打出光电子的光子总数为_____________。假定处在量子数为n的激发态的氢原子跃迁到各较低能级的原子数都是处在该激发态能级上的原子总数的1/(n-1)  我是牙膏1年前1
我是牙膏1年前1 -
 无所谓n 共回答了14个问题
无所谓n 共回答了14个问题 |采纳率78.6%16001年前查看全部
- 如图所示为氢原子的能级图,n为量子数.在氢原子核外电子由量子数为2的轨道跃迁到量子数为3的轨道的过程中,将______(
如图所示为氢原子的能级图,n为量子数.在氢原子核外电子由量子数为2的轨道跃迁到量子数为3的轨道的过程中,将______(填“吸收”或“放出”)光子.若该光子恰能使某金属产生光电效应,则一群处于量子数为4的激发态的氢原子在向基态跃迁过程中,有______种频率的光子能使该金属产生光电效应.

 hejiao1291年前1
hejiao1291年前1 -
 向日葵26 共回答了25个问题
向日葵26 共回答了25个问题 |采纳率92%解题思路:核外电子由低能级跃迁到高能级时,吸收光子,由高能级向低能级跃迁则放出光子,放出光子频率数为
.n(n−1) 2 核外电子由低能级跃迁到高能级时,吸收光子,
处于第4能降低上的电子发生的光的频率数为:
n(n−1)
2=6,其中有5种光的频率大于由量子数为2的轨道跃迁到量子数为3的轨道的过程中吸收的光的频率.
所以有5种频率的光子能使该金属产生光电效应.
故答案为:吸收,5.点评:
本题考点: 氢原子的能级公式和跃迁.
考点点评: 本题考查了原子物理的有关知识,尤其是能级跃迁是重点知识,要加强理解和应用,同时对于一些基础知识要加强记忆.1年前查看全部
- 请问四个量子数的量子化条件各是什么?
请问四个量子数的量子化条件各是什么?
如题 一笑传情1年前2
一笑传情1年前2 -
 l82916 共回答了19个问题
l82916 共回答了19个问题 |采纳率78.9%主量子数n n是正整数,n>=1.
角量子数l l是自然数,l1年前查看全部
- 根据玻尔理论,氢原子中,量子数N越大,则下列说法中正确的是( )
根据玻尔理论,氢原子中,量子数N越大,则下列说法中正确的是( )
A.电子轨道半径越大
B.核外电子的速率越大
C.氢原子能级的能量越大
D.核外电子的电势能越小 空许1年前1
空许1年前1 -
 tlbbs 共回答了16个问题
tlbbs 共回答了16个问题 |采纳率81.3%解题思路:量子数越大,轨道半径越大,原子能量变大,根据库仑引力提供向心力得出电子动能的变化,通过能量变化和电子动能变化得出电势能的变化.在氢原子中,量子数越大,电子的轨道半径越大,原子能级的能量越大,
根据
ke2
r2=m
v2
r,知电子动能减小,核外电子速度减小.由于能量增大,电子动能减小,则电势能增大.故A、C正确,B、D错误.
故选:AC.点评:
本题考点: 玻尔模型和氢原子的能级结构.
考点点评: 解决本题的关键知道电子动能、原子能量与轨道半径的关系.知道原子能量等于电子动能和电势能之和.1年前查看全部
- 可见光光子的能量在1.61eV~3.10eV范围内.若氢原子从高能级跃迁到量子数为n的低能级的谱线中有可见光,根据氢原子
可见光光子的能量在1.61eV~3.10eV范围内.若氢原子从高能级跃迁到量子数为n的低能级的谱线中有可见光,根据氢原子能级图可判断n为( ) A.1 B.2 C.3 D.4 
 Ricca1年前1
Ricca1年前1 -
 彭江华 共回答了16个问题
彭江华 共回答了16个问题 |采纳率81.3%根据能级图可有:当n=1时,E 2 -E 1 =10.20eV是最小的光子能量,大于3.10eV,所以n=1不可能;如果n=3时,E 3 =-1.51eV,则从n=∞到n=3的跃迁时发出的光子能量是最大,也小于1.61eV,所以,n=3也不可能.剩下只有n=2才满足条件.故选项ACD错误,B正确.
故选B.1年前查看全部
大家在问
- 1人类文明历史是从创造什么开始的?A 符号 B文字 C 工具 D图画 哪个是正确的呢?
- 2校园内有一个半径为5米的圆形草坪,一部分学生为走“捷径”,在草坪内走出了一条小路AB,如图所示.通过计算可知,这些学生仅
- 3某46被水解成1个四肽,2个三肽,2个六肽3个八肽,则此水解过程需要几个水分子?
- 4已知f[g(x)]=z(x),求f(x)这里的f(x)的x指的是什么?
- 5(2012•成都模拟)设四棱锥P-ABCD的底面ABCD是单位正方形,PB⊥底面ABCD且PB=3,记∠APD=θ,si
- 6一本趣味数学书,小刚已经读的页数比全书的五分之二少12页,没读的页数占全书的四分之三,这本书有多少页?
- 7play,can,students,the,us,basketball,with(连词成句,并翻译)
- 81过抛物线y^2=2px(p>0)的焦点作倾斜角为135度的直线,交抛物线于A,B两点,O为原点,则三角形OAB的面积等
- 9如图所示,用ab表示阴影部分手的面积,当
- 10有一个长方形林场,长5千米,宽200米,这个林场的面积是多少平方千米?
- 11经常清扫表面的灰尘可以防锈吗?为什么?
- 12把 舟过安仁 改写成短文(可以编写时间,地点,人物300,400字)
- 13英语翻译We have shown that STAT3 is expressed and activated duri
- 14Shall I tell John about it?的否定回答的答案是,No,you needn't.和No,you
- 15300g=多少kg那我要把分给谁了?

