新型陶瓷材料是什么?
 以爱情之名2022-10-04 11:39:541条回答
以爱情之名2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 赵振兰 共回答了16个问题
赵振兰 共回答了16个问题 |采纳率93.8%- 新型陶瓷材料是一种新型的无机非金属材料耐高温、强度高(如氮化硅,制造汽轮机叶片、轴承永久性模具等);x0d具有电学特性(做半导体、导体、超导体,用于集成电路的基板等);x0d具有光学特性,具有生物功能等;x0d有氮化硅陶瓷、氧化铝陶瓷等.
- 1年前
相关推荐
- 氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
______SiO2+______C+______N2
______Si3N4+______CO高温
(1)配平上述反应的化学方程式(将化学计量数填在横线上);
(2)该反应的氧化剂是______,其还原产物是______;
(3)该反应的平衡常数表达式为K=c6(CO) c2(N2) ;c6(CO) c2(N2)
(4)若上述反应为放热反应,则其反应热△H______零(填“大于”、“小于”或“等于”);升高温度,其平衡常数值______(填“增大”、“减小”或“不变”);
(5)若使压强增大,则上述平衡向______反应方向移动(填“正”或“逆”);
(6)下列能加快反应速率的措施为:______
①降低温度②将SiO2粉碎③增大焦炭用量④转移出CO
(7)若已知CO生成速率为v(CO)=18mol•L-1•min-1,则N2消耗速率为v(N2)=______mol•L-1•min-1. 云儿一片片1年前1
云儿一片片1年前1 -
 MPTD 共回答了17个问题
MPTD 共回答了17个问题 |采纳率82.4%解题思路:(1)根据氧化还原反应化合价升降总数相等以及质量守恒来解答;
(2)所含元素化合价降低的反应物为氧化剂,氧化剂发生还原反应生成还原产物.
(3)依据化学反应平衡常数概念写出,注意反应物和生成物中固体不写入平衡常数表达式;
(4)反应放热,则△H<0,对于放热反应,升高温度,K会减小;
(5)化学反应是气体体积增大的放热反应,增大压强平衡向气体体积减小的方向进行;
(6)影响化学反应速率的因素:温度、浓度、压强、固体表面积、催化剂等因素;
(7)不同物质表示的化学反应速率之比等于方程式的系数之比.(1)Si的化合价前后未变,N的化合价由0降为-3,C的化合价由0升为+2,生成1个Si3N4化合价降低12,生成1个CO化合价升高2,根据化合价升降总数相等以及质量守恒得,3SiO2+6C+2N2
高温
.
Si3N4+6CO,故答案为:3、6、2、1、6;
(2)所含元素化合价降低的反应物是氧化剂,氧化剂被还原得到的生成物是还原产物,所以N2是氧化剂,Si3N4是还原产物.
故答案为:N2;Si3N4;
(3)依据化学反应方程式,3SiO2+6C+2N2
高温
Si3N4+6CO,△H=QkJ/mol,反应物为气体的是氮气,生成物为气体的是一氧化碳,气体为止为 固体,依据平衡常数概念写出的平衡常数表达式为:K=
c6(CO)
c2(N2),故答案为:K=
c6(CO)
c2(N2);
(4)已知上述反应为放热反应,△H<0,所以Q<0,对于放热反应,升高温度,K会减小;
故答案为:小于;减小;
(5)化学反应是气体体积增大的放热反应,增大压强平衡向气体体积减小的方向进行,反应逆向进行;
故答案为:逆;
(6)①降低温度,反应速率减小,故错误;
②将SiO2粉碎,增大故体表面积,反应速率加快,故正确;
③增大焦炭用量不会改变化学反应速率,故错误;
④转移出CO,会减慢反应速率,故错误.
故选②;
(7)已知平衡时CO生成速率为v(CO)=18mol•L-1•min-1,则N2的生成速率为v(N2)=[2/6]×v(CO)=[1/3]×18mol•L-1•min-1=6mol/L•min;
故答案为:6;点评:
本题考点: 氧化还原反应方程式的配平;反应速率的定量表示方法;化学平衡的影响因素.
考点点评: 题考查了氧化还原方程式的配平、化学平衡的分析判断,平衡常数的影响因素应用,化学反应速率计算,注意平衡常数表达式中固体不写入,固体量的增减对反应速率无影响等知识,题目难度不大.1年前查看全部
- (2014•张家港市模拟)氮化硅是一种新型陶瓷材料的主要成分,能承受高温,可用于制造航天器材等领域.已知氮、硅的原子结构
(2014•张家港市模拟)氮化硅是一种新型陶瓷材料的主要成分,能承受高温,可用于制造航天器材等领域.已知氮、硅的原子结构示意图依次为
 .请推测,氮化硅的化学式为( )
.请推测,氮化硅的化学式为( )
A.Si3N4
B.Si4N3
C.Si3N7
D.Si7N3 北兵马司剧场1年前1
北兵马司剧场1年前1 -
 中尉的眼泪 共回答了15个问题
中尉的眼泪 共回答了15个问题 |采纳率93.3%解题思路:已知氮、硅的原子结构示意图,得氮原子的最外层电子数为5,则容易得3个电子,达稳定结构,带3个负电荷,化合价为-3价;硅原子最外层电子数为4,易失去4个电子,达到稳定结构,带4个正电荷,化合价为+4价.①根据化合价的原则(在化合物中正、负化合价的代数和为零);②化学式中元素的位置:“正价左,负价右”;③化合价数值交叉法书写化学式(即将正、负化合价的数值交叉到相应符号的右下角,但注意原子团看作一体,含约数的一般要约分).第一种方法:设氮化硅的化学式为SixNY,再标出化合价
+4
Six
−3
NY,根据化合价的原则(在化合物中正、负化合价的代数和为零)所以[X/Y]=[3/4],故选A.
第二种方法:①化学式中元素的位置:“正价左,负价右”;②化合价数值交叉法书写化学式(即将正、负化合价的数值交叉到相应符号的右下角,但注意原子团看作一体,含约数的一般要约分).故选A.点评:
本题考点: 化学式的书写及意义;核外电子在化学反应中的作用;原子结构示意图与离子结构示意图.
考点点评: 本题既考查了常见元素的化合价以及化合价的规律和原则,还考查了化学式的书写方法和技巧.1年前查看全部
- 新型陶瓷材料是什么?
 hopehe1年前1
hopehe1年前1 -
 玉麒麟2 共回答了14个问题
玉麒麟2 共回答了14个问题 |采纳率85.7%新型陶瓷材料是一种新型的无机非金属材料耐高温、强度高(如氮化硅,制造汽轮机叶片、轴承永久性模具等);
具有电学特性(做半导体、导体、超导体,用于集成电路的基板等);
具有光学特性,具有生物功能等;
有氮化硅陶瓷、氧化铝陶瓷等.1年前查看全部
- “神七”成功了,我们为之自豪,我们要学着了解科学、了解物质.氮化硅是一种新型陶瓷材料的主要成分,能承受高温,可用于制造业
“神七”成功了,我们为之自豪,我们要学着了解科学、了解物质.氮化硅是一种新型陶瓷材料的主要成分,能承受高温,可用于制造业、航天工业等领域.请推测氮化硅的化学式( )
A. Si3N4
B. Si4N3
C. Si3N7
D. Si7N3 vertel1年前1
vertel1年前1 -
 kangletian 共回答了17个问题
kangletian 共回答了17个问题 |采纳率94.1%解题思路:根据氮、硅的原子结构示意图,得氮原子的最外层电子数为5,则容易得3个电子,达稳定结构,带3个负电荷,化合价为-3价;硅原子最外层电子数为4,易失去4个电子,达到稳定结构,带4个正电荷,化合价为+4价.①根据化合价的原则(在化合物中正、负化合价的代数和为零);②化学式中元素的位置:“正价左,负价右”;③化合价数值交叉法书写化学式(即将正、负化合价的数值交叉到相应符号的右下角,但注意原子团看作一体,含约数的一般要约分).第一种方法:设氮化硅的化学式为SixNY,再标出化合价
+4
Si x
-3
N Y,根据化合价的原则(在化合物中正、负化合价的代数和为零)所以 [X/Y]=[3/4],故选A.
第二种方法:①化学式中元素的位置:“正价左,负价右”;②化合价数值交叉法书写化学式(即将正、负化合价的数值交叉到相应符号的右下角,但注意原子团看作一体,含约数的一般要约分).故选A.点评:
本题考点: 有关化学式的计算和推断.
考点点评: 本题既考查了常见元素的化合价以及化合价的规律和原则,还考查了化学式的书写方法和技巧.1年前查看全部
- (2014•延庆县)下列关于耐高温新型陶瓷材料氮化硅(Si3N4)的叙述正确的是( )
(2014•延庆县)下列关于耐高温新型陶瓷材料氮化硅(Si3N4)的叙述正确的是( )
A.氮化硅中氮元素的质量分数为40%
B.氮化硅是有机高分子合成材料
C.氮化硅中硅与氮的质量比为3:4
D.氮化硅的相对分子质量是140g 孬孬粉子1年前1
孬孬粉子1年前1 -
 健身帅小子 共回答了16个问题
健身帅小子 共回答了16个问题 |采纳率93.8%解题思路:A、根据化合物中元素的质量分数=[相对原子质量×原子个数/相对分子质量]×100%,进行分析判断;
B、有机高分子合成材料是指人工合成的有机高分子(相对分子质量很大的有机物)材料,据此进行分析判断;
C、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断;
D、相对原子质量的国际单位制单位为“一”,符号是“1”一般不写.A、氮化硅中氮元素的质量分数为[14×4/140]×100%=40%,故本选项叙述正确;
B、氮化硅不含碳元素,不属于有机物,不是有机高分子合成材料,故本选项叙述错误;
C、氮化硅中Si、N两种元素的质量比为(28×3):(14×4)=3:2,故本选项叙述错误;
D、氮化硅的相对分子质量是140,故本选项叙述错误;
故选:A.点评:
本题考点: 元素的质量分数计算;相对分子质量的概念及其计算;元素质量比的计算;有机高分子材料的分类及鉴别.
考点点评: 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.1年前查看全部
- 氮化硅(Si3N4)是一种新型陶瓷材料,它可用石英与焦炭在高温的氮气流中反应制得:______SiO2+______C+
氮化硅(Si3N4)是一种新型陶瓷材料,它可用石英与焦炭在高温的氮气流中反应制得:______SiO2+______C+______N2
______Si3N4+______CO高温 .
根据题意完成下列各题:
(1)配平上述化学反应方程式.
(2)为了保证石英和焦炭尽可能的转化,氮气要适当过量.某次反应用了20mol氮气,反应生成了5mol一氧化碳,此时混合气体的平均相对分子质量是______.
(3)分析反应可推测碳、氮气的氧化性:C______N2(填“>”“<”“=”).
(4)氮化硅陶瓷的机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定.以下用途正确的是______.
A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备
B.在电子工业上制成耐高温的电的良导体
C.研发氮化硅的全陶发动机替代同类型金属发动机
D.氮化硅陶瓷的开发受到资源的限制,没有发展前途. 放_55591年前1
放_55591年前1 -
 今夜谁嫁我 共回答了15个问题
今夜谁嫁我 共回答了15个问题 |采纳率86.7%解题思路:(1)由产物CO可知,SiO2与C化学计量数之比为1:2 由产物Si3N4可知SiO2与N2化学计量数之比为3:4,所以SiO2、C、N2化学计量数之比为3:6:4,令SiO2的化学计量数为3,结合元素守恒可知Si3N4、CO化学计量数分别为1、6;
(2)N2与CO的相对分子质量都是28,混合气体的平均相对分子质量不变;
(3)反应中N2作氧化剂,C是还原剂,N2将C氧化;
(4)由信息可知,氮化硅机械强度高,硬度大,热稳定性好,化学性质稳定,氮化硅属于原子晶体,不是电的良导体,制备氮化硅的资源丰富,自然界中有大量的氮气与二氧化硅,具有广阔的发展前景.(1)由产物CO可知,SiO2与C化学计量数之比为1:2 由产物Si3N4可知SiO2与N2化学计量数之比为3:2,所以SiO2、C、N2化学计量数之比为3:6:2,令SiO2的化学计量数为3,C、N2化学计量数分别为6、2,结合元素守恒可知Si3N4、CO化学计量数分别为1、6,配平后方程式为3SiO2+6C+2N2
高温
.
Si3N4+6CO,
故答案为:3;6;2;1;6;
(2)N2与CO的相对分子质量都是28,所以混合气体的平均相对分子质量为28,故答案为:28;
(3)反应中N2作氧化剂,C是还原剂,N2将C氧化为CO,所以氧化性C<N2,故答案为:<;
(4)A.氮化硅热稳定性好,可以用于热工设备,故A正确;
B.氮化硅属于原子晶体,不是电的良导体,故B错误;
C.氮化硅机械强度高,硬度大,可以替代同类型金属发动机,故C正确;
D.制备氮化硅的资源丰富,具有广阔的发展前景,故D错误.
故选:AC.点评:
本题考点: 氧化还原反应方程式的配平;含氮物质的综合应用.
考点点评: 本题主要考查了氧化还原反应配平及计算、氧化性还原性比较等知识,注意掌握氧化还原反应化学方程式常用的配平方法,题目难度中等.1年前查看全部
- (2011•罗定市模拟)佛山是陶瓷之乡,石湾陶瓷闻名全国.氮化硅(Si3N4)是一种新型陶瓷材料的主要成分,能承受高温,
(2011•罗定市模拟)佛山是陶瓷之乡,石湾陶瓷闻名全国.氮化硅(Si3N4)是一种新型陶瓷材料的主要成分,能承受高温,可用于制造业、航天工业等.氮化硅中氮的化合价是( )
A.-3
B.+3
C.+4
D.+5 ymx19861年前1
ymx19861年前1 -
 jpc18 共回答了14个问题
jpc18 共回答了14个问题 |采纳率92.9%解题思路:根据化合物中元素的化合价的代数和为零的原则和化合物中硅元素常显+4价,可以计算出氮化硅中氮元素的化合价.设氮化硅中氮元素的化合价为x.
(+4)×3+x×4=0
x=-3
故选A.点评:
本题考点: 有关元素化合价的计算;常见元素与常见原子团的化合价;化合价规律和原则.
考点点评: 本题主要考查化合价的原则和化合价的计算,难度较小.1年前查看全部
- 锆(Zr)的一种氧化物是耐高温的新型陶瓷材料,经测定,锆原子核内有51个中子,核外有40个电子,其氯化物的相对分子质量为
锆(Zr)的一种氧化物是耐高温的新型陶瓷材料,经测定,锆原子核内有51个中子,核外有40个电子,其氯化物的相对分子质量为233,若锆的氯化物和氧化物中锆的化合价相同.则氧化物的化学式为( )
A. Zr2O
B. ZrO
C. Zr2O3
D. ZrO2 cliar1年前4
cliar1年前4 -
 yiyoyou 共回答了22个问题
yiyoyou 共回答了22个问题 |采纳率95.5%解题思路:就原子来说,质子数=原子序数=核外电子数,质子数+中子数=相对原子质量.首先计算出锆原子的相对原子质量,然后根据氯化物的相对分子质量为233,可以算出锆元素的化合价,最后写出氧化物的化学式.就原子来说,质子数=原子序数=核外电子数,质子数+中子数=相对原子质量.根据题目信息可知,锆原子核内有51个中子,核外有40个电子,所以质子有40个,相对原子质量=51+40=91.
设锆元素的化合价为+X,其氯化物的化学式为:ZrClx,
∵锆的氯化物的相对分子质量为233.
∴91+35.5X=233
得:X=4
∵在锆的氧化物中锆的化合价是+4价,氧元素的化合价是-2价.
∴氧化物的化学式为:ZrO2,故选D.点评:
本题考点: 有关化学式的计算和推断;常见元素与常见原子团的化合价;化合价规律和原则.
考点点评: 掌握相对原子质量和质子、中子之间的关系式,学会根据化合价书写物质的化学式.1年前查看全部
- (2003•上海)氮化硅是一种新型陶瓷材料的主要成分,能承受高温,可用于制造业、航天业等领域.已知氮、硅的原子结构示意图
 (2003•上海)氮化硅是一种新型陶瓷材料的主要成分,能承受高温,可用于制造业、航天业等领域.已知氮、硅的原子结构示意图依次为.请推测,氮化硅的化学式(分子式)为( )
(2003•上海)氮化硅是一种新型陶瓷材料的主要成分,能承受高温,可用于制造业、航天业等领域.已知氮、硅的原子结构示意图依次为.请推测,氮化硅的化学式(分子式)为( )
A.Si3N4
B.Si4N3
C.Si3N7
D.Si7N3 黄香倪1年前1
黄香倪1年前1 -
 zhaxiufang 共回答了13个问题
zhaxiufang 共回答了13个问题 |采纳率100%解题思路:根据氮、硅的原子结构示意图,分析得出元素的化合价,然后利用化合价来书写化学式.由氮原子的结构示意图
 ,可以看出最外层电子数为5,容易得到3个电子,则N元素的化合价为-3价;由硅原子的结构示意图
,可以看出最外层电子数为5,容易得到3个电子,则N元素的化合价为-3价;由硅原子的结构示意图 ,可以看出最外层电子数为4,一般不容易失去也不容易得到电子,但可以与其它元素以共用电子对形成化合物,则元素的化合价为+4价,则
,可以看出最外层电子数为4,一般不容易失去也不容易得到电子,但可以与其它元素以共用电子对形成化合物,则元素的化合价为+4价,则
+4
Si
−3
N,化合价不能约分可直接交叉,使化合物中正负化合价的代数和为0,得化学式为Si3N4,
故选A.点评:
本题考点: 有关化学式的计算和推断;核外电子在化学反应中的作用;化合价规律和原则.
考点点评: 本题考查学生利用化合价来书写物质的化学式,学生应能根据原子结构得出元素在形成化合物时的化合价,然后可利用化合价和化合价的原则来书写化学式.1年前查看全部
- (8分)氮化硅(Si 3 N 4 )是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
(8分)氮化硅(Si 3 N 4 )是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
□SiO 2 +□C+□N 2 □Si 3 N 4 +□CO
□Si 3 N 4 +□CO
(1)配平上述反应的化学方程式(将化学计量数填在方框内);
(2)该反应的氧化剂是 ,其还原产物是 ;
(3)若知上述反应为放热反应,则其反应热△ H 零(填“大于”、“小于”或“等于”);升高温度,其平衡常数值 (填“增大”、“减小”或“不变”);
(4)若使压强增大,则上述平衡向 反应方向移动(填“正”或“逆”);
(5)若已知CO生成速率为 v (CO)=18mol/(L.min),则N 2 消耗速速率为 v (N 2 )= mol/(L.min)。 yuyu7101年前1
yuyu7101年前1 -
 fairyking 共回答了20个问题
fairyking 共回答了20个问题 |采纳率100%(1)3,6,2,1,6(2分)
(2)N 2 ,Si 3 N 4 (3)小于减小(4)逆(5)6(每空1分)
(1)反应中碳元素的化合价从0价升高到+2价,失去2个电子;氮元素的化合价从0价降低到-3价,得到3个电子。所以根据电子的得失守恒可知,还原剂和氧化剂的物质的量之比是3︰1,所以配平后的化学计量数分别依次是3,6,2,1,6。
(2)根据(1)可知氮气是氧化剂,其还原产物是Si 3 N 4 。
(3)放热反应的△H小于0。升高温度平衡向吸热的逆反应方向移动,因此平衡常数减小。
(4)根据配平后的方程式可知,正反应是体积增大的,所以增大压强,平衡向逆反应方向移动。
(5)根据反应速率之比是相应的化学计量数之比可知,氮气的消耗速率是18mol/(L.min)÷3=6mol/(L.min)。1年前查看全部
- (2010•集美区质检)下列关于耐高温新型陶瓷材料氮化硅(Si3N4)的叙述正确的是( )
(2010•集美区质检)下列关于耐高温新型陶瓷材料氮化硅(Si3N4)的叙述正确的是( )
A.14g氮化硅中含硅8.4g
B.氮化硅中Si、N两种元素的质量比为4:3
C.氮化硅的相对分子质量为144
D.氮化硅中氮元素的质量分数为60% 臭口狗1年前0
臭口狗1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 属于新型陶瓷材料的是什么
 1165936871年前1
1165936871年前1 -
 alex1209 共回答了14个问题
alex1209 共回答了14个问题 |采纳率100%新型陶瓷材料在性能上有其独特的优越性.在热和机械性能方面,有耐高温、隔热、高硬度、耐磨耗等;在电性能方面有绝缘性、压电性、半导体性、磁性等;在化学方面有催化、耐腐蚀、吸附等功能;在生物方面,具有一定生物相容性能,可作为生物结构材料等.但也有它的缺点,如脆性.因此研究开发新型功能陶瓷是材料科学中的一个重要领域.
按化学成分划分
主要分为两类:一类是纯氧化物陶瓷,如Al2O3、ZrO2、MgO、CaO、BeO、ThO2等;另一类是非氧化物系陶瓷,如碳化物、硼化物、氮化物和硅化物等.
按性能与特征划分
可分为:高温陶瓷、超硬质陶瓷、高韧陶瓷、半导体陶瓷.电解质陶瓷、磁性陶瓷、导电性陶瓷等.随着成分、结构和工艺的不断改进,新型陶瓷层出不穷.
按其应用不同划分
又可将它们分为工程结构陶瓷和功能陶瓷两类.1年前查看全部
- 【锆(Zr)的一种氧化物是耐高温的新型陶瓷材料,经测定,锆原子核内有51个中子,核外有40个电子,
【锆(Zr)的一种氧化物是耐高温的新型陶瓷材料,经测定,锆原子核内有51个中子,核外有40个电子,
锆(Zr)的一种氧化物是耐高温的新型陶瓷材料,经测定,锆原子核内有51个中子,核外有40个电子,其氯化物的相对分子质量为233,若锆钻氯化物和这种氧化物中的化合价相同.则氧化物的化学式为( )
因为:锆的氯化物的相对分子质量为233.
∴91+35.5X=233
【想问问这个公式是什么,还有35. 钱的前身21年前3
钱的前身21年前3 -
 327484693 共回答了20个问题
327484693 共回答了20个问题 |采纳率90%因为Cl的化合价为-1价 所以和Zr组成的氯化物的 化学式一定是 ZrClx
那么该物质的分子量计算方法就是 91+35.5X=233 35.5是氯的原子量1年前查看全部
- (16分)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
(16分)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:

(1)配平上述反应的化学方程式(将化学计量数填在方框内);
(2)该反应的氧化剂是 ,其还原产物是 ;
(3)该反应产生标准状况下11.2升CO气体,则电子转移 摩尔。
(4)若有1摩尔焦炭与足量的SiO2、氮气反应,电子转移 (填大于、等于或小于)2摩尔,理由是 。 诚实_hh1年前1
诚实_hh1年前1 -
 紫眸豹豹 共回答了27个问题
紫眸豹豹 共回答了27个问题 |采纳率88.9%(1)3,6,2,1,6 (4分)
(2)N2(2分),Si3N4(2分)
(3)1 (3分)
(4)小于(2分) 可逆反应不能进行到底(3分)。
略1年前查看全部
- “神七”成功了,我们为之自豪,我们要学着了解科学、了解物质.氮化硅是一种新型陶瓷材料的主要成分,能承受高温,可用于制造业
“神七”成功了,我们为之自豪,我们要学着了解科学、了解物质.氮化硅是一种新型陶瓷材料的主要成分,能承受高温,可用于制造业、航天工业等领域.请推测氮化硅的化学式( )
A.Si3N4
B.Si4N3
C.Si3N7
D.Si7N3 linhui_ruru1年前1
linhui_ruru1年前1 -
 zhupch 共回答了12个问题
zhupch 共回答了12个问题 |采纳率83.3%解题思路:根据氮、硅的原子结构示意图,得氮原子的最外层电子数为5,则容易得3个电子,达稳定结构,带3个负电荷,化合价为-3价;硅原子最外层电子数为4,易失去4个电子,达到稳定结构,带4个正电荷,化合价为+4价.①根据化合价的原则(在化合物中正、负化合价的代数和为零);②化学式中元素的位置:“正价左,负价右”;③化合价数值交叉法书写化学式(即将正、负化合价的数值交叉到相应符号的右下角,但注意原子团看作一体,含约数的一般要约分).第一种方法:设氮化硅的化学式为SixNY,再标出化合价
+4
Si x
-3
N Y,根据化合价的原则(在化合物中正、负化合价的代数和为零)所以 [X/Y]=[3/4],故选A.
第二种方法:①化学式中元素的位置:“正价左,负价右”;②化合价数值交叉法书写化学式(即将正、负化合价的数值交叉到相应符号的右下角,但注意原子团看作一体,含约数的一般要约分).故选A.点评:
本题考点: 有关化学式的计算和推断.
考点点评: 本题既考查了常见元素的化合价以及化合价的规律和原则,还考查了化学式的书写方法和技巧.1年前查看全部
- (2009•开封一模)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3Si
(2009•开封一模)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g)
Si3N4+6CO(g),下列叙述正确的是( )高温 .
A.氮化硅晶体属于分子晶体
B.氮化硅的摩尔质量为140g
C.上述反应中每生成1molSi3N4,N2得到12mol电子
D.在氮化硅的合成反应中,N2是还原剂,SiO2是氧化剂 小草0011年前1
小草0011年前1 -
 LASTDRIVER 共回答了10个问题
LASTDRIVER 共回答了10个问题 |采纳率90%解题思路:反应3SiO2+6C+2N2
Si3N4+6CO中,C元素化合价升高,N元素化合价降低,反应中C是还原剂,N2是氧化剂,结合反应的方程式解答.高温 .A、氮化硅氮原子和硅原子构成的原子晶体,不是分子晶体,故A错误;B、氮化硅的摩尔质量为140g/mol,故B错误;C、反应3SiO2+6C+2N2 高温 . Si3N4+6CO中,所有C元素化合价共升高了12价,所以每生成1mol...
点评:
本题考点: 氧化还原反应的电子转移数目计算;分子晶体.
考点点评: 本题考查氧化还原反应,题目难度不大,注意把握元素化合价的变化,为解答该题的关键,易错点为C,注意从化合价变化的角度判断转移电子的数目.1年前查看全部
- (2012•梧州模拟)氮化硅(Si3N4)是一种新型陶瓷材料,它可通过以下反应制得:3SiO2+6C+2N2
(2012•梧州模拟)氮化硅(Si3N4)是一种新型陶瓷材料,它可通过以下反应制得:3SiO2+6C+2N2
Si3N4+6CO,有关说法不正确的是( )高温 .
A.该反应的平衡常数表达式为K=c6(CO) c2(N2)
B.若增大压强,则上述平衡向逆反应方向移动
C.该反应中只有N2是氧化剂
D.该反应在高温下反应,△H一定大于零 湖光月夜1年前1
湖光月夜1年前1 -
 xiaowu1532 共回答了21个问题
xiaowu1532 共回答了21个问题 |采纳率90.5%解题思路:A、化学平衡常数K=[生成物平衡浓度系数次幂之积/反应物平衡浓度系数次幂之积];
B、增大压强,平衡向着气体系数和减小的方向进行;
C、化合价降低元素所在的反应物是氧化剂;
D、根据反应能否自发进行的判据△H-T△S<0来判断.A、3SiO2+6C+2N2
高温
.
Si3N4+6CO的平衡常数表达式K=
c6(CO)
c2(N2),故A正确;
B、增大压强,平衡向着气体系数和减小的方向即逆方向进行,故B正确;
C、化合价降低的元素是N,所在的反应物氮气是氧化剂,故C正确;
D、在高温下进行的反应,不一定是吸热反应,故D错误.
故选D.点评:
本题考点: 化学平衡的影响因素.
考点点评: 本题考查学生影响化学平衡移动的因素知识,注意知识的迁移和应用是关键,难度不大.1年前查看全部
- 已知氮、硅原子结构示意图如图. 氮化硅是一种新型陶瓷材料的
已知氮、硅原子结构示意图如图. 

氮化硅是一种新型陶瓷材料的主要成分,能承受高温,可用于制造业、航天业等.
试写出氮化硅的化学式_ _________ .
医学研究表明:偏硅酸有软化血管的作用,对心脏病、高血压有一定疗效.偏硅酸是二元酸,又是含氧酸.则偏硅酸的化学式为 _________ . 也曾因梦送钱财1年前1
也曾因梦送钱财1年前1 -
 红糖棒棒 共回答了22个问题
红糖棒棒 共回答了22个问题 |采纳率81.8%Si 3 N 4 ;H 2 SiO 3 .1年前查看全部
- (2014•海港区一模)下列关于耐高温新型陶瓷材料氮化硅(Si3N4)的叙述正确的是( )
(2014•海港区一模)下列关于耐高温新型陶瓷材料氮化硅(Si3N4)的叙述正确的是( )
A.氮化硅中氮元素的化合价为+4
B.氮化硅是有机高分子合成材料
C.氮化硅中硅与氮的质量比为3:4
D.氮化硅中氮元素的质量分数为40% daphne2261年前1
daphne2261年前1 -
 8291101 共回答了12个问题
8291101 共回答了12个问题 |采纳率100%解题思路:A、根据化合价原则进行分析.
B、有机高分子合成材料是指人工合成的有机高分子(相对分子质量很大的有机物)材料,据此进行分析判断.
C、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
D、根据化合物中元素的质量分数公式进行分析解答.A、硅元素显+4价,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:3×(+4)+4x=0,则x=-3价,故选项说法错误.
B、氮化硅不含碳元素,不属于有机物,不是有机高分子合成材料,故选项说法错误.
C、氮化硅中硅与氮的质量比为(28×3):(14×4)≠3:4,故选项说法错误.
D、氮化硅中氮元素的质量分数为[14×4/28×3+14×4]×100%=40%,故选项说法正确.
故选:D.点评:
本题考点: 有关元素化合价的计算;元素质量比的计算;元素的质量分数计算;有机高分子材料的分类及鉴别.
考点点评: 本题难度不大,考查同学们结合新信息、灵活运用有机高分子合成材料、化学式的有关计算进行分析问题、解决问题的能力.1年前查看全部
- (2009•兖州市模拟)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3S
 (2009•兖州市模拟)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g)
(2009•兖州市模拟)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g)
Si3N4(s)+6CO(g)高温 .
(1)该反应的平衡常数表达式为K=K=
,[c(CO)]6 [c(N2)]2 K=;
,[c(CO)]6 [c(N2)]2
(2)若知上述反应为放热反应,则升高温度,其平衡常数值______(选填“增大”、“减小”
或“不变”); 若已知CO生成速率为v(CO)=18mol•L-1•min-1,则N2消耗速率为v(N2)=______.
(3)达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图:
若不改变N2、CO的量,则图中t4时引起平衡移动的条件可能是______;图中t6时引起变化的条件是______;图中表示平衡混合物中CO的含量最高的一段时间是______. zcqmig1年前1
zcqmig1年前1 -
 yanmingth 共回答了24个问题
yanmingth 共回答了24个问题 |采纳率95.8%解题思路:(1)根据平衡常数等于气体生成物的浓度幂之积除以气体反应物的浓度幂之积计算;
(2)反应放热,△H<0,根据升高温度平衡移动的方向判断平衡常数的变化;根据速率之比等于化学计量数之比计算反应速率;
(3)t4时正逆反应速率都较原平衡时的速率大,可升高温度或增大压强;t6时正逆反应速率都较原平衡时的速率大,但平衡不移动,前后气体系数之和不等,只能是使用催化剂;在反应向逆反应之前衡混合物中CO的含量最高;(1)平衡常数等于气体生成物的浓度幂之积除以气体反应物的浓度幂之积,则K=
[c(CO)]6
[c(N2)]2,故答案为:K=
[c(CO)]6
[c(N2)]2;
(2)反应放热,△H<0,升高温度平衡移动逆反应方向移动,平衡常数减小,速率之比等于化学计量数之比,则v(N2)=[1/3]×v(CO)=[1/3]×18mol•L-1.min‑1=6 mol•L-1.min‑1,
故答案为:减小;6 mol•L-1•min-1;
(3)t4时正逆反应速率都较原平衡时的速率大,可升高温度或增大压强;t6时正逆反应速率都较原平衡时的速率大,但平衡不移动,前后气体系数之和不等,只能是使用催化剂;在t4时反应向逆反应方向移动,则t3~t4时平衡混合物中CO的含量最高,
故答案为:升高温度或缩小体积;加入了催化剂;t3~t4.点评:
本题考点: 化学平衡的影响因素;化学平衡常数的含义;用化学平衡常数进行计算.
考点点评: 本题考查化学平衡的移动,难度不大,做题时注意外界条件对化学平衡的影响.1年前查看全部
- (17分)氮化硅是一种新型陶瓷材料,它可由石英晶体与焦炭颗粒在高温的氮气流中,通过如下反应制得:3SiO 2 + 6C
(17分)氮化硅是一种新型陶瓷材料,它可由石英晶体与焦炭颗粒在高温的氮气流中,通过如下反应制得:3SiO 2 + 6C + 2N 2
 Si 3 N 4 + 6CO,该反应过程中的能量变化如图⑵所示;回答下列问题:
Si 3 N 4 + 6CO,该反应过程中的能量变化如图⑵所示;回答下列问题: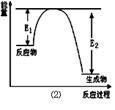
(1)上述反应中的还原剂是 ,还原产物是 。
(2)该反应是 (填“吸热”或“放热”)反应。
(3)在一定温度下,上述反应在4L密闭容器内进行,用M、N两种物质描述其物质的量随时间变化的曲线如图⑶所示: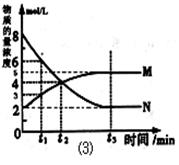
①M、N表示的物质分别为 、 。
②比较t 2 时刻,正逆反应速率大小 (正)
(正)  (逆) 。
(逆) 。
(填“>”、“=”、“<”)。.
③若t 2 =2min,计算反应开始至t 2 时刻,M的平均化学反应速率为 。
④t 3 时刻化学反应达到平衡时反应物的转化率为 。
(4)①某种氢燃料电池是用固体金属氧化物陶瓷作电解质,某电极上发生的电极反应为:A极H 2 -2e - +O 2 - ===H 2 O;则A极是电池的 极 (填“正”或“负”)。
②上述合成氮化硅的反应产生的尾气不能排放,经过处理以后可以用下图所示的仪器测量尾气中CO的含量。多孔电极中间的固体氧化锆—氧化钇为电解质,这种固体电解质允许O 2- 在其间通过,其工作原理如图⑷所示,其中多孔Pt电极a、b分别是气体CO、O 2 的载体。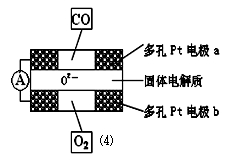
Ⅰ.该电池的正极为 (填a或b);O 2 流向 (填 “正极”或“负极”)
Ⅱ.该电池的正极反应式为 ,负极反应式为 。 pure2181年前1
pure2181年前1 -
 汤潜 共回答了22个问题
汤潜 共回答了22个问题 |采纳率95.5%(1)C;Si 3 N 4 ;(2)放热 ;(3)① CO 、N 2 ; ② (正) > (逆) ③ 1mol/(L·min);④ 75% ;(4)① 负 。②Ⅰ. b ;负极; Ⅱ.正极反应为O 2 +4e - ===2O 2 - ;负极反应为CO-2...1年前查看全部
- 氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2+6C+2N2
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2+6C+2N2
Si3N4+6CO.下列叙述正确的是( )高温 .
A.Si3N4的摩尔质量是154g
B.在氮化硅的合成反应中,N2是还原剂,SiO2是氧化剂
C.Si3N4既是氧化产物,又是还原产物
D.1mol SiO2发生反应,N2得到4mol电子 toofmw1年前1
toofmw1年前1 -
 xpai 共回答了20个问题
xpai 共回答了20个问题 |采纳率85%解题思路:该反应中N元素化合价由0价变为-3价、C元素化合价由0价变为+2价,所以氮气是氧化剂、碳是还原剂、氮化硅是还原产物、一氧化碳是氧化产物,再结合二氧化硅和转移电子之间的关系式计算.A.Si3N4的摩尔质量是154g/mol,故A错误;
B.该反应中N元素化合价由0价变为-3价、C元素化合价由0价变为+2价,所以氮气是氧化剂,二氧化硅中各元素化合价不变,所以二氧化硅既不是氧化剂也不是还原剂,故B错误;
C.氮化硅是还原产物,故C错误;
D.当1mol SiO2发生反应,有[2/3]mol氮气参加反应,则N2得到电子的物质的量=
2
3mol×6=4mol,故D正确;
故选D.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查了氧化还原反应,明确反应中元素化合价变化即可解答,根据基本概念、元素化合价变化、物质之间的关系式解答,题目难度不大.1年前查看全部
- 锆(Zr)的一种氧化物是耐高温的新型陶瓷材料,经测定,锆原子核内有51个中子,核外有40个电子,其氯化物的相对分子质量为
锆(Zr)的一种氧化物是耐高温的新型陶瓷材料,经测定,锆原子核内有51个中子,核外有40个电子,其氯化物的相对分子质量为233,若锆的氯化物和氧化物中锆的化合价相同.则氧化物的化学式为( )
A. Zr2O
B. ZrO
C. Zr2O3
D. ZrO2 郑春映1年前2
郑春映1年前2 -
 中文组合1 共回答了22个问题
中文组合1 共回答了22个问题 |采纳率86.4%解题思路:就原子来说,质子数=原子序数=核外电子数,质子数+中子数=相对原子质量.首先计算出锆原子的相对原子质量,然后根据氯化物的相对分子质量为233,可以算出锆元素的化合价,最后写出氧化物的化学式.就原子来说,质子数=原子序数=核外电子数,质子数+中子数=相对原子质量.根据题目信息可知,锆原子核内有51个中子,核外有40个电子,所以质子有40个,相对原子质量=51+40=91.
设锆元素的化合价为+X,其氯化物的化学式为:ZrClx,
∵锆的氯化物的相对分子质量为233.
∴91+35.5X=233
得:X=4
∵在锆的氧化物中锆的化合价是+4价,氧元素的化合价是-2价.
∴氧化物的化学式为:ZrO2,故选D.点评:
本题考点: 有关化学式的计算和推断;常见元素与常见原子团的化合价;化合价规律和原则.
考点点评: 掌握相对原子质量和质子、中子之间的关系式,学会根据化合价书写物质的化学式.1年前查看全部
- 氮化硅(Si 3 N 4 )是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中通过以下反应制得 (1)配平上述反应的化
氮化硅(Si 3 N 4 )是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中通过以下反应制得 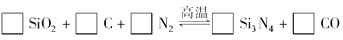
(1)配平上述反应的化学方程式(将化学计量数填在方框内);
(2)该反应中的氧化剂是________,其还原产物是________;
(3)该反应的平衡常数表达式为K=________;
(4)若知上述反应为放热反应,则其反应热ΔH________零(填“大于”“小于”或“等于”);升高温度,其平衡常数值________(填“增大”“减小”或“不变”);
(5)若使压强增大,则上述平衡向________反应方向移动(填“正”或“逆”);
(6)若已知CO生成速率为v(CO)=18 mol/(L·min),则N 2 消耗速率为v(N 2 )=________mol/(L·min). 永远期待中1年前1
永远期待中1年前1 -
 jie_511 共回答了20个问题
jie_511 共回答了20个问题 |采纳率80%1年前查看全部
- (2009•营口模拟)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
(2009•营口模拟)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
3SiO2(s)+6C(s)+2N2(g) Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g)
(1)该反应的氧化剂是______,其还原产物是______;
(2)该反应的平衡常数表达式为 K=c6(CO) c2(N2) ;c6(CO) c2(N2)
(3)若知上述反应为放热反应,则其反应热△H______0(填“>”、“<”或“=”);升高温度,其平衡常数值______(填“增大”、“减小”或“不变”); 若已知CO生成速率为v(CO)=18mol•L-1•min-1,则N2消耗速率为v(N2)=______.
(4)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率v与时间t的关系如图.
图中t4时引起平衡移动的条件可能是______;图中表示平衡混合物中CO的含量最高的一段时间是______.
(5)若该反应的平衡常数为K=729,则在同温度下1L密闭容器中,足量的SiO2和C与2mol N2充分反应,则N2的转化率是多少?(写出计算过程)提示:272=729. nduo1年前1
nduo1年前1 -
 dhysfu 共回答了17个问题
dhysfu 共回答了17个问题 |采纳率88.2%解题思路:(1)根据化合价的变化判断氧化剂和还原产物;
(2)根据平衡常数等于气体生成物的浓度幂之积除以气体反应物的浓度幂之积计算;
(3)反应放热,△H<0,根据升高温度平衡移动的方向判断平衡常数的变化,根据速率之比等于化学计量数之比计算反应速率;
(4)t4时正逆反应速率都较原平衡时的速率大,可升高温度或增大压强,在反应向逆反应之前衡混合物中CO的含量最高;
(5)根据平衡常数计算.(1)反应中N元素的化合价降低,有0价降为-3价,则氧化剂为氮气,氧化剂对应的生成物为还原产物,应为氮化硅,
故答案为:氮气;氮化硅;
(2)平衡常数等于气体生成物的浓度幂之积除以气体反应物的浓度幂之积,则K=
c6(CO)
c2(N2),故答案为:K=
c6(CO)
c2(N2);
(3)反应放热,△H<0,升高温度平衡移动逆反应方向移动,平衡常数减小,速率之比等于化学计量数之比,
则v(N2)=[1/3]×v(CO)=[1/3×18mol•L-1.min‑1=6 mol•L-1.min‑1,
故答案为:<;减小;6 mol•L-1.min‑1;
(4)t4时正逆反应速率都较原平衡时的速率大,可升高温度或增大压强,在t4时反应向逆反应方向移动,则t3~t4时平衡混合物中CO的含量最高,
故答案为:升高温度或增大压强,t3~t4;
(5)设反应的N2的物质的量为x,
3SiO2(s)+6C(s)+2N2(g) Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g)
起始:2mol 0
转化:x 3x
平衡:2-x 3x
则平衡时N2的浓度为(2-x)mol/L,CO的浓度为3x mol/L,则有:
(3x)6
(2−x)2]=729,解之得x=1,
则N2的转化率是
1
2×100%=50%,
故答案为:50%.点评:
本题考点: 化学平衡的计算;氧化还原反应;吸热反应和放热反应;反应速率的定量表示方法;化学平衡常数的含义;化学平衡的影响因素;化学反应速率与化学平衡图象的综合应用.
考点点评: 本题考查化学平衡的有关计算,本题难度较大,做题时注意平衡常数的计算和应用.1年前查看全部
- 锆(Zr)的一种氧化物是耐高温的新型陶瓷材料,经测定,锆原子核内有51个中子,核外有40个电子,其氯化物的相对分子质量为
锆(Zr)的一种氧化物是耐高温的新型陶瓷材料,经测定,锆原子核内有51个中子,核外有40个电子,其氯化物的相对分子质量为233,若锆的氯化物和氧化物中锆的化合价相同.则氧化物的化学式为( )
A. Zr2O
B. ZrO
C. Zr2O3
D. ZrO2 飘飘红辣椒1年前1
飘飘红辣椒1年前1 -
 皮皮和宝宝 共回答了20个问题
皮皮和宝宝 共回答了20个问题 |采纳率90%解题思路:就原子来说,质子数=原子序数=核外电子数,质子数+中子数=相对原子质量.首先计算出锆原子的相对原子质量,然后根据氯化物的相对分子质量为233,可以算出锆元素的化合价,最后写出氧化物的化学式.就原子来说,质子数=原子序数=核外电子数,质子数+中子数=相对原子质量.根据题目信息可知,锆原子核内有51个中子,核外有40个电子,所以质子有40个,相对原子质量=51+40=91.
设锆元素的化合价为+X,其氯化物的化学式为:ZrClx,
∵锆的氯化物的相对分子质量为233.
∴91+35.5X=233
得:X=4
∵在锆的氧化物中锆的化合价是+4价,氧元素的化合价是-2价.
∴氧化物的化学式为:ZrO2,故选D.点评:
本题考点: 有关化学式的计算和推断;常见元素与常见原子团的化合价;化合价规律和原则.
考点点评: 掌握相对原子质量和质子、中子之间的关系式,学会根据化合价书写物质的化学式.1年前查看全部
- 1.锆(Zr)的一种氧化物是一种耐高温的新型陶瓷材料,经测定锆原子核内有51个中子,核外有40个电子,其氯化物的相对分子
1.锆(Zr)的一种氧化物是一种耐高温的新型陶瓷材料,经测定锆原子核内有51个中子,核外有40个电子,其氯化物的相对分子质量是233.若锆在氯化物和氧化物中的化合价相同,则该氧化物的化学式为( )
A.Zr2O B.ZrO C.Zr2O3 D.ZrO2
2.下列叙述中,能用质量守恒定律解释的是( )
A.化学反应中反应物的质量等于生成物的质量
B.镁在氧气中燃烧后,生成物的质量大于镁的质量
C.氯酸钾加热分解后,生成的氯化钾质量比氯酸钾减少了
D.1.24g磷和1.6g氧气化合,正好生成了2.84g的五氧化二磷 轻轻如风1年前9
轻轻如风1年前9 -
 lq_42 共回答了18个问题
lq_42 共回答了18个问题 |采纳率77.8%1 根据原子核内有51个中子,核外有40个电子,可知Zr有40个电子,质量数为91
根据氯化物的相对分子质量是233,可知含有Cl的个数为(233-91)/35.5=4
化学式为ZrCl4 +4价 氧化物为ZrO2 选A
2 质量守恒定只能应用于化学反应
反应前后,各反应物的总质量=各生成物的总质量
A 不正确 应该是,化学反应中各反应物的总质量等于各生成物的总质量
B.正确 镁条比燃烧后所得氧化镁的质量小,能用质量守恒定律解释,因为生成的MgO中还有O2的质量
C.正确 氯酸钾加热分解后,生成的氯化钾质量比氯酸钾减少了,能用质量守恒定律解释,因为生成的KCl中少了O2的质量
D.正确 1.24g磷和1.6g氧气化合,正好生成了2.84g的五氧化二磷,符合定义.1年前查看全部
- 氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2+6C+2N2=高温=Si3N4+6CO.下列叙述正确的是
A该反应的氧化剂是SiO2和N2
B该反应的还原产物是Si3N4
C该反应中氧化剂和还原剂的质量比为9:7
D1mol Si3N4生成时共转移6mol电子
还有B中还原产物应该是氧化剂被还原的产物吧,就应该是CO? 长生剑玉京1年前3
长生剑玉京1年前3 -
 魔域桃源88 共回答了17个问题
魔域桃源88 共回答了17个问题 |采纳率94.1%A 反应中N的化合价降低,所以N2是氧化剂,Si化合价没变化,所以不是氧化剂
B 氧化剂对应的是还原产物,所以B正确
C 氧化剂 N2 还原剂C 质量比 2*28:6*12=7:18
D 该反应转移电子数:N从0价到-3,降低3,一共4个,所以转移为12mol电子
综上 B1年前查看全部
- (2005•杭州)氮化硅(Si3N4)是一种新型陶瓷材料的主要成分,能承受高温,可用于制造业、航天工业等.氮化硅属于(
(2005•杭州)氮化硅(Si3N4)是一种新型陶瓷材料的主要成分,能承受高温,可用于制造业、航天工业等.氮化硅属于( )
A.金属单质
B.非金属单质
C.化合物
D.混合物 思念落叶1年前1
思念落叶1年前1 -
 daili147 共回答了18个问题
daili147 共回答了18个问题 |采纳率94.4%解题思路:本题考查利用化合物的概念来判断物质是否为化合物,抓住化合物中至少两种元素,且只有一种物质组成.氮化硅中只有一种物质组成的,并且氮化硅是由硅元素、氮元素两种元素组成的,所以氮化硅是化合物,故选C.
点评:
本题考点: 单质和化合物的判别.
考点点评: 应抓住概念的要点来判断物质的类别,了解常见物质的组成.1年前查看全部
- 氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:

(1)该反应的平衡常数表达式为K=c6(CO) c2(N2) ;c6(CO) c2(N2)
(2)若知上述反应为放热反应,则其反应热△H______零(填“大于”、“小于”或“等于”);升高温度,其平衡常数值______(填“增大”、“减小”或“不变”);
(3)若使压强增大,则上述平衡向______反应方向移动(填“正”或“逆”);
(4)若已知CO生成速率为v(CO)=18mol/(L.min),则N2消耗速速率为v(N2)=______ mol/(L.min). xgz5011年前1
xgz5011年前1 -
 037ahhf 共回答了18个问题
037ahhf 共回答了18个问题 |采纳率94.4%解题思路:(1)化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,注意固体、纯液体浓度为常数,不用写固体、纯液体的浓度;
(2)对于放热反应,反应热△H<0;
该反应为放热反应,升高温度平衡逆反应进行,化学平衡常数减小;
(3)增大压强平衡向气体体积减小的方向移动;
(4)根据速率之比等于化学计量数之比计算.(1)可逆反应3SiO2(s)+6C(s)+2N2(g)⇌Si3N4(s)+6CO(g)的平衡常数K=
c6(CO)
c2(N2),故答案为:
c6(CO)
c2(N2);
(2)对于放热反应,反应热△H<0;该反应为放热反应,升高温度平衡逆反应进行,化学平衡常数减小,故答案为:小于;减小;
(3)该反应正反应是气体体积增大的反应,增大压强平衡向气体体积减小的方向移动,即向逆反应移动,故答案为:逆;
(4)已知CO生成速率为v(CO)=18mol/(L•min),根据速率之比等于化学计量数之比,则N2消耗速率为:v(N2)=[1/3]v(CO)=[1/3]×18mol/(L•min)=6mol/(L•min),故答案为:6.点评:
本题考点: 化学平衡常数的含义;反应速率的定量表示方法;化学平衡的影响因素.
考点点评: 本题考查化学平衡常数与影响因素、影响平衡移动的因素、化学反应速率计算等,比较基础,注意方程式中物质的状态,注意基础知识的掌握.1年前查看全部
- 锆(Zr)的一种氧化物是耐高温的新型陶瓷材料,经测定,锆原子核内有51个中子,核外有40个电子,其氯化物的相对分子质量为
锆(Zr)的一种氧化物是耐高温的新型陶瓷材料,经测定,锆原子核内有51个中子,核外有40个电子,其氯化物的相对分子质量为233,若锆的氯化物和氧化物中锆的化合价相同.则氧化物的化学式为( )
A. Zr2O
B. ZrO
C. Zr2O3
D. ZrO2 溪里鱼1年前1
溪里鱼1年前1 -
 安眠花宝 共回答了20个问题
安眠花宝 共回答了20个问题 |采纳率90%解题思路:就原子来说,质子数=原子序数=核外电子数,质子数+中子数=相对原子质量.首先计算出锆原子的相对原子质量,然后根据氯化物的相对分子质量为233,可以算出锆元素的化合价,最后写出氧化物的化学式.就原子来说,质子数=原子序数=核外电子数,质子数+中子数=相对原子质量.根据题目信息可知,锆原子核内有51个中子,核外有40个电子,所以质子有40个,相对原子质量=51+40=91.
设锆元素的化合价为+X,其氯化物的化学式为:ZrClx,
∵锆的氯化物的相对分子质量为233.
∴91+35.5X=233
得:X=4
∵在锆的氧化物中锆的化合价是+4价,氧元素的化合价是-2价.
∴氧化物的化学式为:ZrO2,故选D.点评:
本题考点: 有关化学式的计算和推断;常见元素与常见原子团的化合价;化合价规律和原则.
考点点评: 掌握相对原子质量和质子、中子之间的关系式,学会根据化合价书写物质的化学式.1年前查看全部
大家在问
- 1一个长方体 切成3个完全一样的正方体 每个正方体的表面积是18平方分米 原来长方体的表面积是?
- 2站可以组什么词
- 3设计实验证明蛋白质在人体内被消化
- 4用所给单词的适当形式填空。 I()(go)on a trip tomorrow YesterdayI()(see)my
- 5“我的梦想,在每个醒来的早晨敲打我的心房,告诉自己成功的道路还很漫长。所有经历风雨的温柔与坚强,今天我终于站在这年轻的战
- 6英语翻译Investors in Money Market:Provides a placefor warehousin
- 7一个圆柱体,它的高是3.2米,低面半径是62.5厘米,请问该圆柱体的面积怎么算
- 8《生命 生命》这篇课文讲了那些关于生命的事例.
- 9如图,D为等边三角形ABC内一点,DB=DA,BF=AB,∠1=∠2,则∠BFD的度数是多少?
- 10the tuition and fees for college are much higher than ever b
- 11mach当火柴讲时有复数吗
- 129—1=8*1 25—9=8*2 49—25=8*3 81—49=8*4,观察上式,你发现了什么规律?用式子(字母)表示
- 13Is his birthday on january 5th? 回答用ye
- 14学会放弃 作文
- 15一下几何体中,对角线长度一定相等的是( )

