把分步算式列成综合算式216÷9=24 50-4=46 24÷6=4 前提是只能用两个÷ 一个- 最后答案是4
 white_knight2022-10-04 11:39:541条回答
white_knight2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 xxye 共回答了24个问题
xxye 共回答了24个问题 |采纳率91.7%- 50-216÷9÷6=4
- 1年前
相关推荐
- 磷酸是几元酸?能电离出几个氢离子就是几元酸 是第一步 还是分步总共电离出的?
 cdnj1年前1
cdnj1年前1 -
 叶子静 共回答了19个问题
叶子静 共回答了19个问题 |采纳率89.5%磷酸是三元弱酸,可电离出3个H+ ,由于是弱酸,分步电离,一次电离出一个H+,因此能三级电离1年前查看全部
- 用三个棱长为4分米的正方体拼成一个长方体,求长方体的表面积.(式子要分步的 )
 nvkpd1年前2
nvkpd1年前2 -
 LY0xFFFF 共回答了19个问题
LY0xFFFF 共回答了19个问题 |采纳率78.9%那长方体的长为12宽于高都为4
那就是长*宽 12*4=48 长*高 12*4=48 宽*高 4*4=16
表面积 (48+48+16)*2=2241年前查看全部
- 硫酸会不会分步电离,为什么?若会,那硫酸钠和硫酸会生成硫酸氢钠吗?
 苯蛋er1年前3
苯蛋er1年前3 -
 凡东 共回答了15个问题
凡东 共回答了15个问题 |采纳率80%硫酸的电离本来是分布的,但高中教材里面认为硫酸是强电解质,就认为是一步电离.大学里好像会改过来的.
会生成硫酸氢钠,当硫酸过量时.1年前查看全部
- 水果店运来3车苹果,每车重200千克.这些苹果正好能装25箱,平均每箱苹果重多少千克?分步怎么写?
 笨笨火1年前1
笨笨火1年前1 -
 阴气勃勃 共回答了19个问题
阴气勃勃 共回答了19个问题 |采纳率94.7%200×3=600(千克)
600÷25=24(千克)1年前查看全部
- 南北半球副热带环流位置的成因?区别亚热带常绿阔叶林带和亚热带常绿硬叶林带分步差异?
 一地在九1年前1
一地在九1年前1 -
 ss累了13 共回答了23个问题
ss累了13 共回答了23个问题 |采纳率87%洋流的形成之初主要是受盛行风的影响,就是我们说的风海流.三圈环流中,低纬信风,北半球是东北风,吹拂海水自东向西流动,遇见大陆后,向北流动,即为大陆东岸暖流.中纬度西风为西南风,吹拂海水自西向东流动,遇见陆地后向北向南流动,即为大陆西岸的中低纬寒流和中高纬暖流.
不知道你看明白没有,南半球一样的原因.归根到底就是先受盛行风影响出现风海流,再受陆地阻挡,改变水流方向.
亚热带常绿阔叶林带对应的气候是亚热带季风气候,出现在25--35度大陆东岸.
亚热带常绿硬叶林对应的气候是地中海气候,分布在30--40度大陆西岸1年前查看全部
- 一个直角三角形的三条边的长度分别为6厘米,8厘米,10厘米,求这个直角三角形面积 要分步答题【五年级的题】
 xnty19851年前1
xnty19851年前1 -
 Zorro2002 共回答了16个问题
Zorro2002 共回答了16个问题 |采纳率93.8%设此直角三角形的面积为s,短直角边长为a,长直角边长为b,则a=6,b=8.根据面积公式,得:s=1/2*ab=1/2*6*8=24(平方厘米)---①.另设此直角三角形的斜边长为c,斜边上的高长为h.则,由面积公式,得:s=1/2*ch.由①知:s=1/2*ab=24,所以1/2*ch=24.因为斜边c的长为10厘米,即:1/2*10*h=24,所以,可得:h=24/5=4.8(厘米).1年前查看全部
- H3PO4在水中的电离方程式是什么?(分步电离)
 kankan200620061年前2
kankan200620061年前2 -
 zbwzmc 共回答了19个问题
zbwzmc 共回答了19个问题 |采纳率84.2%H3PO4==H+ + H2PO4-
H2PO4- ==H+ +HPO42-
HPO42-==H+ PO43-
第一步电离程度较大,第二步次之,第三部最小.
都是可逆的.1年前查看全部
- 请列分步算式,和单位名称!1.一个长方形,长30米,宽20米,如果宽减少5米,活动场地的面积会减少多少?2.一个长方形,
请列分步算式,和单位名称!
1.一个长方形,长30米,宽20米,如果宽减少5米,活动场地的面积会减少多少?2.一个长方形,长30米,宽20米,如果长增加10米,活动场地的面积会增加多少?3.一个长方形,长30米,宽20米,如果长增加10米、宽减少5米,活动场地的面积会发生怎样的变化? comenow20041年前3
comenow20041年前3 -
 jyes826fk1da0 共回答了18个问题
jyes826fk1da0 共回答了18个问题 |采纳率94.4%{1}:30*20-30*{20-5}=...{平方米}{2}:{30+10}*20-30*20=.平方米
{3}:30*20=600{平方米}{30+10}*{20-5}=40*15=600{平方米}600平方米=600平方米 答 .不变.1年前查看全部
- 原电池 电解池 条件原电池 电解池 在书写化学方程式时条件(如电解这个条件)要写吗?各个极的分步反应的条件要写吗?
 贵州莽夫1年前2
贵州莽夫1年前2 -
 xibo_1983 共回答了18个问题
xibo_1983 共回答了18个问题 |采纳率83.3%电解池要写通电
原电池因为是要自发进行的,所以不写
各个极都不写条件1年前查看全部
- 1苯酚是弱电解质吗?2金属氧化物是强电解质吗?3氢氧化铜是分步电离的吗?4共价化合物一定是非电解质吗?
 victor2681年前1
victor2681年前1 -
 yardtau 共回答了14个问题
yardtau 共回答了14个问题 |采纳率85.7%1是(苯酚钠水解呢,所以苯酚是弱电解质)
2不一定(这也太绝对了吧,活泼金属氧化物是强电解质,这是没有错误的.由于在熔融状态下,全部电离为离子,可以导电.
它溶于水能导电的是对应的碱,变成了新的物质,新的物质也应该是强电解质,如氧化钠,在熔融状态下可以导电,溶于水生成氢氧化钠溶液,也可以导电.写离子方程式时,能拆开的物质是在溶液中全部电离的物质,而活泼金属的氧化物在水中不能存在,所以不能拆开.),
3不是(虽然是沉淀但是却是强电解质,为什么呢?因为沉淀并不是不溶而是难溶,它溶于水的部分是完全电离的,所以说是强电解质,一步电离,不会两步的),
4不是(举个例子双氧水H2O2也叫过氧化氢他就是弱电解质,但是是共价化合物)1年前查看全部
- 关于偏铝酸钠与碳酸的反应..用碳酸如何从偏铝酸钠中把氢氧化铝沉淀出来?化学方程式怎么写的?还有原理什么?是分步反应的吗?
关于偏铝酸钠与碳酸的反应..
用碳酸如何从偏铝酸钠中把氢氧化铝沉淀出来?化学方程式怎么写的?还有原理什么?是分步反应的吗?
额.那那个氢离子是水中的还是碳酸中的? fxcgfc453531年前2
fxcgfc453531年前2 -
 g9hd9 共回答了19个问题
g9hd9 共回答了19个问题 |采纳率94.7%反应原理是双水解,双水解就是互促到底的一种反应.归属复分解反应.其中偏铝酸根能够水解生成偏铝酸和氢氧根.而氢氧根又能与碳酸中的氢离子中和,所以随着氢氧根的减小,偏铝酸根就能彻底的转化成偏铝酸.偏铝酸不能单独存在所以结合一分子水生成氢氧化铝沉1年前查看全部
- 亚氯酸钠和硫酸分步反应方程式
 bofan_1191年前1
bofan_1191年前1 -
 IciIvi 共回答了16个问题
IciIvi 共回答了16个问题 |采纳率87.5%据我推算:
NaClO2+H2SO4===NaHSO4+HClO2
4HClO2===3 ClO2 + 1/2 Cl2 + 2H2O
第二个方程式是绝对正确的(见高等教育出版社 无机化学第四版下P477),第一个方程式是我推出来的,根据酸的解离常数,亚氯酸是1.1*10^-2,硫酸是二级解离常数是1.02*10^-2,也是就是说酸的强弱是硫酸>亚氯酸>硫酸氢根,所以推出的生成硫酸氢钠和亚氯酸.
希望能对你有所帮助.1年前查看全部
- 氯化铝和碳酸钠的水解方程是什么?碳酸钠分步水解,那还可以把三个式子合并吗?
 gauss161年前1
gauss161年前1 -
 ihvk8912612 共回答了16个问题
ihvk8912612 共回答了16个问题 |采纳率81.3%可以
2AlCl3+3Na2CO3=2Al(OH)3+3CO2+3H2O1年前查看全部
- 化学热力学中理想气体膨胀问题理想气体的等温膨胀,虽然始终态相同,一步膨胀致终态,所做的功最少.分步膨胀致终态,体系所做的
化学热力学中理想气体膨胀问题
理想气体的等温膨胀,虽然始终态相同,一步膨胀致终态,所做的功最少.分步膨胀致终态,体系所做的功将增大;所分步骤越多,体系做的功越大.当分成无数步减压膨胀的极限情况,体系将做最大功.
这是为何,求具体解释. 周村烧饼nemo1年前1
周村烧饼nemo1年前1 -
 zoyor6 共回答了28个问题
zoyor6 共回答了28个问题 |采纳率92.9%无限分步就把分子维持在原来的动能状态,相当于你不需要给大量分子加速,然后平衡了又摩擦散热(热损耗).1年前查看全部
- 一道应用题,用算式解,要过程!跪求!希望用分步算式!
一道应用题,用算式解,要过程!跪求!希望用分步算式!
商场购进一批洗衣机,按30%的利润定价,售出60%.以后打八折出售,这批洗衣机的实际利润是多少? susanhelen1年前6
susanhelen1年前6 -
 最爱紫园 共回答了26个问题
最爱紫园 共回答了26个问题 |采纳率92.3%令该批洗衣机总进价为m
按30%的利润定价,售出60%,售价为:m×(1+30%)×60% = 0.78m
剩余40%按八折出售,售价为:m×(1+30%)×40%×80% = 0.416m
总售价 = 0.78m+0.416m = 1.196m
实现利润:(1.196m-m)/m×100% = 19.6%1年前查看全部
- 如何分步鉴别苯乙醇甲醛苯酚和1已烯
 光影如电1年前1
光影如电1年前1 -
 gcj3b 共回答了20个问题
gcj3b 共回答了20个问题 |采纳率80%1已稀加溴变色1年前查看全部
- 求乙醛的银镜反应书中给的银镜反应是叠加后的总反应,我想知道其中的分步反应,书中写的是乙醛被氢氧化二氨合银氧化成乙酸,乙酸
求乙醛的银镜反应
书中给的银镜反应是叠加后的总反应,我想知道其中的分步反应,
书中写的是乙醛被氢氧化二氨合银氧化成乙酸,乙酸又与氨反应生成乙酸氨等
求具体的反应方程式,是分步的那种,不要叠加后的总反应
线上等,请不懂的不要凑热闹.
希望懂的人来,别像第一个自己不懂,就随便找类似的答案复制过来
求分布的化学反应方程式 痛也苦也1年前2
痛也苦也1年前2 -
 lbue 共回答了12个问题
lbue 共回答了12个问题 |采纳率100%CH3CHO + 2Ag(NH3)2OH → CH3COOH + 2Ag↓+ 4 NH3+ H2O
CH3COOH + NH4 — CH3COONH4
楼主你说的是这意思吗?这2个分步反应?1年前查看全部
- 氯化铝分步水解方程式?
 CHAVIO1年前4
CHAVIO1年前4 -
 郭雨涵 共回答了22个问题
郭雨涵 共回答了22个问题 |采纳率81.8%Al3+ + H2O ==== Al(OH)2+ + H+
Al(OH)2+ + H2O ==== Al(OH)2+ + H+
Al(OH)2+ + H2O ==== Al(OH)3+ + H+1年前查看全部
- 圆锥锥台表面积公式不要分步计算的,要直接求锥台表面积的公式
 薰烈1年前2
薰烈1年前2 -
 sophia715 共回答了19个问题
sophia715 共回答了19个问题 |采纳率89.5%“蔷薇失色”:您好.
如果一定要列总式的话,(不分步),公式如下:
锥台表面积=[(r²+R²)+L(r+R)]∏
其中r为上底半径,R为下底半径,L为锥台侧面长度,∏为圆周率.
以上公式我是从《常用金属材料手册》上摘录下来的,请核查,祝好,再见 .1年前查看全部
- 先列分步算式,再列综合算式,算24点
先列分步算式,再列综合算式,算24点
7、12、5、1 zaihang11年前4
zaihang11年前4 -
 jskw 共回答了18个问题
jskw 共回答了18个问题 |采纳率88.9%答:分步:7-5=2 2X1=2 2X12=24
综合:(7-5)X1X12=241年前查看全部
- 请问:24+8=32 根据分步算式怎样列出综合算式并计算?
 爱到你烦1年前1
爱到你烦1年前1 -
 zerohb 共回答了12个问题
zerohb 共回答了12个问题 |采纳率91.7%3*8+8=(3+1)*8=4*8=321年前查看全部
- 已知H2(g)+[1/2]O2(g)=H2O (l);△H=─285.8KJ/moL可通过两种途径来完成分步进
已知H2(g)+[1/2]O2(g)=H2O (l);△H=─285.8KJ/moL可通过两种途径来完成分步进行的热效应如下:
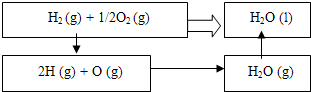
(1)H2(g)=2H△H1=+431.8KJ/moL
(2)[1/2]O2(g)=O (g)△H2=+244.3KJ/moL
(3)2H (g)+O (g)=H2O (g)△H3=______
(4)H2O (g)→H2O (l)△H=-44kJ/moL. 苏诺安安1年前1
苏诺安安1年前1 -
 yali5211 共回答了16个问题
yali5211 共回答了16个问题 |采纳率100%解题思路:依据热化学方程式和盖斯定律计算得到,反应流程中可知,反应H2(g)+[1/2]O2(g)=H2O (l)△H=─285.8KJ/moL,焓变等于反应(1)(2)(3)(4)反应焓变之和.H2(g)+[1/2]O2(g)=H2O (l)△H=-285.8KJ/moL,依据盖斯定律,反应焓变和起始物质和终了物质有关于变化过程无关,所以根据盖斯定律
(1)H2(g)=2H△H1=+431.8KJ/moL
(2)[1/2]O2(g)=O (g)△H2=+244.3KJ/moL
(3)2H (g)+O (g)=H2O (g)△H3
(4)H2O (g)→H2O (l)△H=-44kJ/moL
(1)+(2)+(3)+(4)=△H=-285.8KJ/moL
则(+431.8KJ/moL)+(+244.3KJ/moL)+△H3+(-44kJ/moL)=-285.8KJ/moL,
解得△H3=-917.9KJ/mol;
故答案为:-917.9KJ/mol.点评:
本题考点: 用盖斯定律进行有关反应热的计算.
考点点评: 本题考查了热化学方程式和盖斯定律的计算应用,理解盖斯定律含义是关键,题目较简单.1年前查看全部
- 求函数y=5x^3–3x^5+1的单调区间和极值!麻烦分步写出来!
 骑着蜗牛冲红灯1年前0
骑着蜗牛冲红灯1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 排列的计算“分步”和“分类”如何正确的区分?
 leifan11241年前1
leifan11241年前1 -
 我的世界只有自己 共回答了17个问题
我的世界只有自己 共回答了17个问题 |采纳率94.1%分步:所分各步相互依存,仅当所分各步依次完成,这事才算完成;
分类:所分各类相互独立,不论用哪一类办法中的哪一种方法'这事都可完成;(无需依次完成),1年前查看全部
- 已知多元弱酸在水溶液中的电离是分步进行的,且第一步电离程度远大于第二步电离程度,第二步电离程度远大于第三步电离程度…
已知多元弱酸在水溶液中的电离是分步进行的,且第一步电离程度远大于第二步电离程度,第二步电离程度远大于第三步电离程度…
今有HA、H2B、H3C三种一元、二元、三元弱酸,根据“较强酸+较弱酸盐=较强酸盐+较弱酸”的反应规律,它们之间能发生下列反应:
① HA+HC2-(少量)=A-+H2C-
② H2B(少量)+2 A-=B2-+2HA
③ H2B(少量)+ H2C-=HB-+H3C
回答下列问题:
⑴相同条件下,HA、H2B、H3C三种酸中酸性最强的是_________.
⑵A-、B2-、C3-、HB-、H2C-、HC2-六种离子中,最易结合质子的是_________,最难结合质子的是_________.
⑶下列反应的离子方程式中正确的是(填写标号)_________.
(A) H3C+3 A-=3HA+ C3-
(B) HB-+ A-= HA+ B2-
(C) H3C+ B2-= HB-+ H2C-
⑷完成下列反应的离子方程式.
①H3C+OH-(过量)= _________
②HA(过量)+ C3-= _________ cangjian1年前1
cangjian1年前1 -
 uhurtmyheart 共回答了22个问题
uhurtmyheart 共回答了22个问题 |采纳率86.4%HB-、H2C-、HC2-也看成酸
① HA+HC2-(少量)=A-+H2C-
说明多的HA不能与H2C-反应生成H3C,故酸性强弱
H2C-<HA<H3C
②H2B(少量)+2 A-=B2-+2HA
说明HA<HB-
③ H2B(少量)+ H2C-=HB-+H3C
生成的HB-不能与H2C-反应生成H3C,故
H2C-<HB-<H3C<H2B
得到酸性强弱HC2-<H2C-<HA<HB-<H3C<H2B
(1)H2B
(2)C3-(酸性越弱越容易结合质子)
(3)BC
(A)H2C-<HA,生成物应该是H2C-
(B)HA<HB-,对的
(C)HB-<H3C,对的
(4)①H3C+3OH-(过量)=C3- +3H2O
②2HA(过量)+ C3-= H2C-+2A-1年前查看全部
- 把俩道分步算式合成一道综合算式60-18=42 180除10=18
 1442951年前1
1442951年前1 -
 粉红少女猪 共回答了12个问题
粉红少女猪 共回答了12个问题 |采纳率83.3%=60-(180/10)1年前查看全部
- 应用题?(分步解答)快速1:甲乙两地相距1120千米,AB两车同时从甲地开往乙地,A车每小时行60千米,B车每小时行48
应用题?(分步解答)快速
1:甲乙两地相距1120千米,AB两车同时从甲地开往乙地,A车每小时行60千米,B车每小时行48千米,经过几小时两车相距57.6千米?
2:甲班有46人,乙班有53人,从甲班调几人到乙班,乙班的人数刚好是甲班的2倍? stillwater1年前1
stillwater1年前1 -
 温迪的奶茶 共回答了24个问题
温迪的奶茶 共回答了24个问题 |采纳率95.8%解:设经过x小时两车相距57.6千米,
则60x-48x=57.6
x=4.8
2.解:设甲班调了x人到乙班,则此时甲班人数为(46-x)人,乙班人数为(53+x)人,依据题意得:53+x=2(46-x),所以x=131年前查看全部
- 一道应用题 (只求分步计算)衬衫出售价60元,比进货价贵百分之二十,如果进货100件,则进货价可下降百分之十,但卖不完的
一道应用题 (只求分步计算)
衬衫出售价60元,比进货价贵百分之二十,如果进货100件,则进货价可下降百分之十,但卖不完的商品不能退.现衬衫进货100件,先按60元出售,然后降价百分之10出售,共卖出95件衬衫,盈利为900元.(1)原来进货价是多少?(2) 如果进货100件,全部按出售60元卖出,盈利多少元?(3)现在先按60元出售的衬衫 有多少件 wzm9998881年前1
wzm9998881年前1 -
 恰恰舞的风情 共回答了13个问题
恰恰舞的风情 共回答了13个问题 |采纳率92.3%(1)
原来进货价=60÷(1+20%)×(1-10%)=45元
(2)
100×(60-45)=1500元
(3)
设先按60元出售的衬衫 有x件,则降价百分之10后售出95-x件
60x+60(1-10%)(95-x)-45×100=900
60x+5130-54x-4500=900
9x=270
x=30
先按60元出售的衬衫 有30件1年前查看全部
- 应用题?分步计算妈妈去买苹果,带的钱如果买2千克还多4.8元,买5千克则差0.6元.每千克是多少元?
 crystaltoto1年前3
crystaltoto1年前3 -
 huangnnua 共回答了22个问题
huangnnua 共回答了22个问题 |采纳率90.9%4.8+0.6=5.4(元)
5-2=3(千克)
5.4/3=1.8(元)
答:每千克1.8元.1年前查看全部
- 解方程的应用题,最好用分步.甲,乙两工程队修一条长1400米的公路,他们从两端同时开工,甲队每天修80米,乙队每天修60
解方程的应用题,最好用分步.
甲,乙两工程队修一条长1400米的公路,他们从两端同时开工,甲队每天修80米,乙队每天修60米,多少天后能够修完这条公路? lgn3841年前2
lgn3841年前2 -
 mmmxz 共回答了22个问题
mmmxz 共回答了22个问题 |采纳率81.8%设需要x天
(80+60)x=1400
140x=1400
x=1400÷140
x=101年前查看全部
- 一道应用题,写完整分步算式 一个长方体玻璃容器,从里面量长、宽均为2dm,想容器中倒入5L水,再把土豆放入水中,这时容器
一道应用题,写完整分步算式
一个长方体玻璃容器,从里面量长、宽均为2dm,想容器中倒入5L水,再把土豆放入水中,这时容器内的水是13cm.这个土豆的体积是多少? 饕餮米米1年前4
饕餮米米1年前4 -
 绝版百年孤独 共回答了17个问题
绝版百年孤独 共回答了17个问题 |采纳率82.4%13厘米=1.3分米
5升=5立方分米
这个土豆的体积
=2*2*1.3-5
=5.2-5
=0.2(立方分米)1年前查看全部
- 亚硫酸根的盐类水解方程式是什么,一步还是分步完成
亚硫酸根的盐类水解方程式是什么,一步还是分步完成
RT
 longxiangw1年前1
longxiangw1年前1 -
 chriswu1979 共回答了17个问题
chriswu1979 共回答了17个问题 |采纳率88.2%NAHSO4+H2O=NAOH+H2SO4
NAHSO3+H2O=NAOH+H2SO3,一步完成,同时发生.
1.部分酸式盐溶于水呈碱性,例如,碳酸氢钠,磷酸一氢钠,硫氢化钠.
因为弱酸根离子水解产生氢氧根离子比电离产生的氢离子多
2、部分酸式盐溶于水呈酸性,例如,硫酸氢钠,亚硫酸氢钠,磷酸二氢钠.
因为弱酸根离子水解产生氢氧根离子比电离产生的氢离子少
3、有些弱酸弱碱盐呈酸性,例如,草酸铵,氟化铵,亚硫酸铵
因为阳离子水解产生的氢离子比阴离子水解产生的氢氧根离子多
4.有些弱酸弱碱盐呈碱性,例如,次氯酸铵,碳酸铵,硫化铵
因为阳离子水解产生的氢离子比阴离子水解产生的氢氧根离子少1年前查看全部
- 已知多元弱酸在水溶液中的电离是分步进行的,且第一步电离程度远大于第二步电离程度,第二步电离程度远大于第三步电离程度.
已知多元弱酸在水溶液中的电离是分步进行的,且第一步电离程度远大于第二步电离程度,第二步电离程度远大于第三步电离程度.
今有HA,H2B,H3C三种一元,二元,三元弱酸,根据"较强酸+较弱酸盐==较强酸盐+较弱酸"的反应规律,它们之间能发生下列反应:①HA+HC2-(少量)==A- +H2C-,②H2B(少量)+2A-==B2- +2HA,③H2B(少量)+H2C- ==HB- +H3C
回答下列问题
(1)A-,B2-,C3-,HB-,H2C-,HC2-六种离子中,最易结合质子的是_____,最难结合质子的是______
(2)下列反应的离子方程式中正确的是(填写标号)_____
A.H3C+3A- ==3HA+C3-
B.HB- +A- ==HA+B2-
C.H3C+B2- ==HB- +H2C-
(4)完成下列反应的离子方程式:HA(过量)+C3- ==__________
如何判断H3C和HB-的强弱?以及HB-和HA的强弱?苦思不得其解。 zhengquan91年前1
zhengquan91年前1 -
 kaibulk 共回答了11个问题
kaibulk 共回答了11个问题 |采纳率72.7%第一题考查的是离子的酸碱性的判断,碱性越强,结合氢离子(质子)的能力越强,反之,酸性越强,电离出质子的能力越强即越难结合质子,所以第一题的答案是:HC2;HB
第二题也是一样,较强酸+较弱酸盐==较强酸盐+较弱酸
所以答案是:B
第三题同理:=A-+H2C1年前查看全部
- 苯(苯的同系物):分步:①KMnO4(H+)溶液;②NaOH溶液;③分液
苯(苯的同系物):分步:①KMnO4(H+)溶液;②NaOH溶液;③分液
为什么要先加酸性高锰酸钾直接加氢氧化钠不行吗高一 一米6零1年前1
一米6零1年前1 -
 紫夜雨 共回答了15个问题
紫夜雨 共回答了15个问题 |采纳率93.3%要分离苯和苯的同系物,首先要知道苯的同系物上有什么.有烃基.苯环连上烃基后,不溶于水,但是可以被酸性高锰酸钾氧化成有机羧酸,酸碱可以中和生成溶于水的盐,而在这个过程中,苯是稳定的,不反应且不溶于水,所以分液就可以分离出较纯净的苯1年前查看全部
- ..着急呀.希望可以标出题号,并用分步解答...
..着急呀.希望可以标出题号,并用分步解答...
六年级一班和六年级二班的同学到社区养护草坪,每班养护这块草坪的一半,快到中午时,一班完成了任务的四分之三,二班完成了任务的六分之五.
(1)这时两个班各养护这块草坪的几分之几?
(2)这时两个班还各剩这块草坪的百分之几没有养护?
(3)这时如果一班养护了180平方米,那么整个草坪有多少平方米?
(4)你会用(3)题的结果,对(1)、(2)题进行检验吗? 5空你想要么1年前7
5空你想要么1年前7 -
 salake 共回答了16个问题
salake 共回答了16个问题 |采纳率93.8%(1)一班 1/2×3/4=3/8,二班 1/2×5/6=5/12
(2)一班 1/2-3/8=1/8,二班 1/2-5/12=1/12
(3)一班要养护草坪 180/(3/4)=240平方米,那么整个草坪就是480平方米.
(4)检验(1)一班180/480=3/8,二班240×(5/6)=200,200/480=5/12
检验(2)一班(240-180)/480=1/8,二班(240-200)/480=1/12
检验完毕1年前查看全部
- 已知多远弱酸在水溶液中的电离是分步进行的,且第一步电离的程度远远大于第二步电离,第二步电离的程度远远大于第三步电离.现有
已知多远弱酸在水溶液中的电离是分步进行的,且第一步电离的程度远远大于第二步电离,第二步电离的程度远远大于第三步电离.现有HA,H2B,H3C三种物质,根据强酸制弱酸原理,他们之间能发生如下反应:
1.HA+HC2-(少量) ——A-+H2C-
2.H2B(少量)+2A- —— B2-+2HA
3.H2B(少量)+H2C- —— HB-+H2C
则这六种反应离子中,最容易结合质子的是( )
这三种酸中 酸性最强的是()
写出离子方程式:
H3C+A-
HB-+A-
H3C+B2- toeast1年前1
toeast1年前1 -
 hauber 共回答了13个问题
hauber 共回答了13个问题 |采纳率92.3%根据以上3个反应, 可得出: 酸性: H2B > H3C > HA HA > H2C- 所以最易结合质子的是 HC--(当然C---更容易, 但是题目中没提到) 如果你是高中生, 可以认为: HA = 醋酸 H2B = H2SO4 H3C = H3PO4 这样判断就很简单啦... 还有问题的话, 信息讨论. :-)1年前查看全部
- 关于排列组合的分步计数如果A={-1,0,1},B={2,3,4,5,6},f表示从集合A到集合B的映射,那么满足x+f
关于排列组合的分步计数
如果A={-1,0,1},B={2,3,4,5,6},f表示从集合A到集合B的映射,那么满足x+f(x)+x*f(x)为奇数的映射有( )个.<*号为 乘 > LTSJ5201年前1
LTSJ5201年前1 -
 小芜96 共回答了24个问题
小芜96 共回答了24个问题 |采纳率95.8%因x+f(x)+x*f(x)=(x+1)*[f(x)+1]-1.故由题设可知,y=(x+1)*[f(x)+1]必为偶数.(1)当x=-1时,y=0*[f(-1)+1]=0.故由题设知,f(-1)的像可有5种选择.(2)当x=0时,y=f(0)+1为偶数,故此时f(0)的像有2种选择.选3或5.(3)当x=1时,y=2f(1)为偶时,同(1)可知,此时f(1)的像有5种选择.综上由分步计数原理知,符合题设的映射有5*2*5=50种.1年前查看全部
- (2014•杭州一模)二元弱酸是分步电离的,25时碳酸和草酸的Ka如表:
(2014•杭州一模)二元弱酸是分步电离的,25时碳酸和草酸的Ka如表:
(l)设有下列四种溶液:H2CO3 Ka1=4.3×10-7 H2C2O4 Ka1=5.6×10-2 Ka2=5.6×10-11 Ka2=5.42×10-5
A.0.1mol•L-1的Na2C2O4溶液B.0.1mol•L-1的NaHC2O4溶液
C.0.1mol•L-1的Na2CO3溶液D.0.1mol的NaHCO3溶液
其中,c(H+)最大的是______,c(OH-)最大的是______.
(2)某化学实验兴趣小组同学向用大理石和稀盐酸制备CO2后残留液中滴加碳酸钠溶液,在溶液中插人pH传感器,测得pH变化曲线如图所示.
刚开始滴人碳酸钠溶液时发生反应的离子方程式为______,BC段发生反应的离子方程式为______,D点时混合溶液中由水电离产生的c(OH-)=______ mol•L-1. 给不起永远1年前1
给不起永远1年前1 -
 梁朝zz 共回答了24个问题
梁朝zz 共回答了24个问题 |采纳率79.2%解题思路:(1)相同条件下,酸的电离平衡常数越大,则酸的酸性越强,酸根离子的水解程度越小,则溶液的碱性越弱;
(2)溶液pH<7,说明溶液呈酸性,酸和碳酸钠溶液反应生成氯化钠和水、二氧化碳,当pH不变时,碳酸钠和氯化钙发生复分解反应,碳酸钠为强碱弱酸盐,其溶液呈碱性,根据水的离子积常数计算氢氧根离子浓度.(1)相同条件下,酸的电离平衡常数越大,则酸的酸性越强,酸根离子的水解程度越小,则溶液中氢氧根离子浓度越小,氢离子浓度越大,根据电离平衡常数知,酸性强弱顺序是:草酸>草酸氢根离子>碳酸>碳酸氢根离子,离子水解强弱顺序是:碳酸根离子>碳酸氢根离子>草酸根离子>醋酸氢根离子,
根据离子水解程度知,草酸氢根离子水解程度最小,则其溶液碱性最弱,氢离子浓度最大,所以氢离子浓度最大的是B,水解程度最强的是C,则溶液C中碱性最强,氢氧根离子浓度最大,
故答案为:B;C;
(2)溶液pH<7,说明溶液呈酸性,酸和碳酸钠溶液反应生成氯化钠和水、二氧化碳,离子方程式为:2H++CO32-=H2O+CO2↑,当pH不变时,碳酸钠和氯化钙发生复分解反应,离子方程式为Ca2++CO32-=CaCO3↓,碳酸钠为强碱弱酸盐,其溶液呈碱性,D点时混合溶液中由水电离产生的c(OH-)=
10−14
10−10mol/L=10-4 mol/L,
故答案为:2H++CO32-=H2O+CO2↑;Ca2++CO32-=CaCO3↓;10-4.点评:
本题考点: 弱电解质在水溶液中的电离平衡;离子方程式的书写.
考点点评: 本题考查了盐类水解,明确弱酸的电离平衡常数与酸根离子水解程度的关系是解本题关键,难点是(2)题,会根据曲线变化趋势确定发生的反应,结合溶液中溶质的性质来分析解答,难度中等.1年前查看全部
- 分步算式组成综合箅式
分步算式组成综合箅式

 170682741年前1
170682741年前1 -
 ddcc89 共回答了23个问题
ddcc89 共回答了23个问题 |采纳率91.3%(1)14×4-14×4÷7=48
(2)80-36÷12+23=1001年前查看全部
- 求下面阴影部分的面积.单位;分米 用分步算式
 jxhybj1年前1
jxhybj1年前1 -
 divad06 共回答了23个问题
divad06 共回答了23个问题 |采纳率95.7%你图上是厘米
直角三角形面积是(10+6)×6÷2=48平方厘米
右下方的面积是6×6-3.14×6×6÷4=7.74平方厘米
所以面积是48-7.74=40.26平方厘米1年前查看全部
- H2CO3、H2S等被称为多元弱酸,多元弱酸在水中的H+的电离是分步进行的,且第一步电离程度远大于第二步电离程度,第二步
H2CO3、H2S等被称为多元弱酸,多元弱酸在水中的H+的电离是分步进行的,且第一步电离程度远大于第二步电离程度,第二步电离程度远大于第三步电离程度……
含有HA、H2B、H3C三种一元、二元、三元弱酸,根据“较强酸+较弱酸盐=较强酸盐+较弱酸”的反应规律,它们之间能发生下列反应:
(1)HA+Na2HC(少量)=NaA+NaH2C
(2)H2B(少量)+2NaA=Na2B+2HA
(3)H2B(少量)+NaH2C=NaHB+H3C
则相同情况下,HA、H2B、H3C中酸性由强到弱的顺序是( )
A、HA>H2B>H3C
B、H2B>H3C>HA
C、HA>H3C>H2B
D、H3C>H2B>HA
还望高手不惜赐教, yanhugame1年前3
yanhugame1年前3 -
 felix_82 共回答了18个问题
felix_82 共回答了18个问题 |采纳率94.4%答案B
即使这个题在高中也是一个非常有难度的题,我尽量解释,你尽量理解.
为了好解释,我们暂且把H2C-、HC^2-也看成酸,因为他们也能电离出氢离子,也具有酸性.
先看(2)H2B(少量)+2NaA=Na2B+2HA ,根据“较强酸+较弱酸盐=较强酸盐+较弱酸”可知少量的H2B就能把HA置换出来,得到H2B>HA
同理(3)得到H2B>H3C
这个题最难的就在于H3C和HA的判断
这用到的一个信息,而且涉及到量的关系.
(1)HA+Na2HC(少量)=NaA+NaH2C
HA和少量的Na2HC反应,如果HA>H3C,那么生成的将是H3C,而不是NaH2C,因此H3C>HA
也就是说H3C>HA> H2C->HC^2-
题中应用的是强酸置弱酸的规律,给你举个例子
CO2+H2O+Ca(ClO)2==CaCO3+2HCLO H2CO3>HClO 漂白粉的作用原理
2HCl+Na2CO3==2NaCl+CO2+H2O
类似的还有高沸点酸置低沸点酸、难挥发酸置易挥发酸
如硫酸+氯化钠==硫酸氢钠+氯化氢1年前查看全部
- 求积分:∫[x^2/(x-1)^100]dx.得的结果和答案总是不一样,就是用的分步积分.
 gggwww1年前2
gggwww1年前2 -
 采心zx 共回答了15个问题
采心zx 共回答了15个问题 |采纳率86.7%∫[(x^2- 1+1)/(x-1)^100]dx=∫[(x+1)/(x-1)^99]dx+∫[1/(x-1)^100]dx
=∫[(x - 1+2)/(x-1)^99]dx+∫[1/(x-1)^100]dx
=∫[1/(x-1)^98]dx+∫[2/(x-1)^99]dx+ ∫[1/(x-1)^100]dx
=(- 1/97)[1/(x-1)^97]+(- 2/98)[1/(x-1)^98]+(- 1/99)[1/(x-1)^99]+C1年前查看全部
- 高中数学问题:关于排列组合的3个球放入4杯子中求3球在同一杯子的概率 详细过程、分步计算 还有遇到类似题应如何套用公式
 wanggang99011年前1
wanggang99011年前1 -
 流浪的文字 共回答了22个问题
流浪的文字 共回答了22个问题 |采纳率90.9%设杯子是A,B,C,D,则第一个球放入A杯的概率是1/4.三球都放入A杯的概率是(1/4)^3=1/64. 同样,三球都放入B杯或C杯或D杯的概率都是1/64. 则三球放入同一杯的概率是(1/64)*4=1/16. 这题主要是分情况讨论,没有什么公式。做题不要老是记公式,会记错的,也不利于解题方法的掌握。...1年前查看全部
- 求过程,必采纳,用四年级的方法解答,要用分步算式题目是生产小组计划,每天生产40个零件30天完成任务,实际提前六天完成任
求过程,必采纳,用四年级的方法解答,要用分步算式题目是生产小组计划,每天生产40个零件30天完成任务,实际提前六天完成任务,实际每天生产零件多少个?
 opcqiqi1年前0
opcqiqi1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 根据分步算式,列出综合算式.(1)3025-2965=6016×225=36003600÷60=60综合算式:_____
根据分步算式,列出综合算式.
(1)3025-2965=6016×225=3600
3600÷60=60
综合算式:______;
(2)207×14=2898468÷18=26
2898-26=2872
综合算式:______. 与心飞扬1年前1
与心飞扬1年前1 -
 水如风 共回答了25个问题
水如风 共回答了25个问题 |采纳率96%(1)(16×225)÷(3025-2965)
=3600÷60
=60;
(2)207×14-468÷18
=2898-26
=2872.
故答案为:(16×225)÷(3025-2965);207×14-468÷18.1年前查看全部
- 像天上的星星和棋盘孑的棋子那样四散分步.形容数量多,分布广.的成语
 bluekiss001年前1
bluekiss001年前1 -
 jaffa_good 共回答了20个问题
jaffa_good 共回答了20个问题 |采纳率65%星罗棋布1年前查看全部
- 人教版六年级下册数学练习三的1.2.3.6的答案是什么?是人教版的 要工式,要分步
 vy4ever1年前4
vy4ever1年前4 -
 yykkhl 共回答了23个问题
yykkhl 共回答了23个问题 |采纳率91.3%1; 21平方米 22.4平方米
2,50π平方里米 48π平方里米 128π平方里米
6,s;108 π平方里米1年前查看全部
- 可以分步写也可以用方程)一筐苹果连筐重49千克,卖出这筐苹果的三分之二后,连筐重17千克,这筐苹果重多少千克?
 cysky1年前3
cysky1年前3 -
 最初的飞雪 共回答了19个问题
最初的飞雪 共回答了19个问题 |采纳率84.2%卖出的苹果钟量为49-17=32
总苹果重量为32/(2/3)=481年前查看全部
- e的ax次方乘x平方 怎么求积分 应该用分步积分的,可是正确答案竟然有1/a^3怎么算都算不出啊T
e的ax次方乘x平方 怎么求积分 应该用分步积分的,可是正确答案竟然有1/a^3怎么算都算不出啊T
e的ax次方乘x平方 怎么求积分
应该用分步积分的,可是正确答案竟然有1/a^3怎么算都算不出啊T^T Fanniejj1年前1
Fanniejj1年前1 -
 秋叶杨 共回答了20个问题
秋叶杨 共回答了20个问题 |采纳率85%一种简便的方法是
对x^2一直求导为
x^2->2x->2->0
对e^ax一直积分为
e^ax->(1/a) e^ax-> (1/a^2)e^ax-> (1/a^3)e^ax
所以答案为:(x^2)* (1/a) e^ax-2x* (1/a^2) e^ax +2* (1/a^3) e^ax+C 所以楼主不要奇怪有 (1/a^3) e^ax1年前查看全部
大家在问
- 1不定代词和形容词的位置怎么放。
- 2如图,在三角形ABC中,AD垂直于BC,CE垂直于AB,AD=8厘米,CE=7厘米,AB+BC=21厘米,三角形ABC的
- 3各位好心的哥哥姐姐,我有几个题不会,帮帮我吧~
- 4Dr. Yang worked ______ three days ago. [
- 5词组算出、解决的翻译
- 6any 和 some
- 7如图把一个长20厘米,宽15厘米,高18厘米的礼品盒包扎起来,问,至少需要包扎带多少厘米?(打节处每处长8厘米)
- 8(2014•郑州二模)如图,OA是⊙O的半径,弦BC⊥OA,D是⊙O上一点,若∠ADC=26°,则∠AOB的度数为(
- 979又79分之71乘以8分之1怎样简算
- 10自动控制原理,根轨迹分析∠(2j)和∠(-1+j) 这两个角度分别是多少呢?怎么换算成角度的呢? 另
- 11已知函数f(x)=[1/3]x3+[1−a/2]x2-ax-a,x∈R,其中a>0.
- 12how many m___are there in a basketball team?
- 13风能可以称为机械能吗风能和水能能通称为机械能吗?热能和内能一样吗,能互相转换吗?机械能包含有哪些能?
- 14在电场中电场力的方向是怎样的?
- 15鲁人身善织履,妻善织缟,而欲徒于越.或谓之曰:“子必穷矣!”鲁人曰:“何也?”曰:“屡为履之也,而越人先行;缟为冠之也,
