(2009•武威)原子结构中与元素化学性质关系最密切的是( )
 jj525112022-10-04 11:39:541条回答
jj525112022-10-04 11:39:541条回答A.电子层数
B.质子数
C.最外层电子数
D.中子数

已提交,审核后显示!提交回复
共1条回复
 率苇 共回答了15个问题
率苇 共回答了15个问题 |采纳率100%- 解题思路:根据元素的化学性质与最外层电子数的关系来解答.
元素的化学性质决定于最外层电子数,与其它粒子数都无关,
故选:C.点评:
本题考点: 核外电子在化学反应中的作用.
考点点评: 了解元素的化学性质与最外层电子数的关系可以帮助解答许多有关微观粒子的题目. - 1年前
相关推荐
- (2008•武威)甲、乙两车从A、B两地同时出发经过6小时相遇,甲车每小时比乙车快5千米,两车的速度比是7:8,求A、B
(2008•武威)甲、乙两车从A、B两地同时出发经过6小时相遇,甲车每小时比乙车快5千米,两车的速度比是7:8,求A、B两地相距多少千米?
 滚棍_0071年前1
滚棍_0071年前1 -
 lulu___520 共回答了20个问题
lulu___520 共回答了20个问题 |采纳率90%解题思路:车的速度比是7:8,如果看作份数,也就是甲车比乙车每小时少行1份,又知甲车每小时比乙车快5千米,即1份是5千米,那么全程为(5×7+5×8)×6,计算得解.5÷(8-7)=5(千米),
(5×7+5×8)×6,
=(35+40)×6,
=75×6,
=450(千米);
答:A、B两地相距450千米.点评:
本题考点: 简单的行程问题.
考点点评: 此题也可这样解答:5÷([8/15]-[7/15])×6,解答即可.1年前查看全部
- (2014•武威)2月29日,新发布的《环境空气质量标准》中增加了PM2.5监测指标.PM2.5是指大气中直径小于或等于
(2014•武威)2月29日,新发布的《环境空气质量标准》中增加了PM2.5监测指标.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,对人体健康影响更大,主要来源之一是化石燃料的燃烧.下列措施能减少PM2.5污染的是( )
A.鼓励开私家车出行
B.鼓励使用太阳能热水器
C.鼓励用煤火力发电
D.鼓励用液化石油气作燃料 浓浓咖啡他吗1年前1
浓浓咖啡他吗1年前1 -
 幸福有点累 共回答了19个问题
幸福有点累 共回答了19个问题 |采纳率89.5%解题思路:A、私家车越多,燃烧的化石燃料越多;
B、太阳能热水器不需燃烧化石燃料;
C、煤属于化石燃料;
D、液化石油气也属于化石燃料.A、私家车越多,燃烧的化石燃料越多,生成的微小颗粒物越多,会增加PM2.5污染,故A不符合题意;
B、太阳能热水器不需燃烧化石燃料,是洁净的能源,不会增加PM2.5污染,故B符合题意;
C、煤属于化石燃料,燃烧生成微小颗粒物,会增加PM2.5污染,故C不符合题意;
D、液化石油气也属于化石燃料,燃烧生成微小颗粒物,会增加PM2.5污染,故D不符合题意.
故选:B点评:
本题考点: 空气的污染及其危害.
考点点评: 环境的污染与保护是社会关注的焦点问题,与之相关的考题就成为中考的热点之一.1年前查看全部
- (2009•武威)物质的用途与性质密切相关,下列说法不正确的是( )
(2009•武威)物质的用途与性质密切相关,下列说法不正确的是( )
A.氮气常用作保护气,是由于氮气的化学性质不活泼
B.洗涤剂常用来洗涤油污,是因为洗涤剂有乳化功能
C.铁制栏杆表面常涂“银粉漆”(铝粉)防生锈,是由于铝的化学性质比铁稳定
D.CO、H2常用来冶炼金属,是因为它们都具有还原性 炽虎1年前1
炽虎1年前1 -
 孤寂飞扬 共回答了16个问题
孤寂飞扬 共回答了16个问题 |采纳率100%A、氮气化学性质很稳定,一般不与其他物质发生化学反应,可以用作保护气,故A正确;
B、洗涤剂能将油污乳化为液体小珠滴,易与洗涤,故B正确;
C、铝能与氧气反应生成氧化铝具有保护功能,而非铝化学性质稳定,故C错误;
D、一氧化碳和氢气等具有还原性,常用来冶炼金属,故D正确,
故选:C.1年前查看全部
- (2009•武威)规范的实验操作是实验成功的前提.请回答:
(2009•武威)规范的实验操作是实验成功的前提.请回答:
(1)量取6mL稀硫酸,应选用______mL的量筒;
(2)胶头滴管用过后应______,再去吸取其它药品;
(3)倾倒液体时,标签应______,瓶口要挨着试管口;
(4)实验室加热烧杯里的液体时,烧杯的底部应垫放______. hehe呵呵1年前1
hehe呵呵1年前1 -
 lyclwslw 共回答了13个问题
lyclwslw 共回答了13个问题 |采纳率100%解题思路:(1)量筒量液时要注意量程的选择,应选择略大于量取液体体积的量程,选取的量程太大,会因刻度不精确而使量取的液体体积不准确,选取的量程太小,多次量取会有误差.
(2)胶头滴管用完后,不清洗,再去吸取别的药品,会污染别的药品.
(3)防止残留的药品腐蚀标签,倾倒药品时标签要向着手心.
(4)烧杯的底部面积较大,加热时,为了受热均匀,应垫上石棉网.(1)量取6mL液体,应选用与6毫升相近的量程,则应选10毫升量程的量筒.
(2)胶头滴管用完后,洗涤干净晾干,防止污染别的药品.
(3)防止残留的药品腐蚀标签,倾倒药品时标签要向着手心.
(4)烧杯的底部面积较大,加热时,为了受热均匀,应垫上石棉网.
故答案:(1)10;(2)清洗;(3)向着手心;(4)石棉网.点评:
本题考点: 测量容器-量筒;用于加热的仪器;液体药品的取用.
考点点评: 化学实验的基本操作是做好化学实验的基础,学生要在平时的练习中多操作,掌握操作要领,使操作规范.1年前查看全部
- (2011•武威)溶解度曲线为我们定量描述物质的溶解性提供了便利.关于如图的溶解度曲线说法错误的是( )
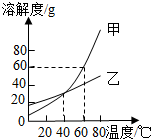 (2011•武威)溶解度曲线为我们定量描述物质的溶解性提供了便利.关于如图的溶解度曲线说法错误的是( )
(2011•武威)溶解度曲线为我们定量描述物质的溶解性提供了便利.关于如图的溶解度曲线说法错误的是( )
A.20℃时,甲物质的溶解度小于乙物质的溶解度
B.将20℃时甲物质的饱和溶液升温到40℃,溶液的质量不变
C.甲物质的溶解度受温度的影响比乙大
D.60℃时,甲、乙两种物质的饱和溶液中溶质的质量分数相等 断线a风筝1年前1
断线a风筝1年前1 -
 yaoaiwei 共回答了19个问题
yaoaiwei 共回答了19个问题 |采纳率89.5%解题思路:根据固体的溶解度曲线可以:①查出某物质在某温度下的溶解度,②比较不同物质在同一温度下的溶解度的大小,③判断物质的溶解度受温度变化的变化情况等;某物质的饱和溶液中溶质的质量分数和同温度下的该物质的溶解度的关系为:溶液中溶质的质量分数=[溶解度/100+溶解度]×100%.A、由两物质的溶解度曲线可知,在20℃时,甲的溶解度小于乙的溶解度,故A正确;
B、由于甲的溶解度随温度的升高而增大,因此升温时甲的饱和溶液就会变成不饱和溶液,但溶液中溶质的质量分数不发生变化,故B正确;
C、由两物质的溶解度曲线不难看出,甲物质的溶解度受温度的影响大,故C正确;
D、由于在60℃时,甲的溶解度比乙大,因此甲的饱和溶液中溶质的质量分数大,故D错误.
故选D点评:
本题考点: 固体溶解度曲线及其作用;溶质的质量分数、溶解性和溶解度的关系.
考点点评: 本题难度不是很大,主要考查了固体溶解度曲线的意义和对固体溶解度概念的理解,从而培养学生的理解能力和解决问题的能力.1年前查看全部
- (2011•武威)“绿色化学”要求工业生产尽可能不产生废物,即实现“废物零排放”.下列反应类型最容易实现“零排放”的是(
(2011•武威)“绿色化学”要求工业生产尽可能不产生废物,即实现“废物零排放”.下列反应类型最容易实现“零排放”的是( )
A.化合反应
B.置换反应
C.分解反应
D.复分解反应 天生nn1年前1
天生nn1年前1 -
 合适选择 共回答了9个问题
合适选择 共回答了9个问题 |采纳率100%解题思路:根据化合反应、置换反应、分解反应和复分解反应的定义来回答此题,从反应物和生成物的种类入手,反应物中的原子是否全部转化到欲制取的产物中了.符合上述要求的只有化合反应,因为它只生成一种物质,原子的利用率肯定为100%,而其他反应类型都有多种产物生成.
故选A.点评:
本题考点: 绿色化学;化合反应及其应用.
考点点评: “绿色化学”要看反应物中的原子是否全部转化到欲制取的产物中了,即产物只有一种物质的反应.1年前查看全部
- (2011•武威)化学就在我们身边,它与我们的生活和生产息息相关.在“食醋、维生素C、食盐、熟石灰”中选择适当的物质填空
(2011•武威)化学就在我们身边,它与我们的生活和生产息息相关.在“食醋、维生素C、食盐、熟石灰”中选择适当的物质填空.
(1)缺乏______会引起坏血病;
(2)可用于改良酸性土壤的是______;
(3)日常生活中用来调味和防腐的是______;
(4)可用于检验鸡蛋壳中含有碳酸盐的是______. 我好你也好1年前1
我好你也好1年前1 -
 ppvf 共回答了16个问题
ppvf 共回答了16个问题 |采纳率93.8%解题思路:根据物质的性质进行分析,食醋能与碳酸盐反应生成气体,缺维生素C会引起坏血病,食盐具有咸味,能用来作调味品,熟石灰具有碱性.(1)缺乏维生素C会引起坏血病,故填:维生素C;
(2)熟石灰具有碱性,能用来改良酸性土壤,故填:熟石灰;
(3)食盐具有咸味,能用作厨房调味品,故填:食盐;
(4)食醋中的醋酸能与蛋壳中的碳酸盐反应生成二氧化碳气体,可以用于检验蛋壳中含有碳酸盐,故填:食醋.点评:
本题考点: 酸碱盐的应用;生命活动与六大营养素.
考点点评: 本题考查了常见物质的用途,完成此题,可以依据物质的性质进行.1年前查看全部
- (2011•武威)在化学课上,甲同学将燃烧的钠迅速伸入到盛有CO2的集气瓶中,钠在其中
(2011•武威)在化学课上,甲同学将燃烧的钠迅速伸入到盛有CO2的集气瓶中,钠在其中
继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质.黑色颗粒和白色物质是什么?
【进行猜想】甲认为黑色颗粒是______,白色物质可能是______或______,乙同学还认为白色物质是氢氧化钠.
甲同学立刻认为乙同学的猜想是错误的,其理由是______
【查阅资料】氧化钠为白色粉末,溶于水生成氢氧化钠:Na2O+H2O═2NaOH
【实验探究】甲同学对白色物质进行实验探究.
【反思评价】丙同学认为方案1得到的结论不正确,其理由是______实验方案 实验操作 实验现象 结论 方案1 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 溶液变成红色 白色物质
为Na2O方案2 ①取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 出现白色沉淀 白色物质
是______.②静置片刻,取上层清液于试管中,滴加无色酚酞试液 无明显现象
【得出结论】钠在二氧化碳中燃烧的化学方程式为4Na+3CO2
2Na2CO3+C点燃 .4Na+3CO2.
2Na2CO3+C点燃 . harriet19781年前1
harriet19781年前1 -
 a31531 共回答了16个问题
a31531 共回答了16个问题 |采纳率87.5%解题思路:根据题干中信息可知,钠与二氧化碳中发生了反应生成一种黑色物质和一种白色物质;其中由于反应物含有钠元素、碳元素、氧元素,那么生成的物质也必须是含有这几种元素,那么黑色固体物质只能是炭,白色物质是什么?根据后面的实验结论和现象可猜到白色物质只能是Na2CO3,根据化学中质量守恒,决不可能是氢氧化钠,因为反应物中无氢元素;根据氢氧化钠、氧化钠和碳酸钠的性质可知,钠在空气中燃烧生成碳酸钠和炭.(1)根据所学过的黑色物质:炭、二氧化锰、四氧化三铁、生铁和氧化铜中可以推测出应该是炭,若其他物质都违背化学反应的事实
(2)由后面方案2可推测白色物质还可能是碳酸钠;但不可能是氢氧化钠,反应物中没有氢元素;由于碳酸钠溶液也是呈现碱性,所以法案1不可靠;
(3)由方案2得出它们反应生成碳酸钠和前面黑色物质是炭,故化学方程式4Na+3CO2═2Na2CO3+C
故正确答案:【进行猜想】炭(C);Na2CO3;Na2O;反应物中无氢元素(或违背质量守恒定律)
【实验探究】Na2CO3
【反思评价】Na2CO3溶液显碱性也会使酚酞变红
【得出结论】4Na+3CO2
点燃
.
2Na2CO3+C点评:
本题考点: 金属的化学性质;实验探究物质的组成成分以及含量;碳酸钠、碳酸氢钠与碳酸钙;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题是一道综合性很强的实验探究题,主要考查学生的实验探究能力、分析问题和解决问题的实际能力.解答这种综合性强的探究题,关键是理解题意,找到准确的出发点定位.1年前查看全部
- (2013•武威)化学课外小组设计了一套如图所示的气体发生及收集装置,并探究该装置的多功能性.
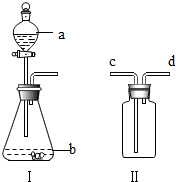 (2013•武威)化学课外小组设计了一套如图所示的气体发生及收集装置,并探究该装置的多功能性.
(2013•武威)化学课外小组设计了一套如图所示的气体发生及收集装置,并探究该装置的多功能性.
(1)甲同学认为装置Ⅰ可作为实验室制取O2的发生装置,则Ⅰ的a仪器中应加入______,b仪器中应加入______,反应的化学方程式为2H2O2
2H2O+O2↑MnO2 .2H2O2,装置Ⅱ中从______管口进气即可作为O2的收集装置.
2H2O+O2↑MnO2 .
(2)乙同学认为装置Ⅰ可作为实验室制取二氧化碳的发生装置,则Ⅰ的a仪器应加入______,b仪器中应加入______.
(3)如果要用装置Ⅱ收集H2,则应从______管口进气. wg198309131年前1
wg198309131年前1 -
 一叶孤城2005 共回答了8个问题
一叶孤城2005 共回答了8个问题 |采纳率87.5%解题思路:(1)甲同学认为装置Ⅰ可作为实验室制取O2的发生器,则为固体与液体反应,只能为双氧水与二氧化锰反应;因为氧气的密度大于空气,故从长导管进气;
(2)乙同学认为利用装置Ⅰ可作为实验室制二氧化碳的发生器,则为稀盐酸与大理石或石灰石反应,根据氢气的密度小于空气可知应从短导管进气.(1)甲同学认为装置Ⅰ可作为实验室制取O2的发生器,则为固体与液体反应,则Ⅰ的a仪器中可加入 双氧水或过氧化氢溶液,b仪器加入 二氧化锰,反应的化学方程式为 2H2O2
MnO2
.
2H2O+O2↑,因为氧气的密度大于空气,则装置Ⅱ要作为O2的收集装置应从 c管口进气,将空气挤压到集气瓶上部排出;
(2)乙同学认为利用装置Ⅰ可作为实验室制二氧化碳的发生器,则为稀盐酸与大理石或石灰石反应,则Ⅰ中a仪器可加入 稀盐酸,b中加入 大理石或石灰石.根据氢气的密度小于空气则装置Ⅱ要作为H2的收集装置应从 d管口进气,将空气挤压到集气瓶底部排出;
故答为:(1)双氧水或过氧化氢溶液;二氧化锰;2H2O2
MnO2
.
2H2O+O2↑;c;
(2)稀盐酸;大理石或石灰石; d.点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;实验室制取氧气的反应原理;二氧化碳的实验室制法;书写化学方程式、文字表达式、电离方程式.
考点点评: 熟练掌握实验制取氧气、二氧化碳和氢气的原理、收集方法;实验室确定气体发生装置时应考虑的因素是反应物状态和反应条件,确定气体收集装置时应考虑的因素是气体的溶解性和密度,结合题意即可顺利解答.1年前查看全部
- (2011•武威)将下列各组物质分别加入水中,能大量共存且得到无色透明溶液的是( )
(2011•武威)将下列各组物质分别加入水中,能大量共存且得到无色透明溶液的是( )
A.CaCl2HClNaNO3
B.FeCl3NaClKNO3
C.K2CO3Ba(NO3)2 NaOH
D.KOHHCl( NH4)2SO4 crazy11801年前1
crazy11801年前1 -
 愤怒的无忌 共回答了23个问题
愤怒的无忌 共回答了23个问题 |采纳率87%解题思路:根据复分解反应发生的条件可知,若物质之间相互交换成分不能生成水、气体、沉淀,则能够在溶液中大量共存;本题还要注意能得到无色透明溶液,不能含有明显有颜色的铜离子、铁离子和亚铁离子等.A、三者之间不反应,能大量共存,且不存在有色离子,符合无色透明的要求,故选项正确.
B、三者之间不反应,能大量共存,但FeCl3溶于水呈黄色,故选项错误.
C、K2CO3与Ba(NO3)2反应生成碳酸钡白色沉淀,不能大量共存,故选项错误.
D、KOH与(NH4)2SO4反应生成氨气和水,不能大量共存,故选项错误.
故选A.点评:
本题考点: 离子或物质的共存问题.
考点点评: 本题考查物质的共存问题,判断物质在溶液中能否共存,主要看溶液中的各物质之间能否发生反应生成沉淀、气体、水;还要注意特定离子的颜色.1年前查看全部
- (2009•武威)已知A、B可发生中和反应.在常温下D为液体,X是目前应用最广泛的金属,Y常 用作
(2009•武威)已知A、B可发生中和反应.在常温下D为液体,X是目前应用最广泛的金属,Y常用作食品干燥剂.各物质间的转化关系如图所示:

(1)E的化学式为______,列举E的用途一例:______;
(2)D与Y反应的化学方程式为______;
(3)D反应生成E、F的化学方程式为2H2O
2H2↑+O2↑通电 .2H2O.
2H2↑+O2↑通电 . youandao1年前1
youandao1年前1 -
 hobjian 共回答了14个问题
hobjian 共回答了14个问题 |采纳率92.9%解题思路:根据D和E、F可以相互转化及转化的条件,且D又是由中和反应生成的,所以D就是水,F会与X反应生成黑色固体,所以F就是氧气,E就是氢气,Y常用作食品干燥剂,会与水反应生成B,所以Y就是氧化钙,B就是氢氧化钙,A、B可发生中和反应,A就是酸,A和X反应会生成浅绿色溶液和氢气,所以X就是铁,G就是四氧化三铁,将推出的物质验证即可;根据推出的反应物、生成物书写方程式.D和E、F可以相互转化及转化的条件,且D又是由中和反应生成的,所以D就是水,F会与X反应生成黑色固体,所以F就是氧气,E就是氢气,Y常用作食品干燥剂,会与水反应生成B,所以Y就是氧化钙,B就是氢氧化钙,A、B可发生中和反应,A就是酸,A和X反应会生成浅绿色溶液和氢气,所以X就是铁,G就是四氧化三铁,因此:
(1)F是氢气,化学式为:H2;可以利用其可燃性,做燃料(或利用其还原性,用于冶炼金属等);
(2)D与Y反应就是水和氧化钙反应产生氢氧化钙,反应的方程式为:CaO+H2O=Ca(OH)2;
(3)D反应生成E、F,是电解水的反应,反应的方程式为:2H2O
通电
.
2H2↑+O2↑;
故答案为:(1)H2;利用其可燃性,做燃料(或利用其还原性,用于冶炼金属等);(2)CaO+H2O=Ca(OH)2;(3)2H2O
通电
.
2H2↑+O2↑.点评:
本题考点: 物质的鉴别、推断;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题为框图式物质推断题,完成此题,关键是根据题干提供信息直接得出有关物质的化学式,然后依据物质的性质推断得出其他物质的化学式,带入验证符合条件即可.1年前查看全部
- (2014•武威模拟)袋子里有10个红球和若干个蓝球,小明从袋子里有放回地任意摸球,共摸100次,其中摸到红球次数是25
(2014•武威模拟)袋子里有10个红球和若干个蓝球,小明从袋子里有放回地任意摸球,共摸100次,其中摸到红球次数是25次,则袋子里蓝球大约有( )
A.20
B.30
C.40
D.50 FM1101年前1
FM1101年前1 -
 linweiyang 共回答了19个问题
linweiyang 共回答了19个问题 |采纳率100%解题思路:首先根据多次试验摸球次数求得概率,然后利用概率的公式求得篮球的个数.∵共摸100次,其中摸到红球次数是25次,
∴摸到红球的概率为[25/100]=[1/4],
∵袋子里有10个红球和若干个蓝球,
∴设篮球有x个,则[10/10+x]=[1/4],
解得:x=30,
故选B.点评:
本题考点: 利用频率估计概率.
考点点评: 本题考查利用频率估计概率,一般方法:如果一个事件有n种可能,而且这些事件的可能性相同,其中事件A出现m种结果,那么事件A的概率P(A)=[m/n].关键是根据红球的频率得到相应的等量关系.1年前查看全部
- (2007•武威)甲醛(CH2O)是家庭装修后造成室内污染的主要有害气体,下列关于甲醛的说法正确的是( )
(2007•武威)甲醛(CH2O)是家庭装修后造成室内污染的主要有害气体,下列关于甲醛的说法正确的是( )
A.甲醛是由碳、水两种物质组成
B.甲醛是由碳、氢、氧三种元素组成
C.一个甲醛分子由一个碳原子、一个氢分子和一个氧原子构成
D.甲醛由一个碳元素、两个氢元素、一个氧元素组成 yangqm1年前1
yangqm1年前1 -
 乞力马扎罗的雨 共回答了17个问题
乞力马扎罗的雨 共回答了17个问题 |采纳率82.4%由甲醛的化学式可知:
甲醛由碳、氢、氧三种元素组成,因此选项A错误,选项B正确;
1个甲醛分子由1个碳原子、2个氢原子和1个氧原子构成,因此选项C错误;
元素只讲种类,不讲个数,因此选项D错误.
故选B.1年前查看全部
- (2009•武威)人体内一些液体的正常pH范围如下表.在这些液体中一定呈酸性的是( )
(2009•武威)人体内一些液体的正常pH范围如下表.在这些液体中一定呈酸性的是( )
血浆 乳汁 唾液 胆汁 胰液 胃液 pH范围 7.35~7.45 6.6~7 6.6~7.1 7.1~7.3 7.5~8.0 0.9~1.5
A.血浆
B.胃液
C.乳汁
D.唾液 luoyongqin1年前1
luoyongqin1年前1 -
 前世的一面之约 共回答了23个问题
前世的一面之约 共回答了23个问题 |采纳率87%解题思路:当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,呈碱性.据此分析判断即可.A、血浆的pH大于7,显碱性,故选项错误;
B、胃液的pH小于7,显酸性,故选项正确;
C、乳汁的pH为6.6~7,显酸性或中性,故选项错误;
D、唾液的pH为6.6~7.1,显酸性或中性或碱性,故选项错误.
故选B.点评:
本题考点: 溶液的酸碱性与pH值的关系.
考点点评: 解答本题要充分理解溶液的酸碱性和溶液pH大小之间的关系,只有这样才能对相关方面的问题做出正确的判断.1年前查看全部
- (2014•武威一模)今年冰岛火山爆发迫使欧洲的民航飞机停飞,火山灰里含有大量的硅酸钙(CaSiO3),硅酸钙中Si元素
(2014•武威一模)今年冰岛火山爆发迫使欧洲的民航飞机停飞,火山灰里含有大量的硅酸钙(CaSiO3),硅酸钙中Si元素的化合价为( )
A.-2价
B.+2价
C.+3价
D.+4价 milkpeach1年前1
milkpeach1年前1 -
 注定成灰 共回答了15个问题
注定成灰 共回答了15个问题 |采纳率100%解题思路:根据物质硅酸钙的化学式CaSiO3,利用化合物中各元素的化合价代数和为0的原则,由化合物中钙、氧为+2、-2价,计算化合物中Si元素的化合价.设化合物CaSiO3中Si元素化合价为n价,依化合物中各元素化合价代数和为零的原则,有(+2)+n+(-2)×3=0,解之得n=+4;
故选D.点评:
本题考点: 有关元素化合价的计算.
考点点评: 根据化合物中各元素的化合价代数和为0,利用化合物的化学式可计算其中未知的元素化合价.1年前查看全部
- (2009•武威)在下表内填写符合要求的化学符号.
(2009•武威)在下表内填写符合要求的化学符号.
符号表示的意义
五个氧分子
硅元素
铁离子氧化锌中锌
元素显正二价
四个硫原子化学符号 ______ ______ ______
O+2 Zn
O+2 Zn ______  mukeqq1年前1
mukeqq1年前1 -
 思余12 共回答了21个问题
思余12 共回答了21个问题 |采纳率90.5%解题思路:分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字.
书写元素符号时应注意:①有一个字母表示的元素符号要大写;②由两个字母表示的元素符号,第一个字母大写,第二个字母小写.
离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字.
化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后.
原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则5个氧分子可表示为:5O2.
硅元素的元素符号为:Si.
由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字,故铁离子可表示为:Fe3+.
由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故氧化锌中锌元素显正二价可表示为:
+2
ZnO.
由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故四个硫原子表示为:4S.
故答案为:
符号表示的意义
五个氧分子
硅元素
铁离子 氧化锌中锌
元素显正二价
四个硫原子
化学符号 5O2 Si Fe3+
+2
ZnO 4S点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本题难度不大,主要考查同学们对常见化学用语(元素符号、原子符号、分子符号、化合价、离子符号等)的书写和理解能力.1年前查看全部
- (2014•武威)下列成语所描述的动物行为中,属于先天性行为的是( )
(2014•武威)下列成语所描述的动物行为中,属于先天性行为的是( )
A.鹦鹉学舌
B.惊弓之鸟
C.老马识途
D.金鸡报晓 wen52551年前1
wen52551年前1 -
 PIAOPIAOTATA 共回答了15个问题
PIAOPIAOTATA 共回答了15个问题 |采纳率86.7%解题思路:动物的行为从获得的途径可分为先天性行为和学习行为,先天性行为是动物生来就有的,由动物体内的遗传物质所决定的行为;学习行为是在遗传因素的基础上,通过环境因素的作用,由生活经验和学习而获得的行为,据此答题.ABC、鹦鹉学舌、惊弓之鸟、老马识途是动物在遗传因素的基础上,通过环境因素的作用,由生活经验和学习而获得的行为,属于学习行为.
D、金鸡报晓是动物生来就有的,由动物体内的遗传物质所决定的行为,属于先天性行为.
故选:D点评:
本题考点: 动物的先天性行为和学习行为的区别.
考点点评: 明确动物的先天性行为是由遗传物质决定的行为,是一种本能.1年前查看全部
- (2014•武威质检)如图所示,A、B两段同种材料制成的实心导体电阻值相等,A导体比B导体的长度和横截面积都小.将它们串
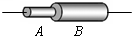 (2014•武威质检)如图所示,A、B两段同种材料制成的实心导体电阻值相等,A导体比B导体的长度和横截面积都小.将它们串联在电路中,通电一段时间后,A导体升高的温度______(选填“大于”、“等于”或“小于”)B导体升高的温度.
(2014•武威质检)如图所示,A、B两段同种材料制成的实心导体电阻值相等,A导体比B导体的长度和横截面积都小.将它们串联在电路中,通电一段时间后,A导体升高的温度______(选填“大于”、“等于”或“小于”)B导体升高的温度.  zhwping1年前1
zhwping1年前1 -
 zss620617 共回答了18个问题
zss620617 共回答了18个问题 |采纳率94.4%解题思路:因为甲乙两电阻串联,通过的电流相等、通电时间相同,根据焦耳定律判断产生热量的多少,再根据导体的长度和横截面积判断两导体的质量关系,根据Q=cm△t判断两导体的温度变化.由题意可知,两者的电阻相同,因两电阻串联,所以通过的电流相等;
根据Q=I2Rt可知,相同时间内产生的热能相等;
根据m=ρV可知,A的长度和截面积都小,则A的体积小,mA就小;
根据Q=cm△t可知,热量相同时,质量小,升高的温度就高.
故答案为:大于.点评:
本题考点: 焦耳定律;热量的计算;影响电阻大小的因素.
考点点评: 本题考查了学生对串联电路的电流特点、焦耳定律、吸热公式的了解和掌握,虽然涉及的知识点多,但做题时只要细心解决不难.1年前查看全部
- (2010•武威)除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
(2010•武威)除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
物质 杂质 除杂所用的试剂和方法 A CaO固体 CaCO3固体 加入适量的稀盐酸 B NaOH溶液 Ca(OH)2溶液 先加入过量的Na2CO3溶液,再过滤 C CO2气体 CO气体 点燃 D H2气体 HCl气体 先通过NaOH溶液,再通过浓硫酸
A.A
B.B
C.C
D.D zhmilan1年前1
zhmilan1年前1 -
 xsmf 共回答了25个问题
xsmf 共回答了25个问题 |采纳率100%解题思路:除杂质的原则:首先方法要可行,既要能除掉杂质,又不能和需要的物质反应,同时也不能添加新的杂质,另外,实验操作越简单越好.根据杂质的状态不同,要把杂质转化成沉淀,可溶性物质或气体而除去.A、氧化钙和碳酸钙都能和盐酸反应,故不可行.
B、加入过量的碳酸钠会带入新的碳酸钠杂质,不可行.
C、二氧化碳中混有少量一氧化碳不能点燃,因为没有支持燃烧的物质,故不可行.
D、除去氢气中的氯化氢气体,先通过氢氧化钠溶液,除掉氯化氢,再通过浓硫酸干燥,除去水分,可行.
故选D点评:
本题考点: 物质除杂或净化的探究.
考点点评: 除杂质的题目,要在符合原则的基础上,根据物质不同的性质,具体情况具体分析.1年前查看全部
- (2013•武威)祁连玉因盛产于祁连山而得名(如图).地质学鉴定其矿物是蛇纹石,其化学式为Mg6[Si4O10](OH)
 (2013•武威)祁连玉因盛产于祁连山而得名(如图).地质学鉴定其矿物是蛇纹石,其化学式为Mg6[Si4O10](OH)8,则Mg6[Si4O10](OH)8中Si元素的化合价是( )
(2013•武威)祁连玉因盛产于祁连山而得名(如图).地质学鉴定其矿物是蛇纹石,其化学式为Mg6[Si4O10](OH)8,则Mg6[Si4O10](OH)8中Si元素的化合价是( )
A.+1
B.+2
C.+3
D.+4 wszjk1年前1
wszjk1年前1 -
 amandaphy 共回答了15个问题
amandaphy 共回答了15个问题 |采纳率100%解题思路:根据在化合物中正负化合价代数和为零,结合蛇纹石的化学式进行解答本题.镁元素显+2价,氧元素显-2价,氢氧根显-1价,设硅元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+2)×6+4x+(-2)×10+(-1)×8=0,则x=+4价.
故选D.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题难度不大,掌握利用化合价的原则(化合物中正负化合价代数和为零)计算指定元素的化合价的方法即可正确解答本题.1年前查看全部
- (2010•武威)“闻香识茶”意思是通过闻的方法判断出茶的类别.人们能够闻到茶香的原因是( )
(2010•武威)“闻香识茶”意思是通过闻的方法判断出茶的类别.人们能够闻到茶香的原因是( )
A.分子之间存在间隔
B.分子质量和体积很小
C.分子在不断的运动
D.分子是由原子构成的 左岸生活1年前1
左岸生活1年前1 -
 gdszgd 共回答了21个问题
gdszgd 共回答了21个问题 |采纳率95.2%解题思路:利用构成物质的微粒是在不断运动的基本观点来解释“闻香识茶”.人们能够闻到茶香的原因是茶中含有特殊气味的分子运动到了我们的鼻子之中的缘故.而能够通过闻的方法来判断茶的类别则是因为不同的茶的气味上会不微小的差异.
点评:
本题考点: 利用分子与原子的性质分析和解决问题.
考点点评: 本题考查学生运用微粒的基本特征解释日常生活现象.1年前查看全部
- (2012•武威)下列说法错误的是( )
(2012•武威)下列说法错误的是( )
A.断裂的玻璃不能复原,是因为分子间有斥力
B.沿海地区昼夜温差较小,主要原因是水的比热容较大
C.切割机切铁片时火星四溅,这是用做功的方式改变了物体的内能
D.柴油机在吸气冲程中,进气门打开排气门关闭,将空气吸入气缸 林欣如1年前1
林欣如1年前1 -
 essien_lau 共回答了17个问题
essien_lau 共回答了17个问题 |采纳率94.1%解题思路:(1)分子间存在相互的引力和斥力,分子间距离大于分子直径10倍的时候,分子间既无引力,也无斥力.
(2)相同质量的物体吸收相同的热量,比热容大的升高的温度少;
(3)改变物体的内能:做功、热传递;
(4)吸气冲程中,进气门打开排气门关闭,排气冲程正好相反.A、断裂的玻璃分子间的距离大于分子直径的10倍以上,超出了分子力的作用范围;故A错误,符合题意;
B、沿海地区昼夜温差较小,主要原因是水的比热容较大,故B正确,不符合题意;
C、切割机切铁片时火星四溅,这是用做功的方式改变了物体的内能,故C正确,不符合题意;
D、吸气冲程中,进气门打开排气门关闭,将空气吸入气缸,故D正确,不符合题意.
故选A.点评:
本题考点: 分子间的作用力;做功改变物体内能;比热容解释简单的自然现象;内燃机的四个冲程.
考点点评: 本题考查的知识点比较多,主要有分子间作用力、比热容、做功、四个冲程等有关问题,实际是为了考查学生对所学物理知识的综合应用能力.1年前查看全部
- (2008•武威)如图所示的有关二氧化碳性质的实验中,只能证明二氧化碳的物理性质的是( )
(2008•武威)如图所示的有关二氧化碳性质的实验中,只能证明二氧化碳的物理性质的是( )
A.
B.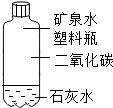
C.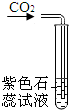
D.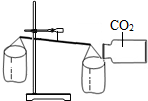
 屋内仍继续下雨1年前1
屋内仍继续下雨1年前1 -
 tiger尹 共回答了9个问题
tiger尹 共回答了9个问题 |采纳率100%解题思路:物理性质是指物质不需要发生化学变化就表现出来的性质.化学性质是指物质在化学变化中表现出来的性质.而化学变化的本质特征是变化中有新物质生成,因此,判断物理性质还是化学性质的关键就是看表现物质的性质时是否有新物质产生.A、稀盐酸与石灰石反应生成二氧化碳,二氧化碳密度大,聚集在烧杯底部,又因为二氧化碳不支持燃烧,所以下方的蜡烛先灭,既有二氧化碳的化学性质,也有二氧化碳的物理性质,不符合题意,故A不符合题意;B、二氧化碳...
点评:
本题考点: 实验探究物质的性质或变化规律;二氧化碳的物理性质.
考点点评: 了解物理性质、化学性质是一对与物理变化、化学变化有密切关系的概念,联系物理变化、化学变化来理解物理性质和化学性质,则掌握起来并不困难.1年前查看全部
- (5kk9•武威)下列日常生活r的物质可看作纯净物的是( )
(5kk9•武威)下列日常生活r的物质可看作纯净物的是( )
A.
B.
C.
D.
 abs3211年前1
abs3211年前1 -
 漫漫长路 共回答了19个问题
漫漫长路 共回答了19个问题 |采纳率84.2%解题思路:纯净物是由一种物质组成的物质.混合物是由多种物质组成的物质.据此逐项分析即可.A、雪碧汽水二含有水、碳酸、苯甲酸钠等多种物质,属于混合物,故选项错误.
i、空气二含有氮气、氧气等多种物质,属于混合物,故选项错误.
C、金刚石二只含有金刚石一种物质,可看做纯净物,故选项正确.
D、铂铱合金二含有铂、铱等金属,属于混合物,故选项错误.
故选C.点评:
本题考点: 纯净物和混合物的判别.
考点点评: 解答本题要充分理解纯净物和混合物的区别,要分析物质是由几种物质组成的,如果只有一种物质组成就属于纯净物.如果有多种物质就属于混合物.1年前查看全部
- (2011•武威)下列物质中,与盐酸不反应的是( )
(2011•武威)下列物质中,与盐酸不反应的是( )
A.CuO
B.Ba(OH)2
C.H2SO4
D.Na2CO3 yjsh2051年前1
yjsh2051年前1 -
 责任与爱情 共回答了27个问题
责任与爱情 共回答了27个问题 |采纳率96.3%解题思路:根据酸的化学性质:酸能与金属氧化物反应生成盐和水,能与碱反应生成盐和水,能与碳酸盐反应生成盐、水和二氧化碳,据此进行分析判断.A、氧化铜属于金属氧化物,能与盐酸反应生成氯化铜和水,故选项不符合题意.
B、Ba(OH)2属于碱,能与盐酸反应生成氯化钡和水,故选项不符合题意.
C、盐酸与硫酸不反应,故选项符合题意.
D、Na2CO3属于碳酸盐,能与盐酸反应生成氯化钠、水、二氧化碳,故选项不符合题意.
故选C.点评:
本题考点: 酸的化学性质.
考点点评: 本题难度不大,考查酸的化学性质,熟练掌握酸的化学性质并能灵活运用是正确解答本题的关键.1年前查看全部
- (2007•武威)石灰石是我市主要矿产之一,小江同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验.
(2007•武威)石灰石是我市主要矿产之一,小江同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验.
试通过分析计算:实验步骤 ①称取烧杯的质量 ②将适量盐酸加入烧杯中并称重 ③称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 ④待反应完全后,称重 实验图示 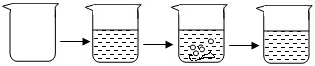
实验数据 烧杯的质量为50.0g 烧杯和盐酸的质量为100.0g 石灰石样品样品的质量为12.0g 烧杯和其中混合物的质量为107.6g
(1)该实验中生成的二氧化碳的质量是多少克?
(2)该石灰石样品的纯度是否符合要求?(假设石灰石样品中的杂质不与盐酸反应也不溶于水) 888290951年前1
888290951年前1 -
 阿风儿 共回答了16个问题
阿风儿 共回答了16个问题 |采纳率87.5%(1)根据质量守恒定律得:反应放出CO2的质量=(100.0g+12.0g)-107.6g=4.4g;
(2)设12.0g石灰石样品中含CaCO3质量为x
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 4.4g
100
x=
44
4.4g
x=
100×4.4g
44=10.0g
该石灰石样品的纯度为:
10.0g
12.0g×100%=83.3%
因83.3%<85%,所以该石灰石样品的纯度不符合要求.
答:(1)该实验中生成的二氧化碳的质量是4.4g;(2)该石灰石样品的纯度不符合要求.1年前查看全部
- (2010•武威)2010年上海世博会中国馆-“东方之冠”给人强烈的视觉冲击,它的主体结构为四根巨型钢筋混凝上制成的陔心
 (2010•武威)2010年上海世博会中国馆-“东方之冠”给人强烈的视觉冲击,它的主体结构为四根巨型钢筋混凝上制成的陔心筒.其中钢属于( )
(2010•武威)2010年上海世博会中国馆-“东方之冠”给人强烈的视觉冲击,它的主体结构为四根巨型钢筋混凝上制成的陔心筒.其中钢属于( )
A.金属材料
B.合成材料
C.天然材料
D.复合材料 appleclub1年前1
appleclub1年前1 -
 zhw2526 共回答了20个问题
zhw2526 共回答了20个问题 |采纳率95%由于金属材料是指金属元素或以金属元素为主构成的具有金属特性的材料的统称,钢属于铁的一种重要合金,是含有一定量碳的金属铁,应属于金属材料的范畴.
故选A1年前查看全部
- (2008•武威)某同学欲配置40g质量分数为9%的氯化钠溶液,全部操作过程如图所示,看图回答问题:
(2008•武威)某同学欲配置40g质量分数为9%的氯化钠溶液,全部操作过程如图所示,看图回答问题:

(1)称量时,应称取______g 食盐,把水的密度近似地看作1g/mL,则须量取______mL水,如果有10mL、50mL和100mL的量筒,最好选取______mL的量筒.
(2)实验中使用玻璃棒的目的是______.
(3)如果所配得的溶液溶质的质量分数比小于9%,你认为可能的原因有(写一条):______. 855891311年前1
855891311年前1 -
 y730210 共回答了12个问题
y730210 共回答了12个问题 |采纳率91.7%解题思路:(1)根据“溶质的质量=溶液的质量×溶质的质量分数”计算配制溶液所需食盐的量及“溶剂的质量=溶液的质量-溶质的质量”计算出水的量并换算成体积,并根据“量程稍大于所量液体体积”的原则选择量筒;
(2)明白溶解时玻璃棒的作用,为加快溶解需要使用玻璃棒;
(3)分析结果偏小的原因:一是食盐量偏少,二是水的量偏多.找出造成上述两种可能的错误操作.(1)食盐的质量=40g×9%=3.6g;水的质量=40g-3.6g=36.4g,合36.4mL;
需要量取36.4mL水所以在“10mL、50mL和100mL的量筒”中选择最接近此体积的50mL的量筒.
故答案为:3.6,36.4,50;
(2)溶解操作中用玻璃棒进行搅拌,可以加快食盐的溶解,直到固体物质全部溶解.
故答案为:加速溶解;
(3)如果所配得的溶液溶质的质量分数小于9%,要从食盐的量少和水的量多分析:造成食盐量不足3.6g的原因有:药品和砝码位置颠倒、将食盐移入烧杯时未全部倒入、溶解时搅拌不彻底还有食盐未溶解;
造成量水的体积>36.4mL的操作可能是量取水时仰视读数等.
故答案为:量取水时仰视读数(合理即可)点评:
本题考点: 一定溶质质量分数的溶液的配制.
考点点评: 量取液体读数时视线:与凹液面最低处保持在同一水平面上称之为平视,从高处向下看称为俯视,读数大于实际体积;从低处向上看称为仰视,读数小于实际体积.1年前查看全部
- (2013•武威)紫薯因富含硒元素被誉为“抗癌大王”.硒元素的部分信息如图所示.下列说法不正确的是( )
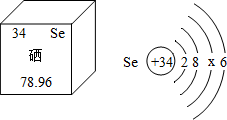 (2013•武威)紫薯因富含硒元素被誉为“抗癌大王”.硒元素的部分信息如图所示.下列说法不正确的是( )
(2013•武威)紫薯因富含硒元素被誉为“抗癌大王”.硒元素的部分信息如图所示.下列说法不正确的是( )
A.硒是一种非金属元素
B.硒元素的质子数为34
C.硒的原子结构示意图中x=18
D.在化学反应中,硒原子容易失去2个电子 潘驴等小钱1年前1
潘驴等小钱1年前1 -
 luckystar0803 共回答了18个问题
luckystar0803 共回答了18个问题 |采纳率94.4%解题思路:根据图中元素周期表可以获得的信息:原子序数、元素种类等,原子序数=质子数,当质子数=核外电子数,为原子;进行分析判断即可.A、根据元素周期表中的一格中获取的信息,该元素的名称是硒,属于非金属元素,故选项说法正确.
B、根据元素周期表中的一格中获取的信息,该元素的原子序数为34,又原子序数=质子数,因此硒元素的质子数为34,故选项说法正确.
C、当质子数=核外电子数,为原子,由硒的原子结构示意图,则34=2+8+x+6,解得x=18,故选项说法正确.
D、由硒的原子结构示意图可知,原子最外层电子数为6,在化学反应中,硒原子容易得到2个电子形成稳定结构,故选项说法错误.
故选D.点评:
本题考点: 元素周期表的特点及其应用;原子结构示意图与离子结构示意图.
考点点评: 本题难度不大,考查学生灵活运用元素周期表中元素的信息及辨别元素种类的方法、原子中核内质子数和核外电子数之间的关系等进行分析解题的能力.1年前查看全部
- 求大地坐标的含义比如在武威的一个点X=4223959.007,Y=18256697.770,H=1844.520,(图纸
求大地坐标的含义
比如在武威的一个点X=4223959.007,Y=18256697.770,H=1844.520,(图纸上说是80系,6°带,中央子午线105°).在谷歌地球上看到的这个点的经纬度为:北38.1157°,东102.227°,高1849米(在一定的误差范围内).
我的问题是:如果X表示该点到赤道的距离(我是这么算的:3.14*2*38.1157*6356755.2882/360=4226652.43,与X误差2693).那么Y代表什么,18*6=108,但图纸上却说是105中央子午线,还有后面的2556697代表该店到哪条经线的距离. 就在回1年前1
就在回1年前1 -
 woonight 共回答了24个问题
woonight 共回答了24个问题 |采纳率79.2%话说 里边的X Y 代表的 不是分别到经线和纬线的距离 都是到达80坐标系原点的距离,
80坐标系原点 坐标为东经108°55'、34°32',海拔高度417.20米
你要是想把空间直角坐标系的坐标 转成大地的 有专门软件的 .
至于几度带的问题 Y坐标如果是8位,那么对我国的格网坐标来说前两位就是带号,大于25的就是3度带.你这个就是6度的
俺是群里的 浮夸 有事群里问就行 嘿嘿1年前查看全部
- (2009•武威)将甲、乙两种金属片分别放入硫酸铜溶液中,甲表面析出金属铜,乙没有发生反应.据此判断,三种金属的活动性顺
(2009•武威)将甲、乙两种金属片分别放入硫酸铜溶液中,甲表面析出金属铜,乙没有发生反应.据此判断,三种金属的活动性顺序是( )
A.甲>铜>乙
B.铜>甲>乙
C.乙>铜>甲
D.甲>乙>铜 mulan2371年前1
mulan2371年前1 -
 sophiehyl 共回答了16个问题
sophiehyl 共回答了16个问题 |采纳率81.3%解题思路:在金属活动性顺序中位于前面的金属能把位于后面的金属从它们的化合物溶液中置换出来.将甲、乙两种金属片分别放入硫酸铜溶液中,甲表面析出金属铜,乙没有发生反应.说明甲比铜活泼,乙没有铜活泼,所以三种金属的活动性顺序是甲>铜>乙,故B、C、D均不正确.
故选:A.点评:
本题考点: 金属活动性顺序及其应用.
考点点评: 本题直接考查金属活动性顺序的第三点应用.1年前查看全部
- (2014•武威一模)20℃时,食盐的溶解度为36g,在20℃时,50g水中加入了20g食盐,充分溶解后所形成的溶液的质
(2014•武威一模)20℃时,食盐的溶解度为36g,在20℃时,50g水中加入了20g食盐,充分溶解后所形成的溶液的质量是( )
A.70g
B.66g
C.68g
D.136g iky_b7ddu__0eef1年前1
iky_b7ddu__0eef1年前1 -
 丫丫2 共回答了11个问题
丫丫2 共回答了11个问题 |采纳率81.8%解题思路:根据溶解度定义考虑本题,再看20g食盐放入50克水中是否全部溶解.溶解度为36克是指在100克水里达到饱和状态所溶解的溶质质量为36g,所以将20g食盐放入50克水中只能溶解18g,所以所得食盐溶液的质量为68g.
故选C.点评:
本题考点: 固体溶解度的概念.
考点点评: 将一定质量物质溶于水中所得溶液质量,要先根据溶解度算出能够溶解多少,不溶的,不能算溶液质量.1年前查看全部
- (2008•武威)期末化学实验老师整理药品时,拿出一瓶久置的氢氧化钙粉末[Ca(OH)2)],他让小王和大伟对这瓶氢氧化
(2008•武威)期末化学实验老师整理药品时,拿出一瓶久置的氢氧化钙粉末[Ca(OH)2)],他让小王和大伟对这瓶氢氧化钙粉末的组成进行实验探究.
(1)提出问题:这瓶氢氧化钙是否已经生成碳酸钙(CaCO3)而变质?
(2)进行猜想:①氢氧化钙全部变为碳酸钙;②氢氧化钙部分变为碳酸钙;③氢氧化钙没有变质.
(3)设计实验方案、进行实验:下表是对猜想①进行实验探究的过程示例:
请你另选择一种猜想参与探究,完成下表.实验步骤 实验现象 实验结论 取样,加适量水,搅拌,过滤
①取少量滤液于试管中,滴入酚酞试液
②取少量滤液于试管中,加入盐酸①滤液不变色
②有气泡产生氢氧化钙全部变为碳酸钙
(4)反思与应用:实验步骤 实验现象 实验结论 取样,加适量水,搅拌,过滤
①取少量滤液于试管中,滴入酚酞试液
②取少量滤液于试管中,加入盐酸① ②
氢氧化钙变质是由于与空气中的______发生反应的缘故,反应的化学程式是:______,因此氢氧化钙应______保存. 龙裔绝色1年前1
龙裔绝色1年前1 -
 klfrdamo 共回答了18个问题
klfrdamo 共回答了18个问题 |采纳率94.4%解题思路:由于氢氧化钙能和空气中的二氧化碳发生化学反应生成碳酸钙和水,因此只要鉴别出碳酸钙和氢氧化钙的存在,就可以探究出氢氧化钙是全部变质、部分变质还是全部变质.若选择第二种方案则答案为
实验现象实验结论
①滤液变为红色
②有气泡冒出氢氧化钙部分变为碳酸钙若选择第三种方案则答案为
实验现象实验结论
①滤液变为红色
②无气泡冒出氢氧化钙没有变质(4)氢氧化钙变质是由于与空气中的 二氧化碳发生反应的缘故.
故答案为:二氧化碳,CO2+Ca(OH)2=CaCO3↓+H2O,密封点评:
本题考点: 药品是否变质的探究;猜想与事实验证;二氧化碳的化学性质;碱的化学性质;碳酸钠、碳酸氢钠与碳酸钙;书写化学方程式、文字表达式、电离方程式.
考点点评: 该题主要考查了氢氧化钙和碳酸钙的化学性质.1年前查看全部
- (2014•武威模拟)如图:⊙M在直角坐标系中,圆心M在y轴正半轴上,弧AB所对的圆心角是120°,⊙M的半径是2cm.
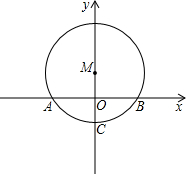 (2014•武威模拟)如图:⊙M在直角坐标系中,圆心M在y轴正半轴上,弧AB所对的圆心角是120°,⊙M的半径是2cm.
(2014•武威模拟)如图:⊙M在直角坐标系中,圆心M在y轴正半轴上,弧AB所对的圆心角是120°,⊙M的半径是2cm.
(1)求点M的坐标.
(2)求过A、B、C三点的抛物线的解析式.
(3)点D是弦AB所对的优弧上一动点,求四边形ACBD面积的最大值.
(4)在(2)中的抛物线上是否存在一点P,使得点P、A、B为顶点的三角形与△ABC相似?若存在求出点P的坐标;若不存在,说明理由. lhl33201年前0
lhl33201年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2014•武威模拟)下列图形是中心对称图形而不是轴对称图形的是( )
(2014•武威模拟)下列图形是中心对称图形而不是轴对称图形的是( )
A.正三角形
B.等腰梯形
C.矩形
D.平行四边形 yakxi1年前1
yakxi1年前1 -
 weiweio2 共回答了17个问题
weiweio2 共回答了17个问题 |采纳率94.1%解题思路:根据轴对称图形与中心对称图形的概念求解.A、是轴对称图形,不是中心对称图形,故本选项错误;
B、是轴对称图形,不是中心对称图形,故本选项错误;
C、是轴对称图形,也是中心对称图形,故本选项错误;
D、不是轴对称图形,是中心对称图形,故本选项正确.
故选D.点评:
本题考点: 中心对称图形;轴对称图形.
考点点评: 考查了中心对称图形与轴对称图形的概念.轴对称图形的关键是寻找对称轴,图形两部分折叠后可重合,中心对称图形是要寻找对称中心,旋转180度后与原图重合.1年前查看全部
- (2010•武威)我省著名品牌“祁连山”水泥享誉全国.该厂化验室为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足
(2010•武威)我省著名品牌“祁连山”水泥享誉全国.该厂化验室为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水).有关实验数据见下表:
请计算:反应前 反应后 实验 烧杯和稀盐酸的质量 石灰石样品的质量 烧杯和其中混合物的质量 数据 180g 12g 187.6g
(1)反应生成二氧化碳的质量为______g.
(2)该石灰石中碳酸钙的质量分数.(精确到0.1%) hongshaohan1年前1
hongshaohan1年前1 -
 萧花飞颐 共回答了15个问题
萧花飞颐 共回答了15个问题 |采纳率100%解题思路:(1)依据反应前后物质的质量的变化可以求出生成的二氧化碳质量;
(2)利用二氧化碳的质量结合方程式对相关问题进行解答即可;(1)由质量守恒定律可得反应生成的二氧化碳质量是187.6g-12g-180g=4.4 g;(2)设该石灰石样品中碳酸钙的质量为x.CaCO3+2HCl═CaCl2+H2O+CO2↑100&nb...
点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 本考点考查了根据化学方程式的计算,属于表格型计算题.要充分利用“遇到差值想气体”,根据质量守恒定律求气体的质量,然后再求其它物质的质量,要会分析表格的数据.做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律,本考点主要出现在计算题中1年前查看全部
- (2013•武威)为探究物质燃烧的条件,某同学做了如图所示的实验.实验发现水中的白磷和铜片上的红磷都没燃烧,铜片上的白磷
 (2013•武威)为探究物质燃烧的条件,某同学做了如图所示的实验.实验发现水中的白磷和铜片上的红磷都没燃烧,铜片上的白磷着火燃烧(已知白磷的着火点40℃,红磷着火点240℃.)对此实验的认识错误的是( )
(2013•武威)为探究物质燃烧的条件,某同学做了如图所示的实验.实验发现水中的白磷和铜片上的红磷都没燃烧,铜片上的白磷着火燃烧(已知白磷的着火点40℃,红磷着火点240℃.)对此实验的认识错误的是( )
A.可燃物要与氧气接触
B.物质燃烧温度必须要达到着火点
C.铜片上的红磷没燃烧,因为红磷不是可燃物
D.烧杯中热水的作用既供热又使白磷Ⅱ与氧气隔绝 开始也1年前1
开始也1年前1 -
 aa大使者 共回答了15个问题
aa大使者 共回答了15个问题 |采纳率93.3%解题思路:A、根据铜片上的白磷燃烧,水中的白磷不能燃烧来考虑本题;
B、根据铜片上的白磷能燃烧,红磷不能燃烧来考虑;
C、根据燃烧的条件考虑;
D、根据水的作用考虑.A、燃烧的条件是具有可燃物、温度达到该物质的着火点、与氧气接触,铜片上的白磷燃烧,水中的白磷不能燃烧,因为水中没有氧气,故A正确;
B、因为燃烧的条件是具有可燃物、温度达到该物质的着火点、与氧气接触,铜片上的白磷能燃烧,红磷不能燃烧,原因是红磷的着火点高,所以物质燃烧温度必须要达到着火点,故B正确;
C、铜片上的红磷没燃烧,因为红磷没有达到着火点,故C错误;
D、烧杯中热水的作用一是提供热量使白磷达到着火点,二是隔绝空气,故D正确;
故选C.点评:
本题考点: 燃烧与燃烧的条件.
考点点评: 要掌握燃烧的条件,具有可燃物、温度达到该物质的着火点、与氧气接触,知道控制变量的实验的设计方法,只允许有一个变量.1年前查看全部
- (2009•武威)某化学兴趣小组为了测定一工厂废水中硫酸的含量,取100g废水于烧杯中,加入120g质量分数为10%的氢
(2009•武威)某化学兴趣小组为了测定一工厂废水中硫酸的含量,取100g废水于烧杯中,加入120g质量分数为10%的氢氧化钠溶液,恰好完全反应(废水中无不溶物,其它成份不与氢氧化钠反应).请计算:
(1)废水中硫酸的质量分数;
(2)该工厂每天用含氢氧化钙75%熟石灰处理150t这种废水,需要熟石灰多少吨. lqyq1年前1
lqyq1年前1 -
 chenmy2002 共回答了25个问题
chenmy2002 共回答了25个问题 |采纳率92%解题思路:(1)根据硫酸与氢氧化钠反应的化学方程式和氢氧化钠的质量.列出比例式,就可计算出参与反应的H2SO4质量,然后根据质量分数公式计算即可;
(2)根据氢氧化钙与硫酸反应的化学方程式和硫酸的质量,列出比例式,就可计算出需要熟石灰的质量.(1)设参与反应的H2SO4质量为x,
H2SO4+2NaOH=2H2O+Na2SO4
98----80
x---120g×10%
∴[98/80=
x
120g×10%]
解之得:x=14.7g,
废水中硫酸的质量分数为:[14.7g/100g]×100%=14.7%.
(2)设需要熟石灰质量为y,
Ca(OH)2+H2SO4=CaSO4+2H2O
74-----98
75%y--150t×14.7%
[74/98]=[75%y/150t×14.7%]
解之得:y=22.2t.
答:(1)废水中硫酸的质量分数为14.7%;(2)需要熟石灰22.2t.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 本题主要考查学生运用化学方程式进行计算的能力.1年前查看全部
- (2009•武威)下列实验基本操作错误的是( )
(2009•武威)下列实验基本操作错误的是( )
A.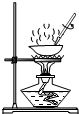
蒸发
B.
稀释浓硫酸
C.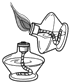
点燃酒精灯
D.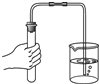
检查装置气密性 wu09021年前1
wu09021年前1 -
 z_k_f806 共回答了19个问题
z_k_f806 共回答了19个问题 |采纳率94.7%A、蒸发时,用玻璃棒不停地进行搅拌,及时散热;图中操作正确,故A正确;
B、稀释浓硫酸的操作,图中正确,一定要注意安全,故B正确;
C、点燃酒精灯时,用火柴点燃,如果用燃着的酒精灯去点燃另一个酒精灯,会引起酒精失火,造成危险.图中操作错误,故C错误;
D、图中检查装置气密性的方法正确,故D正确
故选C.1年前查看全部
- (2013•武威)除去下列物质中所含的杂质,括号内的除杂剂不正确的是( )
(2013•武威)除去下列物质中所含的杂质,括号内的除杂剂不正确的是( )
A.二氧化碳中混有水蒸气(足量生石灰)
B.铜粉中混有铁粉(足量稀硫酸)
C.NaNO3溶液中混有AgNO3(适量NaCl溶液)
D.KOH溶液中混有K2CO3(适量澄清石灰水) chendanzhi19841年前1
chendanzhi19841年前1 -
 kaori_ 共回答了24个问题
kaori_ 共回答了24个问题 |采纳率87.5%解题思路:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.A、生石灰是氧化钙的俗称,与水反应生成氢氧化钙,生成的氢氧化钙与二氧化碳反应生成碳酸钙和水,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的除杂剂错误.
B、铁粉能与稀硫酸反应生成硫酸亚铁的氢气,铜粉不与稀硫酸反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的除杂剂正确.
C、硝酸银溶液能与适量的氯化钠溶液溶液反应生成氯化银沉淀和硝酸钠,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的除杂剂正确.
D、碳酸钾溶液能与澄清的石灰水反应生成碳酸钙沉淀和氢氧化钾,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的除杂剂正确.
故选A.点评:
本题考点: 物质除杂或净化的探究;常见气体的检验与除杂方法;金属的化学性质;盐的化学性质.
考点点评: 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.1年前查看全部
- (2007•武威)石灰石是我市主要矿产之一,小江同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验.
(2007•武威)石灰石是我市主要矿产之一,小江同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验.
试通过分析计算:实验步骤 ①称取烧杯的质量 ②将适量盐酸加入烧杯中并称重 ③称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 ④待反应完全后,称重 实验图示 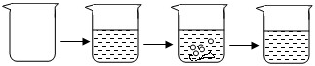
实验数据 烧杯的质量为50.0g 烧杯和盐酸的质量为100.0g 石灰石样品样品的质量为12.0g 烧杯和其中混合物的质量为107.6g
(1)该实验中生成的二氧化碳的质量是多少克?
(2)该石灰石样品的纯度是否符合要求?(假设石灰石样品中的杂质不与盐酸反应也不溶于水) Sunnywei1年前1
Sunnywei1年前1 -
 除却0001 共回答了23个问题
除却0001 共回答了23个问题 |采纳率91.3%(1)根据质量守恒定律得:反应放出CO2的质量=(100.0g+12.0g)-107.6g=4.4g;
(2)设12.0g石灰石样品中含CaCO3质量为x
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 4.4g
100
x=
44
4.4g
x=
100×4.4g
44=10.0g
该石灰石样品的纯度为:
10.0g
12.0g×100%=83.3%
因83.3%<85%,所以该石灰石样品的纯度不符合要求.
答:(1)该实验中生成的二氧化碳的质量是4.4g;(2)该石灰石样品的纯度不符合要求.1年前查看全部
- (2014•武威)化学与生活密切相关,在厨房里蕴藏着许多化学知识.
(2014•武威)化学与生活密切相关,在厨房里蕴藏着许多化学知识.
(1)下列食物中,能提供大量维生素的是______(填字母序号);
A.蔬菜
B.牛奶
C.大米
(2)加钙牛奶中的“钙”是指______(填“元素”或“分子”),老年人身体中一旦缺钙,可能患有的疾病是______;
(3)厨房中的下列物品中,所使用的主要材料属于天然纤维的是______(填字母序号);
A.塑料保鲜膜
B.橡胶手套
C.棉布围裙
(4)我们常用洗涤剂清洗餐具上的油污,这是因为洗涤剂具有______的功能;
(5)厨房中能用来除去水壶中水垢的物质是______(填“食醋”或“食盐水”). huckwin1年前1
huckwin1年前1 -
 尘埃没落定 共回答了15个问题
尘埃没落定 共回答了15个问题 |采纳率86.7%解题思路:(1)A、从蔬菜中含有大量的维生素去分析解答;
B、牛奶中含有大量的蛋白质去分析解答;
C、大米含有大量的糖类去分析解答;
(2)加钙牛奶中的“钙”是指含有钙元素而不是钙单质,老年人缺钙可造成骨质疏松去分析解答;
(3)A、塑料属于合成材料去分析解答;
B、橡胶也属于合成材料去分析解答;
C、棉布是棉花纺出的线织成的布,棉花属于天然有机高分子是天然纤维去分析解答;
(4)从洗涤剂能使植物油在水中分散成无数细小的小液滴,而不聚集成大的油珠,形成的小液滴可以随着水流动去分析解答;
(5)从水垢的主要成分是碳酸钙和氢氧化镁,都能和酸反应生成溶于水的物质,而和食盐不发生反应去分析解答;(1)A、蔬菜中含有大量的维生素;故A正确;
B、牛奶中含有大量的蛋白质;故B错误;
C、大米含有大量的糖类;故C错误;
故选:A;
(2)加钙牛奶中的“钙”是指含有钙元素而不是钙单质,老年人缺钙可造成骨质疏松,
故答案为:元素;骨质疏松;
(3)A、塑料属于合成材料;故A错误;
B、橡胶也属于合成材料;故B错误;
C、棉布是棉花纺出的线织成的布,棉花属于天然有机高分子是天然纤维;故C正确;
故选:C;
(4)我们常用洗涤剂清洗餐具上的油污,这是因为洗涤剂具有乳化功能,能使植物油在水中分散成无数细小的小液滴,而不聚集成大的油珠,形成的小液滴可以随着水流动;
故答案为:乳化;
(5)水垢的主要成分是碳酸钙和氢氧化镁,都能和酸反应生成溶于水的物质,而和食盐不发生反应;
故答案为:食醋.点评:
本题考点: 生命活动与六大营养素;乳化现象与乳化作用;酸的化学性质;有机高分子材料的分类及鉴别;人体的元素组成与元素对人体健康的重要作用.
考点点评: 生活处处有化学,学会用化学知识解决生活中的问题.1年前查看全部
- (2014•武威一模)某花圃所种的花卉缺乏氮元素,则应施用的化肥是( )
(2014•武威一模)某花圃所种的花卉缺乏氮元素,则应施用的化肥是( )
A.K2SO4
B.草木灰
C.CO(NH2)2
D.Ca(H2PO4)2 wangaipeng1年前1
wangaipeng1年前1 -
 fgfhfghfgh 共回答了20个问题
fgfhfghfgh 共回答了20个问题 |采纳率90%解题思路:根据题意,应施用含氮元素的化肥;含有氮元素的肥料称为氮肥,含有磷元素的肥料称为磷肥,含有钾元素的肥料称为钾肥,同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥.根据题意,应施用含氮元素的化肥;
A、K2SO4中含有钾元素,属于钾肥.
B、草木灰中含有钾元素,属于钾肥.
C、CO(NH2)2中含有氮元素,属于氮肥.
D、Ca(H2PO4)2中含有磷元素,属于磷肥.
故选C.点评:
本题考点: 常见化肥的种类和作用.
考点点评: 本题主要考查化肥的分类方面的知识,解答时要分析化肥中含有哪些营养元素,然后再根据化肥的分类方法确定化肥的种类.1年前查看全部
- (2008•武威)下列物质中,遇水就变得“冷冰冰”的是( )
(2008•武威)下列物质中,遇水就变得“冷冰冰”的是( )
A.氢氧化钠固体
B.生石灰
C.硝酸铵
D.浓硫酸 zhoulinty1年前1
zhoulinty1年前1 -
 kpzhy 共回答了12个问题
kpzhy 共回答了12个问题 |采纳率83.3%解题思路:根据物质溶于水放热还是吸热来考虑本题,知道常见放热物质有哪些?常见吸热物质有哪些?并能灵活运用.物质溶于水分为两个过程:构成物质的微粒向水中扩散的过程,这一过程需吸热,构成物质的微粒与水分子形成水和分子的过程,这一过程需放热,如果吸热大于放热则溶于水表现为吸热,如果吸热小于放热则溶于水表现为放热,如果吸热等于放热则表现为溶于水温度不变.常见的溶于水放热的有:浓硫酸、生石灰、氢氧化钠固体.常见吸热的有:硝酸铵.
故选C.点评:
本题考点: 溶解时的吸热或放热现象.
考点点评: 要了解物质溶于水的过程,知道为什么放热和吸热,记住溶于水吸热和放热的常见物质.1年前查看全部
- (2007•武威)下列设计方案可行,且化学方程式书写正确的是( )
(2007•武威)下列设计方案可行,且化学方程式书写正确的是( )
A.用NaOH溶液治疗胃酸过多症:NaOH+HCl═NaCl+H20
B.实验室用稀硫酸与大理石反应制取C02:H2S04+CaC03═CaS04+C02+H2O
C.用适量的稀盐酸除去铁表面的锈迹:Fe203+6HCl═2FeCl3+3H2O
D.用点燃方法除去二氧化碳气体中混有的少量一氧化碳:2CO+402
2CO2点燃 . go3g1年前1
go3g1年前1 -
 rain_ling 共回答了19个问题
rain_ling 共回答了19个问题 |采纳率94.7%解题思路:首先判断应用的原理是否正确;若应用原理正确,再根据化学方程式判断正误的方法需考虑:化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.A、氢氧化钠溶液具有腐蚀性,不能用于治疗胃酸过多症.
B、碳酸钙与稀硫酸反应生成微溶于水的硫酸钙,覆盖在大理石表面,阻止反应的进行,不能用于实验室制取C02.
C、铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,该实验设计方案可行,且该化学方程式书写正确,故选项正确.
D、除去二氧化碳中的一氧化碳不能够通氧气点燃,这是因为当二氧化碳(不能燃烧、不能支持燃烧)大量存在时,少量的一氧化碳是不会燃烧的;且除去气体中的气体杂质不能使用气体,否则会引入新的气体杂质.
故选A.点评:
本题考点: 化学实验方案设计与评价;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断,化学方程式正误判断方法是:先看化学式是否正确,再看配平,再看反应条件,再看气体和沉淀,最后短线改成等号.1年前查看全部
- (2014•武威)下列装置常用于实验室制取气体.根据给出的装置回答下列问题
(2014•武威)下列装置常用于实验室制取气体.根据给出的装置回答下列问题
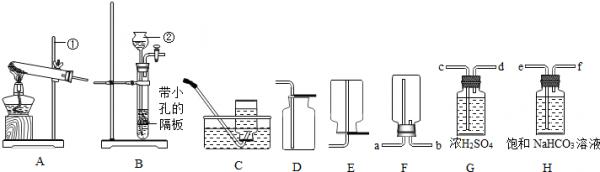
(1)指出编号仪器名称:②______.
(2)实验室利用A装置制取氧气,反应原理用化学方程式表示为2KClO3
2KCl+3O2↑MnO2 .△ 2KClO3.
2KCl+3O2↑MnO2 .△
(3)制取并收集二氧化碳应选择的装置是______(从A--E中选择),使用该套装置制取气体的突出优点是______,该反应原理用化学方程式表示为______改用F装置收集二氧化碳,则气体应从______端进入.制得的二氧化碳中常含有少量的氯化氢气体与水蒸气,欲使个G、H装置将以上杂质气体除去,则装置正确的连接顺序是:混合气体→______(用端口字母表示).
(4)将纯净的二氧化碳气体通入盛有蒸馏水的洗气瓶一段时间后,测得该装置中溶液的pH______(填“>”、“<”或“=”)7. selectld1年前1
selectld1年前1 -
 8535632 共回答了27个问题
8535632 共回答了27个问题 |采纳率88.9%解题思路:要熟悉各种仪器的名称、用途;
书写化学方程式要注意规范性;
制取二氧化碳不需要加热,二氧化碳的密度比空气大;
如果需要除去氯化氢和水时,一般应该先除去氯化氢,后除去水;
二氧化碳能和水反应生成碳酸.(1)②是长颈漏斗.
故答案为:长颈漏斗.
(2)实验室可以用加热高锰酸钾或氯酸钾的方法制取氧气,因为A装置中试管口没有棉花,不能用加热高锰酸钾制取,应该用加热氯酸钾的方法制取,氯酸钾在二氧化锰的催化作用下受热分解生成氯化钾和氧气,反应的化学方程式为:2KClO3
MnO2
.
△2KCl+3O2↑.
故答案为:2KClO3
MnO2
.
△2KCl+3O2↑.
(3)制取二氧化碳可以用B装置,二氧化碳的密度比空气大,可以用向上排空气法收集,用D装置.
故选:B、D.
使用该套装置制取气体的突出优点是:可以随时使反应进行,也可以随时使反应停止.
故答案为:可以随时使反应进行,也可以随时使反应停止.
实验室用大理石或石灰石和稀盐酸反应制取二氧化碳,大理石或石灰石的主要成分是碳酸钙,碳酸钙和稀盐酸反应能生成氯化钙、水和二氧化碳,化学方程式为:
CaCO3+2HCl=CaCl2+H2O+CO2↑.
故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
用F装置收集二氧化碳时,气体应从b端进入.
故选:b.
要除去氯化氢气体与水蒸气,应该先除去氯化氢,再除去水,连接顺序为:混合气体→e→f→c→d.
故答案为:e→f→c→d.
(4)二氧化碳和水反应生成碳酸,碳酸显酸性,pH小于7.
故答案为:<.点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;气体的净化(除杂);实验室制取氧气的反应原理;二氧化碳的实验室制法;二氧化碳的化学性质;溶液的酸碱性与pH值的关系;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查实验设计、杂质去除和化学方程式的书写等方面的知识,书写化学方程式时要注意四步,一是反应物和生成物的化学式要正确,二是遵循质量守恒定律,三是写上必要的条件,四是看是否有“↑”或“↓”.1年前查看全部
- (2007•武威)石灰石是我市主要矿产之一,小江同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验.
(2007•武威)石灰石是我市主要矿产之一,小江同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验.
试通过分析计算:实验步骤 ①称取烧杯的质量 ②将适量盐酸加入烧杯中并称重 ③称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 ④待反应完全后,称重 实验图示 
实验数据 烧杯的质量为50.0g 烧杯和盐酸的质量为100.0g 石灰石样品样品的质量为12.0g 烧杯和其中混合物的质量为107.6g
(1)该实验中生成的二氧化碳的质量是多少克?
(2)该石灰石样品的纯度是否符合要求?(假设石灰石样品中的杂质不与盐酸反应也不溶于水) nn晶231年前1
nn晶231年前1 -
 秋雨冬雪1 共回答了17个问题
秋雨冬雪1 共回答了17个问题 |采纳率88.2%解题思路:(1)石灰石中主要成分碳酸钙可以与盐酸反应生成氯化钙、水和气体二氧化碳;随着反应的发生,二氧化碳不断放出而使烧杯内物质质量减小;完全反应前后烧杯中物质质量差为放出气体二氧化碳的质量;
(2)石灰石样品的纯度=[石灰石样品中碳酸钙的质量/石灰石样品的质量12.0g]×100%,根据反应的化学方程式,可由反应放出二氧化碳的质量计算参加反应的碳酸钙的质量.(1)根据质量守恒定律得:反应放出CO2的质量=(100.0g+12.0g)-107.6g=4.4g;
(2)设12.0g石灰石样品中含CaCO3质量为x
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 4.4g
[100/x=
44
4.4g]
x=[100×4.4g/44]=10.0g
该石灰石样品的纯度为:[10.0g/12.0g]×100%=83.3%
因83.3%<85%,所以该石灰石样品的纯度不符合要求.
答:(1)该实验中生成的二氧化碳的质量是4.4g;(2)该石灰石样品的纯度不符合要求.点评:
本题考点: 含杂质物质的化学反应的有关计算;质量守恒定律及其应用.
考点点评: 根据质量守恒定律,放出气体的反应,反应前各物质的总质量与反应后剩余物质的质量差即为反应放出气体的质量.1年前查看全部
- (2011•武威)不能用燃着的木条鉴别的一组物质是( )
(2011•武威)不能用燃着的木条鉴别的一组物质是( )
A.空气和氧气
B.羊毛织物和化纤织物
C.氦气和二氧化碳
D.聚乙烯塑料和聚氯乙烯塑料 woxiangfa1年前1
woxiangfa1年前1 -
 菊花茶蜜 共回答了25个问题
菊花茶蜜 共回答了25个问题 |采纳率96%解题思路:A、根据空气的成分和氧气的性质及影响燃烧现象的因素判断.
B、根据羊毛和化纤的燃烧气味判断.
C、根据氦气和二氧化碳的化学性质判断.
D、根据的成分和燃烧现象判断.A、空气中含有氧气,只不过浓度比纯氧低,氧气能支持燃烧,燃着的木条在空气中燃烧现象不变,在氧气中燃烧更旺,所以能够鉴别.
B、羊毛的主要成分是蛋白质,燃烧时有烧焦羽毛的气味,化纤是合成纤维,燃烧时有特殊的刺激性气味,所以能够鉴别.
C、氦气和二氧化碳都不燃烧,也不支持燃烧,二者不能用燃着的木条区分,所以不能鉴别.
D、聚氯乙烯塑料中含有氯元素,聚氯乙烯塑料燃烧时会产生强烈的刺激性气味,聚乙烯塑料燃烧不会产生刺激性气味,所以能够鉴别.
故选C点评:
本题考点: 常见气体的检验与除杂方法.
考点点评: 物质的鉴别是初中化学的难重点,也是中考的热点之一,了解物质的物理性质和化学性质,能运用比较法发现和利用物质间的性质差别是解题的关键.1年前查看全部
- (2013•武威)下列转化不能一步实现的是( )
(2013•武威)下列转化不能一步实现的是( )
A.CO→CO2
B.H2O→H2
C.KNO3→KCl
D.Ca(OH)3→NaOH Enliv1年前1
Enliv1年前1 -
 yfy2310 共回答了23个问题
yfy2310 共回答了23个问题 |采纳率95.7%解题思路:A、一氧化碳燃烧能生成二氧化碳;
B、电解水能生成氢气和氧气;
C、硝酸钾不能与其它物质发生复分解反应;
D、氢氧化钙和碳酸钠反应能生成碳酸钙和氢氧化钠.A、一氧化碳燃烧能生成二氧化碳,能一步实现.
B、电解水能生成氢气和氧气,能一步实现.
C、硝酸钾易溶于水,含有钾离子、硝酸根离子的化合物易溶于水,所以硝酸钾不能和其它物质反应生成氯化钾,不能一步实现.
D、氢氧化钙和碳酸钠能够发生复分解反应,生成氢氧化钠和碳酸钙,能一步实现.
故选:C.点评:
本题考点: 物质的相互转化和制备.
考点点评: 本题比较简单,只要熟记教材内容即可顺利解答.1年前查看全部
大家在问
- 1四位同学去植树,第一位同学植的树是其他同学总数的[1/2],第二位同学植的树是其他同学的[1/4],第三位同学植的树是其
- 2西北地区的主要地形是( )A.高原 盆地 山地B.平原 盆地 高原C.丘陵 山地 平原D.山地 盆地 丘陵
- 3people develop ________ preference for a particular style o
- 4关于“顺应天道自然规律”的文言语句
- 5燃料电池是一种将化学反应产生的能量直接转换成电能的装置.下列燃料电池最适合在宇宙飞船上使用的是( )
- 6数学导数系数取值问题求解已知函数f(x)=(lnx)/(x+1)+1/x,如果x大于0 x ≠1时,f(x)大于lnx/
- 7把6封写好的信,任意放入6个写好收信人的信封内,每个信封内放一封信,则恰有2个信封放对信的概率是?
- 8有关四信的名言警句有哪些急
- 9如图所示,在平面直角坐标系中xoy中,边长为2的正方形OABC的顶点A.C分别在x轴y轴的正半轴上,二次函数y=-2/3
- 10反意疑问句怎么回答?和其他与他相关的,
- 11(2009•长春)下列四个数中,小于0的是( )
- 12为什么圆在数学上一般用字母O表示(⊙O)?坐标系原点吗?
- 13help!1*2*3+2*3*4+3*4*5+···+100*101*102
- 14请问 兰州交通大学253信箱 怎么翻译成英文
- 15如图所示,上午8时,一条船从A处出发,以15海里/时的速度向正北航行,10时到B处,从A、B望灯塔C,测得∠NAC=42
