氯化钴为什么在乙醇中是蓝色氯化钴晶体为什么在乙醇中是蓝色
 HttpServletReque2022-10-04 11:39:541条回答
HttpServletReque2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 iengjitga 共回答了14个问题
iengjitga 共回答了14个问题 |采纳率100%- 这个是配位化学的问题.氯化钴本来是蓝色的,但是如果有水分子与钴离子发生络合的话,就形成了水合钴离子,这个水合钴离子是粉红色的(如果我没记错的话).通常情况下,我们看到的氯化钴要么是水溶液,要么是水合氯化钴晶体,都是以粉红色状态存在.而当它溶于乙醇的时候,就会显示出本来的氯合钴离子的颜色,而这个是蓝色的.
- 1年前
相关推荐
- 我把氯化钴溶液滴在卡纸上再烘干是蓝色的,放在空气中由于空气中水份卡纸变为粉红色了!请问在氯化钴溶...
我把氯化钴溶液滴在卡纸上再烘干是蓝色的,放在空气中由于空气中水份卡纸变为粉红色了!请问在氯化钴溶...
我把氯化钴溶液滴在卡纸上再烘干是蓝色的,放在空气中由于空气中水份卡纸变为粉红色了!请问在氯化钴溶液里需加什么化工原料可以改变卡纸的变色速度?
在氯化钴溶液里需加什么化工原料可以使蓝色卡纸在空气中变粉红色的这个反应变慢或更快甚至不变色(保持蓝色)多谢大家!急 断了翅膀的鱼20081年前1
断了翅膀的鱼20081年前1 -
 山上来的 共回答了13个问题
山上来的 共回答了13个问题 |采纳率100%要加吸水剂.可以用硅胶.
硅胶是由硅酸凝胶mSiO2·nH2O适当脱水而成的颗粒大小不同的多孔物质.具有开放的多孔结构,比表面(单位质量的表面积)很大,能吸附许多物质,是一种很好的干燥剂、吸附剂和催化剂载体.1年前查看全部
- 下列物质属于氧化物是( ) A.氧气(O 2 ) B.水(H 2 O) C.乙醇(C 2 H 6 O) D.氯化钴(C
下列物质属于氧化物是( )
A.氧气(O 2 )
B.水(H 2 O)
C.乙醇(C 2 H 6 O)
D.氯化钴(CoCl 2 ) ailinyy1年前1
ailinyy1年前1 -
 巴米扬佛像 共回答了21个问题
巴米扬佛像 共回答了21个问题 |采纳率90.5%A、氧气是一种只有氧元素组成的物质,则属于单质,故A错误;
B、水是一种含有H和O两种元素且有氧元素的物质,则属于氧化物,故B正确;
C、乙醇中含有C、H、O三种元素,属于化合物,但不属于氧化物,故C错误;
D、氯化钴是由金属离子和氯离子形成的化合物,则属于盐,故D错误;
故选B.1年前查看全部
- 氯化钴+镁 注意:有气体,请标明气体符号!那么如何用氯化钴(六水)置换出钴单质呢?
 wushanxiao1年前1
wushanxiao1年前1 -
 powersmile 共回答了15个问题
powersmile 共回答了15个问题 |采纳率100%CoCl2+Mg+2H2O===Co(OH)2(沉淀)+MgCl2+H2(气体)
这是因为Co属于中等活泼金属,排在H的前面,E(Co2+/Co)电机电势比E(H2/H+)更负,所以水中的H+率先得到Mg失去的电子而生成氢气,Co2+与水电离产生的OH-结合生成氢氧化钴的沉淀!1年前查看全部
- (2012•太原二模)用金属钴板(含少量Fe、Ni)制备应用广泛的氯化钴的工艺流程如图:
(2012•太原二模)用金属钴板(含少量Fe、Ni)制备应用广泛的氯化钴的工艺流程如图:
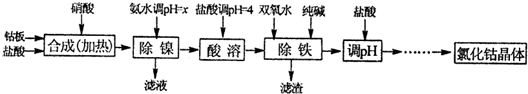
注:钴与盐酸反应极慢,需加入催化剂硝酸才可能进行实际生产.有关钴、镍和铁化合物的性质见表:
(1)“除镍”步骤中,NH3•H2O用量对反应收率的影响见表:从表中可知x=______时,除镍效果最好.化学式 沉淀完全时的pH 有关性质 Co(OH)2 9.4 Co+2HCl=CoCl2+H2↑
Co2++2NH3•H2O=Co(OH)2↓+2NH4+
Co2++2H2O⇌Co(OH)2+2H+
Ni+2HCl=NiCl2+H2↑
Ni2++6NH3•H2O=[Ni(NH3)6]2++6H2OFe(OH)2 9.6 Fe(OH)3 3.7
(2)“除镍”步骤必须控制在一定时间内完成,否则沉淀中将有部分Co(OH)2转化为Co(OH)3,此反应的化学方程式为______.加NH3•H2O调pH 收率/% Ni2+的含量/% 9 98.1 0.08 9.5 98 0.05 10 97.6 0.005 10.3 94 0.005
(3)“除铁”步骤中加入纯碱的作用是(请用离子方程式表示)______.
(4)在“调pH”步骤中,加入盐酸的作用是______.
(5)已知25℃时,KSP[Fe(OH)3]=4.0×10-38,则该温度下反应
Fe3++3H2O⇌Fe(OH)3+3H+的平衡常数K=______.
(6)已知:FeO(s)+CO(g)═Fe(s)+CO2(g)△H=-218kJ•mol-1
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.5kJ•mol-1
写出CO气体还原Fe3O4固体得到Fe固体和CO2气体的热化学方程式:______. 咸鱼kk1年前1
咸鱼kk1年前1 -
 波波AND蓓蓓 共回答了18个问题
波波AND蓓蓓 共回答了18个问题 |采纳率94.4%解题思路:(1)根据表中的数据结合实际来回答判断;
(2)钴离子易从正二价被氧气氧化到正三价;
(3)加入纯碱碳酸钠可以和酸发生反应,起到调节溶液的pH的作用;
(4)钴离子是弱碱阳离子,能发生水解,显示酸性;
(5)根据化学平衡常数表达式结合沉淀溶解溶度积规则进行计算;
(6)依据热化学方程式和盖斯定律计算得到所需让化学方程式.(1)根据表中的数据知道,当pH等于10的时候,收率最高,镍离子的含量最小,除镍效果最好,故答案为:10;
(2)钴离子易从正二价容易被氧气氧化到正三价,发生的化学方程式为:4Co(OH)2+O2+2H2O=4Co(OH)3,故答案为:4Co(OH)2+O2+2H2O=4Co(OH)3;
(3)加入纯碱碳酸钠可以和酸发生反应,在适当的环境下,可以让铁离子形成沉淀而除去,所以加入的纯碱作用是起到调节溶液的pH的作用,2Fe3++3CO32-+H2O=2Fe(OH)3↓+3CO2↑,
故答案为:使得铁离子转化为氢氧化铁沉淀而除去;
(4)钴离子是弱碱阳离子,能发生水解,显示酸性,加入盐酸可以防止Co2+水解,故答案为:防止Co2+水解;
(5)Ksp[Fe(OH)3]=c(Fe3+)×c3(OH-)=4.0×10-38,c(H+)=
10−14
c(OH−),反应Fe3++3H2O⇌Fe(OH)3+3H+的平衡常数
K=
c3(H+)
c(Fe3+)=
10−42
c(Fe3+)c3(OH−)=2.5×10-5,故答案为:2.5×10-5;
(6)①FeO(s)+CO(g)═Fe(s)+CO2(g)△H=-218kJ•mol-1
②Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.5kJ•mol-1
依据盖斯定律①×3+②得到CO气体还原Fe3O4固体得到Fe固体和CO2气体的热化学方程式:Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g)△H=-13.5KJ/mol,
故答案为:Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g)△H=-13.5KJ/mol.点评:
本题考点: 制备实验方案的设计;难溶电解质的溶解平衡及沉淀转化的本质;物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题是一道实验探究题,能较好的考查学生分析和解决问题的能力,注意实验方案的设计原理和步骤利用关系式计算,依据已有的知识结合物质间反应的实验现象进行物质成分的推断,是解答的关键,平时注意打好扎实的基础知识和灵活应用知识解决问题的能力培养,题目难度中等.1年前查看全部
- 6.检验淀粉所用的试剂是( ) A.酒精 B.碘液 C氯化钴纸 D.碳酸盐氢指示剂
6.检验淀粉所用的试剂是( ) A.酒精 B.碘液 C氯化钴纸 D.碳酸盐氢指示剂
5.以下哪些会使大气中二氧化碳含量增加?
(a)抽烟 (b)呼吸作用 (c)光合作用
A.(a)和(b)
B.(a)和(c)
C.(b)和(c)
D.全部都是
人类进行氧气和二氧化碳交换的场所是( )
A.肺泡 B.气管 C.鼻 D.口 yamiii1年前1
yamiii1年前1 -
 xia_0425 共回答了17个问题
xia_0425 共回答了17个问题 |采纳率82.4%检验淀粉所用的试剂是B.碘液 会变蓝
以下哪些会使大气中二氧化碳含量增加 A.(a)和(b)
人类进行氧气和二氧化碳交换的场所是( ) A.肺泡1年前查看全部
- 氯化钴溶于少量水可否得到蓝色溶液?已知配离子CoCl4-为蓝色
 我心里很痛1年前2
我心里很痛1年前2 -
 leonado1985 共回答了18个问题
leonado1985 共回答了18个问题 |采纳率83.3%后面的已知条件为干扰项
氯化钴溶于水后,氯离子的数量不会发生改变,不足以四配位
所以在水中,钴离子以水合离子的形式存在,应该是粉红色的1年前查看全部
- 检验水的存在可用无水的硫酸铜或无水的氯化钴,如果无水的硫酸铜变( )色,或无水的氯化钴变( )色,说明有水存在
 b0w431年前1
b0w431年前1 -
 飞龙去 共回答了22个问题
飞龙去 共回答了22个问题 |采纳率90.9%蓝色;粉红色1年前查看全部
- 氯化钴遇水变成什么色
 酷酷的石头1年前3
酷酷的石头1年前3 -
 niuyunian 共回答了23个问题
niuyunian 共回答了23个问题 |采纳率82.6%无水氯化钴 呈蓝色 遇水 变成 水合氯化钴 呈红色
CoCl2+6H2O------→CoCl2·6H2O1年前查看全部
- 谁知道,氯化钴怎么制的,还有醋酸铀酰锌是干什么的,鉴定钾还是和钾反应生成沉淀啊?
谁知道,氯化钴怎么制的,还有醋酸铀酰锌是干什么的,鉴定钾还是和钾反应生成沉淀啊?
大家看到速回 嫣语林终1年前1
嫣语林终1年前1 -
 京城大少爷07 共回答了15个问题
京城大少爷07 共回答了15个问题 |采纳率86.7%1、氯化钴由氧化钴与盐酸作用而制得.
2、乙酸铀酰锌,化学式ZnUO2(CH3COO)4),俗称醋酸铀酰锌,是铀酰离子与锌生成的复盐.有放射性.用作钠离子的鉴定试剂.Na+ 在中性或弱酸性溶液中与乙酸铀酰锌生成柠檬黄色结晶性沉淀.1年前查看全部
- 不稀释情况下无水氯化钴蓝色溶液怎样转化六水氯化钴红色溶液
 xceel1akr1年前3
xceel1akr1年前3 -
 yghw527 共回答了13个问题
yghw527 共回答了13个问题 |采纳率100%一、试剂和溶液
分析方法中,除特殊规定外,只使用分析纯试剂和蒸馏水.
盐酸(GB 622);
硫酸(GB 625);
重铬酸钾(GB 642);
丙酮(GB 686).
稀盐酸溶液:用1份体积的盐酸与17份体积的蒸馏水混合配制.
氯化钴溶液:用1份质量的氯化钴与3份质量的稀盐酸溶液配制.
三氯化铁溶液:用5份质量的三氯化铁与1.2份质量的稀盐酸溶液配制.
氯铂酸钾溶液:在50mL的烧杯中称取790mg的氯铂酸钾,准确至0.1mg,用稀盐酸溶液溶解.溶解时,可略加热,直至所有的氯铂酸钾全部溶解.冷却至室温后,全部倒入100mL的容量瓶中,用稀盐酸溶液稀释至刻度,混匀.
二、仪器
钠氏比色管:25mL,管外径20mm;
分析天平:感量0.1mg;
架盘天平:感量0.1mg;
容量瓶:25mL、100mL;
移液管:0.1mL、1mL、10mL、50mL.
三、加德纳色标溶液的配制
8号色标的配制.用移液管将氯铂酸钾溶液按下表所示量分别移到8个25mL容量瓶中,用稀盐酸溶液将其稀释至刻度.所配制的溶液为加德纳色标1~8号.
18号色标的配制.用移液管将氯化钴溶液和三氯化铁溶液按表2所示量移到10个100mL的容量瓶中,用稀盐酸溶液将其稀释至刻度.所配制的溶液为加德纳色标9~18号.
色标的存放.配成的加德纳色标应存放在暗处,每半年至少用参比溶液校核一次.
四、试样
将4份质量的环氧树脂溶解于6份质量的丙酮.
五、操作步骤
将试样倒入干净的比色管中,然后把装有试样的比色管与装有加德纳色标溶液的比色管并列放置,在白天的散射光下,从侧面目测,比较颜色.
注:白天散射光,是指日出后到日落前3h,从无日光直接照射的朝北窗户进来的光.
六、结果表示
以与试样溶液颜色相同或最接近的色标号码表示试样的颜色.在需要更精确的表示时,则应说明与其相近的程度.例如,颜色在5和6之间时,则可表示为5、5+、6-和6几档.1年前查看全部
- 药典中比色用氯化钴配制时,加适量盐酸(1-40)使溶解成500ml,适量是多少呢?最后用乙二胺四醋酸二钠滴定
药典中比色用氯化钴配制时,加适量盐酸(1-40)使溶解成500ml,适量是多少呢?最后用乙二胺四醋酸二钠滴定
完了以后还要加适量盐酸调节含量至每1ml含59.5mg氯化钴,这个适量又是多少呢? 陕北小波1年前3
陕北小波1年前3 -
 sun_frog 共回答了22个问题
sun_frog 共回答了22个问题 |采纳率95.5%本身氯化钴有一定体积,把它装进量杯里,再先加总体积少于500毫升的盐酸(1-40),溶解,最后加盐酸混匀后体积为500ml就可以了,应该是就是这样1年前查看全部
- 无水氯化钴配制氯化钴溶液2.配制方法3.配制时需要什么防护措施?4.我在实验室什么防护措施也没有直接用药匙取出直接放入水
无水氯化钴配制氯化钴溶液
2.配制方法
3.配制时需要什么防护措施?
4.我在实验室什么防护措施也没有直接用药匙取出直接放入水中行吗?会有什么后果?
请分条回答,感激不尽.
化学式是CoCl2对吗? masonlc1年前1
masonlc1年前1 -
 无处发泄 共回答了11个问题
无处发泄 共回答了11个问题 |采纳率90.9%是CoCl2.市售氯化钴试剂通常都是水合的,氯化钴溶于水没有任何剧烈的放热过程,也没有强烈的腐蚀作用,按照正常的普通试剂配制方法就行.1年前查看全部
- 两道初中生物题目.1、为研究植物的蒸腾作用 小明选取了一片生长旺盛的蚕豆也 用滤纸把上下表面的水分吸干.将两张浸有氯化钴
两道初中生物题目.
1、为研究植物的蒸腾作用 小明选取了一片生长旺盛的蚕豆也 用滤纸把上下表面的水分吸干.将两张浸有氯化钴溶液的蓝色滤纸相对地贴在叶片的上下表面,并用回形针固定.一段时间后,观察到两张蓝色滤纸先后变成了——.首先出现颜色变化的是覆盖在——表皮的滤纸,这说明——.
2、在一洁净的玻璃板左右两侧,分别滴有少许土壤浸出液和等量蒸馏水,将玻璃板放在火焰上加热,待土壤浸出液和蒸馏水完全蒸发后,观察发生的现象:
①土壤浸出液:——,实验说明里面确有——;
②蒸馏水——. wzp20001年前2
wzp20001年前2 -
 零度风险 共回答了23个问题
零度风险 共回答了23个问题 |采纳率82.6%1.红色(氯化钴不含结晶水呈蓝色,含结晶水呈红色.因此水汽会使滤纸成蓝色)
下表面(叶片的蒸腾作用方式有两种,一是通过角质层的蒸腾,称为角质蒸腾(cuticular transpiration);二是通过气孔的蒸腾,称为气孔蒸腾(stomatal transpiration).而气孔蒸腾是中生和旱生植物(如蚕豆)蒸腾作用的主要方式,气孔位于下表面.这些知识了解就好,初中不做要求)
说明蒸腾作用的水汽是从叶的上下表面散发出来的,而且下表面散发的水分多于上表面散发的水分
2.有少许的白色颗粒晶体产生 无机盐
无明显现象(大概吧,水蒸干了还有什么?)1年前查看全部
- 氯化钴溶液中存在下列平衡:CoCl42-(蓝色)⇌Co2+(粉红色)+4Cl-,向氯化钴稀溶液中加入一定量的浓盐酸,溶液
氯化钴溶液中存在下列平衡:CoCl42-(蓝色)⇌Co2+(粉红色)+4Cl-,向氯化钴稀溶液中加入一定量的浓盐酸,溶液的颜色变化是( )
A.由蓝色变为粉红色
B.红色加深
C.由粉红色变为蓝色
D.蓝色加深 阿牛_1251年前1
阿牛_1251年前1 -
 一梦浮生 共回答了24个问题
一梦浮生 共回答了24个问题 |采纳率95.8%解题思路:向氯化钴稀溶液中加入一定量的浓盐酸,增大Cl-浓度,平衡向逆反应方向移动.向氯化钴稀溶液中加入一定量的浓盐酸,增大Cl-浓度,平衡向逆反应方向移动,溶液的颜色变化是由粉红色变为蓝色,故选C;
点评:
本题考点: 化学平衡的影响因素.
考点点评: 本题考查平衡移动的问题,根据外界条件对可逆反应的影响来确定平衡移动方向,确定溶液颜色的变化.1年前查看全部
- 做叶上、下表皮向外散失水分的实验时,可观察到蓝色的氯化钴滤纸变( ) 色.其中先使蓝色氯化钴滤纸变红色的是固定在( )的
做叶上、下表皮向外散失水分的实验时,可观察到蓝色的氯化钴滤纸变( ) 色.其中先使蓝色氯化钴滤纸变红色的是固定在( )的氯化钴滤纸,此现象可以说明的事实是( ) .
 ay911年前1
ay911年前1 -
 看看就知道 共回答了21个问题
看看就知道 共回答了21个问题 |采纳率90.5%红
上表皮
叶片上表皮向外散失的水分比下表面多.1年前查看全部
- 氯化钴加水变色的原因?氯化钴加水变色由蓝变红的原因?Co(H2O)6^2+ + 2Cl^- = Co(H2O)4Cl2
氯化钴加水变色的原因?
氯化钴加水变色由蓝变红的原因?
Co(H2O)6^2+ + 2Cl^- = Co(H2O)4Cl2 + 2H2O
用化学平衡解释! fudingkun1年前2
fudingkun1年前2 -
 工作的狼 共回答了19个问题
工作的狼 共回答了19个问题 |采纳率94.7%[Co(H2O)6]2+为红色
[Co(H20)4Cl2]为蓝色
加水后[Co(H2O)6]2+,Cl-,[Co(H2O)4Cl2]的浓度均减小,但反应物相对减小得较多,所以平衡像逆反应方向移动
如果知道反应平衡常数的话可以利用平衡常数来计算
K=[Co(H2O)4Cl2]/{[Co(H2O)62+]*[Cl-]^2}
加水后[Co(H2O)6]2+,Cl-,[Co(H2O)4Cl2]的浓度均减小而且减小的比例相同
Q=[Co(H2O)4Cl2]/{[Co(H2O)62+]*[Cl-]^2}增大
Q>K
平衡向逆反应方向移动1年前查看全部
- 将镉(Cd)浸在氯化钴(CoCl2)溶液中,发生反应的离子方程式为:Co2+(aq)+Cd(s)=Co(s)+Cd2+(
 将镉(Cd)浸在氯化钴(CoCl2)溶液中,发生反应的离子方程式为:Co2+(aq)+Cd(s)=Co(s)+Cd2+(aq)(aq表示溶液),如将该反应设计为如右图的原电池,则下列说法一定错误的是( )
将镉(Cd)浸在氯化钴(CoCl2)溶液中,发生反应的离子方程式为:Co2+(aq)+Cd(s)=Co(s)+Cd2+(aq)(aq表示溶液),如将该反应设计为如右图的原电池,则下列说法一定错误的是( )
A.Cd作负极,Co作正极
B.原电池工作时,电子从负极沿导线流向正极
C.根据阴阳相吸原理,盐桥中的阳离子向负极(甲池)移 动
D.甲池中盛放的是CdCl2溶液,乙池中盛放的是CoCl2溶液 ipkd01c_pa511b1年前1
ipkd01c_pa511b1年前1 -
 仔仔妮 共回答了17个问题
仔仔妮 共回答了17个问题 |采纳率94.1%解题思路:A.失电子的金属作负极、发生还原反应的电极作正极;
B.放电时,电子从负极沿导线流向正极;
C.盐桥中阳离子向正极区域移动、阴离子向负极区域移动;
D.含有Cd2+的溶液为负极区域电解质溶液,含有Co2+的溶液为正极区域电解质溶液.A.反应Co2+(aq)+Cd(s)=Co(s)+Cd2+(aq)(aq表示溶液)中Co得电子发生还原反应,则Co作正极、Cd作负极,故A正确;
B.放电时,电子从负极Cd沿导线流向正极Co,故B正确;
C.盐桥中阳离子向正极极区域乙移动、阴离子向负极区域甲移动,故C错误;
D.甲中失电子发生氧化反应,电解质溶液为CdCl2溶液,乙池中盛放的是CoCl2溶液,故D正确;
故选C.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查了原电池原理,明确正负极上发生的电极反应及元素化合价变化是解本题关键,再结合离子移动方向来分析解答,离子移动方向的判断为易错点.1年前查看全部
- 人们常用氯化钴的颜色变化来检验水的存在,可表示为什么?
 登陆名己存在1年前1
登陆名己存在1年前1 -
 威廉zz 共回答了12个问题
威廉zz 共回答了12个问题 |采纳率100%CoCl2·6H2O = CoCl2 + 6H2O (加热)
蓝 粉红
此反应可以正向也可以逆向进行,当CoCl2 在未吸水之前,是粉红色,当吸水之后变成蓝色,这是因为钴易与水形成配合物,发生变化,如果写成配合物的反应,上式也可以用以下表示:
2[Co(H2O)6]Cl2 = Co[CoCl4] + 12H2O
粉红 蓝1年前查看全部
- 请问氯化钴先与过量的浓氨水至沉淀完全溶解,接着加入过30%过氧化氢,最后加6mol.L ̄’的盐酸的反应方程
 小溪的晴天1年前3
小溪的晴天1年前3 -
 北方来客 共回答了11个问题
北方来客 共回答了11个问题 |采纳率90.9%这不就是生成三氯化六氨合钴的反应嘛.
CoCl2 + 6NH3·H2O = [Co(NH3)6]Cl2 + 6H2O
2[Co(NH3)6]Cl2 + H2O2 + 2HCl = 2[Co(NH3)6]Cl3 + 2H2O1年前查看全部
- 水玻璃与硫酸铁,氯化钴,硫酸铝 硫酸铜晶粒反应 为什么会长花
 随便nwa1年前1
随便nwa1年前1 -
 贴身 共回答了14个问题
贴身 共回答了14个问题 |采纳率64.3%猜测:硅酸钠能够和弱酸反应,那么应该可以和强酸弱碱盐反应,生成不溶于水的硅酸,将各个有色物质隔开或者说一定的阻碍(铁离子,铝离子,铜离子什么的都是有颜色的,并且颜色各不相同)而且水玻璃加入盐之后不能晃动,也...1年前查看全部
- 检验水的存在在密封的袋装食品袋内,常用一小包干燥剂,一般是硅胶内加入少量的氯化钴,如果拆开后食品袋后发现硅胶全部变成红色
检验水的存在
在密封的袋装食品袋内,常用一小包干燥剂,一般是硅胶内加入少量的氯化钴,如果拆开后食品袋后发现硅胶全部变成红色,则说明:()
A、食品袋内有较多水分 B、食品袋内没有任何水分
C、食品一定变质无法使用 C、以上各种去情况都有可能
答案是? duchunlei1年前2
duchunlei1年前2 -
 1someday 共回答了16个问题
1someday 共回答了16个问题 |采纳率87.5%在化学工业(级别)中,用氯化亚钴试纸检验(空气中)水的存在.将此种试纸从干燥的瓶中取出(蓝色),放入被检空气中.如变为紫红即为有水. 无水1年前查看全部
- 氯化钴试纸遇可检验水的多少吗
 wangyuanbiao1年前1
wangyuanbiao1年前1 -
 王八易高手 共回答了20个问题
王八易高手 共回答了20个问题 |采纳率95%我觉得可以1年前查看全部
- 氢氧化钴[Co(OH)2]可作涂料和清漆的干燥剂,其制备方法是:把金属钴与稀盐酸反应制得氯化钴(CoCl2),再将氯化钴
氢氧化钴[Co(OH)2]可作涂料和清漆的干燥剂,其制备方法是:把金属钴与稀盐酸反应制得氯化钴(CoCl2),再将氯化钴溶液与氢氧化钠溶液反应制得氢氧化钴.
【查阅资料】氯化钴溶液是粉红色,氢氧化钴是难溶于水的粉红色固体.请回答:
(1)金属钴与稀盐酸反应的化学方程式为______.
(2)氯化钴溶液与氢氧化钠溶液反应的现象是______,化学方程式为______.
(3)下列说法正确的是______.
A.钴的金属活动性比铜的强
B.氢氧化钴可以干燥氯化氢气体
C.氯化钴溶液也能和石灰水反应. 股仕阿土1年前1
股仕阿土1年前1 -
 孤独的浮云 共回答了21个问题
孤独的浮云 共回答了21个问题 |采纳率100%解题思路:(1)根据钴和稀盐酸反应生成氯化钴和氢气书写;
(2)根据氯化钴和氢氧化钠反应生成氯化钠和氢氧化钴粉红色沉淀解答;
(3)A、根据钴能和稀盐酸反应放出氢气说明比铜活泼判断;B、氢气为中性气体,氢氧化钴可干燥氢气判断;C、氯化钴和氢氧化钙反应生成氯化钠和氢氧化钴粉红色沉淀判断.(1)钴和稀盐酸反应生成氯化钴和氢气;故答案:Co+2HCl=CoCl2+H2↑;(2)氯化钴和氢氧化钠反应生成氯化钠和氢氧化钴粉红色沉淀,故答案:有粉红色的沉淀生成;CoCl2+2NaOH=2NaCl+Co(OH)2↓;(3)A、钴能和稀盐...
点评:
本题考点: 碱的化学性质;金属的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题以信息题的形式考查了金属的性质和碱的性质,注重化学知识的综合应用.1年前查看全部
- (2010•上海)氯化钴(CoCl2)试纸常用来检验水是否存在,其中钴(Co)元素的化合价是( )
(2010•上海)氯化钴(CoCl2)试纸常用来检验水是否存在,其中钴(Co)元素的化合价是( )
A.+2
B.+1
C.-2
D.-1 rpcyfc5br70041年前1
rpcyfc5br70041年前1 -
 恋上水的鱼儿 共回答了23个问题
恋上水的鱼儿 共回答了23个问题 |采纳率95.7%解题思路:根据在化合物中正负化合价代数和为零进行解答本题.根据在化合物中正负化合价代数和为零,可知氯化钴中钴(Co)元素的化合价为:x+(-1)×2=0,则x=+2,
故选A.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题考查学生根据在化合物中正负化合价代数和为零进行计算化合物中指定元素的化合价的能力.1年前查看全部
- 有关钴和铁化合物的性质见下表: 化学式 溶度积(室温时)Ksp 沉淀完全时的pH 氯化钴晶体的性质 Co(OH) 2 5
有关钴和铁化合物的性质见下表:
用含钴废料(含少量铁)可制备氯化钴:Co+2HCl═CoCl 2 +H 2 ↑工艺流程如下:化学式 溶度积(室温时)Ksp 沉淀完全时的pH 氯化钴晶体的性质 Co(OH) 2 5.9×10 -15 9.4 CoCl 2 •6H 2 O呈红色,常温下稳定.110°C~120°C时脱水变成蓝色无水氯化钴 Fe(OH) 2 1.6×10 -14 9.6 Fe(OH) 3 1.0×10 -35 x 
试回答:
(1)“净化除铁”中,写出加入CoCO 3 (难溶)调pH时反应的离子方程式______
(2)滤液中(Fe 3+ )≤1.0×10 -5 mol/L时,可视为Fe 3+ 沉淀完全.试计算室温下,Fe(OH) 3 沉淀完全时,则x=______.
(3)②步中用CoCO 3 调pH略大于x的原因是______.
(4)滤液中所含溶质有______,______.
(5)为了防止CoCl 2 •6H 2 O脱水,“干燥”时宜采用的方法或操作是______,______. 82181513141年前1
82181513141年前1 -
 fenfen_1 共回答了20个问题
fenfen_1 共回答了20个问题 |采纳率90%(1))“净化除铁”中,加入CoCO 3 (难溶),CoCO 3 属于碳酸盐,可与酸反应,CoCO 3 +2H + =Co 2+ +H 2 O+CO 2 ↑,通过此反应降低溶液的酸性,调溶液的pH,
故答案为:CoCO 3 +2H + =Co 2+ +H 2 O+CO 2 ↑;
(2)滤液中(Fe 3+ )≤1.0×10 -5 mol/L时,可视为Fe 3+ 沉淀完全,K sp [Fe(OH) 3 ]=1.0×10 -35 =c(Fe 3+ )×c 3 (OH - )=1.0×10 -5 mol•L -1 ×c 3 (OH - ),所以c(OH - )=10 -10 mol•L -1 ,c(H + )=
10-14
10-10 mol•L -1 =10 -4 mol•L -1 ,PH=-lgc(H + )=-lg10 -4 =4;
故答案为:4;
(3)根据(2)分析可知,为了使Fe 3+ 完全沉淀,pH应略大于4,故答案为:使Fe 3+ 完全沉淀;
(4)除去Fe 3+ ,滤液中主要含有NaCl、CoCl 2 、以及极少量的HCl,故答案为:CoCl 2 ;NaCl;
(5)因CoCl 2 •6H 2 O在110°C~120°C时脱水变成蓝色无水氯化钴,所以不能用高温烘干,为了防止CoCl 2 •6H 2 O脱水,“干燥”时宜采用的方法或操作是减压或温度低于110℃或在HCl气流中加热,故答案为:减压或温度低于110℃;或在HCl气流中加热.1年前查看全部
- 氯化钴加几滴溴水再加氢氧化钠,现象?反应方程式?
 abc123441年前1
abc123441年前1 -
 武东华 共回答了14个问题
武东华 共回答了14个问题 |采纳率92.9%CoCl2 + 2NaOH = 2NaCl + Co(OH)2(粉色或蓝色沉淀)
2Co(OH)2 + Br2 + 2NaOH = 2NaBr + 2Co(OH)3(黑色沉淀)
现象就是看到粉色或蓝色沉淀生成并迅速变黑1年前查看全部
- (4分)氢氧化钴[Co(OH) 2 ] 可作涂料和清漆的干燥剂,其制备方法是:把金属钴与稀盐酸反应制得氯化钴(CoCl
(4分)氢氧化钴[Co(OH) 2 ] 可作涂料和清漆的干燥剂,其制备方法是:把金属钴与稀盐酸反应制得氯化钴(CoCl 2 ),再将氯化钴溶液与氢氧化钠溶液反应制得氢氧化钴。
查阅资料:氯化钴溶液是粉红色,氢氧化钴是难溶于水的粉红色固体。请回答:
(1)金属钴与稀盐酸反应的化学方程式为 。
(2)氯化钴溶液与氢氧化钠溶液反应的现象是 ,化学方程式为 。
(3)下列说法正确的是 。
A.钴的金属活动性比铜的强
B.氢氧化钴可以干燥氯化氢气体
C.氯化钴溶液也能和石灰水反应 sohocheboy1年前1
sohocheboy1年前1 -
 qiuyifan1985 共回答了13个问题
qiuyifan1985 共回答了13个问题 |采纳率84.6%1)Co + 2HCl = CoCl 2 + H 2 ↑(2)产生粉红色沉淀,溶液逐渐由粉红色变无色 CoCl 2 +2NaOH ="==Co" (OH) 2 ↓+2NaCl(3)A C
1年前查看全部
- 有关钴和铁化合物的性质见下表: 化学式 溶度积(室温时)Ksp 沉淀完全时的pH 氯化钴晶体的性质 Co(OH) 2 5
有关钴和铁化合物的性质见下表:
化学式 溶度积(室温时)Ksp 沉淀完全时的pH 氯化钴晶体的性质 Co(OH) 2 5.9×10 -15 9.4 CoCl 2 ·6H 2 O呈红色,常温下稳定。110ºC~120ºC时脱水变成蓝色无水氯化钴 Fe(OH) 2 1.6×10 -14 9.6 Fe(OH) 3 1.0×10 -35 x
用含钴废料(含少量铁)可制备氯化钴:Co+2HCl=CoCl 2 +H 2 ↑工艺流程如下:
试回答:
(1)“净化除铁”中,写出加入CoCO 3 (难溶)调pH时反应的离子方程式
(2)滤液中(Fe 3+ )≤1.0×10 -5 mol/L时,可视为Fe 3+ 沉淀完全。试计算室温下,Fe(OH) 3 沉淀完全时,则x= 。
(3)②步中用CoCO 3 调pH略大于x的原因是 。
(4)滤液中所含溶质有 , 。
(5)为了防止CoCl 2 ·6H 2 O脱水,“干燥”时宜采用的方法或操作是 , 。 ieytytyy1年前1
ieytytyy1年前1 -
 280275149 共回答了20个问题
280275149 共回答了20个问题 |采纳率90%(1)CoCO 3 +2H + =Co 2+ +H 2 O+CO 2 ↑
(2)4
(3)使Fe 3+ 完全沉淀
(4)CoCl 2
(5)减压或温度低于110℃或在HCl气流中加热(任写2点)
1年前查看全部
- 氯化钴的溶解度曲线谁有氯化钴在水中的溶解度曲线图,
 waitwait1年前1
waitwait1年前1 -
 可以是小虫 共回答了14个问题
可以是小虫 共回答了14个问题 |采纳率85.7%物质 化学式 0°C 10°C 20°C 30°C 40°C 50°C 60°C 70°C 80°C 90°C 100°C
氯化钴 CoCl2 43.5 47.7 52.9 59.7 69.5 93.8 97.6 101 106 (g/cm2)
写入excel,插入图表,就画除曲线了1年前查看全部
- 硅胶干燥剂里面的氯化钴吸水变色应该是什么色?
硅胶干燥剂里面的氯化钴吸水变色应该是什么色?
粉红色还是蓝色?老师说是粉红色,那么有没有蓝色?分别是什么意义? 幽幽神谷1年前1
幽幽神谷1年前1 -
 zdqzdqzdq 共回答了12个问题
zdqzdqzdq 共回答了12个问题 |采纳率91.7%硅胶干燥剂中的氯化钴变色基本原理为:
CoCl2 + 6H2O = CoCl2·6H2O
(蓝色) (粉红色)
无水二氯化钴是蓝色的,当吸收了水分后变为粉红色.这个反应是可逆的,加热情况下,反应逆向进行,所以干燥剂可以再生,而重复使用.1年前查看全部
- 请问氯化钴晶体因水份而变色,那这个变色反应速度可否加什么化工原料使它比正常变色更快或更慢-甚至不...
请问氯化钴晶体因水份而变色,那这个变色反应速度可否加什么化工原料使它比正常变色更快或更慢-甚至不...
请问氯化钴晶体因水份而变色,那这个变色反应速度可否加什么化工原料使它比正常变色更快或更慢-甚至不变色!急 丁东19801年前1
丁东19801年前1 -
 8wy161794 共回答了21个问题
8wy161794 共回答了21个问题 |采纳率85.7%加点具有络合能力的阴离子,如氯化钠等 或升温降温都会使变色速率变化1年前查看全部
- 干燥的氯化钴试纸用来检验什么
 冷啸臣1年前1
冷啸臣1年前1 -
 喔唷周导 共回答了19个问题
喔唷周导 共回答了19个问题 |采纳率78.9%无水氯化亚钴试纸在实验室中常用来检验水分子的存在,这是因为氯化亚钴遇水会发生水合反应,生成六水氯化亚钴.氯化亚钴是蓝色的,而六水氯化钴是粉色的,因而有此效果.
六水氯化亚钴加热后可变为无水氯化亚钴,因而使用后的试纸经加热后可以重复使用.1年前查看全部
- 硫酸铜和氯化钴试纸测试水有什么区别
硫酸铜和氯化钴试纸测试水有什么区别
如果测试固体是否含有水该用哪一个 lancepiero1年前1
lancepiero1年前1 -
 丁布布 共回答了20个问题
丁布布 共回答了20个问题 |采纳率95%用硫酸铜比较灵敏1年前查看全部
- 如何把六水合氯化钴变成无水氯化钴
 小跃1年前2
小跃1年前2 -
 qbelmt 共回答了12个问题
qbelmt 共回答了12个问题 |采纳率91.7%要在氯化氢气体中加热,在空气中加热会使六水合氯化钴水解成氢氧化钴.1年前查看全部
- 氯化钴和水合氯化钴的分子式怎么写?最快者赏!
 紫丁香3161年前3
紫丁香3161年前3 -
 痛彻心扉的伤 共回答了18个问题
痛彻心扉的伤 共回答了18个问题 |采纳率94.4%分子式有好几种呢
氯化钴结晶体,在常温下是CoCl2.6H2O,呈粉红色;加热至52℃以上失水,就成为紫红色的CoCl2·2H2O.继续加热到90℃,变为蓝紫色的CoCl2·H2O,再加热会全部失水,而成为蓝色的CoCl21年前查看全部
- 氯化钴试纸遇到水会变色吗,从神马颜色变到神马颜色
 poponing5201年前2
poponing5201年前2 -
 twelve1gg 共回答了16个问题
twelve1gg 共回答了16个问题 |采纳率87.5%会的.氯化钴遇水变粉色.1年前查看全部
- 氯化钴与氢氧化钠反应方程式,(反应现象先出现蓝色,静置片刻后出现粉红色沉淀),急!
 30238261年前1
30238261年前1 -
 linwiser 共回答了23个问题
linwiser 共回答了23个问题 |采纳率95.7%CoCl2 + NaOH = Co(OH)Cl↓(蓝色沉淀) + NaCl
CoCl2+2NaOH=Co(OH)2↓(粉红色沉淀)+2NaCl1年前查看全部
- 人们常用氯化钴颜色变化来检验水的存在,变化的的文字表达式
 紫竹23421年前1
紫竹23421年前1 -
 乌痣痱 共回答了24个问题
乌痣痱 共回答了24个问题 |采纳率70.8%无水氯化钴是蓝色的
吸收了水分变成含结晶水的氯化钴(CoCl2·6H2O)时却是粉红色的
氯化钴+水→六水合氯化钴1年前查看全部
- 钴于硫酸反应的现象是什么(Co+H2SO4=COSO4+H2↑)还有将沾了粉红色的氯化钴的干燥滤纸加热滤纸变蓝的化学
钴于硫酸反应的现象是什么(Co+H2SO4=COSO4+H2↑)还有将沾了粉红色的氯化钴的干燥滤纸加热滤纸变蓝的化学
方程式是什么?(Cocl2固体是蓝色的,Cocl2·6H2o和Cocl2溶液是粉红色的) crzgl1年前2
crzgl1年前2 -
 lawyeryong 共回答了19个问题
lawyeryong 共回答了19个问题 |采纳率84.2%现象:生成气体,溶液变为粉红色(二价钴)
方程式:CoCl2.6H2O=加热=CoCl2+6H2O1年前查看全部
- 为什么氯化钴那么贵?100g70元,把金属钴放进氯化铜里不就可以得到吗?
 欧阳逸1年前1
欧阳逸1年前1 -
 myraleaf 共回答了13个问题
myraleaf 共回答了13个问题 |采纳率92.3%你的补充问题很有意思啊!其实金属钴比氯化钴更贵!
工业上是采用氧化钴与盐酸反应制得的!自然界得到氧化钴相对还是方便的,倘若采用金属钴来制备,恐怕100克卖70元,试剂商要赔干了啊!
CoO+2HCl=CoCl2+H2O1年前查看全部
- 无水氯化钴加水 什麽颜色变成什麽颜色?
 acof1年前2
acof1年前2 -
 天地合一023 共回答了19个问题
天地合一023 共回答了19个问题 |采纳率89.5%氯化钴只含有两个结晶水(CoCl2·2H2O),颜色是蓝色的,加湿后变成含有6个结晶水(COCl2·6H2O),颜色变成了粉红色1年前查看全部
- 氯化钴与氢氧化钠咋反应啊?求反应现象与方程式
 单眼皮女生1976661年前1
单眼皮女生1976661年前1 -
 乖乖53000 共回答了17个问题
乖乖53000 共回答了17个问题 |采纳率76.5%钴的化学性质与铁很相似,氯化钴Cocl2易吸收水分,由于吸收水分的不同,而呈现出不同的颜色,变色硅胶中就是利用这个性质.
CoCl2 + NaOH = Co(OH)Cl(蓝色沉淀) + NaCl1年前查看全部
- 氯化钴溶液中存在下列平衡:CoCl 4 2- (蓝色) Co 2+ (粉红色)+4Cl - ,向氯化钴稀溶液中加入一定量
氯化钴溶液中存在下列平衡:CoCl 4 2- (蓝色)
 Co 2+ (粉红色)+4Cl - ,向氯化钴稀溶液中加入一定量的浓盐酸,溶液的颜色变化是
Co 2+ (粉红色)+4Cl - ,向氯化钴稀溶液中加入一定量的浓盐酸,溶液的颜色变化是A.由蓝色变为粉红色 B.红色加深 C.由粉红色变为蓝色 D.蓝色加深  拣破烂到天堂1年前1
拣破烂到天堂1年前1 -
 鸟枪打野鸟 共回答了24个问题
鸟枪打野鸟 共回答了24个问题 |采纳率91.7%C
1年前查看全部
- 无水硫酸铜和无水氯化钴那种是用来检验含水量大小的物质是什么,为什么
 mantise1年前1
mantise1年前1 -
 1f_1 共回答了25个问题
1f_1 共回答了25个问题 |采纳率88%是无水CuSO4,CuSO4的水合物只有一种形式 CuSO4.5H2O
而CoCl2的水合物形式多种,CoCl2有时呈紫色,蓝紫色,蓝色等都是由其结晶水决定的!1年前查看全部
- 氯化钴与无水亚硫酸钠一起溶解,氧化钴会不会影响到无水亚硫酸钠的溶解度?有多大影响?
 xjktwxl1年前2
xjktwxl1年前2 -
 张春磊 共回答了20个问题
张春磊 共回答了20个问题 |采纳率90%氯化钴与无水亚硫酸钠一起溶解,是会发生反应的:
CoCI2 + Na2SO3===CoSO3[沉淀] + 2NaCI
生成难溶的亚硫酸钴沉淀,呈粉红色,亚硫酸盐除了铵及碱金属盐外其他的均难溶
因此不仅影响,而且使得药品性质发生改变1年前查看全部
- 已知氯化钴和盐酸的混合溶液呈紫色,存在如下平衡:Co(H2O)62+(粉红色)+4Cl-⇌CoCl42-(蓝色)+6H2
已知氯化钴和盐酸的混合溶液呈紫色,存在如下平衡:Co(H2O)62+(粉红色)+4Cl-⇌CoCl42-(蓝色)+6H2O△H>0,若使溶液呈粉红色,下列措施可行的是( )
A.升温
B.加压
C.加水稀释
D.滴加浓盐酸 RoyaLNavyclx1年前1
RoyaLNavyclx1年前1 -
 yybraveheart 共回答了14个问题
yybraveheart 共回答了14个问题 |采纳率92.9%解题思路:A.升温平衡正移;
B.反应物与生成物中没有气体,改变压强无影响;
C.加水逆向移动;
D.加盐酸平衡正移.A.已知该反应为吸热反应,升温平衡正移,使溶液呈蓝色,故A错误;
B.反应物与生成物中没有气体,改变压强无影响,溶液的颜色不变,故B错误;
C.已知Co(H2O)62+(粉红色)+4Cl-⇌CoCl42-(蓝色)+6H2O△H>0,加水逆向移动,则溶液变为粉红色,故C正确;
D.已知Co(H2O)62+(粉红色)+4Cl-⇌CoCl42-(蓝色)+6H2O△H>0,加盐酸平衡正移,则溶液变为蓝色,故D错误.
故选 C.点评:
本题考点: 影响盐类水解程度的主要因素.
考点点评: 本题考查平衡移动的问题,根据外界条件对可逆反应的影响来确定平衡移动方向,确定溶液颜色的变化,题目难度不大.1年前查看全部
- 请问氯化钴是否具有放射性?实验可能会用到氯化钴请问是否具有放射性啊?
 恨天低V青岛1年前1
恨天低V青岛1年前1 -
 shenlvyouling 共回答了21个问题
shenlvyouling 共回答了21个问题 |采纳率81%钴60这种同位素才有放射性,它是通过核反应得到的,我们实验用的钴是不会有放射性的.1年前查看全部
大家在问
- 1有5元和10元的人民币43张共340元,5元币和10元币各有多少张?
- 2数至八层,裁如星点是什么修辞手法
- 3有关词语的,像“悬挂,寒冷” 一样,两个字为近义词的,要十个,
- 4已知P(-2,m)Q(n,-3)关于y轴对称,求m+n..三克油喽~
- 5谁能帮我理下染色质 、染色体、染色单体 的关联和区别还有染色体、DNA、基因的关系小女子感激不尽!
- 6大江保卫战 第5小节中 运用的修辞手法有什么
- 7有外星人存在吗?为什么?用英文回答
- 8在公差为正数的等差数列{an}中,a10+a11<0,且a10a11<0,Sn是其前n项和,则使Sn取最小值的n是___
- 9(请先画一个四边形,(似梯形)把四边形的左上角设为A点,左下角设为B点,右上角设为D点,右下角设为C点,再连接DB与AC
- 10函数y=cos²x+sinx的最大值?
- 11下列数字有何规律6,8,12,18,26,36请用一个代数式来表示以上规律
- 12在五个2之间添加什么运算符号可以使它等于零
- 13绞丝旁读什么
- 14绞丝旁加并念什么
- 15氧化铜和浓硝酸反应方程式
