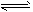氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料.下列有关57号元素镧(La)的说法正确的是______
 姜秋米2022-10-04 11:39:541条回答
姜秋米2022-10-04 11:39:541条回答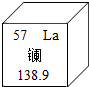 氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料.下列有关57号元素镧(La)的说法正确的是______
氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料.下列有关57号元素镧(La)的说法正确的是______A.该元素原子的质子数为57
B.该元素为非金属元素
C.该元素的相对原子质量为138.9 g
D.______.

已提交,审核后显示!提交回复
共1条回复
 爱家新主张 共回答了14个问题
爱家新主张 共回答了14个问题 |采纳率92.9%- 解题思路:根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可.
A、根据元素周期表中的一格中获取的信息,该元素的原子序数为57;根据原子序数=核电荷数=质子数,则该元素原子的质子数为57,故选项说法正确.
B、根据元素周期表中的一格中获取的信息,该元素的原子序数为24,故选项说法错误.
C、根据元素周期表中的一格中获取的信息,可知该元素的相对原子质量为138.9,相对原子质量单位是“1”,不是“克”,故选项说法错误.
D、根据元素周期表中的一格中获取的信息,该元素的原子序数为57,相对原子质量为138.9等(合理即可).
故答案为:A;该元素的原子序数为57等.点评:
本题考点: 元素周期表的特点及其应用.
考点点评: 本题难度不大,考查学生灵活运用元素周期表中元素的信息及辨别元素种类的方法进行分析解题的能力. - 1年前
相关推荐
- 氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料,镧和镍两种元素原子的本质区别是( )
氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料,镧和镍两种元素原子的本质区别是( )
A.最外层电子数不同
B.中子数不同
C.电子数不同
D.质子数不同 majun191年前1
majun191年前1 -
 o2fc 共回答了12个问题
o2fc 共回答了12个问题 |采纳率100%解题思路:根据元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),据此进行分析解答.元素是质子数(即核电荷数)相同的一类原子的总称,不同种元素最本质的区别是质子数(即核电荷数)不同,所以镧和镍两种元素原子的本质区别是质子数(即核电荷数)不同.
A、决定元素的种类的是质子数(即核电荷数),不是最外层电子数不同,故选项错误.
B、决定元素的种类的是质子数(即核电荷数),不是中子数不同,故选项错误.
C、决定元素的种类的是质子数(即核电荷数),不是电子数不同,故选项错误.
D、决定元素的种类的是质子数(即核电荷数),故选项正确.
故选D.点评:
本题考点: 元素的概念.
考点点评: 本题很简单,考查学生对元素的概念的理解和不同种元素之间的本质区别是质子数不同进行解题的能力.1年前查看全部
- (2013•江西三模)氢是新型清洁能源,但难储运.研究发现,合金可用来储藏氢气.镧( 13957La)和镍(&
(2013•江西三模)氢是新型清洁能源,但难储运.研究发现,合金可用来储藏氢气.镧(
La)和镍(13957
Ni)的一种合金就是储氢材料.该合金的晶胞如图1,镍原子除一个在中心外,其他都在面上,镧原子在顶点上.储氢时氢原子存在于金属原子之间的空隙中.5928
(1)一定条件下,该储氢材料能快速、可逆地存储和释放氢气,若每个晶胞可吸收3个H2,这一过程可用化学方程式表示为:______.
(2)下列关于该储氢材料及氢气的说法中,正确的是______(填序号)
A、该材料中镧原子和镍原子之间存在化学键,是原子晶体
B、氢分子被吸收时首先要在合金表面解离变成氢原子,同时放出热量
C、该材料贮氢时采用常温高压比采用常温常压更好
D、氢气很难液化是因为虽然其分子内氢键作用很强,但其分子间作用力很弱
E、已知镧和镍的第一电离能分别为5.58eV、7.64ev,可见气态镧原子比气态镍原子更容易变成+1价的气态阳离子
(3)某研究性小组查阅的有关镍及其化合物的性质资料如下:
Ⅰ、镍常见化合价为+2、+3价,在水溶液中通常只以+2价离子的形式存在.+3价的镍离子具有很强的氧化性,在水中会与水或酸根离子迅速发生氧化还原反应.
Ⅱ、在Ni2+的溶液中加入强碱时,会生成Ni(OH)2沉淀,在强碱性条件下,该沉淀可以被较强的氧化剂(如NaClO)氧化为黑色的难溶性物质NiO(OH),
Ⅲ、镍易形成配合物,如:Ni(CO)6、(Ni(NH3)6)2+等.
①写出Ni3+的核外电子排布式:______.
②写出将NiO(OH)溶于浓盐酸的化学方程式:______.
(4)Ni(CO)6为正八面体结构,镍原子位于正八面体的中心,配位体CO在正八面体的六个顶点上.若把其中两个CO配位体换成NH3得到新的配合物,则以下物质中互为同分异构体的是______.(填字母编号,任填一组)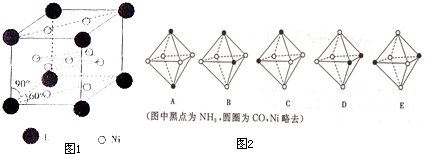
 yyl_sany1年前1
yyl_sany1年前1 -
 我的QQ121309354 共回答了13个问题
我的QQ121309354 共回答了13个问题 |采纳率100%解题思路:(1)利用均摊法确定该晶胞的化学式,再根据反应物、生成物书写方程式;
(2)A.该材料中构成微粒是金属阳离子和自由电子;
B.根据储氢原理为:镧镍合金吸附H2,H2解离为原子,H储存在其中形成LaNixH6判断;
C.根据压强对平衡移动影响分析;
D.氢气分子之间不存在氢键;
E.第一电离能越小越容易失去电子;
(3)①Ni是28号元素,其核外有28个电子,Ni3+核外25个电子,根据构造原理书写其价电子排布式;
②NiO(OH)和浓盐酸发生氧化还原反应生成氯气;
(4)同分异构体有:两个氨气分子位于平行四边形相邻、相对位置或八面体上下两个顶点上.(1)晶胞中去掉氢气分子为镧镍合金,由晶胞结构可知镧镍合金为LaNi5,能可逆地存储和释放氢气,每个晶胞可吸收3个H2,这一过程用化学方程式为:LaNi5+3H2⇌LaNi5H6,
故答案为:LaNi5+3H2⇌LaNi5H6;
(2)A.镧和镍都是金属,贮氢材料为金属晶体,故A错误;
B.根据储氢原理可知,镧镍合金先吸附H2,然后H2解离为原子,该过程用吸收热量,故B错误;
C.吸附氢气的过程为气体体积减小的反应,高压比采用常压更有利于氢气吸收,故C正确;
D.氢气分子之间不存在氢键,故D错误;
E.镧的第一电离能小于镍的第一电离能,说明气态镧原子比气态镍原子更容易变成+1价的气态阳离子,故E正确,
故选:CE;
(3)①Ni是28号元素,其核外有28个电子,Ni3+核外25个电子,根据构造原理知,该离子核外电子排布式为:[Ar]3d7或1s22s22p63s23p63d7,
故答案为:[Ar]3d7或1s22s22p63s23p63d7;
②NiO(OH)和浓盐酸发生氧化还原反应生成氯气、氯化镍和水,反应方程式为:2NiO(OH)+6HCl(浓)=2NiCl2+Cl2↑+4H2O,
故答案为:2NiO(OH)+6HCl(浓)=2NiCl2+Cl2↑+4H2O;
(4)同分异构体有:两个氨气分子位于平行四边形相邻、相对位置或八面体上下两个顶点上,所以有A和B(或A和C、A和D、B和E、C和E、D和E任一组均可),故答案为:A和B(或A和C、A和D、B和E、C和E、D和E任一组均可).点评:
本题考点: 晶胞的计算;原子核外电子排布;同分异构现象和同分异构体.
考点点评: 本题考查了物质结构和性质,涉及同分异构体的判断、核外电子排布式的书写、第一电离能等知识点,根据结构、电子排布式的书写规则、第一电离能的变化规律来分析解答,易错题是(4),会根据图象判断同分异构体,题目难度中等.1年前查看全部
- 氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料.下列有关57号元素镧(La)的说法不正确的是( )
氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料.下列有关57号元素镧(La)的说法不正确的是( )
A.该元素原于的质子数为57
B.该元素原子的核电荷数为57
C.该元素原于的核外电子数为57
D.该元素为非金属元素 2002年3月8日1年前1
2002年3月8日1年前1 -
 wzh1 共回答了18个问题
wzh1 共回答了18个问题 |采纳率72.2%A、该元素原子的质子数等于原子序数,故为57,此项正确.
B、核电荷数等于原子序数,此项正确.
C、在原子中,核外电子数等于原子序数,此项正确.
D、该元素名称为镧,故为金属元素,此项错误.
故选D1年前查看全部
- 氢是新型清洁能源,但难储运.研究发现,镧(La)和镍(Ni)的一种合金是储氢材料.右图是镍元素在周期表中的信息,下列说法
 氢是新型清洁能源,但难储运.研究发现,镧(La)和镍(Ni)的一种合金是储氢材料.右图是镍元素在周期表中的信息,下列说法不正确的是( )
氢是新型清洁能源,但难储运.研究发现,镧(La)和镍(Ni)的一种合金是储氢材料.右图是镍元素在周期表中的信息,下列说法不正确的是( )
A.该元素原子的核电荷数为28
B.该元素原子的质子数为28
C.该元素原子的核外电子数为28
D.该元素原子的中子数为28 xukai871年前1
xukai871年前1 -
 名字是随便取的 共回答了20个问题
名字是随便取的 共回答了20个问题 |采纳率95%解题思路:由上图28号元素镍,可知的信息:该元素的元素符号、相对原子质量、质子数等,然后根据核内质子数=核电荷数=核外电子数可以推出该元素原子电子数.A、上图28号元素镍,可知:镍原子的核电荷数为28,故A正确;
B、上图28号元素镍,可知:镍原子的质子数为28,故B正确;
C、上图28号元素镍,可知:镍原子的核外电子数为28,故C正确;
D、由相对原子质量=质子数+中子数,可知原子的中子数为31而不是28,故D错误.
故选:D.点评:
本题考点: 元素周期表的特点及其应用.
考点点评: 了解元素周期表的特点及其应用,属于基础知识的考查.1年前查看全部
- (2008•深圳一模)氢是新型清洁能源,但难储运.研究发现,合金可用来储藏氢气.镧( 13957La)
(2008•深圳一模)氢是新型清洁能源,但难储运.研究发现,合金可用来储藏氢气.镧(
La) 和镍(13957
Ni) 的一种合金就是储氢材料.该合金的晶胞如图1所示,镍原子除一个在中心外,其他都在面上,镧原子在顶点上.储氢时氢原子存在于金属原子之间的空隙中.5928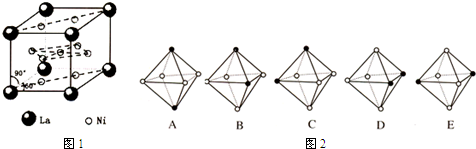
(1)一定条件下,该贮氢材料能快速、可逆地存储和释放氢气,若每个晶胞可吸收 3 个 H2,这一过程用化学方程式表示为:______.
(2)下列关于该贮氢材料及氢气的说法中,正确的是______( 填序号 )
A.该材料中镧原子和镍原子之间存在化学键,是原子晶体
B.氢分子被吸收时首先要在合金表面解离变成氢原子,同时放出热量
C.该材料贮氢时采用常温高压比采用常温常压更好
D.氢气很难液化是因为虽然其分子内氢键很强,但其分子间作用力很弱
E.己知镧和镍的第一电离能分别为 5.58eV、7.64eV,可见气态镧原子比气态镍原子更容易变成+1 价的气态阳离子
I、镍常见化合价为+2、+3,在水溶液中通常只以+2 价离子的形式存在.+3价的镍离子具有很强的氧化性,在水中会与水或酸根离子迅速发生氧化还原反应.
Ⅱ、在Ni2+的溶液中加入强碱时,会生成 Ni(OH)2沉淀,在强碱性条件下,该沉淀可以被较强的氧化剂 (如 NaClO) 氧化为黑色的难溶性物质 NiO(OH).
Ⅲ、镍易形成配合物如 Ni(CO)6、[Ni(NH3)6]2+等.
(3)某研究性学习小组查阅的有关镍及其化合物的性质资料如下:
①写出 Ni3+ 的核外电子排布式:______
②写出将NiO(OH)溶于浓盐酸的离子方程式:______
(4)Ni(CO)6为正八面体结构,镍原子位于正八面体的中心,配位体CO在正八面体的六个顶点上.若把其中两个CO配位体换成 NH3得到新的配合物,则以下物质中互为同分异构体的是图2中的______. ( 填字母编号,任填一组 )( 图中黑点为NH3,圆圈为CO,Ni略去) 迷途猫20071年前1
迷途猫20071年前1 -
 showhope 共回答了15个问题
showhope 共回答了15个问题 |采纳率100%解题思路:(1)利用均摊法确定该晶胞的化学式,再根据反应物、生成物书写方程式;
(2)A.该材料中构成微粒是金属阳离子和自由电子;
B.根据储氢原理为:镧镍合金吸附H2,H2解离为原子,H储存在其中形成LaNixH6判断;
C.根据压强对平衡移动影响分析;
D.氢气分子之间不存在氢键;
E.第一电离能越小越容易失去电子;
(3)①Ni是28号元素,其核外有28个电子,Ni3+核外25个电子,根据构造原理书写其价电子排布式;
②NiO(OH)和浓盐酸发生氧化还原反应生成氯气;
(4)同分异构体有:两个氨气分子位于平行四边形相邻、相对位置或八面体上下两个顶点上.(1)晶胞中去掉氢气分子为镧镍合金,由晶胞结构可知镧镍合金为LaNi5,能可逆地存储和释放氢气,每个晶胞可吸收3个H2,这一过程用化学方程式为:LaNi5+3H2⇌LaNi5H6,
故答案为:LaNi5+3H2⇌LaNi5H6;
(2)A.镧和镍都是金属,贮氢材料为金属晶体,故A错误;
B.根据储氢原理可知,镧镍合金先吸附H2,然后H2解离为原子,该过程用吸收热量,故B错误;
C.吸附氢气的过程为气体体积减小的反应,高压比采用常压更有利于氢气吸收,故C正确;
D.氢气分子之间不存在氢键,故D错误;
E.镧的第一电离能小于镍的第一电离能,说明气态镧原子比气态镍原子更容易变成+1价的气态阳离子,故E正确,
故选:CE;
(3)①Ni是28号元素,其核外有28个电子,Ni3+核外25个电子,根据构造原理知,该离子核外电子排布式为:[Ar]3d7或1s22s22p63s23p63d7,故答案为:[Ar]3d7或1s22s22p63s23p63d7;
②NiO(OH)和浓盐酸发生氧化还原反应生成氯气、氯化镍和水,反应方程式为:2NiO(OH)+6HCl(浓)=2NiCl2+Cl2↑+4H2O,故答案为:2NiO(OH)+6HCl(浓)=2NiCl2+Cl2↑+4H2O;
(4)同分异构体有:两个氨气分子位于平行四边形相邻、相对位置或八面体上下两个顶点上,所以有A和B(或A和C、A和D、B和E、C和E、D和E任一组均可),故答案为:A和B(或A和C、A和D、B和E、C和E、D和E任一组均可).点评:
本题考点: 晶胞的计算;原子核外电子排布;配合物的成键情况.
考点点评: 本题考查了物质结构和性质,涉及同分异构体的判断、核外电子排布式的书写、第一电离能等知识点,根据结构、电子排布式的书写规则、第一电离能的变化规律来分析解答,易错题是(4),会根据图象判断同分异构体,题目难度中等.1年前查看全部
- 氢是新型清洁能源,但难储运。研究发现,镧和镍的一种合金是储氢材料。下列有关57号元素镧(La)的说法不正确的是(
氢是新型清洁能源,但难储运。研究发现,镧和镍的一种合金是储氢材料。下列有关57号元素镧(La)的说法不正确的是()
A.该元素为非金属元素 B.该元素原子的核电荷数为57 C.该元素原子的核外电子数为57 D.该元素原子的质子数为57  黄洪源1年前1
黄洪源1年前1 -
 hafung 共回答了24个问题
hafung 共回答了24个问题 |采纳率75%A
1年前查看全部
- 氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料.下图中的符号表示2个氢原子的是( )
氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料.下图中的符号表示2个氢原子的是( )
A.
B.
C.
D.
 赤浮云1年前1
赤浮云1年前1 -
 项田园 共回答了17个问题
项田园 共回答了17个问题 |采纳率76.5%解题思路:化学符号周围数字表示的意义是不同的,我们学过的元素符号周围的数字共有四种,出现在四个部位:
①正上方:化合价写在元素符号正上方,表示该元素的化合价,如
表示镁元素化合价为+2价.+2 Mg
②右上角:元素符号右上角的数字表示离子所带电荷数,如Mg2+表示镁离子,“2+”表示镁离子带2个单位正电荷.
③右下角:元素符号右下角数字表示物质的一个分子里含该原子的个数(由分子构成的物质),如H2O中的“2”表示一个水分子含有两个氢原子.
④前面:元素符号(或化学式)前面的数字表示微粒的个数(分子、原子、离子),如3N2表示3个氮分子.A、表示氢气;表示氢气的元素为氢元素;表示由一个氢气分子;表示一个氢气分子由2个原子构成;故A错误;
B、图中表示2个氢气分子,故B错误;
C、图中表示2个氢原子,故C正确;
D、图中表示2个氢离子,故D错误.
故选:C.点评:
本题考点: 元素的符号及其意义.
考点点评: 元素的化合价与离子电荷数最易混淆,离子所带电荷数与该元素化合价在数值上一般相同,但书写上不同:化合价写在元素正上方,离子电荷数写在右上角;化合价符号在前,数字在后、离子电荷数数字在前、符号在后;电荷数为1时,“1”可省略,而化合价的数字1则不能省略.1年前查看全部
- (2008•南京)氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料.下列有关57号元素镧(La)的说法不
(2008•南京)氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料.下列有关57号元素镧(La)的说法不正确的是( )
A.该元素原于的质子数为57
B.该元素原子的核电荷数为57
C.该元素原于的核外电子数为57
D.该元素为非金属元素 boris_lll1年前1
boris_lll1年前1 -
 钟语 共回答了19个问题
钟语 共回答了19个问题 |采纳率89.5%解题思路:在原子中:原子序数=核电荷数=质子数=核外电子数,镧元素的元素名称中带金字旁,是金属元素.A、该元素原子的质子数=原子序数,故为57,此项正确;
B、核电荷数=原子序数,此项正确;
C、在原子中,核外电子数=原子序数,此项正确;
D、该元素名称为镧,故为金属元素,此项错误.
故选:D.点评:
本题考点: 原子的定义与构成;元素的简单分类.
考点点评: 在原子中,原子序数=核电荷数=质子数=核外电子数是一条很重要的规律.1年前查看全部
- (2009•平原县)氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料.下列有关57号元素镧(La)的说法
(2009•平原县)氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料.下列有关57号元素镧(La)的说法不正确的是( )
A.该元素为非金属元素
B.该元素原子的核电荷数为57
C.该元素原子的核外电子数为57
D.该元素原子的质子数为57 偶尔灰色1年前1
偶尔灰色1年前1 -
 jackxinqing 共回答了12个问题
jackxinqing 共回答了12个问题 |采纳率100%解题思路:由题意,57号元素镧(La),结合“原子序数=核内质子数=核外电子数=核电荷数”,则可知的信息为:元素分类、核电荷数、核内质子数、核外电子数等.A、由汉语名称“镧”,则知该元素为金属元素,故A错误;
B、由题意,57号元素镧(La),结合“原子序数=核电荷数”,知该元素原子的核电荷数为57,故B正确;
C、由题意,57号元素镧(La),结合“原子序数=核外电子数”,知该元素原子的核外电子数为57,故C正确;
D、由题意,57号元素镧(La),结合“原子序数=核内质子数”,知该元素原子的质子数为57,故D正确.
故选A.点评:
本题考点: 原子的定义与构成;元素的简单分类.
考点点评: 了解原子的定义和构成;熟记规律:“原子序数=核内质子数=核外电子数=核电荷数”;了解元素的简单分类.1年前查看全部
- 氢是新型清洁能源,但难储运,研究发现,镧和镍的一种合金是储氢的良好材料.其中的镧(La)元素核电荷数为57,相对原子质量
氢是新型清洁能源,但难储运,研究发现,镧和镍的一种合金是储氢的良好材料.其中的镧(La)元素核电荷数为57,相对原子质量为139,则下列关于镧元素的说法正确的是( )
A.原子内有139个质子
B.原子核内有57个中子
C.原子核外电子数为82
D.镧元素为金属元素 巡游者-证人1年前1
巡游者-证人1年前1 -
 ww5660261 共回答了20个问题
ww5660261 共回答了20个问题 |采纳率85%解题思路:由题意“镧(La)元素核电荷数为57,相对原子质量为139”,根据“相对原子质量≈质子数+中子数”,可知中子数;根据“原子序数=核内质子数=核外电子数=核电荷数”,可知原子核外电子数.在原子中,核内质子数=核外电子数=核电荷数=57;中子数=139-57=82;由汉语名称“镧”,可知其为金属元素.
故选D.点评:
本题考点: 原子的定义与构成;原子的有关数量计算;元素的简单分类.
考点点评: 了解原子的定义和构成:原子由原子核和核外电子构成,其中原子核由质子和中子构成的;1年前查看全部
- 氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料.下列有关57号元素镧(La)的说法不正确的是( )
氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料.下列有关57号元素镧(La)的说法不正确的是( )
A. 该元素原于的质子数为57
B. 该元素原子的核电荷数为57
C. 该元素原于的核外电子数为57
D. 该元素为非金属元素 wanglvye1年前2
wanglvye1年前2 -
 大万头 共回答了18个问题
大万头 共回答了18个问题 |采纳率100%解题思路:在原子中:原子序数=核电荷数=质子数=核外电子数,镧元素的元素名称中带金字旁,是金属元素.A、该元素原子的质子数=原子序数,故为57,此项正确;
B、核电荷数=原子序数,此项正确;
C、在原子中,核外电子数=原子序数,此项正确;
D、该元素名称为镧,故为金属元素,此项错误.
故选:D.点评:
本题考点: 原子的定义与构成;元素的简单分类.
考点点评: 在原子中,原子序数=核电荷数=质子数=核外电子数是一条很重要的规律.1年前查看全部
- 氢是新型清洁能源,但难储运。研究发现,合金可用来储藏氢气。镧( 139 57 La)和镍( 59 28 Ni)的一种合
氢是新型清洁能源,但难储运。研究发现,合金可用来储藏氢气。镧( 139 57 La)和镍( 59 28 Ni)的一种合 金就是储氢材料。该合金的晶胞如下图,镍原子除一个在中心外,其他都在面上,镧原子在顶点上。储 氢时氢原子存在于金属原子之间的空隙中。 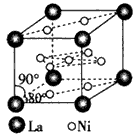
(1)一定条件下,该贮氢材料能快速、可逆地存储和释放氢气,若每个晶胞可吸收3个H 2 ,这一过程用化学方程式表示为:____。
(2)下列关于该贮氢材料及氢气的说法中,正确的是_______ (填序号)
A.该材料中镧原子和镍原子之间存在化学键,是原子晶体
B.氢分子被吸收时首先要在合金表面解离变成氢原子,同时放出热量
C.该材料贮氢时采用常温高压比采用常温常压更好
D.氢气很难液化是因为虽然其分子内氢键很强,但其分子间作用力很弱
(3)某研究性学习小组查阅的有关镍及其化合物的性质资料如下:
写出将NiO(OH)溶于浓盐酸的离子方程式:____。
(4)已知Ni(CO) 6 为正八面体结构,镍原子位于正八面体的中心,CO在正八面体的六个顶点上。若把其中两个CO换成NH 3 得到新化合物,则以下物质中互为同分异构体的是________ 。(填字母编号,任填一组)(图中黑点为NH 3 ,圆圈 为CO,Ni略去)
 YINJIA2NGLIN761年前1
YINJIA2NGLIN761年前1 -
 老郭也 共回答了15个问题
老郭也 共回答了15个问题 |采纳率93.3%1年前查看全部
- 氢是新型清洁能源,但难储运,研究发现,镧和镍的一种合金是储氢的良好材料.其中的镧(La)元素核电荷数为57,相对原子质量
氢是新型清洁能源,但难储运,研究发现,镧和镍的一种合金是储氢的良好材料.其中的镧(La)元素核电荷数为57,相对原子质量为139,则下列关于镧元素的说法正确的是( ) A.原子内有139个质子 B.原子核内有57个中子 C.原子核外电子数为82 D.镧元素为金属元素  l_swallow1年前1
l_swallow1年前1 -
 董凌帆 共回答了22个问题
董凌帆 共回答了22个问题 |采纳率95.5%在原子中,核内质子数=核外电子数=核电荷数=57;中子数=139-57=82;由汉语名称“镧”,可知其为金属元素.
故选D.1年前查看全部
- 氢是新型清洁能源,但难储运。研究发现,镧和镍的一种合金是储氢材料。下列有关57号元素镧(La)的说法不正确的是 [
氢是新型清洁能源,但难储运。研究发现,镧和镍的一种合金是储氢材料。下列有关57号元素镧(La)的说法不正确的是 [ ]A.该元素原子的质子数为57
B.该元素原子的核电荷数为57
C.该元素原子的核外电子数为57
D.该元素原子的质量为57 余吆儿1年前1
余吆儿1年前1 -
 暮露一勺RR 共回答了15个问题
暮露一勺RR 共回答了15个问题 |采纳率100%D1年前查看全部
大家在问
- 1请给他们拿一盒粉笔 英语翻译
- 2从2.3.5.7.11这五个数中,任取2个不同的数分别当做一个分数的分母与分子,分数有几个?真分数有几个?
- 3长城赞 这副对联分别是从哪几个方面来写长城的?表达了作者怎样的感情?
- 4预应力钢绞线下料长度计算6M长预应力刚混吊车梁,配直线预应力钢绞线2束,15.2,用YC60千斤顶一端张拉,XM锚具锚固
- 5(2013•昌平区一模)如图是甲、乙两种物质熔化时的温度-时间图象,其中物质______是晶体,它的熔点是______℃
- 6塑料改性实验员的主要工作是什么
- 7已知a的平方减3a等于7 b的平方加3b等于7 求b除于a加a除于b的值
- 8有关线性代数的问题在求其次线性方程组解的时候,遇到了这样一个问题:设A是3行4列矩阵,A的第一行到第三行分别是:(1、2
- 9四年级(1)班有学生48人,如果再转来3名男生,那么男生的人数是女生人数的2倍,三年级有男生有多少人?
- 10lot's of=?只有一个空格fashion
- 11在△abc中,AH⊥BC 垂足为H,E.F.D.是AB.AC.BC.的中点,求证,四边形DEFH是等腰梯形.
- 12求用短除法求出,40.30.48的最小公倍数,最好是图,可以看到短除法的过程.
- 13一架直升飞机从高度为450米的位置开始,先以20米/秒的速度上升60秒,后以12米/秒的速度下降120秒,这时的直升飞机
- 14一个长方形的周长是24厘米,长和宽都是整厘米数,这个长方形有几种不同情况?
- 15what is on the table?回答