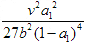一碳化学是以分子中只含有一个碳原子的化合物(如CO、CH4等)为原料合成一系列化工原料和燃料的化学.如图为一碳化学的一种
 zhanglincs2022-10-04 11:39:544条回答
zhanglincs2022-10-04 11:39:544条回答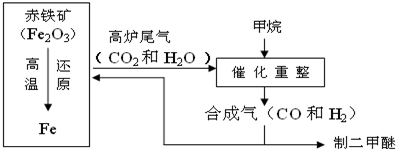 (1)利用高炉尾气中的水蒸气与甲烷催化重整得到合成气,化学方程式为______.
(1)利用高炉尾气中的水蒸气与甲烷催化重整得到合成气,化学方程式为______.(2)课外小组的同学从上述流程中收集到一瓶“合成气”,用下图所示装置进行研究(已知高温条件下,甲烷和氧化铁反应生成CO2和H2O,3H2+Fe2O3
| ||
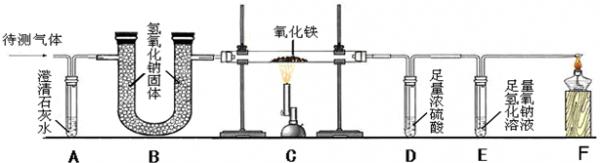
①A中澄清石灰水变浑浊,反应的化学方程式为______.
②C中一氧化碳与氧化铁反应的化学方程式为______.
③B装置中盛有足量的氢氧化钠颗粒,其作用是______.
④实验测量D和E的质量反应后分别增加9.0g和8.8g,推测原混合气体的组成为(假设混合气在C装置中反应完全)______(填字母).
A.CO、H2、CO2; B.CO、H2、CH4; C.CO、H2、CH4、CO2; D.CO2、H2、CH4.

已提交,审核后显示!提交回复
共4条回复
 我在等你回来 共回答了23个问题
我在等你回来 共回答了23个问题 |采纳率95.7%- 解题思路:(1)根据反应物生成物及化学方程式的书写原则正确写出化学方程式.
(2)根据题意,浓硫酸吸收燃烧生成的水而碱石灰用于吸收燃烧生成的二氧化碳,浓硫酸质量与碱石灰质量都增加,说明燃烧既生成了水又生成了二氧化碳,结合可燃物完全燃烧的规律,可判断混合气体中含C、H元素;而利用水、二氧化碳的质量进一步确定混合气体中C、H元素的质量比,对于判断混合气体的组成有决定性作用.(1)高炉尾气中的水蒸气与甲烷催化重整得到合成气,化学方程式为 CH4+H2O
催化剂
.
CO+3H2.
(2)①A中澄清石灰水变浑浊是因为二氧化碳与氢氧化钙反应生成不溶于水的碳酸钙,化学方程式为 CO2+Ca(OH)2═CaCO3↓+H2O.
②一氧化碳与氧化铁反应生成铁和二氧化碳,反应的化学方程式为 3CO+Fe2O3
高温
.
3CO2+2Fe.
③氢氧化钠颗粒具有吸水性,能吸水潮解,且能吸收二氧化碳,因此其作用是 吸收水分,除去二氧化碳.
④A中石灰水变浑浊,说明原气体中有二氧化碳,D装置增加的质量是生成的水的质量,原气体中含有氢元素,且氢元素质量=9g×[2/18]×100%=1g;E装置增加的质量是反应生成的二氧化碳的质量,故原气体中含有碳元素.且碳元素质量=8.8g×[12/44]×100%=2.4g;甲烷气体中C、H元素质量比=12:(1×4)=3:1,则混合气体中C、H元素质量比=2.4g:1g=15:4,因此可判断混合气体中若含有甲烷则一定同时含有CO气体;故选C.
故答案为:
(1)CH4+H2O
催化剂
.
CO+3H2;
(2)①CO2+Ca(OH)2═CaCO3↓+H2O;
②3CO+Fe2O3
高温
.
3CO2+2Fe;
③吸收水分,除去二氧化碳;
④C.点评:
本题考点: 物质的相互转化和制备;实验探究物质的组成成分以及含量;常见气体的检验与除杂方法;气体的净化(除杂);一氧化碳还原氧化铁;书写化学方程式、文字表达式、电离方程式.
考点点评: 可燃物完全燃烧时,可燃物中的碳元素全部生成二氧化碳,可燃物中的氢元素全部生成水;可燃物完全燃烧生成二氧化碳和水,可判断可燃物中一定含C、H元素. - 1年前
 猪宝贝熊宝贝 共回答了1个问题
猪宝贝熊宝贝 共回答了1个问题 |采纳率- CH4+H2O---CO+H2
- 1年前
 lanjingluoye 共回答了8个问题
lanjingluoye 共回答了8个问题 |采纳率- 没有图片没法回答
- 1年前
 zmdl 共回答了1个问题
zmdl 共回答了1个问题 |采纳率- 图在哪里?
- 1年前
相关推荐
- 一碳化学是指以研究分子中只含一个碳原子的化合物[如甲烷(CH 4 )、合成气(CO和H 2 )、CO 2 、CH 3 O
一碳化学是指以研究分子中只含一个碳原子的化合物[如甲烷(ch 4 )、合成气(co和h 2 )、co 2 、ch 3 oh等]为原料来合成一系列化工原料和燃料的化学。科学家提出一种“绿色***”构想:把空气吹入碳酸钾溶液,然后再把co 2 从溶液中提取出来,经化学反应后使空气中的co 2 转变为其它化工原料,如下图所示。 
(1)碳酸钾溶液所起的作用是__________。
(2)目前工业上有一种方法是用co 2 来生产燃料甲醇。一定条件下发生反应:co 2 (g)+3h 2 (g) ch 3 oh(g)+h 2 o(g)
ch 3 oh(g)+h 2 o(g)
① 下图表示该反应过程中能量(单位为kj/mol)的变化,关于该反应的下列说法中,正确的是__________ (填字母)。
a.△h>0,△s>0b.△h>0,△s<0
c.△h<0,△s<0d.△h<0,△s>0
在上图中,曲线_______ (填:a或b)表示使用了催化剂。
② 在压强为5mpa,体积为vl的反应室中,bmolco 2 与 3bmolh 2 在催化剂作用下反应生成甲醇,co 2 的转化率与某物理量的关系如下图。则表中横坐标的物理量为__________,r1时该反应的平衡常数k=________________(用含字母的代数式表示)。当该物理量从r1到 r2进行改变,平衡常数k将________(填“增大”、“不变”或“减小”)。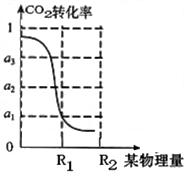
(3)过氧化尿素合成反应式如下:co(nh 2 ) 2 +h 2 o 2 → co(nh 2 ) 2 ·h 2 o 2 △h<0。当n (过氧化氢):n (尿素) 为 1.3∶1,反应时间45 min,用水杨酸作为稳定剂,分别考察反应温度对反应效果的影响如下图所示(活性氧含量可视为co(nh 2 ) 2 ·h 2 o 2 产量的直观表示) 
从图中可以看出,在实验选定的温度范围内,随反应温度的升高,产品活性氧含量先增加而随后减少。
① 根据图中信息,最佳反应温度为__________________。
② 如何说明该反应中在实验选定的温度范围内,随反应温度的升高,产品活性氧含量先增加而随后减少_________________ 。 ka399901年前1
ka399901年前1 -
 mingmei70 共回答了15个问题
mingmei70 共回答了15个问题 |采纳率93.3%1年前查看全部
- 一碳化学是以分子中只含一个碳原子的化合物(如CO、CH 4 等)为原料来合成一系列化工原料和燃料的化学.CO是从煤的气化
一碳化学是以分子中只含一个碳原子的化合物(如CO、CH 4 等)为原料来合成一系列化工原料和燃料的化学.CO是从煤的气化或合成气得到的.
A、煤的气化主要反应有:①2C+O 2 =2CO;②C+H 2 O=CO+H 2 ;③CO+H 2 O=CO 2 +H 2 .上述反应属于化合反应的是______(填序号),属于氧化反应的是______(填序号).
B、合成气可通过天然气的重整得到,如CH 4 +H 2 O=CO+3H 2 .二甲醚(CH 3 OCH 3 )可由合成气(CO和H 2 )在一定条件下制得.用合成气制二甲醚时,还产生了一种可参与大气循环的、常温为液态的氧化物,写出该反应的化学方程式:______.
C、酚醛树脂由苯酚和甲醛缩聚而成,单体甲醛的结构式为______. tclongsi1年前1
tclongsi1年前1 -
 天雨路滑 共回答了23个问题
天雨路滑 共回答了23个问题 |采纳率82.6%1年前查看全部
- 一碳化学是以分子中只含一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学.
一碳化学是以分子中只含一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学.
(1)工业上用天然气和水蒸气在高温条件下发生反应,得到CO和H2,该反应的化学方程式为______,得到的CO和H2的混合气被称为合成气,合成气在工业上可用于合成一系列化工原料和新型燃料,还可用于冶炼某些金属.
(2)某他学兴趣小组的同学在实验室模拟了合成气的制备,并设计实验验证合成气的还原性.
I.用甲烷和水蒸气在高温条件下反应得到合成气.根据(1)中所写的化学方程式.合成气中CO和H2的质量比为______.
Ⅱ.用合成气还原足量氧化铜.实验装置如图所示: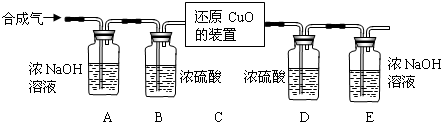
【设计买验步骤】
①连接好装置并检查气密性.
②装入药品,通人一段时间合成气.
③分别称量装置D、E的质量.
④缓缓通入合成气,加热装置C,使其充分反应.
⑤停止加热,继续通入合成气至恢复到室温.
⑥再次分别称量装置D、E的质量.
【完善实验设计】经过讨论同学们认为,装置E后还应添加一个酒精灯,并在实验步骤______(填实验步骤的序号)中点燃(点燃前应对气体验纯).
】进行实验】该小组的同学按上述步骤进行实验,并记录了实验现象和数据:
①装置C中出现______色物质.
②称量数据如表所示.
【现象分析和数据处理】装置D的质量 装置E的质量 反应前 292.4g 198.2g 反应后 296.0g 201.5g
①甲同学根据装置C中的现象,认为是合成气中的CO和H2还原了CuO.
②乙同学通过对上表数据的分析,推测除了CO和H2以外,制得的合成气中可能还有未反应的CH4,且CH4也还原了CuO.试通过计算说明他的推测依据.
③丙同学提出,实验步骤⑤中通入的气体会带走装置E中的部分水蒸气,使实验产生误差.你认为该误差对乙同学的推测结果是否有影响?______(选填“是”或“否”,并说明理由).
【拓展探究】该小组同学对于CH4是否真的能够还原氧化铜提出了质疑并进行探究.
查阅资料:甲烷具有还原性,可以还原氧化铜,生成CO2和H2O;白色的无水硫酸铜遇水会变成蓝色.
实验设计:该小组同学拟用纯净的甲烷气体和如下装置进行实验.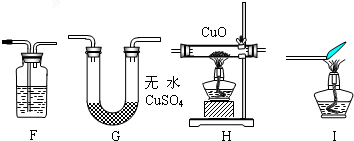
①如图装置F中盛放的试剂名称是______.
②如图装置的正确连接顺序是______(填字母,且每套装置限用一次).
【实验反思】除了可能是CH4也还原了CuO外,出现上表数据关系还可能是因为______(写出一个原因,并说明理由). 姿态万千1年前1
姿态万千1年前1 -
 荷风满袖 共回答了16个问题
荷风满袖 共回答了16个问题 |采纳率93.8%解题思路:(1)根据题中信息结合方程式书写要点书写.
(2)I.根据化学方程式的意义来分析求解.
Ⅱ.[完善实验设计]可分析各装置中发生反应的条件即可.
[进行实验]①可根据反应中各物质的物性来分析.
[现象分析和数据处理]
②分析表中数据可知生成物中CO2、H2O的质量,采用极端分析法讨论若全部是CO和H2参与反应得到的CO2、H2O的质量比与全部是甲烷参与反应得到的二者相比较来分析.
③若带着E装置中的部分水蒸气,对实验数据来说就是测得的H2O的质量将减小.即CO2和H2O的质量比增大,可以和实际试验数据相比较进行分析.
[拓展探究]
①要证明CH4参与反应,就是要证明反应后生成了CO2和H2O.
②根据反应过程来确定顺序,一般验证气体先验证水蒸气,因为中间反应可能带入水汽.
[实验反思因为合成气中有CH4、CO、H2O,是混合气参与的反应,参加反应的物质质量比并不是定值.(1)根据题意,生成物是CO和H2,条件是高温,根据方程式书写要求可以写出.CH4+H2O
高温
.
CO+3H2
(2)I.根据化学方程式知CO和H2的质量比=28:(2×3)=14:3
Ⅱ.[完善实验设计]分析所用各装置中的反应条件可知,装置C中氢气和氧化铜反应需要加热,对应实验步骤为②.
[进行实验]
①反应后装置C中黑色的氧化铜逐渐变为红色的铜,所以装置C中的固体是铜,为红色.
[现象分析和数据处理]
②如果只有CO和H2,还原足量CuO,合成气中CO与H2的分子个数比为1:3.生成物中碳元素与氢元素的质量比为2:1;如果只有CH4还原足量CuO,生成物中碳元素与氢元索的质量比为3:1.现测得CO2的质量:201.5g-198.2g=3.3g,H20的质量:296.0g一292.4g=3.6g
生成物中碳元素与氢元素的质量比:(3•3g×[12/44]):(3.6g×[2/18])=9:4,9;4介于2:1和3:1之间,由此可推测出,除了CO和H2以外,制得的合成气中可能还有来反应的CH4,且CH4也还原了CuO
③否.因为带走水蒸气会使测得的CO2质量偏低,而实际测得的生成物中碳、氢元素的质量比已经大于2:1,所以对推测结果无影响.
[拓展探究]要证明甲烷还原氧化铜,只要证明生成物中有CO2和H2O生成即可,所以F装置应是检验CO2生成的,用澄清石灰水.装置H是还原CuO,G是用来证明水的生成,F是证明二氧化碳生成,I是处理尾气,所以顺序为HGFI.
[实验反思]因为本题是定量性实验,反应物是混合物,在以上的讨论中对反应物参加的可能性进行了分析证明,影响生成物的质量变化的还有参加反应的物质质量大小以及反应过程中是否全部参与反应.所以可以从这两方面进行分析证明.
故答案为:
(1)CH4+H2O
高温
.
CO+3H2
(2)I.14:3
Ⅱ.[完善实验设计]②
[进行实验]红
[现象分析和数据处理]
②如果只有CO和H.还原足量CuO,合成气中CO与H2的分子个数比为1:3.生成物中碳元素与氢元素的质量比为2;1
如果只有CH4还原足量CuO,生成物中碳元素与氢元索的质量比为3:1
现测得CO2的质量:201.5g-198.2g=3.3g H20的质量:296.0g一292.4g=3.6g
生成物中碳元索与氢元索的质量比:(3•3g×[12/44]):(3.6g×[2/36])=9:4
9;4介于2:1和3:1之间
由此可推测出,除了CO和H2以外,制得的合成气中可能还有来反应的CH4,且CH4也还原了CuO.
③否.因为带走水蒸气,将会导致E装置的质量增加减小,从而会使测得的CO2质量偏低,(二氧化碳的质量就是两次称量E装置的质量差),而实际测得的生成物中碳、氢元素的质量比已经大于2:1,所以对推测结果无影响.
[拓展探究]澄清石灰水 H G F I
[实验反思]因为根据测得数据计算,生成物中碳、氧元素的质量比值2:1,所以可能是合成气中参与反应的CO与H2
分子个数比大于1:3(或H2未完全参加反应、生成的水未被完全吸收等).点评:
本题考点: 碳、一氧化碳、氢气还原氧化铜实验;仪器的装配或连接;常见气体的检验与除杂方法;质量守恒定律及其应用;常见化学反应中的质量关系;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题是一道综合性实验探究题,对培养学生分析问题解决问题的能力有一定的提高.1年前查看全部
- 一碳化学是以分子中只含有一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学.CO是从煤的气化或
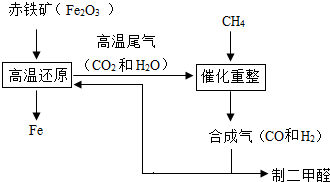 一碳化学是以分子中只含有一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学.CO是从煤的气化或合成气得到的.煤的气化主要反应有:
一碳化学是以分子中只含有一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学.CO是从煤的气化或合成气得到的.煤的气化主要反应有:
(1)2C+O2=2CO
(2)C+H2O=CO+H2
(3)CO+H2O=CO2+H2
A.上述反应属于化合反应的是______(填序号).
B.合成气可通过天然气的重整得到,如CH4+H2O=CO+3H2合成气可制二甲醚,二甲醚被称为21世纪的新型燃料.合成气还可用于冶炼金属,用它冶炼铁的部分生产过程示意如图
(1)二甲醚(CH3OCH3)可由合成气(CO和H2)在一定的条件下制的.用合成气制二甲醚时,还产生了一种可参与大气循环的、常温为液态的氧化物,写出该反应的化学方程式:2CO+4H2
CH3OCH3+H2O一定条件 .2CO+4H2.
CH3OCH3+H2O一定条件 .
(2)合成气在冶炼铁的生产过程中所起的作用是______. holanlau1年前1
holanlau1年前1 -
 娃哈哈f57 共回答了23个问题
娃哈哈f57 共回答了23个问题 |采纳率87%解题思路:A、化合反应是两种和两种以上物质生成一种物质的反应;
(1)根据反应物和生成物书写化学方程式;
(2)可以根据物质的性质和用途及其炼铁原理等方面进行分析、判断,从而得出正确的结论.A、化合反应是两种或两种以上物质反应后生成另一种物质的反应故答案为:(1)
(1)根据反应物生成物和质量守恒书写化学方程式为:2CO+4H2
一定条件
.
CH3OCH3+H2O
(2)合成气为CO和H2 故,它们能把铁从铁矿石中还原出来,做还原剂.
故答案为:A(1)
(1)2CO+4H2
一定条件
.
CH3OCH3+H2O
(2)将铁从铁矿石中还原出来(或还原剂)点评:
本题考点: 物质的相互转化和制备;一氧化碳还原氧化铁;化合反应及其应用;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查了化学方程式的书写及计算及其高炉炼铁等方面的内容.1年前查看全部
大家在问
- 1四道二、三元一次方程计算在线等哦
- 2在“验证机械能守恒定律”的实验中,打点计时器的打点周期为T,当地重力加速度的值为g,测得所用重锤的质量为m。若按实验要求
- 3问题:在细菌作用下,用氨处理含甲醇(CH3OH)的工业废水,使其与氧气反应变为无毒的氮N2 二氧化碳CO2 水H2O,从
- 4设n阶矩阵A是可逆矩阵且A的每行的元素的和是常量a .求证1、a 不等于0 ;2、A的逆矩阵的每行的元素的和为1/a
- 5最小的四位数是______,最大的五位数是______.
- 6列式计算.(1)227乘42,积是多少?(2)一个因数是350,另一个因数是68,积是多少?(3)17个504是多少?(
- 7had to cut a tree down的意思、
- 8It is the farmers who provide us with food,yet they are ____
- 9电流表正极接电源哪极?
- 10要想别人快乐,自己先得快乐.要把阳光散布到别人的心田里,先得自己心里有阳光.
- 11已知椭圆C中心在原点,与椭圆4x^2+9y^2=36的长轴长相等,且经过点(2,-1),求椭圆C的标准方程
- 12有黑色的光吗?是什么颜色光组成的?
- 13研究斜抛运动轨迹的方法有什么?
- 14英语填充题如题(XXX部份为填空处)XXXXXXXXXXXXXXXXXaround.XXXXXXXXXXXXXXXXXb
- 15根据下图所示仪器回答:(1)写出仪器名称:A.______B.______C.______D.______(2)填写仪器