若有两电极板,电容C1:C2=3:2 电荷量Q1:Q2=2:1 板距d1:d2=3:1 若两电子从负极板移向正极,求动能
 天地长久2022-10-04 11:39:541条回答
天地长久2022-10-04 11:39:541条回答若有两电极板,电容C1:C2=3:2 电荷量Q1:Q2=2:1 板距d1:d2=3:1 若两电子从负极板移向正极,求动能增量.

已提交,审核后显示!提交回复
共1条回复
 趣泥骂的 共回答了24个问题
趣泥骂的 共回答了24个问题 |采纳率95.8%- 由qU = △Ek可知,动能增量与电压成正比.
而U = Q/C
两极板的电压之比U1:U2 = (Q1/C1):(Q2/C2) = 4:3
所以两电子的动能增量之比 = 4:3 - 1年前
相关推荐
- 电解原理在化学工业中有广泛的应用。如图表示一个电解池, 装有电解液a;X、Y是两块电极板,通过导线与直流电源相
电解原理在化学工业中有广泛的应用。如图表示一个电解池, 装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。

请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为 ,在X极附近观察到的现象是 。电解液中向X极方向移动的离子是 。
②Y电极上的电极反应式为 ,
(2)如要用电解方法精炼粗铜,电解液a选用CuSO 4 溶液,则:
①X电极的材料是
②Y电极的电极反应式为 (说明:杂质发生的反应不必写出。)
③溶液中的c(Cu 2+ )与电解前相比 (填“变大”、“变小”或“不变”)。 wo369874121年前1
wo369874121年前1 -
 钢筋工李李 共回答了15个问题
钢筋工李李 共回答了15个问题 |采纳率73.3%(1)①2H 2 O + 2e- = H 2 + 2OH - (2H + +2e - =H 2 ↑)有气泡产生,溶液变红 Na + ,H +
②2Cl - - 2e - =Cl 2
(2)①精铜 ②Cu-2e - =Cu 2+ ③变小
1年前查看全部
- 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为______;在X极附近观察到的现象是______.
②Y电极上的电极反应式为______;检验该电极反应产物的方法是______.
(2)如用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是______,电极反应式为______.
②Y电极的材料是______,电极反应式为______.(说明:杂质发生的电极反应不必写出) 了了zz1年前1
了了zz1年前1 -
 jinxuezheng 共回答了22个问题
jinxuezheng 共回答了22个问题 |采纳率86.4%解题思路:(1)电解饱和食盐水时,阳极上是氯离子失电子,阴极上是氢离子得电子,氯气能使湿润的碘化钾淀粉试纸变蓝;
(2)根据电解精炼铜的工作原理知识来回答.(1)①和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,所以该电极附近氢氧根浓度增大,碱性增强,滴入几滴酚酞试液会变红,故答案为:2H++2e-=H2↑;放出气体,溶液变红;
②和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl--2e-=Cl2↑,氯气能使湿润的碘化钾淀粉试纸变蓝,可以用于氯气的检验,
故答案为:2Cl--2e-=Cl2↑;把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色;
(2)①电解方法精炼粗铜,电解池的阴极材料是纯铜,电极反应为:Cu2++2e-=Cu,故答案为:纯铜; Cu2++2e-=Cu;
②电解方法精炼粗铜,电解池的阳极材料是粗铜,电极反应为:Cu-2e-=Cu2+,故答案为:粗铜;Cu-2e-=Cu2+.点评:
本题考点: 电解原理.
考点点评: 本题考查学生电解池的工作原理知识,可以根据所学知识进行回答,难度不大.1年前查看全部
- 电解原理在化学工业中有广泛应用.如图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.请回
 电解原理在化学工业中有广泛应用.如图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)Y的电极名称是______.
(2)若X、Y都是惰性电极,a是硫酸钠溶液,实验开始时,同时在两边各滴入几滴石蕊试剂,一段时间后,在X极附近观察到的现是______,Y极上的电极反应式为______.
(3)若X、Y都是惰性电极,a是足量的CuSO4溶液,写出电解过程的化学方程式2CuSO4+2H2O
2Cu+O2↑+2H2SO4通电 .2CuSO4+2H2O电解一段时间,当电极上通过的电量为0.4mol时,阴极上生成物的质量为______.
2Cu+O2↑+2H2SO4通电 .
(4)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是______.方案 X Y a溶液 A 银 石墨 AgNO3 B 银 铁 AgNO3 C 铁 银 Fe(NO3)3 D 铁 银 AgNO3  sr幻江南1年前1
sr幻江南1年前1 -
 fengdanxailu 共回答了25个问题
fengdanxailu 共回答了25个问题 |采纳率92%解题思路:(1)和电源的正极相连的电极是电解池的阳极;
(2)电解硫酸钠,在阴极上是氢离子得电子的过程,在阳极上氢氧根离子失电子的过程;
(3)根据电解原理书写电解硫酸铜的电池反应,根据电子守恒进行计算即可;
(4)在电镀池中,镀层金属为阳极,镀件是阴极,电镀液是含有镀层金属阳离子的盐,据此回答.(1)Y和电源的正极相连,电极名称是阳极,故答案为:阳极;
(2)电解硫酸钠,在阴极上是氢离子得电子生成氢气的过程,氢离子浓度减小,溶液显碱性,遇到酚酞溶液变红,在阳极上氢氧根离子失电子的过程,即4OH --4e-=2H2O+O2↑,故答案为:产生气泡,溶液变红;4OH --4e-=2H2O+O2↑;
(3)电解硫酸铜,在阴极上是铜离子得电子的过程,在阳极上是氢氧根离子失电子的过程,总反应为:2CuSO4+2H2O
通电
.
2Cu+O2↑+2H2SO4,电极上通过的电量为0.4mol时,根据电极反应:Cu2++2e-=Cu,生成金属铜是0.2mol,即12.8g,故答案为:12.8g;
(4)在铁表面镀一层金属银的电镀池中,镀层金属Ag为阳极,镀件Fe是阴极,电镀液是含有镀层金属阳离子的盐极硝酸银溶液,故答案为:D.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查学生原电池和电解池的工作原理知识,注意电极反应式的书写、根据电子守恒的计算是重点,难度中等.1年前查看全部
- 电解原理在工业中有广泛应用。右图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问
电解原理在工业中有广泛应用。右图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)若X、Y是惰性电极,a是200mLNaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,则电解池中X极上的电极反应为_____,在X极附近观察到的现象是 :_______。Y电极上的电极反应式是_________,检验该电极反应产物的方法是 :________________。当外电路通过0.02 mol电子时,充分混合电解后的溶液,忽略溶液体积变化,理论上溶液的PH值为_______。
(2)如果用电解方法精炼粗铜,电解液a选用CuSO 4 溶液,则X电极的材料是_________,Y电极的材料是______,Y电极反应式是_______________。 Asea_man1年前1
Asea_man1年前1 -
 我是帅哥我怕你 共回答了18个问题
我是帅哥我怕你 共回答了18个问题 |采纳率94.4%(每空1分,共8分)(1)2H + +2e - =H 2 ↑ 有气泡,溶液变红 2Cl - —2e - ==Cl 2 ↑
把湿润的淀粉KI试纸放在Y极附近,试纸变蓝,说明Y极产物为Cl 2 13
(2)纯铜 粗铜 Cu-2e - ==Cu 2+
1年前查看全部
- 电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答下列
电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答下列问题 
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①Y电极上的电极反应式为_________________。
②在X极观察到的现象是_________________。
(2)如果在铁件的表面镀铜以防止铁被腐蚀,电解液a选用CuSO 4 溶液,则:
①X电极对应的金属是___________(填元素名称),其电极反应式为___________________。
②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12g,则电镀时电路中通过的电子为______mol。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因:______________________。 newy331年前1
newy331年前1 -
 abcdefg9 共回答了20个问题
abcdefg9 共回答了20个问题 |采纳率95%(1)①2Cl - -2e - =Cl 2 ↑;②X极附近的溶液变成红色
(2)①Fe;Cu 2+ +2e - =Cu;②0.08;③因为金属的活泼性为Zn>Fe>Cu,故镀铜铁镀层破损后,铁作负极,被腐蚀,镀锌铁镀层破损后,锌作负极,铁被保护1年前查看全部
- 电容器接地问题我想问电容器电极板一块接地以后电量是否不变?为什么?最好能具体点.另外就是我很纠结的问题,题目是这样的:如
电容器接地问题
我想问电容器电极板一块接地以后电量是否不变?为什么?最好能具体点.
另外就是我很纠结的问题,题目是这样的:
如图所示,一水平放置的平行板电容器充完电后一直与电源相连,带正电的极板接地,两极板间在P点固定一带正电的点电荷,若将负极板向下移动一小段距离稳定后(两板仍正对平行)
改变平行板距离后,电容变了,但是电压应该没有变,那还可不可以充电?为什么?而且接地后充进去的电会不会跑掉?
还有就是为什么P点电势变低?
 z888996561年前1
z888996561年前1 -
 honchard 共回答了12个问题
honchard 共回答了12个问题 |采纳率83.3%当一块极板接地时电量不会改变,因为电容C大小没有改变、电压U没有改变,电量Q=CU当然不会变了.
当改变平行板间的距离后C变大了而U没有发生变化,根据公式Q=CU电量Q增大,所以电容充电了.
充进去的电不会跑掉,因为电容不同的极板带的是不同的电荷,极性相反的电荷相互吸引,还有就是因为你一直和电源相连保持极板电压恒定.
电压不变极板间的距离减小,则气息的电场强度增大,p点离正极板的位置没变则这段的电位差增大,现在正极板接地所以为零电位,所以p点的电势更低了.1年前查看全部
- (14分)电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连
(14分)电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,电解开始后,在X极附近观察到溶液变红色,则X极与电源的____极连接,电解时X极上的电极反应为 ;检验Y电极上反应产物的方法是: ,电解过程中的总电解反应式为 。
(2)如果用该装置精炼铜,选用CuSO 4 作电解质溶液,则连接粗铜的是_______极(填写“X”或“Y”),析出Cu的一极的
电极反应式是 ,反应后,电解质溶液CuSO 4 的浓度___(填“变大”、“变小”或“不变”)。 冰淇凌的冬天1年前1
冰淇凌的冬天1年前1 -
 carylee27 共回答了19个问题
carylee27 共回答了19个问题 |采纳率89.5%(1)负极, 2H + +2e - =H 2 ↑ ;
方法是:湿润的淀粉碘化钾试纸变蓝,
反应式为 2NaCl+2H 2 O 2NaOH+ H 2 ↑+ Cl 2 ↑
(2)Y 极, Cu 2+ +2e - =Cu,浓度_变小。
电解开始后,在X极附近观察到溶液变红色,有氢氧根析出,为阴极则X极与电源的负极连接。Y为阳极产生氯气,用湿润的淀粉碘化钾试纸检验。粗铜做阳极,纯铜做阴极,Cu 2+ +2e - =Cu,因为溶液体积变小,所以浓度变大。1年前查看全部
- 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则电解池中X极上的电极反应式为______.在X极附近观察到的实验现象是______.
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
X电极的材料是______,Y电极的材料是______,
Y电极反应式为______.(说明:杂质发生的电极反应不必写出) 1389289991年前1
1389289991年前1 -
 yybbsong 共回答了18个问题
yybbsong 共回答了18个问题 |采纳率88.9%解题思路:(1)若X、Y都是惰性电极,a是饱和NaCl溶液,Y电极上氯离子放电生成氯气,X电极上氢离子放电,同时该电极附近生成氢氧根离子;
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,阳极应该是粗铜、阴极是纯铜,则X电极是纯铜、Y电极是粗铜,阴极上铜离子放电.(1)若X、Y都是惰性电极,a是饱和NaCl溶液,和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,所以该电极附近氢氧根浓度增大,碱性增强,滴入几滴酚酞试液会变红,
故答案为:2H++2e-=H2↑;酚酞变红,有气泡产生;
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,阳极应该是粗铜、阴极是纯铜,则X电极是纯铜、Y电极是粗铜,阳极发生反应为:Cu-2e-=Cu2+,故答案为:纯铜;粗铜; Cu-2e-=Cu2+;点评:
本题考点: 电解原理.
考点点评: 本题考查原电池原理,为高频考点,侧重于学生的分析能力的考查,本题涉及电极反应式的书写、检验等知识点,知道离子放电顺序及电极反应式的书写方法,题目难度不大.1年前查看全部
- 电解原理在化学工业中有着广泛的应用。图甲表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。则下列
电解原理在化学工业中有着广泛的应用。图甲表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。则下列说法不正确的是

A.若此装置用于电解精炼铜,则X为纯铜、Y为粗铜,电解的溶液a可以是硫酸铜或氯化铜溶液 B.按图甲装置用惰性电极电解AgNO 3 溶液,若图乙横坐标 x 表示流入电极的电子的物质的量,则E可表示反应生成硝酸的物质的量,F表示电解生成气体的物质的量 C.按图甲装置用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,加入0.5 mol的碳酸铜刚好恢复到通电前的浓度和pH,则电解过程中转移的电子为2.0 mol D.若X、Y为铂电极,a溶液为500 mL KCl和KNO 3 的混合液,经过一段时间后,两极均得到标准状况下11.2 L气体,则原混合液中KCl的物质的量浓度至少为2.0 mol·L - 1  路人ing1年前1
路人ing1年前1 -
 安利2003 共回答了17个问题
安利2003 共回答了17个问题 |采纳率82.4%C
电解精炼铜时,阳极为粗铜,阴极为纯铜,电解质溶液为可溶性铜盐溶液,A项正确;惰性电极电解AgNO 3 溶液时的反应为4AgNO 3 +2H 2 O 4HNO 3 +4Ag+O 2 ↑,故B项正确;利用电解CuSO 4 溶液的反应式2CuSO 4 +2H 2 O
4HNO 3 +4Ag+O 2 ↑,故B项正确;利用电解CuSO 4 溶液的反应式2CuSO 4 +2H 2 O 2Cu+2H 2 SO 4 +O 2 ↑可知,若电解一段时间CuSO 4 溶液后加入0.5 mol的碳酸铜刚好恢复到通电前的浓度和pH,则电解过程中转移的电子为1.0 mol,C项错;D项,阴极析出氢气,阳极先析出氯气,后析出氧气,因此若两极气体体积相等则阳极产生的气体只能是氯气,利用氯原子守恒可知混合液中 c (KCl)至少为1 mol÷0.5 L=2.0 mol·L - 1 。
1年前查看全部
2Cu+2H 2 SO 4 +O 2 ↑可知,若电解一段时间CuSO 4 溶液后加入0.5 mol的碳酸铜刚好恢复到通电前的浓度和pH,则电解过程中转移的电子为1.0 mol,C项错;D项,阴极析出氢气,阳极先析出氯气,后析出氧气,因此若两极气体体积相等则阳极产生的气体只能是氯气,利用氯原子守恒可知混合液中 c (KCl)至少为1 mol÷0.5 L=2.0 mol·L - 1 。
1年前查看全部
- (20分)电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连
(20分)电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

⑴若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为 。
在X极附近观察到的实验现象是 。
② Y电极上的电极反应式为 。
③总反应方程式: ;
⑵若要在铁制品上镀一定厚度的银层
① X电极材料是 (填铁或银);
② a是 溶液
③ Y电极反应方程式: ;
⑶若X、Y都是铂电极,电解某金属的氯化物(XCl 2 )溶液,当收集到1.12 L氯气时(标准状况),阴极增重3.2 g .
①该金属的相对原子质量是 ;②电路中有 mol电子通过。 包你可爱1年前1
包你可爱1年前1 -
 白松林 共回答了19个问题
白松林 共回答了19个问题 |采纳率100%1年前查看全部
- 电容器的电极板受到的库仑力两个电荷量为1库的点电荷在真空中相距1m时相互作用力为9*10^9N,差不多相当于100万吨物
电容器的电极板受到的库仑力
两个电荷量为1库的点电荷在真空中相距1m时相互作用力为9*10^9N,差不多相当于100万吨物体所受到的重力!那法拉级的电容器两个极板间受到的力呢,肯定很小的,怎么回事? 穿心的痛苦1年前2
穿心的痛苦1年前2 -
 蹲小僵尸蹲 共回答了17个问题
蹲小僵尸蹲 共回答了17个问题 |采纳率82.4%这个问题很好回答,库仑定律的适用条件是,真空中的点电荷.
一个电荷为1库仑的球体,它的体积不可能很小,相距才一米,库仑定理不适用了
也可以这样说,如果小球的电荷量为1 库仑,那它会电离空气放电了,带电量实在太多了
你可以看你们的例题,带电量是极少的
电容也是一样,能带到的电量是很小的1年前查看全部
- 一平行板电容器两极电容D 面积S 其中方有厚度为t的介质 相对介电长度εr 介质两边为空气 设电极板电位差U
一平行板电容器两极电容D 面积S 其中方有厚度为t的介质 相对介电长度εr 介质两边为空气 设电极板电位差U
求:1 介质中的电场强度 电位移 极化强度
2 极板上的电荷量
3 极板和介质间隙中的场强
4 平行板见的电容 cyhgiant1年前1
cyhgiant1年前1 -
 怀念朋友的孩子 共回答了21个问题
怀念朋友的孩子 共回答了21个问题 |采纳率90.5%设平板电容器的板间距为d,空气介质的间距分别为d1、d2,空气相对介电常数为ε0,有(d—t)=( d1—d2),
1, 电位移与介质无关,电位移D=U/d,
电介质中的电场强度Er=D/εr,
极化系数χr=εr—1,极化强度Pr=χr×Er=(εr—1)×Er;
2,电容器的电量Q=C×U.
3,空气介质的电场强度E0=D/ε0.
4,电容器的容量C=S÷[4π×(d1÷ε0+d2÷ε0+t÷εr)]
=S÷{4π×[(d-t)÷ε0+t÷εr]}.1年前查看全部
- 电解原理在化学工业中有广泛应用.如表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问
 电解原理在化学工业中有广泛应用.如表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则可观察到在X极附近观察到的现象是______电极反应式是______检验Y电极反应产物的方法是______电极反应式是______、发生______反应,电解一段时间之后溶液的PH将会______(升高、降低或不变)总方程式为2NaCl+2H2O
2NaOH+H2↑+Cl2↑电解 .2NaCl+2H2O
2NaOH+H2↑+Cl2↑电解 .
(2)若X、Y都是铜电极,a是稀CuSO4溶液,开始实验,X极的电极反应式是______.Y电极的电极反应式是______,电解前后CuSO4溶液的浓度______(变大、变小或不变)若X电极质量增重64克,则在电路中有______mol的电子发生转移. ymwy19851年前1
ymwy19851年前1 -
 我aa 共回答了17个问题
我aa 共回答了17个问题 |采纳率94.1%解题思路:(1)若X、Y都是惰性电极,a是饱和NaCl溶液,X电极上氯离子放电生成黄绿色氯气,电极反应式为2Cl--2e-=Cl2↑,氯气具有强氧化性,能使湿润的淀粉碘化钾试纸变蓝色;Y电极上氢离子放电生成氢气,电极反应式为2H++2e-=H2↑,同时电极附近生成氢氧根离子,导致阴极附近溶液碱性增强;
(2)若X、Y都是铜电极,a是稀CuSO4溶液,Y电极上铜失电子发生氧化反应,X电极上铜离子得电子发生还原反应,该装置为电镀池;根据铜和转移电子之间的关系式计算.(1)X电极上氢离子放电,同时电极附近生成氢氧根离子,导致溶液碱性增强,溶液呈红色,电极反应式为2H++2e-=H2↑;Y电极上氯离子失电子发生氧化反应而生成氯气,氯气具有强氧化性,能将碘离子氧化为碘单质,碘遇淀粉试液变蓝色,所以可以用湿润的碘化钾淀粉试纸放在Y电极附近检验氯气,试纸变蓝色,电极反应式为2Cl--2e-=Cl2↑,电解一段时间之后溶液的PH将会升高,电池反应式为2NaCl+2H2O
电解
.
2NaOH+H2↑+Cl2↑;
故答案为:放出气体,溶液呈红色;2H++2e-=H2↑;把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色;2Cl--2e-=Cl2↑;氧化;升高;2NaCl+2H2O
电解
.
2NaOH+H2↑+Cl2↑;
(2)若X、Y都是铜电极,a是稀CuSO4溶液,X电极上铜离子得电子发生还原反应,电极反应式为Cu2++2e-═Cu,Y电极上铜失电子发生氧化反应,电极反应式为Cu-2e-═Cu2+,该装置为电镀池,阳极上溶解的铜等于阴极上析出的铜,所以溶液浓度不变,X电极增重的物质是Cu,根据铜和转移电子之间的关系式知,转移电子的物质的量=
64g
64g/mol×2=2mol,
故答案为:Cu2++2e-═Cu;Cu-2e-═Cu2+;不变;2.点评:
本题考点: 电解原理.
考点点评: 本题考查了电解原理,根据各个电极上发生的反应及物质的性质来分析解答,知道氯气的检验方法,注意:电解精炼粗铜和电镀铜时溶液中铜离子浓度是否变化,为易错点.1年前查看全部
- 除颤仪的两个电极板对一块放电会是什么情况
 w54f1年前1
w54f1年前1 -
 gzchenyin 共回答了19个问题
gzchenyin 共回答了19个问题 |采纳率94.7%中国神话故事中,关于雷公(雷神)的工作就是手拿两个铜钹一合,随之就是产生一个响雷;如果手拿除颤仪的两个电极板对一块放电,那就是相当于干了一次雷公的工作.
除颤仪因为短路放电,所准备的电能通过短路电流释放,将损坏保护电路甚至整个设备.1年前查看全部
- 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下
 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和CuCl2溶液,则
①电解池中X极上的电极反应式是______.
②Y电极上的电极反应式是______ 检验该电极反应产物的方是______.
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①Y电极的材料是______
②假若电路中有0.04摩尔电子通过时,阴极增重______克. yuwyq1年前1
yuwyq1年前1 -
 坐看云起75 共回答了18个问题
坐看云起75 共回答了18个问题 |采纳率94.4%解题思路:(1)X、Y是两块电极板,通过导线与直流电源相连,与电源正极相连的Y电极为阳极,与电源阴极相连的X电极为阴极,若X、Y都是惰性电极,a是饱和CuCl2溶液,则阳极上是氯离子失电子发生氧化反应,阴极上是溶液中铜离子得到电子生成铜;检验氯气应用湿润的碘化钾淀粉试纸,遇到氯气变蓝色;
(2)电解方法精炼粗铜,电解液a选用CuSO4溶液,粗铜做阳极,精铜做阴极;依据电子守恒计算析出铜的质量.(1)①电解池中X极是阴极,溶液中铜离子得到电子生成铜,电极反应式是:Cu2++2e -=Cu;
故答案为:Cu2++2e -=Cu;
②与电源正极相连的Y电极为阳极,溶液中氯离子失电子发生氧化反应,Y电极上的电极反应式是:2Cl --2e -=Cl2↑,检验氯气的方法是:把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色,说明生成氯气;
故答案为:2Cl --2e -=Cl2↑,把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色;
(2)电解方法精炼粗铜,电解液a选用CuSO4溶液,粗铜做阳极,精铜做阴极;
①Y电极为电解池的阳极,所以Y电极的材料是粗铜;
故答案为:粗铜;
②假若电路中有0.04摩尔电子通过时,阳极电极反应Cu2++2e-=Cu,阴极增重铜0.02mol,质量=0.02mol×64g/mol=1.28g;
故答案为:1.28.点评:
本题考点: 电解原理.
考点点评: 本题考查了电解原理的分析应用,主要是电极反应和电极判断,电子守恒是金属的依据,掌握基础是关键,题目较简单.1年前查看全部
- (12分)电解原理在化学工业中有广泛应用。右图表示一个电解池,其中a为电解质溶液, X、Y是两块电极板,通过导线与直流电
(12分)电解原理在化学工业中有广泛应用。右图表示一个电解池,其中a为电解质溶液, X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)X的电极名称是 (填写“阳极”或“阴极”)。
(2)若X、Y都是惰性电极,a是饱和食盐水,实验开始时,同时在两边各滴入几滴酚酞试液,一段时间后,在X极附近观察到的现象是 ,Y极上的电极反应式为
(3)若X、Y都是惰性电极,a是CuSO 4 溶液,电解一段时间后,阳极上产生气体的体积为0.224L(标准状况下),则阴极上析出金属的质量为 g。
(4)若要用该装置电解精炼粗铜,电解液a选用CuSO 4 溶液,则Y电极的材料是 。
(5)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是 。方案 X Y a溶液 A 银 石墨 AgNO 3 B 银 铁 AgNO 3 C 铁 银 Fe(NO 3 ) 3 D 铁 银 AgNO 3  romabo1年前1
romabo1年前1 -
 lufg 共回答了18个问题
lufg 共回答了18个问题 |采纳率88.9%(12分)(1)阴极 (2)放出气体,溶液变红 2Cl - - 2e - = Cl 2 ↑
(3)1.28g (4)粗铜 (5)D
1年前查看全部
- 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴石蕊试液,则
①电解池中X极上的电极反应式是______.
在X极附近观察到的现象是______.
②Y电极上发生的反应属于______ 反应.
③电解后X极产生白色沉淀,则该沉淀最有可能是(填化学式______.
(2)如要用电解方法实现将铁片镀上一层金属铜,电解液a选用CuSO4溶液,则
①X电极的材料是______
②Y电极反应式是______.
③已知开始时铁片与铜片的质量相同,当电路中有0.4摩尔电子通过时,两极质量相差______克. Jzrr1年前1
Jzrr1年前1 -
 fxsll 共回答了18个问题
fxsll 共回答了18个问题 |采纳率100%解题思路:(1)①电解饱和食盐水时,阴极上是氢离子得电子,生成氢气;
②阳极上是氯离子失电子,生成氯气,氯气能使湿润的碘化钾淀粉试纸变蓝;
(2)①根据电镀池工作原理可知,Fe作阴极,Cu作阳极,利用电源确定阴极;
②阳极铜失去电子发生氧化反应;
③根据得失电子守恒计算溶解的铜和析出的铜的质量.(1)①和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,X电极负极水的电离被破坏,氢氧根离子浓度增大,石蕊溶液呈蓝色;
故答案为:2H++2e-=H2↑;放出气体,溶液呈蓝色;
②和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl--2e-=Cl2↑;
故答案为:氧化;
③和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,X电极负极水的电离被破坏,氢氧根离子浓度增大,和镁离子交换生成白色沉淀,电解后X极产生白色沉淀为氢氧化镁;
胡答案为:Mg(OH)2;
(2)①电解方法铁上镀铜,X为阴极,电解池的阴极材料是铁,电极反应为Cu2++2e-=Cu,阳极是镀层金属铜,Cu-2e -=Cu2+;
故答案为:铁:
②电镀原理分析,Y为阳极,电解池的阳极材料是铜,电极反应为:Cu-2e-=Cu2+,故答案为;Cu-2e-=Cu2+;
③电镀时两极反应为:Y电极:Cu-2e-=Cu2+,X电极上:Cu2++2e-=Cu,若电镀时电路中通过的电子为0.4mol,则Y极上质量减少12.8g,X极上质量增加12.8g,所以A、B两极质量相差25.6g,
故答案为:25.6.点评:
本题考点: 电解原理.
考点点评: 本题考查学生电解池的工作原理知识,明确图中电源的正负极确定电解池的阴阳极是解答的关键,并熟悉电极反应及离子的放电顺序来解答,题目难度中等.1年前查看全部
- 电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下
电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为 ,
在X极附近观察到的现象是 。
②Y电极上的电极反应式为 ,
检验该电极反应产物的方法是 。
③总反应的化学方程式 。
(2)X、Y都是惰性电极,电解CuSO 4 溶液,当电路中通过0.4mol 电子时,析出铜的同时在另一个电极可得 L O 2 (标准状况下) 丢失的爱情在风中1年前1
丢失的爱情在风中1年前1 -
 米澈_贵族血统 共回答了18个问题
米澈_贵族血统 共回答了18个问题 |采纳率88.9%1年前查看全部
- 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为______;在X极附近观察到的现象是______.
②Y电极上的电极反应式为______;检验该电极反应产物的方法是______.
(2)如用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是______,电极反应式为______.
②Y电极的材料是______,电极反应式为______.(说明:杂质发生的电极反应不必写出) 戒了咖啡1年前1
戒了咖啡1年前1 -
 蚊子不吸血 共回答了24个问题
蚊子不吸血 共回答了24个问题 |采纳率91.7%解题思路:(1)电解饱和食盐水时,阳极上是氯离子失电子,阴极上是氢离子得电子,氯气能使湿润的碘化钾淀粉试纸变蓝;
(2)根据电解精炼铜的工作原理知识来回答.(1)①和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,所以该电极附近氢氧根浓度增大,碱性增强,滴入几滴酚酞试液会变红,故答案为:2H++2e-=H2↑;放出气体,溶液变红;...
点评:
本题考点: 电解原理.
考点点评: 本题考查学生电解池的工作原理知识,可以根据所学知识进行回答,难度不大.1年前查看全部
- 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)若X、Y都是惰性电极,a是100mL饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为______.
②Y电极上的电极反应式为______,
③一段时间后,在阴极得到112mL标准状况下的气体,此时溶液的pH为______.
(溶液体积变化忽略不计)
(2)如要用电解方法精炼粗铜,电解液a选用CuSO 4 溶液,则
①X电极的材料是______,电极反应式是______.
②Y电极的材料是______,电极反应式是______.(说明:杂质发生的电极反应不必写出)
 zqbox1601年前1
zqbox1601年前1 -
 injeak 共回答了15个问题
injeak 共回答了15个问题 |采纳率100%(1)①和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H + +2e - =H 2 ↑,
故答案为:2H + +2e - =H 2 ↑;
②和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl - -2e - =Cl 2 ↑,
故答案为:2Cl - -2e - =Cl 2 ↑;
③由2NaOH~H 2 ↑,阴极得到112mL标准状况下的气体,则n(OH - )=
0.112L
22.4L/mol ×2=0.01mol,
c(OH - )=
0.01mol
0.1L =0.1mol/L,所以pH=13,
故答案为:13;
(2)①电解方法精炼粗铜,电解池的阴极材料是纯铜,电极反应为:Cu 2+ +2e - =Cu,故答案为:纯铜;Cu 2+ +2e - =Cu;
②电解方法精炼粗铜,电解池的阳极材料是粗铜,电极反应为:Cu-2e - =Cu 2+ ,故答案为:粗铜;Cu-2e - =Cu 2+ .1年前查看全部
- 电解原理在化学工业中有广泛应用.如图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线
电解原理在化学工业中有广泛应用.如图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线
 电解原理在化学工业中有广泛应用.如图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)Y的电极名称是______.
(2)若X、Y都是惰性电极,a是硫酸钠溶液,实验开始时,同时在两边各滴入几滴石蕊试剂,一段时间后,在X极附近观察到的现是______,Y极上的电极反应式为______.
(3)若X、Y都是惰性电极,a是足量的CuSO4溶液,写出电解过程的化学方程式______电解一段时间,当电极上通过的电量为0.4mol时,阴极上生成物的质量为______.
(4)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是______.方案 X Y a溶液 A 银 石墨 AgNO3 B 银 铁 AgNO3 C 铁 银 Fe(NO3)3 D 铁 银 AgNO3
 狗尾巴大草1年前1
狗尾巴大草1年前1 -
 杨小以 共回答了21个问题
杨小以 共回答了21个问题 |采纳率95.2%(1)Y和电源的正极相连,电极名称是阳极,故答案为:阳极;
(2)电解硫酸钠,在阴极上是氢离子得电子生成氢气的过程,氢离子浓度减小,溶液显碱性,遇到酚酞溶液变红,在阳极上氢氧根离子失电子的过程,即4OH --4e-=2H2O+O2↑,故答案为:产生气泡,溶液变红;4OH --4e-=2H2O+O2↑;
(3)电解硫酸铜,在阴极上是铜离子得电子的过程,在阳极上是氢氧根离子失电子的过程,总反应为:2CuSO4+2H2O
通电
.
2Cu+O2↑+2H2SO4,电极上通过的电量为0.4mol时,根据电极反应:Cu2++2e-=Cu,生成金属铜是0.2mol,即12.8g,故答案为:12.8g;
(4)在铁表面镀一层金属银的电镀池中,镀层金属Ag为阳极,镀件Fe是阴极,电镀液是含有镀层金属阳离子的盐极硝酸银溶液,故答案为:D.1年前查看全部
- 物理中的将一电极板与电源正极相连,是正极吸走了金属板的电子使金属板带了正电还是因为金属板成了正极的一部分从而带了正电呢?
 豹20081年前1
豹20081年前1 -
 宁子_无语 共回答了20个问题
宁子_无语 共回答了20个问题 |采纳率95%从你讲的情况看,应该属于电化学的范畴.时间长了,我也记不太清了.不过,正极电势高,带负电的电子在电路通的状态下,会向正极聚集.但是你的描述,只是说与正极相连,没有说通路,应该是你所描述的第二种情况,是金属板成了正极的一部分.1年前查看全部
- 电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以
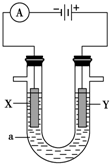 电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚
酞试液,则:
①电解池中X极上的电极反应式为______,在X极附近观察到的现象是______.
②Y电极上的电极反应式为______,检验该电极反应产物的方法是______.
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是______,电极反应式为______.
②Y电极的材料是______,电极反应式为______.(说明:杂质发生的电极反应不必写出)
③溶液中的c(Cu2+)与电解前相比______(填“变大”、“变小”或“不变”).
(3)如利用该装置实现铁上镀锌,电极X上发生的反应为______,电解池盛放的电镀液的浓度与电解前相比______(填“变大”、“变小”或“不变”). 正在回忆1年前1
正在回忆1年前1 -
 甜甜芒果 共回答了13个问题
甜甜芒果 共回答了13个问题 |采纳率76.9%解题思路:(1)①X电极上氢离子放电生成氢气,同时电极附近生成氢氧根离子,导致溶液呈碱性,酚酞遇碱变红色;
②Y电极上氯离子放电生成氯气,用湿润的淀粉碘化钾试纸检验氯气;
(2)电解精炼粗铜时,粗铜作阳极,纯铜作阴极,阳极上溶解铜和其它物质,根据转移电子守恒知,阴极上析出铜的物质的量大于阳极溶解铜的物质的量;
(3)电镀时,镀层作阳极,镀件作阴极,阳极溶解的金属等于阴极析出的金属.(1)①和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,所以该电极附近氢氧根浓度增大,碱性增强,滴入几滴酚酞试液会变红,
故答案为:2H++2e-=H2↑或2H2O+2e-=H2+2OH-;放出气体,溶液变红;
②和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl--2e-=Cl2↑,
氯气和碘化钾反应生成碘单质,碘遇淀粉试液变蓝色,所以可以用湿润的淀粉碘化钾试纸检验氯气,如果湿润的淀粉碘化钾试纸变蓝色,就说明生成的氯气,故答案为:2Cl--2e-═Cl2↑;把湿润的淀粉碘化钾试纸放在Y电极附近,试纸变蓝色,说明生成了Cl2;
(2)①电解精炼粗铜时,粗铜作阳极,纯铜作阴极,所以X电极材料是纯铜,该电极上铜离子得电子生成铜,电极反应式为:Cu2++2e-═Cu,
故答案为:纯铜;Cu2++2e-═Cu;
②粗铜作阳极,所以Y电极材料是粗铜,该电极上铜失电子发生氧化反应,电极反应式为,故答案为:粗铜;Cu-2e-═Cu2+;
③阳极上铜和其它较活泼的金属失电子,阴极上只有铜离子得电子,根据转移电子相等知,析出的铜大于溶解的铜,所以溶液中铜离子浓度变小,故答案为:变小;
(3)电镀时,镀层锌作阳极,镀件作阴极,阳极上电极反应式为Zn2++2e-═Zn,阳极溶解金属的质量等于阴极析出金属的质量,所以溶液中金属阳离子浓度不变,
故答案为:Zn2++2e-═Zn;不变.点评:
本题考点: 电解原理.
考点点评: 本题以电解原理为载体考查了电解精炼和电镀等知识点,明确各个电极上放电的物质或离子是解本题关键,根据得失电子书写电极反应式,知道氯气的检验方法,难度不大.1年前查看全部
- 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴石蕊试液,则
实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式是______.在X极附近观察到的是______.
②Y电极上的电极反应式是______,检验该电极反应产物的方法是______.
(2)如要用电解方法实现将铁片镀上一层金属铜,电解液a选用CuSO4溶液,则
①X电极的材料是______②Y电极反应式是______.
③已知开始时铁片与铜片的质量相同,当电路中有0.4摩尔电子通过时,两极质量相差______克. 小依香1年前1
小依香1年前1 -
 phenson 共回答了13个问题
phenson 共回答了13个问题 |采纳率92.3%解题思路:(1)①电解饱和食盐水时,阴极上是氢离子得电子,生成氢气;
②阳极上是氯离子失电子,生成氯气,氯气能使湿润的碘化钾淀粉试纸变蓝;
(2)①根据电镀池工作原理可知,Fe作阴极,Cu作阳极,利用电源确定阴极;
②阳极铜失去电子发生氧化反应;
③根据得失电子守恒计算溶解的铜和析出的铜的质量.(1)①和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,所以该电极附近氢氧根浓度增大,碱性增强,滴入几滴酚酞试液会变红,故答案为:2H++2e-=H2↑;放出气体,溶液变红;
②和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl--2e-=Cl2↑,氯气能使湿润的碘化钾淀粉试纸变蓝,可以用于氯气的检验,
故答案为:2Cl--2e-=Cl2↑;把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色;
(2)①负极连接电解池的阴极,所以X极是阴极是Fe;故答案为:Fe;
②Y极是阳极,铜在阳极上失去电子,发生氧化反应,生成铜离子电极反应式是Cu-2e -=Cu2+,故答案为:Cu-2e -=Cu2+;
③电镀时两极反应为:Y电极:Cu-2e-=Cu2+,X电极上:Cu2++2e-=Cu,若电镀时电路中通过的电子为0.4mol,则Y极上质量减少12.8g,X极上质量增加12.8g,所以A、B两极质量相差25.6g,
故答案为:25.6.点评:
本题考点: 电解原理.
考点点评: 本题考查学生电解池的工作原理知识,明确图中电源的正负极确定电解池的阴阳极是解答的关键,并熟悉电极反应及离子的放电顺序来解答,题目难度中等.1年前查看全部
- 与电源断开电极板相互靠近电场强度怎么变?
与电源断开电极板相互靠近电场强度怎么变?
C不是随d减小而增大吗,C=Q/U,电源断开即电量不变,C减小-→U减小
U=Ed,d也减小,那么E不是有增大、不表两种情况吗? 流星雪糕1年前1
流星雪糕1年前1 -
 翎的幻想 共回答了22个问题
翎的幻想 共回答了22个问题 |采纳率100%电源断开,电量Q不变.
相互靠近的话,距离变小,电容变小.Q不变,电压变大.电场强度变大1年前查看全部
- (16分)电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板(X、Y都是惰性电极),A
(16分)电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板(X、Y都是惰性电极),A、B 是出口,通过导线与直流电源相连。

请回答以下问题:
(1). 若a是CuCl 2 溶液,则
①X电极的现象是 ,
电极反应式是 。
②在B出口放一块湿润的KI-淀粉试纸会变为 色。
(2).若a饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式是 。
在X极附近观察到的现象是 。
② Y电极上的电极反应式是 。
(3). 若a是400mL 2mol /LCuSO 4 溶液,一段时间阴极增重1.28g(该极无气体放出),则溶液的PH为 ,阳极可收集标况下气体 mL 无情_风_飘零1年前1
无情_风_飘零1年前1 -
 柔软舒适好心情 共回答了19个问题
柔软舒适好心情 共回答了19个问题 |采纳率94.7%(1).①x电极上有红色物质析出, Cu 2+ + 2e - = Cu ② 蓝
(2)① 2H + +2 e - =H 2 ↑;无色溶液变红②2Cl - —2 e - =Cl 2 ↑ (3). 1、22.4
1年前查看全部
- (14分)电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连
(14分)电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为 。
在X极附近观察到的现象是 。
②Y电极上的电极反应式为 ,
检验该电极反应产物的方法为 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO 4 溶液,则:
①X电极的材料是 ,电极反应式为 。
②Y电极的材料是 ,电极反应式为 。(说明:杂质发生的电极反应不必写出) lyjx1年前1
lyjx1年前1 -
 zbond 共回答了16个问题
zbond 共回答了16个问题 |采纳率87.5%(1)①2H + +2e-=H 2 ↑ 有气泡产生,溶液变红
②2Cl - -2e-=Cl 2 ↑湿润的淀粉碘化钾试纸放在管口,变蓝。
(2)①纯铜 Cu 2+ +2e - =Cu ②粗铜Cu- 2e - = Cu 2+
考查电化学的应用。
(1)①根据装置图可知,Y与电源的正极相连,作阳极,X电极和电源的负极相连,作阴极,溶液中的氢离子放电生成氢气,电极反应式是2H + +2e – ="=" H 2 ↑。同时阴极溶液中的水的电离平衡被破坏,所以阴极周围溶液显碱性,溶液呈红色。
②Y电极是阳极,溶液中的氯离子放电,生成氯气,电极反应式是2Cl - -2 e - === Cl 2 ↑。由于氯气具有强氧化性,可以使碘化钾淀粉试纸显蓝色,据此可以鉴别,即湿润的淀粉碘化钾试纸放在管口,变蓝。
(2)①粗铜精炼时,纯铜和电源的负极相连,作阴极,溶液中的铜离子放电,所以X电极是纯铜,电极反应式是Cu 2+ +2 e – = Cu。
②粗铜精炼时,粗铜和电源的正极相连,作阳极,失去电子,所以Y电极是粗铜,电极反应式是Cu-2e - === Cu 2+ 。1年前查看全部
- (6分)电解原理在化学工业上有着广泛的应用。图中电解池a为电解液,X和Y是两块电极板。则:
(6分)电解原理在化学工业上有着广泛的应用。图中电解池a为电解液,X和Y是两块电极板。则:

(1)若X和Y均为惰性电极,a为饱和的NaCI溶液,则电解时检验Y电极反应产物的方法是 。
(2)若X、Y分别为石墨和铁,A乃为饱和的NaCl溶液,则电解过程中生成的白色固体物质露置在空气中,可观察到的现象为 。
(3)若X和Y均为惰性电极,a为一定浓度的硫酸铜溶液,通电一段时间后,向所得溶液中加入0.1 mol Cu(OH) 2 ,恰好恢复电解前的浓度和pH,则电解过程中转移的电子的物质的量为 。 niubin01201年前1
niubin01201年前1 -
 王喜贵 共回答了15个问题
王喜贵 共回答了15个问题 |采纳率73.3%(1)将湿润的淀粉碘化钾试纸靠近Y及支管口,试纸变蓝,说明有氯气生成
(2)白色固体迅速变为灰绿色,最终变为红褐色 (3)0.4 mol
(1)Y是阳极产物,所以Y是氯气,极易氯气可以利用其氧化性,即将湿润的淀粉碘化钾试纸靠近Y及支管口,试纸变蓝,说明有氯气生成。
(2)此时铁是阳极,所以铁失去电子,生成亚铁离子。阴极氢离子放电,从而产生氢氧化钠,进而生成氢氧化亚铁沉淀。氢氧化亚铁不稳定,极易被氧气氧化生成氢氧化铁,所以现象就是白色固体迅速变为灰绿色,最终变为红褐色。
(3)向所得溶液中加入0.1 mol Cu(OH) 2 ,恰好恢复电解前的浓度和pH,说明反应中阴极是铜和氢气,阳极生成氧气,根据原子守恒可知,氧气是0.1mol,所以转移电子是0.1mol×4=0.4mol。1年前查看全部
- 如图所示为用于火灾报警的离子式烟雾传感器原理图,在网罩1内,有电极板2和3,a、b端接电源,4是一块放射性同位素镅241
如图所示为用于火灾报警的离子式烟雾传感器原理图,在网罩1内,有电极板2和3,a、b端接电源,4是一块放射性同位素镅241,它能放射出一种很容易使气体电离的粒子.平时镅放射出来的粒子使两个电极间的空气电离,形成较强的电流,发生火灾时,烟雾进入网罩内,烟的颗粒吸收空气中的离子和镅放射出来的粒子,导致电流变化,报警器检测出这种变化,发出报警.有关这种报警器的下列说法正确的是( ) A.镅放射出来的是α粒子 B.镅放射出来的是β粒子 C.有烟雾时电流减弱 D.有烟雾时电流增强 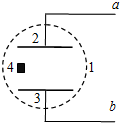
 kelinsiman11年前1
kelinsiman11年前1 -
 sparklinewine 共回答了18个问题
sparklinewine 共回答了18个问题 |采纳率94.4%它在内外电离室里面有放射源镅241,电离产生的正、负离子,在电场的作用下各自向正负电极移动.在正常的情况下,内外电离室的电流、电压都是稳定的.一旦有烟雾窜逃外电离室.干扰了带电粒子的正常运动,电流,电压就会有所改变,破坏了内外电离室之间的平衡,于是无线发射器发出无线报警信号,通知远方的接收主机,将报信息传递警出去.故AC正确,BD错误;
故选AC1年前查看全部
- 电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下
电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题: 
(1)若X、Y都是惰性电极,a是NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
① Y电极上的电极反应式为_____________。在X极附近观察到的现象是__________。
②电解总反应离子方程式为 ______________。
(2)要在铁件的表面镀铜防止铁被腐蚀,则:
① Y电极的材料是_____________(选填纯铁、纯铜或纯锌),电极反应式是__________。电解液a选用___________溶液,电解过程中其浓度____________(选填增大、减小或不变)。
② 若电镀前X、Y两电极的质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12 g,则电镀时电路中通过的电子为____________mol。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因: ________________。 蓝色忧郁于帆1年前1
蓝色忧郁于帆1年前1 -
 afrajiang 共回答了18个问题
afrajiang 共回答了18个问题 |采纳率94.4%1年前查看全部
- 在宽为d两个电极板之间放入宽为d/2的云母片.若云母片的相对介电常数是ξr=7,空气的相对介电常数是ξ0=1.则这两个极
在宽为d两个电极板之间放入宽为d/2的云母片.若云母片的相对介电常数是ξr=7,空气的相对介电常数是ξ0=1.则这两个极板的电容?
 r8vwsb1年前2
r8vwsb1年前2 -
 觉悟不高 共回答了16个问题
觉悟不高 共回答了16个问题 |采纳率100%这是两个串联的电容器
C1=2ε0S/d C2=7C1
1/C=1/C1+1/C2
C=7C1/8=7ε0S/4d=7C'/4
C'是未放云母时的电容.1年前查看全部
- Ⅰ、电解原理在化学工业中有广泛应用.图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.
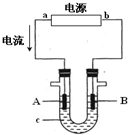 Ⅰ、电解原理在化学工业中有广泛应用.图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.
Ⅰ、电解原理在化学工业中有广泛应用.图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.
(1)若A、B都是惰性电极,c是饱和NaCl溶液,实验开始时,同时向U型管两边各滴入几滴酚酞试液,试判断
①a是______极(填“正”或“负”);
②B电极上的电极反应式为______,
(2)如要用电解方法精炼粗铜,电解液c选用CuSO4溶液,则B电极的材料是______,电极反应式为______.
(3)用惰性电极电解CuSO4溶液.若阴极上析出Cu的质量为3.2g,则阳极上产生的气体在标准状况下的体积为______;
Ⅱ、设计出燃料电池使汽油氧化直接产生电流是对21世纪最富有挑战性的课题之一.最近有人制造了一种燃料电池,一个电极通入空气,另一电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-离子.回答如下问题:
(1)以庚烷(C7H16)代表汽油,这个电池放电时发生的化学反应的化学方程式是:______
(2)这个电池的负极发生的反应是:______;正极发生的反应是:______;固体电解质里的O2-向______(填“正”或“负”)极移动(1分) wuliangnet1年前1
wuliangnet1年前1 -
 道法自然也 共回答了21个问题
道法自然也 共回答了21个问题 |采纳率81%解题思路:Ⅰ、(1)①根据电流的流向是从电源的正极→电解池的阳极来判断电极;②阴极是阳离子的得电子过程;(2)电解精炼铜时,阳极材料是粗铜,阴极材料是纯铜;(3)根据电解时的阴极和阳极反应方程式进行计算;Ⅱ、(1)燃料电池的总反应是燃料在氧气中燃烧的反应;(2)燃料电池的负极反应是燃料失电子的氧化反应,正极是氧气得电子的还原反应,在原电池中,电解质里的阳离子移向正极,阴离子移向负极.Ⅰ、(1)①电流的流向是从电源的正极→电解池的阳极,所以a是正极,故答案为:正;
②和电源的正极a相连的A是电解池的阳极,所以B是电解池的阴极,电极反应为:2H++2e-═H2↑,故答案为:2H++2e-═H2↑;
(2)电解精炼铜时,阳极材料是粗铜,阴极材料是纯铜,B是电解池的阴极,发生铜离子的得电子反应,故答案为:纯铜;Cu2++2e-═Cu;
(3)用惰性电极电解CuSO4溶液,阴极上的电极反应为:Cu2++2e-→Cu,当析出Cu的质量为3.2g,则转移电子0.1mol,阳极上的电极反应为:4OH-→4e-+2H20+O2↑,转移电子0.1mol时,阳极上产生的气体的物质的量是0.025mol,在标准状况下的体积为0.025mol×22.4L/mol=0.56L,故答案为:0.56L;
Ⅱ、(1)燃料电池的总反应是燃料在氧气中燃烧的反应,即C7H16+11O2=7CO2+8H2O,故答案为:C7H16+11O2=7CO2+8H2O;
(2)燃料电池的负极反应是燃料失电子的氧化反应,即C7H16+22O2--44e-=7CO2+8H2O; 正极是氧气得电子的还原反应,即11O2+44e-=22O2-;原电池中电解质里的阴离子移向负极,故答案为:C7H16+22O2--44e-=7CO2+8H2O;11O2+44e-=22O2-;负极.点评:
本题考点: 原电池和电解池的工作原理;铜的电解精炼;电极反应和电池反应方程式;化学电源新型电池.
考点点评: 本题考查学生原电池和电解池的工作原理,要求学生熟记教材知识,学以致用.1年前查看全部
- 电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以
电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题 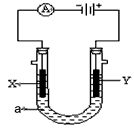
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
电解池中X极上的电极反应式为_______________________。 Y电极上的电极反应式为_______________________,检验该电极反应产物的方法是_______________________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO 4 溶液,则
①X电极的材料是______________,电极反应式是_______________________。
②Y电极的材料是______________,电极反应式是_______________________。 具云水趣1年前1
具云水趣1年前1 -
 杨杨逸晨 共回答了28个问题
杨杨逸晨 共回答了28个问题 |采纳率92.9%(1)2H + +2e - ==H 2 ↑;2Cl - -2e - ==Cl 2 ↑;把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色
(2)①纯铜;Cu 2+ +2e - ==Cu;② 粗铜;Cu-2e - ==Cu 2+1年前查看全部
- (10分)电解原理在化学工业中有广泛的应用。如图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连
(10分)电解原理在化学工业中有广泛的应用。如图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
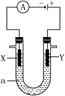
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X电极上的电极反应式为________。在X极附近观察到的现象是________。
②Y电极上的电极反应式为________,检验该电极反应产物的方法是________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO 4 溶液,则
①X电极的材料是________,电极反应式为________________。
②Y电极的材料是________,电极反应式为________________(说明:杂质发生的电极反应不必写出)。 不想在风中1年前1
不想在风中1年前1 -
 主犯不使用 共回答了20个问题
主犯不使用 共回答了20个问题 |采纳率90%(1)①2H + +2e - ====H 2 ↑ 放出气体,溶液变红 ②2Cl - -2e - ====Cl 2 ↑ 把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色
(2)①纯铜 Cu 2+ +2e - ="===Cu " ②粗铜 Cu-2e - ====Cu 2+
X与电源负极相连作阴极(2H + +2e - ====H 2 ↑),放出H 2 ,剩余OH - ,使酚酞试液变红。Y与电源正极相连作阳极(2Cl - -2e - ====Cl 2 ↑),放出Cl 2 ,使湿润的KI淀粉试纸变蓝。电解精炼铜,粗铜作阳极(Cu-2e - ====Cu 2+ ),纯铜作阴极(Cu 2+ +2e - ====Cu)。1年前查看全部
- (7分)电解原理在化学工业中广泛的应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请
(7分)电解原理在化学工业中广泛的应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
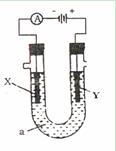
(1)若X、Y都是惰性电极,a是饱和CuSO 4 溶液,实验开始时,同时在两边各滴入石蕊试液,则①Y电极上的电极反应式为
②在Y电极附近观察到的现象是
(2)若X、Y都是铜电极,a是浓度均为2mol·L -1 的AgNO 3 与Cu(NO 3 ) 2 的混合溶液1L,电解一段时间后X电极上有12.8g铜析出,此时直流电源已输出 mol电子。
(3)用石墨电极电解100mLH 2 SO 4 和CuSO 4 混合液,通电一段时间后,两极各出现气体3.36L(标准状况),求原来溶液中CuSO 4 的浓度 。 恋上茉莉清茶1年前1
恋上茉莉清茶1年前1 -
 511500 共回答了9个问题
511500 共回答了9个问题 |采纳率88.9%(1)①4OH - →O 2 + 2H 2 O+ 4 e - (1分)②溶液变红色,产生无色气泡(2分)
(2)2.4(2分)(3)1.50mol/L(2分)
略1年前查看全部
- (10分)电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X,Y是两块电极板,通过导线与直流电源相连。
(10分)电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X,Y是两块电极板,通过导线与直流电源相连。

(1)若X是锌,Y是碳棒电极,a是饱和NaCI溶液,则①该原理可制得化工原料有 ;②Y极的电极反应式为
(2)若要用电解方法精炼粗铜,则①电解液a选用 ;②Y电极反应式是 。(说明:杂质发生的电极反应不必写出)
(3)若要在某铁制小饰品上镀上一层银,则①Y电极的材料是 ;②X电极反应式是 。 fenglinbi1年前1
fenglinbi1年前1 -
 大灰521 共回答了15个问题
大灰521 共回答了15个问题 |采纳率86.7%(1)①氢气、氯气和氢氧化钠(2分)②2Cl - +2e=Cl 2 (2分)
(2)①CuSO 4 溶液(1分) ②Cu-2e - = Cu 2+ (2分)
(3)①银(1分) ②Ag + +e - = Ag(2分)
略1年前查看全部
- 电解原理在化学工业中有广泛应用。下图表示一个电解池, 装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以
电解原理在化学工业中有广泛应用。下图表示一个电解池, 装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题 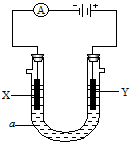
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式是_________________。在X极附近观察到的现象是________________。
②Y电极上的电极反应式是________________,检验该电极反应产物的方法是________________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO 4 溶液,则
①X电极的材料是________________,电极反应式是________________
②Y电极的材料是________________,电极反应式是________________(说明:杂质发生的电极反应不必写出) hoverdream1年前1
hoverdream1年前1 -
 平江不肖生 共回答了14个问题
平江不肖生 共回答了14个问题 |采纳率100%(1)①2H + +2e - ==H 2 ↑;放出气体,溶液变红;②2Cl - -2e - ==Cl 2 ;把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色。
(2)①纯铜;Cu 2+ +2e - ==Cu;②粗铜;Cu-2e - ==Cu 2+1年前查看全部
- 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下
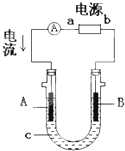 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)如要进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,电解液c选用CuSO4溶液,则:
①A电极的材料是______,电极反应式是______.(说明:杂质发生的电极反应不必写出)
②下列说法正确的是______.
a.电能全部转化为化学能
b.在电解精炼过程中,电解液中伴随有Al3+、Zn2+产生
c.溶液中Cu2+向阳极移动
d.在阳极的底部可回收Ag、Pt、Au等金属
(2)用惰性电极电解CuSO4溶液.若阴极析出Cu的质量为12.8g,则阳极上产生的气体在标准状况下的体积为______L.
(3)利用反应2Cu+O2+2H2SO4═2CuSO4+2H2O可制备CuSO4,若将该反应设计为电解池,其电解质溶液需用______,阳极材料是用______,阴极电极反应式为______. skywalker6191年前1
skywalker6191年前1 -
 水果有益 共回答了26个问题
水果有益 共回答了26个问题 |采纳率76.9%解题思路:(1)①根据电流方向知,a是正极,b是负极,电解精炼中,粗铜作阳极,纯铜作阴极;
②a.电能不能全部转化为化学能;
b.在电解精炼过程中,阳极上金属放电;
c.溶液中Cu2+向阴极移动;
d.在阳极的底部可回收不活泼金属;
(2)根据转移电子相等计算;
(3)该反应不能自发进行,所以只能设计成电解池,失电子的金属作阳极,反应方程式中溶液为电解质溶液,阴极上得电子发生还原反应.(1)①根据电流方向知,a是正极,b是负极,电解精炼中,粗铜作阳极,纯铜作阴极,
A是阳极,则A极材料是粗铜,阳极上铜失电子发生氧化反应,电极反应式为:Cu-2e-=Cu2+,
故答案为:粗铜;Cu-2e-=Cu2+;
②a.电能不能全部转化为化学能,还有部分转化为热能,故错误;
b.在电解精炼过程中,阳极上金属放电,所以电解液中伴随有Al3+、Zn2+产生,故正确;
c.溶液中Cu2+向阴极移动,故错误;
d.在阳极的底部可回收不活泼金属,如Ag、Pt、Au,故正确;
故选bd;
(2)电解硫酸铜溶液时,阳极上氢氧根离子放电,生成1mol氧气需要4mol电子,根据转移电子相等得阳极上产生的气体在标准状况下的体积=
12.6g
64g/mol×2
4×22.4L/mol=2.24L,
故答案为:2.24;
(3)该反应不能自发进行,所以只能设计成电解池,失电子的金属作阳极,反应方程式中溶液为电解质溶液,阴极上得电子发生还原反应,所以若将该反应设计为电解池,其电解质溶液需用稀硫酸,阳极材料是用 铜,阴极电极反应式为O2+4H++4e-=2H2O,
故答案为:硫酸溶液;铜;O2+4H++4e-=2H2O.点评:
本题考点: 电解原理.
考点点评: 本题考查了电解原理,正确判断阴阳极是解本题关键,注意根据转移电子守恒计算阳极上生成气体的体积,为难点.1年前查看全部
- 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X,Y是两块电极板,通过导线与直流电源相连.
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X,Y是两块电极板,通过导线与直流电源相连.
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X,Y是两块电极板,通过导线与直流电源相连.
(1)若X是锌,Y是碳棒电极,a是饱和NaCI溶液,则①该原理可制得化工原料有______;②Y极的电极反应式为______
(2)若要用电解方法精炼粗铜,则①电解液a选用______;②Y电极反应式是______.(说明:杂质发生的电极反应不必写出)
(3)若要在某铁制小饰品上镀上一层银,则①Y电极的材料是______;②X电极反应式是______. myasura1年前1
myasura1年前1 -
 wyjfjha 共回答了14个问题
wyjfjha 共回答了14个问题 |采纳率85.7%解题思路:(1)若X是锌、Y是碳棒,a是氯化钠溶液,阳极上氯离子放电,阴极上氢离子放电;
(2)若要用电解方法精炼粗铜,阳极为粗铜,阴极为纯铜,电解质为可溶性的铜盐,阳极上铜失电子发生氧化反应;
(3)若要在铁上镀银,镀层作阳极,镀件作阴极,电解质为含有与阳极材料相同金属元素的可溶性盐,阴极上银离子得电子发生还原反应.(1)①若X是锌、Y是碳棒,a是氯化钠溶液,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,同时溶液中产生氢氧化钠,则该原理可制得化工原料氢气、氯气和氢氧化钠,故答案为:氢气、氯气和氢氧化钠;
②Y电极上氯离子反应生成氯气,电极反应式为2Cl-+2e=Cl2↑,故答案为:2Cl-+2e=Cl2↑;
(2)①若要用电解方法精炼粗铜,阳极为粗铜,阴极为纯铜,电解质为可溶性的铜盐,如硫酸铜,则a为硫酸铜溶液,故答案为:CuSO4溶液;
②Y电极上铜失电子生成铜离子,电极反应式为:Cu-2e-=Cu2+,故答案为:Cu-2e-=Cu2+;
(3)①若要在铁上镀银,镀层作阳极,镀件作阴极,要想在铁上镀银,则阳极材料是Ag,故答案为:Ag;
②X电极上银离子得电子生成银,电极反应式为Ag++e-=Ag,故答案为:Ag++e-=Ag.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题以电解原理为载体考查了电镀和电解精炼,明确电镀时镀层和镀件分别作哪种电极、电解精炼时混合物和纯净物分别作哪种电极、阳极材料与电解质溶液的关系是解本题关键,难度不大.1年前查看全部
- 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)若X、Y都是惰性电极,a是100mL饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为______.
②Y电极上的电极反应式为______,
③一段时间后,在阴极得到112mL标准状况下的气体,此时溶液的pH为______.
(溶液体积变化忽略不计)
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是______,电极反应式是______.
②Y电极的材料是______,电极反应式是______.(说明:杂质发生的电极反应不必写出) angel_z9891年前1
angel_z9891年前1 -
 xmz138 共回答了14个问题
xmz138 共回答了14个问题 |采纳率100%解题思路:(1)电解饱和食盐水时,由电源可知,X为阴极,Y为阳极,阳极上是氯离子失电子,阴极上是氢离子得电子;(2)根据电解精炼铜的工作原理知识来回答.(1)①和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,
故答案为:2H++2e-=H2↑;
②和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl--2e-=Cl2↑,
故答案为:2Cl--2e-=Cl2↑;
③由2NaOH~H2↑,阴极得到112mL标准状况下的气体,则n(OH-)=[0.112L/22.4L/mol]×2=0.01mol,
c(OH-)=[0.01mol/0.1L]=0.1mol/L,所以pH=13,
故答案为:13;
(2)①电解方法精炼粗铜,电解池的阴极材料是纯铜,电极反应为:Cu2++2e-=Cu,故答案为:纯铜;Cu2++2e-=Cu;
②电解方法精炼粗铜,电解池的阳极材料是粗铜,电极反应为:Cu-2e-=Cu2+,故答案为:粗铜;Cu-2e-=Cu2+.点评:
本题考点: 电解原理.
考点点评: 本题考查学生电解池的工作原理知识,明确图中电源的正负极确定电解池的阴阳极是解答的关键,并熟悉电极反应及离子的放电顺序来解答,题目难度中等.1年前查看全部
- 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请完成以下
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请完成以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请完成以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中化学反应方程式为2H2O+2NaCl
H2↑+Cl2↑+2NaOH通电 .2H2O+2NaCl.在X极附近观察到的现象是______.
H2↑+Cl2↑+2NaOH通电 .
②检验Y电极上反应产物的方法是______.
③当导线中有0.1mol的电子通过时,在标况下理论上两极可收集的气体的体积共______L
(2)如要用电解方法精炼含有少量Zn、Fe、Ag、Au杂质的粗铜,电解液a选用CuSO4溶液,则X电极的材料是______,此电极反应式为______.
(3)若想利用此装置在铁上镀银,则电解液a可以选用______,Y极上的电极反应式为______. 嗲qq1年前1
嗲qq1年前1 -
 E网情迷 共回答了26个问题
E网情迷 共回答了26个问题 |采纳率88.5%解题思路:(1)电解饱和食盐水时,阳极上是氯离子失电子,阴极上是氢离子得电子,氯气能使湿润的碘化钾淀粉试纸变蓝,阳极电子守恒和电极反应计算;(2)根据电解精炼铜的工作原理知识来回答;(3)依据电镀原理分析,镀层做阳极,待镀金属做阴极,含镀层金属离子的盐为电解质溶液.(1)①若X、Y都是惰性电极,a是饱和NaCl溶液,阳极氯离子失电子生成氯气,阴极是溶液中氢离子得到电子生成氢气,反应的化学方程式为:2H2O+2NaCl 通电 . H2↑+Cl2↑+2NaOH;和电源的负极相连的电极X...
点评:
本题考点: 电解原理.
考点点评: 本题考查学生电解池的工作原理知识,主要是电解精炼,电镀原理的分析,电极反应电极判断是解题关键,可以根据所学知识进行回答,难度中等.1年前查看全部
- 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为______.
②Y电极上的电极反应式为______,
③该反应的总反应方程式是:______
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是______,电极反应式是______.
②Y电极的材料是______,电极反应式是______.
(3)若a为CuSO4溶液,则电解时的化学反应方程式为2CuSO4+2H2O
2Cu+O2↑+2H2SO4、2H2O电解 .
O2↑+2H2↑电解 .2CuSO4+2H2O通过一段时间后,向所得溶液中加入0.2molCu(OH)2粉末,恰好恢复电解前的浓度和pH,则电解过程中转移的电子的物质的量为______.
2Cu+O2↑+2H2SO4、2H2O电解 .
O2↑+2H2↑电解 .
(4)若电解含有0.04molCuSO4和0.04molNaCl的混合溶液400ml,当阳极产生的气体672mL(标准状况下)时,溶液的C(H+)=______(假设电解后溶液体积不变). xukunlunshan1年前1
xukunlunshan1年前1 -
 szj_erry 共回答了19个问题
szj_erry 共回答了19个问题 |采纳率84.2%解题思路:(1)电解饱和氯化钠溶液时,由电源可知,X为阴极,Y为阳极,阳极上是氯离子离子失电子,阴极上是氢离子得电子;
(2)根据电解精炼铜的工作原理知识来回答;
(3)若a为CuSO4溶液,则X电极上铜离子放电,当铜离子放电完全后,氢离子再放电;Y电极上氢氧根离子放电;通过一段时间后,向所得溶液中加入0.2molCu(OH)2粉末能使溶液恢复原状,相当于加入0.2molCuO、0.2molH2O,根据氧气和转移电子之间的关系式计算;
(4)若电解含有0.04molCuSO4和0.04molNaCl的混合溶液400ml,阳极上先氯离子放电后氢氧根离子放电,假设阳极上氯离子完全放电,则生成n(Cl2)=[1/2]n(NaCl)=0.02mol,当阳极产生的气体672mL(标准状况下)时,生成气体的物质的量=[0.672L/22.4L/mol]=0.03mol>0.02mol,在阳极上还有氧气生成,生成氧气的物质的量为0.01mol,阳极上转移电子的物质的量=2n(Cl2)+4n(O2)=0.04mol+0.04mol=0.08mol,阴极上铜离子完全放电时转移电子的物质的量=2×0.04mol=0.08mol,所以阴极上氢离子不放电,根据生成氧气的量计算c(H+).(1)①和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,故答案为:2H++2e-=H2↑;②和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl--2e-=Cl...
点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查学生电解池的工作原理知识,明确图中电源的正负极确定电解池的阴阳极是解答的关键,并熟悉电极反应及离子的放电顺序来解答,题目难度中等.1年前查看全部
- 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下
 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则电解池中X极上的电极反应式为______.在X极附近观察到的现象是______.
(2)Y电极上的电极反应式为______,当有4mol电子转移时,产生的气体在
标准状况下的体积是______L
(3)该电解饱和NaCl溶液的总反应式为2Cl-+2H2O
Cl2↑+H2↑+2OH-通电 .2Cl-+2H2O.
Cl2↑+H2↑+2OH-通电 . jhanyu1年前1
jhanyu1年前1 -
 半兽人闯hh 共回答了14个问题
半兽人闯hh 共回答了14个问题 |采纳率92.9%解题思路:(1)若X、Y都是惰性电极,a是饱和NaCl溶液,X电极上氢离子放电,同时X电极附近有氢氧根离子生成,导致溶液呈碱性,无色酚酞试液遇碱液变红色;
(2)Y电极上氯离子放电生成氯气,电极反应式为2Cl--2e-=Cl2↑,根据电极反应计算;
(3)电解氯化钠溶液,产物是氯气、氢气、氢氧化钠.(1)若X、Y都是惰性电极,a是饱和NaCl溶液,X电极上氢离子放电生成氢气,反应为:2H++2e-=H2↑,同时X电极附近有氢氧根离子生成,导致溶液呈碱性,无色酚酞试液遇碱液变红色,所以看到的现象是溶液变红色,
故答案为:2H++2e-=H2↑;放出气体、溶液变红色;
(2)Y电极上氯离子放电生成氯气,电极反应式为2Cl--2e-=Cl2↑,当有4mol电子转移时,产生的气体在标准状况下的体积2×22.4L=44.8L,故答案为:2Cl--2e-=Cl2↑;44.8L;
(3)电解氯化钠溶液,产物是氯气、氢气、氢氧化钠,即2Cl-+2H2O
通电
.
Cl2↑+H2↑+2OH-;
故答案为:2Cl-+2H2O
通电
.
Cl2↑+H2↑+2OH-.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查了电解原理,明确离子放电顺序是解本题关键,会正确书写电极反应式,题目难度不大.1年前查看全部
- 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下
 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下
问题:
(1)若A、B都是惰性电极,c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,则:
①a是______ 极(填“正”或“负”) B极附近溶液呈______性.
②电解池中A极上的电极反应式为______.
(2)如要进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,电解液c选用CuSO4溶液,则:
①A电极的材料是______,B电极反应式是______.
②下列说法正确的是______.
a.电能全部转化为化学能
b.在电解精炼过程中,电解液中伴随有Al3+、Zn2+产生
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(3)用惰性电极电解CuSO4溶液.若阴极析出Cu的质量为12.8g,则阳极上产生的气体在标准状况下的体积为______L.
(4)利用反应2Cu+O2+2H2SO4═2CuSO4+2H2O可制备CuSO4,若将该反应设计为电解池,其电解质溶液需用______,阳极材料是用______,阴极电极反应式______. yang_ymy1年前1
yang_ymy1年前1 -
 琉璃猫22 共回答了22个问题
琉璃猫22 共回答了22个问题 |采纳率81.8%解题思路:(1)①根据电流方向知,a是正极、b是负极,则A是阳极、B是阴极,阴极上氢离子放电,同时阴极附近有氢氧根离子生成,导致溶液碱性增强;
②A电极上氯离子放电生成氯气;
(2)①电解精炼粗铜时,粗铜作阳极、纯铜作阴极,阴极上铜离子放电生成铜;
②a.电能全部转化为化学能、热能等;
b.粗铜中,越活泼的金属越容易失电子;
c.电解质溶液中Cu2+向阴极移动;
d.利用阳极泥可回收Ag、Pt、Au等金属;
(3)阴极析出Cu的质量为12.8g转移电子的物质的量=
×2=0.4mol,根据转移电子相等计算;12.8g 64g/mol
(4)根据电池反应式知,稀硫酸作电解质溶液,阳极是Cu,阴极上氧气得电子发生还原反应.(1)①根据电流方向知,a是正极、b是负极,则A是阳极、B是阴极,阴极上氢离子放电,同时阴极附近有氢氧根离子生成,导致溶液碱性增强,无色酚酞试液遇碱变红色,所以B电极附近溶液呈红色,故答案为:正;碱;
②A电极上氯离子放电生成氯气,电极反应式为2Cl--2 e-═Cl2↑,故答案为:2Cl--2 e-═Cl2↑;
(2)①电解精炼粗铜时,粗铜作阳极、纯铜作阴极,所以A的电极材料是粗铜,阴极上铜离子放电生成铜,
电极反应式为Cu2++2e-═Cu,故答案为:粗铜;Cu2++2e-═Cu;
②a.电能全部转化为化学能、热能等,故错误;
b.粗铜中,越活泼的金属越容易失电子,所以电解液中伴随有Al3+、Zn2+产生,故正确;
c.电解质溶液中Cu2+向阴极移动,硫酸根离子向阳极移动,故错误;
d.阳极上较活泼的金属失电子,导致阳极材料疏松,则Ag、Pt、Au以单质进入电解质溶液中,所以利用阳极泥可回收Ag、Pt、Au等金属,故正确;
故选b、d;
(3)阴极析出Cu的质量为12.8g转移电子的物质的量=
12.8g
64g/mol×2=0.4mol,根据转移电子相等得氧气体积=
0.4mol
4×22.4L/mol=2.24L,故答案为:2.24;
(4)根据电池反应式知,稀硫酸作电解质溶液,阳极是Cu,阴极上氧气得电子发生还原反应,电极反应式为O2+4H++4e-=2H2O,故答案为:H2SO4;Cu;O2+4H++4e-=2H2O.点评:
本题考点: 电解原理.
考点点评: 本题考查了电解原理,涉及电解精炼、物质的量的计算等知识点,明确阴阳极上放电的物质或离子是解本题关键,再结合转移电子相等计算,难点是电极反应式的书写,要结合电解质溶液酸碱性书写,题目难度不大.1年前查看全部
- 铅蓄电池放电,正负两个电极板都会附着硫酸铅沉淀吗
 0--0--91年前1
0--0--91年前1 -
 梦中听涛 共回答了17个问题
梦中听涛 共回答了17个问题 |采纳率76.5%是的,通过化学公式就能得知呀1年前查看全部
- 电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液c;A、B分别是两块电极板,通过导线与直流电源相连.
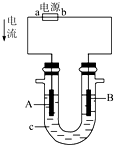 电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液c;A、B分别是两块电极板,通过导线与直流电源相连.
电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液c;A、B分别是两块电极板,通过导线与直流电源相连.
(1)若A、B都是惰性电极,电解质溶液c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞溶液,试判断:
①a是______极(填“正”或“负”),B是______极(填“阴”或“阳”);
②A电极上的电极反应式为______,B电极上的电极反应式为______;
③检验A电极产物的方法是______.
(2)用惰性电极电解CuSO4溶液.若阴极上析出Cu的质量为3.2g,则阳极上产生的气体在标准状况下的体积为______;常温下,若将电解后的溶液稀释至1L,则溶液的pH约为______. tianqibucuo1年前1
tianqibucuo1年前1 -
 bobhmz 共回答了17个问题
bobhmz 共回答了17个问题 |采纳率88.2%解题思路:(1)电解饱和食盐水时,由电流流向可知,A为阳极与电源正极相连,B为阴极与电源负极相连,阳极上是氯离子失电子,阴极上是氢离子得电子;A电极生成的氯气检验方法是利用氯气使湿润的淀粉碘化钾试纸变蓝检验;
(2)根据电解精硫酸铜的电极反应和电子守恒,氢离子守恒分析计算.(1)①由电流流向可知,和电源的正极相连的电极A极是阳极,和电源的负极相连的电极B极是阴极,该a为正极,b为负极.A为阳极,B为阴极,
故答案为:正;阴;
②A电极为阳极,溶液中氯离子发生失电子的氧化反应,即2Cl--2e-=Cl2↑,B电极为电解池的阴极,电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑;
故答案为:2Cl--2e-=Cl2↑;2H++2e-=H2↑;
③检验氯气的方法是用湿润的淀粉碘化钾试纸检验生成的气体,气体能使试纸变蓝色,
故答案为:用湿润的淀粉碘化钾试纸检验生成的气体,气体能使试纸变蓝色;
(2)电解硫酸铜溶液时,阳极上氢氧根离子放电,生成1mol氧气需要4mol电子;生成3.2gCu转移电子数为[3.2g/64g/mol]×2=0.1mol,根据转移电子相等得阳极上产生的气体在标准状况下的体积=[0.1mol/4]×22.4L/mol=0.56L;阴极电极反应:4OH--4e-=2H2O+O2↑,消耗氢氧根离子物质的量,0.1mol,溶液中增加氢离子物质的量为0.1mol,常温下,若将电解后的溶液稀释至1L,溶液中氢离子浓度=[0.1mol/1L]=0.1mol/L,溶液pH=1,
故答案为:0.56L;1.点评:
本题考点: 电解原理.
考点点评: 本题考查学生电解池的工作原理知识,明确图中电源的正负极确定电解池的阴阳极是解答的关键,并熟悉电极反应及离子的放电顺序来解答,题目难度中等.1年前查看全部
- 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下
 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下
问题:
(1)若A、B都是惰性电极,c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,则:
①a是正正 极(填“正”或“负”) B极附近溶液呈碱碱性.
②电解池中A极上的电极反应式为2Cl--2e-═Cl2↑2Cl--2e-═Cl2↑.
(2)如要进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,电解液c选用CuSO4溶液,则:
①A电极的材料是粗铜粗铜,B电极反应式是Cu2++2e-═CuCu2++2e-═Cu.
②下列说法正确的是bdbd.
a.电能全部转化为化学能
b.在电解精炼过程中,电解液中伴随有Al3+、Zn2+产生
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(3)用惰性电极电解CuSO4溶液.若阴极析出Cu的质量为12.8g,则阳极上产生的气体在标准状况下的体积为2.242.24L.
(4)利用反应2Cu+O2+2H2SO4═2CuSO4+2H2O可制备CuSO4,若将该反应设计为电解池,其电解质溶液需用稀硫酸稀硫酸,阳极材料是用CuCu,阴极电极反应式O2+4H++4e-=2H2OO2+4H++4e-=2H2O. cornermen1年前1
cornermen1年前1 -
 茕孑yyw 共回答了15个问题
茕孑yyw 共回答了15个问题 |采纳率66.7%(1)①根据电流方向知,a是正极、b是负极,则A是阳极、B是阴极,阴极上氢离子放电,同时阴极附近有氢氧根离子生成,导致溶液碱性增强,无色酚酞试液遇碱变红色,所以B电极附近溶液呈红色,故答案为:正;碱;
②A电极上氯离子放电生成氯气,电极反应式为2Cl--2 e-═Cl2↑,故答案为:2Cl--2 e-═Cl2↑;
(2)①电解精炼粗铜时,粗铜作阳极、纯铜作阴极,所以A的电极材料是粗铜,阴极上铜离子放电生成铜,
电极反应式为Cu2++2e-═Cu,故答案为:粗铜;Cu2++2e-═Cu;
②a.电能全部转化为化学能、热能等,故错误;
b.粗铜中,越活泼的金属越容易失电子,所以电解液中伴随有Al3+、Zn2+产生,故正确;
c.电解质溶液中Cu2+向阴极移动,硫酸根离子向阳极移动,故错误;
d.阳极上较活泼的金属失电子,导致阳极材料疏松,则Ag、Pt、Au以单质进入电解质溶液中,所以利用阳极泥可回收Ag、Pt、Au等金属,故正确;
故选b、d;
(3)阴极析出Cu的质量为12.8g转移电子的物质的量=
12.8g
64g/mol×2=0.4mol,根据转移电子相等得氧气体积=
0.4mol
4×22.4L/mol=2.24L,故答案为:2.24;
(4)根据电池反应式知,稀硫酸作电解质溶液,阳极是Cu,阴极上氧气得电子发生还原反应,电极反应式为O2+4H++4e-=2H2O,故答案为:H2SO4;Cu;O2+4H++4e-=2H2O.1年前查看全部
- 电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.
电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.
请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为______,在X极附近观察到的现象是______.
电解液中向X极方向移动的离子是______.
②Y电极上的电极反应式为______.
(2)如要用电解方法精炼粗铜,电解液a选用CuSO 4 溶液,则:
①X电极的材料是______.
②Y电极的电极反应式为______.(说明:杂质发生的反应不必写出)
③溶液中的c(Cu 2+ )与电解前相比______(填“变大”、“变小”或“不变”).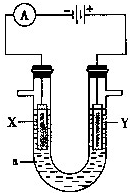
 L柒八zao1年前1
L柒八zao1年前1 -
 superzhu 共回答了21个问题
superzhu 共回答了21个问题 |采纳率85.7%(1)①和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H + +2e - =H 2 ↑,所以该电极附近氢氧根浓度增大,碱性增强,滴入几滴酚酞试液会变红,
故答案为:2H + +2e - =H 2 ↑或2H 2 O+2e-=H 2 +2OH - ;放出气体,溶液变红;
②和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl - -2e - =Cl 2 ↑,故答案为:2Cl - -2e - =Cl 2 ↑;
(2)①电解方法精炼粗铜,电解池的阴极材料是纯铜,电极反应为:Cu 2+ +2e - =Cu,故答案为:精铜;
②电解方法精炼粗铜,电解池的阳极材料是粗铜,电极反应为:Cu-2e - =Cu 2+ ,故答案为:粗铜;Cu-2e - =Cu 2+ ;
③粗铜做阳极,其中的杂质锌、镍等也会失电子,所以依据电子守恒,阴极析出的铜比阳极溶解的铜多,溶液中铜离子浓度减小,故答案为:变小.1年前查看全部
- 想不明白为什么放电时,电荷从正极板移向负极板,电荷量会减少,不是电荷仍在电极板上吗
 oxylin1年前3
oxylin1年前3 -
 小风飕飕 共回答了18个问题
小风飕飕 共回答了18个问题 |采纳率88.9%所谓充电,并不是往里面灌入电荷,而是让系统中原有的正负电荷彼此分离,同样,放电则是正负电荷的中和,我们所说的电量是指分离后的正电荷或者负电荷的量,放电的时候正负电荷都是减少的1年前查看全部
大家在问
- 1有三个质量都为m的小球a b c在同一位置将a竖直上抛 将b水平抛出 让c自由下落 运动了相同的时间 则:(不计空气阻力
- 2对于某些特殊形式的三元一次方程,若先求出x+y+z的值,再用整体相加减法求解,怎样解下面的方程组比较方便
- 31、有一个棱长为40cm的正方体零件,它的上下两个面的正中间各有一个直径为4cm的圆孔,孔深为10cm,求这个零件的表面
- 4关于英语中P、K、T读音我想知道一下,P、K、T这个三音除了在S后面要读B、G、D,在K、X后面接P、K、T是不是也读成
- 5“蛇鼠一窝”怎么解释?
- 6一片普通的槐树叶,在作者看来却是全世界最美的一片,精心保存,为什么
- 7英语翻译The Florida State Attorney has offered Bieber the chance
- 8用恰当的关联词语,将下面三个短句组合成一个复句。(句序合理,语意贯通;可以删去和调换词语,但不得改变原意)
- 9数学方程问题,很简单现有面值为5元和2元的人民币32涨,共计100元 问两种人民币各有多少张?今天脑子坏了 想不出来了
- 10is some one smoking变成陈述句
- 11The ___(short) of water is serious.
- 12这个故事和孩子们的饮食习惯有关 英语翻译
- 13田老师讲课能给我留下深刻的印象,并且影响到我今后的发展
- 14阅读说明文《蜂鸟》,完成文后小题。(10分)
- 15(2012•鼓楼区一模)某型号小轿车的小轿车的质量是600kg,额定功率为40kW,轮胎与地面的接触总面积2000cm2



