电极极化解释
 离不开-你2022-10-04 11:39:541条回答
离不开-你2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 kabuqinuo1 共回答了20个问题
kabuqinuo1 共回答了20个问题 |采纳率100%- 当有外电场作用时,相对平衡的电极电位数值将发生变化.通常把在—定电流作用下的电极电位与相对平衡的电极电位的差值,称为电极极化.
- 1年前
相关推荐
- 甲烷燃料电池电极方程
 ft6354861年前2
ft6354861年前2 -
 霜竹 共回答了14个问题
霜竹 共回答了14个问题 |采纳率100%碱性介质下的甲烷燃料电池
负极:CH4+10OH - - 8e-===CO32- +7H2O
正极:2O2+8e-+4H2O===8OH-
离子方程式为:CH4+2O2+2OH-===CO32-+3H2O
总反应方程式为:CH4+2O2+2KOH===K2CO3+3H2O
酸性介质下的甲烷燃料电池:
负极:CH4-8e-+2H2O===CO2+8H+
正极:2O2+8e-+8H+===4H2O
总反应方程式为:2O2+CH4===2H2O+CO21年前查看全部
- 电极电势问题
电极电势问题
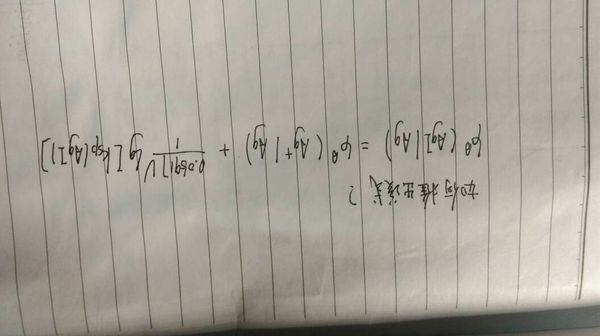
 linna8191年前1
linna8191年前1 -
 wanxixi 共回答了19个问题
wanxixi 共回答了19个问题 |采纳率84.2%AgI | Ag 电极的电势相当于 Ag+ |Ag 电极的电势.只是Ag+的浓度不是1.
这样你给出浓度即可.
最后的结果是你写的那个式子1年前查看全部
- 电极电势问题如图6.9
 单身的贵猪1年前1
单身的贵猪1年前1 -
 江山1977 共回答了12个问题
江山1977 共回答了12个问题 |采纳率66.7%正极反应:AgBr(s) + e = Ag + Br-
负极反应:Ag - e = Ag+
电池反应:AgBr(s) = Ag+ + Br-
lg Ksp = n(正极电极电势 - 负极电极电势)/0.0592
= 1*(0.0713 -0.7996)/0.0592
Ksp = 4.98 *10^-131年前查看全部
- 阳极电极电势如何计算?如何降低阳极电极电势?
 njce1年前1
njce1年前1 -
 sophia927 共回答了22个问题
sophia927 共回答了22个问题 |采纳率90.9%氧化态的化学电势减去还原态的化学电势,
降低氧化态的浓度等1年前查看全部
- 已知电极反应:(Cr2O7)2-+6e+14H+==== 2Cr3++7H2O,φθ=1.23V,
已知电极反应:(Cr2O7)2-+6e+14H+==== 2Cr3++7H2O,φθ=1.23V,
设[(Cr2O7)2-]=[ Cr3+]=1.0mol/l,问电极电势为:
在PH=1时, xinquan8281年前2
xinquan8281年前2 -
 搜狐快发钱 共回答了26个问题
搜狐快发钱 共回答了26个问题 |采纳率96.2%用nerst方程
E=E0-(RT/nF)ln([Cr3+]^2/[(Cr2O7)2][H+]^14)
E0=1.23V
[Cr3+]=1mol/L
[(Cr2O7)2]=1mol/L
[H+]=0.1mol/L
经计算得
+1.092V1年前查看全部
大家在问
- 1磨宝石用英语怎么说
- 2直线y=2x+b与函数y=e的x次方+x的图像的某一切线重合则b=?
- 3<<饮湖上初晴后雨>>主要描写__表达了诗人__
- 4在函数y=2的x次方的图象上求一点,使过此点的切线满足下列条件:平行于直线xIn4-y+3=0
- 5一个大圆有3个大小不等的小圆,这些小圆的圆心在大圆的同一条直径上,已知小圆的圆心在大圆的同一条直径
- 6一个残疾人面对困境不低头的文章,起个什么题目好呢
- 7(数学)选择,要写出列式.
- 8“如果物体的速度发生变化,则物体受到的合外力的冲量一定不为零”这句话对吗?
- 9教师节是几月几号,往 一 的反义词
- 10模仿"金秋中,瞻读你的美丽"的诗.六点半前完成有财富给
- 11带月字的反义词成语
- 12筷子提米实验实验目的
- 13求第三秒末的瞬时速度,时间t到底是3还是4
- 14直线运动的质点,第一秒内10的速度匀速运动,第二秒内,7的速度运动.第二秒末瞬时速度多少?这三秒内...
- 15一桶油第一次用去20%,第二次比第一次多用去20千克还剩下22千克.
