中学实验室制18种气体的化学方程式和方法
 yuzhongni2022-10-04 11:39:541条回答
yuzhongni2022-10-04 11:39:541条回答以及要注意的要点

已提交,审核后显示!提交回复
共1条回复
 我dd了 共回答了15个问题
我dd了 共回答了15个问题 |采纳率100%- 1,常见气体的制取和检验
⑴氧气
制取原理——含氧化合物自身分解
制取方程式——2KClO3 2KCl+3O2↑
装置——略微向下倾斜的大试管,加热
检验——带火星木条,复燃
收集——排水法或向上排气法
⑵氢气
制取原理——活泼金属与弱氧化性酸的置换
制取方程式——Zn+H2SO4 === H2SO4+H2↑
装置——启普发生器
检验——点燃,淡蓝色火焰,在容器壁上有水珠
收集——排水法或向下排气法
⑶氯气
制取原理——强氧化剂氧化含氧化合物
制取方程式——MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
装置——分液漏斗,圆底烧瓶,加热
检验——能使湿润的蓝色石蕊试纸先变红后褪色;
除杂质——先通入饱和食盐水(除HCl),再通入浓H2SO4(除水蒸气)
收集——排饱和食盐水法或向上排气法
尾气回收——Cl2+2NaOH=== NaCl+NaClO+H2O
⑷硫化氢
①制取原理——强酸与强碱的复分解反应
②制取方程式——FeS+2HCl=== FeCl2+H2S↑
③装置——启普发生器
④检验——能使湿润的醋酸铅试纸变黑
⑤除杂质——先通入饱和NaHS溶液(除HCl),再通入固体CaCl2(或P2O5)(除水蒸气)
⑥收集——向上排气法
⑦尾气回收——H2S+2NaOH=== Na2S+H2O或H2S+NaOH=== NaHS+H2O
⑸二氧化硫
①制取原理——稳定性强酸与不稳定性弱酸盐的复分解
②制取方程式——Na2SO3+H2SO4=== Na2SO4+SO2↑+H2O
③装置——分液漏斗,圆底烧瓶
④检验——先通入品红试液,褪色,后加热又恢复原红色;
⑤除杂质——通入浓H2SO4(除水蒸气)
⑥收集——向上排气法
⑦尾气回收——SO2+2NaOH=== Na2SO3+H2O
⑹二氧化碳
①制取原理——稳定性强酸与不稳定性弱酸盐的复分解
②制取方程式——CaCO3+2HClCaCl2+CO2↑+H2O
③装置——启普发生器
④检验——通入澄清石灰水,变浑浊
⑤除杂质——通入饱和NaHCO3溶液(除HCl),再通入浓H2SO4(除水蒸气)
⑥收集——排水法或向上排气法
⑺氨气
①制取原理——固体铵盐与固体强碱的复分解
②制取方程式——Ca(OH)2+2NH4ClCaCl2+NH3↑+2H2O
③装置——略微向下倾斜的大试管,加热
④检验——湿润的红色石蕊试纸,变蓝
⑤除杂质——通入碱石灰(除水蒸气)
收集——向下排气法
⑻氯化氢
①制取原理——高沸点酸与金属氯化物的复分解
②制取方程式——NaCl+H2SO4Na2SO4+2HCl↑
③装置——分液漏斗,圆底烧瓶,加热
④检验——通入AgNO3溶液,产生白色沉淀,再加稀HNO3沉淀不溶
⑤除杂质——通入浓硫酸(除水蒸气)
⑥收集——向上排气法
⑼二氧化氮
①制取原理——不活泼金属与浓硝酸的氧化—还原;
②制取方程式——Cu+4HNO3===Cu(NO3)2+2NO2↑+2H2O
③装置——分液漏斗,圆底烧瓶(或用大试管,锥形瓶)
④检验——红棕色气体,通入AgNO3溶液颜色变浅,但无沉淀生成
⑤收集——向上排气法
⑥尾气处理——3NO2+H2O===2HNO3+NO
NO+NO2+2NaOH===2NaNO2+H2O
⑩一氧化氮
①制取原理——不活泼金属与稀硝酸的氧化—还原;
②制取方程式——Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O
③装置——分液漏斗,圆底烧瓶(或用大试管,锥形瓶)
④检验——无色气体,暴露于空气中立即变红棕色
⑤收集——排水法
⑾一氧化碳
①制取原理——浓硫酸对有机物的脱水作用
②制取方程式——HCOOHCO↑+H2O
③装置——分液漏斗,圆底烧瓶
④检验——燃烧,蓝色火焰,无水珠,产生气体能使澄清石灰水变浑浊
⑤除杂质——通入浓硫酸(除水蒸气)
⑥收集——排水法
⑿甲烷
①制取方程式——CH3COONa+NaOH CH4↑+Na2CO3
②装置——略微向下倾斜的大试管,加热
③收集——排水法或向下排空气法
⒀乙烯
①制取原理——浓硫酸对有机物的脱水作用
②制取方程式——CH3CH2OH CH2=CH2↑+H2O
③装置——分液漏斗,圆底烧瓶,加热
④除杂质——通入NaOH溶液(除SO2,CO2),通入浓硫酸(除水蒸气)
收集——排水法
⒁乙炔
①制取原理——电石强烈吸水作用
②制取方程式——CaC2+2H2OCa(OH)2+CH CH↑
③装置——分液漏斗,圆底烧瓶(或用大试管,锥形瓶)
④检验——无色气体,能燃烧,产生明亮的火焰,并冒出浓的黑烟
⑤除杂质——通入硫酸铜溶液(除H2S,PH3),通入浓硫酸(除水蒸气)
收集——排水法或向下排气法 - 1年前
相关推荐
- 1、(填空题)中学实验室常用的电流表和电压表都是磁电式仪表,当表内电路中通有电流的时,他们的指针会发生偏转,可以猜想这些
1、(填空题)中学实验室常用的电流表和电压表都是磁电式仪表,当表内电路中通有电流的时,他们的指针会发生偏转,可以猜想这些仪表里面除了导线和指针外,还有一定的 ,你所依据的原理是
 jiapangdun1年前4
jiapangdun1年前4 -
 笨笨爱阿童木 共回答了25个问题
笨笨爱阿童木 共回答了25个问题 |采纳率92%还要有线圈或是电磁铁也可以.原理是电流的磁效应.
电流表我拆开看过,里面没有磁体.1年前查看全部
- (2014?遂平县二模)如图所示为我们中学实验室常用的电压表,它是一种磁电式仪表,当表内有电流通过时,
(2014?遂平县二模)如图所示为我们中学实验室常用的电压表,它是一种磁电式仪表,当表内有电流通过时,
 (2014?遂平县二模)如图所示为我们中学实验室常用的电压表,它是一种磁电式仪表,当表内有电流通过时,它的指针会发生偏转.由此现象,可以猜想电压表里面除了导线和指针外,还一定有______,你依据的原理是______.
(2014?遂平县二模)如图所示为我们中学实验室常用的电压表,它是一种磁电式仪表,当表内有电流通过时,它的指针会发生偏转.由此现象,可以猜想电压表里面除了导线和指针外,还一定有______,你依据的原理是______.
 fjfqzz1年前1
fjfqzz1年前1 -
 biaobiao31984 共回答了12个问题
biaobiao31984 共回答了12个问题 |采纳率75%电压表是一种磁电式仪表,当表内有电流通过时,它的指针会发生偏转,说明肯定是受到了力的作用,并且是受电流的影响产生了这个力,我们会想到通电导体在磁场中会受到力的作用,所以这些仪表里还一定有磁体.
故答案为:磁体,通电导体在磁场中受力运动.1年前查看全部
- 中学实验室用下图装置制取少量溴苯,请填写下列空白。 (1)在烧瓶a中装的试剂是苯、液溴和铁屑,导管b的作用有两个:一是导
中学实验室用下图装置制取少量溴苯,请填写下列空白。 
(1)在烧瓶a中装的试剂是苯、液溴和铁屑,导管b的作用有两个:一是导气,二是兼起________的作用。
(2)反应过程中在导管c的下口附近可以观察到有白雾出现,这是由于反应生成的__________遇水蒸气形成的。
(3)反应完毕后,向锥形瓶d中滴入AgNO 3 溶液,有________________ 生成。
(4)反应完毕后,将烧瓶a中的液体倒人盛有冷水的烧杯里,可以观察到烧杯底部有_____________色不溶于水的液体,这是溶解了_______________的溴苯的粗产品。
(5)写出烧瓶a中发生反应的化学方程式:________________________________。
(6)提纯粗溴苯的方法是_____________ ,纯净的溴苯是_________色,密度比水_________(填 “小”或“大”)的油状液体。 小小锋儿21年前1
小小锋儿21年前1 -
 yetties 共回答了16个问题
yetties 共回答了16个问题 |采纳率81.3%1年前查看全部
- 小明所在学习小组,用中学实验室常见器材设计了如图所 示的装置来验证机械能守恒定律。图中a、b为两重物,用轻绳相连,b 的
小明所在学习小组,用中学实验室常见器材设计了如图所 示的装置来验证机械能守恒定律。图中a、b为两重物,用轻绳相连,b 的质量大于a的质量,滑轮为轻质光滑滑轮。实验时从图示位置静止释放 b,b下降且落到桌面后不再反弹,a上升但不与滑轮相碰。小明的学习小 组已测量了a上升的总高度h 1 ,要研究b从下落到刚要与桌面相碰这一过 程中,a、b组成系统的机械能是否守恒,他们还需要测量的物理量有:______、______、______。(填被测的三个物理量,及表示这三个物理量的字母若表达式______成立(用设定的字母表示),即可验证机械能守恒定律成立。

 jyknick1年前1
jyknick1年前1 -
 夜交藤 共回答了23个问题
夜交藤 共回答了23个问题 |采纳率73.9%1年前查看全部
- [高一化学]利用下列方法,可以在中学实验室里从空气中制取氮气的是:
[高一化学]利用下列方法,可以在中学实验室里从空气中制取氮气的是:
利用下列方法,可以在中学实验室里从空气中制取氮气的是:
A.把空气液化
B.把空气缓缓通过加热了的铜网
C.把空气缓缓通过加热了的镁网
D.把空气通过装有氢氧化钠的洗气瓶
为什么? yumeng201年前1
yumeng201年前1 -
 pengnankai840801 共回答了16个问题
pengnankai840801 共回答了16个问题 |采纳率93.8%A项在中学实验室无法完成;B项可以除去氧气,剩余的可以认为都是氮气,因为其含量很高;C项中,镁可以与氮气反应生成化合物,比如:Mg3N4等;D项不能除去氧气,达不到目的.故选B.1年前查看全部
- 中学实验室可用同一种装置制备不同的气体,若只有右图装置制备气体
中学实验室可用同一种装置制备不同的气体,若只有右图装置制备气体

(1)请在下表空格中填上所需药品
(2)写出表中药品制备O 2 的化学方程式所制气体 药品 分液漏斗内 烧瓶中 O 2 MnO 2 H 2 稀H 2 SO 4 Cl 2 浓HCl MnO 2 SO 2 浓H 2 SO 4 Na 2 SO 3 CO 2 稀H 2 SO 4 石灰石
。
(3)表中给全药品的项目中,不能用于制备相应气体的有(可不填满)
①气体 ,理由 。
②气体 ,理由 。
③气体 ,理由 。 山麓睿智1年前1
山麓睿智1年前1 -
 我在听海 共回答了28个问题
我在听海 共回答了28个问题 |采纳率92.9%1年前查看全部
- 今天是某附属中学实验室的开放日,初三七班的同学来到实验室,实验室的桌上摆放有如图所示的仪器:
今天是某附属中学实验室的开放日,初三七班的同学来到实验室,实验室的桌上摆放有如图所示的仪器:

(1)班长让同学完成的第一个任务是写出仪器的名称,同学们完成任务的情况如图所示,其中名称有错误的是______(填序号).
(2)用高锰酸钾制取氧气还需要的玻璃仪器是______.
(3)某同学想用如图所示制取CO2,班长指出这需要太多的稀盐酸才能淹没漏斗的下管口,起到液封的作用.有位同学选用了上面的一种仪器,加在如图g装置上,既解决了液封的问题,又可以减少酸的用量,请把仪器画在图中应该放置的位置. qingwaxxwz1年前1
qingwaxxwz1年前1 -
 所得瓦房店 共回答了17个问题
所得瓦房店 共回答了17个问题 |采纳率88.2%解题思路:(1)要熟悉各种仪器的名称、用途和使用方法;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
(3)不同的实验装置,功能不同.(1)f是集气瓶,常用来收集气体.
故填:f.
(2)用高锰酸钾制取氧气需要的玻璃仪器有试管、水槽、导管、集气瓶、酒精灯等.
故填:酒精灯.
(3)可以把试管放在漏斗的下方,既解决了液封的问题,又可以减少酸的用量,试管在图中放置的位置如下图所示:
点评:
本题考点: 氧气的制取装置;氧气的收集方法;二氧化碳的实验室制法.
考点点评: g装置中,为了形成液封、节约液体药品,也可以把漏斗换成长颈漏斗,为了节约液体药品,控制反应速率,也可以把漏斗换成分液漏斗或注射器等.1年前查看全部
- 某学生进行实验需要90mL 2.00mol•L-1的NaOH溶液,该生利用中学实验室条件进行溶液配制,试回答下
某学生进行实验需要90mL 2.00mol•L-1的NaOH溶液,该生利用中学实验室条件进行溶液配制,试回答下列各题:
(1)下列仪器中,必须用到的是______
A.锥形瓶 B.200mL容量瓶C.量筒D.胶头滴管
E.100mL容量瓶F.天平
(2)该生需要称量的Na0H固体质量为______;若要实施配制,除上述仪器外,还缺少的仪器是______.
(3)容量瓶上除有刻度线和规格(或容积)外还应标有______,在使用前必须的操作是______.
(4)如图所示,下列实验操作与方法正确的是:______
(5)配制完毕后,教师指出有部分同学进行了下列某一项错误操作,你认为这些操作会导致所得溶液浓度偏高的是______
A.容量瓶使用前经蒸馏水清洗后没有干燥
B.将溶解后的溶液立即转入容量瓶
C.洗涤烧杯和玻璃棒的溶液倒入水槽中
D.反复倒转摇匀后,液面低于刻度线,再加蒸馏水至刻度线
E.定容时俯视容量瓶刻度线
F.定容时仰视容量瓶刻度线. guanzhong_daoke1年前1
guanzhong_daoke1年前1 -
 流年暄寂 共回答了14个问题
流年暄寂 共回答了14个问题 |采纳率100%解题思路:(1)配制90mL溶液,需要选用100mL容量瓶,根据配制100mL 2.00mol•L-1的NaOH溶液步骤选择使用的仪器;
(2)根据100mL 2.00mol•L-1的NaOH溶液中含有溶质氢氧化钠的物质的量计算出质量;根据已有的仪器选择分析还缺少的仪器;
(3)根据容量瓶的构造进行解答;根据容量瓶的构造分析所以前必须的操作;
(4)根据摇匀溶液方法、给试管中液体加热、胶头滴管使用方法、过滤操作方法进行判断;
(5)根据c=[n/V]可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量n和溶液的体积V引起的,误差分析时,关键要看配制过程中引起n和V怎样的变化,若n比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若n比理论值大,或V比理论值小时,都会使所配溶液浓度偏大.(1)实验室没有90mL容量瓶,所以应该选用100mL容量瓶配制溶液,配制100mL 2.00mol•L-1的NaOH溶液使用的仪器有:托盘天平、药匙、玻璃棒、烧杯、100mL容量瓶、胶头滴管等,所以使用的仪器有:D.胶头滴管E.100mL容量瓶 F.天平,
故答案为:DEF;
(2)100mL 2.00mol•L-1的NaOH溶液中含有氢氧化钠的物质的量为:2.00mol•L-1×0.1L=0.2mol,需要氢氧化钠的质量为:40g/mol×0.2mol=8.0g;以上仪器中还缺少的仪器为:玻璃棒、烧杯,
故答案为:8.0g;玻璃棒、烧杯;
(3)容量瓶上标有容积、刻度线、温度;容量瓶上有瓶塞,使用容量瓶时必须检查是否漏水,
故答案为:温度; 检漏;
(4)A.分液漏斗使用前需检验是否漏水,检查时一手托住瓶底,另一只手摁住瓶塞,倒转检查,故A正确;
B.用试管加热液体时,液体不能超过试管容积的[1/3],且用拇指顶住试管夹短柄,故B错误;
C.用胶头滴管滴加液体时不能将胶头滴管插入到试管内部,故C错误;
D.过滤时漏斗下端应紧贴烧杯内壁,故D错误;
故选A.
(5)A.容量瓶使用前经蒸馏水清洗后没有干燥,对配制的溶液体积和溶质的物质的量都没有影响,根据c=[n/V]可得,不影响配制结果,故A错误;
B.将溶解后的溶液立即转入容量瓶,热的溶液体积偏大,冷却后体积变小,导致配制的溶液体积偏小,根据c=[n/V]可得,溶液浓度偏高,故B正确;
C.洗涤烧杯和玻璃棒的溶液倒入水槽中,导致配制的溶液中溶质的物质的量减小,根据c=[n/V]可得,配制的溶液浓度偏低,故C错误;
D.反复倒转摇匀后,液面低于刻度线,再加蒸馏水至刻度线,导致加入的蒸馏水体积偏大,根据c=[n/V]可得,配制的溶液浓度偏低,故D错误;
E.定容时俯视容量瓶刻度线,导致加入的蒸馏水体积偏小,根据c=[n/V]可得,配制的溶液浓度偏高,故E正确;
F.定容时仰视容量瓶刻度线,导致加入的蒸馏水体积偏大,根据c=[n/V]可得,配制的溶液体积偏低,故F错误;
故选BE.点评:
本题考点: 配制一定物质的量浓度的溶液.
考点点评: 本题考查了配制一定物质的量浓度的溶液的方法,该题是中等难度的试题,试题基础性强,贴近高考;该题难易适中,注重灵活性,侧重对学生能力的培养和解题方法的指导和训练,有利于培养学生的逻辑思维能力和严谨的规范实验操作能力;该题的难点在于误差分析,注意掌握误差分析的方法和技巧.1年前查看全部
- (2014•遂平县二模)如图所示为我们中学实验室常用的电压表,它是一种磁电式仪表,当表内有电流通过时,它的指针会发生偏转
 (2014•遂平县二模)如图所示为我们中学实验室常用的电压表,它是一种磁电式仪表,当表内有电流通过时,它的指针会发生偏转.由此现象,可以猜想电压表里面除了导线和指针外,还一定有______,你依据的原理是______.
(2014•遂平县二模)如图所示为我们中学实验室常用的电压表,它是一种磁电式仪表,当表内有电流通过时,它的指针会发生偏转.由此现象,可以猜想电压表里面除了导线和指针外,还一定有______,你依据的原理是______.  小猪喔喔1年前1
小猪喔喔1年前1 -
 万hh咸宁 共回答了25个问题
万hh咸宁 共回答了25个问题 |采纳率92%解题思路:解题的关键是要掌握:通电导体在磁场中会受到力的作用.电压表是一种磁电式仪表,当表内有电流通过时,它的指针会发生偏转,说明肯定是受到了力的作用,并且是受电流的影响产生了这个力,我们会想到通电导体在磁场中会受到力的作用,所以这些仪表里还一定有磁体.
故答案为:磁体,通电导体在磁场中受力运动.点评:
本题考点: 磁场对通电导线的作用.
考点点评: 本题考查了学生对“通电导体在磁场中受力运动”的理解和灵活运用,要求学生对本知识点充分理解熟练掌握才行.1年前查看全部
- 北半球地磁场的竖直分量向下.如图所示,在北京某中学实验室的水平桌面上,放置边长为L的正方形闭合导体线圈abcd,线圈的a
北半球地磁场的竖直分量向下.如图所示,在北京某中学实验室的水平桌面上,放置边长为L的正方形闭合导体线圈abcd,线圈的ab边沿南北方向,ad边沿东西方向.下列说法中正确的是( )
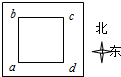 A. 若使线圈向东平动,则a点的电势比b点的电势低
A. 若使线圈向东平动,则a点的电势比b点的电势低
B. 若使线圈向北平动,则a点的电势比b点的电势低
C. 若以ab为轴将线圈向上翻转,则线圈中感应电流方向为a→b→c→d→a
D. 若以ab为轴将线圈向上翻转,则线圈中感应电流方向为a→d→c→b→a jstones1年前1
jstones1年前1 -
 zhup23 共回答了16个问题
zhup23 共回答了16个问题 |采纳率100%解题思路:根据楞次定律判断出感应电流的方向,从而判断出电势的高低.A、线圈向东平动时,ba和cd两边切割磁感线,且两边切割磁感线产生的感应电动势大小相同,根据右手定则知,a点的电势比b点的电势低.故A正确.
B、向北平动时,bc和ad两边切割磁感线,且两边切割磁感线产生的感应电动势大小相同,a、b两点的电势相等.故B错误.
C、若以ab为轴将线圈向上翻转,向下的磁通量减小量,感应电流的磁场方向应该向下,则感应电流的方向为a→b→c→d→a.故C正确,D错误.
故选AC.点评:
本题考点: 楞次定律.
考点点评: 解决本题的关键掌握楞次定律判断感应电流的方向,以及会通过右手定则判断电势的高低.1年前查看全部
- (2014•大连二模)在大连某中学实验室的水平桌面上,放置一矩形闭合导体线圈,如图所示,线圈的ab边沿南北方向,ad边沿
 (2014•大连二模)在大连某中学实验室的水平桌面上,放置一矩形闭合导体线圈,如图所示,线圈的ab边沿南北方向,ad边沿东西方向.仅考虑地磁场的影响,下列说法中正确的是( )
(2014•大连二模)在大连某中学实验室的水平桌面上,放置一矩形闭合导体线圈,如图所示,线圈的ab边沿南北方向,ad边沿东西方向.仅考虑地磁场的影响,下列说法中正确的是( )
A.若使线圈向东平动,则a点的电势比b点的电势高
B.若使线圈向东平动,则a点的电势与b点的电势相等
C.若以bc为轴将线圈向上翻转90°过程中,则线圈中感应电流方向为abcda
D.若以bc为轴将线圈向上翻转90°过程中,则线圈中感应电流方向为adcba hanyuhu1年前1
hanyuhu1年前1 -
 wxts1981 共回答了11个问题
wxts1981 共回答了11个问题 |采纳率100%解题思路:根据地磁场的分布,结合楞次定律,可确定感应电流的方向,从而确定电势的高低,即可求解.A、若使线圈向东平动,由地磁场的磁感线是地理南极指向北极,则穿过线圈的磁通量不变,因此线圈中没有感应电动势,故AB错误;
C、若以bc为轴将线圈向上翻转90°过程中,则穿过线圈的磁通量在减小,且向下磁场,根据楞次定律可知,线圈中感应电流方向为abcda,故C正确,D错误;
故选:C.点评:
本题考点: 法拉第电磁感应定律;楞次定律.
考点点评: 考查地磁场的分布,掌握楞次定律的应用,注意“增反减同”的理解.1年前查看全部
- 中学实验室用如图所示装置制取少量溴苯。请填写下列空白。
中学实验室用如图所示装置制取少量溴苯。请填写下列空白。

(1)在烧瓶a中装的试剂是苯、溴和铁屑。导管b的作用有两个:一是导气,二是兼起__________的作用。
(2)反应过程中在导管c的下口附近可以观察到白雾出现,这是由于反应生成的________遇水蒸气而形成的。
(3)反应完毕后,向锥形瓶d中滴入AgNO 3 溶液,有__________生成。
(4)反应完毕后,将烧瓶a中的液体倒入盛有冷水的烧杯里,可以观察到烧杯底部有__________色不溶于水的液体。这是溶解了__________的粗溴苯。
(5)写出烧瓶a中发生反应的化学方程式:__________________________________。 zuihui1271年前1
zuihui1271年前1 -
 我是小猪我怕 共回答了18个问题
我是小猪我怕 共回答了18个问题 |采纳率94.4%1年前查看全部
- 如何测定室温下水的饱和蒸气压?摄氏0度冰的蒸气压?(中学实验室条件)
 superbigww1年前2
superbigww1年前2 -
 nanjind 共回答了13个问题
nanjind 共回答了13个问题 |采纳率100%取一个水银气压计(托里拆里管),读出水银柱高度,
例如是760mmHg.用玻璃滴管吸取一小滴水,将滴管口伸到
水银槽内,将水挤入托里拆里管,水滴浮到水银面上,水
银柱受到水蒸气的压力高度下降.下降的高度(例如17.5
mmHg)就是这个温度下水的饱和蒸气压.1年前查看全部
大家在问
- 1语文五年级下册第三课只拣儿童可分几段
- 259 59 58 55 48 () A 45 B 40 C 36 D33 请思路
- 3第一个字是”一“的成语.如:一心一意 一马当先 一窍不通
- 4It seems that I can't walk into your world at
- 5六年级上科学练习册4.4,4.5及p51-53答案
- 6He spoke roughly in order to belie his air of gentility.
- 7小刚家在图书馆正西方向400米处,小雨家在图书馆正东方向500米处,( )离图书馆近.
- 8将二氧化碳通入饱和氨盐水中,需要加压条件的原因是?
- 9waht'sthis in english,为什么回答必须得是it is.
- 10X=根号3+1,Y=根号3-1,求X平方Y+XY平方分之X方+Y方的值
- 11如何判断session失效的时间?如果session失效,如何取得session中值.
- 12这个句子怪怪的Nobody before Jane fully understood chimp behaviour.句
- 13认真观察漫画,给它拟一个标题(8个字以内)
- 14(2012•青岛模拟)下面几个验证性小实验中,说法不正确的是( )
- 15麻烦您解释一下下题(逻辑)的理由







