{NH3+CO2+H2O==NH4HCO3 NH4HCO3+NACl==NH4Cl+NaHCO3 这两个方程式怎么和成一
 雪花飞飞舞2022-10-04 11:39:541条回答
雪花飞飞舞2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 风中的紫蔷薇 共回答了20个问题
风中的紫蔷薇 共回答了20个问题 |采纳率85%- 要想合成一个总反应,只要把两个化学反应方程式相加,然后合并即可:
NH3+CO2+H2O+NH4HCO3+NaCl=NH4HCO3 +NH4Cl+NaHCO3
NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3 - 1年前
相关推荐
- NH3+CO2+H2O为什么生成碳酸氢铵
 asdfiyhaegkrh1年前1
asdfiyhaegkrh1年前1 -
 一邻 共回答了19个问题
一邻 共回答了19个问题 |采纳率89.5%因为NH3溶于水会成为NH4.OH,这东西又是碱性,CO2微溶于水是酸性,然后两个就反应了成了碳酸氢铵1年前查看全部
- NH4HCO3=NH3+CO2+H2O
NH4HCO3=NH3+CO2+H2O
试说明在通常条件下NH4HCO3易于分解的原因 Crystal_sz1年前2
Crystal_sz1年前2 -
 liweiyacong 共回答了22个问题
liweiyacong 共回答了22个问题 |采纳率90.9%NH4HCO3(s)NH3(g)+ CO2(g)+ H2O(g)
ΔGθ == 31.3kJ/mol > 0
分解反应方向是自发反应方向1年前查看全部
- NH4HCO3---NH3+CO2+H2O怎样配平
 虚伪一辈子1年前1
虚伪一辈子1年前1 -
 凶女魔是救我 共回答了22个问题
凶女魔是救我 共回答了22个问题 |采纳率72.7%NH4HCO3=加热=NH3+CO2+H2O
本身就是平的呀1年前查看全部
- NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl的反应类型是什么?
 ihyy1231年前2
ihyy1231年前2 -
 癌症晚期x 共回答了19个问题
癌症晚期x 共回答了19个问题 |采纳率94.7%写成离子方程式为
NH3+CO2+H2O=(HCO3^-)+(NH4^+)
也就是
NH3+H2CO3=(HCO3^-)+(NH4^+)
NH3是碱(能接受质子的是碱),H2CO3是酸(能提供质子的是酸).应为酸碱中和反应.1年前查看全部
- 已知反应NH4HCO3=NH3+CO2+H2O,为了将混有硫酸钠,碳酸氢铵的NACL提纯,并制得纯净的NACL溶液某同学
已知反应NH4HCO3=NH3+CO2+H2O,为了将混有硫酸钠,碳酸氢铵的NACL提纯,并制得纯净的NACL溶液某同学设计了如
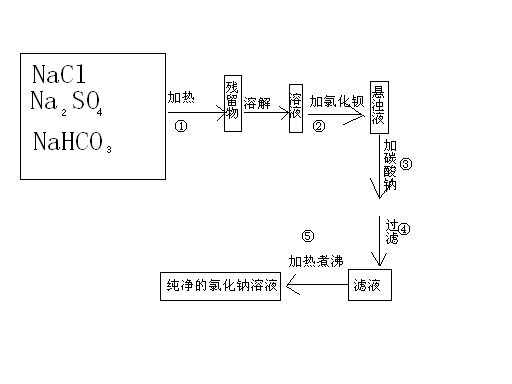
操作①中加热时盛放药品的仪器是?再加热过程中应不断?(操作名称) Bruce__Zhang1年前2
Bruce__Zhang1年前2 -
 lihai530 共回答了16个问题
lihai530 共回答了16个问题 |采纳率100%图片与题目描述有不一致的地方:题目中是碳酸氢铵,图片中则是NaHCO3.
固体混合物加热的仪器最好使用坩埚,加热充分、防止固体飞溅.加热过程中应不断搅拌,使NH4HCO3完全分解.1年前查看全部
- 高中化学侯氏制碱法的原理问题NACL+NH3+CO2+H2O==NAHCO3+NH4CL 这个反应的原理是什么?是溶解度
高中化学侯氏制碱法的原理问题
NACL+NH3+CO2+H2O==NAHCO3+NH4CL 这个反应的原理是什么?是溶解度的差异么?那么详细的过程是怎样的,请大家帮我下.详细点最好...谢谢了! 傻B强1年前1
傻B强1年前1 -
 ss的默默 共回答了14个问题
ss的默默 共回答了14个问题 |采纳率100%氨气与水和二氧化碳反应生成一分子的碳酸氢铵,这是第一步.第二步是:碳酸氢铵与氯化钠反应生成一分子的氯化铵和碳酸氢钠沉淀,碳酸氢钠之所以沉淀是因为它的溶解度较小.根据 NH4Cl 在常温时的溶解度比 NaCl 大,而在低温下却比 NaCl 溶解度小的原理,在 278K 283K(5 10 ℃ ) 时,向母液中加入食盐细粉,而使 NH4Cl 单独结晶析出供做氮肥.1年前查看全部
- (2005•济南)某研究性学习小组学习了工业“侯氏制碱法”的原理后,知道:NaCl+NH3+CO2+H2O=NaHCO3
(2005•济南)某研究性学习小组学习了工业“侯氏制碱法”的原理后,知道:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl.
[提出问题]能否在实验室模拟“侯氏制碱法”中制取NaHCO3的过程呢?
[实验验证]如图是该学习小组进行模拟实验时所用到的部分主要装置.已知浓氨水遇生石灰会产生大量的NH3.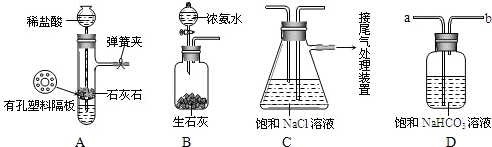
请回答下列问题:
(1)检验A装置气密性的方法是:塞紧带长颈漏斗的橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于试管内的水面,停止加水后,若______,说明装置不漏气.
(2)D是连接在装置A与装置C之间的气体净化装置,进气口是______(填a或b),D的作用是除去______气体.
(3)实验时先向饱和NaCl溶液中通入较多的NH3(溶液显碱性),再通入足量的CO2,其原因是______.(填写序号)
①使CO2更易被吸收②NH3比CO2更易制取③CO2的密度比NH3大
(4)用______的方法将生成的NaHCO3晶体从混合物中分离出来.
[得出结论]利用“侯氏制碱法”在实验室可以制取NaHCO3. 诺丁山A1年前1
诺丁山A1年前1 -
 灏馨 共回答了14个问题
灏馨 共回答了14个问题 |采纳率100%解题思路:(1)注入一定量的水后,试管内气体被压缩管内压强增大,使得出现液面差;液面差保持不变时,说明装置不漏气;
(2)为使气体通过溶液,气体从a通入溶液,混在气体中的HCl与溶液中的碳酸氢钠反应而被吸收;
(3)二氧化碳与水反应形成不稳定的碳酸,致使水吸收二氧化碳量较少;而把二氧化碳通入溶有氨气而呈碱性的水中,会使生成的碳酸与氨水发生反应,而增大二氧化碳气体的吸收;
(4)把固体与液体所形成混合物中固体分离出来的方法为过滤.(1)随水的注入管内加压增大,漏斗内液体不能再流入试管,使长颈漏斗与管内液面出现液面差,并且液面差保持不变,说明装置气密性良好;
故答案为:漏斗中与试管中的液(水)面差保持不再变化或漏斗中的液(水)面不再下降;
(2)气体从a管通入时才能使气体通过溶液而达到净化气体的目的;装置D内盛放的碳酸氢钠溶液能与混在气体中的HCl发生反应生成氯化钠、水和二氧化碳,从而除去混在气体中的HCl;
故答案为:a;氯化氢(或HCl);
(3)先通入氨气,氨气与水形成呈碱性的氨水可与二氧化碳与水生成的碳酸发生反应,更有利于二氧化碳气体的吸收;
故答案为:①;
(4)通过过滤,可把混在溶液中的碳酸氢钠晶体分离出来;
故答案为:过滤.点评:
本题考点: 猜想与事实验证;实验操作注意事项的探究;过滤的原理、方法及其应用;检查装置的气密性;气体的净化(除杂).
考点点评: 根据装置中的药品的性质及装置的连接方式,是准确判断或理解装置作用的一种有效方法.1年前查看全部
- 配平与完成下列反应的化学方程式KMnO4-----K2MnO4+MnO2+O2 NH4HCO3-----NH3+CO2+
配平与完成下列反应的化学方程式
KMnO4-----K2MnO4+MnO2+O2 NH4HCO3-----NH3+CO2+H2O C2H6+O2-----CO2+H2O
SO2+NaOH----Na2SO3+H20 一溜赖青菜1年前3
一溜赖青菜1年前3 -
 苦乐酸甜 共回答了23个问题
苦乐酸甜 共回答了23个问题 |采纳率73.9%2KMnO4=△=K2MnO4+MnO2+2O2
NH4HCO3=△=NH3+CO2+H2O
2C2H6+5O2=燃烧=4CO2+6H2O
SO2+2NaOH=Na2SO3+H2O1年前查看全部
- NH3+CO2+H2O===NH4HCO3 的离子方程式?如题
NH3+CO2+H2O===NH4HCO3 的离子方程式?如题
如题. 真的不会游泳的鱼1年前2
真的不会游泳的鱼1年前2 -
 yuansediao 共回答了13个问题
yuansediao 共回答了13个问题 |采纳率76.9%NH3+CO2+H2O===NH4+ + HCO3- 前面是氨根离子,后面是碳酸氢跟离子1年前查看全部
- 工业上采用氨碱法生产纯碱,其反应的化学反应原理为NH3+CO2+H2O+NaCl═NaHCO3+NH4ClNH3+CO2
工业上采用氨碱法生产纯碱,其反应的化学反应原理为NH3+CO2+H2O+NaCl═NaHCO3+NH4ClNH3+CO2+H2O+NaCl═NaHCO3+NH4Cl;2NaHCO3
Na2CO3+CO2↑+H2O2NaHCO3△ .
Na2CO3+CO2↑+H2O.氨盐水比食盐水更容易吸收二氧化碳的原因是氨气溶于水后显碱性,二氧化碳的水溶液显酸性,酸碱易中和氨气溶于水后显碱性,二氧化碳的水溶液显酸性,酸碱易中和,氨盐水吸收二氧化碳后,首先结晶析出的是碳酸氢钠碳酸氢钠,该现象说明了该温度下,碳酸氢钠的溶解度比NH4Cl少的多该温度下,碳酸氢钠的溶解度比NH4Cl少的多.△ .  你是我的女神1年前1
你是我的女神1年前1 -
 无力揽狂澜 共回答了18个问题
无力揽狂澜 共回答了18个问题 |采纳率88.9%解题思路:根据氨碱法生产纯碱的反应原理书写化学方程式,注意条件和配平;氨气溶于水呈碱性,更容易吸收酸性氧化物二氧化碳,在一定温度下,碳酸氢铵的溶解度比氯化铵小的多,会先从溶液中析出.氨碱法生产纯碱的化学反应原理是用氨气和二氧化碳与氯化钠和水反应生成碳酸氢钠,然后加热碳酸氢钠制取碳酸钠;氨气溶于水所得氨水呈碱性,比水更易吸收二氧化碳;在一定温度下,碳酸氢铵的溶解度比氯化铵的溶解度小,故碳酸氢铵能首先从溶液中析出.
故答案为:NH3+CO2+H2O+NaCl═NaHCO3+NH4Cl; 2NaHCO3
△
.
Na2CO3+CO2↑+H2O.氨气溶于水后显碱性,二氧化碳的水溶液显酸性,酸碱易中和,碳酸氢钠,该温度下,碳酸氢钠的溶解度比NH4Cl少的多.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式;固体溶解度的影响因素;物质的相互转化和制备.1年前查看全部
- (2010•六合区模拟)“NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
(2010•六合区模拟)“NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl2NaHCO3≜Na2CO3+CO2↑+H2O”是著名的“侯氏制碱法”的重要反应.同学们对上述反应涉及的有关知识发表了下列见解.其中不正确的是( )
A.该条件下NaHCO3的溶解度较小
B.副产品氯化铵是一种氮肥
C.析出固体后的溶液为NaHCO3的不饱和溶液
D.二氧化碳在制纯碱的过程中可循环使用 寥了B46B431年前1
寥了B46B431年前1 -
 kbces 共回答了17个问题
kbces 共回答了17个问题 |采纳率88.2%解题思路:(1)从NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl可以看出,碳酸氢钠的溶解度小,以沉淀的形式析出;
(2)NH4Cl中含有氮元素,属于氮肥
(3)判断溶液是否饱和,可以采用两种方式:判断溶液底部是否存在晶体或加入晶体看是否能溶解.A、从NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl可以看出,碳酸氢钠以沉淀的形式析出.所以说明碳酸氢钠的溶解度小,在该温度下结晶析出;A选项正确;B、氮磷钾三种元素中只存在氮元素的化肥,属于氮肥.氯化铵只含有氮元素,...
点评:
本题考点: 饱和溶液和不饱和溶液;常见化肥的种类和作用;化学方程式的概念、读法和含义.
考点点评: 做此题时,要根据题给的信息,逐一分析,找出有用的信息,解决问题.1年前查看全部
- Nacl+NH3+Co2+H2o生成什么Hclo和什么反应生成O2Ca(HCO3)2+NaoH 生成Na2co3和什么N
Nacl+NH3+Co2+H2o生成什么Hclo和什么反应生成O2Ca(HCO3)2+NaoH 生成Na2co3和什么Na2sio3+H2so4生成SO2和什么H2so3怎么反应生成SO2NO2+NH3生成什么
 笑悟净1年前2
笑悟净1年前2 -
 大龄LOLI小暴 共回答了18个问题
大龄LOLI小暴 共回答了18个问题 |采纳率94.4%NaHCO3 NH4Cl1年前查看全部
- (2008•张家界)侯德榜先生潜必研究制碱技术,成功地发明了联合制碱法.其中关键一步的反应原理可表示为:NH3+CO2+
(2008•张家界)侯德榜先生潜必研究制碱技术,成功地发明了联合制碱法.其中关键一步的反应原理可表示为:NH3+CO2+H2O+NaCl═NaHCO3+X,则X的化学式为( )
A.NH3
B.NH3C1
C.NH4C1
D.NH5C1 hailuosun1年前1
hailuosun1年前1 -
 li598333861 共回答了22个问题
li598333861 共回答了22个问题 |采纳率81.8%解题思路:根据反应前后原子种类、数目不变,利用反应的化学方程式,判断生成物X的分子构成,确定物质X的化学式.反应的化学方程式NH3+CO2+H2O+NaCl═NaHCO3+X,可知可知反应前各原子个数为:
反应前 反应后
Na原子 1 1
Cl原子 1 0
N原子 1 0
H原子 5 1
C原子 1 1
O原子 3 3
根据反应前后原子种类、数目不变,可判断生成物X的一个分子由4个H原子、1个N原子、1个Cl原子构成,4个H原子与1个N原子可形成NH4+,因此可确定物质X的化学式可表示为NH4Cl.
故选C.点评:
本题考点: 有关化学式的计算和推断.
考点点评: 根据化学变化前后原子的种类、数目不变,由反应的化学方程式,可以推断反应中某物质的分子构成及物质化学式的确定.1年前查看全部
- 著名的“侯氏制碱法”第一步反应是向饱和氨化盐水中通入二氧化碳,该反应可表示为NaCl+NH3+CO2+H2O=NaHCO
著名的“侯氏制碱法”第一步反应是向饱和氨化盐水中通入二氧化碳,该反应可表示为NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl有关物质的溶解度数据如下(g/100g水):
NaCl NaHCO3NH4Cl
10℃35.88.1533.0
45℃37.014.050.0
现在45℃时,向434g饱和食盐水中通入适量氨气,再向其中通入二氧化碳后,按上述反应进行完全.试计算并回答下列问题(计算结果保留三位有效数字).
(1)反应完全后45℃时析出的晶体的化学式是______,并计算析出晶体的质量.
(2)过滤除去晶体后再降温至10℃,此时析出的晶体是(填化学式)______,计算所析出晶体的质量. 吹鼓手1年前1
吹鼓手1年前1 -
 mcq116 共回答了15个问题
mcq116 共回答了15个问题 |采纳率93.3%解题思路:(1)45℃时,434g饱和食盐水中,NaCl的质量为434g×[37/137]=117g,n(NaCl)=[117g/58.5g/mol]=2mol,根据反应的方程式计算生成NaHCO3的质量,结合溶解度计算析出晶体的质量;
(2)计算出水的质量,结合各物质的溶解度判断析出晶体并计算质量.(1)45℃时,434g饱和食盐水中,NaCl的质量为434g×[37/137]=117g,n(NaCl)=[117g/58.5g/mol]=2mol,
则NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl
1 1
2mol 2mol
n(NaHCO3)=2mol,
m(NaHCO3)=2mol×84g/mol=168g,
此时,溶液中水的质量为434g×[100/137]-2×18g=280g,
溶解NaHCO3的质量为[280/100]×14≈39.0g,
所以析出的质量为168g-39g=129g,
答:析出NaHCO3晶体的质量为129g;
(2)由(1)可知水的质量为280g,则过滤除去晶体后再降温至10℃,
溶解NaHCO3的质量为8.15g×[280/100]=22.8g,
析出NaHCO3的质量为39.0-22.8=16.2g,
生成的NH4Cl质量为2mol×53.5g/mol=107g,
溶液溶解的NH4Cl质量为33.0g×[280/100]=92.4g,
则析出的NH4Cl质量为107g-92.4g=14.6g,
所以析出的物质的为NH4Cl和NaHCO3,总质量为16.2g+14.6g=30.8g,
答:析出的物质的为NH4Cl和NaHCO3,总质量为30.8g.点评:
本题考点: 化学方程式的有关计算;纯碱工业(侯氏制碱法);溶液中溶质的质量分数及相关计算.
考点点评: 本题考查纯碱的制备和计算,题目难度较大,注意有关溶解度计算的方法.1年前查看全部
- 侯氏制碱法 NH3+CO2+H2O=NH4HCO3 NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl 2Na
侯氏制碱法 NH3+CO2+H2O=NH4HCO3 NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl 2NaHCO3=Na2CO3+CO2+H2O
NH3+CO2+H2O=NH4HCO3
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
2NaHCO3=Na2CO3+CO2+H2O
第二部为什么会有向下箭头? lw38871年前1
lw38871年前1 -
 zmag 共回答了20个问题
zmag 共回答了20个问题 |采纳率95%NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl 氯化铵易溶于水、碳酸氢钠溶解度小会析出结晶沉淀向下箭头.1年前查看全部
- 配平与完成下列化学反应方程式.(1)KMnO4-K2MnO4+MnO2+O2(2)NH4HCO3-NH3+CO2+H2O
配平与完成下列化学反应方程式.
(1)KMnO4-K2MnO4+MnO2+O2
(2)NH4HCO3-NH3+CO2+H2O
(3)C2H6+O2-CO2+H2O
(4)SO2+NaOH-Na2SO3+H2O trinitong1年前1
trinitong1年前1 -
 敏娃子 共回答了28个问题
敏娃子 共回答了28个问题 |采纳率96.4%解题思路:因为反应前后元素种类不变,各种元素的原子个数相等,所以根据质量守恒定律,配平化学方程式.(1)利用奇数配偶法或观察法,配平各原子个数.故:2KMnO4═K2MnO4+MnO2+O2↑
(2)利用定一法,把NH4HCO3的计量数定为1.故:NH4HCO3═NH3+CO2↑+H2O
(3)先配有机物,把有机物的计量数定为1,且配平顺序为C-H-O,最后配单质氧气.故:2C2H6+7 O2═4CO2+6H2O
(4)利用观察法,配平各原子的个数,原则:先复杂,后简单.故:SO2+2NaOH═Na2SO3+H2O点评:
本题考点: 化学方程式的配平.
考点点评: 灵活运用“根据质量守恒定律,配平化学方程式.”1年前查看全部
大家在问
- 1一台抽水机0.9小时可以抽水45吨,一小时可以抽水多少吨?抽一吨水需要多少小时?
- 2帮我算一下梯形的面积下边是12cm,上边的长度没有标出来,高是4cm.面积是多少啊?
- 3一个不为0的数乘百分数,积()这个数
- 4绘画是画家通过自己的意志和技艺对客观事物进行表现和再创造为什么不对?
- 5帮忙翻译一句英语.Struggling firms and new businesses facing mounting
- 6为什么把可乐和洗洁精这两种物质混合后,成为PH为7的液体,就不具有腐蚀性了呢?
- 7鞋帽店以每双15元的价格购进一批凉鞋,售价比进价高2成,当卖到还剩5双时,出去购进凉鞋的全部开销外,
- 8钱塘湖春行 描写初春景物的词有哪些好处是什么
- 9描写大漠风光的诗句
- 10把一段长20分米的圆柱形木头沿着底面直径劈开,表面积增加80平方分米,原来这段圆柱形木头的表面积是多少?(π取3)
- 11科学手抄报 我要做一个关于动物方面的手抄报,或者不关于动物也可以,做哪个方面比较容易,有意义
- 12一个语文读音薄雪和薄雾的薄字的读音.
- 13在“谁也没有见到过风”中“谁”读“shui”还是“shei”
- 14表达鼓励他人用什么成语
- 15求山园小梅中的好句
