亚硫酸铵和氢氧化钠反应的化学方程式,
 新鲜的旧qq2022-10-04 11:39:544条回答
新鲜的旧qq2022-10-04 11:39:544条回答
已提交,审核后显示!提交回复
共4条回复
 淡香女人 共回答了17个问题
淡香女人 共回答了17个问题 |采纳率88.2%- 常温下:(NH4)2SO3+2NaOH==2NH3·H2O+Na2SO3
一般写这个:(NH4)2SO3+2NaOH =Δ= 2NH3↑+2H2O+Na2SO3 - 1年前
 0afc 共回答了15个问题
0afc 共回答了15个问题 |采纳率73.3%- 应该不能反应吧……
- 1年前
 TINTIN的kk 共回答了33个问题
TINTIN的kk 共回答了33个问题 |采纳率- 常温下:(NH4)2SO3+2NaOH==2NH3·H2O+Na2SO3
一般写这个:(NH4)2SO3+2NaOH =Δ= 2NH3↑+2H2O+Na2SO3 - 1年前
 薛一琦 共回答了34个问题
薛一琦 共回答了34个问题 |采纳率- (NH4)2SO3+2NaOH ==加热== 2NH3(g)+Na2SO3+H2O
- 1年前
相关推荐
- 一固体混合物.可能有氯化钙一固体混合物,可能有氯化钙、碳酸氢铵,烧碱,亚硫酸铵,将它溶于水得到无色澄清溶液,无其他明显现
一固体混合物.可能有氯化钙
一固体混合物,可能有氯化钙、碳酸氢铵,烧碱,亚硫酸铵,将它溶于水得到无色澄清溶液,无其他明显现象,想溶液中加入硝酸钡溶液,产生白色沉淀,再加硝酸,沉淀全部(注意是全部)消失,肯定含有 拄拐棍的鸟1年前2
拄拐棍的鸟1年前2 -
 NavyBlue_KING 共回答了16个问题
NavyBlue_KING 共回答了16个问题 |采纳率93.8%1、溶于水后,得到无色澄清溶液.
结论①:说明其中 CaCl2和NH4HCO3两者之间有一个不存在.
2、加入硝酸钡,有沉淀生成.
结论②:说明含有CO32-和SO32-,所以,结论①中,CaCl2是不存在的.
3、继续加入硝酸,沉淀全部消失.
结论③:说明其中不含有SO32-,否则会被HNO3氧化,变为SO42-,BaSO4沉淀是不溶于HNO3的
所以呢:肯定没有CaCl2、肯定没有 (NH4)2SO3.
肯定含有: NH4HCO3
可能含有:烧碱
祝学习进步~
回答满意请采纳~1年前查看全部
- 亚硫酸铵与二氧化硫反应生成亚硫酸氢铵化学方程式
 youfar1年前1
youfar1年前1 -
 大大uu 共回答了16个问题
大大uu 共回答了16个问题 |采纳率87.5%(NH4)2SO3 +SO2+H2O=2NH4HSO31年前查看全部
- 亚硫酸铵与浓氢氧化钾反应的化学方程式
 dwei_wang1年前0
dwei_wang1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 硫酸溶液跟亚硫酸铵溶液共热的方程式
 gsq9922811年前1
gsq9922811年前1 -
 圈圈泡泡 共回答了17个问题
圈圈泡泡 共回答了17个问题 |采纳率100%H2SO4+(NH4)2SO3=2NH4SO4+H2O+SO2
新年快乐,希望采纳.1年前查看全部
- 亚硫酸铵和过氧化氢反应的离子方程式
 蠢过猪1年前1
蠢过猪1年前1 -
 sdxiaoyushui 共回答了17个问题
sdxiaoyushui 共回答了17个问题 |采纳率88.2%铵根不会被氧化,被氧化的是SO32-
SO32- + H2O2 = H2O + SO42-1年前查看全部
- 为什么亚硫酸铵和少量硫酸反应生成亚硫酸氢铵
为什么亚硫酸铵和少量硫酸反应生成亚硫酸氢铵
2.为什么硫酸氢钠在水中电离出氢离子和硫酸根离子 在熔融状态下电离出硫酸氢根离子?
3.微容物作产物时打不打沉淀符号? 阿里乐乐1年前4
阿里乐乐1年前4 -
 Leox2000 共回答了21个问题
Leox2000 共回答了21个问题 |采纳率90.5%1、严格说是亚硫酸氢铵和硫酸铵,因为亚硫酸根结合氢离子能力比硫酸大的多,可以看成强酸制弱酸.亚硫酸和硫酸是不会发生氧化还原反应的,因为没有中间价态.
2、硫酸氢根和硫酸一样,是由共价键形成的,所以在熔融状态下不电离.硫酸氢根在水中受水分子的作用而电离出氢离子,常温下电离度约30%.
3、要根据题目中的意思,题目说是沉淀就要写,尤其是推断题.1年前查看全部
- 亚硫酸铵和硫酸怎么反应?
 林昕烨1年前2
林昕烨1年前2 -
 zhangtianyei 共回答了23个问题
zhangtianyei 共回答了23个问题 |采纳率95.7%强酸和SO3反应必生成SO2(气体)和H2O.那么反应式中就还有NH4没出现,而弱酸根离子都被生成SO2了,那么就只剩下S04拉,那么还有种生成物就必然是(NH4)2SO4
反应方程式就是:
(NH4)2SO3+H2SO4==(NH4 )2SO4+H2O+SO2
你也可以这样想,
(NH4)2SO3+H2SO4=(NH4)2SO4+H2SO3;
H2SO3=H2O+SO2;
合并起来就是:(NH4)2SO3+H2SO4==(NH4 )2SO4+H2O+SO21年前查看全部
- 以硫酸工业的SO2尾气、氨水、石灰石、焦炭、碳酸氢铵和氯化钾等为原料,可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等
以硫酸工业的SO2尾气、氨水、石灰石、焦炭、碳酸氢铵和氯化钾等为原料,可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等物质.合成路线如下:
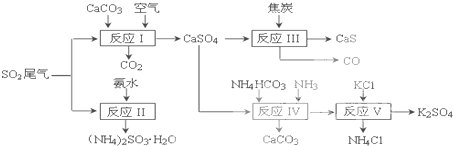
(1)写出反应Ⅰ的化学方程式______.
(2)生产中,向反应II中的溶液中加入适量还原性很强的对苯二酚等物质,其目的是______.
(3)下列有关说法正确的是______.
a.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
b.反应Ⅲ中氧化剂与还原剂的物质的量之比为4:1
c.反应Ⅳ需控制在60~70℃,目的之一是减少碳酸氢铵的分解
d.反应Ⅴ中的副产物氯化铵可用作氮肥
(4)反应Ⅴ在25℃、40%乙二醇溶液中进行,不断有硫酸钾晶体从溶液中析出,硫酸钾的产率会超过90%,选用40%乙二醇溶液的原因是______.
(5)(NH4)2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,写出二氧化氮与亚硫酸铵反应的化学方程式______. wang158098231年前1
wang158098231年前1 -
 yuyi919 共回答了15个问题
yuyi919 共回答了15个问题 |采纳率93.3%解题思路:(1)根据反应物和生成物写出反应的化学方程式;
(2)亚硫酸氨中的硫为+4价,易被空气中的氧气氧化;
(3)a.依据流程图结合反应生成物分析,过量的空气把亚硫酸钙氧化为硫酸钙;
b.反应Ⅲ化学方程式为:CaSO4+4C=CaS+4CO↑,氧化剂为CaSO4,还原剂为C;
c.防止碳酸氢铵在温度过高时分解;
d.氯化铵是一种氮肥;
(4)利用硫酸钾在不同溶剂中溶解度的不同,达到析出晶体的目的;
(5)二氧化氮具有强氧化性能氧化亚硫酸铵反应,生成硫酸铵,本身被还原为氮气,结合原子守恒配平写出.(1)碳酸钙、二氧化硫和氧气反应生成硫酸钙和二氧化碳,方程式为2CaCO3+2SO2+O2═2CaSO4+2CO2,故答案为:2CaCO3+2SO2+O2═2CaSO4+2CO2;
(2)对苯二酚具有还原性,空气中的氧气具有氧化性,亚硫酸氨中+4价的硫具有还原性,故答案为:防止亚硫酸铵被氧化;
(3)a.过量的空气把亚硫酸钙氧化为硫酸钙,故a正确;
b.反应Ⅲ化学方程式为:CaSO4+4C=CaS+4CO↑,氧化剂为CaSO4,还原剂为C,氧化剂与还原剂物质的量之比为1:4,故b错误;
c.防止碳酸氢铵在温度过高时分解得不到需要的目标产物,故c正确;
D、氯化铵含N元素,是一种氮肥,故d正确;
故答案为:acd;
(4)反应V中选用了40%的乙二醇溶液,温度控制在25℃,此时硫酸钾的产率超过90%,选用40%的乙二醇溶液原因是利用乙二醇降低硫酸钾溶解度,有利于析出,
故答案为:乙二醇是有机溶剂能减小K2SO4的溶解度,使硫酸钾充分析出;
(5)④(NH4)2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统,二氧化氮与亚硫酸铵反应,二氧化氮具有强氧化性能氧化亚硫酸铵反应,生成硫酸铵,本身被还原为氮气,由原子守恒可知化学方程式为4(NH4)2SO3+2NO2=4(NH4)2SO4+N2,
故答案为:4(NH4)2SO3+2NO2=4(NH4)2SO4+N2.点评:
本题考点: 制备实验方案的设计;二氧化硫的化学性质.
考点点评: 本题考查二氧化硫的性质及物质的制备,为高频考点,把握习题中的信息及发生的反应为解答的关键,侧重二氧化硫的还原性及学生分析能力的考查,题目难度中等.1年前查看全部
- SO2气体通入Na2SO3溶液中 硫酸溶液跟亚硫酸铵溶液共热 Na2SO3在空气中变质转化成硫酸钠
 qwer111q1年前1
qwer111q1年前1 -
 ujswamsvmj 共回答了18个问题
ujswamsvmj 共回答了18个问题 |采纳率83.3%SO2+Na2SO3+H2O=2NaHSO3
H2SO4+(NH4)2SO3=(NH4)2SO4+SO2+H2O
2Na2SO3+O2=2Na2SO41年前查看全部
- 亚硫酸氢铵如何变成亚硫酸铵
 3647808351年前1
3647808351年前1 -
 linushe 共回答了13个问题
linushe 共回答了13个问题 |采纳率92.3%加一些氨水
NH4HSO4+NH3·H2O=(NH4)2SO4+H2O1年前查看全部
- 请问,硫代硫酸铵水溶液和亚硫酸铵水溶液,哪个还原性更加强?哪个稳定性更强?
 tytpabg1年前2
tytpabg1年前2 -
 老_将 共回答了20个问题
老_将 共回答了20个问题 |采纳率80%应该是SO32-的还原性强.
同样和I2反应,SO32-可以被氧化为SO42-,而S2O32-只能被氧化成S4O62-.1年前查看全部
- 亚硫酸氢铵与氢氧化钡反应方程式 亚硫酸铵与氢氧化钡反应方程式 亚硫酸氢铵与硫酸反应方程式
亚硫酸氢铵与氢氧化钡反应方程式 亚硫酸铵与氢氧化钡反应方程式 亚硫酸氢铵与硫酸反应方程式
亚硫酸铵与硫酸反应方程式 渴望你的保护1年前2
渴望你的保护1年前2 -
 packyzhen 共回答了12个问题
packyzhen 共回答了12个问题 |采纳率91.7%亚硫酸氢铵与氢氧化钡反应方程式:Ba(OH)2+2NH4HSO3=BaSO3↓+4H2O+2NH3↑
亚硫酸铵与氢氧化钡反应方程式:Ba(OH)2+(NH4)2SO3=BaSO3↓+2H2O+2NH3↑
亚硫酸氢铵与硫酸反应方程式:2NH4HSO3+ H2SO4=(NH4)2SO4+2H2O+SO2↑
亚硫酸铵与硫酸反应方程式:(NH4)2SO3+ H2SO4=(NH4)2SO4+H2O+SO2↑1年前查看全部
- 亚硫酸氢铵 亚硫酸铵 反应式为?
 gzhill1年前2
gzhill1年前2 -
 无用鬼 共回答了13个问题
无用鬼 共回答了13个问题 |采纳率92.3%(NH4)2SO3-----NH3+SO2+H2O
亚硫酸氢铵产物也一样,没配平,自己配1年前查看全部
- 硫代硫酸铵水溶液和亚硫酸铵水溶液,哪个还原性更加强?请不要抄,
 月明2221年前1
月明2221年前1 -
 6aatc 共回答了27个问题
6aatc 共回答了27个问题 |采纳率85.2%(1)硫代硫酸根的还原性应该是强于亚硫酸根的,你看一下S的价态就行了
(2)或者,你可以看硫代硫酸钠是怎么制备的:
头两种方法都是亚硫酸盐或者SO2和低价态的硫磺或者硫化物反应生成的,氧化还原反应中,氧化剂的氧化性强于氧化产物,故亚硫酸根的氧化性强于硫代硫酸根,或者,反过来说,硫代硫酸根的还原性应该是强于亚硫酸根的.
(3)楼主也可以自己去查一下氧化还原电势,硫代硫酸根的值应该小于亚硫酸根的1年前查看全部
- 硫酸和亚硫酸铵反应是氧化还原还是复分解?
 品牌策划1年前4
品牌策划1年前4 -
 无意随形 共回答了21个问题
无意随形 共回答了21个问题 |采纳率81%硫酸和亚硫酸铵中的硫处于相邻价态.是不可能发生氧化还原反应的.1年前查看全部
- 亚硫酸铵和硫酸反应生成那些物质
 丁十七1年前3
丁十七1年前3 -
 drforever 共回答了14个问题
drforever 共回答了14个问题 |采纳率92.9%(NH4)2SO3 + H2SO4 ===(NH4)2SO4+H20+SO2(g)
强酸制弱酸的反应1年前查看全部
- 过硫酸铵和亚硫酸钠氧化还原引发体系,应该先加过硫酸铵还是先加亚硫酸铵啊,还是可以同时加啊
 ralf89191年前2
ralf89191年前2 -
 执着变迁 共回答了14个问题
执着变迁 共回答了14个问题 |采纳率85.7%一般氧化剂最后加1年前查看全部
- 亚硝酸钠,碳酸氢钠,亚硫酸铵,硅酸钠,怎么用硫酸鉴别
 最好的你1年前2
最好的你1年前2 -
 fengxing31 共回答了19个问题
fengxing31 共回答了19个问题 |采纳率100%加入硫酸有红棕色气体生成的是亚硝酸钠
加入硫酸有气体生成的是碳酸氢钠
加入硫酸有沉淀生成的是硅酸钠
加入硫酸生成有刺激性气体的是亚硫酸铵.1年前查看全部
- 亚硫酸根不是中强酸根吗,铵根不是弱碱酸根吗,亚硫酸铵应该是强酸弱碱盐呀,可他为何显碱性
亚硫酸根不是中强酸根吗,铵根不是弱碱酸根吗,亚硫酸铵应该是强酸弱碱盐呀,可他为何显碱性
哥哥或姐姐们,可以讲的祥细些吗?老师刚提到我不太懂, buddy50241年前3
buddy50241年前3 -
 llwxm 共回答了20个问题
llwxm 共回答了20个问题 |采纳率90%强酸弱碱盐是因为阳离子与水电离产生的氢氧根结合,使氢离子浓度高于氢氧根离子,使溶液呈酸性.水解…………1年前查看全部
- 硫酸与亚硫酸铵共热反应方程式会氧化生成硫酸铵么?
 提子包我的最爱1年前2
提子包我的最爱1年前2 -
 mihubumihu 共回答了17个问题
mihubumihu 共回答了17个问题 |采纳率82.4%这个反应其实就是酸与亚硫酸根反应啊!这个不是氧化还原反应,是复分解反应!
2H+ +SO32-==H2O +SO2
楼上的专家你说对不?嘿嘿.
楼主明白了没有?1年前查看全部
- 亚硫酸铵和亚硫酸氢铵化学式
 别总说我帅1年前1
别总说我帅1年前1 -
 风中桃花 共回答了14个问题
风中桃花 共回答了14个问题 |采纳率78.6%亚硫酸铵(NH4)2SO3
亚硫酸氢铵NH4HSO31年前查看全部
- 硫酸铵、亚硫酸铵、亚硫酸氢的酸性哪个强,为什么?
 wangzhengjie1年前2
wangzhengjie1年前2 -
 yxg_ez 共回答了21个问题
yxg_ez 共回答了21个问题 |采纳率90.5%按照水中电离强度度排列,
三种物质在水溶液中的酸性:硫酸铵>亚硫酸铵>亚硫酸氢胺1年前查看全部
- 请问,亚硫酸钠水溶液和亚硫酸铵水溶液,哪个更加稳定,哪个可以长期存放?
 我不爱喜之郎1年前1
我不爱喜之郎1年前1 -
 kevin0525 共回答了23个问题
kevin0525 共回答了23个问题 |采纳率95.7%亚硫酸钠水溶液更加稳定
亚硫酸铵发生双水解(双水解是指溶液中的阳离子、阴离子同时发生水解,一个结合水电离的H+,一个结合水电离的OH-,双水解的程度比一般水解程度要大),因为亚硫酸显碱性,而铵根显酸性,所以他们是存在双水解的``但是亚硫酸铵显酸性的``
显然是亚硫酸钠可以长期存放
亚硫酸根水解 SO₃²¯+H₂O HSO₃¯+OH¯1年前查看全部
- 为何制取硫酸完了之后用氨水吸收尾气再用H2SO4处理?氨水吸收产生亚硫酸铵,再加硫酸不又产生so2啦?
 keyong198201291年前3
keyong198201291年前3 -
 我是一条胖头鱼 共回答了22个问题
我是一条胖头鱼 共回答了22个问题 |采纳率86.4%用硫酸处理亚硫酸铵,把二氧化硫赶出,这时的二氧化硫不含氮、氧等气体,可以液化生产液体二氧化硫,也可以直接回硫酸系统再生产硫酸.亚硫酸盐不稳定,会形成二次污染.1年前查看全部
大家在问
- 1stay是行为动词还是系动词?
- 2英语的英标怎么练习发音啊 感觉发不准 怎么办呢
- 3铝的逸出功是4.2eV,现在将波长200nm的光照射铝表面.求:
- 4every minute must be made full use_____English
- 5有趣的倒顺词,补充相声中省略掉的内容!
- 6secret什么意思
- 7“Chen Weifu”(陈威甫)请问这样音译对吗?字母的大小写与字母之间的间隔正确吗?
- 8西方经济学:Net export effect
- 9they want to know who____更强壮
- 10已知A. B是常见的碱,甲. 乙是常见的盐,C是一种常见的无色无味的气体。这几种物质间的转化关系如图所示。请回答: (1
- 11多酚氧化酶的作用
- 12It will be snowy tomorrow.(改为同义句) There ()()()tomorrow
- 13角A等于90度,BD是三角形ABC的角平分线,DE是BC的垂直平分线,求角ABC和角CDE的度数
- 14已知sina+√3*cosa=(2m+1)/(3-m),求m的取值范围,我要用分离参数法,先把m分离出来,就是化成m=…
- 15用度表示56°25′12〃急数学!
