品红溶液的作用是什么?
 牛娃他哥2022-10-04 11:39:545条回答
牛娃他哥2022-10-04 11:39:545条回答
已提交,审核后显示!提交回复
共5条回复
 wangyue001 共回答了25个问题
wangyue001 共回答了25个问题 |采纳率80%- 红色溶液用来鉴定SO2,会使品红溶液褪色.但由于SO2的漂白是暂时性的,生成一种不稳定的物质,加热已褪色的品红溶液其还会变回原来的颜色.不能检验酸碱.用于羊毛、丝绸织物和锦纶织物的染色还用于生物着色.
- 1年前
 nn199937 共回答了1个问题
nn199937 共回答了1个问题 |采纳率- 检验二氧化硫气体 并且在加热后会退色 知识基础啊
- 1年前
 sdfwqgqwguwq 共回答了2个问题
sdfwqgqwguwq 共回答了2个问题 |采纳率- 红色溶液用来鉴定SO2,会使品红溶液褪色。但由于SO2的漂白是暂时性的,属于化合反应,生成一种不稳定的物质,加热已褪色的品红溶液其还会变回原来的颜色。
- 1年前
 飞翔中的蓝色 共回答了2个问题
飞翔中的蓝色 共回答了2个问题 |采纳率- 工业染色剂和高中试验SO2的漂白性
- 1年前
 dlhcxg 共回答了25个问题
dlhcxg 共回答了25个问题 |采纳率- 其一:充当某些试剂的染色剂;
其二:中学化学中验证SO2的存在;
其三:某些实验中用水现象不明显,加品红后方便观察;
其四:用于棉、人造纤维、纸张、皮革的印染。 - 1年前
相关推荐
- SO2只能使品红溶液漂白吗。。。。。。注意“只能”。
 zxcvlsafjlk3jlkj1年前3
zxcvlsafjlk3jlkj1年前3 -
 hbsxxxy 共回答了16个问题
hbsxxxy 共回答了16个问题 |采纳率81.3%不是.
二氧化硫褪色原理是与苯胺类染料加成退色.品红只是苯胺类染料中的一种.
或者如一楼所说二氧化硫通过自身的还原性使得有颜色的氧化性物质通过相互之间的作用而褪色.1年前查看全部
- 在品红溶液中通入二氧化硫气体,会褪色,加热后,却会回复?
在品红溶液中通入二氧化硫气体,会褪色,加热后,却会回复?
加热后,却会恢复,请问为什么? m6310121年前1
m6310121年前1 -
 lzj97126 共回答了16个问题
lzj97126 共回答了16个问题 |采纳率81.3%二氧化硫会褪色是生成了不稳定的物质,加热后这些物质就分解了,所以就褪色了1年前查看全部
- 干燥或是湿润的氯气能使品红溶液褪色吗?
 HMILWY1年前3
HMILWY1年前3 -
 菠萝111 共回答了19个问题
菠萝111 共回答了19个问题 |采纳率89.5%湿润的氯气肯定是可以使品红溶液褪色的
干燥的氯气也可以,因为是把氯气通入品红溶液,所以氯气还是能和水接触生成次氯酸,使品红溶液褪色1年前查看全部
- 氯气通入品红溶液为什么不褪色但是通入时没加热啊?
 youlan4101年前1
youlan4101年前1 -
 塔罗牌zhi恋 共回答了20个问题
塔罗牌zhi恋 共回答了20个问题 |采纳率80%二氧化硫可以和某些有机物化合作用漂白【如品红】,氯气溶于水,部分和水反应,生成具有强氧化行的次氯酸,可以氧化行漂白、消毒.品红不具有还原行,故不被氯气漂白1年前查看全部
- 为什么活性炭的吸附性能使品红溶液褪色
 zxjzxj771年前1
zxjzxj771年前1 -
 jackalamenta 共回答了16个问题
jackalamenta 共回答了16个问题 |采纳率93.8%因为活性炭多孔,可以吸附细小的杂质颜色等,所以可使品红褪色1年前查看全部
- 石蕊溶液会被氧化吗?像品红溶液那样?遇到强氧化性酸先变红后褪色吗?
石蕊溶液会被氧化吗?像品红溶液那样?遇到强氧化性酸先变红后褪色吗?
会的再答,大侠们,看到类似问题的答案,我的心很寒! biggirl021年前2
biggirl021年前2 -
 猪说不认识我 共回答了15个问题
猪说不认识我 共回答了15个问题 |采纳率86.7%浓硝酸和氯气和石蕊反应,先是变红,然后褪色,这个就是石蕊被氧化了的结果1年前查看全部
- 二氧化硫通入品红溶液,红色褪去,加热显红色
二氧化硫通入品红溶液,红色褪去,加热显红色
一开始是不是利用它的漂白性?那加热显红色是什么性质?
氯气通入品红溶液,品红溶液褪色,是利用它的什么性质? 叶无静1年前4
叶无静1年前4 -
 阿当001 共回答了14个问题
阿当001 共回答了14个问题 |采纳率85.7%二氧化硫和氯气都能使品红褪色,但不同的是加热后有褪色有不褪色,这是因为两者褪色的机理不同:二氧化硫使品红褪色,原理是它和品红化合生成无色的有机物,但加热时,该有机物不稳定,有分解回品红,所以会出现再次变红现象;与之相反,氯气是先和水反应生成次氯酸(HClO),而次氯酸的强氧化性使有机物品红结构破坏,不可逆!从而褪色,加热不了恢复!能懂吗,就是因为各自褪色机理不同造成的.1年前查看全部
- 下列关于氯水的叙述不正确的是:A.新制氯水可是品红溶液褪色B.氯水放置数天后酸性增强C.新制氯水和救治氯水中加入AgNO
下列关于氯水的叙述不正确的是:
A.新制氯水可是品红溶液褪色
B.氯水放置数天后酸性增强
C.新制氯水和救治氯水中加入AgNO3溶液都能生成不溶于稀硝酸的白色沉淀
D.新制氯水呈黄绿色是因为含有HCI分子
希望分析的尽量透彻, 奇缘饿狼1年前5
奇缘饿狼1年前5 -
 熊大明 共回答了21个问题
熊大明 共回答了21个问题 |采纳率81%选D.
A新制氯水中含有HClO分子具有强氧化性可使品红褪色;
B氯水放置数天溶液中HClO分解成HCl,弱酸变强酸所以酸性增强;
C不管新制还是久制的氯水中都含有Cl-所以都可与AgNO3反应生成AgCl沉淀;
D新制氯水呈黄绿色是因为Cl2分子溶于水的缘故.1年前查看全部
- 二氧化硫为啥会使品红溶液褪色?是因为跟其他物质反应才褪色生成使品红褪色的物质?还是直接跟品红本身反应?最好有化学方程式
 kcqr1年前2
kcqr1年前2 -
 llll2 共回答了21个问题
llll2 共回答了21个问题 |采纳率81%因为品红是一种有机有色物质,SO2可以和有机色素结合生产无色物质1年前查看全部
- 向品红溶液中通入一种常见气体后,品红溶液褪色.请设计一个探究性实验方案(要求不另加任何试剂),判断通入的气体是氯气还是二
向品红溶液中通入一种常见气体后,品红溶液褪色.请设计一个探究性实验方案(要求不另加任何试剂),判断通入的气体是氯气还是二氧化硫
 jam_bboy1年前2
jam_bboy1年前2 -
 哭与笑之黯然 共回答了15个问题
哭与笑之黯然 共回答了15个问题 |采纳率93.3%将已褪色的品红溶液加热,看是否恢复红色.不恢复:氯气;恢复:二氧化硫1年前查看全部
- 有两种白色粉末A、B,分别与H2SO4反应都生成不溶于硝酸的物质C,同时生成无色气体分别为D与E.D、E分别通入品红溶液
有两种白色粉末A、B,分别与H2SO4反应都生成不溶于硝酸的物质C,同时生成无色气体分别为D与E.D、E分别通入品红溶液,D褪色而E不能;D能使溴水褪色而E不能.试确定:
A____ B____C____D_____E_____
发生反应的离子方程式______,_____,_____,____,_____.(共五个) 你的眼泪231年前1
你的眼泪231年前1 -
 Butear 共回答了20个问题
Butear 共回答了20个问题 |采纳率85%BaSO3
BaCO3
BaSO4
SO2
CO21年前查看全部
- 氯气 过氧化氢 臭氧 二氧化硫 分别使品红溶液变色的原理?
 头是如此铁1年前3
头是如此铁1年前3 -
 tenney83 共回答了14个问题
tenney83 共回答了14个问题 |采纳率78.6%氯气和水反应生成强氧化性的次氯酸使品红褪色
过氧化氢有强氧化性
臭氧也具有强氧化性
二氧化硫和品红反应,生成不稳定的硫化物,使之暂时褪色1年前查看全部
- 乙烯能使品红溶液褪色么?So2能么?,NaOH能吸SO2么?
 你最SB1年前3
你最SB1年前3 -
 去了又来 共回答了22个问题
去了又来 共回答了22个问题 |采纳率90.9%乙烯不能使品红溶液褪色,二氧化硫可以使品红溶液褪色,氢氧化钠溶液能吸收二氧化硫1年前查看全部
- 品红溶液中通入足量的SO2后,滴加BaCl2
品红溶液中通入足量的SO2后,滴加BaCl2
是否有沉淀?
若像品红溶液中通入足量的CO2后,滴加BaCl2
是否有沉淀 丫头11181年前3
丫头11181年前3 -
 zhageis2 共回答了17个问题
zhageis2 共回答了17个问题 |采纳率100%…都不会有沉淀产生,原因…弱酸无法置强酸.反应根本不会发生!1年前查看全部
- so2通入品红溶液先退色,加热后恢复原色.这句话不对,
 不知道的了1年前1
不知道的了1年前1 -
 stevene_alone 共回答了14个问题
stevene_alone 共回答了14个问题 |采纳率85.7%正确1年前查看全部
- 亚硫酸具有漂白性,能使品红溶液褪色.这句话为什么是对的啊?
 huangpeiyang1年前1
huangpeiyang1年前1 -
 nanfeiyan0111 共回答了18个问题
nanfeiyan0111 共回答了18个问题 |采纳率94.4%没有错误.其原理SO2溶于水变成H2SO3,SO2与品红形成不稳定无色物质,褪色.1年前查看全部
- 品红溶液是什么物质的溶液它是酸性还是碱性
 hu009591年前1
hu009591年前1 -
 癞蛤蟆屁特 共回答了18个问题
癞蛤蟆屁特 共回答了18个问题 |采纳率94.4%品红,常用作染色剂.分子式C20H19N3,分子量301.38.又称碱性品红.棕红色晶体.微溶于水,水溶液呈红色.溶于乙醇和酸.用于棉、人造纤维、纸张、皮革的印染,也用于喷漆、墨水等.品红可与二氧化硫结合成不稳定的无色物质,经较长时间或受热时又可分解,出现结合成不稳定的无色物质,经较长时间或受热时又可分解,出现红色.可由苯胺、邻甲苯胺、对甲苯胺与硝基苯在铁和氯化锌存在时加热制成 品红主要有两种:碱性品红和盐基品红分子式分别是:NH2CH3C6H3C:C6H4(NH2)(Cl)C6H4-NH2; NH2C6H4C:C6H4(NH2)(Cl)C6H4NH2 物理性质:有金属光泽的深绿色结晶.溶于水和醇;不溶于醚 物理性质:有金属光泽的深绿色结晶.溶于水和醇;不溶于醚,所以品红还可作为区别醛和酮的一种试剂.通常需要密封保存.工业用途:用于蚕丝、腈纶、羊毛和单宁媒染棉纤维的染色.也用于皮革、纸张、羽毛、麦秆、竹、木等的着色和制造色淀.本品与孔雀绿和制造色淀.本品与孔雀绿拼染腈纶绒线可得黑色,色泽乌黑,并且日晒牢度比分别单独应用时有明显提高.在高中化学试验中常利用品红的还原性和不稳定性来检验SO2的漂白性,还有品红还是一种常用的生物染色剂.利用如上所说品红的性质,实验室经常用它来鉴别二氧化硫气体.二氧化硫具有漂白性,可以使品红溶液褪色,但漂白后的物质不稳定,在加热之后品红又会恢复原有的颜色.品红在颜色 利用如上所说品红的性质,实验室经常用它来鉴别二氧化硫气体.二氧化硫具有漂白性,可以使品红溶液褪色,但漂白后的物质不稳定,在加热之后品红又会恢复原有的颜色.品红在颜色上来说,是指比大红略浅的颜色.品红色与黄色、蓝色是颜色的三原色,而大红色属于光的三原色,并非颜色的三原色.另外两种光的原色是绿色和蓝色.品红色,又称为洋红色(英语:Magenta),是介于红色和蓝色之间的颜色.在光谱中品红色并非是单一波长的光,而是.由等量的红光与蓝光混合而得.品红色与黄色、青色构成了减法三原色之一.品红色的补色是绿色1年前查看全部
- 品红溶液的主要成分是什么啊,如题,都有哪些物质可使它腿色
 老四2171年前1
老四2171年前1 -
 小虫12 共回答了16个问题
小虫12 共回答了16个问题 |采纳率87.5%品红主要有两种:碱性品红和盐基品红分子式分别是:
NH2CH3C6H3C:C6H4(NH2)(Cl)C6H4-NH2; NH2C6H4C:C6H4(NH2)(Cl)C6H4NH2
物理性质:有金属光泽的深绿色结晶.溶于水和醇;不溶于醚.通常需要密封保存.
工业用途:
用于蚕丝、腈纶、羊毛和单宁媒染棉纤维的染色.也用于皮革、纸张、羽毛、麦杆、竹、木等的着色和制造色淀.本品与孔雀绿拼染腈纶绒线可得黑色,色泽乌黑,并且日晒牢度比分别单独应用时有明显提高.
在高中化学试验中常利用品红的还原性和不稳定性来检验SO2的漂白性,还有品红还是一种常用的生物染色剂.
高中化学中的品红经常出现在鉴定氧化性气体的题目里,主要是二氧化硫.品红的化学结构不稳定,可以被这些氧化性气体氧化掉而褪色.1年前查看全部
- 能使品红溶液褪色的试剂有什么?
 maohuan0001年前2
maohuan0001年前2 -
 诗韵清绝白玉 共回答了19个问题
诗韵清绝白玉 共回答了19个问题 |采纳率94.7%二氧化硫、双氧水、过氧化钠、活性炭1年前查看全部
- 能使品红溶液退色的试剂有什么如题
 thecyf1年前6
thecyf1年前6 -
 wyf1231332 共回答了21个问题
wyf1231332 共回答了21个问题 |采纳率95.2%SO2,(有漂白性,但不稳定,容易恢复红色)
氯气(与水生成次氯酸,有漂白性)
类似的还有漂白粉(caclo2)漂白剂(Naclo2)1年前查看全部
- 为什么二氧化硫和潮湿的氯气通入品红溶液不退色?
 chrylz1年前6
chrylz1年前6 -
 qb841214 共回答了23个问题
qb841214 共回答了23个问题 |采纳率82.6%因为发生了如下的反应:
SO2 + Cl2 + 2H20 = H2S04 + 2HCl
反应物当中的水来自于潮湿的的氯气,反应后生成的物质在常温下难以具有强氧化性氧化品红这种有机色素.1年前查看全部
- 改良苯酚品红溶液和醋酸洋红的作用区别
 lzw19821年前1
lzw19821年前1 -
 济南uu 共回答了11个问题
济南uu 共回答了11个问题 |采纳率100%改良的苯酚品红溶液是低温诱导染色体变异用的,醋酸洋红是观察植物细胞有丝分裂时用的1年前查看全部
- 臭氧的化学性质有哪些?能使品红溶液褪色体现了它的什么化学性质
 密码连接1年前1
密码连接1年前1 -
 爪子帮 共回答了12个问题
爪子帮 共回答了12个问题 |采纳率83.3%很强的氧化性.
体现了氧化性.1年前查看全部
- 硫酸与氯气同时通入品红溶液中为什么不变色
 五柳狂歌1年前3
五柳狂歌1年前3 -
 xieanni 共回答了12个问题
xieanni 共回答了12个问题 |采纳率100%硫酸怎么通入品红
这个说SO2比较多
SO2和Cl2以体积比1:1混合会失去漂白能力
原因:发生反应:SO2+Cl2+2H2O=2HCl+H2SO4
HCl和H2SO4均无漂白能力的1年前查看全部
- 高二化学(测1mol氢气体积)测1mol氢气的体积时,储液瓶中加入品红溶液,为什么?测SO2、CO2气体时还能否继续使用
高二化学(测1mol氢气体积)
测1mol氢气的体积时,储液瓶中加入品红溶液,为什么?测SO2、CO2气体时还能否继续使用?如不能,应用什么溶液代替较好?常温常压下,根据液体量瓶上的刻度范围,镁条约取多少克?由计算所得. hunterhb1年前1
hunterhb1年前1 -
 no_too 共回答了15个问题
no_too 共回答了15个问题 |采纳率73.3%个人认为: 品红本身有颜色,用它来做储液瓶添加剂更便于观测. 其次,测SO2、CO2气体时不能继续使用,原因是SO2会使品红褪色(会消耗SO2),而CO2则是易溶于水(同样测不准) 代替溶液应该用有机溶剂吧,四氯化碳应该可以(目的是不反应,且不消耗气体) 最后,真的是常温常压吗?是不是应该算标况啊...总之,你所选的镁条制得的H2一定要小于液体量瓶上的刻度范围!1年前查看全部
- 向溶液中加氢氧化钡,产生白色沉淀,再加稀盐酸产生的气体,不使品红溶液褪色,使石灰水浑浊,这样为什么不能验证溶液中含有碳酸
向溶液中加氢氧化钡,产生白色沉淀,再加稀盐酸产生的气体,不使品红溶液褪色,使石灰水浑浊,这样为什么不能验证溶液中含有碳酸根离子?
 jamin071年前1
jamin071年前1 -
 shufan5212000 共回答了17个问题
shufan5212000 共回答了17个问题 |采纳率94.1%溶液中可能是碳酸氢根1年前查看全部
- 酸性能使品红变色的条件 是不是酸性条件就可以使品红溶液变红?co2和so2都可以使品红溶液变红,其中SO2过量,容液会褪
酸性能使品红变色的条件
是不是酸性条件就可以使品红溶液变红?
co2和so2都可以使品红溶液变红,其中SO2过量,容液会褪色,而co2却不能褪色, 平胸是美德1年前5
平胸是美德1年前5 -
 梦西游 共回答了16个问题
梦西游 共回答了16个问题 |采纳率100%品红溶液是一种红色的溶液,SO2是因为有氧化性所以才会暂时把品红溶液退为透明色,如果加热会使品红溶液变回原来的红色,而CO2是二氧化碳根本没有关系~会让品红溶液永久褪色的是CL2与水发生反应生成HCLO(次氯酸),也是一种制造漂白液和漂白精的化学成分!亲!后面的有很多化学方程式要记住的,好好加油吧!1年前查看全部
- 一道化学题,关于品红和CO2证明碳与浓硫酸共热生成SO2和CO2,混合气体先通过品红溶液,再通过高锰酸钾,最后通过澄清的
一道化学题,关于品红和CO2
证明碳与浓硫酸共热生成SO2和CO2,混合气体先通过品红溶液,再通过高锰酸钾,最后通过澄清的石灰水.先通过品红溶液,品红退色,说明混合气体里有SO2.
我想请问的是,如果先通过品红和高锰酸钾溶液(注意是溶液),CO2不是会溶于水吗,即使非常少,实验是否还是不够精确?纠结中…… ling13251年前4
ling13251年前4 -
 ttq12345 共回答了17个问题
ttq12345 共回答了17个问题 |采纳率88.2%是定性实验,不是定量实验.证明有就行,不管生成多少.1年前查看全部
- 酸可使品红颜退色吗?加热后会使品红溶液变回红色莫?(就好象so2一样)
酸可使品红颜退色吗?加热后会使品红溶液变回红色莫?(就好象so2一样)
在做莫尔盐实验时监定有无fe3+ fe2+ so3 so4时 有一个现象:当加入过量盐酸到溶液再滴加一到两滴品红时红色褪去,当加热溶液时溶液边回红色
当时就判断有so3:'(
要知莫尔盐只有so4,当时老师就讲"酸性对品红有影响"
当加少量盐酸时,重复实验发现溶液真无变化
我想问的是酸性真的对品红真有影响麽~作用是如何的
 xinwen04121年前1
xinwen04121年前1 -
 ukpont1 共回答了17个问题
ukpont1 共回答了17个问题 |采纳率94.1%中学实验室中品红是一种三苯甲烷系染料,颜色来源于它的大共轭体系,能使品红褪色的物质有很多,如:碱、酸、亚硫酸、亚硫酸盐、卤素单质、HCN以及一些强氧化性物质等等,加热能否恢复呈红色就看其共轭结构能否恢复1年前查看全部
- SO2的水溶液和Cl2的水溶液均能使品红溶液褪色,将So2和Cl2按1:1体积比(同温同压)混合后通入品红溶液中,品红不
SO2的水溶液和Cl2的水溶液均能使品红溶液褪色,将So2和Cl2按1:1体积比(同温同压)混合后通入品红溶液中,品红不褪色,其原因是——
 chenguahua6481年前1
chenguahua6481年前1 -
 CAREFOR 共回答了16个问题
CAREFOR 共回答了16个问题 |采纳率100%虽然SO2和Cl2能使品红溶液褪色,但原理不一样.SO2使其褪色的原理是与品红反应生成不稳定化合物,加热的时候就会分解,变回红色.Cl2使其褪色的原理是Cl2与水反应生成次氯酸HCLO和盐酸.使品红褪色是因为次氯酸根在发挥作用.次氯酸中的氯元素是+1价的,有很强的氧化性,起漂白作用,使品红褪色.这种褪色是不可逆的.1年前查看全部
- SO2使品红溶液,高锰酸钾溶液,Br2水褪色分别体现的是什么性质(漂白、还原) 还原性的加方程式
 nimamad1年前3
nimamad1年前3 -
 bbyebb1zn 共回答了21个问题
bbyebb1zn 共回答了21个问题 |采纳率95.2%与品红溶液反应是发生了化合反应,因反应后的生成不稳定,所以,加热仍能复原.体现的是漂白性.
与后面两个反应是还原性.1年前查看全部
- Cl2和SO2混合气体通入品红溶液中有什么现象,离子方程式是?
 2496352141年前2
2496352141年前2 -
 CLON23 共回答了13个问题
CLON23 共回答了13个问题 |采纳率84.6%可能退色,也可能不褪色
SO2+2H2O+Cl2=H2SO4+2HCl结果导致氯气和二氧化硫中至少一种反应完!最后,是否腿色得看起比例!只要不是1:1,而且量够,就能腿色1年前查看全部
- SO2只能使品红溶液退色,不能使其他颜色的溶液褪色?
 定的kk1年前1
定的kk1年前1 -
 rings55 共回答了16个问题
rings55 共回答了16个问题 |采纳率81.3%二氧化硫使带色的物质脱色属于化学反应1年前查看全部
- 1反应开始一段时间后,观察到B,D两个试管中的品红溶液出现的现象是?2停止通气后,再给B,D两个试管分别加热,两试管中的
1反应开始一段时间后,观察到B,D两个试管中的品红溶液出现的现象是?2停止通气后,再给B,D两个试管分别加热,两试管中的现象分别为
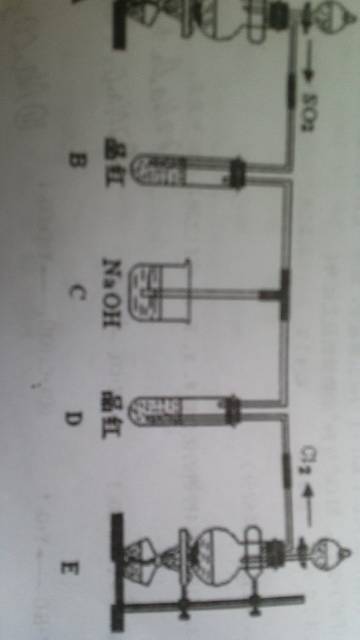
 dagang79791年前1
dagang79791年前1 -
 草鞋诗人 共回答了11个问题
草鞋诗人 共回答了11个问题 |采纳率100%SO2与Cl2都能对有色物质漂白,但二者漂白的原理不同.SO2与有色物质反应生成结构不稳定的无色物质,这种物质在外界条件变化时(如加热)或者一段时间后会自动分解为有色物质,所以SO2的漂白是暂时的,不稳定的,可逆的.而C...1年前查看全部
- 能使品红溶液褪色的有哪些?
 乖乖猪兜兜1年前3
乖乖猪兜兜1年前3 -
 绿色身份 共回答了13个问题
绿色身份 共回答了13个问题 |采纳率84.6%SO2(或H2SO3)能使品红溶液褪色,能使品红溶液褪色的就远不止SO2了.可用简单的实验证明:
(1) Cl2、NO2、O3等气体,能使品红溶液迅速褪色.
(2)稀H2SO4、稀HCl、稀HNO3能使品红溶液迅速褪色.
(3)双氧水、溴水、碘水,也能使品红溶液褪色.1年前查看全部
- 能使品红溶液褪色的,高中阶段学的有哪些?
 毛毛me1年前1
毛毛me1年前1 -
 桔子变橙子 共回答了19个问题
桔子变橙子 共回答了19个问题 |采纳率94.7%SO2:与品红中的有色物质结合而是品红褪色.
活性炭:具有吸附性Cl2,过氧化氢,过氧化物 硝酸,次氯酸 ,臭氧等:发生化学反映使其褪色1年前查看全部
- 化学 so2使品红溶液褪色,为什么说明它有漂白性,不是是因为亚硫酸跟品红结合么?
 zzb_hz1年前2
zzb_hz1年前2 -
 123872302 共回答了13个问题
123872302 共回答了13个问题 |采纳率84.6%这也是漂白性的一种1年前查看全部
- 都有哪些气体能使品红溶液褪色?
 子规声断1年前2
子规声断1年前2 -
 fffeona 共回答了18个问题
fffeona 共回答了18个问题 |采纳率83.3%强氧化性气体,如氯气、臭氧等1年前查看全部
- 有关乙烯乙烯为什么不能使品红溶液褪色?反而能使酸性高猛酸钾溶液褪色?二氧化硫又是如何的?
 野蛮花园1年前1
野蛮花园1年前1 -
 章鱼王子殿 共回答了15个问题
章鱼王子殿 共回答了15个问题 |采纳率93.3%褪色的原理大致分为三种:
1:化合褪色(如SO2与品红结合成化合物)
2:氧化褪色(如高猛酸钾溶液与乙烯发生氧化还原反应)
3:吸附褪色(如活性炭将品红溶液中的红色物质吸附后使溶液褪色)
乙烯不能与品红结合成化合物,品红也不能将乙烯氧化,吸附更不用说了,所以乙烯不能使品红褪色1年前查看全部
- 二氧化硫使品红溶液褪色体现了什么?
 239107371年前1
239107371年前1 -
 badfox007 共回答了19个问题
badfox007 共回答了19个问题 |采纳率89.5%体现了其漂白性.1年前查看全部
- cl2和so2 都具有漂白作用,能使品红溶液褪色,若将等物质的量的cl2 so2 混合后 在通入品红与 bacl2混合溶
cl2和so2 都具有漂白作用,能使品红溶液褪色,若将等物质的量的cl2 so2 混合后 在通入品红与 bacl2混合溶液 能观察到得现象 (多选)
A溶液很快褪色 B溶液不退色 C出现沉淀 D不出现沉淀 朵朵绿1年前3
朵朵绿1年前3 -
 lanhuomiao 共回答了30个问题
lanhuomiao 共回答了30个问题 |采纳率90%BC
Cl2会氧化SO2为SO4 2-
SO2+Cl2+H2OBaSO4↓+2HCl
由于SO2和Cl2全部消耗完,所以溶液不退色,出现白色沉淀.1年前查看全部
- 能够使品红溶液褪色的原理是什么
 wangzhejll1年前1
wangzhejll1年前1 -
 歌德列车 共回答了18个问题
歌德列车 共回答了18个问题 |采纳率83.3%有挺多种的:
1活性炭是吸附性使其褪色的,但是是永久性的推色
2过氧化钠是氧化性使其褪色的,是永久性的推色,是过氧化钠中的过氧根具有强烈的氧化性是品红褪色
3不是有次氯酸根的都能使其永久褪色,因为次氯酸根的氧化性只有在酸性条件下才最强,中性和碱性条件会减弱他的氧化性
4二氧化硫是由于加合反应使其褪色,二氧化硫和品红重某种物质进行反应使其褪色,但是是短暂的,进位加热以后品红又会变红
5臭氧也是因为具有强氧化性,也是和过氧化钠一样具有强氧化性的过氧基团
6因为品红在碱性条件下才会变红,这三种都是酸,加入以后中和了溶液里的碱性,品红处于酸性条件下当然褪色了啊
7因为溴水碘水里面有次溴酸,次碘酸,这些酸和次氯酸一样都具有强氧化性,所以是品红褪色,也是永久性的褪色
最后注意,凡是永久性让品红褪色的肯定破坏了品红的内部结构1年前查看全部
- 某酸式盐A与NaOH溶液共热生成无色气体B,与稀盐酸共热时生成能使品红溶液褪色的气C.
 1britney11年前2
1britney11年前2 -
 laxdf 共回答了22个问题
laxdf 共回答了22个问题 |采纳率95.5%(1)盐和碱生成气体肯定是氨气,和品红褪色是SO2.
所以A是NH4HSO3
(2)A到C化学方程式:
NH4HSO3+HCl=加热l=NH4Cl+H2O+SO2↑
离子方程式:
HSO3-十H+ =△= H2O+SO2↑
(3)A与过量氢氧化钠共热:
NH4+十HSO3-十2OH- = NH3↑十2H2O十SO32-1年前查看全部
- 品红溶液与酸碱会变色吗?怎么有人说会有人说不会?我只知道可以用来检验SO2
 易箜1年前1
易箜1年前1 -
 sheeptiger 共回答了19个问题
sheeptiger 共回答了19个问题 |采纳率94.7%品红溶液不是酸碱指示计,所以不能使酸碱变色1年前查看全部
- SO2能够使品红溶液褪色,也能使高锰酸钾溶液和溴水等褪色,原理是否相同
 噗下雨1年前2
噗下雨1年前2 -
 风追司马2004 共回答了27个问题
风追司马2004 共回答了27个问题 |采纳率88.9%不相同
使品红溶液褪色是SO2的漂白性
使高锰酸钾溶液和溴水等褪色是SO2的还原性1年前查看全部
- (3分)(2012•山东)下列由相关实验现象所推出的结论正确的是( ) A.Cl 2 、SO 2 均能使品红溶液褪色,
(3分)(2012•山东)下列由相关实验现象所推出的结论正确的是( )
A.Cl 2 、SO 2 均能使品红溶液褪色,说明二者均有氧化性 B.向溶液中滴加酸化的Ba(NO 3 ) 2 溶液出现白色沉淀,说明该溶液中一定有SO 2 ﹣ 4 C.Fe与稀HNO 3 、稀H 2 SO 4 反应均有气泡产生,说明Fe与两种酸均发生置换反应 D.分别充满HCl、NH 3 的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水  2745275501年前1
2745275501年前1 -
 rui_costa1102 共回答了15个问题
rui_costa1102 共回答了15个问题 |采纳率93.3%D A、二氧化硫和有色物质生成无色物质,只能说明二氧化硫有漂白性.B、亚硫酸根离子能被硝酸氧化生成硫酸根离子而造成干扰.C、铁与稀硝酸反应生成的气体是一氧化氮.D、根据烧瓶内溶液的变化现象判断气体压强...1年前查看全部
- 二氧化硫可以漂白品红溶液是有强氧化性但它应该是有弱氧化性啊
 一面湖水8881年前2
一面湖水8881年前2 -
 风飞飘 共回答了15个问题
风飞飘 共回答了15个问题 |采纳率100%SO2的漂白性,不是因为它有氧化性,而是能与“某些”有色物质化合,生成“不稳定”的无色物质,所以褪色.
也因为无色物质不稳定,加热或者时间长了还会分解,恢复原来的颜色.1年前查看全部
- SO2气体是品红溶液褪色,那么是否只有SO2才可让其推色?
 娃哈哈n1301年前1
娃哈哈n1301年前1 -
 一波我心如水 共回答了17个问题
一波我心如水 共回答了17个问题 |采纳率82.4%不是.二氧化硫使溶液褪色的漂白原理是氧化还原反应.其他氧化剂也能够使品红溶液褪色.
品红褪色的氧化还原反应还可以使用各种强氧化剂如高锰酸钾,次氯酸钠等.1年前查看全部
- 已知盐酸加到品红溶液中,能使品红溶液的红色加深.试推测:
已知盐酸加到品红溶液中,能使品红溶液的红色加深.试推测:
(1)向品红溶液中通过量SO2的过程中的现象为 ___ ;加热后的现象为 ___ .
(2)向品红溶液中通入过量Cl2的过程中,观察到的现象为 ___ .
(3)向品红溶液中通入物质的量比为1:1且足量的SO2和Cl2后现象为 ___ .
 apppril1年前4
apppril1年前4 -
 朗姆酒 共回答了14个问题
朗姆酒 共回答了14个问题 |采纳率85.7%解题思路:(1)根据SO2的漂白原理来解释;
(2)根据Cl2的漂白原理来解释;
(3)根据SO2的还原性来解释.(1)因二氧化硫漂白原理在于能与有机色素结合成无色的不稳定化合物,加热后,无色不稳定的化合物分解,又恢复原来的颜色.当向品红溶液中通入过量的SO2时,发生如下反应:SO2+H2O⇌H2SO3,生成的酸能使品红溶液红色加深,因SO2过量,SO2与品红溶液结合成不稳定的无色物质而褪色,加热无色物质分解又逐渐恢复到原来的红色,
故答案为:溶液颜色先变深后又逐渐褪去;逐渐恢复原来的红色;
(2)Cl2的漂白原理是和H2O反应生成的HClO具有强氧化性,与二氧化硫漂白原理不同.当向品红溶液中通入Cl2,因Cl2+H2O⇌HClO+HCl,同样生成了酸,品红溶液红色加深,因Cl2过量,Cl2与水反应产生的HClO氧化有色物质而使其褪色,加热后不再恢复红色,故答案为:溶液的颜色先变深后又逐渐褪去;
(3)已知盐酸加到品红溶液中,能使品红溶液的红色加深,当向品红溶液中通入1:1的SO2和Cl2时,两者发生以下反应:Cl2+SO2+2H2O═2HCl+H2SO4,因生成了酸,使品红溶液颜色加深,故答案为:溶液的红色比原来加深.点评:
本题考点: 二氧化硫的化学性质;氯气的化学性质.
考点点评: 本题主要考查了二氧化硫、Cl2的漂白原理,两者的漂白原理不同,需要注意的是虽然两者都有漂白性,但两者以1:1通入溶液时不具有漂白性,原因是两者发生反应:Cl2+SO2+2H2O═2HCl+H2SO4.1年前查看全部
大家在问
- 1不含非极性共价键的分子晶体一定是共价化合物?
- 2一个不等边三角形有两条边是3厘米和7厘米,第三边长是奇数
- 3不等边三角形,已知两条边的长,求第三边长?
- 4动能定理能否使用如果一个物体的两个分运动不垂直,能否先求出各个分运动的动能,然后相加求动能?为什么?
- 5细菌但染色法时为什么干燥和固定不能合为一步
- 6想知道在这种情况下 能不能用动能定理?在整个过程中能不能用?
- 7选择合适的词语、古诗句、名言警句和歇后语、谚语填空
- 8酶的活性准确定义是什么?以我的理解,和底物、产物(两者不作为抑制剂)没关系呀.
- 9犹豫的近义词是什么?
- 10Are you tired?Everybody gets tired sometimes.When you are ti
- 11为什么奇函数的定积分的值为0我对图像不清楚积分域怎么定义的 哪种才是关于原点对称 为什么关于y和x轴同时对称 就可以用4
- 12简爱英文简介100单词以内
- 13化学平衡移动中转化率是怎样定义的
- 14电解质和非电解质怎么更好的区分
- 15物体密度不同,体积相同,如何判断浮力大小
