(2009•维扬区模拟)下列各组物质的溶液混合后,最终不一定有沉淀生成的是( )
 专为发帖2022-10-04 11:39:541条回答
专为发帖2022-10-04 11:39:541条回答A.Ba(OH)2H2SO4HCl
B.CuCl2Ba(NO3)2CaCl2
C.BaCl2Na2CO3HNO3
D.AgNO3H2SO4HCl

已提交,审核后显示!提交回复
共1条回复
 喧闹的戏言 共回答了17个问题
喧闹的戏言 共回答了17个问题 |采纳率88.2%- 解题思路:A、根据氢氧化钡与硫酸反应生成硫酸钡沉淀和水,其中硫酸钡既不溶于水不也不溶于酸进行解答;
B、根据CuCl2Ba(NO3)2CuCl2溶液混合没有水、气体、和沉淀生成,所以不反应进行解答;
C、根据氯化钡与碳酸钠反应生成碳酸钡沉淀,碳酸钡能与稀硝酸反应生成硝酸钡、水和二氧化碳进行解答;
D、根据硝酸银和盐酸反应生成氯化银白色沉淀和硝酸,其中氯化银不溶于水也不溶于酸进行解答.A、氢氧化钡与硫酸反应生成硫酸钡沉淀和水,其中硫酸钡既不溶于水不也不溶于稀盐酸,所以Ba(OH)2、H2SO4、HCl溶液混合后可生成BaSO4沉淀;故A一定有沉淀生成;
B、CuCl2Ba(NO3)2CaCl2溶液混合没有水、气体、和沉淀生成,所以不反应;故B一定没有沉淀生成;
C、BaCl2、Na2CO3、HNO3溶液混合BaCl2与Na2CO3可生成BaCO3沉淀,生成的BaCO3沉淀又可与HNO3反应生成Ba(NO3)2、H2O和CO2;若HNO3量不足则会有沉淀生成,若HNO3过量则不会有沉淀生成;故C不一定有沉淀生成;
D、硝酸银和盐酸反应生成氯化银白色沉淀和硝酸,其中氯化银不溶于水也不溶于酸,AgNO3、H2SO4、HCl溶液混合后可生成AgCl沉淀;故D一定有沉淀生成;
故选C.点评:
本题考点: 复分解反应及其发生的条件.
考点点评: 既不溶于水也不能溶于酸的白色沉淀为硫酸钡或氯化银;其它不溶于水的沉淀都可与酸反应而消失. - 1年前
相关推荐
- (2009•维扬区模拟)下列各组物质的溶液混合后,最终不一定有沉淀生成的是( )
(2009•维扬区模拟)下列各组物质的溶液混合后,最终不一定有沉淀生成的是( )
A. Ba(OH)2H2SO4HCl
B. CuCl2Ba(NO3)2CaCl2
C. BaCl2Na2CO3HNO3
D. AgNO3H2SO4HCl dragoonchen1年前1
dragoonchen1年前1 -
 JAZEmm 共回答了21个问题
JAZEmm 共回答了21个问题 |采纳率85.7%解题思路:A、根据氢氧化钡与硫酸反应生成硫酸钡沉淀和水,其中硫酸钡既不溶于水不也不溶于酸进行解答;
B、根据CuCl2Ba(NO3)2CuCl2溶液混合没有水、气体、和沉淀生成,所以不反应进行解答;
C、根据氯化钡与碳酸钠反应生成碳酸钡沉淀,碳酸钡能与稀硝酸反应生成硝酸钡、水和二氧化碳进行解答;
D、根据硝酸银和盐酸反应生成氯化银白色沉淀和硝酸,其中氯化银不溶于水也不溶于酸进行解答.A、氢氧化钡与硫酸反应生成硫酸钡沉淀和水,其中硫酸钡既不溶于水不也不溶于稀盐酸,所以Ba(OH)2、H2SO4、HCl溶液混合后可生成BaSO4沉淀;故A一定有沉淀生成;
B、CuCl2Ba(NO3)2CaCl2溶液混合没有水、气体、和沉淀生成,所以不反应;故B一定没有沉淀生成;
C、BaCl2、Na2CO3、HNO3溶液混合BaCl2与Na2CO3可生成BaCO3沉淀,生成的BaCO3沉淀又可与HNO3反应生成Ba(NO3)2、H2O和CO2;若HNO3量不足则会有沉淀生成,若HNO3过量则不会有沉淀生成;故C不一定有沉淀生成;
D、硝酸银和盐酸反应生成氯化银白色沉淀和硝酸,其中氯化银不溶于水也不溶于酸,AgNO3、H2SO4、HCl溶液混合后可生成AgCl沉淀;故D一定有沉淀生成;
故选C.点评:
本题考点: 复分解反应及其发生的条件.
考点点评: 既不溶于水也不能溶于酸的白色沉淀为硫酸钡或氯化银;其它不溶于水的沉淀都可与酸反应而消失.1年前查看全部
- (2009•维扬区模拟)原煤中含有硫元素,在燃烧过程中产生的二氧化硫会造成大气的污染.某煤场向原煤中加入适量的生石灰制成
(2009•维扬区模拟)原煤中含有硫元素,在燃烧过程中产生的二氧化硫会造成大气的污染.某煤场向原煤中加入适量的生石灰制成供居民采暖用的“环保煤”,以减少二氧化硫的排放,消弱二氧化硫对空气的污染.燃烧时生石灰吸收二氧化硫的化学方程式为:
2CaO+mSO2+O2
nCaSO4.请回答下列问题:高温 .
(1)m值是______;
(2)反应前后硫元素的化合价由______价变为______价.
(3)若煤厂一次共加入含氧化钙80%的生石灰1400t,则理论上最多可吸收二氧化硫多少吨? gbgt1年前1
gbgt1年前1 -
 鼓都摸你 共回答了12个问题
鼓都摸你 共回答了12个问题 |采纳率100%解题思路:(1)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式计算m的值即可.
(2)根据在化合物中正负化合价代数和为零,结合含硫物质的化学式进行解答.
(3)由生石灰的质量、氧化钙的质量分数,根据反应的化学方程式可以列式计算出可吸收二氧化硫的质量.(1)根据反应的化学方程式2CaO+mSO2+O2
高温
.
nCaSO4,反应物中钙原子的个数为2,故n为2;根据硫原子个数相等,则m为2.故答案为:2.
(2)氧元素显-2价,设SO2中硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×2=0,则x=+4价.
钙元素显+2价,氧元素显-2价,设CaSO4中硫元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:(+2)+y+(-2)×4=0,则y=+6价.
故答案为:+4;+6.
(3)1400t生石灰中含氧化钙的质量为1400t×80%=1120t,
设理论上最多可吸收二氧化硫的质量为x.
2CaO+2SO2 +O2
高温
.
2CaSO4
112128
1120t x
[112/128=
1120t
x] x=1280t.
答:理论上最多可吸收二氧化硫1280t.点评:
本题考点: 含杂质物质的化学反应的有关计算;有关元素化合价的计算;质量守恒定律及其应用.
考点点评: 本题难度不大,掌握原子守恒来确定物质的化学式的方法、利用化合价的原则计算指定元素化合价的方法、注意代入方程式计算的必须是纯物质的质量是解题的关键.1年前查看全部
- (2009•维扬区模拟)某无色混合气体可能含有N2、H2、CO、CO2、H2O等几种混合气体,使该混合气体依次通过紫色石
(2009•维扬区模拟)某无色混合气体可能含有N2、H2、CO、CO2、H2O等几种混合气体,使该混合气体依次通过紫色石蕊试液时没有变化,通过无水硫酸铜变蓝,通过灼热的氧化铜时有红色的铜生成,通过澄清石灰水时,石灰水变浑浊,则该混合气中一定有的气体和肯定没有的气体分别是( )
A.H2O、CO2
B.H2、CO
C.CO、CO2
D.H2、CO2 mayingjie1981年前1
mayingjie1981年前1 -
 青衫女子 共回答了17个问题
青衫女子 共回答了17个问题 |采纳率94.1%解题思路:题属于推断题,根据题目给出的信息:当该气体通过紫色石蕊试液时,没有变色,说明一定没有二氧化碳;通过无水硫酸铜变蓝,说明有水;通过灼热的氧化铜时有红色铜生成,再通过澄清石灰水时,石灰水变浑浊,该气体中一定含有一氧化碳;氮气和氢气对上述实验现象无影响,因此可能有,也可能没有.当该气体通过紫色石蕊试液时,没有变色,说明一定没有二氧化碳;通过无水硫酸铜变蓝,说明有水;通过灼热的氧化铜时有红色铜生成,再通过澄清石灰水时,石灰水变浑浊,该气体中一定含有一氧化碳;氮气和氢气对上述实验现象无影响,因此可能有,也可能没有.所以混合气体中一定含有水和一氧化碳,一定不含二氧化碳,可能含有氢气和氮气.
故选AD点评:
本题考点: 常见气体的检验与除杂方法.
考点点评: 本考点属于物质的推断题,做本类题型时,要注意题目给出的信息,利用已知条件来解决有关的问题.本题考查了常见气体的化学性质,还有检验气体的实验流程,综合性比较强,要认真掌握.1年前查看全部
- (2009•维扬区模拟)填表 物质名称 ______ 氢氧化铁 ______ 盐酸 ______ 液氧 化学式 CuSO
(2009•维扬区模拟)填表
物质名称 ______ 氢氧化铁 ______ 盐酸 ______ 液氧 化学式 CuSO4 ______ Mg ______ H2SO4 ______ 颜色 ______ ______ ______ ______ ______ 淡蓝色  nxfdddd1年前1
nxfdddd1年前1 -
 童虎1 共回答了29个问题
童虎1 共回答了29个问题 |采纳率93.1%解题思路:根据物质的名称、物理性质、及化学式的正确书写方法,进行解答.CuSO4名称为:硫酸铜溶液,蓝色;
氢氧化铁由+3价的铁元素和-1价的氢氧根构成,化学式为:Fe(OH)3;为红褐色;
Mg 名称:镁,是银白色金属;
盐酸的化学式为:HCl;是一种无色的液体;
H2SO4 名称:硫酸,是一种无色的液体;
液氧的化学式为:O2;
故答案为:
物质名称 硫酸铜溶液 镁 硫酸
化学式 Fe(OH)3 HCl O2
颜色 蓝色 红褐色 银白色 无色 无色点评:
本题考点: 化学式的书写及意义;有关元素化合价的计算.
考点点评: 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础.1年前查看全部
- (2009•维扬区模拟)有一空气中暴露过的NaOH固体,分析测知含水6.62% Na2CO3
(2009•维扬区模拟)有一空气中暴露过的NaOH固体,分析测知含水6.62%Na2CO3 2.38%NaOH91%将此样品1g加到46g质量分数为3.65%的盐酸中,过量的盐酸用质量分数为4.43%的NaOH溶液中和,用去20.59g,蒸干中和后的溶液,可得到固体的质量为( )
A.1.33g
B.2.62g
C.3.43g
D.无法确定 瓶盖1261年前1
瓶盖1261年前1 -
 潘朵拉2006 共回答了28个问题
潘朵拉2006 共回答了28个问题 |采纳率82.1%解题思路:因为46g3.65%的稀盐酸与碳酸钠、氢氧化钠溶液都反应,因为过量的盐酸用氢氧化钠中和,故氯元素全部与钠元素结合生成氯化钠;先求出46g3.65%的稀盐酸的氯元素的质量,再利用化学式的计算即可求出氯化钠的质量.46g3.65%的稀盐酸与碳酸钠、氢氧化钠溶液都反应,因为过量的盐酸用氢氧化钠中和,故氯元素全部与钠元素结合生成氯化钠;则46g3.65%的稀盐酸的氯元素的质量为:46g×3.65%×[35.5/35.5+1]=1.633g;所以生成的氯化钠质量是:[1.633g
35.5/35.5+23]=2.62g.
故选B点评:
本题考点: 酸的化学性质;根据化学反应方程式的计算.
考点点评: 本题是运用化学中的基本思想质量守恒思想,通过化合物中某元素的质量分数的计算,得到需要求得的物质质量,从而培养了学生的创新思维能力.1年前查看全部
- (2009•维扬区模拟)下列分别盛有不同物质的容器中,所盛物质属于单质的是______,属于混合物的是______,属于
(2009•维扬区模拟)下列分别盛有不同物质的容器中,所盛物质属于单质的是______,属于混合物的是______,属于氧化物的是______.(填字母)
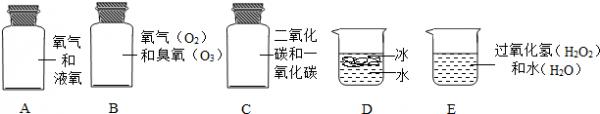
 kana_jia1年前1
kana_jia1年前1 -
 无可奈何也 共回答了21个问题
无可奈何也 共回答了21个问题 |采纳率90.5%解题思路:单质是由同种元素组成的纯净物;
混合物是由两种或两种以上的物质混合而成的物质;
氧化物是由两种元素组成的化合物,其中一种元素是氧元素.氧气和液氧均是由氧元素组成的纯净物,均属于单质;
氧气和臭氧、二氧化碳和一氧化碳、过氧化氢和水等都是由两种或两种以上物质组成的混合物;
冰水共存物是由两种元素组成的化合物,而且其中一种元素是氧元素,属于氧化物;
故答案为:A,BCE,D.点评:
本题考点: 物质的简单分类.
考点点评: 解答此类题要充分理解物质的分类方法方面的知识,掌握了物质的分类方法才能对物质进行正确的分类.1年前查看全部
- (2009•维扬区模拟)(l)CaCl2溶液和NaHCO3,溶液反应生成CaCO3沉淀.为表示这个反应写出了下列两个反应
(2009•维扬区模拟)(l)CaCl2溶液和NaHCO3,溶液反应生成CaCO3沉淀.为表示这个反应写出了下列两个反应方程式:CaCl2+NaHCO3=CaCO3+NaCl+HCl
CaCl2+2NaHCO3=CaCO3↓+2NaCl+CO2↑+H2O
你认为哪一个反应的化学方程式不合理,并简述理由.______
(2)已知难溶的物质在一定条件下可转化成更难溶的物质.将白色Mg(OH)2加到FeCl3溶液中有红棕色沉淀生成.请写出反应的化学方程式并简述理由.
______. 无梦无心1年前1
无梦无心1年前1 -
 306543503 共回答了17个问题
306543503 共回答了17个问题 |采纳率100%解题思路:(1)根据复分解反应及其发生的条件来判断反应是否合理;
(2)根据难溶的物质在一定条件下可转化成更难溶的物质来分析化学反应.(1)因CaCl2+NaHCO3=CaCO3+NaCl+HCl反应的生成物中CaCO3能与HCl反应,则该反应不合理,
而CaCl2+2NaHCO3=CaCO3↓+2NaCl+CO2↑+H2O反应有沉淀和气体、水生成,则该反应合理,
故答案为:第一个化学方程式不合理,因为CaCO3将与HCl反应;
(2)由难溶的物质在一定条件下可转化成更难溶的物质,则白色Mg(OH)2加到FeCl3溶液中有红棕色沉淀生成,
是因为Fe(OH)3比Mg(OH)2更难溶,其反应为3 Mg(OH)2+2 FeCl3═3 MgCl2+2 Fe (OH)3↓,
故答案为:3Mg(OH)2+2FeCl3═3MgCl2+2Fe(OH)3↓,因Fe(OH)3比Mg(OH)2更难溶.点评:
本题考点: 离子或物质的共存问题;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查学生利用信息来判断反应的发生,抓住习题中的信息利用物质的溶解性来分析反应是解答的关键.1年前查看全部
- (2009•维扬区模拟)在配置10%的氯化钠溶液的过程中,会导致溶液中氯化钠的质量分数大于10%的原因是…( )
(2009•维扬区模拟)在配置10%的氯化钠溶液的过程中,会导致溶液中氯化钠的质量分数大于10%的原因是…( )
A.称量氯化钠固体时所用天平的砝码上粘有杂质
B.将称量好的氯化钠固体倒入烧杯中时,有部分氯化钠固体散落在实验桌上
C.用量筒量取水时仰视读数
D.盛装溶液的试剂瓶中有一块碎玻璃 雪囚1年前1
雪囚1年前1 -
 神秘紫hh 共回答了24个问题
神秘紫hh 共回答了24个问题 |采纳率91.7%解题思路:由公式:溶质质量分数=[溶质质量/溶质质量+溶剂质量]×100%可以看出,若溶质质量偏小,将导致溶质质量分数偏小;若溶剂质量偏大也会导致溶质质量分数偏小.针对每项操作分析,将导致溶质或溶剂的质量如何改变,最后作出正确判断.A、称量氯化钠固体时所用天平的砝码上粘有杂质,则称取的氯化钠固体的质量偏大,即溶质的质量偏大,所以在配置过程中会导致溶液中氯化钠的质量分数大于10%;故本选项正确;
B、将称量好的氯化钠固体倒入烧杯中时,有部分氯化钠固体散落在实验桌上,则氯化钠固体的质量偏小,即溶质的质量偏小,所以在配置过程中会导致溶液中氯化钠的质量分数小于10%;故本选项错误;
C、用量筒量取水时仰视读数,将导致所取水体积偏大,导致溶质质量分数偏小;故本选项错误;
D、盛装溶液的试剂瓶中有一块碎玻璃,则溶质氯化钠的质量偏小,导致溶质质量分数偏小;故本选项错误;
故选A.点评:
本题考点: 一定溶质质量分数的溶液的配制;测量容器-量筒;称量器-托盘天平.
考点点评: 该题以溶液配制为载体,考查了错误或不规范操作引起的溶质质量分数变化的问题,解答时要认真分析错误操作导致的溶质或溶剂质量的改变,再结合溶质质量分数的计算公式,最后作出正确判断.1年前查看全部
- (2009•维扬区模拟)保大灾后无大疫,四川汶川大地震后,医务人员在灾区使用了大量的消毒液,其中有一种消毒液叫次氯酸钠(
(2009•维扬区模拟)保大灾后无大疫,四川汶川大地震后,医务人员在灾区使用了大量的消毒液,其中有一种消毒液叫次氯酸钠(次氯酸钠的化学式为NaClO).关于次氯酸钠的说法错误的是( )
A.NaClO由三种元素组成
B.NaClO中氯元素的质量分数为47.65%
C.NaClO的相对分子质量为74.5 g
D.NaClO中含有NaCl,故可代替食盐来使用 qiyuanfei1年前1
qiyuanfei1年前1 -
 易风之 共回答了25个问题
易风之 共回答了25个问题 |采纳率96%解题思路:A、根据次氯酸钠的化学式为NaClO分析其元素组成;
B、根据根据某元素的质量分数=[该元素原子的相对原子质量的总和/物质的相对分子质量]×100%分析即可;
C、根据相对分子质量的概念进行分析即可;
D、次氯酸钠是一种化合物,不是混合物,据此判断.A、根据次氯酸钠的化学式为NaClO可知,次氯酸钠由三种元素组成,故A说法正确;
B、NaClO中氯元素的质量分数为[35.5/23+35.5+16]×100%=47.65%,故B说法正确.
C、物质的相对分子质量没有单位千克,故C说法错误;
D、次氯酸钠是一种化合物,不是混合物,次氯酸钠和食盐的性质不同.故D说法错误.
故选CD.点评:
本题考点: 物质的元素组成;相对分子质量的概念及其计算;元素的质量分数计算.
考点点评: 此题主要考查根据化学式判断组成元素的种类、求化合物中某元素的质量分数及物质的相对分子质量等知识点,此题为基础题,需学生会熟练分析掌握.1年前查看全部
- (2009•维扬区模拟)说法正确的是( )
(2009•维扬区模拟)说法正确的是( )
A.地壳中含量最多的元素是铝
B.工业制氧气过程是化学变化
C.镁在氧气中比在空气中燃烧剧烈,有耀眼白光,并生成白色固体
D.用肥皂水鉴别硬水、软水时,硬水产生泡沫较多 沙鳗1年前1
沙鳗1年前1 -
 没有过客之冬天雪 共回答了18个问题
没有过客之冬天雪 共回答了18个问题 |采纳率94.4%解题思路:A、根据地壳中元素的含量分析;
B、根据化学变化的特征分析工业制氧气过程;
C、根据镁在氧气中燃烧的现象分析;
D、根据硬水、软水中含有的成分分析.A、地壳中含量最多的元素是氧,故A错误;
B、在工业制氧气过程中没有其他物质生成,属于物理变化,故B错误;
C、镁在氧气中比在空气中燃烧剧烈,有耀眼白光,并生成白色固体,故C正确;
D、由于硬水中含有较多的钙、镁俩字的化合物,在加入肥皂水时产生的浮渣多,泡沫少,故D错误.
故选C.点评:
本题考点: 地壳中元素的分布与含量;氧气与碳、磷、硫、铁等物质的反应现象;硬水与软水;化学变化和物理变化的判别.
考点点评: 本题所考查的知识都是课本的基础知识,应加强基础知识的学习和积累.1年前查看全部
- (2009•维扬区模拟)下图所示为实验室常用的制取气体的实验装置:
(2009•维扬区模拟)下图所示为实验室常用的制取气体的实验装置:
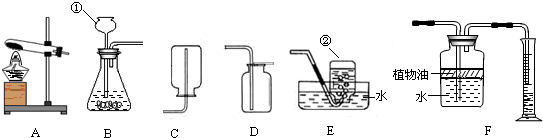
据此回答下列问题:
(1)写出带标号仪器的名称:①______②______.
(2)实验室通常用高锰酸钾制取氧气,该反应的化学方程式为2KMnO4
K2MnO4+MnO2+O2↑△ .2KMnO4,选用的发生装置是______(填字母,下同),以高锰酸钾作试剂利用此装置制氧气时,装置应作的改进是______.用过氧化氢溶液和二氧化锰混合制取氧气的化学方程式是
K2MnO4+MnO2+O2↑△ .2H2O2
2H2O+O2↑MnO2 .2H2O2.
2H2O+O2↑MnO2 .
(3)实验室用稀盐酸和石灰石反应制取CO2时,选用的收集装置是______.F装置可用来测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是______. 褪色的照片1年前1
褪色的照片1年前1 -
 伊人有情 共回答了21个问题
伊人有情 共回答了21个问题 |采纳率90.5%解题思路:(1)根据装置图及仪器的作用,辨识常用仪器并正确写出仪器的名称;
(2)高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰和氧气,需要选取装置A作为反应的发生装置;分解过程中高锰酸钾的小颗粒会随氧气流出试管,因此通常在试管口放一团棉花对气体进行过滤;使用二氧化碳催化过氧化氢分解生成水和氧气,此反应也可用于制取氧气;
(3)根据二氧化碳密度大于空气且能溶于水,在收集二氧化碳时只能使用向上排空气法收集;采取F装置测量二氧化碳的体积时,为避免二氧化碳溶于水或与水反应而影响体积的测量,应使二氧化碳不能直接接触装置内的水,可采取油层隔离水与二氧化碳的接触.(1)仪器①为向装置内添加液体反应物的长颈漏斗;仪器②为用于收集气体的集气瓶;
故答案为:长颈漏斗;集气瓶;
(2)高锰酸钾在加热条件下,分解生成锰酸钾、二氧化锰和氧气,需要选择可用于加热的A装置用作发生装置;该装置的试管口应放置一团棉花,防止高锰酸钾进入导管;在二氧化锰催化下,过氧化氢分解生成水和氧气;
故答案为:2KMnO4
△
.
K2MnO4+MnO2+O2↑;A;在试管口放一团棉花;2H2O2
MnO2
.
2H2O+O2↑;
(3)利用二氧化碳密度大于空气而能溶于水的性质,可采取D装置的向上排空气法收集二氧化碳;为防止二氧化碳溶解于F装置中的水中而影响对气体二氧化碳体积的测量,在水面放一层油以隔离二氧化碳与水的接触;
故答案为:D;防止CO2溶于水(或防止CO2与水反应、防止CO2与水接触).点评:
本题考点: 氧气的制取装置;量气装置;常用仪器的名称和选用;二氧化碳的实验室制法;书写化学方程式、文字表达式、电离方程式.
考点点评: 根据制取气体的反应选择发生装置时,依据反应所需要药品的状态和反应条件进行判断;发生装置分为:固液不需加热型和对固体加热型两种发生装置.1年前查看全部
- (2009•维扬区模拟)在一定量的稀盐酸中逐滴加入下列物质至过量,其对应的曲线变化(V为加入溶液的体积)正确的是( )
(2009•维扬区模拟)在一定量的稀盐酸中逐滴加入下列物质至过量,其对应的曲线变化(V为加入溶液的体积)正确的是( )
A.
B.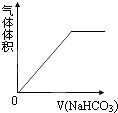
C.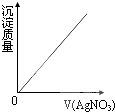
D.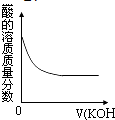
 zuigeji1年前1
zuigeji1年前1 -
 angliel 共回答了26个问题
angliel 共回答了26个问题 |采纳率92.3%解题思路:盐酸显酸性,可以与氢氧化钾反应生成氯化钾和水,与硝酸银溶液反应生成氯化银沉淀和硝酸,与碳酸钠反应生成二氧化碳气体,据此分析解答即可.A、盐酸显酸性,其pH小于7,而图象显示开始时pH大于7,故A错误;
B、盐酸与硝酸银反应生成不溶水的氯化银沉淀,当加入的硝酸银把盐酸反应完全后,沉淀质量不再增加,故B正确;
C、碳酸氢钠可以与盐酸反应生成二氧化碳气体,当加入的碳酸钠把盐酸反应完全后,气体的体积不再增加,故C错误;
D、向盐酸中加入氢氧化钾溶液,二者会反应生成氯化钾和水,盐酸不断被消耗,故其溶质的质量分数不断减小,当盐酸完全被消耗尽,其质量分数变为零,故D错误,
故选B.点评:
本题考点: 酸的化学性质;溶液的酸碱性与pH值的关系.
考点点评: 本题考查了盐酸的化学性质,完成此题,可以依据盐酸的性质进行.1年前查看全部
- (2009•维扬区模拟)下列各组物质的溶液混合后,最终不一定有沉淀生成的是( )
(2009•维扬区模拟)下列各组物质的溶液混合后,最终不一定有沉淀生成的是( )
A. Ba(OH)2H2SO4HCl
B. CuCl2Ba(NO3)2CaCl2
C. BaCl2Na2CO3HNO3
D. AgNO3H2SO4HCl 等待VSoo1年前3
等待VSoo1年前3 -
 creaze110 共回答了14个问题
creaze110 共回答了14个问题 |采纳率92.9%解题思路:A、根据氢氧化钡与硫酸反应生成硫酸钡沉淀和水,其中硫酸钡既不溶于水不也不溶于酸进行解答;
B、根据CuCl2Ba(NO3)2CuCl2溶液混合没有水、气体、和沉淀生成,所以不反应进行解答;
C、根据氯化钡与碳酸钠反应生成碳酸钡沉淀,碳酸钡能与稀硝酸反应生成硝酸钡、水和二氧化碳进行解答;
D、根据硝酸银和盐酸反应生成氯化银白色沉淀和硝酸,其中氯化银不溶于水也不溶于酸进行解答.A、氢氧化钡与硫酸反应生成硫酸钡沉淀和水,其中硫酸钡既不溶于水不也不溶于稀盐酸,所以Ba(OH)2、H2SO4、HCl溶液混合后可生成BaSO4沉淀;故A一定有沉淀生成;
B、CuCl2Ba(NO3)2CaCl2溶液混合没有水、气体、和沉淀生成,所以不反应;故B一定没有沉淀生成;
C、BaCl2、Na2CO3、HNO3溶液混合BaCl2与Na2CO3可生成BaCO3沉淀,生成的BaCO3沉淀又可与HNO3反应生成Ba(NO3)2、H2O和CO2;若HNO3量不足则会有沉淀生成,若HNO3过量则不会有沉淀生成;故C不一定有沉淀生成;
D、硝酸银和盐酸反应生成氯化银白色沉淀和硝酸,其中氯化银不溶于水也不溶于酸,AgNO3、H2SO4、HCl溶液混合后可生成AgCl沉淀;故D一定有沉淀生成;
故选C.点评:
本题考点: 复分解反应及其发生的条件.
考点点评: 既不溶于水也不能溶于酸的白色沉淀为硫酸钡或氯化银;其它不溶于水的沉淀都可与酸反应而消失.1年前查看全部
- (2009•维扬区模拟)(1)图甲是两种元素在周期表中的信息,图乙是氟原子的原子结构示意图.
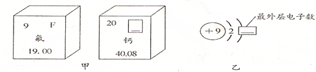
(2009•维扬区模拟)(1)图甲是两种元素在周期表中的信息,图乙是氟原子的原子结构示意图.
请完成下列问题:
①图甲方框的横线上填的是______,图乙方框横线上的数字是______;
②图甲所示两种元素形成化合物的化学式为______.
(2)学好化学能使我们更好地认识各种现象,更轻松、合理地解决实际问题.请回答:
①家里炒菜时油锅着火,最好的灭火方法是______;
②有的胃病患者胃酸过多,常服用一些含氢氧化铝的药物,有关反应的化学方程式为______. ngsn0trjkkfd0ng1年前1
ngsn0trjkkfd0ng1年前1 -
 新进小虫 共回答了16个问题
新进小虫 共回答了16个问题 |采纳率87.5%解题思路:(1)①正确书写元素符号即可;根据在原子中,原子序数=质子数=核电荷数=核外电子数,进行解答;
②根据化合物化学式的书写步骤:归类→定序→标价→交叉→约简,进行解答;
(2)①根据灭火的原理和方法:清除可燃物或使可燃物与其他物品隔离;隔绝氧气或空气;如油锅着火时,可盖严锅盖;使温度降低着火点以下;进行解答;
②根据书写化学方程式的步骤:写配注等,正确书写方程式即可.(1)①图甲方框的横线上填的是元素的元素符号:Ca,
根据在原子中,原子序数=质子数=核电荷数=核外电子数,可知图乙方框横线上的数字是:9-2=7;
故答案为:Ca;7;
②根据化合物化学式的书写步骤,氟元素的化合价为-1价,钙元素的化合价为+2价,形成化合物的化学式
为:CaF2;故答案为:CaF2 ;
(2)①根据灭火的原理和方法,油锅着火,最好的灭火方法是:盖严锅盖,隔绝氧气或空气,达到灭火的目的;或立即放入切好的菜,能降低油的温度到着火点以下,从而达到灭火的目的;
故答案为:盖严锅盖(或立即放入切好的菜);
②根据书写化学方程式的步骤,胃病患者服用含氢氧化铝药物的化学方程式为:Al(OH)3+3HCl=AlCl3+3H2O;
故答案为:Al(OH)3+3HCl=AlCl3+3H2O.点评:
本题考点: 元素周期表的特点及其应用;酸碱盐的应用;灭火的原理和方法.
考点点评: 本题考查学生在原子中,原子序数=质子数=核电荷数=核外电子数,及化学式、化学方程式正确书写的方法掌握与应用.1年前查看全部
- 扬州市维扬区2008年小学六年级语文调研试卷答案
 yuanluning1年前3
yuanluning1年前3 -
 外一半 共回答了21个问题
外一半 共回答了21个问题 |采纳率90.5%我不在扬州市维扬区!1年前查看全部
- (2009•维扬区模拟)已知某两种物质在光照条件下能发生化学反应,其微观示意图如图:
(2009•维扬区模拟)已知某两种物质在光照条件下能发生化学反应,其微观示意图如图:

则下列说法正确的是( )
A.图示中共有4种分子
B.该反应属于化合反应
C.图示中的反应物都是单质
D.该图示不符合质量守恒定律 报料王1年前1
报料王1年前1 -
 zmh1005 共回答了22个问题
zmh1005 共回答了22个问题 |采纳率90.9%解题思路:依据单质含有一种元素,化合物含有多种元素,因此从图示分析,该反应是反应物是一种化合物和一种单质,生成物是两种化合物,根据反应特点,不属于化合,分解,置换,复分解中的任何一中反应类型,该反应在发生时反应前后原子的种类和个数均未变化,故一定会遵循质量守恒定律.A、图示中反应物有两种,生成物有两种,共四种物质,四物质均有不同的分子构成含四种分子,故此说法正确.
B、图示中的生成物是两种化合物,不符合化合反应“多变一”的特征,故此说法错误.
C、因为该反应的反应物中含一种单质和一种化合物,故此说法错误.
D、反应前后原子的数目不变,符合质量守恒定律,故此说法错误.
故选A.点评:
本题考点: 微粒观点及模型图的应用;单质和化合物的判别;反应类型的判定;质量守恒定律及其应用.
考点点评: 分子由原子构成,构成不同的分子属于不同种物质的分子,由同种原子构成的分子属于单质分子,由不同种原子构成的分子属于化合物的分子.1年前查看全部
- (2009•维扬区模拟)下列各组物质的溶液混合后,最终不一定有沉淀生成的是( )
(2009•维扬区模拟)下列各组物质的溶液混合后,最终不一定有沉淀生成的是( )
A. Ba(OH)2H2SO4HCl
B. CuCl2Ba(NO3)2CaCl2
C. BaCl2Na2CO3HNO3
D. AgNO3H2SO4HCl gavin75151年前1
gavin75151年前1 -
 预期幸福 共回答了16个问题
预期幸福 共回答了16个问题 |采纳率93.8%解题思路:A、根据氢氧化钡与硫酸反应生成硫酸钡沉淀和水,其中硫酸钡既不溶于水不也不溶于酸进行解答;
B、根据CuCl2Ba(NO3)2CuCl2溶液混合没有水、气体、和沉淀生成,所以不反应进行解答;
C、根据氯化钡与碳酸钠反应生成碳酸钡沉淀,碳酸钡能与稀硝酸反应生成硝酸钡、水和二氧化碳进行解答;
D、根据硝酸银和盐酸反应生成氯化银白色沉淀和硝酸,其中氯化银不溶于水也不溶于酸进行解答.A、氢氧化钡与硫酸反应生成硫酸钡沉淀和水,其中硫酸钡既不溶于水不也不溶于稀盐酸,所以Ba(OH)2、H2SO4、HCl溶液混合后可生成BaSO4沉淀;故A一定有沉淀生成;
B、CuCl2Ba(NO3)2CaCl2溶液混合没有水、气体、和沉淀生成,所以不反应;故B一定没有沉淀生成;
C、BaCl2、Na2CO3、HNO3溶液混合BaCl2与Na2CO3可生成BaCO3沉淀,生成的BaCO3沉淀又可与HNO3反应生成Ba(NO3)2、H2O和CO2;若HNO3量不足则会有沉淀生成,若HNO3过量则不会有沉淀生成;故C不一定有沉淀生成;
D、硝酸银和盐酸反应生成氯化银白色沉淀和硝酸,其中氯化银不溶于水也不溶于酸,AgNO3、H2SO4、HCl溶液混合后可生成AgCl沉淀;故D一定有沉淀生成;
故选C.点评:
本题考点: 复分解反应及其发生的条件.
考点点评: 既不溶于水也不能溶于酸的白色沉淀为硫酸钡或氯化银;其它不溶于水的沉淀都可与酸反应而消失.1年前查看全部
- (2009•维扬区模拟)如图是一幅贴在汽车加油站上的宣传广告.围绕这幅广告画以下叙述错误的是( )
(2009•维扬区模拟)如图是一幅贴在汽车加油站上的宣传广告.围绕这幅广告画以下叙述错误的是( )

A.玉米汁可用作汽车燃料
B.由玉米生产的酒精汽油可作汽车燃料
C.推广玉米生产的燃料可在一定程度上缓解当前的能源危机
D.以农作物为原料来生产化学品是可行的 bill_wfm1年前1
bill_wfm1年前1 -
 movemovemove 共回答了9个问题
movemovemove 共回答了9个问题 |采纳率100%解题思路:A、玉米汁不能用作汽车燃料;
B、玉米通过发酵可以得到酒精,酒精和汽油的混合物相对于汽油来说是一种比较清洁的燃料;
C、推广玉米生产的燃料对节能环保方面具有重要的意义;
D、以农作物为原料可以得到酒精等化工原料.A、玉米汁不能用作汽车燃料,该广告是说通过农作物发酵可以得到燃料.错误;
B、由玉米生产的酒精汽油可作汽车燃料.正确;
C、推广玉米生产的燃料可在一定程度上缓解当前的能源危机.正确;
D、以农作物为原料来生产化学品是可行的.正确.
故选A.点评:
本题考点: 常用燃料的使用与其对环境的影响.
考点点评: 本题主要考查节能环保方面的知识,解答时要充分理解广告的含义,要把能量转化和节能环保联系起来理解.1年前查看全部
大家在问
- 1回忆随流水逝去 的英语怎么说如题所示.
- 2四棱台的表面积斜高上底边长10和8,下底边长16和20,高是2斜高和表面积怎么求?最好有图啊..
- 3新概念第2册 78课文
- 4Listen ang choose the right picture是什么意思
- 5将F=8N的力分解为F1、F2,其中F1=4N,则F2不可能是( )
- 6若二元一次方程3x+4y=0,-3x+2y=-18和2x-my=-1有公共解,则m=
- 7《过松源晨炊漆公店 》中体现上山下山后又要上山下山的感受的句子是哪句?
- 8反应物或生成物有固体,怎么判断化学平衡
- 9求英语作文:I Love ZhengZhou
- 10《白雪歌送武判官归京》中表现作者送别友人后依依不舍和无限怅惘之情的句子是哪一句?
- 11我有一道较难的物理题目现在有两个开关,一个灯泡,能否设计一个这样的电路图:当两个开关同时闭合或同时断开时,灯泡会不亮;当
- 12how to build up your confidence in english
- 13某土建工程动用15台挖运土机械,每台机械每小时能挖土3㎡或运土2m³,为了使挖土的工作和运土的工作同时结束,如
- 14第4的第二小题,第五题,
- 15How to use a computer properly
