LiFePO4(磷酸亚铁锂)是可充电电池的电极材料,其中含有______种非金属元素,已知PO4的化合价为-3,则氢氧化
 无晓舞4465326082022-10-04 11:39:541条回答
无晓舞4465326082022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 棉花糖毛毛兔 共回答了20个问题
棉花糖毛毛兔 共回答了20个问题 |采纳率95%- 解题思路:根据元素的分类进行分析磷酸亚铁锂中有几种非金属元素;根据化合物中正负化合价的代数和为零的原则计算出锂元素的化合价,然后利用化合价书写化学式的方法分析氢氧化锂的化学式;根据物质中某元素的质量分数的计算公式进行分析铁的氧化物的化学式.
磷酸亚铁锂是由锂、铁、磷和氧四种元素组成的,其中磷、氧属于非金属元素;根据化合物中正负化合价的代数和为零的原则,亚铁显-2价,设磷酸亚铁锂中锂元素的化合价是x,则x+(+2)+(-3)=0,解得x+1,因此氢氧化锂的化学式应表示为LiOH;设铁的氧化物的化学式为FexOy,则[56x/56x+16y]×50%=[56/158],解得[x/y]=[16/23],因此铁的氧化物的化学式是Fe16O23
故答案为:2;LiOH;Fe16O23点评:
本题考点: 元素的简单分类;化学式的书写及意义;有关化学式的计算和推断.
考点点评: 本题考查了元素的分类、化合价以及物质中某元素的质量分数等有关知识,难度不大. - 1年前
相关推荐
- (2014•武汉模拟)锂的化合物用途广泛.Li3N是非常有前途的储氢材料;LiFePO4、Li2FeSiO4等可以作为电
(2014•武汉模拟)锂的化合物用途广泛.Li3N是非常有前途的储氢材料;LiFePO4、Li2FeSiO4等可以作为电池的正级材料.回答下列问题:
(1)将锂在纯氮气中燃烧可制得Li3N,其反应的化学方程为6Li+N2
2Li3N点燃 .6Li+N2.
2Li3N点燃 .
(2)氮化锂在氢气中加热时可得到氨基锂(LiNH2),其反应的化学方程式为:Li3N+2H2
LiNH2+2LiH,氧化产物为______(填化学式).在270℃时,该反应可逆向发生放出H2,因而氮化锂可作为储氢材料,储存氢气最多可达Li3N质量的______%(精确到0.1).△ .
(3)将Li2CO3、FeC2O4•2H2O和SiO2粉末均匀混合,在800℃的氩气中烧结6小时制得Li2FeSiO4,写出反应的化学方程式Li2CO3+FeC2O4•2H2O+SiO2
Li2FeSiO4+CO↑+CO2↑+2H2O高温 .Li2CO3+FeC2O4•2H2O+SiO2,制备Li2FeSiO4的过程必须在惰性气体氛围中进行,其原因是______.
Li2FeSiO4+CO↑+CO2↑+2H2O高温 .
(4)将一定浓度磷酸二氢铵、氯化锂混合溶液作为电解液,以铁棒为阳极,石墨为阴极,电解析出LiFePO4沉淀,阳极的电极反应式为______.
(5)磷酸亚铁锂电池充放电过程中,发生LiFePO4与Li1-xFePO4之间的转化,电池放电时负极发生的反应为
LixC6-xe-═xLi++6C,写出电池放电时反应的化学方程式______. yemmihhy7091年前1
yemmihhy7091年前1 -
 小小笑话 共回答了14个问题
小小笑话 共回答了14个问题 |采纳率78.6%(1)锂与氮气在点燃条件下与氮气发生反应生成Li3N,该反应的化学方程式为:6Li+N2 点燃 . 2Li3N,故答案为:6Li+N2 点燃 . 2Li3N;(2)反应Li3N+2H2△.&nb...1年前查看全部
- LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠,已知P的化合价为+5价,则LiFePO4中Fe的
LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠,已知P的化合价为+5价,则LiFePO4中Fe的化合价为( )
【注:LiFePO4中的4在右下角】
A.+1
B.+2
C.+3
D.+4 schoolboy_19771年前5
schoolboy_19771年前5 -
 pioupiou 共回答了25个问题
pioupiou 共回答了25个问题 |采纳率96%Li +1价,P +5价,O -2价
所以+1+x+5-2×4=0
得到Fe是+2价
也可以一起考虑PO4是-3价(磷酸根是-3价),Li+1价,Fe自然是+2价1年前查看全部
- 写出电极反应 1.Li+FePO4=LiFePO4 2.CH3OH碱性燃料电池
 吃好吃好1年前4
吃好吃好1年前4 -
 Rusty 共回答了16个问题
Rusty 共回答了16个问题 |采纳率87.5%总反应 Li + FePO4 = LiFePO4
负极:Li + e- = Li+
正极:FePO4 + e- + Li+ = LiFePO4
总反应 2CH3OH + 3 O2 + 4OH- = 2 CO32- + 6 H2O
正极:3 O2 + 12 e- + 6 H2O = 12 OH-
负极:2CH3OH - 12 e- + 16 OH- = 2 CO32- + 12 H2O
(必须配平电子得失数目)1年前查看全部
- 磷酸铁锂动力电池电池反应为LiFePO4→充电 ←放电 FePO4+Li 电池的正极材料是LiFePO4 负极材料是石墨
磷酸铁锂动力电池电池反应为LiFePO4→充电 ←放电 FePO4+Li 电池的正极材料是LiFePO4 负极材料是石墨,含Li+导电固体为电解质.已知金属锂是一种很活泼的碱金属,性质与钠相似.下列有关磷酸锂动力电池说法正确的是.
A.放电时正极材料质量减少
B.放电时电池内部Li+向负极移动
C.在锂电池的研发过程中,使用水溶液以降低成本将是一个重要的研究方向
D.充电时池阳极反应为LiFePO4=FePO4+Li+ +e- 哪里的那里1年前1
哪里的那里1年前1 -
 懂你369 共回答了19个问题
懂你369 共回答了19个问题 |采纳率84.2%答案选D.
A错,因为电池的正极材料是LiFePO4,而放电时生成 LiFePO4.故正极材料质量应增加.
B错,放电时负极失去的电子经外电路流入正极,故正极表面是带负电的,所以LI+是向正极方向移动.
C错,金属锂是一种很活泼的碱金属,性质与钠相似.而钠可以与水在常温剧烈反应,故锂也可以与冷水反应.所以该电池不可以用水作为溶剂.
D正确.充电时的阳极反应为氧化反应,该电极方程式是正确的.1年前查看全部
- LiFePO4,已知Li为+1价,则Fe的化合价为
LiFePO4,已知Li为+1价,则Fe的化合价为
LiFePO4,已知Li为+1价,则Fe的化合价为------ 100度C1年前2
100度C1年前2 -
 jtl9 共回答了18个问题
jtl9 共回答了18个问题 |采纳率94.4%原子团磷酸根PO4的化合价是-3价,其中P的化合价是+5价.
又已知Li是+1价,所以Fe是+2价1年前查看全部
- 已知LiFePO4新型锂离子动力电池放电时总反应式为FePO4+Li═LiFePO4,则下列有关说法不正确的是( )
已知LiFePO4新型锂离子动力电池放电时总反应式为FePO4+Li═LiFePO4,则下列有关说法不正确的是( )
A.放电时,正极反应为FePO4+Li++e-═LiFePO4
B.充电时,动力电池上标注“+”的电极反应与外接电源的正极相连
C.放电时,电池内部Li+向负极移动
D.充电时,阴极上Li+得到电子被还原 haifeng80711年前1
haifeng80711年前1 -
 真显 共回答了16个问题
真显 共回答了16个问题 |采纳率100%解题思路:原电池工作时,负极发生氧化反应,正极发生还原反应,阳离子向电源正极移动,阴离子向负极移动;充电时,电池正极与外接电源正极相连,电池负极与外接电源负极相连,以此解答该题.放电时,正极上FePO4得电子发生还原反应,电极反应式为:FePO4+Li++e-═LiFePO4,故A正确;
B.充电时动力电池上标注“+”的电极应与外接电源的正极相连,发生氧化反应:LiFePO4-e-=FePO4+Li+,故B正确;
C.放电时,电池内部Li+向正极移动,故C错误;
D.充电时,阴极上Li+得到电子被还原,发生还原反应,故D正确;
故选C.点评:
本题考点: 化学电源新型电池.
考点点评: 本题考查化学电源新型电池知识,本题难度不大,注意根据电池反应书写电极反应式的方法,以及离子的定向移动问题.1年前查看全部
- LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车.电池反应为:FePO4+Li LiFePO4,电
LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车.电池反应为:FePO4+Li LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含U导电固体为电解质.下列有关LiFePO4电池说法正确的是
A.可加入硫酸以提高电解质的导电性
B.放电时电池内部Li向负极移动.
C.充电过程中,电池正极材料的质量减少
D.放电时电池正极反应为:FePO4+Li++e-=LiFePO4
请说明理由 mama宝宝1年前2
mama宝宝1年前2 -
 MERRYASw 共回答了14个问题
MERRYASw 共回答了14个问题 |采纳率92.9%A不对因为Li是活泼的碱金属不能用活泼氢溶剂如水 乙醇 硫酸溶液做电解质
负极应含li
负极含锂故锂离子应向正极移动B错
充电时正极电解失去li离子质量减少
C D 正确
这是高三学的 你们课改了吧1年前查看全部
- LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车.电池反应为:FePO4+Li=LiFePO4,电
LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车.电池反应为:FePO4+Li=LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含U导电固体为电解质.下列有关LiFePO4电池说法正确的是( )
A.可加入硫酸以提高电解质的导电性
B.放电时电池内部Li+ 向负极移动.
C.充电过程中,电池正极材料的质量减少
D.放电时电池正极反应为:FePO4 + Li+ + e- =LiFePO4
这是一道双选题
 jmzhuang1年前5
jmzhuang1年前5 -
 MAGGIEWEI607 共回答了13个问题
MAGGIEWEI607 共回答了13个问题 |采纳率84.6%首先明确一点 充电 是电解池 放电 是 原电池
A加硫酸 和锂反应 错
B放电时负极产生大量的阳离子 Li+不可能 向负极移动 错
排除法 而且双选 则为CD1年前查看全部
- (2013•安庆二模)磷酸铁锂(LiFePO4)被认为是最有前途的锂离子电池正极材料.某企业利用富铁浸出液生成磷酸铁锂,
(2013•安庆二模)磷酸铁锂(LiFePO4)被认为是最有前途的锂离子电池正极材料.某企业利用富铁浸出液生成磷酸铁锂,开辟了处理硫酸亚铁废液一条新途径.其主要流程如下:
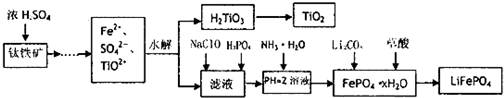
已知:H2LiO3是种难溶于水的物质.
(1)钛铁矿用浓硫酸处理之前,需要粉碎,其目的______
(2)TiO2+水解生成H2TiO3的离子方程式______
(3)加入NaClO发生反应的离子方程式______
(4)在实验中,从溶液中过滤出H2TiO3后,所得滤液浑浊,应如何操作______.
(5)为测定钛铁矿中铁的含量,某同学取经浓硫酸等处理的溶液(此时钛铁矿中的铁己全部转化为二价铁离子),采取KMnO4标准液滴定Fe2+的方法:(不考虑KMnO4与其他物质反应)在滴定过程中,若未用标准液润洗滴定管,则使测定结果______. (填“偏高、偏低、无影响”),滴定终点的现象______.滴定分析时,称取a g钛铁矿,处理后,用cmol/LKMnO4标准液滴定,消耗VmL,则铁元素的质量分数的表达式为[28cV/a]%[28cV/a]%. 寂寥散人1年前1
寂寥散人1年前1 -
 winner_ty 共回答了14个问题
winner_ty 共回答了14个问题 |采纳率100%解题思路:(1)根据接触面积对反应速率影响解答;
(2)TiO2+水解生成H2TiO3,同时生成氢离子;
(3)ClO-具有强氧化性,将Fe2+氧化为Fe3+,自身被还原为Cl-,酸性条件下,同时生成水;
(4)从溶液中过滤出H2TiO3后,所得滤液浑浊,需要更换过滤器,重新过滤;
(5)未用标准液润洗滴定管,导致消耗KMnO4溶液体积偏大,测定Fe2+的质量增大;滴定到达终点,滴入最后一滴KMnO4溶液,溶液颜色为紫红色,且半分钟内部不褪去;根据电子转移守恒,可得关系式:5Fe2+~KMnO4,据此计算.(1)将钛铁矿粉碎,可以增大表面积,增大浓硫酸的接触面积,加快反应速率,故答案为:增大表面积,增大浓硫酸的接触面积,加快反应速率;(2)TiO2+水解生成H2TiO3,同时生成氢离子,反应离子方程式为:TiO2++2H2O...
点评:
本题考点: 常见金属元素的单质及其化合物的综合应用;物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题考查化学工艺流程、对操作的理解评价、物质分离提纯、氧化还原反应滴定应用等,需要学生具备扎实的基础,综合考查学生分析解决问题的能力,难度中等.1年前查看全部
- (2013•宁德模拟)磷酸铁锂电池(LPF)是一种新型钮电池,其正极材料是LiFePO4,负极材料是石墨,含Li+导电固
(2013•宁德模拟)磷酸铁锂电池(LPF)是一种新型钮电池,其正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解质,化学方程式为:LiC+xFePO4
xLiFePO4+C.下列说法正确的是( )放电 充电
A.放电时,电池内部Li+向负极移动
B.放电时,FeP04得到电子
C.充电时,石墨电极接电源的正极
D.充电时,电解池阴极反应式为:Li++e-→Li hongqlyg1年前1
hongqlyg1年前1 -
 于成龙999 共回答了12个问题
于成龙999 共回答了12个问题 |采纳率91.7%解题思路:A、原电池中,电解质中的阳离子移向正极;
B、放电时,该装置是原电池,根据正极反应为:FePO4+Li++e-═LiFePO4来回答;
C、充电时,电池的正极和电源的正极相连;
D、充电时,电解池阴极发生得电子的还原反应,阴极反应和原电池中负极反应相反.A、原电池中,电解质中的阳离子移向正极,所以电池内部Li+向正极移动,故A错误;
B、放电时,该装置是原电池,正极反应为:FePO4+Li++e-═LiFePO4,即FeP04得到电子,故B正确;
C、充电时,电池的正极是LiFePO4,应该和电源的正极相连,故C错误;
D、充电时,电解池阴极发生得电子的还原反应,即Li++e-→Li,故D正确.
故选BD.点评:
本题考点: 化学电源新型电池.
考点点评: 本题考查化学电源新型电池知识,本题难度不大,注意根据电池反应书写电极反应式的方法,明确离子的定向移动问题.1年前查看全部
- 采用LiFePO4作正极的 磷酸铁锂电池的正负极方程式,和总反应式
 双双表昧1年前2
双双表昧1年前2 -
 海来阿衣思不模 共回答了29个问题
海来阿衣思不模 共回答了29个问题 |采纳率82.8%负极反应:C6Li-xe-==C6Li1-x+xLi+(C6Li表示锂原子嵌入石墨形成复合材料)
正极反应:Li(1-x)MO2 + xLi+ + xe- == LiMO2(LiMO2表示含锂的过渡金属氧化物)
把LiMO2改成LiFePO4就可以了1年前查看全部
- LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠.已知该电池放电时的电极反应式为:正极
LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠.已知该电池放电时的电极反应式为:正极 FePO4+Li++e-=LiFePO4; 负极 Li-e-=Li+ 下列说法中正确的是( )
A.充电时电池反应为FePO4+Li=LiFePO4
B.充电时动力电池上标注“+”的电极应与外接电源的正极相连
C.放电时电池内部Li+向正极移动
D.放电时,在正极上是Li+得电子被还原 Dolphin_in_sky1年前1
Dolphin_in_sky1年前1 -
 捣蛋安娜 共回答了9个问题
捣蛋安娜 共回答了9个问题 |采纳率77.8%解题思路:A、由原电池的电极反应得到电池反应,FePO4+Li=LiFePO4,充电时正好相反;
B、充电器的正极(+)与电池正极(+)连接,充电器的负极(-)与电池负极(-)连接;
C、放电时阳离子移向正极;
D、放电时原电池正极是铁元素化合价降低得到电子.A、依据原电池的电极反应得到电池反应,FePO4+Li=LiFePO4,充电时电池反应为LiFePO4=FePO4+Li,故A错误;
B、充电器的正极(+)与电池正极(+)连接,充电器的负极(-)与电池负极(-)连接,充电时动力电池上标注“+”的电极应与外接电源的正极相连,故B正确;
C、依据原电池的正极反应可知 FePO4+Li++e-═LiFePO4,放电时电池内部Li+向正极移动,故C正确;
D、原电池的正极反应可知 FePO4+Li++e-═LiFePO4,锂元素化合价未变,化合价变化的是铁元素得到电子,故D错误;
故选BC.点评:
本题考点: 常见化学电源的种类及其工作原理.
考点点评: 本题考查了原电池和电解池的工作原理的应用,主要是电极反应的性质分析,原电池电池反应和电解池电池反应的应用,理解原电池和电解池的基本原理是解题的关键.1年前查看全部
- (2014•鄂尔多斯一模)LiFePO4新型锂离子电池因其原材料丰富、对环境友好、循环性能和安全性能好的特点,具有广阔的
(2014•鄂尔多斯一模)LiFePO4新型锂离子电池因其原材料丰富、对环境友好、循环性能和安全性能好的特点,具有广阔的应用前景.已知该电池放电时的电极反应式为:正极:FePO4+Li++e-=LiFePO4,负极:Li-e-=Li+,下列说法中正确的是( )
A.充电时阳极反应为Li++e-=Li
B.充电时动力电池上标注“-”的电极应与外接电源的负极相连
C.放电时电池内部Li+向负极移动
D.放电时,在正极上是Li+得电子被还原 kbc51571年前1
kbc51571年前1 -
 zhangmwmcm 共回答了20个问题
zhangmwmcm 共回答了20个问题 |采纳率100%解题思路:根据电池反应可知,放电时LiFePO4电池负极反应为Li-e-═Li+,正极反应为FePO4+Li++e-═LiFePO4;充电时的阳极上LiFePO4失电子,阴极上Li+得电子,根据原电池和电解池的工作原理来回答.A、充电时,阳极上LiFePO4失电子,阴极上Li+得电子,则充电时阴极反应为Li++e-=Li,故A错误;
B、充电时,电池的负极上Li+离子得电子生成Li,所以动力电池上标注“-”的电极应与外接电源的负极相连,故B正确;
C、放电时,电池内部阳离子向正极移动,则Li+向正极移动,故C错误;
D、放电时,是原电池的工作原理,正极反应为:FePO4+Li++e-═LiFePO4,则在正极上是FePO4得电子被还原,故D错误;
故选B.点评:
本题考点: 化学电源新型电池.
考点点评: 本题考查化学电源新型电池知识,本题难度不大,注意根据电池反应书写电极反应式的方法,以及离子的定向移动问题.1年前查看全部
- LiFePO4中Fe的化合价是多少?
 yilagy011年前4
yilagy011年前4 -
 胡中耀 共回答了23个问题
胡中耀 共回答了23个问题 |采纳率87%+1 x -3
Li Fe PO4
+1+x+(-3)=0
x=+2
LiFePO4中Fe的化合价是+21年前查看全部
- LiFePO4(磷酸亚铁锂)是可充电电池的电极材料,其中含有______种非金属元素,已知PO4的化合价为-3,则氢氧化
LiFePO4(磷酸亚铁锂)是可充电电池的电极材料,其中含有______种非金属元素,已知PO4的化合价为-3,则氢氧化锂的化学式应表示为______.LiFePO4中铁的质量分数约为某铁的氧化物中铁的质量分数的50%,则该铁的氧化物化学式为______.(已知:Mr(LiFePO4)=158)
 快乐摩天轮1年前1
快乐摩天轮1年前1 -
 黄小明_ii 共回答了15个问题
黄小明_ii 共回答了15个问题 |采纳率100%解题思路:根据元素的分类进行分析磷酸亚铁锂中有几种非金属元素;根据化合物中正负化合价的代数和为零的原则计算出锂元素的化合价,然后利用化合价书写化学式的方法分析氢氧化锂的化学式;根据物质中某元素的质量分数的计算公式进行分析铁的氧化物的化学式.磷酸亚铁锂是由锂、铁、磷和氧四种元素组成的,其中磷、氧属于非金属元素;根据化合物中正负化合价的代数和为零的原则,亚铁显-2价,设磷酸亚铁锂中锂元素的化合价是x,则x+(+2)+(-3)=0,解得x+1,因此氢氧化锂的化学式应表示为LiOH;设铁的氧化物的化学式为FexOy,则[56x/56x+16y]×50%=[56/158],解得[x/y]=[16/23],因此铁的氧化物的化学式是Fe16O23
故答案为:2;LiOH;Fe16O23点评:
本题考点: 元素的简单分类;化学式的书写及意义;有关化学式的计算和推断.
考点点评: 本题考查了元素的分类、化合价以及物质中某元素的质量分数等有关知识,难度不大.1年前查看全部
大家在问
- 1they are such naughty boys
- 2may i help you ,yes please 还是thank for your help 答案是yes plea
- 3一个直角三角形三条边分别是8厘米10厘米6厘米.这个三角形的周长是多少?面积是多少?
- 4这是一个我们应该尽我们所能学好英语的时期.英语怎么说 要用到This was a time when……
- 5汉语译成英语:你必须准时到校(must 表示命令的语气,必须)
- 6有哪些古人可以用来作为作文材料?
- 7Jenny puts a new film ________ her&
- 85分之4时=多少分?
- 9有人知道有关PLC的英语文章吗?
- 10若关于x的不等式组x>m-1 x>m+2的解集是x大于-1,则m=?
- 11海市蜃楼的图像前后左右上下是否一样?
- 12浙江省嘉兴市秀洲区中山西路3288号博尔玛产业园B区9幢4楼 如何翻译成英文?
- 13某同学用伏安法测一节干电池的电动势和内阻,现备有下列器材:
- 14小林跟小刘是两师徒,两人工作所得四六分成.这个月他们工作的总额为3000块.但师傅小林工作时间为200小时,徒弟小刘工作
- 15有关星星的诗句;<<出师表>>表明感情线索的句子,诸葛亮志趣的句子
