硝酸铜与硫酸反应吗RT
 gelei1682022-10-04 11:39:541条回答
gelei1682022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 orchidww 共回答了18个问题
orchidww 共回答了18个问题 |采纳率100%- 肯定不反应,铜离子不能被氧化,各离子可以共存
- 1年前
相关推荐
- 高一化学题,求解答。一定量的铜与100ml一定浓度的硝酸恰好完全反应生成硝酸铜和NO、NO2、N2O4的混合气体,将该混
高一化学题,求解答。
一定量的铜与100ml一定浓度的硝酸恰好完全反应生成硝酸铜和NO、NO2、N2O4的混合气体,将该混合气体收集在集气瓶中,把集气瓶倒立在水中,通入4.48L的氧气(在标准状况下)可以使集气瓶充满溶液。则下列说法一定正确的是:
A.铜的质量为12.8g B.硝酸的物质的量浓度为12mol/L
C.体现酸性的硝酸为0.8mol D.被还原的硝酸为0.4mol
求解答过程。谢谢啊。。
 lisaloving99991年前1
lisaloving99991年前1 -
 xiaona_97 共回答了17个问题
xiaona_97 共回答了17个问题 |采纳率76.5%铜在反应过程中被氧化,硝酸中的+5价氮原子,被还原为一氧化氮二氧化氮四氧化二氮。
然后在集气瓶中,氮的氧化物被氧气所氧化,并全部转化为硝酸。
根据电子得失计算,可以知道,铜所被氧化失去的电子和氧气氧化氮氧化物得到的电子是相等的。氧气4.48L是0.2mol,得到电子0.8mol,所以铜的物质的量为0.4mol,即12.8g。
A是一定正确的。
而BCD由于硝酸和铜的...1年前查看全部
- 往硝酸银、硝酸铜和硝酸锌的混合溶液中加入一定量的铁粉,充分反应后,有金属析出,过滤后往滤渣中加入稀盐酸,有无色气体放出,
往硝酸银、硝酸铜和硝酸锌的混合溶液中加入一定量的铁粉,充分反应后,有金属析出,过滤后往滤渣中加入稀盐酸,有无色气体放出,则滤液中一定存在的物质是( )
A. 硝酸铜和硝酸亚铁
B. 硝酸亚铁和硝酸锌
C. 硝酸银和硝酸铜
D. 硝酸银和硝酸锌 的排练之中1年前1
的排练之中1年前1 -
 天外肥猪 共回答了16个问题
天外肥猪 共回答了16个问题 |采纳率87.5%解题思路:由题意“向只溶解有硝酸银、硝酸铜和硝酸锌的混合溶液中加入一定量的铁粉”,根据金属活动性顺序,可知活动性:锌>铁>铜>银,则会有铜或银被置换出来;金属活动性越差,被置换出来的可能性越大;因为“充分反应后溶液中仍有金属固体,过滤后往滤渣中加入盐酸,有无色气体放出”,则说明铁过量.根据金属活动性顺序,可知活动性:锌>铁>铜>银,则会有铜或银被置换出来;可知铁不会与硝酸锌溶液反应;因为过滤后往滤渣中加盐酸,铜、铁、银中只有铁能和盐酸反应放出气泡.所以滤渣中有铁.因为铁会与硝酸银和硝酸铜反应,所以滤液中就不能再有硝酸银和硝酸铜了,只有硝酸亚铁.则滤液中一定存在的物质是硝酸亚铁和硝酸锌.
故选:B.点评:
本题考点: 金属的化学性质.
考点点评: 熟记金属活动性顺序“K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au”及其应用原则,学会处理实际问题.1年前查看全部
- 某工厂的废水中含有硝酸银和硝酸铜两种溶质,为分别回收金属银和金属铜,先向溶液中加入足量的金属铜片,充分反应后,取出铜片;
某工厂的废水中含有硝酸银和硝酸铜两种溶质,为分别回收金属银和金属铜,先向溶液中加入足量的金属铜片,充分反应后,取出铜片;再加入一定量的铁粉.请回答下列问题.
(1)加入足量的金属铜片,充分反应后,发生反应的化学方程式为______;
(2)加入一定量的铁粉后,将反应的混合物过滤,得到滤液和滤渣,将滤渣洗涤、干燥,取少量滤渣向其中加入稀盐酸,没有明显现象.则滤渣中一定含有的物质是①______;滤液中一定含有的离子是②______. 3zhongdian1年前1
3zhongdian1年前1 -
 舞舞潇潇 共回答了18个问题
舞舞潇潇 共回答了18个问题 |采纳率94.4%解题思路:(1)根据化学方程式的书写方法进行书写;(2)因为是分别回收金属银和金属铜,所以先向溶液中加入足量的金属铜片,充分反应后,取出铜片过滤,得到银和硝酸铜溶液;再加入一定量的铁粉,是用铁与硝酸铜溶液反应,生成铜和硝酸亚铁,将滤渣洗涤、干燥,取少量滤渣向其中加入稀盐酸,没有明显现象,说明滤渣中没有铁,说明铁参加了反应,再进行分析即可.(1)反应物是铜和硝酸银,生成物是银和硝酸铜,用观察法配平,所以方程式是:Cu+2AgNO3=2Ag+Cu(NO3)2;
(2)因为是分别回收金属银和金属铜,所以先向溶液中加入足量的金属铜片,充分反应后,取出铜片过滤,得到银和硝酸铜溶液;再加入一定量的铁粉,是用铁与硝酸铜溶液反应,生成铜和硝酸亚铁,将滤渣洗涤、干燥,取少量滤渣向其中加入稀盐酸,没有明显现象,说明滤渣中没有铁,说明铁参加了反应,铁与硝酸铜溶液反应,生成铜和硝酸亚铁,所以滤渣中一定含有的物质是铜;滤液是硝酸亚铁溶液,所以滤液中一定含有的离子是Fe2+ 和NO3-.
故答案为:(1)Cu+2AgNO3=2Ag+Cu(NO3)2;(2)铜(Cu);Fe2+ 和NO3-.点评:
本题考点: 金属的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题关键是要熟悉化学方程式的书写方法,知道铁与硝酸铜反应生成铜和硝酸亚铁,熟记金属与盐反应需要满足的条件.1年前查看全部
- 硝酸铜固体受热分解,产物有氧化铜、二氧化氮和氧气,该反应的化学方程式怎么样写
 99845134211年前6
99845134211年前6 -
 虚拟的天堂 共回答了22个问题
虚拟的天堂 共回答了22个问题 |采纳率90.9%2Cu(NO3)2=△=2CuO+4NO2+O2
希望对你有所帮助!1年前查看全部
- 向硝酸铜和硝酸银的混合溶液中加入一定量的铁粉,充分反应后发现有少量金属析出,过滤后往滤液中滴加盐酸,有白色沉淀生成,则析
向硝酸铜和硝酸银的混合溶液中加入一定量的铁粉,充分反应后发现有少量金属析出,过滤后往滤液中滴加盐酸,有白色沉淀生成,则析出的少量金属为( )
A. Cu和Ag
B. Ag
C. Fe和Ag
D. Fe和Cu 小熊fxs1年前2
小熊fxs1年前2 -
 泡烂了 共回答了17个问题
泡烂了 共回答了17个问题 |采纳率94.1%解题思路:根据金属活动性,判断金属与盐溶液发生反应的关系.根据滤液与稀盐酸反应的现象,判断滤液的组成,并依据滤液中的金属离子判断析出金属;向滤液中滴加稀盐酸出现白色沉淀,说明滤液中含有硝酸银溶液;在硝酸银、硝酸铜的混合溶液中加入一定量的铁粉,根据金属活动性,铁粉首先与硝酸银反应,硝酸银被完全置换后,铁粉开始与硝酸铜进行置换反应;由于滤液中含有硝酸银,说明加入的铁粉不足,没能完全置换出溶液中的银离子,所以,析出的金属只有银.由以上分析可知:
A、由于溶液中含有银离子,析出的金属中不可能含有Cu.故A错误;
B、析出的少量金属为银.故B正确;
C、由于溶液中含有银离子,析出的金属中不可能含有Fe.故C错误;
D、由于溶液中含有银离子,析出的金属中不可能含有Fe和Cu.故D错误.
故选B.点评:
本题考点: 金属活动性顺序及其应用.
考点点评: 金属与盐的混合溶液反应时,置换反应按金属活动性由弱到强的顺序先后反应,首先把溶液中金属活动性最弱的金属从溶液中置换出来.1年前查看全部
- 某溶液含硝酸铜、硝酸银、硝酸钡三种溶质,为使上述三种物质分别转化为沉淀分离出来,现提供碳酸钠溶液、盐酸、氢氧化钠溶液三种
某溶液含硝酸铜、硝酸银、硝酸钡三种溶质,为使上述三种物质分别转化为沉淀分离出来,现提供碳酸钠溶液、盐酸、氢氧化钠溶液三种试剂,若要求每次只加一种试剂分离出一种沉淀,那么所加试剂的顺序应为______、______、______.
 黄钧1年前1
黄钧1年前1 -
 冰凉如水 共回答了14个问题
冰凉如水 共回答了14个问题 |采纳率85.7%解题思路:先分析Cu(N03)2、AgN03、Ba(N03)2三种物质与Na2C03溶液、稀盐酸、NaOH溶液三种试剂的反应情况,再使Cu(N03)2、AgN03、Ba(N03)2三种溶质中的阳离子分步沉淀出来,分析第一种物质必须只沉淀一种阳离子,第二种物质只能与剩余的两种物质中的一种阳离子反应生成沉淀.Na2C03溶液能将Cu(N03)2、AgN03、Ba(N03)2三种溶质中的阳离子全部沉淀依次生成碳酸铜沉淀、碳酸银沉淀、碳酸钡沉淀,又因要将Cu(N03)2、AgN03、Ba(N03)2三种溶质中的阳离子分步沉淀出来,故①Na2C03溶液只能放在最后,②稀盐酸只与硝酸银反应产生氯化银白色沉淀,故先选用②稀盐酸,③NaOH溶液能与Cu(N03)2、Ba(N03)2中的硝酸铜反应生成蓝色氢氧化铜沉淀,然后再用碳酸钠沉淀钡离子.
故答案:②③①点评:
本题考点: 混合物的分离方法;盐的化学性质.
考点点评: 本题考查了盐的性质,利用盐的性质将他们分步沉淀,考查了分析问题和解决问题的能力.1年前查看全部
- 稀硫酸和硝酸铜溶液哪个导电能力强
 琼美那珠1年前1
琼美那珠1年前1 -
 albert3418 共回答了16个问题
albert3418 共回答了16个问题 |采纳率93.8%溶液的导电能力与溶液中离子的浓度、离子所带的电荷数有关.
离子带的电荷数越多、离子浓度越大,溶液的导电能力越强.1年前查看全部
- 硝酸铜和稀盐酸不能反应原因是什么?不是生成HNO3要挥发吗 生成气体
 幸福如上帝1年前1
幸福如上帝1年前1 -
 柠檬vs樱桃 共回答了26个问题
柠檬vs樱桃 共回答了26个问题 |采纳率100%一般来说,一个酸与盐反,生成的酸的酸性要弱于参加反应的酸,盐酸与硝酸都是强酸,且后者的酸性强于前者,所以此反应不会发生;再浓硝酸才易挥发,同样,浓盐酸也易挥发,所以不能根据生成的酸易挥发就说能反应.1年前查看全部
- 含有硝酸银和硝酸铜溶液,加入一定量铁,过滤获得固体和溶液M,滴加稀盐酸无现象,M中含有的溶质是那些物质
 人面桃花红过1年前3
人面桃花红过1年前3 -
 red_blue 共回答了22个问题
red_blue 共回答了22个问题 |采纳率86.4%可能是硝酸铜和硝酸银,一定含硝酸亚铁,根据金属活动性顺序,铜在银前面,铁不会先置换铜,否则铜会置换银,所以固体可能是铜和银1年前查看全部
- 求硝酸铜的质子守恒,物料守恒,电荷守恒及其离子浓度大小顺序
 温州051年前1
温州051年前1 -
 wasshohoku 共回答了21个问题
wasshohoku 共回答了21个问题 |采纳率81%电荷守恒:2c(Cu2+)+c(H+)=c(NO3-)+c(OH-)
物料守恒:c(Cu2+)+c(Cu(OH)2)=c(NO3-)/2
质子守恒:c(H+)=c(OH-)+2c(Cu(OH)2)
离子浓度:c(NO3-)>c(Cu2+)>c(H+)>c(OH-)1年前查看全部
- 把铁粉、锌粉放入硝酸银和硝酸铜的混合液中,充分反应后过滤,滤出的金属中一定含有( )
把铁粉、锌粉放入硝酸银和硝酸铜的混合液中,充分反应后过滤,滤出的金属中一定含有( )
A. Fe
B. Cu
C. Ag
D. Cu和Ag mt78945612301年前4
mt78945612301年前4 -
 匣中尺水 共回答了18个问题
匣中尺水 共回答了18个问题 |采纳率83.3%解题思路:根据四种金属活动性由强到弱的顺序:锌铁铜银,当把铁粉、锌粉加入到硝酸铜和硝酸银的混合溶液中时,银首先被锌置换出来,在银完全置换后,铜才能被置换出来;当锌反应完后铁再和混合溶液反应.四种金属活动性由强到弱的顺序:锌铁铜银,当把铁粉、锌粉加入到硝酸铜和硝酸银的混合溶液中时,锌先置换硝酸银中的银,当银被完全置换之后再置换硝酸铜中的铜,当锌完全反应完,混合溶液中还有硝酸银或硝酸铜时铁再与它们反应.因此滤出的金属中一定含有银.
故选C点评:
本题考点: 金属活动性顺序及其应用.
考点点评: 金属放入盐的混合溶液中,总是把活动性最弱的金属最先置换完,再按由弱到强的顺序一一进行置换.1年前查看全部
- 硝酸铜和生石灰反应方程式
 j0o0ja1年前3
j0o0ja1年前3 -
 wanjia734 共回答了18个问题
wanjia734 共回答了18个问题 |采纳率94.4%CaO+H2O+Cu(NO3)2=Cu(OH)2↓+Ca(NO3)21年前查看全部
- 在硝酸铜溶液中按2:1的比例加入尿素溶液这句话怎么理解,谁是2,谁是1?
 bobo858181年前1
bobo858181年前1 -
 guckicghkhgcgch 共回答了16个问题
guckicghkhgcgch 共回答了16个问题 |采纳率81.3%这里的2:1应该是指体积比.
2是硝酸铜,1是尿素.
2:1加入的意思是:
2体积硝酸铜溶液中加入1体积尿素溶液中.
至于溶液的浓度,应该会有说明吧?1年前查看全部
- 向硝酸银和硝酸铜的混合溶液中加入一定量的铁粉,充分反应后发现有少量金属析出,过滤后向滤液中插入一根铜丝,有银白色固体生成
向硝酸银和硝酸铜的混合溶液中加入一定量的铁粉,充分反应后发现有少量金属析出,过滤后向滤液中插入一根铜丝,有银白色固体生成,则过滤时滤出的固体为
A,Fe和Cu B.Fe和Ag C.Ag D.Cu和Ag
为什么? huaweikm1年前1
huaweikm1年前1 -
 moon3174 共回答了15个问题
moon3174 共回答了15个问题 |采纳率93.3%D 第一个反应生成铜 第二个反应生成白银1年前查看全部
- 下列各组物质能在pH=1的无色溶液中大量共存的是A硝酸钾、硝酸铜、氯化钠B碳酸钠、硝酸钾、氯化氨C硫酸...
下列各组物质能在pH=1的无色溶液中大量共存的是A硝酸钾、硝酸铜、氯化钠B碳酸钠、硝酸钾、氯化氨C硫酸...
下列各组物质能在pH=1的无色溶液中大量共存的是A硝酸钾、硝酸铜、氯化钠B碳酸钠、硝酸钾、氯化氨C硫酸镁、硝酸钠、氯化钾.为什么这么做? 01cjj1年前3
01cjj1年前3 -
 chibaol 共回答了13个问题
chibaol 共回答了13个问题 |采纳率84.6%选C,pH=1含有大量的H+,无色溶液要求不能含有有色离子,大量共存要求不能反应.
A.不可能,Cu(NO3)2是蓝色的.
B.不可能,2H+ +CO32-=H2O+CO2↑
C.可以共存,没有有色离子.1年前查看全部
- 氢氧化铜,氯化铜,硝酸铜,硫酸铜溶液都是蓝色的吗,哪些不是
 cwapril_431年前2
cwapril_431年前2 -
 xyq010045 共回答了25个问题
xyq010045 共回答了25个问题 |采纳率80%氯化铜,硝酸铜,硫酸铜溶液都是蓝色的
氢氧化铜不溶于水,不会形成溶液,而是以固体形式存在,其颜色为蓝色固体.1年前查看全部
- 硝酸铜溶液的颜色是什么硝酸铜颜色
 feihu98991年前1
feihu98991年前1 -
 一粟粟 共回答了19个问题
一粟粟 共回答了19个问题 |采纳率89.5%纯净的溶液是蓝色.但用浓硝酸制取时混入棕色的NO2气体溶解其中,溶液可能呈绿色.
蓝色是[Cu(H2O)4]2+的颜色.水过量时形成的[Cu(H2O)6]2+也是蓝色的.
----
溶液中含有铜离子,并非一定为蓝色.例如浓CuCl2溶液中,[Cu(H2O)4]2+显蓝色,[CuCl4]2-显绿色,它们共存时的混合色则为绿色,所以浓的CuCl2溶液显绿色.1年前查看全部
- 化学式的书写硝化钠 氢氧化钙 硝酸硝化镁 氢氧化铁 硝酸银硝化镁 氢氧化亚铁 硝酸钡硝酸铜 硫化铜 硝酸钾硝酸钙 氢氧化
化学式的书写
硝化钠 氢氧化钙 硝酸
硝化镁 氢氧化铁 硝酸银
硝化镁 氢氧化亚铁 硝酸钡
硝酸铜 硫化铜 硝酸钾
硝酸钙 氢氧化铜 硝酸铵
硫酸钠 氢氧化镁 硝酸钠
硫酸氢钠 氢氧化铝 碳酸氢钠
硫酸镁 氢氧化钡 碳酸钙
硫酸钙 氢氧化钠 碳酸银
硫酸钡 氯酸钾 碳酸镁
硫酸铝 盐酸 碳酸氢铵
硫酸铜 碳酸
硫酸钾 磷酸
硫酸铵 硫酸铁
硫酸亚铁 亚硫酸铁 好像有点多哦.不过, 胖胖之家50341年前3
胖胖之家50341年前3 -
 找人1 共回答了19个问题
找人1 共回答了19个问题 |采纳率100%硝化钠 NaNO3 氢氧化钙 Ca(OH)2 硝酸HNO3
硝化镁Mg(NO3)2 氢氧化铁Fe(OH)3 硝酸银AgNO3
硝化镁 Mg(NO3)2 氢氧化亚铁 Fe(OH)2 硝酸钡Ba(NO3)2
硝酸铜 Cu(NO3)2 硫化铜 CuS 硝酸钾KNO3
硝酸钙 Ca(NO3)2 氢氧化铜Cu(OH)2 硝酸铵NH4NO3
硫酸钠 Na2SO4 氢氧化镁 Mg(OH)2 硝酸钠NaNO3
硫酸氢钠 NaHSO4 氢氧化铝Al(OH)3 碳酸氢钠NaHCO3
硫酸镁 MgSO4 氢氧化钡 Ba(OH)2 碳酸钙CaCO3
硫酸钙 CaSO4 氢氧化钠 NaOH 碳酸银Ag2CO3
硫酸钡 BaSO4 氯酸钾 KClO3 碳酸镁MgCO3
硫酸铝 Al2(SO4)3 盐酸 HCl 碳酸氢铵NH4HCO3
硫酸铜 CuSO4 碳酸H2CO3
硫酸钾 K2SO4 磷酸H3PO4
硫酸铵 (NH4)2SO4 硫酸铁Fe2(SO4)3
硫酸亚铁 FeSO4 亚硫酸铁 Fe2(SO3)3
新春快乐!1年前查看全部
- 1.碳酸钠在水中的电离方程式 2.硫酸 3.硝酸 4.硝酸铜 5.碳酸氢钙 6.硝酸铵 7.硫酸铝 8.高锰酸钾 9.氯
1.碳酸钠在水中的电离方程式 2.硫酸 3.硝酸 4.硝酸铜 5.碳酸氢钙 6.硝酸铵 7.硫酸铝 8.高锰酸钾 9.氯酸钾 10.氢氧化钙 11.磷酸钠 12.硝酸钡 13 氯化铁 14.氯化铵
 wyjie20021年前1
wyjie20021年前1 -
 liulimei 共回答了23个问题
liulimei 共回答了23个问题 |采纳率82.6%1.Na2CO3==2Na++HCO3- 2.H2SO4==2H++SO42- 3.HNO3==H++NO3- 4.Cu(NO3)2==Cu2++2NO3- 5.Ca(HCO3)2==Ca2++2HCO3- 6.NH4NO3==NH4++NO3- 7.Al2(SO4)3==2Al3++3SO42- 8.KMnO4==K++MnO4- 9.KCl==K++Cl- 10.Ca(OH)2==Ca2++2OH- 11.Na3PO4==3Na++PO43- 12.Ba(NO3)2==Ba2++2NO3- 13.FeCl3==Fe3++3Cl- 14.NH4Cl==NH4++Cl-1年前查看全部
- .进行下列各反应,要得到相同质量的硝酸铜,消耗硝酸的物质的量最大的是( )
.进行下列各反应,要得到相同质量的硝酸铜,消耗硝酸的物质的量最大的是( )
A.铜和浓硝酸 B.铜和稀硝酸反应
C.氧化铜和硝酸反应 D.氢氧化铜和硝酸反应 lt1m1年前2
lt1m1年前2 -
 ss也要看 共回答了18个问题
ss也要看 共回答了18个问题 |采纳率88.9%以下是我个人的分析~~希望可以帮助你
铜和浓硝酸
4HNO3(浓)+Cu=Cu(NO3)2+2NO2+2H2O
铜和稀硝酸
8HNO3(稀)+3Cu=Cu(NO3)2=2NO+4H2O
氧化铜和硝酸反应
CuO+HNO3====Cu(NO3)2+H2O
氢氧化铜和硝酸反应
2HNO3+Cu(OH)2=Cu(NO3)2+2H2O
由于要得到相同质量的硝酸铜,所以统一所有方程式硝酸铜的化学计量数,
得到~~~~~~
铜和浓硝酸
12HNO3(浓)+3Cu==3Cu(NO3)2+6NO2+6H2O
铜和稀硝酸
8HNO3(稀)+3Cu==3Cu(NO3)2+2NO+4H2O
氧化铜和硝酸反应
3CuO+3HNO3==3Cu(NO3)2+3H2O
氢氧化铜和硝酸反应
3HNO3+3Cu(OH)2==3Cu(NO3)2+6H2O
统一以后再看硝酸前面的化学计量数,计量数最大的那个,消耗的硝酸最多,
所以选 A.铜和浓硝酸1年前查看全部
- 氢氧化钡和硝酸 氯化钙和硝酸铜 硝酸银和氯化钠 氯化铁和氢氧化钾 哪对能共存与水溶液
 路人-男1年前1
路人-男1年前1 -
 斯莱特林魔法师 共回答了12个问题
斯莱特林魔法师 共回答了12个问题 |采纳率83.3%氢氧化钡和硝酸 不能共存,生成水和硝酸钡
氯化钙和硝酸铜 能共存
硝酸银和氯化钠 不能共存,生成氯化银白色沉淀和硝酸钠
氯化铁和氢氧化钾 不能共存,生成氢氧化铁红褐色沉淀和氯化钾1年前查看全部
- 某样固体样品中,可能含有碳酸钠,硫酸钠,氯化钠,硝酸铜,硝酸钙中的一种或几种.将样品溶于水中得到
某样固体样品中,可能含有碳酸钠,硫酸钠,氯化钠,硝酸铜,硝酸钙中的一种或几种.将样品溶于水中得到
无色溶液,滴加氯化钡溶液后产生白色沉淀,过滤,向白色沉淀中加入少量的稀硫酸,沉淀全部溶解,推断该固体中肯定存在( )肯定不存在( ) 流荒1年前2
流荒1年前2 -
 火安奇 共回答了21个问题
火安奇 共回答了21个问题 |采纳率95.2%将样品溶于水中得到无色溶液,说明一定没有硝酸铜
滴加氯化钡溶液后产生白色沉淀,过滤,向白色沉淀中加入少量的稀硫酸,沉淀全部溶解,那么沉淀应该是碳酸钡而不是硫酸钡,所以一定有碳酸钠,一定没有硫酸钠
有碳酸钠,则不可能有硝酸钙,因为它们会反应生成沉淀,不能共存
综上,一定有碳酸钠,一定没有硫酸钠、硝酸铜、硝酸钙,不能确定有没有的是氯化钠1年前查看全部
- 欲配制250ml0.1mol/L的硝酸铜溶液,需称取结晶硝酸铜Cu(NO3).3H2O_____克
 jjyyjjyy71年前1
jjyyjjyy71年前1 -
 学柏拉图 共回答了15个问题
学柏拉图 共回答了15个问题 |采纳率93.3%需Cu(NO3)2·3H2O_____克.242g/mol×0.25mol/L×0.1L=6.05g1年前查看全部
- 超紧急:CU2S + HNO3 = CU(NO3)2 + NO + S + H2O中文:硫化铜+硝酸=硝酸铜 + 一氧化
超紧急:
CU2S + HNO3 = CU(NO3)2 + NO + S + H2O
中文:硫化铜+硝酸=硝酸铜 + 一氧化氮 + 单质硫+水 naitou1年前5
naitou1年前5 -
 丢了的经典001 共回答了32个问题
丢了的经典001 共回答了32个问题 |采纳率87.5%3Cu2S+16HNO3=6Cu(NO3)2+4NO↑+3S↓+8H2O
一个Cu升1价,一个硫升2价,所以整体法,一个Cu2S升4价,而一个N降3价
所以3Cu2S 4NO 然后铜,硫原子守恒,所以6Cu(NO3)2 3S 氮原子守恒,所以16HNO3然后是氢守恒 8H2O,最后检查O1年前查看全部
- 乙炔黑能否将硝酸铜溶液中的铜离子还原成铜单质
乙炔黑能否将硝酸铜溶液中的铜离子还原成铜单质
采用 什么方法能让反应发生 viviliuliu1年前4
viviliuliu1年前4 -
 海南帅哥 共回答了25个问题
海南帅哥 共回答了25个问题 |采纳率96%不行 虽然乙炔黑表面积大 活性大 但是毕竟是碳啊 在溶液中反应的活性很小
碳在溶液中是不可能还原金属离子的
只要是在溶液中 无论改变条件还是加入催化剂 都不行1年前查看全部
- 氧化铜和稀硝酸反应方程式 我网上查说是生成硝酸铜和水.可是 氧化铁 与稀硝酸反应生成 硝酸铁 和 一氧化氮和水,因为硝酸
氧化铜和稀硝酸反应方程式
我网上查说是生成硝酸铜和水.可是 氧化铁 与稀硝酸反应生成 硝酸铁 和 一氧化氮和水,因为硝酸有强氧化性,那为什么 氧化铜 与它反应不生成一氧化氮呢? 慕头猪猪1年前1
慕头猪猪1年前1 -
 娇那 共回答了18个问题
娇那 共回答了18个问题 |采纳率94.4%CuO+2HNO3=Cu(NO3)2+H2O 不用考虑太多.CuO的反应就是上边的那个. 金属氧化物,金属单质,与HNO3的反应是非常复杂的,与HNO3的浓度有关,只要浓度一变,产物就完全不同了.1年前查看全部
- 铁和石墨在氯化钠溶液以及铜和银在硝酸铜溶液中如何形成原电池?
铁和石墨在氯化钠溶液以及铜和银在硝酸铜溶液中如何形成原电池?
希望能回答 感激不尽 Suzi叶1年前2
Suzi叶1年前2 -
 大象希形 共回答了20个问题
大象希形 共回答了20个问题 |采纳率95%形成原电池首先要有一个能释放能量的氧化还原反应,第一个是溶解在食盐水中的氧气氧化了铁释放能量,所以负极:Fe-2e-=Fe2+ 正极:O2+4e-+2H2O=4OH-
第二个应该是铜和银在硝酸银溶液中形成原电池,这时的释放能量的氧化还原反应是铜与硝酸银反应,负极:Cu-2e-=Cu2+ 正极:2Ag+ + 2e- = 2Ag1年前查看全部
- 为什么硫酸铜能溶解铜?如题原题:把同样大小,同样质地的除去氧化膜的铝片分别投入同浓度的硝酸铜和硫酸铜溶液中,生成铜的速率
为什么硫酸铜能溶解铜?
如题
原题:把同样大小,同样质地的除去氧化膜的铝片分别投入同浓度的硝酸铜和硫酸铜溶液中,生成铜的速率哪个快。答案是硫酸铜快。原因就是硝酸铜能溶解铜。答案就是这么写的。 merry_days1年前3
merry_days1年前3 -
 I行云流水 共回答了14个问题
I行云流水 共回答了14个问题 |采纳率92.9%硝酸铜水解酸性,
水解出来的H+和硝酸根形成稀HNO3
稀硝酸会把铝置换出来的铜溶解掉一部分
硫酸铜水解虽然也为酸性
但形成的稀硫酸不能溶解铜1年前查看全部
- 下列物质中,化学式书写错误的是 [ ] A. 硝酸铜:Cu(NO 3 )
下列物质中,化学式书写错误的是 [ ]A. 硝酸铜:Cu(NO 3 ) 2
B. 硫酸铝:AlSO 4
C. 二氧化氮:NO 2
D. 氧化亚铁:FeO feibalilei1年前1
feibalilei1年前1 -
 幽灵公主12 共回答了20个问题
幽灵公主12 共回答了20个问题 |采纳率80%B1年前查看全部
- 一种烟火药剂的组成中含有硝酸铜,当燃烧时,可产生绿色火焰,发生如下反应:2Cu(NO3)2=2cuO+O2+4X .X的
一种烟火药剂的组成中含有硝酸铜,当燃烧时,可产生绿色火焰,发生如下反应:2Cu(NO3)2=2cuO+O2+4X .X的化学是:————
 LYJ_CAD1年前3
LYJ_CAD1年前3 -
 ky0400 共回答了23个问题
ky0400 共回答了23个问题 |采纳率91.3%NO21年前查看全部
- (2006•雅安)把一定量的铁粉放入硝酸银和硝酸铜的混合液中,充分反应后有少量金属析出,过滤后在滤液中滴加盐酸,无明显变
(2006•雅安)把一定量的铁粉放入硝酸银和硝酸铜的混合液中,充分反应后有少量金属析出,过滤后在滤液中滴加盐酸,无明显变化,则下列有关说法中肯定正确的是( )
A.析出的少量金属中一定有铜
B.析出的少量金属中一定有银
C.滤液中一定含有硝酸铜
D.滤液中可能含有硝酸银 果汁点点1年前1
果汁点点1年前1 -
 WEIB__ren_ren 共回答了13个问题
WEIB__ren_ren 共回答了13个问题 |采纳率92.3%解题思路:根据金属活动性顺序,上面金属的活动性:铁>铜>银:因为“把一定量的铁粉放入硝酸银和硝酸铜的混合液中”,所以铁会与硝酸银和硝酸铜分别反应生成银和铜;而硝酸银足够多的话,则铜消失,而银一定存在;又因为“在滤液中滴加盐酸,无明显变化”,则铁一定反应完,也一定无硝酸银,因为氯离子与银离子会形成沉淀;A、硝酸银足够多的话,铜与硝酸银反应,则铜消失,故A错误;
B、根据金属活动性顺序,银的金属活动性最差,所以析出的少量金属中一定有银,故B正确;
C、如果铁足量,滤液中不会含有硝酸铜,故C错误;
D、因为盐酸与硝酸银反应生成白色沉淀,而“在滤液中滴加盐酸,无明显变化”,则一定无硝酸银,故D错误.
故选B.点评:
本题考点: 金属活动性顺序及其应用.
考点点评: 利用金属活动性顺序,可知金属的活动性;学会利用它们处理和解释问题.1年前查看全部
- 用 石墨做电极 电解硝酸铜 硝酸银混合溶液 现象
 yyyyppoo1年前1
yyyyppoo1年前1 -
 nn胜雪 共回答了13个问题
nn胜雪 共回答了13个问题 |采纳率76.9%在阴极有银析出,阴极变银白色.
在阳极有无色气体(O2)放出.1年前查看全部
- 硝酸铜水如何将铜提取?硝酸水里含铜,如何将硝酸和铜分解,将铜提取出来?硝酸已将铜溶解,硝酸里含大量的铜,如何将铜与硝酸分
硝酸铜水如何将铜提取?
硝酸水里含铜,如何将硝酸和铜分解,将铜提取出来?
硝酸已将铜溶解,硝酸里含大量的铜,如何将铜与硝酸分解,炼制出纯铜?注意要详细说明 良辰美景zwj1年前3
良辰美景zwj1年前3 -
 雨桑子 共回答了22个问题
雨桑子 共回答了22个问题 |采纳率90.9%置换反应,加金属活动性比铜强的就行. - -
楼上说的铁锌等都可以. - -1年前查看全部
- 硫酸和Zn原电池反应加入硝酸铜要考虑置换反应吗?
 myetone1年前1
myetone1年前1 -
 mtdj352 共回答了16个问题
mtdj352 共回答了16个问题 |采纳率87.5%因为化学反应就是电子转移的过程,通过原电池是这个电子转移的速率加快,所
以原电池就会加快反映的速率.
因为Zn在稀硫酸中再加入Cu(N03)2,这样锌就能把铜置换出来.就因为这样铜
就附和在锌的表面,够成了闭合回路,而稀硫酸里面有氢离子和硝酸根离子,这
样就构成了一个原电池1年前查看全部
- 硝酸铜溶液里加盐酸再加铜,会发生什么反应?
硝酸铜溶液里加盐酸再加铜,会发生什么反应?
肯定有"红棕色气体放出"吗? sophiahit1年前1
sophiahit1年前1 -
 _gg不觉晓_ 共回答了21个问题
_gg不觉晓_ 共回答了21个问题 |采纳率95.2%铜会溶解,并有红棕色气体放出.因为加入盐酸后,提供了H+,和溶液中的NO3-结合,又相当于有了HNO3.1年前查看全部
- (2008•宝山区二模)现有硝酸铜和硝酸镁的两种溶质组成的混合溶液,进行如下实验:
(2008•宝山区二模)现有硝酸铜和硝酸镁的两种溶质组成的混合溶液,进行如下实验:

根据实验推断(1)滤液乙中的溶质是H2SO4和FeSO4或HCl和FeCl2H2SO4和FeSO4或HCl和FeCl2.
(2)混合溶液Cu(NO3)2和Mg(NO3)2与固体A所涉及到的反应的化学方程式为:Fe+Cu(NO3)2=Cu+Fe(NO3)2Fe+Cu(NO3)2=Cu+Fe(NO3)2. sung19771年前1
sung19771年前1 -
 876373151 共回答了16个问题
876373151 共回答了16个问题 |采纳率87.5%(1)将混合溶液中的溶质和滤液中的溶质对比,可以看出,加入过量的固体A是铁,所以固体甲中有铁和铜,加入溶液B会生成气体,,铜不与B反应,所以B是盐酸或硫酸,B是过量的,所以反应后的溶液中除了剩余的酸,也有生成的盐,故答案为:H2SO4和FeSO4或HCl和FeCl2,
(2)混合溶液中的溶质和滤液中的溶质对比,可以看出,加入过量的固体A是铁,铁的活动性排在铜之前,镁之后,会置换出铜,不会置换出镁,
故答案为:Fe+Cu(NO3)2=Cu+Fe(NO3)21年前
31年前查看全部
- 在硝酸铜和硝酸银溶液的混合溶液中加入一定量的铁粉,充分反应后过滤,下列有关结论正确的是( )A. 滤渣中一定含有银
在硝酸铜和硝酸银溶液的混合溶液中加入一定量的铁粉,充分反应后过滤,下列有关结论正确的是( )A. 滤渣中一定含有银
B. 滤液中一定含有铜
C. 在滤液中间加入稀盐酸,若生成白色沉淀,则滤渣中一定含有铜
D. 在滤液中加入稀盐酸,若没有白色沉淀产生,则滤渣中一定含有铁 武作1年前5
武作1年前5 -
 乾坤之子 共回答了12个问题
乾坤之子 共回答了12个问题 |采纳率100%解题思路:根据三种金属活动性由强到弱的顺序:铁铜银,当把铁粉加入到硝酸铜和硝酸银的混合溶液中时,银首先被置换出来,在银完全置换后,铜才能被置换出来;
一定量的铁粉,可能完全转换出铜和银,也可能只置换出全部的银或是置换出部分的银.A、根据反应规律,加入铁粉,一定能转换出金属银,所以滤渣中一定含有银;结论正确;
B、如果一定量的铁粉恰好完全置换出银、铜,则滤液中就不再含铜;此结论不正确;
C、滤液中滴加稀盐酸可检查银是否被完全置换,滴入稀盐酸有白色沉淀,说明银没有全部被置换、铁粉量不足,铜不能被置换出来.结论不正确;
D、滤液中滴入稀盐酸没有白色沉淀,只能说明硝酸银全部反应,但硝酸铜是否完全反应尚不明确,更无法判断铁粉是否剩余.结论不正确.
故选A点评:
本题考点: ["金属活动性顺序及其应用"]
考点点评: 金属放入盐的混合溶液中,总是把活动性最弱的金属最先置换完,再按由弱到强的顺序一一进行置换.1年前查看全部
- 加热硝酸铜结晶水合物和硝酸银的混合物110.2克使之完全分解,得到固体残渣48.4克.将反应产生的气体通...
加热硝酸铜结晶水合物和硝酸银的混合物110.2克使之完全分解,得到固体残渣48.4克.将反应产生的气体通...
加热硝酸铜结晶水合物和硝酸银的混合物110.2克使之完全分解,得到固体残渣48.4克.将反应产生的气体通过水充分吸收后,剩余气体为1.68升(标准状况)原混合物中硝酸铜结晶水合物的化学式. 游啊乐悠悠1年前2
游啊乐悠悠1年前2 -
 阿包 共回答了21个问题
阿包 共回答了21个问题 |采纳率85.7%设硝酸铜结晶水合物为Cu(NO3)2·nH2O,其物质的量为x,AgNO3的物质的量为y
2Cu(NO3)2·nH2O=2CuO+ 4NO2↑ + O2↑ 4NO2+O2+2H2O=4HNO3
2 2 4 1 4 1
x x 2x 0.5x 2x 0.5x
2AgNO3=2Ag+2NO2↑+O2↑ 4NO2+O2+2H2O=4HNO3
2 2 2 1 4 1
y y y 0.5y y 0.25y
由以上方程式或知最终得到的气体是O2,且为0.25y,0.25y=1.68/22.4 y=0.3mol
氧化铜与银的质量=48.4g,即有80x+108y=48.4,得x=0.2mol
原混合物中结晶水的质量=110.2-(0.2*188+0.3*170)=21.6g,n(H2O)=21.6/18=1.2mol
则硝酸铜结晶水合物中n[Cu(NO3)2]:n(H2O)=0.2:1.2=1:6
所以硝酸铜结晶水合物为Cu(NO3)2·6H2O1年前查看全部
- 向硝酸银硝酸铜硝酸镁的混合溶液中加入一定质量的锌反应后过滤得到滤渣A和B.(1)反应前后溶液质量不变,A中一定含?(2)
向硝酸银硝酸铜硝酸镁的混合溶液中加入一定质量的锌反应后过滤得到滤渣A和B.(1)反应前后溶液质量不变,A中一定含?(2)反应后溶液质量减少B中一定含金属?可能含金属离子?
在没有其他人回答了吗 novopgwa1年前1
novopgwa1年前1 -
 玉明道 共回答了17个问题
玉明道 共回答了17个问题 |采纳率94.1%:(1)由于锌在镁后,在银和铜前,因此锌可以和硝酸银和硝酸铜反应,但由于银和锌相差远,因此锌先和硝酸银溶液反应
Zn+2AgNO3=2Ag+Zn(NO3)2,
65 216
Zn+Cu(NO3)2=Cu+Zn(NO3)2
65 64
根据化学方程式不难看出,每65份质量的锌就会从溶液中置换出216份质量的银,会使溶液质量减少,同理,锌和硝酸铜溶液反应会使溶液质量增多,因此若溶液质量不变,说明锌即和硝酸银溶液反应,也和硝酸铜溶液反应,因此A中一定含有金属银和铜,故答案为:Ag和Cu;
(2)由上可知,溶液质量减少,说明锌一定和硝酸银溶液,可能和硝酸铜溶液反应,由于硝酸镁溶液不参与反应,因此溶液中一定含有镁离子和生成的锌离子,而铜离子和银离子无法确定,
故答案为:Mg2+和Zn2+Cu2+和Ag+.1年前查看全部
- 铜能否一步变为硝酸铜,若能,加什么
 hh821年前3
hh821年前3 -
 mllis 共回答了23个问题
mllis 共回答了23个问题 |采纳率82.6%能,加稀硝酸就能变成硝酸铜
3CU+(稀)8HNO3=3CU(NO3)2+2NO+4H2O1年前查看全部
- 氧化铜中混有硝酸铜怎么办
 lala_ss3331年前2
lala_ss3331年前2 -
 lsloveljf 共回答了17个问题
lsloveljf 共回答了17个问题 |采纳率94.1%加热,硝酸铜会分解为氧化铜1年前查看全部
- (2013•南岗区一模)张南同学为了验证铝、铜、银的金属活动性顺序,设计了如下实验方案:将铝丝、银丝分别插入到硝酸铜溶液
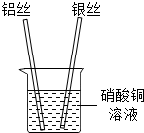 (2013•南岗区一模)张南同学为了验证铝、铜、银的金属活动性顺序,设计了如下实验方案:将铝丝、银丝分别插入到硝酸铜溶液中,如图,根据实验现象可以判断出三种金属的金属活动性强弱顺序.请回答下列问题.
(2013•南岗区一模)张南同学为了验证铝、铜、银的金属活动性顺序,设计了如下实验方案:将铝丝、银丝分别插入到硝酸铜溶液中,如图,根据实验现象可以判断出三种金属的金属活动性强弱顺序.请回答下列问题.
(1)判断铝的活动性比铜强的现象是______;若没有观察到预期现象,其原因是______(不考虑硝酸铜溶液).
(2)上述实验中发生反应的化学方程式为______;由此实验得出三种金属的活动性顺序为______. NICOLE_MAOMAO1年前1
NICOLE_MAOMAO1年前1 -
 mitchboy 共回答了19个问题
mitchboy 共回答了19个问题 |采纳率89.5%解题思路:根据在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来分析现象及结论.(1)铝的活动性比铜强,因此会置换出硫酸铜中的铜,现象为:铝的表面附着一层红色的固体;若铝没有除锈,表面有一层致密的保护膜,就不会和硫酸铜发生反应,因此观察不到预期现象;
(2)铝与硝酸铜反应生成硝酸铝和铜,反应的化学方程式为:2Al+3Cu(NO3)2=2Al(NO3)3+3Cu;由于在银的表面不会出现一层红色的固体,说明银的活动性比铜弱,因此三种金属的活动性顺序为:铝>铜>银;
故答案为:(1)铝的表面附着一层红色的固体;铝没有除锈,表面有一层致密的保护膜;(2)2Al+3Cu(NO3)2=2Al(NO3)3+3Cu;铝>铜>银.点评:
本题考点: 金属活动性顺序及其应用.
考点点评: 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行分析,还要注意化学方程式的书写.1年前查看全部
- (2004•北京)现有硝酸银、硝酸铜和硝酸镁三种物质组成的混合溶液,进行下列实验:
(2004•北京)现有硝酸银、硝酸铜和硝酸镁三种物质组成的混合溶液,进行下列实验:

根据实验推断:
(1)固体甲是______;
(2)滤液2中的溶质是______(写化学式);
(3)滤液2跟固体a反应的化学方程式是______. 傲视君主1年前1
傲视君主1年前1 -
 萱家草草 共回答了14个问题
萱家草草 共回答了14个问题 |采纳率78.6%解题思路:(1)根据四种金属的活动性强弱关系:镁>锌>铜>银,判断向混合溶液中加入一定量锌粒可能发生的反应;
(2)根据铜、银不和硫酸反应,锌可置换出酸中的氢,可知b为稀硫酸;
(3)加入锌,除去过量的稀硫酸.(1)由于镁、锌、铜、银的金属活动性强弱为镁>锌>铜>银,向硝酸镁、硝酸铜、硝酸银溶液中加入过量的锌,锌可置换出硝酸铜、硝酸银中的铜和银,所以固体甲为铜、银、锌的混合物;
(2)锌可和酸反应,铜和银不与酸反应,加入过量的b(稀硫酸),过滤,得到固体铜和银,滤液2的溶质为硫酸锌、硫酸;
(3)滤液2中加入过量锌,过滤,得到硫酸锌溶液.
故答案为:
(1)Cu、Ag、Zn的混合物;
(2)ZnSO4、H2SO4;
(3)Zn+H2SO4=ZnSO4+H2↑.点评:
本题考点: 金属活动性顺序及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 金属放入盐的混合溶液,金属按盐中金属活动性由弱到强的顺序和盐先后反应,即先与活动性最弱的金属的盐反应.1年前查看全部
- 碘化氢和氯化钾反应方程式?硝酸铜溶液是什么颜色?
碘化氢和氯化钾反应方程式?硝酸铜溶液是什么颜色?
是溶液!
那氯酸钾呢 12一条搁浅的鱼1年前3
12一条搁浅的鱼1年前3 -
 77897782 共回答了14个问题
77897782 共回答了14个问题 |采纳率92.9%碘化氢和氯化钾反应方程式,人家貌似没反应.
硝酸铜溶液稀的是蓝色,浓的是绿色,取决于水合铜离子的浓度.1年前查看全部
- 有ABCDEF六种物质,它们是硝酸铜,碳酸钠,氯化钡,稀硫酸,氢氧化钙五种溶液和铁,凡用直线连接的两物质均可反应,(1)
有ABCDEF六种物质,它们是硝酸铜,碳酸钠,氯化钡,稀硫酸,氢氧化钙五种溶液和铁,凡用直线连接的两物质均可反应,(1)推断:B是______.(2)C和F反应的化学方程式是________(3)E+D反应的化学方程式是__________.为什么?

 woshimolhm1年前3
woshimolhm1年前3 -
 孤灯明月 共回答了13个问题
孤灯明月 共回答了13个问题 |采纳率92.3%A.H2SO4 B.Ca(OH)2 C.Na2CO3 D.Cu(NO3)2 E.Fe F.BaCl2
(1)B是Ca(OH)2
(2)Na2CO3+BaCl2=BaCO3↓+2NaCl 生成沉淀
(3)Fe+Cu(NO3)2=Cu+Fe(NO3)2 置换反应
关于这类题 = =主要是看反不反应,一般反应都会有生成气体或者沉淀.或者是酸碱反应这样的.然后往后类推吧.1年前查看全部
- 小刚也查阅了一分资料,了解到氯化铜溶液,硝酸铜溶液中均含有铜离子,氯化钠溶液中含有氯离子,硝酸钠溶液含硝酸离子.他于是马
小刚也查阅了一分资料,了解到氯化铜溶液,硝酸铜溶液中均含有铜离子,氯化钠溶液中含有氯离子,硝酸钠溶液含硝酸离子.他于是马上到实验室观察氯化钠,硝酸钠,氯化铜,硝酸铜溶液的颜色,基于这些溶液的颜色他可以作一个判断,若 ,则可以得出结论——铜离子使硫酸铜溶液呈现蓝色.
 我是驹1年前1
我是驹1年前1 -
 riot转圈圈 共回答了19个问题
riot转圈圈 共回答了19个问题 |采纳率89.5%若 氯化铜,硝酸铜溶液为蓝色,氯化钠,硝酸钠溶液为无色 ,则可以得出结论——铜离子使硫酸铜溶液呈现蓝色.1年前查看全部
- 写出下列离子鼓号的化学式1.氧离子 2.+2价的钙 3.两个氢离子 4.氦气 5.氢氧化钙6.硝酸铜 7.碳酸钾 8.硫
写出下列离子鼓号的化学式
1.氧离子 2.+2价的钙 3.两个氢离子 4.氦气 5.氢氧化钙
6.硝酸铜 7.碳酸钾 8.硫酸铵 9.磷酸铵 10.氧化钾
11.氯化铝 12.磷酸 13.碳酸 14.硝酸 15.硫酸 16.氧化镁 倩颖红妆1年前1
倩颖红妆1年前1 -
 vcbc 共回答了12个问题
vcbc 共回答了12个问题 |采纳率91.7%1.O2-
2.Ca2+
3.2H+
4.He
5.Ca(OH)2
6.Cu(NO3)2
7.K2CO3
8.(NH4)2SO4
9.(NH4)3PO4
10.K2O
11.AlCl3
12.H3PO4
13.H2CO3
14.HNO3
15.H2SO4
16.MgO1年前查看全部
- 硝酸铜与氯化铁反应化学的方程式 二氧化碳与氯化钙的化学方程式 氯化铝与硫酸钠的化学方程式
硝酸铜与氯化铁反应化学的方程式 二氧化碳与氯化钙的化学方程式 氯化铝与硫酸钠的化学方程式
氯化镁与碳酸钠的化学方程式 Louisazhang1年前4
Louisazhang1年前4 -
 271681698 共回答了12个问题
271681698 共回答了12个问题 |采纳率100%硝酸铜与氯化铁 、 二氧化碳与氯化钙 、 氯化铝与硫酸钠都不反应!
氯化镁与碳酸钠的化学方程式:
MgCI2+Na2CO3==MgCO3↓+2NaCI1年前查看全部
- 若制取18.8g硝酸铜,至少需要消耗10%的稀硝酸多少克?
 hexiansheng1年前3
hexiansheng1年前3 -
 tomcatfire 共回答了18个问题
tomcatfire 共回答了18个问题 |采纳率83.3%3Cu+8HNO3=3Cu(NO3)2+2NO+4H2O
----------504--------564
-----------X*10%----18.8
X=168克
至少需要消耗10%的稀硝酸168克1年前查看全部
大家在问
- 1甘油催化氧化反应方程式
- 22.3g Na中含多少摩尔电子?跟足量水反应中失去多少摩尔电子?
- 3“通过阅读我学会许多丰富的知识和成长的启示”用英语怎么说
- 4已知x+1分之A + x-1分之B等于(x+1)(x-1)分之x-3求A.B的值
- 5食堂里买2包味精和5包糖共41元,如果买4包味精和2包糖共42元.问味精和糖各需多少钱
- 6食堂里买2包味精和2包糖共用去41元,如果买4包味精和2包糖要用42元.每包味精多少元?每包糖多少元?
- 7食堂里买2包味精和5包糖共用了41元,如果买4包味精和2包糖要用42元.糖和味精每包各多少元?
- 8为什么铜粉加入稀硫酸中,再加入硝酸铜液体,铜粉溶解.化学方程式怎么写啊
- 9硝酸铜怎么生成铜
- 10解方程-3x=-4x+1时,两边都加上几得x=1,是根据等式性质1.
- 11学生图书馆有故事书80本,故事书的本数正好是连环画的6分之5,故事书和连环画共有多少本?
- 12单人旁加三撇是什么字?
- 13在硝酸铜、硝酸银的混合溶液中,加入一定质量的锌粉,锌为什么先跟银反应再跟铜反应
- 14李奶奶卖饮料 一种是大瓶装 每箱12瓶 批发价21.6元 一种是小瓶装 每箱24瓶 批发价20.4元 李奶奶按零售价卖
- 15侺把单人旁去掉读什么字
