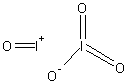非极性运输是一种怎样的运输方式?
 jacient2022-10-04 11:39:541条回答
jacient2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 guww 共回答了16个问题
guww 共回答了16个问题 |采纳率87.5%- 就是在植物体内的通过韧皮部进行的运输,例如植物生长素的横向运输!
- 1年前
相关推荐
- 怎样判断非极性公价键和极性公价键?
 半岭屋人1年前2
半岭屋人1年前2 -
 老ww03 共回答了14个问题
老ww03 共回答了14个问题 |采纳率71.4%看分子造型是不是对称的
如果不是对称的 就是极性 反之 非极
或者 容于水的就是极
溶于有机溶剂的就是非极
酒精例外1年前查看全部
- 为什么脂肪是非极性化合物,就可以以无水形式存在体内
 zqo81年前3
zqo81年前3 -
 伍陆柒捌 共回答了17个问题
伍陆柒捌 共回答了17个问题 |采纳率82.4%知道“相似相容”原理吧,即极性化合物易溶于极性溶质,非极性化合物易溶于非极性溶质.脂肪为非极性物质而水为极性物质,故体内脂肪可以以无水形式存在.1年前查看全部
- 电负性相同的元素形成的的化合物为非极性化合物吗?()
 Dylan861年前1
Dylan861年前1 -
 杨晓露 共回答了24个问题
杨晓露 共回答了24个问题 |采纳率79.2%不是
空间结构立体对称的就是非极性化合物1年前查看全部
- '在非极性分子中不可能存在非极性键'这句话对吗
'在非极性分子中不可能存在非极性键'这句话对吗
请举出例子哈, haojiexp20001年前2
haojiexp20001年前2 -
 李宁小样 共回答了16个问题
李宁小样 共回答了16个问题 |采纳率93.8%不对,如氯气是非极性分子,但含有Cl-Cl非极性键.1年前查看全部
- 为什么苯无极性,甲苯、乙苯有极性?甲基乙基不都是非极性的么?
 fbkf1年前2
fbkf1年前2 -
 优先拥抱 共回答了18个问题
优先拥抱 共回答了18个问题 |采纳率94.4%分子有没有极性直接看对称性即可
苯分子高度对称,无极性;甲苯和乙苯都不对称,都有极性.烷烃中的C-H键其实有微弱的极性,但是不影响性质的讨论,所以一般当做非极性键处理.1年前查看全部
- 水的化学性质水是极性分子,怎么判断极性和非极性?极性分子的特点是什么?以水为例.水为什么可以溶解固体和气体.
 xhkj1201年前2
xhkj1201年前2 -
 yyypx 共回答了20个问题
yyypx 共回答了20个问题 |采纳率85%水的原子结构是H-O-H,但不是直线的,而是呈120角(大概)的,这就是其产生极性的原因,水是含有极性键的极性分子;像二氧化碳(O=C=O)则是直线型的,是非极性的,这是含有极性键的非极性分子.
水可以溶解固体如氯化钠,而且溶解的比较多,因为氯化钠也是极性的,而氧气则比较少,氧气是非极性的.
总的一个原则:相似相溶.都是有机物或者都是无机物,都是极性分子,都是非极性分子.
如:油脂溶解于乙醇里的量肯定是多于溶解于水中的量的.1年前查看全部
- SO3空间结构 分子极性如题,有人说是极性分子,有人说非极性.有人说平面三角形,有人说三角锥..
 青眼相吊1年前1
青眼相吊1年前1 -
 4dog444 共回答了18个问题
4dog444 共回答了18个问题 |采纳率88.9%气态的SO3是一种具有D3h对称的平面正三角形分子,非极性分子1年前查看全部
- 极性键和非极性化合物有什么区别?
 zhyrain1年前1
zhyrain1年前1 -
 ww公鼠 共回答了24个问题
ww公鼠 共回答了24个问题 |采纳率87.5%极性键是两个不同的原子之间的共价键,是一种作用力.而非极性化合物是一种化合物,你可以根据物理中的和外力为零来判断,比如说二氧化碳,它是里面有碳碳双键是平面性分子,所以和外力为零,所以就是非极性化合物1年前查看全部
- 离子化合物有无极性分子和非极性分子之分?
 萧湘夜雨1231年前1
萧湘夜雨1231年前1 -
 月季花开 共回答了24个问题
月季花开 共回答了24个问题 |采纳率75%离子化合物本身就是有正离子和负离子组成的,所以不存在极性分子和非极性分子.你可以这样理解(心里这样想,不要说出来):离子化合物都是极性分子.1年前查看全部
- 1.极性运输和非极性运输都是主动运输吗?2.横向运输是非极性运输吗?
 落叶飞雪1101年前4
落叶飞雪1101年前4 -
 偶名斯文 共回答了13个问题
偶名斯文 共回答了13个问题 |采纳率84.6%1.极性运输和非极性运输都是主动运输
2.横向运输是非极性运输
因为这些运输都是生长素从低浓度的一侧向高浓度的一侧运输的1年前查看全部
- SO2 为什么溶于苯?若根据相似相容 那么一个极性 一个非极性不溶若根据元素 一个无机 一个有机?
 zyb_shy1年前1
zyb_shy1年前1 -
 子都且狂 共回答了14个问题
子都且狂 共回答了14个问题 |采纳率92.9%哪里看到二氧化硫溶解于苯?
请看化工词典的解释:
二氧化硫又称亚硫酸酐.无色有刺激性气味的气体.密度2.927g/cm3.凝固点-72.7℃.沸点-10℃.易溶于丙酮、乙醇、甲酸等多种有机溶剂,溶于水(0℃时溶解度22.8g/l00ml,90℃时溶解度0.58g/100ml).水溶液呈酸性.在硫酸溶液中的溶解度以硫酸浓度为85%时为最小.液态时为良好的溶剂.化学性质极其稳定.2000℃以上发生热分解,也可通过电场放电、紫外线或X射线辐射等分解.在钒催化剂存在下,被氧化为三氧化硫.在高温或催化剂存在下被氢或含碳化合物还原为硫化氢.与硫化氢反应生成元素硫.由硫黄燃烧或由黄铁矿等含硫矿物焙烧制得.也可由石膏或芒硝制得,或由含硫烟气中回收.主要用于生产三氧化硫,硫酸,亚硫酸盐,硫代硫酸盐.也用作蒸薰剂,漂白剂,防腐剂,消毒剂,还原剂,冷冻剂和溶剂.还用于造纸、食品、纺织、皮革、染料、医药等工业.1年前查看全部
- 二氧化碳是极性分子还是非极性分子,为什么?...还有哪些极性分子和非极性分子?
 儒雅狼君1年前2
儒雅狼君1年前2 -
 挂云帆 共回答了20个问题
挂云帆 共回答了20个问题 |采纳率95%一、二氧化碳是非极性分子
二、原因:虽然它是由两种不同的元素组成的,但是分子是不是极性分子关键看的是分子中的电荷中心是不是产生了偏移.二氧化碳的结构是——碳原子在正中间,两个氧原子分别在两边,他们像是在跷跷板的两端,谁的电性也不比谁的强,整个分子是对称的,电荷中心是在分子中间,分子整体显示非极性.
三、由同种元素组成的双原子分子,如氢气、氯气等肯定是非极性分子.另外,多原子分子如果中心原子(如二氧化碳中的碳原子)最外层电子全部参与成键(如二氧化碳中碳原子最外层有4个电子,现在全部拿出来与氧原子构成共价键),那么这个分子就是非极性分子.
说了这么一堆不知道你懂了没有,我高中时也不是很懂这个,你可以找几个例子按照这个原则对照一下,在多做几道这个类型的题,就能掌握了.加油哦~1年前查看全部
- 氨根离子为10电子粒了,是否呈非极性?
氨根离子为10电子粒了,是否呈非极性?
其中氮原子的化合价是否为-3价,一般说呈非极性的粒子中,主元素的化合价的绝对值应等于该原子归外层上的电子数,这二者是否矛盾? boysonny1年前4
boysonny1年前4 -
 ha1976 共回答了22个问题
ha1976 共回答了22个问题 |采纳率100%铵根离子是极性键构成的非极性离子,是与甲烷相似的正四面体结构,中心原子N呈现不等性sp3杂化,形成四个轨道其中三个与H成键便生成了NH3;然而有一个轨道上存在故对电子所以与H+形成配位键从而形成铵根离子.此时N原子由不等性SP3杂化,变为等性SP3杂化,此时的四个N-H是对等的,看不出哪个是配位键,哪个是一般共价键.因而整个原子团是非极性的.1年前查看全部
- 化学中的双键是是什么意思?极性与非极性的分子俗套点的解释,让人听得懂.
化学中的双键是是什么意思?极性与非极性的分子俗套点的解释,让人听得懂.
我刚学化学,电子云是什么? cqkk131se_7fc01年前4
cqkk131se_7fc01年前4 -
 隔壁二爷爷 共回答了23个问题
隔壁二爷爷 共回答了23个问题 |采纳率91.3%双键指的是一根σ键(电子云头碰头相互作用) 和一根π键(电子云肩并肩相互作用)
单键的话只有σ键,双键的话多了π键.
极性分子与非极性分子差别就是正负电荷不重合.
极性指的是电子云偏向某方,如果正负电荷不重合的话就是说电子云从正电荷偏移到负电荷那边去了
比如说 O=C=O C为正电荷的,两个O为负电荷的.两个O对称,负电荷中心在中间,刚好和C的正电荷重合,所以是非极性的.1年前查看全部
- 有极性键又有非极性键的非极性分子
有极性键又有非极性键的非极性分子
a二氧化硫
b甲烷
c氯乙烷
d乙炔
请给出明确地解释 132130694901年前1
132130694901年前1 -
 降龙014 共回答了16个问题
降龙014 共回答了16个问题 |采纳率87.5%D,乙炔,乙炔中碳碳叁键是非极性键,碳氢键是极性键,整个有高度的对称性,是非极性分子.1年前查看全部
- 极性物质有非极性物质有什么区别?
极性物质有非极性物质有什么区别?
我刚刚上初三
尽量用白话 7346640371年前3
7346640371年前3 -
 小粉子1985 共回答了13个问题
小粉子1985 共回答了13个问题 |采纳率92.3%极性分子就是分子中正电荷中心与负电荷中心不重合的分子
非极性分子就是分子中正电荷中心与负电荷中心重合的分子
物质的极性与非极性与分子中化学键的极性与非极性无关
一般而言,物质的分子中原子核正电荷量的总和与电子负电荷量总和相等,故物质显中性.由于电子和原子核都在不停的快速运动,则造成分子中局部存在正电荷中心和负电荷中心,二者不重合者为极性分子,重合者为非极性分子.分子极性的大小取决于正、负电荷中心带电荷的绝对值和正、负电荷中心间距离的大小,二者之积称为偶极矩,其值的大小则是一个分子极性大小的量度.
极性分子间常以正负偶极相吸引而聚集在一起,如极性的水分子则是如此,因此液态水变成气态的单个水分子,需能量克服偶极间的相互作用力,从而水的沸点也就高于非极性物质(如苯)的沸点.
物质的极性大小决定于分子中原子间吸引电子以能力的差别,相同原子组成的分子无此种差别则为非极性,有差别者一般为极性.丙烯酸酯的酯基(-COOR)中,有两个吸电子能力极强的氧原子(O),故是强极性分子.不难理解,丙烯酸酯涂料涂在极性基材上,则粘附力强而牢固,若它涂在非极性基材上,则效果不佳.1年前查看全部
- 什么是极性物质和非极性物质?谢谢
 xweric1年前1
xweric1年前1 -
 路线图 共回答了17个问题
路线图 共回答了17个问题 |采纳率76.5%极性物质就是组成该物质的粒子之间所受合力不为零,即分子没有达到相对平衡;
非极性物质则相反.1年前查看全部
- 含有极性键的非极性分子金刚石白磷甲烷哪个是
 ameirose1年前5
ameirose1年前5 -
 JF_fuchen9890 共回答了14个问题
JF_fuchen9890 共回答了14个问题 |采纳率100%甲烷是
前两者是单质,只有非极性键1年前查看全部
- 即含有极性键又含有非极性键的非极性分子
即含有极性键又含有非极性键的非极性分子
列举出几个,过氧化钠是吗? 银幻想1年前3
银幻想1年前3 -
 豹图腾 共回答了17个问题
豹图腾 共回答了17个问题 |采纳率88.2%如:C2H6 ,C2H4 C2H2 但过氧化钠不是1年前查看全部
- 怎样判断有机溶剂是强极性的、弱极性的或是非极性的?
 so9101年前1
so9101年前1 -
 diegoren 共回答了25个问题
diegoren 共回答了25个问题 |采纳率88%看分子式.如果分子是对称的,则是非极性溶剂;
如果略微有一点不对称,一般是弱极性溶剂;
如果不对称程度比较高,则为高极性溶剂.
非极性的溶剂很少,低极性的溶剂一般包括烃类、氯化烷烃、硝基化烷烃;
中极性的溶剂包括酮类、酯类、醚类和醇醚类;
高极性的溶剂包括醇类和水.
你还可以查一些化工手册,根据偶极矩和氢键力来判断极性.1年前查看全部
- 为什么:co2,甲烷,水是极性键?h2o2和ch3cooh是又有极性又有非极性?过氧化钠又有离子键又有非极性键的?
 买49只飘马鞋1年前4
买49只飘马鞋1年前4 -
 晓玉玉 共回答了22个问题
晓玉玉 共回答了22个问题 |采纳率90.9%在做这样的题目的时候,要区分两组不同的概念.第一.极性键和非极性键的概念.第二.极性分子和非极性分子的概念.离子键 阴阳离子通过静电作用所形成的化学键 阴、阳离子间的相互作用 活泼金属和不活泼非金属通过得失电...1年前查看全部
- 一些橡胶溶于苯中是由于非极性间的相似相溶原理吗?
 qiuxiahui1年前1
qiuxiahui1年前1 -
 317490797 共回答了17个问题
317490797 共回答了17个问题 |采纳率88.2%一些橡胶溶于苯是由于非极性间的相似相溶原理,是溶解度相近缘故.1年前查看全部
- SO2是极性分子还是非极性分子?那SO3呢?为什么?
 AGAINAIR‘S1年前6
AGAINAIR‘S1年前6 -
 贫客 共回答了14个问题
贫客 共回答了14个问题 |采纳率78.6%楼上很明显是瞎扯
SO2折线形分子,有极性
SO3平面,S位于O构成的正三角形中心,无极性1年前查看全部
- NO2中的化学键同学说它和臭氧一样,形成了一个大π建.它是极性还是非极性的?
 yuki姣1年前2
yuki姣1年前2 -
 米有什么不可以 共回答了18个问题
米有什么不可以 共回答了18个问题 |采纳率88.9%形成了一个大π键
是极性分子1年前查看全部
- 极性运输和非极性运输 从浓度上区分 怎样分
 qylhb0011年前1
qylhb0011年前1 -
 lpceblis 共回答了23个问题
lpceblis 共回答了23个问题 |采纳率91.3%极性运输就是物质只能从植物形态学的上端往下运输,而不能倒转过来运输.比如生长素的极性运输:茎尖产生的生长素向下运输,再由根基向根尖运输.生长素是唯一具有极性运输特点的植物激素,其他类似物并无此特性.根尖虽然也产生生长素,且浓度高于根基部,但产生量很少,主要依靠运输,极性运输方向为向顶运输(《高中生物奥赛讲义》,373页;武维华编《植物生理学》:“植物根中的生长素也表现极性运输的性质,不过是由根基部向根尖方向的运输,即向顶运输.”).这种生长素的极性运输可以逆浓度梯度进行.极性运输是主动运输,需要载体和能量.
非极性运输是指植物体内物质的运输不受形态学的上下端影响,所以可以是主动运输也可是被动运输.除极性运输外的运输方式偶尔称为非极性运输,因为非极性运输并不常用.1年前查看全部
- 极性健和非极性健的主要区别?
 fishyxt1年前1
fishyxt1年前1 -
 ferragamo 共回答了18个问题
ferragamo 共回答了18个问题 |采纳率83.3%在单质分子中,同种原子形成共价键,两个原子吸引电子的能力相同,共用电子对不偏向任何一个原子,因此成键的原子都不显电性.这样的共价键叫做非极性共价键,简称非极性键.
在化合物分子中,不同种原子形成的共价键,由于两个原子吸引电子的能力不同,共用电子对必然偏向吸引电子能力较强的原子一方,因而吸引电子能力较弱的原子一方相对的显正电性.这样的共价键叫做极性共价键,简称极性键.
参考资料:高中第一册化学教材
不同种元素的原子间形成的键,都是极性键.(水是极性健.)共用电子对偏向非金属性强原子一方,这种带部分正负电荷叫极性键.1年前查看全部
- 请列举几个高中化学常见的非极性分子
请列举几个高中化学常见的非极性分子
要最右边的原子的下标是双数的. 上帝的玫瑰1年前3
上帝的玫瑰1年前3 -
 掂掂的海岸 共回答了26个问题
掂掂的海岸 共回答了26个问题 |采纳率96.2%氧气``氮气``二氧化碳``乙炔……1年前查看全部
- 乙醇是极性共价化合物?书上说乙醇是极性共价化合物,丁烷是非极性共价化合物.这是不是因为乙醇中有-OH,算作极性,而丁烷中
乙醇是极性共价化合物?
书上说乙醇是极性共价化合物,丁烷是非极性共价化合物.
这是不是因为乙醇中有-OH,算作极性,而丁烷中没有? 微色芽芽1年前1
微色芽芽1年前1 -
 juajua 共回答了13个问题
juajua 共回答了13个问题 |采纳率100%不是的 简单的判断方法 看分子是否对称(要有两条对称轴)
乙醇明显不对称 一端有羟基
丁烷是链状烷烃 对称
像水 分子不是直线型 不对称 所以有极性1年前查看全部
- 下列化合物中,既含有极性键又含有非极性见的是
下列化合物中,既含有极性键又含有非极性见的是
A` NA2O2
B` CH3COONA sonjack1年前2
sonjack1年前2 -
 fkk7 共回答了20个问题
fkk7 共回答了20个问题 |采纳率95%A是过氧化钠,由过氧根离子和钠离子组成
过氧根只有共价键,然后再由极性键和钠离子构成的...没错的1年前查看全部
- 极性化合物和非极性化合物的区别.
 漂在猪海1年前2
漂在猪海1年前2 -
 taotao33 共回答了15个问题
taotao33 共回答了15个问题 |采纳率93.3%极性分子是电荷分布不均匀的分子占多数,所以记住几个非极性分子的例子.
非极性分子就是电荷分布均匀的分子,
如三角锥型的甲烷 P4 ,直线型的双原子单质H2 O2 CL2,直线型的CO2.CS2等,平面三角形的BF3 BCL3
等1年前查看全部
- 为什么极性分子酒精会和非极性分子苯互溶
 蓝键轻敲_1年前1
蓝键轻敲_1年前1 -
 shinyawa 共回答了19个问题
shinyawa 共回答了19个问题 |采纳率89.5%苯分子虽然没有极性,但是苯分子的π电子流动性极强,容易被外界电场极化生成诱导偶极,在酒精中可以视为有一定极性
而且乙醇还有一个非极性基团(乙基)1年前查看全部
- 非单原子单质物质为什么是非极性?
 紫苍吹雪1年前1
紫苍吹雪1年前1 -
 潇洒弟 共回答了16个问题
潇洒弟 共回答了16个问题 |采纳率93.8%是否是极性的 还要开物质的空间结构 看是否能抵消极性 从而总体看就是 非极性的了 双原子的当然是非极性的 但多原子就不一定了 因为空间结构 可能不能抵消极性 总体看就是极性的了1年前查看全部
- 酒精是极性分子还是非极性分子?为什么当苯酚滴在皮肤上可以用酒精冲洗?
 月夜西楼1年前1
月夜西楼1年前1 -
 a54534dcc015047b 共回答了19个问题
a54534dcc015047b 共回答了19个问题 |采纳率94.7%酒精是水和乙醇的混合物,两种分子都是极性分子.
苯酚溶于酒精,究竟对皮肤无毒.就这么简单1年前查看全部
- 既含有极性键又含有非极性键的化合物,属于极性化合物还是非极性化合物啊?
 xyp198009271年前1
xyp198009271年前1 -
 koby1 共回答了26个问题
koby1 共回答了26个问题 |采纳率92.3%极性1年前查看全部
- 怎么判断一个共价化合物是极性还是非极性.
 kenny_he1年前4
kenny_he1年前4 -
 NXLI 共回答了22个问题
NXLI 共回答了22个问题 |采纳率90.9%判断极性分子和非极性分子的最本质方法是:极性分子一个分子内正负电荷中心不重合而非极性分子内正负电荷中心是重合的 极性键存在于不同种元素间 存在极性键的物质不一定是极性分子.区分极性分子和非极性分子的方法:非极性分子的判据:中心原子化合价法和受力分析法 1、中心原子化合价法:组成为ABn型化合物,若中心原子A的化合价等于族的序数,则该化合物为非极性分子.如:CH4,CCl4,SO3,PCl5 2、受力分析法:若已知键角(或空间结构),可进行受力分析,合力为0者为非极性分子.如:CO2,C2H4,BF3 3、同种原子组成的双原子分子都是非极性分子.不是非极性分子的就是极性分子了!
极性分子:HX,CO,NO,H2O,H2S,NO2,SO2,SCl2,NH3,H2O2,CH3Cl,CH2Cl2,CHCl3,CH3CH2OH
非极性分子:Cl2,H2,O2,N2,CO2,CS2,BF3,P4,C2H2,SO3,CH4,CCl4,SiF4,C2H4,C6H6,PCl5,汽油非极性键:两个相同的非金属原子之间形成的共价键.极性键:两个不相同的非金属原子之间形成的共价键.非极性键形成的非极性分子:空间构型完全对称的分子.极性键形成的非极性分子:空间构型不对称的分子.极性键形成的极性分子:空间构型不对称的分子.判断化合物是什么类型的依据是:含离子键的化合物就是离子化合物,仅含有共价键的化合物就是共价化合物.1年前查看全部
- 高中常见的非极性分子有哪些?如题
 o518871年前1
o518871年前1 -
 sdfdsfds23 共回答了16个问题
sdfdsfds23 共回答了16个问题 |采纳率93.8%非极性分子:Cl2,H2,O2,N2,CO2,CS2,BF3,P4,C2H2,SO3,CH4,CCl4,SiF4,C2H4,C6H6,PCl51年前查看全部
- 金刚石为什么不能溶于非极性溶剂
 eeTONGXUE1年前1
eeTONGXUE1年前1 -
 ayftingyu 共回答了26个问题
ayftingyu 共回答了26个问题 |采纳率76.9%相似相容的原理.
金刚石是原子晶体,三维网状结构,结构与有机溶剂大相径庭,当然不会溶.1年前查看全部
- 为什么有机物易溶于非极性溶剂?
 MISATHINKS1年前1
MISATHINKS1年前1 -
 大颗果粒 共回答了23个问题
大颗果粒 共回答了23个问题 |采纳率95.7%因为有机物大都是非极性分子,由于相似相容,所以易溶于非极性溶剂1年前查看全部
- 为什么含两个或两个以上碳的醇 易溶于非极性溶剂
为什么含两个或两个以上碳的醇 易溶于非极性溶剂
甲醇低溶解度于非极性溶剂中,例如己烷,而为什么含两个或两个以上碳的醇 易溶于己烷~· 不可捧梅1年前1
不可捧梅1年前1 -
 永恒~的爱 共回答了27个问题
永恒~的爱 共回答了27个问题 |采纳率96.3%非极性溶剂 由非极性分子组成,是指分子中各原子的化学键的合力为零,如CCl4分子为正四面体,四个C-Cl键的合力为零,CCl4分子无极性,CCl4就是非极性溶剂 .非极性溶剂 "脂肪油(fattyoils) "液状石蜡(1iquidparaffin) "醋酸乙酯(ethyloleate) "肉豆蔻酸异丙酯(isopropylmyristate) .非极性溶剂是由非性分子溶液组成的溶剂,非极性分子多由共价键构成,无或电子活性很小.最简单准确的说就是偶极矩为零的溶剂.知道什么是偶极矩吗?非极性溶剂是由非性分子溶液组成的溶剂,非极性分子多由共价键构成,无或电子活性很小.
偶极矩小的溶剂
通过理解非极性溶剂的意义来明白什么叫极性溶剂
一、相似相溶原理
1.极性溶剂(如水)易溶解极性物质(离子晶体、分子晶体中的极性物质如强酸等);
2.非极性溶剂(如苯、汽油、四氯化碳、酒精等)能溶解非极性物质(大多数有机物、Br2、I2等);
3.含有相同官能团的物质互溶,如水中含羟基(—OH)能溶解含有羟基的醇、酚、羧酸.
二、有机物的溶解性与官能团的溶解性
1.官能团的溶解性:
(1)易溶于水的官能团(即亲水基团)有—OH、—CHO、—COOH、—NH2.
(2)难溶于水的官能团(即憎水基团)有:所有的烃基(—CnH2n+1、—CH=CH2、—C6H5等)、卤原子(—X)、硝基(—NO2)等.
2.分子中亲水基团与憎水基团的比例影响物质的溶解性:
(1)当官能团的个数相同时,随着烃基(憎水基团)碳原子数目的增大,溶解性逐渐降低;
例如,溶解性:CH3OH>C2H5OH>C3H7OH>……,一般地,碳原子个数大于5的醇难溶于水.
(2)当烃基中碳原子数相同时,亲水基团的个数越多,物质的溶解性越大;
例如,溶解性:CH3CH2CH2OH
(3)当亲水基团与憎水基团对溶解性的影响大致相同时,物质微溶于水;
例如,常见的微溶于水的物质有:苯酚 C6H5—OH、苯胺 C6H5—NH2、苯甲酸 C6H5—COOH、正戊醇 CH3CH2CH2CH2CH2—OH(上述物质的结构简式中“—”左边的为憎水基团,右边的为亲水基团);乙酸乙酯 CH3COOCH2CH3(其中—CH3和—CH2CH3为憎水基团,—COO—为亲水基团).
(4)由两种憎水基团组成的物质,一定难溶于水.
例如,卤代烃 R-X、硝基化合物R-NO2 ,由于其中的烃基R—、卤原子—X和硝基—NO2均为憎水基团,故均难溶于水.
三、液态有机物的密度
1.难溶于水,且密度小于水的有机物
例如,液态烃(乙烷、乙烯、苯、苯的同系物……),液态酯(乙酸乙酯、硬脂酸甘油酯……),一氯卤代烷烃(1-氯乙烷……),石油产品(汽油、煤油、油脂……)
注:汽油产品分为直馏汽油和裂化汽油(含不饱和烃).
2.难溶于水,且密度大于水的有机物
例如:四氯化碳、氯仿、溴苯、二硫化碳1年前查看全部
- 有关相似相溶的原理的问题关于含有氢键的物质容易互溶的原理我知道了,不过还有个问题,氢键是不是也可以存在于非极性分子中?-
有关相似相溶的原理的问题
关于含有氢键的物质容易互溶的原理我知道了,不过还有个问题,氢键是不是也可以存在于非极性分子中?- -
那除去氢键,其他分子晶体的相似相溶又是为什么呢?希望能解释得详细一点.
我知道极性分子易溶于极性分子中,非极性分子易溶于非极性分子中。但是为什么会这样 峻川1年前3
峻川1年前3 -
 huahaiyong 共回答了11个问题
huahaiyong 共回答了11个问题 |采纳率100%所谓极性就是分子一段带有部分正电荷(非整数基本电荷),一端带有等量负电荷(又称为偶极,即”两极“),这样的电荷系统,称为电偶极子.非极性分子由于电子的位置是随机的,任一瞬间分子均存在极性(瞬间偶极),只是平均而言没有极性.分子间力本质上起源于分子间的电相互作用(即偶极子间的相互作用).有关基本概念楼主可参见本人对下列问题的回答http://zhidao.baidu.com/question/483469378.html .
溶解过程是破坏溶质分子间力,和一部分溶剂分子间力(假定溶剂量较溶质明显多),而形成溶质和溶剂分子间力的过程.如果这个过程能量降低(即生成的分子间力所对应的势能减小量,大于破坏分子间力引起的势能增大量,引力越强,相互作用势能越低),则该过程可以发生.
这和化学反应的原理完全相同,只是现在涉及的是分子间力,而不是化学键的断裂和形成.分子间力和化学键力都是电磁力没有本质区别,只是数量级不同而已.将化学键力视为广义的分子间力,则该原理可以适用于一切物质的溶解过程.
溶解过程同时是熵增加(分子排列无序度增大)的过程(涉及气体溶解的过程可能有例外),即便溶解过程的能量稍有升高,溶解仍可以发生.如果能量大幅上升,则溶解过程不能发生(发生的程度微乎其微,宏观上看不出任何变化,例如聚乙烯在水中).这和化学反应有不同之处,化学反应的熵未必增加,而溶解过程通常都是熵增加过程,因此溶解过程比化学反应容易讨论.
以上是溶解过程的基本物理化学原理(实际上都是物理原理,想从根本上回答化学问题最终都归结到物理原理).以下进一步讨论.
极性分子间存在固有偶极之间作用产生的强的定向力(也称取向力),同时存在一定的相互诱导偶极与固有偶极间的作用力(诱导力),还具有瞬时偶极间的作用力(色散力).
非极性分子间只存在色散力,色散力主要取决于分子量的大小,因此分子量相当时,极性分子间的引力明显强于非极性分子.极性分子和非极性分子间引力作用有色散力和诱导力,不过诱导力通常比较小,因此极性分子和非极性分子间引力与分子量相当的非极性分子间的引力大小相当.
现在考虑极性化合物乙醇溶于水的例子.乙醇分子间引力较强(但不及水分子间引力强,由沸点可以较准确判断),乙醇进入水中,在水分子的无规则碰撞下,其中的分子可以被动能足够大的水分子陆续”打出“进入水中,水分子立即将这些分子包围,之间形成多个氢键(同时还具有定向力,诱导力和色散力,氢键与普通分子间力也无本质区别,稍强一点而已),同时破坏了部分水分子间的引力.这个过程中能量变化很复杂,对溶解不利的是乙醇分子间引力较强,水分子间引力也很强,有利的是乙醇与水分子间的引力也很强,故总能量变化从微观上难以定性讨论.但我们可以从宏观上得知该过程没有明显吸热或放热(实际上稍有放热),即能量基本不变.而溶解过程是熵增大的过程,只要能量不是大幅上升,溶解就可以发生,能量升高越小越易溶,能量降低越多,就更加易溶.
再如极性HCl气体溶于水的过程.这个过程中气态变溶液态,熵有减小趋势,而形成溶液后水分子排列状况较纯水无序度增大,熵有增大趋势,总体而言熵变化不很大.这时主要因素是溶解过程能量大幅降低.HCl分子进入水中发生电离,破坏H-Cl键能量升高,而产物H+与水分子水合是个剧烈的放热反应,释放的能量供破坏H-Cl键和水分子间引力还有明显富余,因此是能量较多降低,放热较多的过程,易于发生.
再考虑非极性气体CH4溶于水的过程.假定可以溶解,与上面类似,熵不会大幅变化.主要看能量是否降低.CH4分子间只存在较弱的色散力,水分子间存在很强的引力,假定溶解发生CH4和水分子间存在色散力和诱导力,其中色散力与CH4分子间相当,而诱导力通常情况下都很小(大多情况无需考虑).很显然,溶解过程相当于要净的破坏水分子间的强引力,能量大幅升高.从而过程难以发生,溶解度极小.
氢键是不是也可以存在于非极性分子中?含有H-X键可以形成氢键的分子通常都是极性分子,非极性分子中通常不存在H-X键.例外如正硅酸Si(OH)4,整体非极性,可以存在氢键,不过正硅酸通常条件下容易变成偏硅酸(极性分子).
以上内容比较复杂,事实上仍有很多需要讨论的内容,限于篇幅,先讨论到此.如有不明欢迎追问.1年前查看全部
- 怎么样判断XYn分子是极性分子还是非极性分子呢?
怎么样判断XYn分子是极性分子还是非极性分子呢?
如怎么判断BF3是非极性而CH4是极性分子? 水一贴1年前1
水一贴1年前1 -
 houjihong 共回答了14个问题
houjihong 共回答了14个问题 |采纳率100%视情况而定,不过楼上的言论真吓人,CH4是极性分子?天,不要误人子弟.
总之,杂化方式必须与n的值对应,如:sp杂化必须n=2,sp2杂化必须n=3,
sp3杂化必须n=4,这样才无极性.如:BF3是sp2杂化,n=3,则为非极性;NH3是sp3杂化,n=3则为极性,etc.1年前查看全部
- 单质分子一定不含有极性健,对吗.那O3是极性分子还是非极性分子
 2-1241年前5
2-1241年前5 -
 cynag2008 共回答了15个问题
cynag2008 共回答了15个问题 |采纳率100%解析:单质分子一定不含有极性健,这句话正确.因为相同原子之间只能形成非极性键.
O3是极性分子.因为O3中含有两个西格玛键和一个派43键,是角形分子,键的合力不为0,所以它是极性分子.
注:派43键是指三个O原子中有一个提供2个单电子和两个O原子各提供1个单电子形成派43键.这是大学里学的内容.1年前查看全部
- 关于二氧化硅晶体叙述正确的是A含极性公价键 B属极性分子 C属非极性分子 D导热性差 E化学性质稳定 F是良好的电的导体
关于二氧化硅晶体叙述正确的是
A含极性公价键 B属极性分子 C属非极性分子 D导热性差 E化学性质稳定 F是良好的电的导体
是多选的 8568561年前3
8568561年前3 -
 全球最佳坤宠 共回答了22个问题
全球最佳坤宠 共回答了22个问题 |采纳率86.4%ABE1年前查看全部
- 甲苯是非极性溶剂吗?有人说是 那为什么是是非极性的?它的结构为一个苯环和相连的甲基所有烃都为非极性的吗?为什么啊
 斤斗小民1年前1
斤斗小民1年前1 -
 而陪 共回答了18个问题
而陪 共回答了18个问题 |采纳率94.4%严格地说不是非极性的.但是甲苯分子的极性很小,可能被近似认为是非极性溶剂.
不是所有的烃都是非极性的.但是烃类的极性普遍比较小.这个和组成它的原子,和其成键方式有关.C和H的电负性差值本来就不是非常大.1年前查看全部
- 四氯化碳为什么是非极性化合物CCl4为什么是非极性化合物?氯的最外层电子不是接近8,又显负价,为什么电子不是偏向它?另外
四氯化碳为什么是非极性化合物
CCl4为什么是非极性化合物?氯的最外层电子不是接近8,又显负价,为什么电子不是偏向它?另外,系统命名法怎么确定哪条是离主链最近的支链? harrie81年前1
harrie81年前1 -
 yzedu2000 共回答了18个问题
yzedu2000 共回答了18个问题 |采纳率88.9%分子的结构,不是只用一个化学式就能够说明的.还要看它的空间排列.四氯化碳分子中,四个氯原子分布在正四面体的四个顶点处,碳原子在这个正四面体的中心.也就是说,这个结构在空间上是对称的.就算电子有偏向,也是对称着向四周偏向,对整体的极性并没有影响.
你所谓确定最近的支链,其实是说你搞不懂从哪个方向编号吧?原则上要比较两种方向上的编号,看那种编号出现了第一个比对方对应位置小的编号,就采用哪种.已经不是老规定中编号总和最小的那个了.打个可能是不存在的比方:从两头编号,一种是2,3,9,一种是2,4,6;选择第一种.两种编号第一个都是2,分辨不出来,继续往下看,第二个数字,一个是3,一个是4,3比较小,就选择有3的那种编号.即2,3,9那种.尽管2+3+9〉2+4+6,但还是用第一种.1年前查看全部
- I2O4 分子 是极性还是非极性的?
I2O4 分子 是极性还是非极性的?
能用分子图像说明下吗? hzzxxzy1年前1
hzzxxzy1年前1 -
 ln257 共回答了24个问题
ln257 共回答了24个问题 |采纳率79.2%1年前查看全部
- 组成分子的所有化学键均为非极性键,则分子一般为非极性分子?请问特殊情况是什么?
组成分子的所有化学键均为非极性键,则分子一般为非极性分子?请问特殊情况是什么?
烷烃均为 非极性分子吗? 随风的树叶1年前4
随风的树叶1年前4 -
 之痕 共回答了21个问题
之痕 共回答了21个问题 |采纳率90.5%不是 比如 O3 不是非极性分子
烷烃只有结构对称的情况下才有可能式非极性的分子 ,很多带支链的都不是非极性分子.
比如1-丙烯 ,2-甲基丙烷等等都不是非极性分子.1年前查看全部
- 1,2-二氯乙烯 同分异构极性cl H H H 谁是极性谁是非极性\ / \ / c = c c = c / \ / \
1,2-二氯乙烯 同分异构极性
cl H H H 谁是极性谁是非极性
/ /
c = c c = c
/ /
H cl cl cl haihang386541年前1
haihang386541年前1 -
 mandarinduck 共回答了18个问题
mandarinduck 共回答了18个问题 |采纳率88.9%极性大小的判断是大学无机化学的内容,可以根据键能来进行计算,中学阶段只要求定性的了解!
是否是极性分子,以及极性的大小,与分子中正负电子中心有关!正负电荷中心中和或抵消,就是非极性分之,否则就是极性分之!
仔细的说····
极性是矢量,是有方向的.对于两原子之间形成的共价键的极性取决于这两个原子的电负性之差,电负性相差越大,则他们形成的共价键的极性越大.对于两个原子以上的化合物(我们关心的大多为有机物),两原子成键的极性还跟其他原子或者基团有关.对于某复杂化合物,他的极性等于化合物中各键极性的矢量之和.这就是说,我们计算某化合物的极性大小的时候必须先确定该化合物的空间立体结构.这样才能把其中各键的极性正确相加.
此处cl-是拉电子基团而显负电,只要两个负电荷中心(cl-)在分子中关于中心对称,两正电荷中心(H-)也关于中心对称,整个分子无极性.所以
cl H H H
/ /
c = c c = c
/ /
H cl 非极性 cl cl 极性分子1年前查看全部
- (2009•郑州一模)下列物质分子中,既含有极性键又含有非极性键的非极性分子是( )
(2009•郑州一模)下列物质分子中,既含有极性键又含有非极性键的非极性分子是( )
A.C2H4
B.Br2
C.Na2O2
D.H2O2 蔓妹儿1年前1
蔓妹儿1年前1 -
 xsf04 共回答了27个问题
xsf04 共回答了27个问题 |采纳率100%解题思路:非极性共价键为同种非金属元素的原子间形成共价键;极性共价键是由不同种非金属元素的原子间易形成的共价键;由极性键构成的分子,若结构对称,正负电荷的中心重合,则为非极性分子,据此进行判断.A.乙烯分子中含有碳氢极性键和碳碳非极性键,由于乙烯分子结构对称,乙烯分子为非极性分子,故A正确;
B.溴分子中共价键为非极性键,不存在极性键,故B错误;
C.过氧化钠为离子化合物,不存在极性键且不属于极性分子,故C错误;
D.H2O2分子中含有氧氢极性共价键和氧氧非极性共价键,但是双氧水结构不对称,属于极性分子,故D错误;
故选:A.点评:
本题考点: 极性键和非极性键;极性分子和非极性分子.
考点点评: 本题考查化学键的极性、分子极性,题目难度不大,明确化学键、分子极性判断的方法是解答本题的关键,注意熟悉常见分子的构型,试题培养了学生灵活应用所学知识解决实际问题的能力.1年前查看全部
大家在问
- 1以下那项有关酸的陈述是正确的?a:用于汽车电池中的是硝酸b:人体胃部会分泌出硫酸c:可在醋中找到乙酸d:浓氢氯酸是可氧化
- 2用高傲的,高傲地,高傲得,很高傲各造一句话
- 3化学变化是指在变化过程中产生了( )的变化?
- 4物理变化和化学变化的本质区别是:化学变化在变化过程只有_____________变化则没有
- 54厘米 乘 4厘米 等于多少厘米 0.04米乘0.04米等于多少米 是不是我有什么概念性的错误》?
- 622+290=312和312/13=24应该怎么列综合算式
- 7加速度的时间能为负吗
- 8怎样比较分子极性大小
- 9非极性运输,极性运输,横向运输这三者的关系
- 10成人每分钟大约吸入氧气8升,大约需要空气多少升?
- 11为减少含硫煤对大气的污染,宜在煤中加入的物质是() A.熟石膏 B.生石灰 C.硅石 D.烧碱
- 12And don’t eat anything___ four hours .A.to B.for C.at D.of
- 13化学中酸的命名?正酸,过一酸,亚酸,偏酸,亚次酸,焦酸等等的酸是怎么区分的?其他物质也是这样的吗
- 14"嗟尔远道之人胡为乎来哉"中的“为”念第几声?
- 15“其险也如此,嗟尔远道之人胡为乎来哉”里的“也”是什么意思