水合肼用盐酸中和处理可以么
 找不到名2022-10-04 11:39:542条回答
找不到名2022-10-04 11:39:542条回答
已提交,审核后显示!提交回复
共2条回复
 旮旮角角 共回答了16个问题
旮旮角角 共回答了16个问题 |采纳率87.5%- 水合肼为碱性,可以与盐酸反应:
N2H4 + 2HCl = N2H6Cl2
水合肼的水溶性很大,但有毒,最好用酸性高锰酸钾溶液洗涤容器:
4KMnO4 + 6H2SO4 + 5N2H4 = 4MnSO4 + 2K2SO4 + 5N2 + 16H2O - 1年前
 phy1987 共回答了1个问题
phy1987 共回答了1个问题 |采纳率- 可以
- 1年前
相关推荐
- C7H9NO和N2H4·H2O在高温和常温密闭空间里有什么反应?(对氨基苯甲醚和水合肼)
 愤怒的小A1年前1
愤怒的小A1年前1 -
 any_lengyang 共回答了13个问题
any_lengyang 共回答了13个问题 |采纳率69.2%这两者没有反应.
肼只能和不饱和键发生加成反应,比如和羰基发生加成反应.
你说的化合物,其中的氨基以及醚键都不能和肼反应.
欢迎追问,在线回答1年前查看全部
- 一摩尔硝酸镍的重量还有一摩尔肼的重量 80%水合肼 70%水合肼 50%水合肼的重量 1摩尔的
 基围虾00001年前3
基围虾00001年前3 -
 娃哈哈li6 共回答了19个问题
娃哈哈li6 共回答了19个问题 |采纳率78.9%一摩尔物质的质量在数值上等于其相对分子质量
所以:
一摩尔硝酸镍的质量 = 290.81g
一摩尔肼的质量 = 32g
一摩尔80%水合肼的质量 = 40g
一摩尔70%水合肼的质量 = 45.7g
一摩尔50%水合肼的质量 = 64g1年前查看全部
- 想要将80%的水合肼稀释到17%,该如何操作?蒸馏水和水合肼的滴加顺序有没有特殊要求?
 KM5566541年前1
KM5566541年前1 -
 俏豆 共回答了16个问题
俏豆 共回答了16个问题 |采纳率87.5%分类:化学 | 浏览11次1年前查看全部
- 硝酸与水合肼反应方程式
 55bairen551年前1
55bairen551年前1 -
 犬马之才 共回答了22个问题
犬马之才 共回答了22个问题 |采纳率81.8%少量硝酸:
N2H4·H2O + HNO3 = N2H5NO3 + H2O
N2H4·H2O + H+ = N2H5+ + H2O
过量硝酸:
N2H4·H2O + 2 HNO3 = N2H6(NO3)2 + H2O
N2H4·H2O + 2 H+ = N2H6+ + H2O
N2H4与NH3是类似的,N2H5(+)和N2H6(2+)都是用配位键形成的离子,类似于NH4+1年前查看全部
- (2013•湖州二模)水合肼是一种重要的精细化工原料,纯品为无色透明的油状液体,在高温下分解成N2、NH3和H2.水合肼
(2013•湖州二模)水合肼是一种重要的精细化工原料,纯品为无色透明的油状液体,在高温下分解成N2、NH3和H2.水合肼具有还原性,能与碘反应:N2H4+2I2═N2+4HI.在农药、医药及有机合成中有广泛用途.用尿素法制备水合肼,可分为两个阶段,第一阶段为低温氯化阶段,第二阶段为高温水解阶段,总反应方程式为:(NH2)2CO+NaClO+2NaOH→N2H4•H2O+NaCl+Na2CO3
实验步骤:
步骤1.向30%的NaOH溶液中通入Cl2,保持温度在30℃以下,至溶液显浅黄绿色停止通Cl2.静置,检测NaClO的浓度后,倾出上层清液,配制所需浓度的NaClO和NaOH的混合溶液.
步骤2.称取一定质量尿素配成溶液,置于冰水浴.将一定体积步骤1配得的溶液倒入分液漏斗中,慢慢滴加到尿素溶液中,0.5h左右滴完后,继续搅拌0.5h.
步骤3.将步骤2所得溶液,转移到三口烧瓶(见图甲)并加入5gKMnO4作催化剂,边搅拌边急速升温,在108℃回流5min.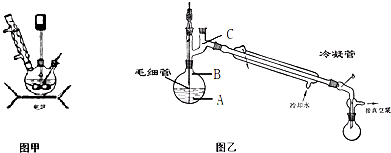
(1)步骤1中检测NaClO浓度的目的是______.步骤2中冰水浴的作用是______.
(2)粗产品倒入图乙的烧瓶中进行减压蒸馏.减压蒸馏的原理是______.在烧瓶中插入一根毛细管,通过蒸馏即可得到纯品.在减压蒸馏过程中毛细管的作用是______,温度计水银球放置的位置是______(填写图中A、B、C).
(3)测定水合肼的质量分数可采用下列步骤:
a.准确称取1.250g试样,经溶解、转移、定容等步骤,配制250mL溶液.
b.移取10.00mL于锥形瓶中,加入20mL水,摇匀.
c.用0.1000mol•L-1碘的标准溶液滴定至溶液出现微黄色且0.5min内不消失,记录消耗溶液的体积.
d.进一步操作与数据处理
①使用容量瓶前要先检漏并洗净,检漏的操作方法是______.
②滴定时,碘的标准溶液盛放在______滴定管中(填“酸式”或“碱式”);称取1.250g试样时所用的仪器是______.
③若本次滴定消耗碘的标准溶液为18.00mL,则产品中N2H4•H2O的质量分数为______.
④为获得更精确的滴定结果,步骤d中进一步的操作是______. 弱水十瓢1年前1
弱水十瓢1年前1 -
 红鸟 共回答了22个问题
红鸟 共回答了22个问题 |采纳率95.5%解题思路:(1)由(NH2)2CO+NaClO+2NaOH→N2H4•H2O+NaCl+Na2CO3可知,检测NaClO浓度可确定尿素和NaOH的用量,步骤2中冰水浴可使温度恒定,减少副反应的发生;
(2)减压蒸馏可使液体在较低温度下沸腾,在减压蒸馏过程中毛细管可起防止暴沸的作用,蒸馏时温度计在蒸馏烧瓶的支管处;
(3)①查漏的操作为在容量瓶中注入适量水,塞上瓶塞,食指顶住瓶塞,另一只手托住瓶底,倒立过来,观察是否漏水,若不漏水,将瓶正立并将瓶塞旋转180°后,再次检验;
②碘水能腐蚀碱式滴定管的橡胶,称取1.250g应选用电子天平;
③由N2H4+2I2=N2+4HI,反应中消耗单质碘的物质的量是1.8×10-3mol,则根据反应的方程式可知水合肼的物质的量是0.9×10-3mol,以此计算质量分数;
④要减少实验误差,则步骤d中进一步操作主要是重复步骤b和c2~3次,依据测得的结果,取平均值.(1)由(NH2)2CO+NaClO+2NaOH→N2H4•H2O+NaCl+Na2CO3可知,检测NaClO浓度可确定尿素和NaOH的用量,步骤2中冰水浴可使温度恒定,减少副反应的发生,
故答案为:确定所需尿素与NaOH的用量;减少副反应的发生;
(2)减压蒸馏可使液体在较低温度下沸腾,在减压蒸馏过程中毛细管可起防止暴沸的作用,蒸馏时温度计在蒸馏烧瓶的支管处,即应在图中的C处,
故答案为:通过减小体系压强,可以使液体在较低温度下沸腾;防止暴沸;C;
(3)①实验的第一步操作为查漏,操作为在容量瓶中注入适量水,塞上瓶塞,食指顶住瓶塞,另一只手托住瓶底,倒立过来,观察是否漏水,若不漏水,将瓶正立并将瓶塞旋转180°后,再次检验,故答案为:在容量瓶中注入适量水,塞上瓶塞,食指顶住瓶塞,另一只手托住瓶底,倒立过来,观察是否漏水,若不漏水,将瓶正立并将瓶塞旋转180°后,再次检验;
②碘水能腐蚀碱式滴定管的橡胶,则碘水应装在酸式滴定管中,称取1.250g应选用电子天平,故答案为:酸式滴定管;电子天平;
③由N2H4+2I2=N2+4HI,反应中消耗单质碘的物质的量是1.8×10-3mol,则根据反应的方程式可知水合肼的物质的量是0.9×10-3mol,所以产品中N2H4.H2O的质量分数为
0.9×10−3mol×25×50g/mol
1.250g=90%,故答案为:90%;
④减少实验误差,则步骤d中进一步操作主要是重复步骤b和c2~3次,依据测得的结果,取平均值,故答案为:重复步骤b和c1~2次.点评:
本题考点: 性质实验方案的设计;物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题是高考中的常见题型,属于中等难度的试题,试题综合性强,难易适中,侧重对学生基础知识的巩固与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,同时也注重对学生答题能力的培养和方法指导,有利于培养学生的逻辑思维能力和发散思维能力.1年前查看全部
- 还原500克氯化银需多少克水合肼
 木冰儿1年前1
木冰儿1年前1 -
 洪亮_abc 共回答了9个问题
洪亮_abc 共回答了9个问题 |采纳率88.9%一水合肼是强还原剂,1mol肼可以还原4molAg,x0d500gAgCl的物质的量是500/143.5 mol,所以只需0.87mol水合肼,质量x0d0.87*50 =39g.x0dAgCl的Ag的质量分数是108/143.5=75.26%.500gAgCl含Ag=378g.x0d因为还原出来的Ag是细微颗粒的银粉,所以灰黑色的沉淀.1年前查看全部
- 请问哪位做过水合肼还原硝基的反应?
 rainshu01071年前1
rainshu01071年前1 -
 newdays365 共回答了24个问题
newdays365 共回答了24个问题 |采纳率91.7%用钯碳和水合肼可以还原,很简单,可以用个氮气保护,但是你的分子结构如果存在苄基的话就不要用水合肼了,因为会掉1年前查看全部
- 氢氟酸和水合肼会不会发生化学反应
 tianl1071年前1
tianl1071年前1 -
 xiaohuamandy 共回答了13个问题
xiaohuamandy 共回答了13个问题 |采纳率76.9%水合肼是碱性可以和酸性氢氟酸生成水合肼氟酸盐.1年前查看全部
- 水合肼85% 80%等指的是重量百分比还是体积百分比
 20023011441年前1
20023011441年前1 -
 aikeyeung 共回答了19个问题
aikeyeung 共回答了19个问题 |采纳率89.5%是体积比
(这一点无论是从日常实验还是标准来看都是一样的)1年前查看全部
- 贵金属提炼时使用水合肼还原贵金属问题
贵金属提炼时使用水合肼还原贵金属问题
贵金属提炼时使用水合肼还原贵金属的原理是什么?还要使用其他的催化剂么?对反应条件有何要求?如PH,温度等/ syqnet1年前1
syqnet1年前1 -
 此人已挂失 共回答了17个问题
此人已挂失 共回答了17个问题 |采纳率94.1%一种无色发烟的、具有腐蚀性和强还原性的液体化合物NH2NH2 [hydrazine],它是比氨弱的碱,通常由水合肼脱水制得,主要用作火箭和喷气发动机的燃料部分,用在制备盐(如硫酸盐)及有机衍生物中1年前查看全部
- 金、钯溶于王水后,用亚硝酸钠反应还原提纯黄金后的分离液与水合肼还原重金属,这个过程的反应方程式是怎样的呀?
 weiqian1231年前2
weiqian1231年前2 -
 神在左右 共回答了18个问题
神在左右 共回答了18个问题 |采纳率100%首先金、钯都能溶于王水:
HNO3 + 4HCl + Au ====NO↑ + H[AuCl4] + 2H2O
3Pd + 12HCl + 2HNO3 =====2NO↑ + 3H2[PdCl4] + 4H2O
加入亚硝酸钠作为还原剂,选择性还原出金的单质.在这个过程中亚硝酸钠转为硝酸钠.
3NO2- + 2AuCl4- + 3H2O ====2Au↓ + 3NO3- + 6H+ +8Cl-
之所以能做到这一点,可能是因为电对AuCl4- /Au 高达1.0V,而钯对应电对的电势我记不清了,不过应该在0.7V左右.
接下来用水合肼这种非常强的还原剂将钯还原出来:
N2H4 + 2H2[PdCl4] ====2Pd↓ + N2↑ + 8HCl
当然,肼作为碱性物质,还会和盐酸反应成盐.
欢迎追问!1年前查看全部
- 含Au王水 用草酸或水合肼还原
 梧聊白金1年前3
梧聊白金1年前3 -
 iamfine 共回答了13个问题
iamfine 共回答了13个问题 |采纳率84.6%是可以的,有还原性就行了.我用的是亚硫酸钠还原的,得到的是海绵金,黄褐色的.沉淀干燥后高温灼烧变为黄色,金属光泽.1年前查看全部
- 用水合肼还原银氨溶液的一点疑问,银氨溶液银的溶度40g以下一升,还原温度50度左右,还原出来的银没有金属光泽,也没有在一
用水合肼还原银氨溶液的一点疑问,银氨溶液银的溶度40g以下一升,还原温度50度左右,还原出来的银没有金属光泽,也没有在一点集中,银表面灰色(带一点黑色),烘干之后白色,也没有金属光泽,用手搓一下成细小粉粒.有金属硬的感觉.在还原烧杯壁上有一层银,把银乱下,银表面发光,是一层银皮.
为什么银沉淀没有在一点集中.
为什么银沉淀没有金属光泽(烘干也没有).(是不要处理瓶壁,如要又怎样处理)
为什么在还原烧杯壁上有一层带金属光泽的银皮 itistobe1年前1
itistobe1年前1 -
 真难申请啊 共回答了17个问题
真难申请啊 共回答了17个问题 |采纳率100%反应实在反应物接触的地方产成的,这和固体+液体的反应就不一样了,所以不会一点集中1年前查看全部
- 肼解反应操作.邻苯二甲酰亚胺与水合肼的反应.反应条件?催化剂选择?溶剂选择?后处理方法?你给我的答案又是去复制的,你们自
肼解反应操作.
邻苯二甲酰亚胺与水合肼的反应.
反应条件?催化剂选择?溶剂选择?后处理方法?
你给我的答案又是去复制的,你们自己没有做过这类反应吗? 刘川本人1年前1
刘川本人1年前1 -
 饶命 共回答了13个问题
饶命 共回答了13个问题 |采纳率84.6%化学的东西很多 都得参考文献,谁能保证什么反应都做过.
给你个例子如下
叔丁胺盐酸盐的合成.
在装有球型回流冷凝器的2升瓶中加入203克(1摩尔)叔丁基邻苯二甲酰亚胺,一升95%的乙醇和59克(1摩尔)的85%水合肼.溶液加热至回流2小时,冷却,加入盐酸(约100毫升.)调节溶液ph至刚果红试纸显强酸性,但酸不要过量.将反应产生的大量沉淀物邻苯二甲酰肼收集到直径15厘米的布氏漏斗中,并用4x100ml 95%乙醇冲洗.合并滤液和洗液,减压浓缩至约200毫升.加入1升水,过滤去除掉任何不溶性物质,再将滤液浓缩至约300-350毫升.如果再有不溶性物质出现仍然用过滤方法将其除去,然后减压蒸除所有溶剂.粗品胺盐酸盐按如下方法精制:将粗品溶解于500毫升无水乙醇,过滤除去不容物,滤液中加入500ml干乙醚.
具体如下:粗胺盐酸盐用无水乙醇溶解,每克粗品约用无水乙醇5毫升,加入绝对乙醚(乙醇量的50%),将以上溶液在冰箱冷却析晶几个小时.将所有的纯品叔丁胺盐酸盐用布氏漏斗过滤收集,并在真空干燥器中干燥.重量约为79-97克(72-88%),熔点270-290 并升华.1年前查看全部
大家在问
- 1狮子王2的英文内容简介和影评一切有关狮子王2的英文的东西 剧本除外
- 2把下列二次函数化为y=a(x+k)²+h的形式
- 3夜宿山寺的诗句是什么?
- 4三极管实现放大作用的内部结构条件和外部偏置条件有哪些?
- 5一个圆柱形铁皮水桶底面半径3分米他的侧面展开正好是一个正方形求这个水桶的容积
- 6下列不能发生化学反应的是铁和氢氧化钠溶液 氧化亚铁粉末和二氧化硅铁粉末共热氯化铁溶液中加入氨水氢氧化铁胶体中加入盐酸请告
- 7Kate was not at school for three days=Kate was () () for thr
- 8这个曲线上切线斜率能求么?已知几个点的坐标,在坐标纸上描出这几个点然后用平滑的曲线连接起来,能求出曲线在这几个点的斜率么
- 9氧气汇流排总公司告诉您气体汇流排包括哪些?
- 102005年11月11日,北京2008奥运会吉祥物“福娃”诞生.回答1--3题.
- 11求一影响光合作用的因素的实验方案!(co2浓度、光照强度、温度是最常见的影响光合作用强度的因素,根据
- 12求古诗《夏意》的意思
- 13popular意思 because意思
- 14(-2)的15次方是( )数,(-2)的20次方是( )数,-2的15次方是( )数,-22的20次方是( )数(填正或
- 15悲愤欲绝的绝和这个词是什么意思还有与世长辞
