碱石灰可干燥哪些物质,反应式为?
 gcm20032022-10-04 11:39:541条回答
gcm20032022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 lgq4472618 共回答了23个问题
lgq4472618 共回答了23个问题 |采纳率87%- 碱石灰能干燥碱性或中性气体,例如O2、H2、NH3、CH4、C2H4、C2H2等气体,它的干燥原理是利用碱石灰中的氢氧化钙或氢氧化钠的吸水能力,吸去气体中的水蒸气. 望采纳.
- 1年前
相关推荐
- 化学实验室常用的干燥剂“碱石灰”,碱石灰是由固体烧碱NaOH和生石灰CaO组成的混合物,极易与空气中水蒸汽和CO2反应而
化学实验室常用的干燥剂“碱石灰”,碱石灰是由固体烧碱NaOH和生石灰CaO组成的混合物,极易与空气中水蒸汽和CO2反应而变质.某探究小组对一瓶久置空气中的“碱石灰”作了如下探究:
假设与猜想:猜想Ⅰ:没有变质,“碱石灰”只含有CaO、固体NaOH;
猜想Ⅱ:已完全变质,“碱石灰”全部变成了CaCO3和Na2CO3.
则CaO与水反应的反应方程式为______.
活动与探究:如图所示:
解释与结论:
(1)若Ca(OH)2、CaCO3和Na2CO3投入到水中不会放热,则由操作②现象判断:猜想Ⅱ______(填:成立、不成立).
(2)操作④发生反应的化学方程式为______;由操作⑤⑥的现象判断:滤液中含有______(写化学式);由此判断猜想Ⅰ______(填:成立、不成立).
(3)综合上述(1)和(2)的结论,判断该样品变质情况为______.
应用与拓展:由上述实验说明,化学实验室中干燥剂“碱石灰”应采用保存方法为______;操作③中玻璃棒的作用是______. 7456921年前1
7456921年前1 -
 xalw 共回答了22个问题
xalw 共回答了22个问题 |采纳率77.3%解题思路:假设与猜想:直接写出氧化钙反应的化学方程式
【解释与结论】(1)CaCO3和Na2CO3投入到水中不会放热,而步骤②中放出热量,所以猜想Ⅱ不成立,
(2)向滤渣中加入稀盐酸产生气体,可以知道该滤渣中含有碳酸钙,向滤液中加入稀盐酸和氢氧化钙后产生了气体和沉淀,可以判断在滤液中含有碳酸钠.
(3)结合实验,可以知道在固体中含有碳酸钙,碳酸钠和氧化钙,可以据此作出判断.
【应用与拓展】对于能够和空气中的成分反应而发生变质的物质,必须密封保存.【猜想】直接写出氧化钙和水的化学方程式,故本题答案为:CaO+H2O=Ca(OH)2;
【解释与结论】(1)CaCO3和Na2CO3投入到水中不会放热,而步骤②中放出热量,所以猜想Ⅱ不成立,故本题答案为:不成立
(2)向滤渣中加入稀盐酸产生气体,可以知道该滤渣中含有碳酸钙,向滤液中加入稀盐酸和氢氧化钙后产生了气体和沉淀,可以判断在滤液中含有碳酸钠,这说明在固体中有碳酸钙和碳酸钠,所以猜想Ⅰ不成立,故本题答案为:CaCO3+2HCl=CaCl2+CO2↑+H2O; Na2CO3;不成立
(3)结合实验,可以知道在固体中含有碳酸钙,碳酸钠和氧化钙或者氢氧化钠,故可以判断干燥剂是部分变质,故本题答案为:部分变质;
【应用与拓展】对于能够和空气中的成分反应而发生变质的物质,必须密封保存,在过滤时玻璃棒的作用就是引流,故本题答案为:密封;引流(或导流),防止溶液外溅.
故本题答案为:【猜想】CaO+H2O=Ca(OH)2;
【解释与结论】(1)不成立
(2)CaCO3+2HCl=CaCl2+CO2↑+H2O; Na2CO3;不成立
(3)部分变质;
【应用与拓展】密封;引流(或导流),防止溶液外溅.点评:
本题考点: 药品是否变质的探究;证明碳酸盐;生石灰的性质与用途;盐的化学性质;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 熟练掌握碳酸钠、碳酸钙等碳酸盐和氢氧化钠、氧化钙的化学性质,能根据所给的实验或者自己设计实验来验证它们是否变质,并熟练的写出相应的化学方程式:CaCO3+2HCl=CaCl2+CO2↑+H2O;CaO+H2O=Ca(OH)21年前查看全部
- 关于苯的溴代反应如图所示,请问此反应中碱石灰、氢氧化钠溶液和蒸馏水的作用,和起作用时涉及的化学方程式.麻烦写详细点,我真
关于苯的溴代反应
如图所示,请问此反应中碱石灰、氢氧化钠溶液和蒸馏水的作用,和起作用时涉及的化学方程式.
麻烦写详细点,我真的是没有财富值了为了学习,体谅体谅,谢谢了!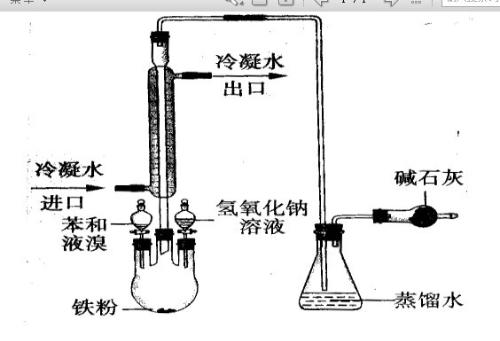
 goostop1年前1
goostop1年前1 -
 紫苹果 共回答了22个问题
紫苹果 共回答了22个问题 |采纳率90.9%碱石灰是除去溢出的溴化氢,蒸馏水是为了吸收溴化氢,氢氧化钠是除去反应多余的液溴,纯化产物.
方程式:C6H6+Br2→Fe→C6H5Br+HBr
2 NaOH+Br2==NaBr+NaBrO+H2O
Ca(OH)2+2HBr==CaBr2+H2O1年前查看全部
- 有以下6种物质,结合 有以下6种物质,结合相关问题填空: ①Al ②FeCl 3 溶液 ③SO 2 ④碱石灰 ⑤液氨
有以下6种物质,结合
有以下6种物质,结合相关问题填空:
①Al ②FeCl 3 溶液 ③SO 2 ④碱石灰 ⑤液氨 ⑥NaOH固体
(1)能导电的是___________;属于非电解质的是___________
(2)碱石灰常用作干燥剂,其不能干燥下列___________气体(以上各空用相关编号填写)
A.H 2 B.NH 3 C.CO 2 D.O 2
(3)①与⑥溶液反应的产物中Al的化合价为___________价;其反应的化学方程式为:______________________________
(4)向②溶液中加入KI溶液后,用CCl 4 萃取,CCl 4 层呈紫色,写出该反应过程的离子方程式:
________________________________ 阿B为什么1年前1
阿B为什么1年前1 -
 lkxvcjlk23jlkfaj 共回答了17个问题
lkxvcjlk23jlkfaj 共回答了17个问题 |采纳率88.2%(1)①②;③⑤
(2)C
(3)+3;2Al+2H 2 O+2NaOH==2NaAlO 2 +3H 2 ↑
(4)2Fe 3+ +2I - ==2Fe 2+ +I 21年前
51年前查看全部
- 实验室用无水醋酸钠和碱石灰制甲烷,若要制乙烷可选择的试剂是碱石灰和( ),化学方程式:
 ailemon1年前4
ailemon1年前4 -
 轨辰qq 共回答了27个问题
轨辰qq 共回答了27个问题 |采纳率85.2%(无水CH3CH2COONa)
CH3CH2COONa+NaOH---→CH3CH3↑+Na2CO3
条件是 CaO加热1年前查看全部
- 动物需要呼吸的实验中碱石灰的作用是
 虎笑风中1年前1
虎笑风中1年前1 -
 jin109 共回答了22个问题
jin109 共回答了22个问题 |采纳率90.9%将动物呼出的二氧化碳完全吸收干净1年前查看全部
- 标况下1.68升无色可燃气体,在足量O2中燃烧,产物通过足量的澄清石灰水得到白色沉淀15g,或用足量的碱石灰吸收产物,增
标况下1.68升无色可燃气体,在足量O2中燃烧,产物通过足量的澄清石灰水得到白色沉淀15g,或用足量的碱石灰吸收产物,增重9.3g.1.计算产物中水的质量.2.若气体为单一气体,推断其分子式 3.若气体是两种等物质的量的气体混合,其中一种是烃,写出分子式
 小马过大河1年前0
小马过大河1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 在硅与氯气反应制四氯化硅的装置中为什么要将反应产物先通入放在冷水中的集气瓶内然后再通过碱石灰?通...
在硅与氯气反应制四氯化硅的装置中为什么要将反应产物先通入放在冷水中的集气瓶内然后再通过碱石灰?通...
在硅与氯气反应制四氯化硅的装置中为什么要将反应产物先通入放在冷水中的集气瓶内然后再通过碱石灰?通过碱石灰是为了除氯气,但为什么还要先通入置于冷水中的集气瓶内,也就是为什么要让四氯化硅和氯气的混合气体先变为液态? xx残留1年前1
xx残留1年前1 -
 dudu961 共回答了16个问题
dudu961 共回答了16个问题 |采纳率93.8%为了让四氯化硅气体先变为液态与氯气分离1年前查看全部
- 硅胶,碱石灰,生石灰的化学式
 evlawjzx1年前1
evlawjzx1年前1 -
 yester1314 共回答了19个问题
yester1314 共回答了19个问题 |采纳率89.5%硅胶:mSiO2·nH2O 属非晶态物质 碱石灰:就是熟石灰 Ca(OH)2 生石灰:CaO1年前查看全部
- 为什么用H2吹肥皂泡要先通过碱石灰干燥剂
为什么用H2吹肥皂泡要先通过碱石灰干燥剂
用氢气流吹肥皂泡,为什么要在球形管里装碱石灰呢?是干什么用的,如果直接吹会怎样.不行吗. 却尘1年前1
却尘1年前1 -
 klb914 共回答了22个问题
klb914 共回答了22个问题 |采纳率90.9%氢气实验室制法是用Zn和酸反应制得,用碱石灰是用来干燥氢气和除去杂质酸,这样可以避免酸与肥皂水反应 因为肥皂水是显碱性的1年前查看全部
- 有两种气态烃组成的混合气体20ml与氧气混合后,进行完全燃烧,燃烧产物通过浓硫酸时,体积减少30ml,然后通过碱石灰,体
有两种气态烃组成的混合气体20ml与氧气混合后,进行完全燃烧,燃烧产物通过浓硫酸时,体积减少30ml,然后通过碱石灰,体积又减少了40ml(均折算为标准状况下),求混合烃的组成(我知道c:H=2:3,)
 zz0071年前3
zz0071年前3 -
 snowhcm 共回答了19个问题
snowhcm 共回答了19个问题 |采纳率89.5%看看哪两种烃原子数加起来平均数是2:3,是不是仅剩下乙炔和乙烯(摩尔数之比为1:1)、乙炔和乙烷(摩尔数之比为3:1)1年前查看全部
- 为什么干燥NH3只能用碱石灰?请写出其原理
 tom_11081年前1
tom_11081年前1 -
 smogfog 共回答了20个问题
smogfog 共回答了20个问题 |采纳率80%因为NH3是碱性气体,所以不能用H2SO4等酸性干燥剂干燥1年前查看全部
- hcl.fecl3.so2.碱石灰,氨气,na9h.其中哪两个相遇会产生白烟
 khkh1年前2
khkh1年前2 -
 丫雅oo 共回答了14个问题
丫雅oo 共回答了14个问题 |采纳率92.9%HCl+NH3=NH4Cl(白烟)1年前查看全部
- 常用的固体干燥剂有原始铁粉,烧碱,生石灰或碱石灰.小明认为原始干燥剂肯定不是烧碱或碱石灰的理由?
常用的固体干燥剂有原始铁粉,烧碱,生石灰或碱石灰.小明认为原始干燥剂肯定不是烧碱或碱石灰的理由?
还有铁粉 mingtaoqiu31年前3
mingtaoqiu31年前3 -
 fjeb4 共回答了16个问题
fjeb4 共回答了16个问题 |采纳率81.3%用过的干燥剂是白色且完全不溶于水1年前查看全部
- 下面气体既能用浓硫酸干燥,又能用碱石灰干燥的是?
下面气体既能用浓硫酸干燥,又能用碱石灰干燥的是?
二氧化碳,氨气,一氧化碳,氯气
反映的话方程式是什么? lele198220041年前4
lele198220041年前4 -
 基督教321 共回答了19个问题
基督教321 共回答了19个问题 |采纳率89.5%是一氧化碳,
CO2与碱石灰反应,氨气与浓硫酸反应,氯气与碱石灰反应.
CO2+2NaOH=Na2CO3+H2O,或CO2+NaOH=NaHCO3
NH3+H2SO4=NH4HSO4,2NH3+H2SO4=(NH4)2SO4,
Cl2+2NaOH=NaCl+NaClO+H2O1年前查看全部
- 既可以被浓硫酸干燥也可以被碱石灰干燥的是?
既可以被浓硫酸干燥也可以被碱石灰干燥的是?
A.氧气、氢气、一氧化碳B.氢气、氯气、氧气C.氨气、二氧化硫、氧气D.氨气、二氧化硫、碘化氢 weisensky1年前1
weisensky1年前1 -
 夏语ly 共回答了19个问题
夏语ly 共回答了19个问题 |采纳率94.7%一氧化碳CO1年前查看全部
- 请问丙方案为什么不可以?通过碱石灰测出二氧化碳的质量 通过浓硫酸测出水的质量 再用总量减去水的质量和二氧化碳的质量不就是
请问丙方案为什么不可以?通过碱石灰测出二氧化碳的质量 通过浓硫酸测出水的质量 再用总量减去水的质量和二氧化碳的质量不就是一氧化碳年的质量吗
(2006•盐城)某有机物6.4g在8.0g氧气中燃烧,得到一氧化碳、二氧化碳、水蒸气的混合气体共14.4g为测定混合气体中各种气体的质量,甲、乙、丙三位同学设计了下列实验方案(假定每步反应都完全进行,每次都能准确测定装置的质量变化)
甲方案:将混合气体先通过浓硫酸,再通过用酒精灯加热的氧化铁
乙方案:将混合气体先通过浓硫酸,再通过碱石灰(CaO、NaOH的混合物)
丙方案:将混合气体先通过碱石灰,再通过浓硫酸
下列对三种实验方案的评价正确的是( )
A.三种实验方案都能测定混合气体的组成
B.三种实验方案都不能测定混合气体的组成
C.甲乙两种实验方案都能测定混合气体的组成,但甲方案需作改进,添加尾气处理装置
D.甲乙两种实验方案都能测定混合气体的组成,但乙方案需作改进,添加尾气处理装置 zengturks1年前3
zengturks1年前3 -
 NESTA我的爱 共回答了20个问题
NESTA我的爱 共回答了20个问题 |采纳率100%碱石灰 能与二氧化碳反应也能与水反应,所以 丙方案不对1年前查看全部
- 初中化学科学探究 为什么(4)不选B啊,碱石灰在这里有什么作用啊.
初中化学科学探究

为什么(4)不选B啊,碱石灰在这里有什么作用啊.
 月亮爱大海1年前3
月亮爱大海1年前3 -
 panamway 共回答了11个问题
panamway 共回答了11个问题 |采纳率100%前面浓硫酸是用来干燥CO2气体,后面的浓氢氧化钠用来吸收co2、,一般浓氢氧化钠的量是足够吸收CO2的,所以不需要用后面的碱石灰吸收,因为即使吸收,它还会吸收水分,因此不是吸收的纯CO2,这样会是实验结果偏差大,这里它就是用来吸收水的1年前查看全部
- 碱石灰能干燥CO2和O2吗?
 hellotuzi1年前2
hellotuzi1年前2 -
 种菜妹别走 共回答了15个问题
种菜妹别走 共回答了15个问题 |采纳率100%能干燥O2,但不能干燥CO2,因为CO2会和碱石灰反应生成碳酸钙和水1年前查看全部
- 制溴苯时的几个问题1.制溴苯时,干燥管中的碱石灰的作用是?2.反应过程中,(1)锥形瓶的上方的导管为什么不插入液面下?(
制溴苯时的几个问题
1.制溴苯时,干燥管中的碱石灰的作用是?
2.反应过程中,(1)锥形瓶的上方的导管为什么不插入液面下?(2)在导管的末端能看到什么实验现象?这是由于反应生成的(3)遇锥形瓶中的(4)而形成(5)的小液滴. 刺鱼鱼刺1年前1
刺鱼鱼刺1年前1 -
 清茶中的泪 共回答了15个问题
清茶中的泪 共回答了15个问题 |采纳率93.3%碱石灰是用于吸收溴化氢气体
导管不插入液面下是为了防倒吸
导管的末端出现小液滴是溴化氢凝结成的1年前查看全部
- 在标准状况下,112ML某气态烃完全燃烧后生成二氧化碳和水蒸气的体积之比是3:4,把燃烧物产物通过碱石灰,质量增加1.0
在标准状况下,112ML某气态烃完全燃烧后生成二氧化碳和水蒸气的体积之比是3:4,把燃烧物产物通过碱石灰,质量增加1.02g,求气态烃的分子式.
这两个体积怎么能比一块去?一个气体一个液体啊 怎么求 jion88881年前3
jion88881年前3 -
 badpjj 共回答了21个问题
badpjj 共回答了21个问题 |采纳率95.2%他说的是二氧化碳与水蒸气之比的体积,水蒸气已经是气态存在了.
生成物只有二氧化碳与水蒸气,通过碱石灰增重,那么就是有1.02g的水与二氧化碳生成.112ml的气体是112ml/22.4l=0.005mol(一摩尔的气体体积为22.4l),气体体积比就是物质量比,即CO2:H2O=3:4(二氧化碳分子量44,水分子量18)两则总质量为1.02.设二氧化碳为3xmol,水为4xmol,得出,x=0.005,则二氧化碳为0.015mol,水为0.02mol.根据元素守恒,水中的氢与二氧化碳中的碳都只来源于烃,则碳=0.015/0.05=3,H=0.02*2/0.05=8,所以烃为C3H81年前查看全部
- 某有机物13.2g在过量的氧气中完全燃烧,把燃烧后的气体缓慢通过足量的碱石灰,碱石灰增重44.88g;若把燃烧后的气体通
某有机物13.2g在过量的氧气中完全燃烧,把燃烧后的气体缓慢通过足量的碱石灰,碱石灰增重44.88g;若把燃烧后的气体通过浓硫酸,浓硫酸增重15.84g.已知该有机物的蒸气密度是相同条件下氢气的30倍.
为什么说 该有机物的蒸气密度是相同条件下氢气的30倍得出M(有机物)=60 moon_spa1年前1
moon_spa1年前1 -
 cappuccin_w 共回答了13个问题
cappuccin_w 共回答了13个问题 |采纳率92.3%因为有机物蒸汽密度是相同条件下氢气的30倍,根据 密度比 = 相对分子质量比
所以该有机物相对分子质量为:30*2 = 601年前查看全部
- 某一元有机羧酸的铵盐 7.7g,与足量的碱石灰混合后共热,收集的氨气[标况下]的体积为2,24L,
某一元有机羧酸的铵盐 7.7g,与足量的碱石灰混合后共热,收集的氨气[标况下]的体积为2,24L,
则形成此盐的有机羧酸结构简式为:乙酸 地狱下的天使1年前1
地狱下的天使1年前1 -
 小虫子523 共回答了21个问题
小虫子523 共回答了21个问题 |采纳率100%CxHyCOONH4+OH- =NH3
0.1 mol 0.1mol
7.7g
CxHyCOONH4分子量为77,可以知道 CxHyCOOH的分子量为60,就只能乙酸了, CH3COOH1年前查看全部
- (5分)有机物A是烃的含氧衍生物,1.38gA完全燃烧后,若将燃烧的产物通过碱石灰,碱石灰的质量会增加3.06g;若将燃
(5分)有机物A是烃的含氧衍生物,1.38gA完全燃烧后,若将燃烧的产物通过碱石灰,碱石灰的质量会增加3.06g;若将燃烧产物通过浓硫酸,浓硫酸的质量会增加1.08g;取4.6gA与足量的金属钠反应,生成的气体在标准状况下的体积为1.68L;A不与纯碱反应。该有机物的质谱图中质荷比的最大值是92。通过计算确定A的分子式和结构简式。
 叉嘴米菲兔1年前0
叉嘴米菲兔1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 以下是我们熟悉的实验室制取气体的发生装置、收集装置以及净化装置(装置⑦中碱石灰为固体氢氧化钠和氧化钙的混合物).
以下是我们熟悉的实验室制取气体的发生装置、收集装置以及净化装置(装置⑦中碱石灰为固体氢氧化钠和氧化钙的混合物).

请根据装置图回答下列问题:
(1)若用装置⑥净化气体,则气体应从______端通入(填“a”或“b”).
(2)实验室用过氧化氢溶液和二氧化锰制取一瓶干燥氧气,应选用的装置为______、(填装置的编号),其反应方程式为2H2O2
2H2O+O2↑MnO2 .2H2O2.
2H2O+O2↑MnO2 . amxh1年前1
amxh1年前1 -
 dearkathy2006 共回答了26个问题
dearkathy2006 共回答了26个问题 |采纳率92.3%解题思路:(1)洗气装置中导管长进短出;
(2)用过氧化氢溶液和二氧化锰制取一瓶干燥氧气,选择固液常温制气的发生装置,用浓硫酸干燥,排空气法收集.(1)若用装置⑥净化气体,则气体应从长导管进入,故从b通入;
(2)用过氧化氢溶液和二氧化锰制取一瓶干燥氧气,选择固液常温制气的发生装置②,用浓硫酸干燥,选择⑥,氧气的密度比空气大,用向上排空气法收集,反应方程式是:2H2O2
MnO2
.
2H2O+O2↑;
故答案为:(1)b;(2)②⑥③;2H2O2
MnO2
.
2H2O+O2↑.点评:
本题考点: 常用气体的发生装置和收集装置与选取方法.
考点点评: 洗气装置中导管长进短出,据反应物状态和反应条件选择发生装置,据气体的密度和溶解性选择收集装置,浓硫酸具有吸水性,可作干燥剂.1年前查看全部
- 碱石灰与水与CO2混合会怎样?写出方程式.
 大饼比油条好吃1年前3
大饼比油条好吃1年前3 -
 不是你的就别动 共回答了21个问题
不是你的就别动 共回答了21个问题 |采纳率85.7%碱石灰是氢氧化钠和氧化钙的混合物
CaO + H2O === Ca(OH)2(此反应放出热量)
CO2 +Ca(OH)2 ==CaCO3↓+ H20
2NaOH + CO2 ==== Na2CO3 + H2O1年前查看全部
- 某气态烃4mL加入30mL氧气,完全燃烧后冷却到室温,体积为20mL,再通过碱石灰,气
某气态烃4mL加入30mL氧气,完全燃烧后冷却到室温,体积为20mL,再通过碱石灰,气
体还剩余4mL,求该烃分子式.
答案是C4H10 lis81881年前1
lis81881年前1 -
 狒狒0831 共回答了28个问题
狒狒0831 共回答了28个问题 |采纳率92.9%用通式.CxHy+(x+y/4)O2===xCO2+y/2H2O(条件为点燃)完全燃烧,说明无烃和CO,后冷却到室温说明水是液态.再通过碱石灰,气体还剩余4ml,说明有O2剩余.减去O2的体积,20-4=16ml的CO2产生
CxHy+(x+y/4)O2===xCO2+y/2H2O
1 x
4 16
通过1/4=x/16的比值计算.得到x=4
CxHy+(x+y/4)O2===xCO2+y/2H2O
1 4+y/4
4 30-4
1/4=4+(y/4)/30-4得到y=10.
所以CxHy=C4H10.1年前查看全部
- 实验室制取甲烷的反应1.碱石灰中CaO不是不参加反应么,他是干什么用的?2.反应方程式CH3COONa+NaOH==加热
实验室制取甲烷的反应
1.碱石灰中CaO不是不参加反应么,他是干什么用的?
2.反应方程式CH3COONa+NaOH==加热==Na2CO3+CH4↑
是什么基本反应类型? 翻跟斗1年前1
翻跟斗1年前1 -
 橡皮公主 共回答了15个问题
橡皮公主 共回答了15个问题 |采纳率86.7%CaO应该吸收水分,是Na2CO3能够析出使反应能向CH4产生方向进行;应该算复分解反应的一种吧,其实应该是产生了自由基促使反应的进行的.1年前查看全部
- 一氧化碳,二氧化碳,水蒸气,氢气通过碱石灰,气体体积减小是怎么回事
 xinyalei1年前1
xinyalei1年前1 -
 zs984102241 共回答了12个问题
zs984102241 共回答了12个问题 |采纳率91.7%因为碱石灰可以与二氧化碳和水蒸气反应.
CaO+H2O=Ca(OH)2
CaO+CO2=CaCO3
2NaOH+CO2=Na2CO3+H2O1年前查看全部
- 取标准状况下CH4和过量O2的混合气体840ml,点燃,将燃烧后的产物用过量碱石灰(CaO和NaOH)吸收,碱石灰增重0
取标准状况下CH4和过量O2的混合气体840ml,点燃,将燃烧后的产物用过量碱石灰(CaO和NaOH)吸收,碱石灰增重0.600g.
计算:(1)碱石灰吸收后所剩气体的体积为_______(标准状况).
(2)原混合气体中CH4跟O2的体积比为________
答案是(1)336ml (2)1:4 卖笑的1年前1
卖笑的1年前1 -
 祸由心生 共回答了27个问题
祸由心生 共回答了27个问题 |采纳率96.3%因为是过量的氧,
所以CH4是完全燃烧产生CO2和H2O.
而碱石灰吸收燃烧产物是CO2和H2O.
一个CH4产生一个CO2和2个H2O
所以是成比例吸收的
就相当于吸收CH4·O4
0.6/(16*5)=7.5*10^-3mol
840/1000=0.84L
0.84/22.4=0.0375mol
所以0.0375mol中有7.5*10^-3mol是CH4
所以7.5*10^-3/0.0375=1:5
所以原混合气体中CH4跟O2的体积比为1:4
CH4+2O2====CO2+2H2O
所以还有两份的O2没有用完.SO剩下40%
840ML*0.4=336ML1年前查看全部
- 气体干燥问题 下列常用的干燥剂中,不能用来干燥氯气的是A.浓硫酸 B.无水氯化钙 C.碱石灰 D.磷酸酐(P2O5)
 skel1年前6
skel1年前6 -
 罗基野山猫 共回答了18个问题
罗基野山猫 共回答了18个问题 |采纳率94.4%生石灰:CaO 遇水生成氢氧化钙 而氯气会和氢氧化钙反应,这个问题也好理解,在教材上高一第四章介绍的!就是用氯气和石灰乳反应来制漂白粉.没有水反应不容易进行,但是有水的话反应就可以进行,因此不能用生石灰、熟石灰或是碱石灰来进行干燥1年前查看全部
- 请问一道关于酸碱盐的化学题:碱石灰是化学实验室常用的干燥剂.其制法如下:在氢氧化钠溶液中加入氧化钙粉末搅拌,在90℃的烘
请问一道关于酸碱盐的化学题:
碱石灰是化学实验室常用的干燥剂.其制法如下:在氢氧化钠溶液中加入氧化钙粉末搅拌,在90℃的烘干箱中干燥30分钟左右,所得的白色固体就是碱石灰.
相关资料:氢氧化钙在250℃以下不分解;氢氧化钠在580℃以下不分解.
某学习小组在老师的指导下欲探究碱石灰的成分.请参与他们的探究.
(1)提出猜想:该碱石灰的成分可能是如下几种情况.
①氢氧化钠、氧化钙; ②氢氧化钠、氢氧化钙;③氢氧化钠、氢氧化钙、水;
④氢氧化钠、氢氧化钙、氧化钙;⑤氢氧化钠、氢氧化钙、氧化钙、水.
以上猜想中,不需要通过实验就能排除的是( ) ,
理由是 ( ).
(2)设计实验:
①称取4.0g碱石灰样品;②在250度时,加热至恒重,测质量减轻了0.6g;
③将剩余物在580度时加热至恒重,测质量又减轻0.7g.
(3)得出结论:该碱石灰的实际成分是( )
(4)应用:有些气体不能用碱石灰干燥,请列举两种:
( ) 、 ( ) qq冰季1年前1
qq冰季1年前1 -
 仁辛人爱 共回答了19个问题
仁辛人爱 共回答了19个问题 |采纳率84.2%答:5,因为水和氧化钙不共存.
250度时减轻重量可以由下面方程式解释
Ca(OH)2Na2O+H2O
Y 0.7g
Y=3.1g
X+Y=5.6g大于4.0克,说明在250度时减少的水不全都是氢氧化钙分解产生的,在碱石灰样品中本身就含有水,所以实际成分是;③氢氧化钠、氢氧化钙、水
酸性气体不可以,比如HCl,二氧化碳,二氧化硫等等1年前查看全部
- 一定量乙醇和氧气在密闭容器中燃烧后的产物为二氧化碳一氧化碳和水…产物分别经过浓硫酸和碱石灰…浓硫酸曾重10.8克碱石灰曾
一定量乙醇和氧气在密闭容器中燃烧后的产物为二氧化碳一氧化碳和水…产物分别经过浓硫酸和碱石灰…浓硫酸曾重10.8克碱石灰曾重13.2克求乙醇和氧气物质的量分别是多少?如乙醇和足量金属钠充分反应则标况下生成气体的体积是多少?
 xiaoxly1年前2
xiaoxly1年前2 -
 青火炫然 共回答了16个问题
青火炫然 共回答了16个问题 |采纳率100%浓硫酸吸收的是水,可知水有0.6mol,碱石灰增重的是吸收了二氧化碳,可知二氧化碳有0.3mol,因为乙醇燃烧后氢全部变成水了,所以由水量可知乙醇原来有0.2mol,那么乙醇中含碳0.4mol,因为生成二氧化碳0.3mol,所以一氧化碳有0.1mol.那么由反应方程式中氧原子守恒可得,反应中消耗的氧气为(0.3*2+0.1+0.6-0.2)/2=0.55(mol)
由于乙醇与足量钠反应生成的氢气物质的量为乙醇的一半,所以氢气为0.1mol,即生成标准状况下氢气2.24L.1年前查看全部
- 请问碱石灰的成分是什么*^_^*谢谢合作…
 www198405211年前4
www198405211年前4 -
 wqerw 共回答了21个问题
wqerw 共回答了21个问题 |采纳率90.5%碱石灰是氢氧化钠和氧化钙的混合物
它可以吸收气体中的酸性气体,比如二氧化碳或者二氧化硫之类的,因为有碱存在吗
此外还能吸收气体中的水,可以作为干燥剂,但是只能干燥碱性气体,因为它和酸性气体反应!1年前查看全部
- 实验室可用如图所示装置干燥(碱石灰是氢氧化钠和生石灰的混合物)、收集气体R,并吸收多余的R,则R可能是( )
 实验室可用如图所示装置干燥(碱石灰是氢氧化钠和生石灰的混合物)、收集气体R,并吸收多余的R,则R可能是( )
实验室可用如图所示装置干燥(碱石灰是氢氧化钠和生石灰的混合物)、收集气体R,并吸收多余的R,则R可能是( )
A.CO2
B.NH3
C.CO
D.SO2 lxorb1年前1
lxorb1年前1 -
 苦难1 共回答了14个问题
苦难1 共回答了14个问题 |采纳率92.9%解题思路:可以根据图中信息进行分析、判断,从而得出正确的结论.碱石灰的主要成分是氧化钙和固体氢氧化钠,不能干燥酸性气体;收集方法适合气体的密度比空气小,尾气处理说明气体极易溶于水,据此即可解答.A、二氧化碳能与碱石灰反应,不能被碱石灰干燥,故A错误;
B、氨气易溶于水,碱石灰可以干燥氨气,且密度比空气小,故B正确;
C、碱石灰能干燥一氧化碳,但是一氧化碳难溶于水,不能通过水吸收,故C错误;
D、二氧化硫能与碱石灰反应,不能被碱石灰干燥,故D错误;
故选B.点评:
本题考点: 根据浓硫酸或烧碱的性质确定所能干燥的气体;常用气体的收集方法.
考点点评: 本题考查实验装置的选择,解答本题时既要考虑物质的水溶性,又要考虑气体是否能和干燥剂发生化学反应,完成此题,可以依据物质的性质进行,题目难度不大.1年前查看全部
- ①碱石灰是实验室常用的干燥剂,它是氧化钙、氢氧化钠的固体混合物. 除了能吸收水蒸气外,碱石灰还能吸收常见的气体是 ___
①碱石灰是实验室常用的干燥剂,它是氧化钙、氢氧化钠的固体混合物. 除了能吸收水蒸气外,碱石灰还能吸收常见的气体是 _______ (选填编号,只有一个答案,多选不得分).
A.氧气 B.一氧化碳 C.二氧化碳 D.氢气
②实验室中利用草酸亚铁晶体(FeC 2 O 4 ·2H 2 O)受热分解得到一定量的 CO,反应的方程式 为:FeC 2 O 4 ·2H 2 O→铁的氧化物+CO+CO 2 +2H 2 O该反应属于 ______ (填写基本反应类型),根据质量守恒定律,可以推知产物中“铁的氧化物”的化学式是 _______
③加热草酸亚铁可选用下列“A、B、C”三套装置中的 ______ (选填编号“A、B、C”).写出下列仪器“a”的名称是 ______ .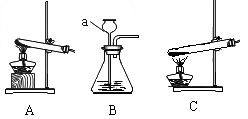
④草酸亚铁晶体的摩尔质量是 _________ (写全单位),若有1.8g 草酸亚铁晶体充分反应可得 到CO气体的物质的量是多少?请写出计算过程:
⑤草酸亚铁晶体受热分解得到的气体通过碱石灰后,用来与氧化铜反应,并检验反应得到的气体产物.整套装置如图:
写出“乙”处 反应的 现象是 ___________ ,反应的 化学方程式 为 _____________ ,该反应中还原剂是. 甲、丙两处所盛放的试液分别是 ___________ 、 _________ ,其中“甲”处所盛放该试液的作用是 ___________________ .  代代12号1年前1
代代12号1年前1 -
 精彩哥 共回答了18个问题
精彩哥 共回答了18个问题 |采纳率88.9%①C ②分解反应;FeO ③A;长颈漏斗 ④180克/摩尔;设1.8g 草酸亚铁晶体充分反应可得到CO气体的质量为x: FeC 2 O 4 ·2H 2 O FeO+CO↑+CO 2 ↑+2H 2 O 180...1年前查看全部
- 哪些物质可以用碱石灰干燥?哪些又可以用浓硫酸干燥?同时可以用这两种的物质干燥的又有哪些?
 emusp1年前3
emusp1年前3 -
 laputa19 共回答了10个问题
laputa19 共回答了10个问题 |采纳率90%浓H2SO4:具有强烈的吸水性,常用来除去不与H2SO4反应的气体中的水分.例如常作为H2、O2、CO、SO2、N2、HCl、CH4、CO2、Cl2等气体的干燥剂.
固体氢氧化钠和碱石灰:吸水快、效率高、价格便宜,是极佳的干燥剂,但不能用以干燥酸性物质.常用来干燥氢气、氧气、氨和甲烷等气体.
同时可以干燥的是H2、O2、CO、N2、CH4等1年前查看全部
- Ca(OH)2能作干燥剂吗?它不是碱石灰的组成之一吗?为什么不能作干燥剂?
 xaddhhj1年前1
xaddhhj1年前1 -
 3872504 共回答了25个问题
3872504 共回答了25个问题 |采纳率100%一般不用Ca(OH)2做干燥剂,因为它的吸水性不强,常常用碱石灰(NaOH和CaO的混合物)但这类碱性物质不能用于二氧化碳等要与他们反应的气体干燥.而这些气体却常常用浓硫酸来干燥.1年前查看全部
- 氨气中含有水蒸气用什么来除去?氨气中的水蒸气用什么来除去?既然不能用氯化钙也不能用酸性试剂,那用碱性的行吗?例如碱石灰
 北海道的狼1年前4
北海道的狼1年前4 -
 老勇618 共回答了18个问题
老勇618 共回答了18个问题 |采纳率100%碱石灰,应用碱性干燥剂1年前查看全部
- CO2.SO2.H20.的检验顺序.顺序怎样?用品红.澄清石灰水和碱石灰.
 郭剑20021年前3
郭剑20021年前3 -
 eedolls 共回答了28个问题
eedolls 共回答了28个问题 |采纳率78.6%先来水的,通入含有碱石灰的干燥管,如果干燥管中的碱石灰重量增加就说明含有水,再检验SO2,因为二氧化硫和二氧化碳都能使澄清石灰水变浑浊,所以应先检验SO2,通入品红溶液,品红褪色就能证明..然后一定要出去SO2,用NaOH.最后检验CO2,通入澄清石灰水,这个简单有沉淀就可以了1年前查看全部
- A盐和碱石灰反应,微热时放出一种气体B,再经强热又放 出一种气体C.在同温同压下,气体B与C的密度相近,余 下的残渣中加
A盐和碱石灰反应,微热时放出一种气体B,再经强热又放 出一种气体C.在同温同压下,气体B与C的密度相近,余 下的残渣中加入硝酸又有一种气体D放出,气体D通入一 种淡黄色的固体中可得到气体E.请确定各物质的分子式.和有关化学反应方程式.
 ykbe1年前1
ykbe1年前1 -
 jayy141548 共回答了21个问题
jayy141548 共回答了21个问题 |采纳率90.5%A盐:碳酸铵((NH4)2CO3)B气体:NH3,C气体:H2O
(NH4)2CO3+2NaOH=微热=2NH3↑+2H2O+Na2CO3
强热的过程是水蒸发的过程
D气体为CO2
Na2CO3+2HNO3=2NaNO3+H2O+CO2↑
E气体为氧气:
2CO2+2K2O2=2K2CO3+O2↑1年前查看全部
- 碱石灰如何吸收CL2
 helloboyboy1年前1
helloboyboy1年前1 -
 zhangzuola880819 共回答了22个问题
zhangzuola880819 共回答了22个问题 |采纳率95.5%氯气首先在水中生成次氯酸和盐酸,然后这两种物质再和碱石灰作用1年前查看全部
- 计算(1)碱石灰吸收后所剩气体的体积(2)原混合气体中CH4跟O2的体积比
计算(1)碱石灰吸收后所剩气体的体积(2)原混合气体中CH4跟O2的体积比
取标准状况下CH4和过量O2的混合气体896mL,点燃,将燃烧后的气体用过量碱石灰吸收,碱石灰增重0.8g.若将点燃后的气体用过量浓硫酸吸收,则浓硫酸增重0.36g. liuyuanhua1年前1
liuyuanhua1年前1 -
 冒_泡泡 共回答了16个问题
冒_泡泡 共回答了16个问题 |采纳率100%(1)
反应生成
n(H20)=0.36/18=0.02mol
n(CO2)=(0.8-0.36)/44=0.01mol
由反应得
CH4 + 2O2 ---> CO2 + 2H2O
0.01mol 0.02mol 0.01mol
V剩气=0.896-0.01*22.4-0.02*22.4+0.01*22.4=0.448L 即448mL
(2)
原混合气
V(CH4)=224mL
故V(CH4):V(O2)=1:31年前查看全部
- 实验室常用的干燥剂碱石灰是CaO和NaOH的固体混合物,极易与空气中的水蒸气和二氧化碳反应而变质.某同学对一瓶久置的碱石
实验室常用的干燥剂碱石灰是CaO和NaOH的固体混合物,极易与空气中的水蒸气和二氧化碳反应而变质.某同学对一瓶久置的碱石灰作了如下探究:
【提出猜想】猜想一:没有变质,只有CaO和NaOH两种固体; 猜想二:已完全变质,碱石灰全部变成了CaCO3和Na2CO3.
【实验探究】实验过程与现象如下图所示:
【做出判断】(1)若把Ca(OH)2、CaCO3和Na2CO3加入水中不会放出热量,侧由操作b中的现象可判断猜想二______(填“成立”或“不成立”).
(2)操作f中发生反应的化学方程式为______;
由操作e、f中的现象可判断滤液里含有______(填化学式),由此判断猜想一______(填“成立”或“不成立”).
(3)综合(1)、(2)中的结论,判断该碱石灰的变质情况为______.
【拓展应用】(4)由上述实验说明,在实验室存放碱石灰应______保存. 狗JB1年前1
狗JB1年前1 -
 红米411 共回答了15个问题
红米411 共回答了15个问题 |采纳率100%解题思路:(1)根据物质溶于水的温度变化情况进行分析,
(2)根据推导确定混合物的成分进行分析,
(3)根据实验现象进行分析,
(4)根据上面的实验结论进行分析.(1)混合物加水后试管壁发热,但是Ca(OH)2、CaCO3和Na2CO3加入水中不会放出热量,所以C猜想二不成立.
(2)浑浊液中的滤渣中滴加盐酸,产生气泡,说明混合物中有碳酸钙,滤液中滴加盐酸有气泡,加澄清石灰水有沉淀生成,说明滤液中有碳酸钠,但是如果只有氧化钙和氢氧化钠就不会生成碳酸钙沉淀和碳酸钠.
(3)从(2)中的推导可知,混合物中既有CaO和NaOH,也有CaCO3和Na2CO3.
(4)通过实验可知,碱石灰在空气中极易变质.
故答案为:
(1)不成立,
(2)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH 碳酸钠 不成立
(3)部分变质
(4)密封、防潮点评:
本题考点: 物质的鉴别、推断;空气中常见酸碱盐的质量或性质变化及贮存法;酸、碱、盐的鉴别;书写化学方程式、文字表达式、电离方程式.
考点点评: 在解此类题时,先根据题中的现象推出确定的物质,对于不确定的物质要设计实验进行验证.1年前查看全部
- 高中化学除杂有关CO2实验室中除去生成气体中的CO2我只知道有氢氧化钠、碱石灰、石灰水还有什么液体和固体可以除主要是固体
高中化学除杂有关CO2
实验室中除去生成气体中的CO2
我只知道有氢氧化钠、碱石灰、石灰水
还有什么液体和固体可以除
主要是固体、、高中阶段哦,稍微超一点只要能理解也行
为啥要问固体除杂、、给个例子吧
将一种烃燃烧,生成的有水二氧化碳
现在要检测它俩的质量,将生成气体先通入广口瓶(长进短出),然后过U形管
因为要测质量所以要先除水、、后除二氧化碳
广口瓶放浓硫酸无疑问,U形管内放什么去除二氧化碳? orthodox1年前2
orthodox1年前2 -
 derrick8511 共回答了21个问题
derrick8511 共回答了21个问题 |采纳率76.2%首先你要明白co2是酸性氧化物
而酸性氧化物之间是有一定的通性的通性1.与水反应生成相应的酸(除了二氧化硅SiO2,它不与水反应)2.与碱反应生成盐和水3.与碱性氧化物反应故Co2能与任何碱性氧化物反应1年前查看全部
- 碱石灰中的NaOH有什么作用?为何不全用CaO
 qjjx1年前1
qjjx1年前1 -
 长弓生日 共回答了18个问题
长弓生日 共回答了18个问题 |采纳率100%氢氧化钠起到干燥作用
碱与水接触后将与二氧化碳反应,CaO与二氧化碳反应生成的碳酸钙不溶于水,将阻碍水分的吸收1年前查看全部
- 烃气体的燃烧燃烧产物中,水是用浓硫酸来鉴别?二氧化碳使用碱石灰来鉴别吗?
 心南南1年前1
心南南1年前1 -
 夜的蓝天 共回答了15个问题
夜的蓝天 共回答了15个问题 |采纳率93.3%水应该用无水硫酸铜鉴别
浓硫酸是用来吸收水分并称重的
而CO2是用澄清石灰水鉴别
用碱石灰吸收CO2并称重~1年前查看全部
- 在通常情况下能够共存,并都能用浓硫酸干燥,也能用碱石灰干燥的气体是
在通常情况下能够共存,并都能用浓硫酸干燥,也能用碱石灰干燥的气体是
a.NH3 N2 H2
b.SO2 H2S O2
c.N2 H2 CO
d.HCl Cl2 CO2
为什么啊 虫虫飞飞2000条1年前6
虫虫飞飞2000条1年前6 -
 gracie_wang 共回答了16个问题
gracie_wang 共回答了16个问题 |采纳率87.5%c 因为不反应
浓硫酸可干燥酸性和中性气体,而碱石灰可干燥碱性和中性气体
要二者都可行,只可以是中性气体
a 氨气是碱性
b 二氧化硫是酸性,硫化氢是酸性
d 全是酸性1年前查看全部
- 一体积某烃燃烧后生成的二氧化碳比水蒸气少一体积,0.1mol该烃燃烧后生成产物全部被碱石灰吸收.碱石灰增重32.8g,求
一体积某烃燃烧后生成的二氧化碳比水蒸气少一体积,0.1mol该烃燃烧后生成产物全部被碱石灰吸收.碱石灰增重32.8g,求其分子式= =
 冷落自己的举动1年前1
冷落自己的举动1年前1 -
 阳光满巷头 共回答了25个问题
阳光满巷头 共回答了25个问题 |采纳率92%是C5H12.1年前查看全部
大家在问
- 1小华和小明体重的比是5:4,小明和小红体重比是3:2,小华和小红的体重比是______.
- 2一个长方体,长宽高的和是230厘米,己知长和宽的比为2:3,宽和高的比为3:4,那么长方体的长是多少,
- 3in let's the first the see penguins zoo 连词成句
- 4在这个宇宙中到底有没有外星人?
- 5物体从静止开始作匀加速直线运动,第10s末的速度为2m/s,则下列说法中正确的是 A.前10s内的位移为10m
- 6可否用臭氧代替氧气用于生化池曝气?
- 7如果你是一位导演,准备拍摄一组以“思念祖国,思念家乡”为内容的镜头
- 8有pH值低于0或者高于14的物质吗?
- 9往返于甲、乙两地的客车,中途有停靠五个站(包括甲、乙两站),如果站与站之间的路程及站于甲、乙两地之间的路程都不相等.假如
- 10要使10分之X是假分数,15分之X是真分数,X可能是( )
- 11如果二十九分之五 ÷a>二十九分之五 *a,那么a是( )(填真分数、假分数.)
- 12公园门票每张售价25元,节假日优惠,买4张送1张.5个人节日去游公园,平均每人要花多少元?
- 13已知点O是边长为a等边△ABC内一点,过O作OD⊥AB,OE⊥BC,OF⊥AC,证明AD+BE+CF=3/2a
- 14我会努力的用英语怎么说?同题
- 15英语翻译请我英文好的帮忙翻译下!人的一生很短暂,或许只是匆匆的几十年,我很庆幸我的生命中有你的出现,想要一辈子守护你!遇
