阳极泥的产生阳极泥是因为电解时周围空了,所以还原性较弱的一些杂质因为没法附着而掉落吗?那如果是电解粗铜,杂质ni,ag,
 yechm64642022-10-04 11:39:541条回答
yechm64642022-10-04 11:39:541条回答阳极泥是因为电解时周围空了,所以还原性较弱的一些杂质因为没法附着而掉落吗?那如果是电解粗铜,杂质ni,ag,au,杂质ni把cu,ag,au都给包住了,阳极泥会有cu吗?

已提交,审核后显示!提交回复
共1条回复
 鱼儿- 共回答了20个问题
鱼儿- 共回答了20个问题 |采纳率95%- 1.是的.
2.我认为会有.但是一般情况下杂质好像没有猛到能把原始金属抱起来... - 1年前
相关推荐
- 关于阳极泥的问题?我知道比电极金属不活泼的贵重金属会会作为阳极泥沉淀下来,那比电极金属活泼但不参与反应的金属怎么办?
 快乐难找1年前1
快乐难找1年前1 -
 米特兰的晨星 共回答了17个问题
米特兰的晨星 共回答了17个问题 |采纳率76.5%比金属活泼但不参与反应的金属?这类在教学中一般都不考虑的,而且没必要探讨.要真想追究,它们也在阳极泥里.比如精炼粗铜,那些活泼的铝、铁等当然会反应,失去电子在电镀液中以离子的形式存在.比铜活泼但不反应的就和比铜不活泼的金属一起成为阳极泥了.有不周到的地方,请多原谅!1年前查看全部
- 用硫酸做电解质溶液的粗铜精炼的电解池,阳极泥成分是金属Ag还是硫酸盐Ag2SO4
 zy198602021年前2
zy198602021年前2 -
 4802647 共回答了20个问题
4802647 共回答了20个问题 |采纳率85%按理说,电性比铜正的银,在阳极泥中大部分是以金属Ag的极细粉末存在,(只有极少量银能被二价的铜离子所氧化进入溶液).1年前查看全部
- 高二化学电解池精炼铜中阳极上的粗铜上的物质为什么除铜以外的物质其他的都会变成沉淀(阳极泥)?
高二化学电解池精炼铜中阳极上的粗铜上的物质为什么除铜以外的物质其他的都会变成沉淀(阳极泥)?
还有就是为什么铜的纯度达不到100%按理说是可以的啊? 惯性消失1年前1
惯性消失1年前1 -
 小红鱼 共回答了20个问题
小红鱼 共回答了20个问题 |采纳率95%粗铜上有比铜活泼的铁、镍等金属,也有不活泼的银、铂等金属,阳极反应按金属的活泼性顺序来进行,铁镍先转化为离子,铜再转化,因为电极上主要是铜,所以只要有铜,银铂就不能失去电子,只能以单质形式沉淀到溶液中.1年前查看全部
- 化学研究性学习小组在实验室条件下以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含
化学研究性学习小组在实验室条件下以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定.已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应).
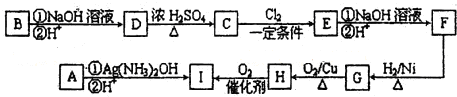
步骤一:电解精制:电解时,粗铜应与电源的______极相连.阴极上的电极反应式为______.
步骤二:电解完成后,该小组同学按如图流程对电解液进行处理:稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该反应的离子方程式:______. 树叶1001年前1
树叶1001年前1 -
 铭豆小猪 共回答了16个问题
铭豆小猪 共回答了16个问题 |采纳率87.5%解题思路:电解精炼铜时,精铜做阴极,粗铜作阳极,阴极上是铜离子得电子;金属银可以和硝酸反应得到硝酸银以及水和一氧化氮,据此回答.在电解精炼铜时,阳极反应是金属锌、铁、镍等先失电子,阴极上是铜离子得电子产生铜,Cu2++2e=Cu,精铜做阴极,粗铜作阳极,金属银可以和稀硝酸反应生成硝酸银、一氧化氮和水,即3Ag+4H++NO3-=3Ag++NO↑+2H2O,故答案为:正;Cu2++2e=Cu;3Ag+4H++NO3-=3Ag++NO↑+2H2O.
点评:
本题考点: 电解原理.
考点点评: 本题涉及有关电解精炼铜、金属银的化学性质等综合知识,难度不大.1年前查看全部
- 电解后Fe、Zn、Ag等杂质会沉积在电解槽底部形成阳极泥
电解后Fe、Zn、Ag等杂质会沉积在电解槽底部形成阳极泥
为什么错,错在哪里 基本爱1年前1
基本爱1年前1 -
 5528222 共回答了20个问题
5528222 共回答了20个问题 |采纳率95%阳极泥的主要成分是Ag、Au等贵金属,Fe、Zn不会再阳极泥中.1年前查看全部
- 下列对于电化学说法正确的是( ) A.电解精练铜时,阳极泥中常含有金属金、银、锌等 B.为保护浸入海水中的钢闸门,可在
下列对于电化学说法正确的是( ) A.电解精练铜时,阳极泥中常含有金属金、银、锌等 B.为保护浸入海水中的钢闸门,可在闸门表面镶上铜锭 C.充电电池放电时,化学能转变为电能 D.铅蓄电池放电时的负极和充电时的阴极均发生氧化反应  小民啊哥1年前1
小民啊哥1年前1 -
 wyl0828 共回答了19个问题
wyl0828 共回答了19个问题 |采纳率89.5%A.电解精练铜时,阳极泥中常含有金属金、银等,Zn比Cu活泼,则阳极泥中不含有Zn,故A错误;
B.Cu的活泼性比Fe的弱,Cu作正极,不能保护Fe,所以为保护浸入海水中的钢闸门,一般在闸门表面镶上锌锭,故B错误;
C.充电电池,放电时为原电池,则化学能转变为电能,故C正确;
D.原电池中负极发生氧化反应,电解池中阴极发生还原反应,故D错误;
故选C.1年前查看全部
- 在用电解池精炼Cu的时候,为什么粗Cu中的Ag会形成阳极泥?Ag又不是惰性电极?
在用电解池精炼Cu的时候,为什么粗Cu中的Ag会形成阳极泥?Ag又不是惰性电极?
而且它阳离子的放电顺序也在铜离子之前啊.为什么不形成Ag+? 如风飘逸9191年前1
如风飘逸9191年前1 -
 swl860701 共回答了10个问题
swl860701 共回答了10个问题 |采纳率90%Ag是极少量的,不是一大块电极,是混杂在粗铜中的,很少,所以会沉积在阳极形成阳极泥.
而且Ag是在Cu之后放电的.1年前查看全部
- 以硫酸铜溶液作电解液,对含有杂质铁,锌,银的粗铜进行电解精炼.杂质银以什么形式变成阳极泥?为什么?
 idlenow1年前1
idlenow1年前1 -
 zzzzzppppp99 共回答了19个问题
zzzzzppppp99 共回答了19个问题 |采纳率89.5%阳极:锌——锌离子
铁——铁离子
铜——铜离子
银——活泼性在铜后面,不反应,变成单质沉淀1年前查看全部
- 电解精炼铜时,阳极泥中含有Zn,Fe,Ag,Au等金属哪里错了?
 沉默的飞扬1年前1
沉默的飞扬1年前1 -
 yangwenxuan1983 共回答了16个问题
yangwenxuan1983 共回答了16个问题 |采纳率87.5%Zn,Fe比铜活泼,在阳极比Cu优先失电子进入溶液,阳极泥中应该是比Cu不活泼的金属及杂质1年前查看全部
- 【急】为什么粗铜中的金和银以阳极泥的形式出现
【急】为什么粗铜中的金和银以阳极泥的形式出现
①在电解精炼铜时 粗铜中的金和银是以单质的形式作为阳极泥沉淀在电解池的池底 我知道这个结论 为什么不是通电使金和银氧化失电子形成金属阳离子再被镀到精铜上
②粗铜中有铁 电解时铁以例子的形式存在 可否理解为当电解质溶液中的铜离子全部被镀到阴极后 就可以再把铁离子镀到阴极上?麻烦作答 芥子微尘1年前2
芥子微尘1年前2 -
 yy的痛 共回答了22个问题
yy的痛 共回答了22个问题 |采纳率95.5%1)因为金、银比铜更难失电子,因此总是铜先失电子,以离子形式脱落,进入溶液.阳极上的铜在溶解的时候,杂于其中的金和银就脱落下来.如果阳极是纯银的话,电压足够的情况下,银也会以离子形式进入溶液,但此时铜溶下来了,银根本就不能在阳极上了,掉下来了.
2)可以这么理解.铜比铁更易得电子,所以铜先镀到阴极,当铜镀完后,继续通电,铁会镀上去.1年前查看全部
- 阳极泥 失电子为什么比铜氧化性强的不失电子,而当阳极有锌等杂质时,铜仍能失电子
 我的侄子好可爱1年前2
我的侄子好可爱1年前2 -
 残灯明灭 共回答了18个问题
残灯明灭 共回答了18个问题 |采纳率88.9%当阳极中存在比铜活泼性强的金属时,主要失电子的是杂质,但铜也要失电子,只不过是少数而已.等到杂质金属的含量低到一定程度时,就主要是铜失电子了.你可以类比这样一个问题来看,在往镀件上镀锌的时候,用的电解质溶液是氯化锌,氯化锌的溶液因水解显酸性,因此溶液中存在一定浓度的氢离子,氢离子的氧化性比锌粒子的强,但仍能实现镀锌,这是因为用的氯化锌溶液浓度高,主要是锌离子放电,氢离子也会放电生成氢气,只不过很少罢了.金属原子,只要受到电压,就有失去电子的趋势,但这种趋势的强弱不同,也就是我们说的还原性强弱不同.还原性强的失电子的原子数就多(如杂质锌等),还原性弱的失电子的原子数就少(如铜)1年前查看全部
- 粗铜中的金、银等以化合物的形式存在于阳极泥中 对么?
 lanshanyefei1年前1
lanshanyefei1年前1 -
 灵境 共回答了17个问题
灵境 共回答了17个问题 |采纳率94.1%不对
粗铜中的金、银等以(单质)的形式存在于阳极泥中1年前查看全部
- 粗铜的精炼中,银为什么不会变成金属离子而成为了阳极泥呢?亚铁离子为什么不能附着在精铜上呢?
粗铜的精炼中,银为什么不会变成金属离子而成为了阳极泥呢?亚铁离子为什么不能附着在精铜上呢?
1.如何解释金属活动顺序表中,金属的活泼性强弱?
2.为什么电解粗Ni是Ni以后的物质形成阳极泥,电解粗铜是铜以后的物质形成阳极泥?是因为它们的含量多吗? 安静world1年前4
安静world1年前4 -
 兆伟 共回答了20个问题
兆伟 共回答了20个问题 |采纳率75%首先铜的金属活动性比银强,阳极发生氧化反应,铜比银先失去电子,形成铜离子进入电解质溶液.而电解质溶液中阳离子是是Cu2+,故银单质不能失电子形成银离子.在阴极,发生还原反应,失电子,铜离子的氧化性比亚铁离子的氧化性强,故铜离子的电子,形成精铜.1年前查看全部
- 阳极泥中有没有不活泼金属电解硫酸铜时,银是不是以阳极泥的形式陈在溶液里,还是会像铜一样附着在精铜上?
 neozy1年前1
neozy1年前1 -
 晕你027 共回答了22个问题
晕你027 共回答了22个问题 |采纳率90.9%好像不是电解硫酸铜溶液,应该是电解精炼铜吧?
由于粗铜中金、银等不活泼金属放电顺序排在铜后面,所以它们不能在阳极发生氧化反应变成离子进入溶液,因此会随阳极铜的溶解而沉积在溶液底部,形成阳极泥.
由于它们没有形成离子,所以不会到达阴极,不会像铜一样附着在精铜上.1年前查看全部
- 电解锰中的阳极泥有用吗
 jimmyhua20041年前1
jimmyhua20041年前1 -
 夏日水仙 共回答了15个问题
夏日水仙 共回答了15个问题 |采纳率86.7%Mn离子被还原生成了Mn单质
而Mn单质不溶于电解液
在阳极附近生成的Mn单质就是沉淀
即阳极泥
Mn可以回收再利用的.
一般也用这种方法收集金 银等比较贵重的金属~1年前查看全部
- 什么是黑铜阳极泥?
 tesco2k1年前1
tesco2k1年前1 -
 woshiwenmang 共回答了14个问题
woshiwenmang 共回答了14个问题 |采纳率85.7%在精炼铜的时候,电解池里阳极发生氧化反应,是活泼金属(锌、铝等)先反应,然后等那些粗铜里面的活泼杂质金属反应完了以后,在开始反应铜,形成铜离子,铜离子再到阴极上形成精铜.
等到铜全部反应完的时候,精炼铜结束,阳极剩下的没有反应的东西下沉,形成阳极泥,而那些东西就是金 银等东西.1年前查看全部
- 电解精炼铜(杂质Zn,Au,Pt,Ag)时的阳极泥是啥?
 jeavincf1年前2
jeavincf1年前2 -
 vincentandlaura 共回答了19个问题
vincentandlaura 共回答了19个问题 |采纳率89.5%就是在电极上无法失去电子的金属,金,铂,银等.1年前查看全部
- 金属镍有广泛的用途,粗镍中含有Fe Zn Cu Pt等杂质电解后,电解槽底部的阳极泥只有Cu Pt 为什么
 用馨凌听1年前1
用馨凌听1年前1 -
 红菠菠 共回答了26个问题
红菠菠 共回答了26个问题 |采纳率80.8%因为氧化性:Fe2+< Ni2+ ,Fe>Ni> Cu> Pt,发生氧化反应,即 Zn→ Zn2+ +2e-
Fe→ Fe2+ +2e-
Ni→ Ni2+ +2e-
电解过程中,因为粗镍中含有少量Fe,Zn,Cu,Pt等杂质,因而当阳极溶解Fe,Zn,Ni而阴极析出Ni时,得失电子总数相等,则阳极减少的质量与阴极增加的质量不可能相等;电解后,溶液中存在的金属阳离子除Fe2+和Zn2+外,还可能存在Ni2+ ;因为Fe,Zn.比Ni活泼,所以电解槽底部的阳极泥中不可能存在Fe,Zn,只存在Cu和Pt .1年前查看全部
- 关于电解精炼铜粗铜在阳极 反应 而 其中的金银能金属灰直接以游离态进入阳极泥 是不是 由于铜优先反应使银可以不反应
 杨蔚林1年前2
杨蔚林1年前2 -
 三儿我陪你走 共回答了14个问题
三儿我陪你走 共回答了14个问题 |采纳率100%对的,Cu的金属活泼性在Ag和Au之前,所以Cu先失去电子生成Cu2+进入溶液中,实际情况是由于Cu含量》Ag和Au,所以Ag和Au根本不会进入溶液中.1年前查看全部
- 另一化学研究性学习小组在实验室条件下用以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回
另一化学研究性学习小组在实验室条件下用以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定.已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应).
步骤一:电解精制:电解时,粗铜应与电源的______极相连.阴极上的电极反应式为______.
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理: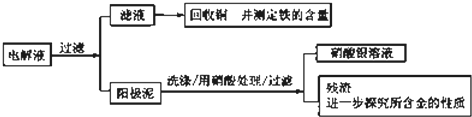
(1)阳极泥的综合利用:稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该步反应的离子方程式:______,残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的信息:
请根据以上信息简要解释溶解阳极泥不用王水的原因______.序号 反应 平衡常数 1 Au+6HNO3⇌Au(NO3)3+3NO2↑+3H20 <<1 2 Au3++4Cl-⇌AuCl4 _ >>1
(2)滤液含量的测定:以下是该小组探究滤液的一个实验流程.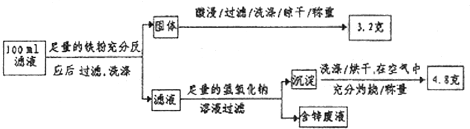
则100mL滤液中Cu2+的浓度为______mol•L-1,Fe2+的浓度为______mol•L-1. 爱笑的小桃夭夭1年前1
爱笑的小桃夭夭1年前1 -
 xhj_he 共回答了21个问题
xhj_he 共回答了21个问题 |采纳率90.5%解题思路:步骤一:电解精炼铜时,精铜做阴极,粗铜作阳极,阴极上是铜离子得电子;
步骤二:(1)金属银可以和硝酸反应得到硝酸银以及水和一氧化氮;金离子可以和氯离子之间发生反应,形成稳定的AuCl4-离子,可以根据化学平衡移动原理来解释;
(2)根据化学反应原理结合原子守恒的思想来计算回答.步骤一:在电解精炼铜时,阳极反应是金属锌、铁、镍等先失电子,阴极上是铜离子得电子产生铜,精铜做阴极,粗铜作阳极,
故答案为:正;Cu2++2e=Cu;
步骤二:(1)金属银可以和稀硝酸反应生成硝酸银、一氧化氮和水,即3Ag+4H++NO3-=3Ag++NO↑+2H2O;根据表中的信息,Au+6HNO3(浓)=Au(NO3)3+3NO2↑+3H2O,并且Au3++4Cl-=AuCl4-,在王水中,含有浓硝酸和浓盐酸,浓盐酸含有大量氯离子,Au3+离子与氯离子形成稳定的AuCl4-离子,使反应2平衡向右移动,则金溶于王水中,故答案为:3Ag+4H++NO3-=3Ag++NO↑+2H2O;浓盐酸含有大量氯离子,Au3+离子与氯离子形成稳定的AuCl4-离子,使反应2平衡向右移动,则金溶于王水中;
(2)100mL的滤液中含有亚铁离子、铜离子、锌离子,当加入足量的金属Fe以后,会将金属铜全部置换出来,所以生成的3.2g金属是Cu,所以铜离子的浓度c=[n/V]=[0.05mol/0.1L]=0.5 mol/L,亚铁离子和氢氧化钠反应生成氢氧化亚铁,在空气中更易被氧化为氢氧化铁,受热分解生成的氧化铁的质量是4.8g,根据原子守恒,亚铁离子的物质的量是:[4.8g/160g/mol]×2=0.06mol,所以亚铁离子的浓度c=[n/V]=[0.06mol/0.1L]=0.6mol/L,故答案为:0.5;0.6.点评:
本题考点: 物质分离和提纯的方法和基本操作综合应用;电解原理.
考点点评: 本题考查有关电解精炼铜、化学平衡移动原理以及物质的含量的测定的综合知识,为高频考点,注意把握实验方法设计与装置的综合分析,题目难度中等.1年前查看全部
大家在问
- 1如图,AD⊥BC于D,EG⊥BC于G,∠E=∠3,试说明:AD平分∠BAC.
- 2天净沙.秋思能显示全篇主旨的一个词语是_____
- 3()gifts do you want填什么(只有how much和how many)
- 4一次数学测验,小强考了95分,比小丽分数的八分之九还多5分.小丽的分数是多少?
- 5将A,B,C,D,E,F六个字母排成一排,且A,B均在C的同侧,则不同的排法共有多少种?(用数字作
- 6在图所示的电路中,电源电压保持不变.闭合电键S,滑动变阻器的滑片在某一位置时,电压表示数为12伏,电流表示数为1.2安.
- 7在直角三角形ABC中,角C=90°,AC=3,BC=4,以点C为圆心,CA为半径的圆与AB、BC分别交
- 8“龟兔赛路”是同学们熟悉的寓言故事,下图表示路程S与时间t之间的关系,那么可以知道:
- 9甲、乙两车同时从A地开往B地,当甲车行了全程的[1/3]时,乙车行了60千米,两车的速度保持不变,当甲车到达终点时,乙车
- 10读拼音写句子。Xiào hěn zhòng yào,bú guò,zhǐ huì xiào shì yuǎn yuǎn
- 11谁能出关于五年级的找规律和解决问题的策略的奥数题并附上答案?
- 12Because she's very beautiful,so I like her.
- 13为减少CO2的排放,另一种途径是将CO2转化成有机物实现碳循环,如CO2与H2在催化剂和加热的条件下反应生成
- 14看图拼字一个外星人把能量通过手传给地球人一条鲸鱼一只大手在上面拉住一只小手一匹马猜五个字第四个是伯求答案
- 15Winter __________.Zoom and Zip don’t skate.They sleep.A.comi
