碳酸亚铁与稀盐酸反应如题,并求理由求理由?
 xuan14302022-10-04 11:39:541条回答
xuan14302022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 sheila_sfi 共回答了23个问题
sheila_sfi 共回答了23个问题 |采纳率87%- 能
碳酸亚铁与稀盐酸能反应
这两者相互交换成分后为:碳酸和氯化亚铁,碳酸不稳定易分解为H2O和CO2,这样生成物中有气体和水的生成了,所以该反应能发生
FeCO3+2HCl=FeCl2+H2O+CO2(气体符号)
原创性回答,请尽早点击下面的“选为满意回答”按钮
如果还没解决您的疑难,
[知识黑洞]和[夕阳无限好]团队的老队员“qaz2231a”祝您学习进步
如还有其他需要帮助的问题,可向我们两个团队求助,我们尽力为您解答 - 1年前
相关推荐
- 碳酸亚铁.碳酸铁高温分解的化学方程式
 星心芯1年前3
星心芯1年前3 -
 tlsa 共回答了21个问题
tlsa 共回答了21个问题 |采纳率81%如果是隔绝空气加热
FeCO3=FeO+CO2
Fe2(CO3)3=Fe2O3+3CO21年前查看全部
- 怎么由碳酸亚铁制得纯铁?
 华江路千千1年前2
华江路千千1年前2 -
 1东9洋8浪0人 共回答了12个问题
1东9洋8浪0人 共回答了12个问题 |采纳率91.7%简单方法 先加酸溶解
FeCO3 + 2HCl = FeCl2 + H2O + CO2
再用金属镁(或锌)还原即可
FeCl2 + Mg = MgCl2 + Fe FeCl2 + Zn = ZnCl2 + Fe
楼上的方法怎么可能 且不说无法变成Fe3O4 就算制得了 哪里去找一氧化碳高温还原呢
当然镁也不便宜 不过易得 建议你去买还原铁粉 便宜 方便 纯度高1年前查看全部
- 100g碳酸亚铁与盐酸充分反应,反应的化学方程式为FeCO3+2HCl=FeCl2↑+H2O,得到标准状况下的二氧化碳1
100g碳酸亚铁与盐酸充分反应,反应的化学方程式为FeCO3+2HCl=FeCl2↑+H2O,得到标准状况下的二氧化碳11.2L
帮帮我吧!
呵呵 应该 FeCO3+2HCl=FeCl2+CO2↑+H2O == 后面还有题目 求该菱铁矿粉中碳酸亚铁的质量分数 假牙0011年前1
假牙0011年前1 -
 float2047 共回答了12个问题
float2047 共回答了12个问题 |采纳率75%你方程式写错了
FeCO3+2HCl=FeCl2+CO2↑+H2O1年前查看全部
- 碳酸亚铁沉淀颜色
 hahases881年前3
hahases881年前3 -
 溽热该奉111 共回答了22个问题
溽热该奉111 共回答了22个问题 |采纳率81.8%干燥时在空气中为白色,在湿润空气中为茶色
如果说是沉淀的话那是在水中了,碳酸亚铁在水中会水解,生成氢氧化亚铁,FeCO3+H2O═Fe(OH)2+CO2
Fe(OH)2是白色的沉淀,在空气中会被氧化,先变灰绿色,再变红棕色,生成Fe(OH)3 .
不存在碳酸亚铁沉淀的问题1年前查看全部
- 碳酸氢铵与硫酸亚铁为什么会生成碳酸亚铁,不是氢氧化亚铁么?
 肚肚鸟1年前2
肚肚鸟1年前2 -
 飘向火的雪 共回答了23个问题
飘向火的雪 共回答了23个问题 |采纳率91.3%楼上不要误导啦!硫酸亚铁与碳酸氢铵最终生成物是碳酸亚铁、硫酸铵、二氧化碳气体和水啦!
怎么会有氢氧化铁呢.
硫酸亚铁与碳酸氢铵的反应,反应的方程式是FeSO4+2NH4HCO3=FeCO3 (沉淀)+CO2(气体)+(NH)2SO4+H2O
关于硫酸亚铁与碳酸氢铵溶液反应生成FeCO3的同时有CO2生成的原因是:
首先,碳酸氢根是一个二元酸根的氢酸根,它既可以进行电离反应:电离出氢离子和碳酸根离子;又可以进行水解反应:水解出碳酸和氢氧根.
其次,正二价的铁与碳酸根反应会有沉淀产生.这样就促进了碳酸氢根的电离.
第三,由于碳酸氢根电离平衡向正方向进行,溶液里的氢离子的浓度就会增大.而浓度增大的氢离子,与溶液中的氢氧根离子结合生成水.这样一来就促进了碳酸氢根的水解.
第四,由于碳酸氢根的水解平衡向正反向进行,溶液中的碳酸浓度增大,回过来促进了正二价的铁离子与碳酸根离子结合生成沉淀.
就这样子形成一个循环.另一方面,当溶液中的碳酸浓度增大到一定程度时,即有CO2气体逸出.1年前查看全部
- 谁告诉我硫酸亚铁 、 碳酸锌 、 硫化铝、氯酸钾、硫酸铁、碳酸亚铁、的化学式啊
 臭臭妈1年前6
臭臭妈1年前6 -
 谁说我认识陈凯歌 共回答了28个问题
谁说我认识陈凯歌 共回答了28个问题 |采纳率78.6%硫酸亚铁:FeSO4
碳酸锌:ZnCO3
硫化铝:Al2S3
氯酸钾:KClO3
硫酸铁:Fe2(SO4)3
碳酸亚铁:FeCO31年前查看全部
- (2014•江都市二模)有20g铁、氧化亚铁、碳酸亚铁的混合物,其中铁元素的质量分数为56%,将混合物加入一定量的稀硫酸
(2014•江都市二模)有20g铁、氧化亚铁、碳酸亚铁的混合物,其中铁元素的质量分数为56%,将混合物加入一定量的稀硫酸中,恰好反应,则反应后溶液中溶质的质量为( )
A.20g
B.15.2g
C.30.4g
D.33.6g 风中的云20021年前1
风中的云20021年前1 -
 eason1974 共回答了19个问题
eason1974 共回答了19个问题 |采纳率94.7%解题思路:根据题意可知铁、氧化亚铁、碳酸亚铁中的铁元素都转化到硫酸亚铁中去了,根据铁元素的质量算出硫酸亚铁的质量.由铁、氧化亚铁、碳酸亚铁的混合物质量为20g,铁元素的质量分数为56%,则可知铁元素质量为:20g×56%=11.2g,根据质量守恒定律铁元素都转化到硫酸亚铁中去了,故用铁元素质量除以硫酸亚铁中铁元素的质量分数,算出硫酸亚铁的质量:[11.2g
56/152×100%]=30.4g
故选:C.点评:
本题考点: 质量守恒定律及其应用;混合物中某元素的质量计算.
考点点评: 已知化合物中某元素的质量,求化合物的总质量方法是:用该元素的质量除以该元素在化合物中的质量分数.1年前查看全部
- 碳酸铁是共价化合物吗碳酸亚铁、碳酸铜、碳酸锌、碳酸银呢?能否介绍以下碳酸盐的性质呢(离子化合物还是共价化合物为主)
 明天的阳光更灿烂1年前1
明天的阳光更灿烂1年前1 -
 best119 共回答了22个问题
best119 共回答了22个问题 |采纳率81.8%碳酸铜,碳酸亚铁,碳酸锌,碳酸银都是沉淀的离子化合物,但是碳酸铁不好说,碳酸铁不存在溶液中,遇水就发生双水解反应Fe2(CO3)3+6H2O=2Fe(OH)3+3CO2↑+3H2O,类似会发生双水解的还有碳酸铝,碳酸盐基本都是离子化合物1年前查看全部
- 亚铁离子和碳酸氢根离子反应为什么会生成碳酸亚铁?
亚铁离子和碳酸氢根离子反应为什么会生成碳酸亚铁?
可题中让我写生成碳酸亚铁的反应方程式 caocaoyishu1年前3
caocaoyishu1年前3 -
 专门来祝福你 共回答了20个问题
专门来祝福你 共回答了20个问题 |采纳率90%Fe2+一般不考虑完全双水解,它与碳酸氢根反应得到碳酸亚铁,碳酸亚铁不会发生完全双水解而分解.
HCO3-会微弱的电离出H+和CO3 2-,Fe2+与CO3 2-结合成了很难溶的FeCO3沉淀,H+与另一分子HCO3-反应生成CO2和H2O.
如果某种金属离子的碳酸盐溶解度不是很小,则这种金属离子就不能与碳酸氢根反应得到碳酸盐.例如,碳酸氢钠与氯化钙混合,并不发生反应,因为水解产生的碳酸根浓度太低,不足以形成CaCO3饱和溶液,更不会析出CaCO3沉淀.只有加热后反应才发生,得到碳酸钙沉淀.1年前查看全部
- 赤铁矿、磁铁矿、菱铁矿的主要成分分别是三氧化二铁、四氧化三铁核碳酸亚铁.这些物质各1t,
赤铁矿、磁铁矿、菱铁矿的主要成分分别是三氧化二铁、四氧化三铁核碳酸亚铁.这些物质各1t,
含铁最多的是( )
A.赤铁矿 B.磁铁矿
C.菱铁矿 D.一样多 hqry1年前1
hqry1年前1 -
 kk幽瞳 共回答了17个问题
kk幽瞳 共回答了17个问题 |采纳率82.4%B 磁铁矿,分子量中铁的比例最多1年前查看全部
- 如何区分二价铁和三价铁的化合物不好意思,我没表达清楚。我的意思是怎么读呢?比如说FeCO3是读碳酸亚铁还是碳酸铁呢?还有
如何区分二价铁和三价铁的化合物
不好意思,我没表达清楚。我的意思是怎么读呢?比如说FeCO3是读碳酸亚铁还是碳酸铁呢?还有FeO? 蔓蔓烟草1年前1
蔓蔓烟草1年前1 -
 xx相处 共回答了25个问题
xx相处 共回答了25个问题 |采纳率96%铁的还原性在金属中算比较强,所以一般的氧化剂只能氧化到+2价,只有遇到像浓硫酸,氯气,氟气,氧气这种强氧化剂才会直接跳到+3价.
区别是Fe3+在溶液中显黄色,而Fe2+显浅绿色,Fe3+氧化性强于Fe2+
与氧气反应出现不同产物是因为反应的速率不同.当铁缓慢氧化时生成Fe2O3,而直接在纯氧里点燃铁就生成Fe3O4
Fe3O4其实可以看做是Fe2O3.FeO
其中两个铁显+3价,一个铁显+2价
由于Fe3O4可以看做是 FeO+Fe2O3,那么我们就把这两部分拆开来看
Fe2O3 中,一个铁是+3,两个铁共显+6价,一个氧是-2,三个氧就是-6,加起来是0
FeO中,一个铁是+2,一个氧是-2,加起来还是0
所以Fe3O4的化合价总和是0
另外如果硬要问Fe3O4中铁的化合价,答案只能是+2和+3,化合价一般不可以用分数表示(除了超氧根离子)1年前查看全部
- 硝酸钾 硝酸根 硝酸钡 硝酸铜 碳酸钠 碳酸钾 碳酸钡 碳酸亚铁 硫酸钠 硫酸铜 硫酸亚铁 硫酸铁的化学式
 davidin1年前1
davidin1年前1 -
 zhzj351 共回答了26个问题
zhzj351 共回答了26个问题 |采纳率84.6%硝酸钾 KNO3硝酸根 NO3-硝酸钡BA(NO3)2 硝酸铜CU(NO3)2 碳酸钠NA2CO3 碳酸钾K2CO3 碳酸钡 BACO3碳酸亚铁FECO3 硫酸钠NA2SO4 硫酸铜CUSO4 硫酸亚铁 FESO4硫酸铁FE2(SO4)3的化学式1年前查看全部
- (2013•天桥区二模)碳酸亚铁(FeCO3)是一种重要的工业盐,也是炼铁所用菱铁矿的主要成分,外观为白色固体,难溶于水
(2013•天桥区二模)碳酸亚铁(FeCO3)是一种重要的工业盐,也是炼铁所用菱铁矿的主要成分,外观为白色固体,难溶于水,遇水和氧气会发生反应,化学方程式为4FeCO3+6H2O+O2=4Fe(OH)3+4CO2.
(1)小亮同学提出三种生成碳酸亚铁的情况,其中正确的是(填序号)______
A.+3价铁的盐溶液与可溶性碳酸盐发生复分解反应;B.+2价铁的盐溶液与可溶性碳酸盐作用;C.铁与氧气、水发生复杂的氧化反应
(2)小亮同学取一定量碳酸亚铁固体于烧杯中,加入足量水,将烧杯放置在天平左盘上,向右盘放入砝码至天平平衡.放置较长时间后(不考虑水分蒸发),观察到天平的指针会______(填“偏左”、“偏右”、“不发生偏转”之一);另外,放置过程中还可观察到的一项实验现象为______.
(3)待上述烧杯中物质的质量不发生变化时,向烧杯中加入溶质质量分数为10%的稀盐酸109.5g,恰好完全反应,求反应后所得不饱和溶液中溶质的质量.(计算结果精确到0.01g) tyliuxing1年前1
tyliuxing1年前1 -
 牛儿神话 共回答了15个问题
牛儿神话 共回答了15个问题 |采纳率93.3%解题思路:(1)根据复分解反应前后各元素化合价不变分析;(2)根据碳酸盐铁、水和氧气反应能生成氢氧化铁和二氧化碳分析质量变化,根据生成物叙述实验现象;(3)根据盐酸中氯化氢的质量计算出生成氯化铁的质量.(1)复分解反应前后元素化合价不变,所以+3价铁的盐溶液与可溶性碳酸盐发生复分解反应生成碳酸铁,不是碳酸亚铁,故A错,+2价铁的盐溶液与可溶性碳酸盐作用能生成碳酸亚铁,故B正确;铁与氧气、水发生复杂的氧化反应,是铁生锈生成主要成分是氧化铁的物质,不属于碳酸亚铁,故C错;
(2)烧杯内质量增加了参加反应氧气的质量,反应后减少的质量是生成了二氧化碳,由方程式可知参加反应的氧气的质量小于生成的二氧化碳的质量,所以放置较长时间后,烧杯内质量减少,所以偏向右端;生成的氢氧化铁是红褐色固体,所以现象是白色固体变成红褐色固体;
(3)HCl的质量=109.5g×10%=10.95g
设所得溶液中溶质FeCl3的质量为x
Fe(OH)3+3HCl=FeCl3+3H2O
109.5 162.5
10.95g x
根据:[109.5/162.5=
10.95g
x]解得x=16.25g.
故答案为:(1)B;(2)偏右;白色固体变成红褐色固体(或产生气泡);(3)16.25g.点评:
本题考点: 物质的相互转化和制备;根据化学反应方程式的计算.
考点点评: 本题属于信息探究题,解题的关键是根据题目所给的信息,提取出有用信息,分析出反应进行的情况,从而进行有关的分析与计算.1年前查看全部
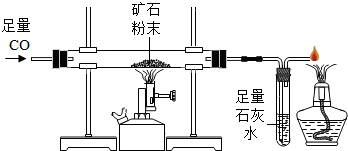
- 利用下图所示装置测定某含菱铁矿的矿石样品中碳酸亚铁的质量分数(杂质不含铁元素且在实验过程中不发生任何变化),实验数据记录
利用下图所示装置测定某含菱铁矿的矿石样品中碳酸亚铁的质量分数(杂质不含铁元素且在实验过程中不发生任何变化),实验数据记录在下表中.
提示:FeCO3
FeO+CO2↑高温 .
(1)该含菱铁矿的矿石样品中碳酸亚铁的质量分数______;实验前 实验后 硬质玻璃管(含样品) 165.6g 159.6g 说明 ①空硬质玻璃管质量为l45.6g
②含铁各物质反应完全
(2)实验结束后盛有澄清石灰水的试管的总质量比反应前的总质量增加______克. 有想法1年前1
有想法1年前1 -
 yujintao8 共回答了16个问题
yujintao8 共回答了16个问题 |采纳率100%解题思路:(1)固体物质的减少主要是因为从碳酸亚铁变成铁,失去了CO3,所以质量的减少为CO3的质量,根据两者的关系求算碳酸亚铁的质量,从而求算出其质量分数.
(2)空硬质玻璃管中减少的质量就是与一氧化碳结合的氧元素的质量,所以要根据与一氧化碳结合的氧元素的质量求算二氧化碳的质量.(1)实验中发生的化学反应有:FeCO3
高温
.
FeO+CO2↑,CO+FeO
高温
.
Fe+CO2↑,CO2+Ca(OH)2═CaCO3↓+H2O.
CO还原菱铁矿最终产物是铁和二氧化碳,实验前后硬质玻璃管(含样品)质量差为165.6g-159.6g=6g,实际上就是FeCO3中失去CO32-的质量,由此可计算出FeCO3的质量为11.6g.实验前硬质玻璃管(含样品)质量为165.6g,空硬质玻璃管质量为145.6g,得出样品质量为20g,故含菱铁矿的矿石样品中碳酸亚铁的质量分数为[11.6g/20g]×100%=58%
所以:因空硬质玻璃管质量是l45.6g,实验前硬质玻璃管(含样品)的质量是165.6g,实验后硬质玻璃管(含样品)的质量是159.6g,参加反应的样品的质量是165.6g-l45.6g=20g,而固体物质的质量减少为165.6g-159.6g=6g,即碳酸根的质量为6g;设碳酸亚铁的质量为x.
FeCO3~CO3
116 60
x6g
[116/60]=[x/6g]
x=11.6g
碳酸亚铁在样品中的质量分数为[11.6g/20.0g]×100%=58%
(2)分析可知碳酸根离子中只有一个氧原子和一氧化碳而生成二氧化碳,而剩余部分直接转化为二氧化碳.设与一氧化碳反应生成的二氧化碳的质量为y,而碳酸亚铁分解所生成的二氧化碳质量为z.
CO3~一氧化碳转化的CO2~碳酸亚铁分解产生的CO2
60 44 44
6g y z
[60/6g]=[44/y]=[44/z]
y=4.4g
z=4.4g
所以二氧化碳总质量为4.4g+4.4g=8.8g.
故答案为:58%;
(2)生成二氧化碳的质量是:8.8g.这些二氧化碳被试管中的澄清石灰水吸收,实验结束后盛有澄清石灰水的试管的总质量比反应前的总质量增加 8.8g.
故答案为:8.8g.点评:
本题考点: 一氧化碳还原氧化铁;根据化学反应方程式的计算.
考点点评: 本题主要考查与化学反应式有关的计算,有一定的难度,需要同学们细心方可做好此题.1年前查看全部
- 碳酸根离子与三价的铁离子不是不能形成物质吗,那怎么还会出现碳酸铁和碳酸亚铁?
 maomao113141年前2
maomao113141年前2 -
 史蒂芬 共回答了17个问题
史蒂芬 共回答了17个问题 |采纳率76.5%解析:
没有碳酸铁Fe2(CO3)3这种物质,只有碳酸盐铁(FeCO3,不溶于水).
Fe3+ 与 (CO3)2- 会发生双水
2Fe3+ + 3(CO3)2- + 3H2O → 2Fe(OH)3↓ + 3CO2 ↑1年前查看全部
- 碳酸亚铁『隔绝空气』加热将碳酸亚铁粉末放入试管中,『隔绝空气高温一段时间后』,冷却,试管内残留一定量的黑色粉末状物质.
碳酸亚铁『隔绝空气』加热
将碳酸亚铁粉末放入试管中,『隔绝空气高温一段时间后』,冷却,试管内残留一定量的黑色粉末状物质.
问:黑色粉末状物质可能是什么?
*注:1.高温分解后,生成物为两种氧化物,反应过程中元素的化合价不变!
2.『隔绝空气』
题目中还有这样一句话,请问是什么意思?
你认为黑色粉末可能是:1.( ),2.( )或二者的混合物。
『猜想的依据是?』
谢谢~ 无语渔者1年前3
无语渔者1年前3 -
 百色阿军 共回答了19个问题
百色阿军 共回答了19个问题 |采纳率78.9%应该是氧化亚铁,但是要是真的要有两种物质的话,我觉得可能就是还有没有反应的碳酸亚铁.1年前查看全部
- 碳酸钠,碳酸钾,碳酸银,碳酸钙,碳酸镁,碳酸钡,碳酸锌,碳酸铜,碳酸亚铁,碳酸铁,碳酸铝的化学式
 隔海看山1年前2
隔海看山1年前2 -
 nightlord 共回答了21个问题
nightlord 共回答了21个问题 |采纳率90.5%Na2co3,k2co3,ag2co3(?),caco3,mgco3,beco3,znco3,cuco3(?),feco3(?),fe2(co3)3(?),al2(co3)3(?)
打问号指有这种物质吗?碳酸酸性可没那么强哦,兄弟1年前查看全部
- 关于碳酸铁&碳酸亚铁比较下这两个东西我只知道都会双水解,具体有什么区别?
 hnczjy1年前1
hnczjy1年前1 -
 zhangsand365 共回答了11个问题
zhangsand365 共回答了11个问题 |采纳率81.8%FECO3是沉淀~很少的水解~
FE2(CO3)3是发生强烈的双水解,沉淀为FE(OH)31年前查看全部
- 碳酸铁双水解方程式是什么,为什么碳酸亚铁稳定碳酸铁不稳定?
 NICHOL1231年前3
NICHOL1231年前3 -
 dfcazgq 共回答了20个问题
dfcazgq 共回答了20个问题 |采纳率95%2 Fe3+ + 3 CO32- + 3 H2O = 2 Fe(OH)3 ↓ + 3CO2↑1年前查看全部
- 硫酸亚铁与稍过量的碳酸氢钠能否反应生成碳酸亚铁 如果能请写出化学反应方程式
硫酸亚铁与稍过量的碳酸氢钠能否反应生成碳酸亚铁 如果能请写出化学反应方程式
如上
题上的意思是可以生成的 ricdong1年前1
ricdong1年前1 -
 薄荷糖啊1980 共回答了21个问题
薄荷糖啊1980 共回答了21个问题 |采纳率81%是这样的
FeSO4+2NaHCO3=FeCO3+H2O+CO2+Na2SO4
FeCO3沉淀,CO2气体1年前查看全部
- 用硫酸亚铁和碳酸氢铵生成的碳酸亚铁如何经济的氧化成氧化铁?
 bleanp1年前1
bleanp1年前1 -
 szhwwhhbb 共回答了7个问题
szhwwhhbb 共回答了7个问题 |采纳率85.7%一定要用FeCO3制取Fe2O3么?
要制取也行:加热FeCO3
因为加热时,FeCO3会水解成Fe(OH)2,部分Fe(OH)2结合空气中的O2和H2O发生反应,生成Fe(OH)3.Fe(OH)3加热灼烧制得的就是Fe2O3了.(注:加热分解FeCO3的方法制取物为Fe2O3和FeO的混合物,不纯)1年前查看全部
- 碳酸亚铁长时间暴露在空气中表面变红褐色的方程式
 ralfyang1年前1
ralfyang1年前1 -
 xcvzhk23jflasdjk 共回答了15个问题
xcvzhk23jflasdjk 共回答了15个问题 |采纳率93.3%FeCO3+H2O→Fe(OH)2+CO2
4Fe(OH)2+2H2O+O2→4Fe(OH)31年前查看全部
- 为什么碳酸铁和碳酸铝会发生双向水解而碳酸亚铁和碳酸铜就不会?
为什么碳酸铁和碳酸铝会发生双向水解而碳酸亚铁和碳酸铜就不会?
他们都是弱酸弱碱盐啊
和化合价有关吗? tokytu1年前1
tokytu1年前1 -
 __心若在梦就在__ 共回答了12个问题
__心若在梦就在__ 共回答了12个问题 |采纳率83.3%这是因为Fe3+,Al3+的水解能力很强,
事实上0.1mol/L FeCl3,AlCl3溶液的PH分别大约等于2和3
在这个PH下,FeCl3溶液的PH大约等于0.1mol/L磷酸,
而 AlCl3的PH则近似等于0.1mol/L甲酸,
也就是说他们的水溶液呈较为明显的酸性,
所以当向体系中加入碳酸盐时,
可以看作是相对强的酸制备相对弱的酸.
以后见到Fe3+就把他当作中强酸,
看到Al3+就当作较强酸处理.
而Fe2+ ,Cu2+ ,Zn2+ ,Mg2+ ,NH4+ ,Ag+ 等
这些阳离子水解性很弱的,
他们大都水解产生的氢离子浓度不足以达到生成碳酸的浓度,
所以不会双水解.
所以以后看到上面6种离子,
就一定要认为他们是很弱的酸(水解后仍比碳酸还弱)1年前查看全部
- 亚硫酸和碳酸亚铁能否生成亚硫酸亚铁?向亚硫酸亚铁中加HNO3先氧化SO32-还是先氧化Fe2+?
 困困01101年前3
困困01101年前3 -
 kingxin207 共回答了21个问题
kingxin207 共回答了21个问题 |采纳率85.7%可以,强酸制弱酸
H2SO3+FeCO3=H2CO3+FeSO3
SO32-1年前查看全部
- 菱铁矿(主要为碳酸亚铁)为什么长期处于空气(O2)中没有变成三价铁离子?
 sfsdgs1年前1
sfsdgs1年前1 -
 meitanju 共回答了24个问题
meitanju 共回答了24个问题 |采纳率75%纯的碳酸铁在干燥的空气中碳酸铁是稳定的.在有水存在的条件下还是会因为氧化与水解而生成茶色的氢氧化铁(水溶液中不存在碳酸铁).而菱铁矿的情况与纯的碳酸铁情况又不一样,菱铁矿的主要成分是碳酸亚铁,也共生有别的金属矿,共生的其他的组成成分(如硫-还原剂)会影响到碳酸亚铁这一组分的稳定性,所以就像你提问中说的那样了.1年前查看全部
- 溶液的二价铁与碳酸根不能共存,是生成碳酸亚铁沉淀还是双水解?自然界能有碳酸亚铁!
 2008kiki1年前3
2008kiki1年前3 -
 我爱_zz 共回答了18个问题
我爱_zz 共回答了18个问题 |采纳率88.9%生成碳酸亚铁沉淀. 三价铁的水解能力强 可以和碳酸根双水解 二价铁不行.1年前查看全部
- 碳酸亚铁在水中不双水解吗
 michael9991年前1
michael9991年前1 -
 beckywang66 共回答了18个问题
beckywang66 共回答了18个问题 |采纳率100%白色三角形结晶.密度3.8g/cm3.不溶于水.1年前查看全部
- 柠檬酸亚铁和碳酸钠反应吗?但是我向柠檬酸亚铁中加如碳酸亚铁并没有沉淀
 邪吻1年前3
邪吻1年前3 -
 顾赛娟 共回答了19个问题
顾赛娟 共回答了19个问题 |采纳率100%由于柠檬酸亚铁是可溶于水的物质,所以反应,也就是普通的复分解反应,
生成最初白色(逐渐变成灰绿)的碳酸亚铁和柠檬酸钠.
3Na2CO3 + Fe3(C6H5O7)2===3FeCO3(沉淀)+2Na3C6H5O71年前查看全部
大家在问
- 1为什么作者把题目定为《星星变奏曲》?
- 2在家 英文
- 3两个相同的瓶子都装满了水,称得它们的重量是6千克,拿出其中一瓶,倒去一半的水,再放在一起称,一共还剩下5千克,一共空瓶子
- 4一什么圆形物(填量词)
- 5甲乙丙丁戊己六人站成一排进行排队,若甲必须排在第一位,乙丙相邻,丁戊不相邻的排法共有多少种
- 6已知函数f(x)=mx²-(m+1)x+1 (1)若方程f(x)=0有两个正实数根,求m的取值范围
- 7气体的温度升高 分子的热运动变得剧烈 分子的平均动能增大 撞击器壁时对器壁的作用力增大 从而气体压强增大
- 8Passage 49:Mrs.Smith Mrs.Smith is very old.She is 72.Her hus
- 9举个例子,教我怎么知道哪个是氧化剂,还原剂,氧化物,还原物,最好有图讲解
- 10不等式2x2+2x−4≤[1/2]的解集为( )
- 11请快速回答细胞膜可以什么,什么和什么是细胞中的能量装换器
- 12斜抛运动中最高点速度为0吗,水平加速度呢
- 13宇宙无限大吗?如果是,那么就有无限多恒星,发出的光远比太阳多,地球就不会出现黑夜,可事实不是这样;如果不是,那宇宙的边在
- 14254个偏旁部首,280个独体字,组合起来有多少个汉字?
- 15苏教版六年级下册《最大的麦穗》的道理可以用哪些生活中的例子说明
