富勒烯属于什么晶系富勒烯是晶体吧,那它属于什么晶系呢?
 喷喷龙2022-10-04 11:39:541条回答
喷喷龙2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 西日雨 共回答了24个问题
西日雨 共回答了24个问题 |采纳率91.7%- 足球烯 面心立方晶体
- 1年前
相关推荐
- 富勒烯C80结构及碳原子算法
 立儿1年前2
立儿1年前2 -
 sky860708 共回答了19个问题
sky860708 共回答了19个问题 |采纳率100%结构就是由五边形和六边形接连而成.
算法:
用欧拉公式 V + F - E = 2
V 多面体顶点数
F 多面体面数
E 多面体棱数
就可以算五边形与六边形的数量了.
设x个五边形,y个六边形.
一个点连三条边,两个点连一条边,所以有棱80*3/2=120
80 + (x + y) - 120 = 2
又因为每个点被三条边瓜分了.
所以有
x*5/3+y*6/3=80
解得
x=12
y=30
12个五边形,30个六边形.1年前查看全部
- 富勒烯 是一种化合物吗
 xiaoxin1171年前3
xiaoxin1171年前3 -
 xzm0864 共回答了22个问题
xzm0864 共回答了22个问题 |采纳率86.4%富勒烯不是化合物
C60(富勒烯)分子是一种由60个碳原子构成的分子,它形似足球,因此又名足球烯(C60这种物质是由C60分子组成的,而不是由原子构成的)C60是单纯由碳原子结合形成的稳定分子,它具有60个顶点和32个面,其中12个为正五边形,20个为正六边形.其相对分子质量约为720.1年前查看全部
- 已知富勒烯C70可与足量氟加成生成C70F70,试推测其分子结构中含有的碳碳单键数为
已知富勒烯C70可与足量氟加成生成C70F70,试推测其分子结构中含有的碳碳单键数为
A.105 B.70 C.35 D.30 一三八1年前1
一三八1年前1 -
 aimeeecho 共回答了21个问题
aimeeecho 共回答了21个问题 |采纳率95.2%A
富勒烯C70就是70个C原子的足球烯,每个碳原子以3个电子形成σ键与其他碳原子相连,剩余1个电子形成离域大π键,故而可以与F加成形成C70F70.
每个C原子有3个σ键,则单键数为
70*3/2=105
因为每个C原子连有3个单键,所以乘以3,而每个单键被计算了2次,所以除以21年前查看全部
- 金刚石是否分子?给大家个提示:C60、C70等富勒烯都被认为是分子,是因为有60或70个碳原子通过共价键结合形成了这些单
金刚石是否分子?
给大家个提示:C60、C70等富勒烯都被认为是分子,是因为有60或70个碳原子通过共价键结合形成了这些单质,二者都被认为是分子。而金刚石也是碳原子间通过碳碳共价单键形成的空间网状结构,确切地说是正四面体结构,所以它不是简单的碳原子单质,也不是用碳元素就能回答的,我想,思绪在风中摇曳的回答在现阶段应该是对的,至少我们应该知道,分子是肉眼看不到的。
我还是倾向于,金刚石是个我们可以看到的巨型分子。 九月燕南飞1年前6
九月燕南飞1年前6 -
 sdfasdfgsa456 共回答了20个问题
sdfasdfgsa456 共回答了20个问题 |采纳率100%不是.它是原子晶体,它由原子通过共价键连接形成空间立体网状结构.取多大金刚石,内部所有原子都联系在一起,所以它的组成粒子是原子.1年前查看全部
- 富勒烯足球状分子C50Cl50,碳碳单键和碳碳双键各是多少?怎么求
 kevin_ku1年前1
kevin_ku1年前1 -
 行之上 共回答了13个问题
行之上 共回答了13个问题 |采纳率76.9%弱弱的问下 富勒烯不是C60么= =
我知道C60的双键计算方法是
由于每个孤立的碳原子周围有三个键(一个双键,两个单键).而每个键却又是两个碳原子所共有,因此棱数=60×3×(1/2)=90 由于单键数+双键数=总棱边数 单键数=2×双键数(即单键数为双键数的2倍) 设单键数为a个,双键数为b个,则 a+b=90 a=2b 所以b=30
至于你说的C50Cl50 = =!1年前查看全部
- 关于富勒烯的碳的个数指的是最大会有几个碳
 细风轻雨1年前1
细风轻雨1年前1 -
 luoj715766 共回答了20个问题
luoj715766 共回答了20个问题 |采纳率90%除C60外,具有封闭笼状结构的还可能有C28、C32、C50、C70、C84……C240、C540等,统称为富勒烯(Fullerene).在数学上,富勒烯的结构都是以五边形和六边形面组成的凸多面体.最小的富勒烯是C20,有正十二面体的构造.没有22个顶点的富勒烯.之后都存在C2n的富勒烯,n= 12,13,14 .在之些小的富勒烯中,都存在着五边形相邻结构.C60是第一个没有相邻的五边形的富勒烯,下一个是C70.在更高的富勒烯中,普遍满足孤立五边形规则(Isolated pentagon rule,IPR),即在n>12时,不存在相邻的五边形结构.1年前查看全部
- 下列各组物质属于同素异形体的是( ) A. 16 O和 18 O B.金刚石、石墨和富勒烯(C 60 ) C.CH 3
下列各组物质属于同素异形体的是( ) A. 16 O和 18 O B.金刚石、石墨和富勒烯(C 60 ) C.CH 3 CH 2 OHCH 3 OCH 3 D.H 2 O和H 2 O 2  ericsean1年前1
ericsean1年前1 -
 ww秘密 共回答了11个问题
ww秘密 共回答了11个问题 |采纳率90.9%A、 16 O和 18 O都不是单质,不属于同素异形体,都是氧元素的不同核素,互为同位素,故A错误;
B、金刚石、石墨和C 60 都是由碳元素形成的不同物质,都是单质,互为同素异形体,故B正确;
C、CH 3 CH 2 OH、CH 3 OCH 3 都不是单质,不属于同素异形体,二者分子式相同,结构不同,互为同分异构体,故C错误;
D、H 2 O和H 2 O 2 都不是单质,因此不属于同分异构体,故D错误;
故选:B.1年前查看全部
- 1996年诺贝尔化学奖授予斯莫利等三位化学家,以表彰他们发现富勒烯(C 60 )开辟了化学研究的新领域。后来,人们又发现
1996年诺贝尔化学奖授予斯莫利等三位化学家,以表彰他们发现富勒烯(C 60 )开辟了化学研究的新领域。后来,人们又发现了一种含碳量极高的链式炔烃──棒碳,它是分子中含300~500个碳原子的新物质,其分子中只含有交替连接的单键和叁键。对于C 60 与棒碳,下列说法正确的是 A.C 60 与棒碳中所有的化学键都是非极性共价键
B.棒碳不能使溴水褪色
C.C 60 在一定条件下可能与CuO发生置换反应
D.棒碳与乙炔互为同系物 许可1年前1
许可1年前1 -
 雷雨洁 共回答了15个问题
雷雨洁 共回答了15个问题 |采纳率86.7%C1年前查看全部
- ①金刚石、石墨和富勒烯②铁丝和铁块③Na和Na+④O2和O3⑤H2和H⑥斜方硫和单斜硫,互为同素异形体的组是
①金刚石、石墨和富勒烯②铁丝和铁块③Na和Na+④O2和O3⑤H2和H⑥斜方硫和单斜硫,互为同素异形体的组是
同素异形体是指由同种元素组成,排列方式不同的单质
这里的排列方式是指原子的排列方式么?
我觉得答案是146 地域里有没有明天1年前2
地域里有没有明天1年前2 -
 xingfuleyuan 共回答了13个问题
xingfuleyuan 共回答了13个问题 |采纳率76.9%同素异形体形成方式
有三种:1.组成分子的原子数目不同,例如:氧气O2和臭氧O3 2.晶格中原子的排列方式不同,例如:金刚石和石墨 3.晶格中分子排列的方式不同,例如:正交硫和单斜硫
所以你说的146是对的(对于富勒烯,它的确是是一种碳的同素异形体 ,楼主不要怀疑)1年前查看全部
- 富勒烯的各分子有封闭笼状结构,它们是否具有相似的性质
 冰箱里的草莓拉拉1年前2
冰箱里的草莓拉拉1年前2 -
 好大一个创可贴 共回答了15个问题
好大一个创可贴 共回答了15个问题 |采纳率86.7%是具有相似性质的1年前查看全部
- 【高中化学题】已知富勒烯C70可与足量氟加成生成C70F70,试推测其分子结构中含有的碳碳单键数为( ).
【高中化学题】已知富勒烯C70可与足量氟加成生成C70F70,试推测其分子结构中含有的碳碳单键数为( ).
已知富勒烯C70可与足量氟加成生成C70F70,试推测其分子结构中含有的碳碳单键数为( ).
A.105 B.70 C.35 D.30
正确答案是:A
以下是我在网上找到的解释:
富勒烯C70就是70个C原子的足球烯,每个碳原子以3个电子形成σ键与其他碳原子相连,剩余1个电子形成离域大π键,故而可以与F加成形成C70F70.
每个C原子有3个σ键,则单键数为
70*3/2=105
怎么知道每个碳原子以3个电子形成σ键与其他碳原子相连,剩余1个电子形成离域大π键? luopidong1年前1
luopidong1年前1 -
 栋栋814 共回答了22个问题
栋栋814 共回答了22个问题 |采纳率90.9%首先明白,C70中,一个C只连接了3个碳原子.这是基础知识,不知道这个就没法做了.
所有富勒烯(C60、C70、C180等等)都是这样的
考虑其中一个碳原子.
C 外层有4个电子,拿出3个与其他3个碳原子形成σ键,这样还剩一个.
于是,这个电子可以与 F原子的单电子形成σ键.
所以一共能形成70个C—F σ键
即 化学式 C70F70.
因为一个C形成3个单键,1个单键被2个C共用,所以1个C平均1.5个单键
C70单键数目 = 70*3/2=105
你查到的解释说得很对,但没必要理解离域大π键.
高中按我说的,一点问题没有1年前查看全部
- 下列关于富勒烯(C60)的描述正确的是( )
下列关于富勒烯(c60)的描述正确的是( )
a每个富勒烯分子由60个碳原子构成
b富勒烯的摩尔质量为60g/mol
c富勒烯是一种化合物
d富勒烯和金刚石是同一种物质
下列物质中,硬度最大的是( )
a玻璃
b大理石
c金刚石
d石墨
下列各组含碳化合物中,其中碳元素的化合价由低到高顺序排列的是( )
a co,c,h2co3
b caco3,co,c
c k2co3,c,co
d c,co,h2co3
木炭和活性炭都具有吸附作用,是因为( )
a常温时,化学性质都不活泼
b颗粒都很小,而且是黑色的
c都具有疏松多孔的结构
d都不具有毒气
下列各组物质中,主要分成属于同一种物质的是( )
a生石灰,熟石灰
b石灰石,氢氧化钙
c氢氧化钙,熟石灰
d生石灰,石灰石
金刚石和石墨的物理性质有很大差异的原因是( )
a金刚石和石墨是有不同元素组成的
b金刚石是单质,石墨是化合物
c金刚石不含杂质,而石墨含有杂质
d金刚石和石墨里碳原子的排列不同
下列物质中,可用于区别澄清石灰水和氢氧化钠溶液的是( )
a盐酸
b二氧化碳
c紫色石蕊试液
d酚酞试液
要使一氧化碳和二氧化碳中含有相同质量的氧,则一氧化碳与二氧化碳的物质的量的比为( )
a 1:2
b 2:1
c 11:14
d 14:11
要使碳与氧化铜恰好完全反应生成铜和二氧化碳,则碳与氧化铜的物质的量比为( )
a 1:1
b 1:2
c 3:20
d 3:40
石墨******时能在方圆几百米范围内撒下大量石墨纤维,造成输电线,电厂设备损坏.这是由于石墨( )
a有放射性
b易燃,易爆
c能导电
d有剧毒
在高炉炼铁的过程中,氧化铁通过反应fe2o3+3co →(高温) 2fe+3co2转变为单质铁,这一反应中的还原剂是( )
a fe2o3
b co
c fe
d co2 股道衷肠1年前2
股道衷肠1年前2 -
 乱湛韶隅 共回答了19个问题
乱湛韶隅 共回答了19个问题 |采纳率73.7%A C D C C D B D B C B1年前查看全部
- 如图是金刚石、石墨、富勒烯(C 60 )的结构示意图,下列说法错误的是( )
如图是金刚石、石墨、富勒烯(C 60 )的结构示意图,下列说法错误的是( ) 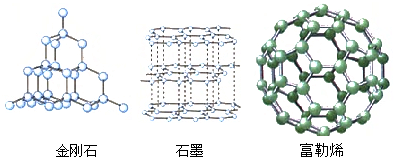
A.三种物质性质相同 B.三种物质是碳元素的同素异形体 C.三种物质碳原子的排列方式不同 D.三种物质完全燃烧后的产物都是CO 2  冷月寒烟11年前1
冷月寒烟11年前1 -
 ---遗憾美--- 共回答了16个问题
---遗憾美--- 共回答了16个问题 |采纳率93.8%A、由三者的结构示意图可知金刚石、石墨和C 60 碳原子的排列方式不同,其化学性质相同,但物理性质不同,故C项说法错误;
B、金刚石、石墨和C 60 都是由碳元素组成的单质,是碳的同素异形体,故B项说法正确;
C、由三者的结构示意图可知金刚石、石墨和C 60 碳原子的排列方式不同,说法正确;
D、因为它们都是碳的单质,其化学性质相同,所以完全燃烧后的产物都是CO 2 ,故D项说法正确.
故选A.1年前查看全部
- 若C80为富勒烯家族,求其结构中五边形和六边形个数?怎么判断其是否为富勒烯家族?
 jf20201年前1
jf20201年前1 -
 sohu19840011 共回答了16个问题
sohu19840011 共回答了16个问题 |采纳率93.8%富勒烯家族的Cn,一定满足一下关系
n≥ 20,并且n一定是偶数
五边形数目=12
六边形数目=n/2 - 10
具体算法已经发送到邮箱.1年前查看全部
- 金刚石、石墨、富勒烯(包括C60、C70和单层或多层的纳米碳管等)都是碳的单质,这些单质互称为碳的同素异形体.将某固体物
金刚石、石墨、富勒烯(包括C60、C70和单层或多层的纳米碳管等)都是碳的单质,这些单质互称为碳的同素异形体.将某固体物质在氧气中完全燃烧,使产物通过澄清石灰水,生成白色沉淀.有关该固体的推测正确的是( )
A.该固体一定是碳的同素异形体
B.该固体一定不是碳的同素异形体
C.该固体中可能含有碳、氢、氧元素
D.该固体中只含有碳、氢元素 我也是来骂人的1年前1
我也是来骂人的1年前1 -
 属猫的女子 共回答了22个问题
属猫的女子 共回答了22个问题 |采纳率86.4%解题思路:将某固体物质在氧气中完全燃烧,使产物通过澄清石灰水,生成白色沉淀可能为碳酸钙,根据元素守恒思想和物质的性质来回答.固体物质在氧气中完全燃烧,使产物通过澄清石灰水,生成白色沉淀,沉淀可能是碳酸钙,该气体是二氧化碳,所以物质中一定含有C元素,可能含有氧元素,氢元素的存在与否也不会影响实验现象,即H元素也不能确定.
A、该固体一定含有C元素,但是不一定是碳的同素异形体,故A错误;
B、该固体一定含有C元素,可能是碳的同素异形体,故B错误;
C、该固体一定含有C元素,可能含有氧元素,还可能含有氢元素,故C正确;
D、该固体一定含有C元素,可能含有氧元素,还可能含有氢元素,故D错误.
故选C.点评:
本题考点: 测定有机物分子的元素组成.
考点点评: 本题通过燃烧法确定物质的组成元素,是有机物元素确定的常用方法,可以根据教材知识来回答,难度不大.1年前查看全部
- C60富勒烯的共用电子对为多少,求详解.
 czq补丁1年前1
czq补丁1年前1 -
 xiaoyan051 共回答了22个问题
xiaoyan051 共回答了22个问题 |采纳率100%一共有60个C,而C单质的所有价电子都用于成键而没有孤对电子存在,所以共用电子个数为60×4=240,即120对.1年前查看全部
- 富勒烯中0D是什么意思
 玻璃上的tt1年前1
玻璃上的tt1年前1 -
 mpd3 共回答了11个问题
mpd3 共回答了11个问题 |采纳率100%零维(0D)
石墨烯是由碳六元环组成的两维(2D)周期蜂窝状点阵结构,它可以翘曲成零维(0D)的富勒烯(fullerene),卷成一维(1D)的碳纳米管(carbon nano-tube,CNT)或者堆垛成三维(3D)的石墨(graphite),因此石墨烯是构成其他石墨材料的基本单元.1年前查看全部
- (2012•虹口区一模)如图是金刚石、石墨、富勒烯(C60)的结构示意图,下列说法错误的是( )
(2012•虹口区一模)如图是金刚石、石墨、富勒烯(C60)的结构示意图,下列说法错误的是( )
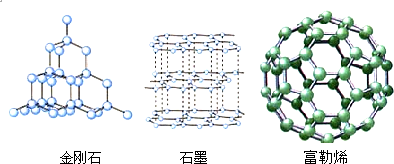
A.三种物质性质相同
B.三种物质是碳元素的同素异形体
C.三种物质碳原子的排列方式不同
D.三种物质完全燃烧后的产物都是CO2 反清覆明1年前1
反清覆明1年前1 -
 谢庆华 共回答了17个问题
谢庆华 共回答了17个问题 |采纳率94.1%解题思路:金刚石、石墨和C60和都是由碳元素组成的单质.金刚石是最为坚固的一种碳结构,其中的碳原子以晶体结构的形式排列,石墨中碳原子以平面层状结构键合在一起,层与层之间键合比较脆弱,因此层与层之间容易被滑动而分开. C60分子是一种由60个碳原子构成的分子,它形似足球,因此又名足球烯. C60是单纯由碳原子结合形成的稳定分子.因它们碳原子的排列结构不同,各自有不同的物理性质,但它们都是碳的单质,所以化学性质相同.A、由三者的结构示意图可知金刚石、石墨和C60碳原子的排列方式不同,其化学性质相同,但物理性质不同,故C项说法错误;
B、金刚石、石墨和C60都是由碳元素组成的单质,是碳的同素异形体,故B项说法正确;
C、由三者的结构示意图可知金刚石、石墨和C60碳原子的排列方式不同,说法正确;
D、因为它们都是碳的单质,其化学性质相同,所以完全燃烧后的产物都是CO2,故D项说法正确.
故选A.点评:
本题考点: 碳元素组成的单质.
考点点评: 本题图形和文字相结合主要考查由碳元素组成的三种物质,要明确这三种物质是同素异形体(相同元素组成,不同形态的单质),同素异形体由于结构不同,彼此间物理性质有差异;但由于是同种元素形成的单质,所以化学性质相似.1年前查看全部
- 1996年诺贝尔化学奖授予发现并制取了一种叫富勒烯的新物质的三位科学家。富勒烯是由碳原子形成的形状类似足球的大分子,其化
1996年诺贝尔化学奖授予发现并制取了一种叫富勒烯的新物质的三位科学家。富勒烯是由碳原子形成的形状类似足球的大分子,其化学式是C 60 。下列说法错误的是 [ ]A.富勒烯属于单质
B.富勒烯是碳的单质
C.富勒烯是由60个碳原子构成的化合物
D.富勒烯的相对分子质量是720 y46561年前1
y46561年前1 -
 tatalalala 共回答了22个问题
tatalalala 共回答了22个问题 |采纳率81.8%C1年前查看全部
- 怎样判断某种Cx是否属于富勒烯家族
 dfi_y3fdgn1f_a41年前1
dfi_y3fdgn1f_a41年前1 -
 yl224 共回答了24个问题
yl224 共回答了24个问题 |采纳率91.7%富勒烯家族的Cn,一定满足一下关系
n≥ 20,并且n一定是偶数
五边形数目=12
六边形数目=n/2 - 10
富勒烯通式可表示为C2n(n为大于等于10的整数).富勒烯是笼状结构,由若干正五边形和正六边形构成.在富勒烯中,每个顶点被3个面共用,每条边被2个面共用.
C2n中,F5表示五边形个数,F6表示六边形个数.
V=2n
F=F5+F6
V=(5F5+6F6)/3
E=(5F5+6F6)/2
V-E+F=2
解得
F5=12
F6=n-10
E=3n
即,任何富勒烯中,五边形数都是12,六边形数是10-n,边数是3n.例如C60中,n=30,五边形数是12,六边形数是20,边数是90.
C四条键,而每个顶点被3条边共用,所以富勒烯中双键数:单键数=1:21年前查看全部
- 1.已知富勒烯家族中的一种分子C80,已知其分子结构中都有正五边形和正六边形构成,请列式计算该笼状分子中的五边形和六边形
1.已知富勒烯家族中的一种分子C80,已知其分子结构中都有正五边形和正六边形构成,请列式计算该笼状分子中的五边形和六边形的个数.
2.某笼状分子,其分子式为:C24H24,有三种特殊的同分异构体,且分子中不含有双键或三键结构,他们都只有一种一氯取代物,而二氯取代物不完全相同,请画出或说明这三种同分异构体的结构,分子中五边形和六边形的数目,并判断他们的稳定性.
也请给出算法:如果是Cx的富勒烯(如C78、C82、C84、C90、C96等),那么其分子结构中五边形和六边形和其棱数(键数)的数目是多少? liaojtong1年前1
liaojtong1年前1 -
 幽幽长天 共回答了17个问题
幽幽长天 共回答了17个问题 |采纳率76.5%1.已知富勒烯家族中的一种分子C80,已知其分子结构中都有正五边形和正六边形构成,请列式计算该笼状分子中的五边形和六边形的个数.
用欧拉公式 V + F -E = 2
V 多面体顶点数
F 多面体面数
E 多面体棱数
设有正五边形x个 正六边形y个 每三条棱共用一个顶点
C80共有80个顶点 棱数为80×3=240
所以 80 + (x + y) - 120 =2
又因为每个五边形包含5/3个碳 每个六边形包含6/3个碳
所以 5/3*x +6/3*y = 80
两方程联立
x = 12
y = 30
2.某笼状分子,其分子式为:C24H24,有三种特殊的同分异构体,且分子中不含有双键或三键结构,他们都只有一种一氯取代物,而二氯取代物不完全相同,请画出或说明这三种同分异构体的结构,分子中五边形和六边形的数目,并判断他们的稳定性.
烃中没有双键三键 说明含有环 每含有一个环 氢原子数减二
含二十四个碳的饱和烷烃应含有氢原子50个 实际有24个 则含有的环数为
(50-24)/2 = 13
同上计算1年前查看全部
- 石墨,富勒烯,金刚石算什么晶体
 湖九1年前1
湖九1年前1 -
 qa6jgb 共回答了16个问题
qa6jgb 共回答了16个问题 |采纳率93.8%富勒烯,金刚石为分子晶体 石墨是过渡型晶体1年前查看全部
- 等物质的量的石墨和富勒烯(碳60)所含的质子数谁多
等物质的量的石墨和富勒烯(碳60)所含的质子数谁多
答案是碳60 为什么 亲亲泡1年前2
亲亲泡1年前2 -
 Ogopogo狼 共回答了29个问题
Ogopogo狼 共回答了29个问题 |采纳率96.6%碳601年前查看全部
- 金刚石、石墨和富勒烯 是碳原子组成的 的单质分子
金刚石、石墨和富勒烯 是碳原子组成的 的单质分子
金刚石、石墨和富勒烯 是碳原子组成的?的单质分子 无泪鬼鬼1年前4
无泪鬼鬼1年前4 -
 yourancn 共回答了18个问题
yourancn 共回答了18个问题 |采纳率77.8%同素异形体.1年前查看全部
- 富勒烯是什么状态的物质
 keven1111年前1
keven1111年前1 -
 旋转世界 共回答了22个问题
旋转世界 共回答了22个问题 |采纳率95.5%富勒烯是于1985年发现的继金刚石和石墨之后碳元素的第三种晶体形态,又一类碳的同素异形体.1年前查看全部
- 富勒烯是什么物质?谁发现的?比如富勒烯是什么颜色、状态的物质?是否是化合物?是自然存在的还是人造的?
 今夜太阳好圆丫1年前2
今夜太阳好圆丫1年前2 -
 wlll24 共回答了20个问题
wlll24 共回答了20个问题 |采纳率95%克罗托等人之所以能够勾画出C60的分子结构,富勒的启示起了关键性作用,因此他们一致建议,用布克米尼斯特·富勒(Buckminster Fuller)的姓名加上一个词尾-ene来命名C60及其一系列碳原子簇,称为Buckminsterfullerene,简称Fullerene,中译名为富勒烯.
近年来,科学家们发现,除金刚石、石墨外,还有一些新的以单质形式存在的碳.其中发现较早并已在研究中取得重要进展的是C60分子.C60分子是一种由60个碳原子构成的分子,它形似足球,因此又名足球烯.C60是单纯由碳原子结合形成的稳定分子,它具有60个顶点和32个面,其中12个为正五边形,20个为正六边形.其相对分子质量约为720.处于顶点的碳原子与相邻顶点的碳原子各用近似于sp2杂化轨道重叠形成σ键,每个碳原子的三个σ键分别为一个五边形的边和两个六边形的边.碳原子杂化轨道理论计算值为sp2.28,每个碳原子的三个σ键不是共平面的,键角约为108°或120°,因此整个分子为球状.每个碳原子用剩下的一个p轨道互相重叠形成一个含60个π电子的闭壳层电子结构,因此在近似球形的笼内和笼外都围绕着π电子云.分子轨道计算表明,足球烯具有较大的离域能.C60具有金属光泽,有许多优异性能,如超导、强磁性、耐高压、抗化学腐蚀、在光、电、磁等领域有潜在的应用前景. 碳纳米管是典型的富勒烯,又称巴基管,是一种管状结构的碳原子簇,直径约几纳米,长约几微米.据理论计算,碳纳米管纤维的强度是钢的100倍,而质量仅为钢的1/7,如果能做成碳纤维,将是理想的轻质高强度材料.碳纳米管还具有极强的储气能力,可以在燃料电池储氢装置上.
C60是一种碳原子簇.它有确定的组成,60个碳原子构成像足球一样的32面体,包括20个六边形,12个五边形.由于这个结构的提出是受到建筑学家富勒(Buckminster Fuller)的启发.富勒曾设计一种用六边形和五边形构成的球形薄壳建筑结构.因此科学家把C60叫做足球烯,也叫做富勒烯,因为32面体的每个顶点上的碳原子跟三个其它的碳原子相邻.如同苯环上每个碳原子都是sp2杂化.p轨道在环的上、下形成π键一样,足球烯每个顶角上的碳原子也都满足sp2杂化的要求,(类似萘环上两个不带氢原子的碳原子)剩余的p轨道在C60分子的外围和内腔形成π键.所以C60是一种烯. 因为C60是石墨、金刚石的同素异形体,因此有科学家联想到用廉价的石墨作原料合成C60,也有人想到它含有苯环单元的结构,或许可以选用苯作原料合成C60.这些设想最后都实现了.现在,1000g苯可以制得3gC70和C60的混合物(它们的比率为0.26~5.7). 大自然鬼斧神工的巧合,这60个C原子在空间进行排列时,形成一个化学键最稳定的空间排列位置,恰好与足球表面格的排列一致.
物理性质
颜色与性状
C60在室温下为紫红色固态分子晶体,有微弱荧光.
分子大小
C60分子的直径约为7.1埃(1埃= 10^ -10 米即一百亿分之一米).
密度
C60的密度为1.68g/cm^3.
溶解性
C60不溶于水等强极性溶剂,在正己烷、苯、二硫化碳、四氯化碳等非极性溶剂中有一定的溶解性.
导电性
C60常态下不导电.因为C60大得可以将其他原子放进它内部,并影响其物理性质,因而不可导电.另外,由于C60有大量游离电子,所以若把可作β衰变的放射性元素困在其内部,其半衰期可能会因此受到影响.
超导性
1991年,赫巴德(Hebard)等首先提出掺钾C60具有超导性,超导起始温度为18K,打破了有机超导体(Et)2Cu[N(CN)2]Cl超导起始温度为12.8K的纪录.不久又制备出Rb3C60的超导体,超导起始温度为29K.掺杂C60的超导体已进入高温超导体的行列.研究显示,这类材料是以晶格里的电洞来传导电流(类似p型半导体),若加入其它分子(例如三溴甲烷)来拉长晶格间距,还可以有效地提升其超导相变温度至117K.中国在这方面的研究也很有成就,北京大学和中国科学院物理所合作,成功地合成了K3C60和Rb3C60超导体,超导起始温度分别为8K和28K.有科学工作者预言,如果掺杂C240和掺杂C540,有可能合成出具有更高超导起始温度的超导体.
磁性
阿勒曼(Allemand)等人在C60的甲苯溶液中加入过量的强供电子有机物四(二甲氨基)乙烯(TDAE),得到了C60(TDAE)C0.86的黑色微晶沉淀,经磁性研究后表明是一种不含金属的软铁磁性材料.居里温度为16.1K,高于迄今报道的其它有机分子铁磁体的居里温度.由于有机铁磁体在磁性记忆材料中有重要应用价值,因此研究和开发C60有机铁磁体,特别是以廉价的碳材料制成磁铁替代价格昂贵的金属磁铁具有非常重要的意义.
化学性
周环反应
富勒烯的[6,6]键可以与双烯体或双烯亲和体反应,如D-A反应.[2+2]环加成可以形成四元环,如苯炔.1,3偶极环加成反应可以生成五元环,被称作Prato反应.富勒烯与卡宾反应形成亚甲基富勒烯.周环反应
加氢还原
富勒烯氢化有几个容易的方法.氢化富勒烯如C60H18,C60H36.然而,完全氢化的C60H60仅仅是假设存在因为分子张力过大.高度氢化富勒烯不稳定,富勒烯与氢气直接反应在高温条件下的直接反应会导致笼结构崩溃,而形成的多环芳烃.
羟基化反应
富勒烯可以通过羟基化反应得到富勒多醇(fullerenols)和富勒醇.其水溶性取决于其(富勒醇)分子中羟基数的多少.一种方法是富勒烯与稀硫酸和硝酸钾反应可生成C60(OH)15.另一种方法是在稀氢氧化钠溶液的催化下反应由TBAH增加24 到26个羟基.羟基化反应也有过用无溶剂氢氧化钠与过氧化氢和富勒烯反应的报道.用过氧化氢与富勒烯的反应合成C60(OH)8,羟基的最大数量,可以达到36至40个.
氧化还原反应
氧化还原反应: 在光照的条件下将C60与O2反应生成环氧化物C60O2,但这种环氧化物不稳定,用矾土分离时能还原成C60.
加成反应
C60可以与氢或卤素单质进行加成.把其完全氢化便得绒毛球烷(Fuzzyball),化学式为C60H60(加成进的氢原子有可能C60在笼内也可能在C60外部).烷基自由基R可与C60反应生成RC60加和物,RC60可生成C60直接键和哑铃状二聚体RC60-C60R.
亲电加成
富勒烯也可以发生亲电反应.可以在富勒烯球外加成24个溴原子.最多亲电加成纪录保持者是C60F48.根据氟硅烷的结构(在硅元素中)还难以预测C60F60是否可能有一些氟原子在“endo”位置(指富勒烯内部),这种化合物是比起球型更类似于一个管状的富勒烯分子.
配位反应
富勒烯在有机金属化学中作为配体.[6,6]双键是缺电子的,通常与金属成键的η= 2(配位化学中的常数).键合模式如η= 5或η=6可以因作为配体的球状富勒烯改变而改变.富勒烯和硫羰基钨W(CO)6在环己烷溶液中,阳光直接照射下反应生成的(η²-C60)5 W(CO)6.
内嵌反应
指通过化学手段选择性地切断富勒烯骨架上的碳碳键来制备开孔富勒烯的反应.开孔后就可能把一些小分子装到碳球中,如氢分子、氦、锂等.第一个开孔富勒烯是在1995由Wudl等报道的.
反加成
反加成反应即Retro-Additions(RA).研究表明,通过RA消去,取代基实现了他们的目的后便与富勒烯主体分离.
与金属的反应
C60与金属的反应分为两种情况:一种是金属被置于C60碳笼的内部;另一种是金属位于C60碳笼的外部: 1)C60碳笼内配合物生成反应.C60碳笼为封闭的中空的多面体结构,其内腔直径为7.1埃,内部可嵌入原子、离子或小分子形成新的团簇分子,C60 + AC60(A).Smalley等人现已发现能与C60生成C60(A)的金属有:K、Na、Cs、La、Ba、Sr、U、Y、Ce、Sm、Eu、Gd、Tb、Ho、Th等.除金属外,He、Ne等惰性气体及LiF、LiCl、NaCl等极性分子亦可移置C60笼中. 2)C60碳笼外键合反应.Ohno等人发现能与C60键合的金属有:V、Fe、Co、Ni、Rh、Cu、La、Yb、Ag等.
颜色反应
C60可以溶于二硫化碳中.颜色呈紫红色.1年前查看全部
- 金刚石、石墨、富勒烯(包括C 60 、C 70 和单层或多层的纳米碳管等)都是碳的单质,这些单质互称为碳的同素异形体.将
金刚石、石墨、富勒烯(包括C 60 、C 70 和单层或多层的纳米碳管等)都是碳的单质,这些单质互称为碳的同素异形体.将某固体物质在氧气中完全燃烧,使产物通过澄清石灰水,生成白色沉淀.有关该固体的推测正确的是( ) A.该固体一定是碳的同素异形体 B.该固体一定不是碳的同素异形体 C.该固体中可能含有碳、氢、氧元素 D.该固体中只含有碳、氢元素  狗一只1年前1
狗一只1年前1 -
 楼少 共回答了23个问题
楼少 共回答了23个问题 |采纳率100%固体物质在氧气中完全燃烧,使产物通过澄清石灰水,生成白色沉淀,沉淀可能是碳酸钙,该气体是二氧化碳,所以物质中一定含有C元素,可能含有氧元素,氢元素的存在与否也不会影响实验现象,即H元素也不能确定.
A、该固体一定含有C元素,但是不一定是碳的同素异形体,故A错误;
B、该固体一定含有C元素,可能是碳的同素异形体,故B错误;
C、该固体一定含有C元素,可能含有氧元素,还可能含有氢元素,故C正确;
D、该固体一定含有C元素,可能含有氧元素,还可能含有氢元素,故D错误.
故选C.1年前查看全部
大家在问
- 1指望的近义词和反义词是什么
- 2学完新概念英语第一册能不能相当于初中学的水平?
- 3有两堆煤,如果从甲堆中取出五分之四吨放入乙堆,这时两堆煤重量相等.如果从乙堆中取出五分之四吨放入乙
- 4关于促销的学后感advantage or disadvantage of the sales promotion for
- 5《师旷问学》中‘何不炳烛乎’在文中起什么作用
- 6新概念英语的第一册是初中水平?
- 7已知(X+1)n方展开式中第二项与第五项系数相等.求第四项
- 8六角密堆积属于什么晶系如题!有没有学者告诉一下.固体物理里的知识.
- 9燃烧、缓慢氧化和自燃的相同点:都属于 ,都 .
- 10You is a short,fat,and idiot
- 11长方形的横截面面积一定,它的体积和长.成什么比例
- 12有甲乙两导体,甲的横截面积是乙的两倍,单位时间内通过乙导体横截面积电荷量是甲的两倍,为什么乙中自由
- 13天上打雷的声音怎样形容
- 14有使内能直接转化为电能的装置
- 151寸等于多少mm?
