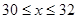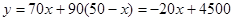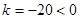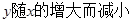新型游标卡尺使用疑问说游标卡尺原理为以准确到0.1毫米的游标卡尺为例,尺身上的最小分度是1毫米,游标尺上有10个小的等分
 gzzyq2022-10-04 11:39:546条回答
gzzyq2022-10-04 11:39:546条回答说游标卡尺原理为以准确到0.1毫米的游标卡尺为例,尺身上的最小分度是1毫米,游标尺上有10个小的等分刻度,总长9毫米,每一分度为0.9毫米,比主尺上的最小分度相差0.1毫米,精度为0.1mm
现有新型卡尺,尺身最小分度为1MM,游标尺有20分度,长39MM,求此卡尺精度

已提交,审核后显示!提交回复
共6条回复
 top_rose 共回答了17个问题
top_rose 共回答了17个问题 |采纳率88.2%- 0.05mm
不管怎样,精度就是 尺身最小分度/游标分度数目 - 1年前
 一半一半39 共回答了1个问题
一半一半39 共回答了1个问题 |采纳率- 20分度的真正长度是19mm, 19mm分成20份即:19/20=0.95mm, 1-0.95=0.05mm (主尺每个格1mm),左边对齐,滑动尺每个格0.95mm向右移动0.05mm跟主尺第一个格对齐,所以精度是0.05mm.
- 1年前
 华采衣兮若英 共回答了3个问题
华采衣兮若英 共回答了3个问题 |采纳率- 其实精确度并不都是用1除以分度数,如厂家生产10分度总长8mm那么精确度就是
1-8/10=0.2mm,对于你说的这种卡尺,20个分度总长是39mm,那么游标尺的每个分度长39/20=1.95mm, 现在我们把主尺上的刻度每2mm看成一大格,用游标的一个分度比主尺上的一个大格短2mm-1.95mm=0.05mm,即游标尺(跟测量抓固定在一起)向前每拨动一个0.05mm必出现一个分度线与主尺... - 1年前
 ok888 共回答了125个问题
ok888 共回答了125个问题 |采纳率- 0.02
- 1年前
 sdfasdqwgqwwq 共回答了115个问题
sdfasdqwgqwwq 共回答了115个问题 |采纳率- 0.02mm,用1mm/20分度
- 1年前
 fdsa2dfa 共回答了6个问题
fdsa2dfa 共回答了6个问题 |采纳率- 我用了好几年了,你说的不是什么新型的游标卡尺,精度是0.05毫米,很简单的原理
移动n.kmm,这时游标的0刻度线过了主尺的n mm刻度,且游标0.k/m刻度与主尺n+0.k/m刻度对齐。(0.k指小数部分,m指游标卡尺的精度,10分度的为0.1,20分度的为0.05,50分度的为0.02,这种方法对20、50分度的游标卡尺同样适用).... - 1年前
相关推荐
- (2007•泉州)(泉州市)二氧化氯(Cl02)是一种新型自来水消毒剂.下列有关二氧化氯说法错误的是( )
(2007•泉州)(泉州市)二氧化氯(Cl02)是一种新型自来水消毒剂.下列有关二氧化氯说法错误的是( )
A.由氯元素和氧元素组成
B.相对分子质量是67.5
C.是一种氧化物
D.氯氧两元素的质量比是1:2 avaforget1年前1
avaforget1年前1 -
 weiminabc 共回答了17个问题
weiminabc 共回答了17个问题 |采纳率76.5%解题思路:A、由二氧化氯(Cl02)可知该物质的元素的组成;
B、相对分子质量,即各种元素的相对原子质量和的总和;
C、氧化物由两种元素组成,其中一种为氧元素;
D、元素的质量比为各种元素的相对原子质量和的比.由二氧化氯(Cl02)具体分析如下:
A、可知由氯元素和氧元素组成,故A正确;
B、相对分子质量=35.5+16×2=67.5,故B正确;
C、是一种氧化物,它由氯元素和氧元素组成,故C正确;
D、氯氧两元素的质量比=35.5:(16×2)=35.5:32,而1:2为原子个数比,故D错误.
故选D.点评:
本题考点: 化学式的书写及意义;从组成上识别氧化物;有关化学式的计算和推断.
考点点评: 了解化学式的书写及其意义,从组成上识别氧化物;了解有关化学式的计算和推断方法及其技巧.1年前查看全部
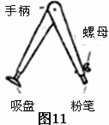
- 如图11是一种新型圆规。它一脚的末端装有吸盘,使用时可将其固定在黑板上,另一脚末端的粉笔通过螺母固定,螺母上刻有细小花纹
如图11是一种新型圆规。它一脚的末端装有吸盘,使用时可将其固定在黑板上,另一脚末端的粉笔通过螺母固定,螺母上刻有细小花纹是为了增大__________,作图时,转动手柄便可在黑板上画出漂亮的圆, 画圆时它是 的(省力/费力),粉笔与黑板间的摩擦是 摩擦(选:滑动、滚动、静)。
、
 阿阳aacc-1688881年前1
阿阳aacc-1688881年前1 -
 喻钊文 共回答了15个问题
喻钊文 共回答了15个问题 |采纳率80%摩擦力,费力,滑动摩擦
分析:(1)摩擦力的概念是:两个互相接触的物体,当它们做相对运动时,在接触面上会产生一种阻碍相对运动的力,这种力就叫摩擦力.根据两个物体的运动情况不同,可将摩擦力分为三种:当一个物体在另一个物体表面滑动时,产生的摩擦力叫滑动摩擦力;当一个物体在另一个物体表面滚动时,产生的摩擦力叫滚动摩擦力;当两个物体未发生相对运动,但有相对运动趋势时,产生的摩擦力叫静摩擦力.抓住物体的运动情况,可判断题目中各属于何种摩擦力.
(2)摩擦力的大小与压力和接触面的粗糙程度有关;
(3)杠杆根据其省力和费力情况,可分为省力杠杆、费力杠杆、等臂杠杆.
(1)螺母上刻有细小花纹是通过增大接触面的粗糙程度来增大摩擦力;
(2)转动手柄便可在黑板上画出漂亮的圆,画圆时动力臂小于阻力臂,故是费力杠杆;
(3)用粉笔在黑板上写字时,粉笔在黑板表面滑动,它们之间间的摩擦是滑动摩擦;
故答案为:(1)摩擦力;(2)费力;(3)滑动.1年前查看全部
- ( )某大型游乐场内的新型滑梯可以等效为
( )某大型游乐场内的新型滑梯可以等效为
某大型游乐场内的新型滑梯可以等效为如图所示的物理模型,一个小朋友在AB段的动摩擦因数μ1<tanθ,BC段的动摩擦因数μ2>tanθ,他从A点开始下滑,滑到C点恰好静止,整个过程中滑梯保持静止状态,则该小朋友从斜面顶端A点滑到底端C点的过程中( )
A.地面对滑梯的摩擦力方向先水平向左,后水平向右
B.地面对滑梯始终无摩擦力作用
C.地面对滑梯的支持力的大小始终等于小朋友和滑梯的总重力的大小
D.地面对滑梯的支持力的大小先小于、后大于小朋友和滑梯的总重力的大小
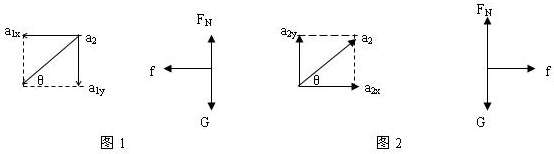
解释上对整体分析的话,有个ab段摩擦力 f 向左,BC段摩擦力向右,但这样有个水平的力系统不就动起来了吗!( 整个过程中滑梯保持静止状态 )那如何理解?. 自由自在071年前2
自由自在071年前2 -
 shz_lwh 共回答了18个问题
shz_lwh 共回答了18个问题 |采纳率77.8%1年前查看全部
- (2012•青州市模拟)某公司向市场投放三种新型产品,经调查发现第一种产品受欢迎的概率为[4/5],第二、第三种产品受欢
(2012•青州市模拟)某公司向市场投放三种新型产品,经调查发现第一种产品受欢迎的概率为[4/5],第二、第三种产品受欢迎的概率分别为p,q(p>q),且不同种产品是否受欢迎相互独立.记ξ为公司向市场投放三种新型产品受欢迎的数量,其分布列为
(1)求该公司至少有一种产品受欢迎的概率;ξ 0 1 2 3 p [2/45] a d [8/45]
(2)求p,q的值;
(3)求数学期望Eξ. wo00001年前1
wo00001年前1 -
 usster 共回答了13个问题
usster 共回答了13个问题 |采纳率84.6%解题思路:设事件Ai表示“该公司第i种产品受欢迎”,i=1,2,3,由题意知P(A1)=[4/5],P(A2)=p,P(A3)=q
(1)求出对立事件“ξ=0”的概率,即可得到该公司至少有一种产品受欢迎的概率;
(2)求出ξ=0,3的概率,利用p+q=1,即可求p,q的值;
(3)求出概率,利用期望公式,即可求得期望.设事件Ai表示“该公司第i种产品受欢迎”,i=1,2,3,由题意知P(A1)=[4/5],P(A2)=p,P(A3)=q
(1)由于事件“该公司至少有一种产品受欢迎”与事件“ξ=0”是对立的,所以该公司至少有一种产品受欢迎的概率是1−P(ξ=0)=1−
2
45=
43
45,
(2)由题意知P(ξ=0)=P(
.
A1
.
A2
.
A3)=
1
5(1−p)(1−q)=
2
45,P(ξ=3)=P(A1A2A3)=[4/5pq=
8
45],整理得pq=
2
9且p+q=1,由p>q,可得p=
2
3,q=
1
3.
(3)由题意知a=P(ξ=1)=[4/5(1−p)(1−q)+
1
5p(1−q)+
1
5(1−p)q=
13
45],
d=P(ξ=2)=1−P(ξ=0)−P(ξ=1)−P(ξ=3)=
22
45
因此Eξ=0×P(ξ=0)+1×P(ξ=1)+2×P(ξ=2)+3×P(ξ=3)=
27
15点评:
本题考点: 离散型随机变量的期望与方差;概率的基本性质;离散型随机变量及其分布列.
考点点评: 本题考查概率的计算,考查数学期望,解题的关键是确定概率,属于中档题.1年前查看全部
- 氯离子插层镁铝水滑石[Mg2Al(OH)6Cl•xH2O]是一种新型离子交换材料,其在高温下完全分解为MgO、Al2O3
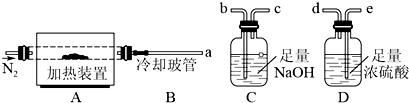
氯离子插层镁铝水滑石[Mg2Al(OH)6Cl•xH2O]是一种新型离子交换材料,其在高温下完全分解为MgO、Al2O3、HCl和水蒸气.冷却玻管B能降低气体的温度,但不能液化水蒸气.现用如图所示装置进行实验确定其化学式(固定装置略去).
(1)Mg2Al(OH)6Cl•xH2O热分解的化学方程式为2[Mg2Al(OH)6Cl•xH2O]
4MgO+Al2O3+2HCl↑+(5+2x)H2O↑高温 .2[Mg2Al(OH)6Cl•xH2O].
4MgO+Al2O3+2HCl↑+(5+2x)H2O↑高温 .
(2)若只通过测定装置C、D的增重来确定x,则装置的连接顺序为______(按气流方向,用接口字母表示),其中C的作用是______.装置连接后,首先要进行的操作的名称是______.
(3)加热前先通N2排尽装置中的空气,称取C、D的初始质量后,再持续通入N2的作用是______、______等.
(4)完全分解后测得C增重3.65g、D增重9.90g,则x=______.若取消冷却玻管B后进行实验,测定的x值将______(填“偏高”或“偏低”). 大头鱼1191年前1
大头鱼1191年前1 -
 zxwcq 共回答了15个问题
zxwcq 共回答了15个问题 |采纳率93.3%解题思路:(1)根据题意:[Mg2Al(OH)6Cl•xH2O]高温下完全分解为MgO、Al2O3、HCl和水蒸气,根据反应物和生成物书写方程式;
(2)应该首先通过D装置吸收水蒸气,后通过C装置吸收HCl;将气体通过洗气瓶进行洗气时,应该从长导管一侧通入气体;
(3)为了避免引起实验误差,保证反应产生的气体全部被装置C、D吸收,所以要通入N2排出装置内残留的气体,同时也是为了防止产生倒吸;
(4)根据反应的方程式计算X的值,若没有冷却玻璃管,由于气温偏高,装置D不能将水蒸汽完全吸收而导致结果偏低.(1)根据题给信息:[Mg2Al(OH)6Cl•xH2O]高温下完全分解为MgO、Al2O3、HCl和水蒸气,可写出其化学方程式:2[Mg2Al(OH)6Cl•xH2O]
高温
.
4MgO+Al2O3+2HCl↑+(5+2x)H2O↑;
(2)装置C的作用是吸收反应生成的HCl气体,装置D的作用是吸收水蒸气,应该首先通过D装置吸收水蒸气,后通过C装置吸收HCl;将气体通过洗气瓶进行洗气时,应该从长导管一侧通入气体,让气体与溶液充分接触反应,故其连接顺序是a→e→d→b;连接好装置后首先应该检查装置的气密性,防止装置漏气,影响测量结果;
(3)因为加热后的装置中含有残留的HCl和水蒸气,为了避免引起实验误差,保证反应产生的气体全部被装置C、D吸收,所以要通入N2排出装置内残留的气体,同时也是为了防止产生倒吸;
将分解产生的气体全部带入装置C、D中完全吸收;防止产生倒吸;
(4)2[Mg2Al(OH)6Cl•xH2O]
高温
.
4MgO+Al2O3+2HCl↑+(5+2x)H2O↑
7318×(5+2x)
3.65g 9.90g
解得x=3,
若没有冷却玻璃管,由于气温偏高,装置D不能将水蒸汽完全吸收而导致结果偏低,
故答案为:(1)2[Mg2Al(OH)6Cl•xH2O]
高温
.
4MgO+Al2O3+2HCl↑+(5+2x)H2O↑;
(2)a→e→d→b;吸收HCl气体;检查装置的气密性;
(3)将分解产生的气体全部带入装置C、D中完全吸收;防止产生倒吸;
(4)3;偏低.点评:
本题考点: 实验探究物质的组成成分以及含量;常见气体的检验与除杂方法;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查化学方程式的书写,对实验装置和实验流程的理解和熟悉实验操作,同时通过计算,确定水分子数.综合性较强,题目难度较大.1年前查看全部
- 两次工业革命所发明了新型交通工具有哪些?
 触动1年前1
触动1年前1 -
 说绍兴方言 共回答了24个问题
说绍兴方言 共回答了24个问题 |采纳率79.2%1885年,德国机械工程师卡尔·本茨制成第一辆汽车,本茨因此被称为“汽车之父”.这种起动方便的汽车有三个轮子,每分钟的转速约二百五十次,时速约十五千米,带有一个用水冷却的单缸发动机,功率为3/4马力,用电点燃.这部汽车使本茨第一个获得汽车专利
20世纪初,美国的莱特兄弟在世界的飞机发展史上做出了重大的贡献.在1903年制造出了第一架依靠自身动力进行载人飞行的飞机“飞行者”1号,并且获得试飞成功.他们因此于1909年获得美国国会荣誉奖.同年,他们创办了“莱特飞机公司”.1年前查看全部
- 据报道,美国夏威夷联合天文中心的科学家探测到宇宙中存在一种新型氢微粒 该微粒由三个氢原子核
据报道,美国夏威夷联合天文中心的科学家探测到宇宙中存在一种新型氢微粒 该微粒由三个氢原子核
(只含质子)和2个电子构成.下列选项正确的是
A.是氢的一种新的同素异形体 B.是氢的一种新的同位素 C.组成可用H3表示
D.比一个普通H2分子多一个氢原子核
答案是D 求解析 丰图蛮蛮1年前1
丰图蛮蛮1年前1 -
 mmmmtt了 共回答了18个问题
mmmmtt了 共回答了18个问题 |采纳率77.8%其实看过后我也比较迷惑,但查过定义后还算是明白了.
A项:同素异形体的定义是是相同元素组成,不同形态的单质,而单质明确规定是由原子组成的.所以,该微粒中有(H+),即使有两个H原子也不能称为是氢的一种新的同素异形体.
B项:同位素是对于原子而言,H的核素有氕、氘、氚,它们互称为同位素,该粒子不是H原子,所以不能称为是氢的一种新的同位素.
C项:因为有质子,带1单位正电,所以应表示为(H3+).
D项:该粒子比氢分子多一个质子,即多一个氢原子核.1年前查看全部
- 随着科技和工农业生产的发展,环境污染日趋严重,已严重威胁到人类的生存.为保护环境,减少对树木的砍伐,一种新型的“石头纸”
随着科技和工农业生产的发展,环境污染日趋严重,已严重威胁到人类的生存.为保护环境,减少对树木的砍伐,一种新型的“石头纸”应运而生.这种纸的主要成分是碳酸钙,外观与普通纸相似.鉴别“石头纸”与普通纸的方法有多种,若分别点燃两种纸,则______是“石头纸”;若要证明石头纸的成分是碳酸盐,则必需的实验操作是______.实验过程中所发生反应的化学方程式为:______;______.
 putong1年前1
putong1年前1 -
 fuying2000 共回答了17个问题
fuying2000 共回答了17个问题 |采纳率100%解题思路:普通纸能燃烧,而“石头纸”不能燃烧;但碳酸盐能与酸反应生成二氧化碳;根据反应原理正确书写化学方程式;普通纸能燃烧,而含碳酸钙的纸不能燃烧;但是“石头纸”是碳酸盐能与酸反应生成使澄清石灰水变浑浊的二氧化碳;
故答案为:不能燃烧的; 取适量石头纸于试管中滴加稀盐酸,将生成气体通入澄清石灰水;CaCO3+2HCl═CaCl2+H2O+CO2↑,
Ca(OH)2+CO2=CaCO3↓+H2O.点评:
本题考点: 证明碳酸盐;书写化学方程式、文字表达式、电离方程式.
考点点评: 了解物质的性质是解答此题的关键,此类题形式新颖,起点高,落脚点低,认真分析题目信息,并结合相关知识分析解答即可.1年前查看全部
- 帮忙翻译一篇摘要~急用本文对不同结构的太阳能集热墙的集热蓄热和通风机理进行了分析,比较它们之间的优缺点,设计了新型结构的
帮忙翻译一篇摘要~急用
本文对不同结构的太阳能集热墙的集热蓄热和通风机理进行了分析,比较它们之间的优缺点,设计了新型结构的太阳能集热墙,在必要假设的条件下建立太阳能集热墙热传递的数学物理模型,利用数值模拟的方法对新型太阳能集热墙的传热性能进行了研究.
研究内容及结论:对太阳能集热墙系统的传热基础理论进行了研究,分析了不同结构的太阳能集热墙的优缺点,分析了太阳能集热墙系统传热过程的影响因素,进而设计了新型结构的太阳能集热墙,建立了新型太阳能集热墙的数学物理模型,并对相关参数进行了确定;对新型太阳能集热墙的空气间层进行了数值模拟,分析了通风口尺寸、集热墙高度及通风口处是否有百叶对集热墙空气间层空气温度和空气流速的影响;针对北方冬季和南方冬季的气候条件,对新型太阳能集热墙体的传热性能进行模拟分析,并针对北方夏季的气候条件,对太阳能集热墙体的夏季通风性能进行模拟分.给出集热墙体温度场、空气间层速度场和出风口的分布图,分析了温度场和速度场的分布规律;对新型太阳能集热墙冬季采暖的日变化情况进行了模拟,给出一天中不同时刻集热墙体的温度场和空气间层速度场的分布图,并给出百叶集热板和出风口平均温度及出风口空气平均流速的变化规律;对新型太阳能集热墙系统采暖房间的温度场进行了模拟,给出室内温度场的分布规律,并对室内温度日变化情况进行了分析,给出室内平均温度的变化规律;用对比分析的方法验证了新型太阳能集热墙的可行性和优越性.
要纯手工翻译的,谢绝用翻译软件翻译的!谢谢 风筝的传说1年前1
风筝的传说1年前1 -
 qinxue1980 共回答了15个问题
qinxue1980 共回答了15个问题 |采纳率93.3%This article on the different structure of solar wall collection hot regenerative heat and ventilation mechanism are analyzed, and the advantages and disadvantages of comparison between them, design the new structure of solar wall, if necessary, under the condition of establishing hypothesis solar wall heat transfer of the physical and mathematical model, the method of numerical simulation of new solar wall of heat and mass transfer properties have been studied.
The research content and conclusion: the solar wall system heat transfer basic theory, the paper analyzes the different structure of solar wall, analyzes the advantages and disadvantages of solar wall system heat transfer process, and then design factors affecting the new structure of solar wall, build a new solar wall of physical and mathematical model, and related parameters were determined, For new solar wall between the air layer is simulated and analyzed vents size, collection hot wall height and vent to inquire whether have shutter collection hot wall between air layer air temperature and velocity of air influence; According to the north and the south in winter winter climate condition, of new solar wall of heat and mass transfer performance is simulated and analyzed, and in the light of the northern summer climate condition, to solar wall summer ventilation performance simulated points. Given collection hot wall temperature field, air between layer velocity field and the outlet, analyzes the distribution of temperature and velocity distribution regularity of, For new solar wall winter heating the diurnal variation condition are simulated, and gives different day moment collection hot wall temperature field and the air layer between the distribution of velocity field, and gives shutter collection hot plate and outlet air outlet average temperature and average flow velocity changes in law; For new solar wall system heating room temperature field simulation, give indoor temperature field distributions, and the indoor temperature, changes are analyzed, the indoor average temperature changes in law; With a contrast analysis method is validated new solar wall is effective and feasible.1年前查看全部
- 目前世界上正在研究一种新型发电机叫磁流体发电机,它可以把气体的内能直接转化为电能.如图所示为它的发电原理图.将一束等离子
 目前世界上正在研究一种新型发电机叫磁流体发电机,它可以把气体的内能直接转化为电能.如图所示为它的发电原理图.将一束等离子体(即高温下电离的气体,含有大量带正电和负电的粒子,从整体上来说呈电中性)喷射入磁感应强度为B的匀强磁场,磁场中有两块面积为S,相距为d的平行金属板与外电阻R相连构成一电路.设气流的速度为v,气体的电导率(电阻率的倒数)为g,则流过外电阻R的电流强度I及电流方向为( )
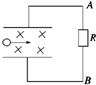
目前世界上正在研究一种新型发电机叫磁流体发电机,它可以把气体的内能直接转化为电能.如图所示为它的发电原理图.将一束等离子体(即高温下电离的气体,含有大量带正电和负电的粒子,从整体上来说呈电中性)喷射入磁感应强度为B的匀强磁场,磁场中有两块面积为S,相距为d的平行金属板与外电阻R相连构成一电路.设气流的速度为v,气体的电导率(电阻率的倒数)为g,则流过外电阻R的电流强度I及电流方向为( )
A.I=[Bdv/R],A→R→B
B.I=[BdvSg/gSR+d],A→R→B
C.I=[Bdv/R],B→R→A
D.I=[BdvS/SR+gd],B→R→A wy4646461年前1
wy4646461年前1 -
 bocai530 共回答了15个问题
bocai530 共回答了15个问题 |采纳率93.3%解题思路:电离的气体含有大量带正电和负电的粒子,进入磁场受洛伦兹力发生偏转,根据左手定则判断出正负电荷的偏转方向,从而确定极板的正负极,确定出电流在外电路中的流向.最终电荷受电场力和洛伦兹力处于平衡,根据平衡求出电动势的大小,从而根据闭合电路欧姆定律求出电流的大小.根据左手定则知正电荷向上偏,负电荷向下偏,上极板带正电,下极板带负电,所以流过外电阻R的电流方向为A→R→B.最终电荷处于平衡有:qvB=q[E/d],解得电动势E=Bdv.内电阻r=ρ
d
S=
d
gs,根据闭合电路欧姆定律有:I=
E
R+r=
Bdv
R+
d
gS=
BdvSg
gSR+d.故B正确,A、C、D错误.
故选B.点评:
本题考点: 霍尔效应及其应用;闭合电路的欧姆定律.
考点点评: 本题综合考查了电阻定律、闭合电路欧姆定律以及磁场的知识,关键掌握左手定则判断洛伦兹力的方向,以及通过平衡求出电源的电动势.1年前查看全部
- 某公路一侧原有路灯106盏,相邻两盏灯的距离为36米,为节约用电,现计划全部更换为新型节能灯,且相邻两盏灯的距离变为70
某公路一侧原有路灯106盏,相邻两盏灯的距离为36米,为节约用电,现计划全部更换为新型节能灯,且相邻两盏灯的距离变为70米,则需更改的新型节能灯有多少盏?(要有过程)
 cffzxs1年前1
cffzxs1年前1 -
 dd13 共回答了1个问题
dd13 共回答了1个问题 |采纳率用106除与701年前查看全部
- 某公司为了开发新产品,用 A 、 B 两种原料各360千克、290千克,试制甲、乙两种新型产品共50件,下表是试验每件新
某公司为了开发新产品,用 A 、 B 两种原料各360千克、290千克,试制甲、乙两种新型产品共50件,下表是试验每件新产品所需原料的相关数据:
(1)设生产甲种产品 x 件,根据题意列出不等式组,求出 x 的取值范围;
A (单位:千克) B (单位:千克) 甲 9 3 乙 4 10
(2)若甲种产品每件成本为70元,乙种产品每件成本为90元,设两种产品的成本总额为 y 元,求出成本总额 y (元)与甲种产品件数 x (件)之间的函数关系式;当甲、乙两种产品各生产多少件时,产品的成本总额最少?并求出最少的成本总额. 海清1年前1
海清1年前1 -
 wjc35 共回答了16个问题
wjc35 共回答了16个问题 |采纳率93.8%1年前查看全部
- 新型纳米材料MFe2Ox(3<x<4)中,M表示+2价的金属元素,在反应中化合价不发生变化.常温下,MFe2Ox能使工业
新型纳米材料MFe2Ox(3<x<4)中,M表示+2价的金属元素,在反应中化合价不发生变化.常温下,MFe2Ox能使工业废气中的SO2转化为S,转化流程如图所示:下列说法中,不正确的是( )

A.SO2是大气污染物
B.SO2是该反应的催化剂
C.x<y
D.Fe在反应前后化合价降低 精灵小飞鼠1年前1
精灵小飞鼠1年前1 -
 天天重名 共回答了28个问题
天天重名 共回答了28个问题 |采纳率85.7%解题思路:A、根据二氧化硫溶入水的性质分析;
B、根据催化剂在化学反应前后性质和质量都不发生变化分析;
C、根据化合价的变化判断反应物在反应中是氧化剂还是还原剂或是催化剂,根据化合价代数和为0判断x与y的关系化合物中各元素化合价的代数和为零分析;
D、根据C选项分析的结论进行解答.A、当二氧化硫溶于水中,会形成亚硫酸(酸雨的主要成分).故SO2是大气污染物.正确;
B、由转化流程图可知,反应前后氧原子的数目改变,SO2转化为S,故可判断SO2参与了反应,所以它不是该反应的催化剂.催化剂是反应前后不会变的物质.故错误;
C、在图示反应中,SO2转化为S,S元素化合价降低,说明SO2在反应中为氧化剂,则MFe2Ox为还原剂,反应后Fe元素的化合价升高,根据化合价代数和,则有(2y-2)>(2x-2),即y>x,故C正确;
D、由C分析可知,在反应前后Fe元素的化合价升高,故该说法错误;
故选BD.点评:
本题考点: 酸雨的产生、危害及防治.
考点点评: 本题主要考查学生根据题目所给的信息和所学的化学知识进行解题的能力,解答时注意根据化合价的变化和化合物化合价代数和为0分析解答问题,要细心分析.1年前查看全部
- 高铁酸钾(K2FeO4)是一种集氧化、吸附、杀菌、灭藻、脱色、除臭等为一的新型高效水处理剂.下列关于该物质的说法正确的是
高铁酸钾(K2FeO4)是一种集氧化、吸附、杀菌、灭藻、脱色、除臭等为一的新型高效水处理剂.下列关于该物质的说法正确的是( )
A.高铁酸钾是由2个钾原子、一个铁原子和4个氧原子构成的
B.高铁酸钾是一种混合物
C.高铁酸钾中含有两种金属元素
D.高铁酸钾分子是由6个原子构成的 qq521425q1年前1
qq521425q1年前1 -
 一定是猪 共回答了16个问题
一定是猪 共回答了16个问题 |采纳率87.5%解题思路:A、根据物质的构成进行分析;
B、根据混合物的概念进行分析;
C、由高铁酸钾的化学式K2FeO4,判断组成元素的种类;
D、根据分子的构成分析.A、宏观物质不能说是由几个原子构成的,应说一个高铁酸钾分子是由2个钾原子、一个铁原子和4个氧原子构成的,故A不正确;
B、根据高铁酸钾是由一种物质组成的,是一种纯净物;故B不正确;
C、根据高铁酸钾的化学式K2FeO4,高铁酸钾由K、Fe、O三种元素组成的化合物,含有两种金属元素;故C正确;
D、一个高铁酸钾分子是由7个原子构成的;故D不正确.
故选:C.点评:
本题考点: 化学式的书写及意义;纯净物和混合物的判别;元素的简单分类.
考点点评: 本题主要考查了物质的分类和化学式的意义,完成此题,可以依据已有的知识进行.1年前查看全部
- 还是用一元一次方程解答,汽车制造厂最近研制出一种耗油低、舒适度好且速度快的新型客车,技术人员做了如下实验:一辆普通客车早
还是用一元一次方程解答,
汽车制造厂最近研制出一种耗油低、舒适度好且速度快的新型客车,技术人员做了如下实验:一辆普通客车早晨5时由A地出发,以每小时60千米的速度开往B地,6时30分这种新型客车也由A地出发开往B地,结果在9时30分追上普通客车,试求这种新型客车的速度 大卡无敌天下1年前5
大卡无敌天下1年前5 -
 2jie12 共回答了22个问题
2jie12 共回答了22个问题 |采纳率95.5%设新车速度为x
60*4.5=3x
x=901年前查看全部
- 甲醇是基础有机化工原料和新型清洁燃料,广泛用于制造各种燃料电池。工业上以甲烷和水蒸气为原料制备甲醇,反应过程如下。
甲醇是基础有机化工原料和新型清洁燃料,广泛用于制造各种燃料电池。工业上以甲烷和水蒸气为原料制备甲醇,反应过程如下。
反应Ⅰ:CH 4 (g)+H 2 O(g) CO(g)+3H 2 (g) △H1
CO(g)+3H 2 (g) △H1
反应Ⅱ:CO(g)+2H 2 (g) CH 3 OH(g) △H2
CH 3 OH(g) △H2
(1)如图是反应1进行过程中的能量变化示意图。根据图象判断,升高温度,反应I的平衡常数将____________ (填“增大”、“减小”或“不变”)。反应I的逆反应的活化能为___________(用含E1、E2的表达式表示)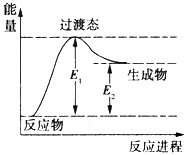
(2)已知在催化剂和一定压强下,反应?能自发进行。若保持容器容积不变,下列措施可增加该反应中CO转化率的是___________(填字母)。
A.适当降低温度
B.将甲醇从反应体系中分离出来
C.充入He,使体系总压强增大
D.按原比例再充入CO和H 2
(3)一种甲醇燃料电池以多孔石墨为电极,一极通入甲醇蒸气,另一极通入氧气,电解质溶液为4L 1 moI/L的KOH溶液。当有3 mol甲醇放电时,电解质溶液中各种离子的浓度由大到小的顺序为_________________
(4)下图甲是一种甲醇燃料电池的结构示意图,甲醇提供质子和电子,电子经外电路到达另一极与氧气反应,电池总反应为2CH 3 OH+3O 2 2CO 2 +4H 2 O。
2CO 2 +4H 2 O。
①M电极的电极反应式为______________________________。
②以上述电池做电源,用乙图所示装置,在实验室中模拟铝制品表面“钝化”处理的过程中,发现Al电极附近逐渐变浑浊并有气泡逸出,原因是(用离子方程式表示):______________。Al电极应接燃料电池的___________(填“M”或“N”)极。 llc4444441年前1
llc4444441年前1 -
 1000712 共回答了29个问题
1000712 共回答了29个问题 |采纳率86.2%1年前查看全部
- 一道物理题离子发动机是一种新型空间发动机,它能给卫星轨道纠偏或调整姿态提供动力,其中有一种离子发动机是让电极发射的电子撞
一道物理题
离子发动机是一种新型空间发动机,它能给卫星轨道纠偏或调整姿态提供动力,其中有一种离子发动机是让电极发射的电子撞击氙原子,使之电离,产生的氙离子经加速电场加速后从尾喷管喷出,从而使卫星获得反冲力,这种发动机通过改变单位时间内喷出离子的数目和速率,能准确获得所需的纠偏动力.假设卫星(连同离子发动机)总质量为M,每个氙离子的质量为m,电量为q,加速电压为U,设卫星原处于静止状态,若要使卫星在离子发动机起动的初始阶段能获得大小为F的动力,则发动机单位时间内应喷出多少个氙离子?此时发动机动发射离子的功率为多大? 4292591701年前1
4292591701年前1 -
 qawsedrf111 共回答了19个问题
qawsedrf111 共回答了19个问题 |采纳率100%跟踪练习第4题有详细答案
【解析】 设离子喷出尾喷管时的速度为v,单位时间内喷出n个离子,则△t时间内喷出离子数为n△t1年前查看全部
- (2014•钦州模拟)“可燃冰”作为新型能源,有着巨大的开发使用潜力.同等条件下,“可燃冰”完全燃烧放出的热量达到煤气的
(2014•钦州模拟)“可燃冰”作为新型能源,有着巨大的开发使用潜力.同等条件下,“可燃冰”完全燃烧放出的热量达到煤气的数十倍,说明“可燃冰”的热值很大.已知q煤气=4.2×107J/kg,若以10倍的关系粗略计算,1kg“可燃冰”完全燃烧放出的热量为______J,这些热量可以使______kg的水从20℃加热至100℃.
 letmesay_21年前1
letmesay_21年前1 -
 海啸猪 共回答了26个问题
海啸猪 共回答了26个问题 |采纳率96.2%∵可燃冰”完全燃烧放出的热量达到煤气的数十倍,
∴“可燃冰”的热值为10q煤气;即q可燃冰=10×4.2×107J/kg=4.2×108J/kg,
则1kg煤气完全燃烧放出的热量:
Q放=m×q可燃冰=1kg×10×4.2×l08J/kg=4.2×l08J,
由题知,Q吸=Q放′=4.2×l08J,
∵Q吸=cm△t,
∴m=
Q吸
c△t=
4.2×108J
4.2×103J/(kg•℃)×(100℃−20℃)=1250kg.
故答案为:4.2×l08;1250.1年前查看全部
- 某道路一侧原有路灯56盏,相邻两盏灯的距离为24米,现计划全部更换为新型的节能灯,且相邻两盏灯的距离变为30米,则需更换
某道路一侧原有路灯56盏,相邻两盏灯的距离为24米,现计划全部更换为新型的节能灯,且相邻两盏灯的距离变为30米,则需更换的新型节能灯有( )
A. 44盏
B. 45盏
C. 46盏
D. 47盏 追名。铁手1年前1
追名。铁手1年前1 -
 燕儿不哭 共回答了16个问题
燕儿不哭 共回答了16个问题 |采纳率75%解题思路:可设需更换的新型节能灯有x盏,根据等量关系:两种安装路灯方式的道路总长相等,列出方程求解即可.设需更换的新型节能灯有x盏,则
30(x-1)=24×(56-1),
30x=1350,
x=45,
则需更换的新型节能灯有45盏.
故选B.点评:
本题考点: 一元一次方程的应用.
考点点评: 本题考查了一元一次方程的应用,解题关键是要读懂题目的意思,根据题目给出的条件,找出合适的等量关系列出方程,再求解.注意根据实际问题采取进1的近似数.1年前查看全部
- (2014•浙江模拟)二甲醚(CH3OCH3)以其优良的性质,被称为21世纪的新型“清洁能源”,在未来可能替代柴油和液化
 (2014•浙江模拟)二甲醚(CH3OCH3)以其优良的性质,被称为21世纪的新型“清洁能源”,在未来可能替代柴油和液化气作为洁净液体燃料使用.工业上以C0和H2为原料生产CH30CH3的新工艺主要发生三个反应:
(2014•浙江模拟)二甲醚(CH3OCH3)以其优良的性质,被称为21世纪的新型“清洁能源”,在未来可能替代柴油和液化气作为洁净液体燃料使用.工业上以C0和H2为原料生产CH30CH3的新工艺主要发生三个反应:
①CO(g)+2H2(g)⇌CH3OH(g)△H1=-91KJ•mol-1
②2CH30H(g)⇌CH30CH3(g)+H20(g)△H2=-24KJ•mol-1
③CO(g)+H2O(g)⇌CO2(g)+H2(g)△H3=-41KJ•mol-1
回答下列问题:
(1)写出新工艺的总反应的热化学方程式:______,平衡常数表达式K=c(CH3OCH3)c(CO2) c3(CO)c3(H2) .c(CH3OCH3)c(CO2) c3(CO)c3(H2)
(2)一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是______(填字母代号).
a.低温高压b.加入催化剂c.减少CO2的浓度d.增加CO的浓度
(3)在某温度下,2L密闭容器中发生反应①,起始时CO、H2的物质的量分别为2mol和6mol,3min后达到平衡,测得CO的转化率为60%,则3min内CO的平均反应速率为______.若同样条件下起始时CO的物质的量为4mol,达到平衡后CH3OH为2.4mol,则起始时H2的物质的量为:______.
(4)某温度下在2L恒容密闭容器中加入CH3OH发生反应②,测得有关数据如下:
则此反应在该温度下的平衡常数为______,若再向容器分别加入甲醇0.02mol、CH3OCH3 1.0mol,此时该反应v正反应______v逆反应(填“>”、“<”或“=”).反应时间/min 0 1 2 3 4 c(CH3OH)/mol•L-1 0.51 0.2 0.1 0.01 0.01
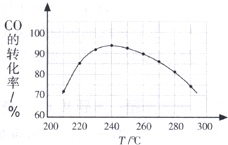
(5)为了寻找合适的反应温度,研究者进行了一系列试验,每次试验保持原料气组成、压强、反应时间等因素不变,试验结果CO转化率随温度变化的规律如图试解释原因是:______. cnlamar1年前1
cnlamar1年前1 -
 xddhh 共回答了7个问题
xddhh 共回答了7个问题 |采纳率85.7%解题思路:(1)根据盖斯定律计算△H;平衡常数指产物浓度系数次幂的乘积与反应物浓度系数次幂的乘积的比值;
(2)要提高CO的转化率,应该不条件平衡正向进行方向判断;
(3)依据化学平衡三段式列式计算,结合平衡常数计算 氢气起始量;
(4)根据表中数据,3分钟后达到平衡状态,计算出该反应的平衡常数;向容器分别加入甲醇0.02mol、CH3OCH31.0mol,重新计算出浓度商,与化学平衡常数对比,判断平衡移动方向;
(5)由图表可知,在较低温时,反应体系均未达到平衡,CO的转化率主要受反应速率影响,随着温度的升高反应速率增大,CO的转化率也增大;在较高温时,反应体系均已达到平衡,随着温度的升高平衡向逆反应方向移动,CO的转化率减小.(1)已知①CO( g)+2H2(g)⇌CH3OH( g)△H1=-91kJ•mol-1,
②2CH30H(g)⇌CH30CH3(g)+H20(g)△H2=-24kJ•mol-1,
③CO(g)+H2O(g)⇌CO2(g)+H2(g)△H3=-41kJ•mol-1,
根据盖斯定律,①×2+②+③得3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g)△H=-247kJ•mol-1,
平衡常数指产物浓度系数次幂的乘积与反应物浓度系数次幂的乘积的比值,所以K=
c(CH3OCH3)c(CO2)
c3(CO)c3(H2);
故答案为:3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g)△H=-247KJ•mol-1,
c(CH3OCH3)c(CO2)
c3(CO)c3(H2);
(2)一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施应使平衡正向进行,3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g)△H=-247KJ•mol-1;
a.反应是气体体积减小的放热反应,低温高压平衡正向进行,一氧化碳转化率增大,故a正确;
b.加入催化剂 改变反应速率不改变化学平衡,一氧化碳转化率不变,故b错误;
c.减少CO2的浓度,平衡正向进行,一氧化碳转化率增大,故c正确;
d.增加CO的浓度,平衡正向进行,一氧化碳转化率减小,故d错误;
故答案为:ac;
(3)在某温度下,2L密闭容器中发生反应①,起始时CO、H2的物质的量分别为2mol和6mol,3min后达到平衡,测得CO的转化率为60%,依据化学平衡三段式列式计算:
CO(g)+2H2(g)⇌CH3OH(g)
起始量(mol/L) 1 3 0
变化量(mol/L) 0.6 0.6 0.2
平衡量(mol/L) 0.4 2.4 0.2
则3min内CO的平均反应速率=[0.6mol/L/3min]=0.2mol/L•min;
若同样条件下起始时CO的物质的量为4mol,达到平衡后CH3OH为2.4mol,设氢气起始量ymol/L
CO(g)+2H2(g)⇌CH3OH(g)
起始量(mol/L)2y 0
变化量(mol/L)1.2 2.4 1.2
平衡量(mol/L) 0.8 y-2.41.2
依据化学平衡常数不变计算得到
1.2
0.8×(y−2.4)2=
0.2
0.4×2.42
y=4.2mol/L;
氢气物质的量为8.4mol
故答案为:0.2 mol•L-1•min-1,8.4 mol;
(4)根据反应方程式:2CH3OH(g)⇌CH3OCH3(g)+H2O(g),
反应前c(CH3OH)/mol•L-1:0.51 0 0
3分钟后达到平衡状态浓度:0.01 0.25 0.25
平衡常数为:
0.25×0.25
0.012=625,
再向容器分别加入甲醇0.02mol、CH3OCH31.0mol反应的浓度商为:
(1.0+0.25)×0.25
0.032≈347.2<625,平衡向着正向移动,正反应速率大于逆反应速率,
故答案为:625;>;
(5)由图表可知,温度低于240℃时,CO的转化率随着温度的升高而增大;温度高于240℃时,CO的转化率随着温度的升高而减小,
在较低温时,各反应体系均未达到平衡,CO的转化率主要受反应速率影响,随着温度的升高反应点评:
本题考点: 化学平衡的计算;热化学方程式;化学平衡的影响因素;化学平衡的调控作用.
考点点评: 本题考查反应热的计算、平衡移动、化学平衡常数等,难度中等,难点在于读图明白温度为240℃时反应体系均已达到平衡.1年前查看全部
- 求出饮料厂可获利润某饮料厂为了开发新产品,用A、B两种果汁原料各19千克、17.2千克,试制甲、乙两种新型饮料共50千克
求出饮料厂可获利润
某饮料厂为了开发新产品,用A、B两种果汁原料各19千克、17.2千克,试制甲、乙两种新型饮料共50千克.甲饮料每千克可获得3元的利润,乙饮料每千克获得2元的利润.甲每千克含A原料0.5千克,含B原料0.3千克.乙每千克含A原料0.2千克,含B原料0.4千克.假设甲种饮料需要配制X千克,请求出饮料厂可获得的最大利润. 893632341年前1
893632341年前1 -
 ustbwht 共回答了28个问题
ustbwht 共回答了28个问题 |采纳率85.7%1:01年前查看全部
- 近几年一种新型的甜味剂“木糖醇”悄悄地走入人们的生活,木糖醇是一种理想的蔗糖代替品,它具有甜味足,溶解性好,防踽齿,适合
近几年一种新型的甜味剂“木糖醇”悄悄地走入人们的生活,木糖醇是一种理想的蔗糖代替品,它具有甜味足,溶解性好,防踽齿,适合糖尿病患者的优点.木糖醇是一种白色粉末状的结晶,结构简式为CH2OH(CHOH)3CH2OH,下列关于木糖醇的叙述中正确的是( )
A.木糖醇不属于糖类
B.木糖醇能跟新制的氢氧化铜浊液反应生成砖红色沉淀
C.它与葡萄糖互为同分异构体
D.可以与乙酸在一定条件下发生酯化反应 浩日1年前1
浩日1年前1 -
 过马路的蛋 共回答了26个问题
过马路的蛋 共回答了26个问题 |采纳率100%解题思路:A.在化学上一般把多羟基醛或多羟基酮或水解后能变成以上两者之一的有机化合物称为糖;
B.能与新制Cu(OH)2悬浊液反应生成红色沉淀的糖类物质中应含有醛基,即为还原性糖;
C.同分异构体是分子式相同,结构不同的化合物;
D.木糖醇含有5个羟基.A.木糖醇结构简式CH2OH(CHOH)3CH2OH,可知木糖醇是一种五元醇,不属于糖类,故A正确;
B.木糖醇不含有醛基,不能与新制的氢氧化铜浊液反应生成红色沉淀,故B错误;
C.木糖醇(CH2OH(CHOH)3CH2OH)与葡萄糖(CH2OH(CHOH)4CHO)分子式不同,不是同分异构体,故C错误;
D.分子中含有羟基,能羧基发生酯化反应,故D正确;
故选AD.点评:
本题考点: 烃的衍生物官能团.
考点点评: 本题考查有机物的结构和性质,为高考常见题型,侧重于考查学生化学知识的应用能力,难度不大,注意把握有机物的结构和官能团的性质1年前查看全部
- 《深圳商报》2004年3月11日报道:近日一种新型太阳能公共卫生间落户北京东郊民巷,该卫生间的能源全部由位于顶部的太阳能
《深圳商报》2004年3月11日报道:近日一种新型太阳能公共卫生间落户北京东郊民巷,该卫生间的能源全部由位于顶部的太阳能电池板提供,它还能将多余的能量储存在蓄电池里.这种能量转化和储存的方式是( )
A. 太阳能转化为内能,再转化为电能
B. 太阳能转化为电能,再转化为化学能
C. 太阳能转化为内能,再转化为化学能
D. 大阳能转化为电能.再转化为光能 河洛风情1年前5
河洛风情1年前5 -
 黯然微哑 共回答了14个问题
黯然微哑 共回答了14个问题 |采纳率92.9%解题思路:能量转化的过程应分成发电和储存电能两部分分析.太阳能电池板发电时是将太阳能转化为电能,多余电能储存在蓄电池中时是将电能转化为化学能.
故选:B.点评:
本题考点: 太阳能的利用.
考点点评: 要注意:蓄电池充电的过程与放电的过程,其能量转化情况刚好相反.1年前查看全部
- 用化学用语填空:(1)1个氧分子______,2个氢原子______,氧化铝______(2)某新型消毒剂由Cl、O两种
用化学用语填空:
(1)1个氧分子______,2个氢原子______,氧化铝______
(2)某新型消毒剂由Cl、O两种元素组成,且每个分子中含有1个Cl原子,2个O原子,该消毒剂的化学式是______. 风-情1年前1
风-情1年前1 -
 zjaklove 共回答了19个问题
zjaklove 共回答了19个问题 |采纳率73.7%(1)根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,因此1个氧分子 表示为:O 2 ;
根据原子的表示方法:用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.因此2个氢原子表示为:2H;
根据化合物化学式的书写步骤:归类→定序→标价→交叉→约简,氧元素的化合价为-2,铝元素的化合价为+3,因此氧化铝的化学式为:Al 2 O 3 ;
(2)根据题意:每个分子中含有1个Cl原子,2个O原子,因此该消毒剂的化学式为:ClO 2 ;
故答案为:
(1)O 2 ,2H,Al 2 O 3 ;
(2)ClO 2 .1年前查看全部
- 高铁电池是一种新型可充电电池,该电池能长时间保持稳定的放电电压。高铁电池的总反应为: 下列判断正确的是 A.充电时阳极反
高铁电池是一种新型可充电电池,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:
 下列判断正确的是
下列判断正确的是A.充电时阳极反应为:2FeO 4 2 - +8H 2 O-6e - =2Fe(OH) 3 +10OH - B.充电时阴极附近溶液的pH变大 C.放电时,负极材料为Zn D.放电时,每转移0.2 mol电子,正极的质量减少6.5 g  landed1年前1
landed1年前1 -
 lzgui 共回答了15个问题
lzgui 共回答了15个问题 |采纳率93.3%BC
该电池放电时,电极反应式为:
负极:3Zn-6e - +6OH - =3Zn(OH) 2
正极:2FeO 4 2- +6e - +8H 2 O=2Fe(OH) 3 +10OH -
该电池充电时,电极反应式为:
阴极:3Zn(OH) 2 +6e - =3Zn+6OH -
阳极:2Fe(OH) 3 +10OH - -6e - =2FeO 4 2- +8H 2 O1年前查看全部
- 英语作文:经过多年艰辛研究,科学家袁隆平发明了新型水稻,这对于解决中国人民的吃饭问题非常有帮助.
英语作文:经过多年艰辛研究,科学家袁隆平发明了新型水稻,这对于解决中国人民的吃饭问题非常有帮助.
1、自我简介 2、表达敬佩 3、请教成功经验 4、说明志向 5、表达祝愿 19822221年前1
19822221年前1 -
 wxandy 共回答了17个问题
wxandy 共回答了17个问题 |采纳率88.2%Yuan Longping (born September 7,1930) is a Chinese agricultural scientist and educator,known for developing the
first hybrid rice varieties in the 1970s.His "hybrid rice" has since been grown in dozens of countries in Africa,America,
and Asia —providing a robust food source in high famine risk areas.
Mr.Yuan won the State Preeminent Science and Technology Award of China in 2000,the Wolf Prize in agriculture
and the World Food Prize in 2004.He is currently is DirectorGeneral of the China National Hybrid Rice R&D Center and
has been appointed as Professor at Hunan Agricultural University,Changsha.He is a member of the Chinese Academy
of Engineering,foreign associate of the US National Academy of Sciences (2006) and the 2006 CPPCC.
Mr.Yuan was born in Beijing,China.He loves playing Majong and the Erhu (Chinese violin),swimming and motorcycling.1年前查看全部
- 三道初二上册物理填空题1 可调光电灯是用一个阻值可以变化的电阻来实现调光的,这个电阻和灯泡应该是( )联的.2 新型的保
三道初二上册物理填空题
1 可调光电灯是用一个阻值可以变化的电阻来实现调光的,这个电阻和灯泡应该是( )联的.
2 新型的保险装置是附加在( )上的,这种开关通常叫( ),当电流过大时会自动断开,俗称( ).
3 在手电筒的完整电路中,干电池的作用是( ),金属外壳相当于( ),其作用是( ),金属外壳上的按钮是一个( ),其作用是( ),小电珠是( ).[我不知道“小电珠”指的是什么] q81727121年前3
q81727121年前3 -
 鬼鬼抽刀 共回答了22个问题
鬼鬼抽刀 共回答了22个问题 |采纳率90.9%串联,
家庭电路,空气开关,跳闸
提供电压(从而提供电流),导线,连接电路,开关,控制电路的闭合与断开,
用电器(就是灯泡)1年前查看全部
- 介绍新型绿色环保可食性包装材料的特性,并按其制备来源进行分类,对其现存问题及发展趋势做了概要阐述
 mayrenyu1年前1
mayrenyu1年前1 -
 天啊怎么回事 共回答了16个问题
天啊怎么回事 共回答了16个问题 |采纳率81.3%随着现代食品工业的发展,食品包装不断更新,一类能完善包装材料的环境保护之间矛盾的新型食品包装技术材料——可食性包装脱颖而出.可食性包装材料是指当包装的功能实现后,该材料可转变为一种动物或人可食用的原料,是一种可实现包装材料功能转型的特殊包装材料.可食性包装材料是一种无废弃物的包装,是一种资源型环保型的包装材料.1年前查看全部
- 一种新型环保电冰箱就是利用环戊烷代替氟里昂进行工作的,如图所示,液态的环戊烷在管子里流动,当它流经冷冻室时就会发生___
 一种新型环保电冰箱就是利用环戊烷代替氟里昂进行工作的,如图所示,液态的环戊烷在管子里流动,当它流经冷冻室时就会发生______现象,吸收热量;接着环戊烷蒸汽在通过冷凝器时又会发生______现象,放出热量.(填物体变化的名称)
一种新型环保电冰箱就是利用环戊烷代替氟里昂进行工作的,如图所示,液态的环戊烷在管子里流动,当它流经冷冻室时就会发生______现象,吸收热量;接着环戊烷蒸汽在通过冷凝器时又会发生______现象,放出热量.(填物体变化的名称)  snrso031年前1
snrso031年前1 -
 花生乐橙搞联合 共回答了20个问题
花生乐橙搞联合 共回答了20个问题 |采纳率90%解题思路:要解决此题,一定要知道汽化过程需要吸收热量,液化是汽化的相反过程,液化过程需要放出热量,而冰箱是用来冷藏食物的,所以结合题意可以得出结论.当电冰箱工作时,制冷剂在冰箱冷冻室内发生汽化而吸热,使冷冻室温度降低;在外面冷凝器中发生液化而放热,将热量散失在空气中.因此制冷剂起到把“热”搬运到冰箱外,使冷冻室长期保持低温.
故答案为:汽化;液化.点评:
本题考点: 汽化及汽化吸热的特点;液化及液化现象.
考点点评: 该题是汽化的实际应用,所以要学会使用物理知识解释生活中的现象,这也是中考时的一个重点.1年前查看全部
- (2014•仪征市二模)活性氧化锌(ZnO) 是一种面向21世纪的新型高功能精细无机产品,近几年有关该物质的制
(2014•仪征市二模)活性氧化锌(ZnO) 是一种面向21世纪的新型高功能精细无机产品,近几年有关该物质的制备成为化工行业研究的热点.某校化学兴趣小组的同学参观了某厂用粗ZnO制备活性ZnO的生产流程,做如下探究.
制备活性氧化锌一种由粗ZnO(含FeO、CuO)制备活性ZnO的流程如图: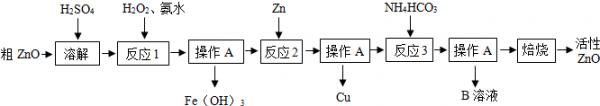
查阅资料:(1)粗ZnO中常含杂质FeO、CuO
(2)反应3是为了制得碱式碳酸锌、碱式碳酸锌经焙烧可制得活性ZnO
(3)已知:几种物质沉淀时的pH如下表:
请问答下列问题:物质 Fe(OH)2 Fe(OH)3 Zn(OH)2 Cu(OH)2 开始沉淀时pH 6.34 1.48 6.2 5.2 完全沉淀时pH 9.7 3.2 8.0 6.4 Fe(OH)2是一种絮状沉淀,不易除去,处理时常将其转化为Fe(OH)3而除去.
(1)溶解前将氧化锌粗品粉碎成细颗粒,目的是______.
(2)写出在粗ZnO样品中加硫酸发生反应的化学方程式______(选写一个).
(3)反应1的目的是将Fe2+氧化为Fe3+,并完全沉淀Fe(OH)3,为了暂不形成Cu(OH)2、Zn (OH)2,该步骤需控制溶液pH的范围是______.
(4)操作A的名称是______,该过程中使用的玻璃仪器有烧杯、______、______.
(5)反应2中加入锌发生的反应属于______反应(填化学反应的基本类型).
(6)B溶液的溶质是(NH4)2SO4,检验其中是否含NH4+的方法为______. Kemissvin1年前1
Kemissvin1年前1 -
 Jim_peng 共回答了18个问题
Jim_peng 共回答了18个问题 |采纳率88.9%解题思路:(1)考虑反应物的接触面积;
(2)考虑ZnO样品与硫酸的反应;
(3)由表格中的数据,推测溶液pH的范围;
(4)操作a是将固体与溶液分离,应采取过滤的方法,过滤所用的主要玻璃仪器有:烧杯、漏斗、玻璃棒;
(5)考虑锌与稀硫酸的反应;
(6)根据氨根与碱反应,生成刺激性气味的气体生成.(1)溶解前将氧化锌粗品粉碎成细颗粒,目的是增大反应物的接触面积或加快溶解速率I制备活性氧化锌.
(2)在粗ZnO样品中加硫酸发生反应的化学方程式 ZnO+H2SO4═ZnSO4+H2O等(写CuO或FeO与硫酸反应也正确);
(3)由表格可知:反应1的目的是将Fe2+氧化为Fe3+,并完全沉淀Fe(OH)3,为了暂不形成Cu(OH)2、Zn (OH)2,该步骤需控制溶液pH的范围是 3.2到5.2;
(4)操作a是将固体与溶液分离,应采取过滤的方法,过滤所用的主要玻璃仪器有:烧杯、漏斗、玻璃棒,故答案为:过滤;烧杯、漏斗、玻璃棒;
(5)反应2中加入锌发生的反应为锌与稀硫酸反应,属于置换反应;
(6)B溶液的溶质是(NH4)2SO4,检验其中是否含NH4+的方法为可加入NaOH浓溶液加热,观察现象,如有刺激性气味的气体生成,则说明含有NH4+,
故答案为:
(1)增大反应物的接触面积或加快溶解速率;
(2)ZnO+H2SO4═Zn SO4+H2O等(写CuO或FeO与硫酸反应也正确);
(3)3.2到5.2;(4)过滤;玻璃棒、漏斗;
(5)置换;(6)可加入NaOH浓溶液加热,观察现象,如有刺激性气味的气体生成,则说明含有NH4+点评:
本题考点: 物质的相互转化和制备;酸的化学性质;盐的化学性质;铵态氮肥的检验;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查学生对工艺流程的理解、阅读获取信息能力、对操作步骤的分析评价、物质的分离提纯、氧化学计算等,是对所学知识的综合运用与能力的考查,需要学生具备扎实的基础知识与综合运用知识、信息进行解决问题的能力.1年前查看全部
- 如图,在新型汽车的研制中,将汽车模型放在风洞中不动,让风高速迎面吹来,通过放在车下测力计(感应压力变化)的示数,可以研究
如图,在新型汽车的研制中,将汽车模型放在风洞中不动,让风高速迎面吹来,通过放在车下测力计(感应压力变化)的示数,可以研究汽车高速行驶的情况,下列说法错误的是()

A.风高速吹来时,车相对地面静止,相对于空气运动 B.风高速吹来时,测力计的示数变大,模型上方气压大,下方气压小 C.车模设计成流线型,可以减小高速运动时空气的阻力 D.这一事例体现了“物体运动和静止的相对性”  Crystal飘1年前1
Crystal飘1年前1 -
 yyy19820101 共回答了12个问题
yyy19820101 共回答了12个问题 |采纳率100%解题思路:当汽车高速行驶时,由于汽车上面的空气流速大,所以压强小,汽车上下面会产生一个压强差,产生一个向上的支持力,所以汽车对测力计的压力减小,
B 错误;此题中让汽车不动,让空气流动,所以体现了运动与静止的相对性。B
1年前查看全部
- (1999•温州)自行车厂今年生产销售一种新型自行车,现向你提供以下有关信息:
(1999•温州)自行车厂今年生产销售一种新型自行车,现向你提供以下有关信息:
(1)该厂去年已备有这种自行车车轮10000只;车轮车间今年平均每月可生产车轮1500只,每辆自行车需装配2只车轮.
(2)该厂装搭车间(自行车最后一道工序的生产车间)每月至少可装搭这种自行车1000辆,但不超过1200辆.
(3)该厂已收到各地客户今年订购这种自行车共14500辆的订货单.
(4)这种自行车出厂销售单价为500元/辆.
设该厂今年这种自行车的销售金额为a万元,请你根据上述信息,判断a的取值范围是______. gw861492841年前1
gw861492841年前1 -
 猫小铺 共回答了16个问题
猫小铺 共回答了16个问题 |采纳率93.8%解题思路:此题主要应求得该厂今年这种自行车的销售量的取值范围.提供了四方面信息:(1)车轮的车库存量及现有的生产能力,(2)装配车间的生产能力,(3)订货量,(4)单价与销售总额.根据(1)知该厂今年的自行车车轮可生产1500×12=18000(只),则今年共有车轮28000只.可以配备14000辆自行车;
根据(2)知该厂今年装搭自行车最少12000辆,最多14400辆.由题意可知,全年共生产车轮1500×12=18000只,再加上原有车轮10000只,共28000只能装配14000辆自行车.根据装配车间的生产能力,全年至少可装配这种自行车12000辆,但不超过14400辆,当然也满足不了订户14500辆的要求.因此,按实际生产要求,该厂今年这种自行车的销售金额a万元应满足:600≤a≤700.
故答案为:600≤a≤700.点评:
本题考点: 一元一次不等式的应用.
考点点评: 解决这类问题的关键是比较生产量与订户量的大小关系,正确理解每一条信息.1年前查看全部
- 2009年12月19日下午,联合国气候变化大会达成《哥本哈根协议》,为减少二氧化碳排放,我国城市公交推出新型节能环保电动
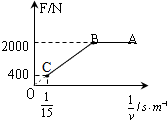
2009年12月19日下午,联合国气候变化大会达成《哥本哈根协议》,为减少二氧化碳排放,我国城市公交推出新型节能环保电动车,在检测某款电动车性能的实验中,质量为8×102kg的电动车由静止开始沿平直公路行驶,达到的最大速度为15m/s,利用传感器测得此过程中不同时刻电动车的牵引力F与对应的速度v,并描绘出F~[1/V]图象(图中AB、BO均为直线),假设电动车行驶中所受的阻力恒定,则( )
 A. 在全过程中,电动车在B点时速度最大
A. 在全过程中,电动车在B点时速度最大
B. BA过程电动车做匀加速运动
C. CB过程电动车作减速运动
D. CB过程电动车的牵引力的功率恒定 Kuai_Q_Sou1年前1
Kuai_Q_Sou1年前1 -
 k4vong 共回答了18个问题
k4vong 共回答了18个问题 |采纳率94.4%解题思路:AB过程牵引力不变,根据牛顿第二定律知,做匀加速直线运动,BC段图线的斜率表示电动车的功率,斜率不变,则功率不变,根据功率与牵引力的关系,判断BC段的运动情况,速度达到最大时,牵引力等于阻力.A、因为横坐标是[1/V],所以全过程中,C点的[1/V]值最小,则速度最大.故A错误.
B、AB段牵引力不变,根据牛顿第二定律知,加速度不变,做匀加速直线运动.故B正确.
C、BC图线的斜率表示电动车的功率,知BC段功率不变,牵引力增大,速度减小,做减速运动.故C,D正确.
故选BCD.点评:
本题考点: 力与运动的关系.
考点点评: 解决本题的关键能够从图线中分析出电动车在整个过程中的运动情况,当牵引力等于阻力时,速度达到最大.1年前查看全部
- 据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:
2CH 3 OH+3O 2 +4OH - 2CO 3 2- +6H 2 O,则下列说法错误的是[ ]
2CO 3 2- +6H 2 O,则下列说法错误的是[ ]A.放电时CH 3 OH参与反应的电极为正极
B.充电时电解质溶液的pH逐渐增大
C.放电时负极的电极反应为:CH 3 OH-6e - +8OH - =CO 3 2- +6H 2 O
D.充电时每生成1mol CH 3 OH转移6mol电子 coangel1年前1
coangel1年前1 -
 poppy05 共回答了10个问题
poppy05 共回答了10个问题 |采纳率90%A1年前查看全部
- 高铁酸钾(K 2 FeO 4 )是一种新型、高效、多功能水处理剂.下列反应可制取K 2 FeO 4 :2Fe(OH) 3
高铁酸钾(K 2 FeO 4 )是一种新型、高效、多功能水处理剂.下列反应可制取K 2 FeO 4 :2Fe(OH) 3 +3Cl 2 +10KOH=2K 2 FeO 4 +6KCl+8H 2 O,对于该反应,下列说法正确的是( ) A.该反应是复分解反应 B.钾元素化合价降低 C.Cl 2 是还原剂 D.Fe(OH) 3 发生氧化反应  正茂ii1年前1
正茂ii1年前1 -
 沙茶牛肉片 共回答了17个问题
沙茶牛肉片 共回答了17个问题 |采纳率94.1%A.Fe和Cl的化合价发生变化,属于氧化还原反应,故A错误;
B.K元素的化合价没有发生变化,故B错误;
C.Cl元素的化合价降低,被还原,Cl 2 是氧化剂,故C错误;
D.Fe元素的化合价升高,被氧化,Fe(OH) 3 发生氧化反应,故D正确.
故选D.1年前查看全部
- 某新型电视机商场按成本价的25%加价,为了吸引顾客,采取降价10%实施降价,结果商场仍获利800元,这种品牌
某新型电视机商场按成本价的25%加价,为了吸引顾客,采取降价10%实施降价,结果商场仍获利800元,这种品牌
电视机成本价多少元?
(光写结果的不给分,写详细过程的加5分,照抄的不采纳) 87115511年前1
87115511年前1 -
 魚絲 共回答了9个问题
魚絲 共回答了9个问题 |采纳率100%设这种品牌电视机成本价x元.
(1+25%)x*(1-10%)-x=800
1.25x*0.9-x=800
1.125x-x=800
0.125x=800
x=64001年前查看全部
- “火立熄”是一种新型的家用灭火用品.“火立熄”接触到火焰3~5秒后炸开,释放的粉末覆盖在可燃物上,同时放出不可燃气体,使
“火立熄”是一种新型的家用灭火用品.“火立熄”接触到火焰3~5秒后炸开,释放的粉末覆盖在可燃物上,同时放出不可燃气体,使火焰熄灭.其灭火原理是( ) A.清除可燃物 B.使可燃物与氧气隔绝 C.降低了可燃物的着火点 D.使温度降低到着火点以下  dfbggfhnjg1年前1
dfbggfhnjg1年前1 -
 胡桃夹梓 共回答了13个问题
胡桃夹梓 共回答了13个问题 |采纳率84.6%.“火立熄”接触到火焰3-5秒后炸开,释放的粉末覆盖在燃烧物上,这样就使可燃物与氧气隔绝,使火焰熄灭.
故选B.1年前查看全部
- 可燃冰是一种新型燃料.他是------和-------在低温高压下混合产生的晶体状物质?
可燃冰是一种新型燃料.他是------和-------在低温高压下混合产生的晶体状物质?
1.水 2.一氧化碳 3.二氧化碳 4.天然气
它是在( )和( )在低温高压下混合产生的晶体状物质? doremi9131年前1
doremi9131年前1 -
 piaobo879 共回答了18个问题
piaobo879 共回答了18个问题 |采纳率83.3%水和天气气1年前查看全部
- (2012•永州)ClO2是新型的饮用水消毒剂.如图是制取ClO2的化学反应微观过程图(表示氯原子,表示钠原子,○表示氧
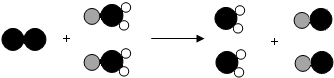 (2012•永州)ClO2是新型的饮用水消毒剂.如图是制取ClO2的化学反应微观过程图(
(2012•永州)ClO2是新型的饮用水消毒剂.如图是制取ClO2的化学反应微观过程图( 表示氯原子,
表示氯原子, 表示钠原子,○表示氧原子),你认为下列从中获取的信息错误的是( )
表示钠原子,○表示氧原子),你认为下列从中获取的信息错误的是( )
A.分子在化学变化中可以再分
B.氧原子的数目在反应前后不变
C.反应中只有一种物质是单质
D.可推出 的化学式为H2O
的化学式为H2O  Baby_Lily1年前1
Baby_Lily1年前1 -
 狂奔乱舞 共回答了14个问题
狂奔乱舞 共回答了14个问题 |采纳率78.6%解题思路:根据微观示意图可知反应的方程式为:Cl2+2NaClO2=2ClO2+2NaCl,分析微粒的变化:分子的种类发生了改变,原子的种类和个数都不变,Cl2属于单质等.A、由微观示意图可知:Cl2经过变化变成了新的分子ClO2;故说法正确;
B、由微观示意图可知:氧原子在反应前后的个数都是4个;故说法正确;
C、Cl2、NaClO2、ClO2、NaCl四种物质中只有Cl2是由一种元素组成的纯净物,属于单质,故说法正确;
D、根据 表示氯原子,○表示氧原子,因此
表示氯原子,○表示氧原子,因此 表示ClO2;故说法错误;
表示ClO2;故说法错误;
故选项为:D.点评:
本题考点: 微粒观点及模型图的应用;单质和化合物的判别.
考点点评: 本题主要考查了在化学变化中分子和原子的关系及其物质的分类方面的知识,可以依据质量守恒定律、分子和原子的区别及物质的微观结构结合图示进行分析.1年前查看全部
- 在新型汽车的研制中,将汽车模型放在风洞中不动,让风迎面吹来,可研究汽车高速行驶的情况,说汽车高速行驶是以______为参
 在新型汽车的研制中,将汽车模型放在风洞中不动,让风迎面吹来,可研究汽车高速行驶的情况,说汽车高速行驶是以______为参照物.此时汽车模型对地面的压力______它的重力(填“大于”、“等于”或“小于”)
在新型汽车的研制中,将汽车模型放在风洞中不动,让风迎面吹来,可研究汽车高速行驶的情况,说汽车高速行驶是以______为参照物.此时汽车模型对地面的压力______它的重力(填“大于”、“等于”或“小于”)  珑玲小桃1年前1
珑玲小桃1年前1 -
 小魔女妖妖耶 共回答了24个问题
小魔女妖妖耶 共回答了24个问题 |采纳率87.5%解题思路:(1)研究物体的运动情况时,首先要选取一个物体作为标准,这个被选作标准的物体叫做参照物.研究对象的运动情况是怎样的,就看它与参照物的相对位置是否变化.
(2)流体压强和流速的关系是:流体流速大的地方,压强小;流体流速小的地方,压强大;风高速吹来时,车相对地面的位置没有发生改变,所以是相对静止的;车相对于流动空气的位置发生了改变,所以是运动的;
风高速吹来时,由于此时汽车上面的空气流速大,故压强小,车下方的空气流速小,压强大,所以此时汽车受到向上的升力;对地面的压力小于自身的重力.
故答案为:流动的空气;小于.点评:
本题考点: 参照物及其选择;气体压强跟体积的关系.
考点点评: 知道运动和静止的相对性,并熟悉流体压强和流速的关系是解决该题的关键.1年前查看全部
- 一家拥有自主知识产权的汽车制造厂,去年生产了一种新型轿车15000辆,由于销路很好,今年他们计划将产量提高7/20,今年
一家拥有自主知识产权的汽车制造厂,去年生产了一种新型轿车15000辆,由于销路很好,今年他们计划将产量提高7/20,今年计划生产这种轿车多少辆?
 gaswoo1年前1
gaswoo1年前1 -
 赵米拉 共回答了24个问题
赵米拉 共回答了24个问题 |采纳率95.8%15000x(1+7/20)得数自己算吧~1年前查看全部
- 某道路一侧原有路灯106盏,相邻两盏灯的距离为36米,现计划全部更换为新型的节能灯,且相邻两盏灯的距离变为70米,则需更
某道路一侧原有路灯106盏,相邻两盏灯的距离为36米,现计划全部更换为新型的节能灯,且相邻两盏灯的距离变为70米,则需更换的新型节能灯有( )
A. 54盏
B. 55盏
C. 56盏
D. 57盏 df4sd1年前4
df4sd1年前4 -
 gyysy 共回答了21个问题
gyysy 共回答了21个问题 |采纳率76.2%解题思路:可设需更换的新型节能灯有x盏,根据等量关系:两种安装路灯方式的道路总长相等,列出方程求解即可.设需更换的新型节能灯有x盏,则
70(x-1)=36×(106-1),
70x=3850,
x=55,
则需更换的新型节能灯有55盏.
故选B.点评:
本题考点: 一元一次方程的应用.
考点点评: 本题考查了一元一次方程的应用,解题关键是要读懂题目的意思,根据题目给出的条件,找出合适的等量关系列出方程,再求解.注意根据实际问题采取进1的近似数.1年前查看全部
- (2013•邵阳)N(NO2)3是科学家2011年发现的一种新型火箭燃料.试计算:
(2013•邵阳)N(NO2)3是科学家2011年发现的一种新型火箭燃料.试计算:
(1)1个N(NO2)3分子中含______个原子.
(2)N(NO2)3的相对分子质量是______.
(3)N(NO2)3中氮元素和氧元素的质量比是______.(化为最简整数比)
(4)N(NO2)3中氮元素的质量分数是______.(精确到0.1%) vt_vanas1年前1
vt_vanas1年前1 -
 WEBBER2891 共回答了18个问题
WEBBER2891 共回答了18个问题 |采纳率94.4%解题思路:(1)根据分子的构成分析;
(2)根据物质的相对分子质量为组成分子的各原子的相对原子质量之和解决;
(3)依据元素的质量比等于各元素相对原子质量和的比分析解答即可;
(4)根据化合物中元素的质量分数[相对原子质量×原子个数/相对分子质量]×100%,进行分析判断.(1)1个N(NO2)3分子中含有的原子个数为1+(1+2)×3=10.
(2)N(NO2)3的相对分子质量为14+(14+16×2)×3=152.
(3)依据元素的质量比等于各元素相对原子质量和的比,所以N(NO2)3中氮元素和氧元素的质量比是14×4:16×6=7:12;
(4)N(NO2)3中氮元素的质量分数为[14×4/152]×100%≈36.8%.
故答案为:(1)10;(2)152;(3)7:12;(4)36.8%;点评:
本题考点: 相对分子质量的概念及其计算;元素质量比的计算;元素的质量分数计算.
考点点评: 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义、有关计算进行分析问题、解决问题的能力.1年前查看全部
- 如图所示是我市部分中小学投入使用的新型安全校车,这种校车的性能完全符合校车12项安全标准.中考期间,××中学的学生乘坐这
如图所示是我市部分中小学投入使用的新型安全校车,这种校车的性能完全符合校车12项安全标准.中考期间,××中学的学生乘坐这种新型安全校车到9km外的考点参加考试,校车行驶了15min后安全到达考点.求:

(1)校车在送考过程中的平均速度;
(2)若校车和学生总质量为9000kg,车轮与地面的接触总面积为0.15m2,求校车对水平路面的压强;
(3)若校车以12m/s的速度在一段平直路面是匀速行驶,校车受到的牵引力是4500N,求校车发动机牵引力的功率. pw381年前1
pw381年前1 -
 vivi_8170 共回答了13个问题
vivi_8170 共回答了13个问题 |采纳率84.6%解题思路:(1)已知校车的行驶的距离和时间,根据速度公式求出平均速度;
(2)校车对水平面上的压力和自身的重力相等,根据G=mg求出其大小,再根据压强公式求出对水平路面的压强;
(3)根据P=Fv求出校车发动机牵引力的功率.(1)校车在送考过程中的平均速度:
v=[s/t]=[9km
15/60h]=36km/h;
(2)校车对水平路面的压力:
F=G=mg=9000kg×10N/kg=90000N,
校车对水平路面的压强:
p=[F/s]=
90000N
0.15m2=6×105Pa;
(3)校车发动机牵引力的功率:
P=F牵v=4500N×12m/s=5.4×104W.
答:(1)校车在送考过程中的平均速度为36km/h;
(2)校车对水平路面的压强6×105Pa;
(3)校车发动机牵引力的功率为5.4×104W.点评:
本题考点: 压强的大小及其计算;变速运动与平均速度;功率的计算.
考点点评: 本题考查了速度、压强、功率的计算,关键是公式和规律的灵活运用以及知道水平面上物体的压力和自身的重力相等.计算过程要注意单位的换算.1年前查看全部
- 阅读材料,回答下列问题.生态旅游农业是以农业生产为依托,开发具有旅游价值的农业资源、农产品、田园风光,是一种新型的“农业
阅读材料,回答下列问题.
生态旅游农业是以农业生产为依托,开发具有旅游价值的农业资源、农产品、田园风光,是一种新型的“农业+旅游业”性质的生态农业模式,也是一种新型园林形式一一观光农业的形式.山区因其特殊的地形地貌,发展生态农业有良好的资源基础,可以在荒山上种植各种果树和茶叶,培育园林绿化树种、花卉、盆景,还可以在房前屋后、塑料大棚中种植各种瓜果、蔬菜.不施用农药和化肥,适当增施有机肥,可种出无毒无害的农产品.每当春暖花开之时、或是硕果累累的秋天,游人如织,游玩采摘尽兴之后,还有无公害绿色食品享用,深受都市人青睐.
(1)步人生态园区,会被塑料大棚中的反季节蔬菜所吸引.清你从有利于种子萌发、植株生长的角度考虑,冬天和早春塑料大棚的主要作用是______.大棚中施加有机肥,可适当提高棚内二氧化碳的含量,从而提高了蔬菜______作用的效率,提高了农产品的产量.夜间适当降低大棚内温度,可抑制蔬菜的______作用,减少有机物的消耗.
(2)想感受清新的空气,请到生态园区来.这里有最大的“空气净化器”一一绿色植物,能很好的维持生物圈中的______
(3)来到盆景花卉区,你会被这里的美景迷住.一位游客忍不住在桅子树上剪下一段带叶的枝条,先将其插在稀释的红墨水中,再把装置放在阳光下照晒至叶脉微红,最后将枝条纵向切开,观察到只______被染红,说明水分和无机盐是通过______来运输的.由此他联想到植物在开花结果期间需水量增大,吸收作用加强,此时所吸收的水分将主要用于植物的______作用
(4)据了解,该生态园内的树木、花卉、盆景只能适度出售并及时补种,以防原有生态系统的______被破坏. 拜托别想那么多1年前1
拜托别想那么多1年前1 -
 li23_00 共回答了18个问题
li23_00 共回答了18个问题 |采纳率88.9%(1)、冬天和早春塑料大棚的主要作用是保温,光合作用是指植物在光下在叶绿体里把二氧化碳和水合成有机物的过程,呼吸作用是植物在线粒体里分解有机物释放能量的过程,要想提高产量就要想办法促进光合作用抑制呼吸作用,让合成的有机物多而分解的少,就会有更多的有机物剩余,就会增产.大棚中施加有机肥,可适当提高棚内二氧化碳的含量促进光合作用合成更多的有机物,温度影响生物的生命活动,夜晚适当降温可以抑制其呼吸作用,使其分解的有机物少.使更多的有机物得以积累.进而增产.
(2)绿色植物通过光合作用,还能够不断消耗大气中的二氧化碳气体,制造氧气排到大气中,维持生物圈中的碳-氧平衡,从而为人类和一切需氧生物的生存创造了必要条件.因此,我们把绿色植物称为“空气净化器”.
(3)植物吸收水分的主要器官是根.茎中有输导组织是植物体内担负物质长途运输的组织,由管状细胞上、下相连而成,贯穿于植物体各个器官内.输导组织根据其构造和功能的不同,分为两类. 导管:导管的主要功能是自下而上运输水和无机盐.筛管:筛管的主要功能是自上而下运输有机物质.我们知道根吸收的水分绝大部分用于蒸腾作用由气孔散失,只用很少部分用于光合作用制造有机物.
(4)在一般情况下,生态系统中各种生物的数量和所占的比例总是维持在相对稳定的.这说明生态系统具有一定的自动调节能力,但这种自动调节能力有一定限度,当人为的或自然因素的干扰超过了这种限度时,生态系统就会遭到破坏.
故答案为:
(1)保温;光合呼吸
(2)碳一氧平衡
(3)木质部;导管;(或木质部中的导管,只填“木质部”不得分)蒸腾
(4)稳定性1年前查看全部
- 手机中使用的锂(Li)电池是新型的高能电池.它的原子结构示意图为锂是一种活动性比铁强的金属.
手机中使用的锂(Li)电池是新型的高能电池.它的原子结构示意图为
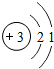 锂是一种活动性比铁强的金属.
锂是一种活动性比铁强的金属.
(1)写出锂离子的符号______;锂的氧化物的化学式为______.
(2)写出锂与稀硫酸反应的化学方程式______. rlbk1年前1
rlbk1年前1 -
 洗澡鱼 共回答了20个问题
洗澡鱼 共回答了20个问题 |采纳率95%解题思路:(1)根据锂的原子结构示意图可知,其最外层电子数为1,在化学反应中易失去1个电子而形成带1个单位正电荷的阳离子;根据元素的正化合价数等于其原子的最外层电子数,氧元素显-2价,写出其氧化物的化学式即可.
(2)锂是一种活动性比铁强的金属,锂与稀硫酸反应生成硫酸锂和氢气,写出反应的化学方程式即可.(1)由锂的原子结构示意图可知,其最外层电子数为1,在化学反应中易失去1个电子而形成带1个单位正电荷的阳离子,锂离子的符号为:.元素的正化合价数等于其原子的最外层电子数,锂元素显+1价,氧元素显-2价,其化学...
点评:
本题考点: 化学符号及其周围数字的意义;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,掌握原子结构示意图的含义、离子符号、化学式与化学方程式的书写是正确解答本题的关键.1年前查看全部
- 某公司计划一年度生产一种新型计算机,下面是各部门提供数据:
某公司计划一年度生产一种新型计算机,下面是各部门提供数据:
人事部:明年生产工人不多于80人,每人每年按2400工时计算;
市场部:预测明年销售量至少为10000台;
技术部:生产一台计算机,平均要用12个工时,每台机器需要安装5个主要部件;供应部:今年年终将库存主要部件2000件,明年还能采购到此种部件80000件.根据上述信息,试判断明年该公司的生产量可能是多少
 自信才快乐1年前1
自信才快乐1年前1 -
 一路阳光灿烂 共回答了26个问题
一路阳光灿烂 共回答了26个问题 |采纳率88.5%可生产台数为x,则约束条件如下:
营销部:x>=10000
技术部和人事部:12x=1年前查看全部
- 1.某新型胃药的一个分子中含有5个氮原子,氮元素的质量分数约为16.5%,求该胃药的相对分子质量?
1.某新型胃药的一个分子中含有5个氮原子,氮元素的质量分数约为16.5%,求该胃药的相对分子质量?
2.在化合物A2BO4中,A元素的质量分数为39.6%,氧元素的质量分数为32.49%,求该化合物的相对分子质量和A和B的相对原子质量?
3.3.2克金属M,在氢气中燃烧后生成4克MO,求金属M的相对原子质量?
4.血红蛋白的相对分子质量为68000,含铁元素的质量分数为0.33%,求平均每个血红蛋白分子中的铁原子个数? lingtingxinyu1年前1
lingtingxinyu1年前1 -
 showshin 共回答了28个问题
showshin 共回答了28个问题 |采纳率92.9%1、5个N,总相对原子质量=70,质量分数16.5%,则该分子的相对分子质量=70/16.5%=424
2、A2BO4中,O的总相对原子质量=64,质量分数32.49%,则化合物相对分子质量=64/32.49%=197,2个A原子的总相对原子质量=197*39.6%=78,则一个A原子的相对原子质量=39.B的相对原子质量=197-64-78=56
3、燃烧方程是:2M+O2===2MO
2x 2(x+16)
3.2 4
x=64
4、铁的总相对原子质量=68000*0.33%=224,个数=224//56=41年前查看全部
- 某电子厂准备投产一种新型电视机,计划两年后使成本降低27.75%,问每年平均要降低成本多少
 bitylxw1年前2
bitylxw1年前2 -
 激流永注 共回答了23个问题
激流永注 共回答了23个问题 |采纳率78.3%15%.
设每年降低x,
(1-x)(1-x)=1-0.2775
1-x=0.85
x=0.151年前查看全部
大家在问
- 1比较4a^2-2a与2a-5的大小
- 2200的2011次方减200的2010次方再减200的2009次方.以此类推减至200的1次方,求此题解答过程与思路..
- 3the library is __ from of there
- 4“仰宇宙之无穷,俯究万类之运动,观古今之须臾,抚四海之一瞬”的含义
- 5函数f(x)的定义域为R,并对切实数x都满足f(2+x)=f(2-x).1)函数y=f(x)的图象关于直线x=2对称.
- 6求教,CAD图中上面一个三角形下面一个圆里面还有字母和数字代表什么?
- 7最高深的问题是没有问题,和没有问题才是最大的问题,这两种说法是不是相互矛盾啊?
- 8怎么临时考好初一语文基础题?我说的是语文试卷的基础部分啊,我的阅读、作文都很好,关键是基础题丢的分最多,现在还有3星期了
- 9请问用NaOH固体吸水后会风化吗?
- 10急求,初三化学公式,都有什么!
- 11我一直搞不清楚吸水的是NaOH固体还是溶液还是均可 能与CO2反应的是NaOH固体还是溶液还是均可?
- 12某物体从上午7时至下午4时的温度与时间关系为m=t的三次幂-5t+100(t=0表示中午12时,t=1表示下午1是).则
- 13()关于生物的这个字怎么解释!蛋白质分解为低分子肽、( )及氨基酸等,()那个字好像打不出来耶,查现代汉语字典也没这个字
- 14幂级数求和:0到正无穷An*X^n=A0+A1*X+A2*X^2+…+…对吗,请赐教多谢
- 15为什么幂级数求和都要确定一个S(0)呢