2NA2O2+2CO2----2NA2CO3+O2 为什么放热啊?
 hongsheng782022-10-04 11:39:541条回答
hongsheng782022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 fengye216 共回答了15个问题
fengye216 共回答了15个问题 |采纳率93.3%- 这需要从多个方面来解释
其实从化学键角度解释最好也最常用
估计你在中学部分才会问这个问题 你可以理解为NA2O2的化学键能 尤其是O22-离子的键能相当的高,而NA2CO3中CO32-和O2的键能都不是很高 由能量守恒定律知道 能量不可能凭空产生也不能凭空消失 由键能高的物质变化为键能低的物质,必然释放能量 即放热
键能高是因为物质不稳定 而稳定的物质键能不必抬高也能由于原子间的作用而“主动”结合在一起
这样是不是好理解些? - 1年前
相关推荐
- (2013•怀柔区二模)潜艇中船员呼吸产生的二氧化碳能通过化学反应2Na2O2+2CO2═2X+O2吸收,则X的化学式为
(2013•怀柔区二模)潜艇中船员呼吸产生的二氧化碳能通过化学反应2Na2O2+2CO2═2X+O2吸收,则X的化学式为( )
A.NaOH
B.Na2C
C.Na2CO2
D.Na2CO3 jarh1年前1
jarh1年前1 -
 茗古屋 共回答了20个问题
茗古屋 共回答了20个问题 |采纳率95%解题思路:根据质量守恒定律:在化学反应中,反应前后原子的种类没有改变,数目没有增减,进行解答本题.根据质量守恒定律:在化学反应中,反应前后原子的种类没有改变,数目没有增减,可推断化学反应2Na2O2+2CO2=2X+O2 中X为Na2CO3,故选D.
点评:
本题考点: 有关化学式的计算和推断.
考点点评: 本题考查学生对质量守恒定律的理解与掌握,并能在解题中灵活应用的能力.1年前查看全部
- 2Na2O2+2CO2═2Na2CO3+O2 1摩尔二氧化碳参与反应电子转移怎么算
 至西汉入朝1年前1
至西汉入朝1年前1 -
 Vampire-1943 共回答了17个问题
Vampire-1943 共回答了17个问题 |采纳率94.1%一摩尔二氧化碳反应实质上就是告诉你一摩尔过氧化钠参与反应,该反应是歧化反应,转移一摩尔电子1年前查看全部
- (2013•虹口区二模)飞船常利用反应2Na2O2+2CO2═2X+O2来提供氧气,“X”的化学式是( )
(2013•虹口区二模)飞船常利用反应2Na2O2+2CO2═2X+O2来提供氧气,“X”的化学式是( )
A.CO
B.Na2O
C.NaOH
D.Na2CO3 Shygirl1年前1
Shygirl1年前1 -
 失意文人 共回答了16个问题
失意文人 共回答了16个问题 |采纳率93.8%解题思路:根据质量守恒定律的实质,化学反应前后原子的种类和数目不变求出化学式.假设横线上的物质为x,据质量守恒定律,在反应前后各元素原子的个数不变.从2Na2O2+2CO2=2x+O2看,钠原子反应前共有4个,反应后除x外没有,所以2x中有4个,从而x中有2个钠原子;氧原子反应前共有8个,反应后除x外有2个,故2x里有6个,从而得出x里有3个;碳原子反应前有2个,反应后除x外没有,故2x里有2个,从而得出x里有1个碳原子,所以x为Na2CO3.
故选D.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 在推断物质的化学式时,一定要注意x前是否有化学计量数.1年前查看全部
- 有许多氧化物在一定条件下都能与Na2O2反应,且反应极有规律.如2Na2O2+2CO2═2Na2CO3+O2,2Na2O
有许多氧化物在一定条件下都能与Na2O2反应,且反应极有规律.如2Na2O2+2CO2═2Na2CO3+O2,2Na2O2+2SO3═2Na2SO4+O2.据此,你认为下列反应方程式中正确的是( )
A.2Na2O2+2SO2═2Na2SO3+O2
B.Na2O2+2NO2═2NaNO2+O2
C.4Na2O2+2Mn2O7═4Na2MnO4+3O2
D.2Na2O2+2N2O5═4NaNO3+O2 田野19741年前1
田野19741年前1 -
 wolf_2000 共回答了15个问题
wolf_2000 共回答了15个问题 |采纳率86.7%解题思路:依据所给的例子可以知道:当过氧化钠与最高价态的氧化物反应生成该元素的最高价态的含氧酸盐和氧气.A、二氧化硫是低价态的硫的氧化物,不符合上述规律,故A错误;
B、二氧化氮是低价态的氮的氧化物,不符合上述规律,故B错误;
C、七氧化二锰是最高价态的锰的氧化物,但Na2MnO4中的锰为+6价,不符合上述规律,故C错误;
D、五氧化二氮是最高价态的氮的氧化物,因此过氧化钠与五氧化二氮反应生成硝酸钠和氧气,故D正确;
故选:D.点评:
本题考点: 钠的重要化合物.
考点点评: 本题根据题目信息得出规律,主要考查化学方程式的书写,难度较大.1年前查看全部
- 2na2o2+2co2 → 2na2co3+o2 哪个是氧化剂哪个是还原剂?
 边缘人¥1年前1
边缘人¥1年前1 -
 gyuue 共回答了20个问题
gyuue 共回答了20个问题 |采纳率95%Na2O2即是还原剂又是氧化剂,Na2O2自身发生氧化还原反应.
Na2O2中一个O化合价升高变成O2中的O,另一个O化合价降低生成Na2CO3中的O1年前查看全部
- 过氧化钠(Na2O2)是一种淡黄色粉末,在通常情况下能跟CO2、H2O、HCl发生反应:2Na2O2+2CO2═2Na2
过氧化钠(Na2O2)是一种淡黄色粉末,在通常情况下能跟CO2、H2O、HCl发生反应:2Na2O2+2CO2═2Na2CO3+O2↑,2Na2O2+2H2O═4NaOH+O2↑,2Na2O2+4HCl═4NaCl+2H2O+O2↑;为了验证CO2跟Na2O2反应产生的气体是O2,某同学设计了如图所示的实验装置.
试回答列问题: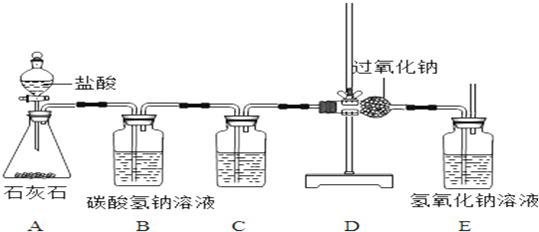
(1)设计B、C装置的目的是净化CO2气体.其中B装置的作用是______;C装置的作用是______,瓶内的液体是______;如果将B、C两瓶内的液体互换,其后果是______.
(2)E装置中氢氧化钠溶液的作用是吸收没有反应的CO2,所发生反应的化学方程式是______.
(3)为了验证CO2和Na2O2反应产生的气体是O2,最后还要进行的操作是______;观察到的现象是______. 3xiazhu1年前1
3xiazhu1年前1 -
 faming110 共回答了14个问题
faming110 共回答了14个问题 |采纳率85.7%解题思路:(1)从题目的信息可以看出:过氧化钠能够和能跟CO2、H2O、HCl发生反应,所以要证明过氧化钠和二氧化碳反应,就要除去混合气体中的水分和氯化氢气体去分析;
(2)从氢氧化钠溶液和CO2反应生成碳酸钠和水去分析;
(3)从氧气具有助燃性去分析.(1)由题目的信息可以看出:过氧化钠能够和能跟CO2、H2O、HCl发生反应,所以要证明过氧化钠和二氧化碳反应,就要除去混合气体中的水分和氯化氢气体.碳酸氢钠溶液和氯化氢反应,不和二氧化碳反应,所以B装置可除去混合气体中的氯化氢气体;所以C装置的作用是除去水分,浓硫酸具有吸水性,可做干燥剂;如果将B、C两瓶内的液体互换,由于B瓶中含有水分,会导致二氧化碳气体中混进水分;
故答案为:除去气体中氯化氢气体 除去水分浓硫酸不能除去气体中的水分;
(2)氢氧化钠溶液和CO2反应生成碳酸钠和水,所发生反应的化学方程式是:2NaOH+CO2═Na2CO3+H2O;故答案为:2NaOH+CO2═Na2CO3+H2O;
(3)由于氧气具有助燃性,所以氧气的检验方法是:用带火星的木条放在E中导管口,如果复燃,证明是氧气;故答案为:用带火星的木条放在E中导管口 带火星的木条复燃.点评:
本题考点: 实验探究物质的性质或变化规律;常见气体的检验与除杂方法;盐的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题综合性较强,考查学生对从题目中获取信息并对所获信息的理解与应用及灵活运用进行分析问题、解决问题的能力.1年前查看全部
- 过氧化钠(Na2O2)在常温下能与人呼出的二氧化碳反应生成氧气,化学方程式为:2Na2O2+2CO2═2Na2CO3+O
过氧化钠(Na2O2)在常温下能与人呼出的二氧化碳反应生成氧气,化学方程式为:2Na2O2+2CO2═2Na2CO3+O2;
 过氧化钠(Na2O2)在常温下能与人呼出的二氧化碳反应生成氧气,化学方程式为:2Na2O2+2CO2═2Na2CO3+O2;为了验证该反应中氧气的产生,某兴趣小组的同学设计了如图所示的实验.
过氧化钠(Na2O2)在常温下能与人呼出的二氧化碳反应生成氧气,化学方程式为:2Na2O2+2CO2═2Na2CO3+O2;为了验证该反应中氧气的产生,某兴趣小组的同学设计了如图所示的实验.
(1)实验室制取二氧化碳的化学方程式为______.
(2)设计A、B装置的目的是净化导入的气体并得到纯净且干燥的CO2.其中,A装置的作用是(用化学方程式表示)______;B装置的作用是______,其瓶内液体应是______;为了确定CO2跟Na2O2反应产生的气体是氧气,最后还要采用的验证实验操作是______.
(3)表明二氧化碳没有被过氧化钠完全吸收的现象是______.
 紫云的天空1年前1
紫云的天空1年前1 -
 就玩斗nn 共回答了15个问题
就玩斗nn 共回答了15个问题 |采纳率93.3%(1)在实验室中,通常用大理石或石灰石与稀盐酸反应来制取二氧化碳;
(2)因为制二氧化碳用的是稀盐酸,而盐酸容易挥发出氯化氢气体,因此需要除去混在二氧化碳中的氯化氢气体和水而设计了A、B装置;碳酸氢钠溶液与氯化氢气体发生反应,后用浓硫酸来进行气体的干燥;
(3)C装置中澄清石灰水不变浑浊,表明CO2已全部被Na2O2完全吸收,若变浑浊,则没有完全吸收.
故答案为:(1)2HCl+CaCO3=CaCl2+H2O+CO2↑;(2)HCl+NaHCO3=NaCl+H2O+CO2↑;干燥气体;浓硫酸;将燃着的木条伸入集气瓶中,带火星的木条复燃;(4)C中澄清石灰水变浑浊.1年前查看全部
- 2Na2O2+2CO2═2Na2CO3+O2因常温常压下发生的反应,1mol二氧化碳的体积>22.4L这是为什么
 唐门Oo癫少1年前1
唐门Oo癫少1年前1 -
 zjs1380 共回答了16个问题
zjs1380 共回答了16个问题 |采纳率100%标准状况下(0摄氏度,1个标准大气压下)1mol二氧化碳是22.4L 热胀冷缩,常温常压下温度是20摄氏度,温度升高了,气体的体积也就变大了!1年前查看全部
- 潜水艇中需配备氧气再生装置.一般利用Na2O2吸收CO2再生氧气,其反应原理为2Na2O2+2CO2═2Na2CO3+O
潜水艇中需配备氧气再生装置.一般利用Na2O2吸收CO2再生氧气,其反应原理为2Na2O2+2CO2═2Na2CO3+O2.如果一个潜艇兵每天大约需要呼吸12m3的氧气(氧气密度为1.429g/L),需Na2O2的质量为( )
A.83596.5g
B.22176g
C.156g
D.17148g 天蓝草碧20071年前1
天蓝草碧20071年前1 -
 zmxice 共回答了13个问题
zmxice 共回答了13个问题 |采纳率100%解题思路:找出已知和待求,计算出二者的相对分子质量,再根据氧气的质量列比例式计算出过氧化钠的质量即可.氧气的质量=12m3×1.429g/L×1000=17148g
设理论上需要过氧化钠的质量为x.
2Na2O2+2CO2═2Na2CO3+O2
156 32
x 17148g
[156/x=
32
17148g]
x=83596.5g
故选:A.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 解答本题容易出错的地方就是相对分子质量的计算,要注意前面的系数.1年前查看全部
- 在 2Na2O2+2CO2═2Na2CO3+O2反应中,
在 2Na2O2+2CO2═2Na2CO3+O2反应中,
(1)用双线桥法标出电子转移的方向和数目______.
(2)______是还原剂,______是氧化剂.
(3)若转移3mol电子,则所产生的氧气在标准状况下的体积为______. wangfo1年前0
wangfo1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 过氧化钠(Na2O2)能吸收人呼出的二氧化碳气体,并产生氧气,供给人的呼吸.其反应的化学方程式为:2Na2O2+2CO2
过氧化钠(Na2O2)能吸收人呼出的二氧化碳气体,并产生氧气,供给人的呼吸.其反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2.现有不纯过氧化钠100.0g(杂质不参加反应)与足量的二氧化碳反应,生成氧气的质量为16g.求过氧化钠的质量分数是多少?
 wanjua1年前1
wanjua1年前1 -
 y1314 共回答了22个问题
y1314 共回答了22个问题 |采纳率86.4%解题思路:根据化学方程式,找出已知和待求,计算出二者的质量关系,再根据氧气的质量列比例式计算出过氧化钠的质量即可.设消耗的过氧化钠的质量为x
2Na2O2+2CO2 ═2Na2CO3+O2
156 32
x16g
[156/32=
x
16g]
x=78g
过氧化钠的质量分数是
78g
100g×100%=78%
答案:过氧化钠的质量分数是过氧化钠的质量分数是点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 解答本题容易出错的地方就是相对分子质量的计算,要注意前面的系数.1年前查看全部
- (2005•河南)物质的用途是由物质的______决定的,过氧化钠跟二氧化碳起反应的化学方程式为:2Na2O2+2CO2
(2005•河南)物质的用途是由物质的______决定的,过氧化钠跟二氧化碳起反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2,因此,过氧化钠可用在呼吸面具上和潜水艇里作为______的来源.
 sdfguhesrh1年前1
sdfguhesrh1年前1 -
 冰点001 共回答了17个问题
冰点001 共回答了17个问题 |采纳率82.4%解题思路:物质的结构决定物质的性质,物质的性质决定物质的用途;氧气的化学性质比较活泼,能够供给呼吸.物质的用途是由物质的性质决定的.故填:性质.
过氧化钠跟二氧化碳反应能生成氧气,可用在呼吸面具上和潜水艇里作为氧气的来源.故填:氧气.点评:
本题考点: 氧气的化学性质;氧气的用途.
考点点评: 本题主要考查物质的性质和用途,解答时要充分理解各种物质的性质,然后再根据物质的性质方面进行分析、判断,从而确定物质的用途.1年前查看全部
- Na2O2可用在潜水艇里作为氧气的一种来源,供人们呼吸所需.Na2O2所发生反应的化学方程为2Na2O2+2CO2═2N
Na2O2可用在潜水艇里作为氧气的一种来源,供人们呼吸所需.Na2O2所发生反应的化学方程为2Na2O2+2CO2═2Na2CO3+O22Na2O2+2CO2═2Na2CO3+O2.在这个反应中,电子转移的总数为2e-2e- 被氧化的是-1-1 价态氧氧元素,氧化剂是Na2O2Na2O2.
 jbb88820021年前1
jbb88820021年前1 -
 lnih 共回答了31个问题
lnih 共回答了31个问题 |采纳率74.2%Na2O2与呼吸产生的二氧化碳反应生成碳酸钠和氧气,该反应为2Na2O2+2CO2═2Na2CO3+O2,该反应中只有过氧化钠中O元素的化合价变化,由-1价,升高为0,由-1价降低为-2价,Na2O2既是氧化剂又是还原剂,该反应中2molNa2O2反应转移2mol电子,即该反应转移2e-,
故答案为:2Na2O2+2CO2═2Na2CO3+O2;2e-;-1;氧;Na2O2.1年前查看全部
- 请用化学用语回答问题:(1)两个镁原子______;(2)化学反应2Na2O2+2CO2═2Na2CO3+X中,X的化学
请用化学用语回答问题:
(1)两个镁原子______;
(2)化学反应2Na2O2+2CO2═2Na2CO3+X中,X的化学式为______. nimazhu1年前1
nimazhu1年前1 -
 fariceliang 共回答了21个问题
fariceliang 共回答了21个问题 |采纳率95.2%解题思路:根据原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字和质量守恒定律进行解答.(1)原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.所以2个镁原子,就可表示为:2Mg;
(2)根据反应的化学方程式2Na2O2+2CO2=2Na2CO3+X,反应物中钠、氧、碳原子个数分别为4、8、2,反应后的生成物中钠、氧、碳原子个数分别为4、6、2,根据反应前后原子种类、数目不变,则每个X分子由2个氧原子构成,则物质X的化学式为O2.
故答案为:(1)2Mg(2)O2点评:
本题考点: 化学符号及其周围数字的意义;质量守恒定律及其应用.
考点点评: 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.1年前查看全部
大家在问
- 1地球上曾经生存过那里人类?现在的我们是哪种人类的后代?
- 2A~H都是初中化学常见的物质,它们的转化关系如下图所示。A、B均为黑色粉末;D、F均为红色固体,且D为单质;C能使澄清石
- 3谢谢 英语(急死了)~!~!~!
- 4质量相同的甲、乙两实心物体,已知甲的密度大于乙的密度,则______的体积较大.如果实心的铁球和铝球的体积相同,则___
- 5(2011•江西)2011年4月至10月期间,中国西安举办第41届世界园艺博览会.假如你想乘坐火车去参观博览会,那么从九
- 6英语单词的比较级 serious
- 7烤面包的架子上一次最多只能放2片面包,正反面都要烤,正面要3分钟,反面要2分钟,那么烤3片面包至少需要多少分钟?
- 8在某一动物种类丰富的森林中,消费者、分解者的种类和数量基本保持稳定,下列有关叙述,错误的是( )
- 9设点F1(-c,0)、F2(c,0)分别是双曲线x2a2−y2b2=1的左右焦点,P为双曲线上的一点,且PF1•PF2=
- 10该气候的特点是( ) A.全年高温多雨 B.冬季寒冷干燥 C.全年温和多雨 D.夏季高温少雨
- 11【你不介意我听音乐吧?】用英语怎么说?并且用【Would you --- my ---- --- to the musi
- 12一个圆形花坛直径是10m,在花坛的周围铺一条2m宽的环形小路,路的面积是多少?
- 13补充条件,编成需要两步计算的应用题,并列出算式.
- 14今有竹高一丈,末折抵地,去本三尺,问折者高几何?
- 15如图abc三个算式,求出x代表几个长方形 几个圆圈 几个黑点 a图 长方形+4个圆圈=2个黑点4个圆圈 b图
