现用四氯化硅和氮气在氢气气氛保护下,加强热发生反应 反应方程式为什么
 雨VS轩2022-10-04 11:39:542条回答
雨VS轩2022-10-04 11:39:542条回答
已提交,审核后显示!提交回复
共2条回复
 低调的天使 共回答了20个问题
低调的天使 共回答了20个问题 |采纳率85%- SiCl4 + 2H2==加热===SI +4HCl
这是制取高纯度硅的办法 - 1年前
 momingji 共回答了14个问题
momingji 共回答了14个问题 |采纳率85.7%- SiCl4+2H2=Si+4HCl?
- 1年前
相关推荐
- 四氯化硅水解制氯化氢工艺流程,主要装置设备?
 enxue26121年前1
enxue26121年前1 -
 dfgasger 共回答了18个问题
dfgasger 共回答了18个问题 |采纳率94.4%不建议这样制取氯化氢,因为成本太高,会造成产品价格太高而市场不能打开的结局,再者污染也很大,除非副产物氧化硅作为其他物料的原料,或者说水解四氯化硅制取其它物料的副产品生产氯化氢,这倒还可以.1年前查看全部
- 为什么四氯化碳不水解,而三氯化硼和四氯化硅却强烈的水解呢?
 百立21年前1
百立21年前1 -
 asdgfiluawgkrth 共回答了18个问题
asdgfiluawgkrth 共回答了18个问题 |采纳率83.3%我只能确定说四氯化碳是一种稳定的化合物,而三氯化硼和四氯化硅不稳定.不过我觉得应该与他们的化学键有关.比如,假设四氯化碳水解,生成碳酸与盐酸,可是碳酸与盐酸的化学键稳定性比不上四氯化碳,而三氯化硼水解产生的硼酸与盐酸的化学键稳定性则比三氯化硼高.众所周知,化学反应的本质是原化学键的断裂与新化学键的形成,而发生的条件就是在反应条件下新产生的化学键比原化学键稳定,所以,这种现象的形成应该与他们化学键的稳定性有关1年前查看全部
- 关于四氯化硅和Si3N4(这叫什么┑( ̄Д  ̄)┍)的所有方程式
 dinkking1年前1
dinkking1年前1 -
 辜缘 共回答了2个问题
辜缘 共回答了2个问题 |采纳率50%可用化学气相沉积法,使SiCl4和N2在H2气氛保护下反应,产物Si3N4积在石墨基体上,形成一层致密的Si3N4层。此法得到的氮化硅纯度较高,其反应如下: SiCl4+2N2+6H2→Si3N4+12HCl1年前查看全部
- 某种硅(Si)的单质为银灰色晶体,常用作半导体材料,不溶于水,在450℃时能与氯气发生反应只生成四氯化硅.请根据上述信息
某种硅(Si)的单质为银灰色晶体,常用作半导体材料,不溶于水,在450℃时能与氯气发生反应只生成四氯化硅.请根据上述信息,归纳整理:
(1)该晶体硅的物理性质是______(答出两点即可);
(2)该晶体硅的化学性质是______. lhg0071年前1
lhg0071年前1 -
 穆吉卜 共回答了25个问题
穆吉卜 共回答了25个问题 |采纳率76%(1)某种硅(si)的单质为银灰色晶体,不溶于水,分别描述的是颜色、状态、溶解性;常用作半导体材料,说明硅具有导电性,以上性质不需要通过化学变化表现出来的,属于物理性质;
(2)在450℃时能与氯气(Cl 2 )发生反应,需要通过化学反应才能表现出来,属于化学性质.
故答为:(1)银灰色晶体,有导电性,不溶于水;(2)在450℃时能与氯气发生反应.1年前查看全部
- 物质在蒸馏后一般为什么态?有一道题时四氯化硅蒸馏为气态,这是特殊的吗?
物质在蒸馏后一般为什么态?有一道题时四氯化硅蒸馏为气态,这是特殊的吗?
物质在蒸馏后一般为什么态?
有一道题时四氯化硅蒸馏为气态,这是特殊的吗? 请记住我1年前3
请记住我1年前3 -
 芝麻萤4 共回答了22个问题
芝麻萤4 共回答了22个问题 |采纳率95.5%蒸馏是把液体变成气体,但是蒸馏后紧跟着就要冷凝,得到的依旧是液态的1年前查看全部
- (1)高温下氢气与四氯化硅(SiCl4)反应可制得高纯度的硅,同时生成氯化氢.该反应的化学方程式为SiCl4+2H2
(1)高温下氢气与四氯化硅(SiCl4)反应可制得高纯度的硅,同时生成氯化氢.该反应的化学方程式为SiCl4+2H2
Si+4HCl高温 .SiCl4+2H2.
Si+4HCl高温 .
(2)根据物质名称,写出下列化学式及符号:
两个钠离子______;两个水分子______; 四个硫酸根离子______. yao09621年前1
yao09621年前1 -
 zhejian 共回答了16个问题
zhejian 共回答了16个问题 |采纳率87.5%解题思路:(1)根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
(2)1个钠离子带1个单位的正电荷,1个水分子由2个氢原子和1个氧原子构成,1个硫酸根离子带2个单位的负电荷.(1)氢气与四氯化硅在高温条件下反应的化学方程式为:SiCl4+2H2
高温
.
Si+4HCl.
故填:SiCl4+2H2
高温
.
Si+4HCl.
(2)两个钠离子可以表示为2Na+;两个水分子可以表示为2H2O; 四个硫酸根离子可以表示为4SO42-.
故填:2Na+;2H2O;4SO42-.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式;化学符号及其周围数字的意义.
考点点评: 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式.1年前查看全部
- 某种硅(Si)的单质为银灰色晶体,常用作半导体材料,不溶于水,在450℃时能与氯气发生反应只生成四氯化硅.请根据上述信息
某种硅(Si)的单质为银灰色晶体,常用作半导体材料,不溶于水,在450℃时能与氯气发生反应只生成四氯化硅.请根据上述信息,归纳整理:
(1)该晶体硅的物理性质是______(答出两点即可);
(2)该晶体硅的化学性质是______. conan62561年前1
conan62561年前1 -
 魂星孟 共回答了17个问题
魂星孟 共回答了17个问题 |采纳率82.4%解题思路:根据物理性质和化学性质的定义进行分析.物质的物理性质是指不需要通过化学变化表现出来的性质;物质的化学性质是指在化学变化中表现出来的性质.(1)某种硅(si)的单质为银灰色晶体,不溶于水,分别描述的是颜色、状态、溶解性;常用作半导体材料,说明硅具有导电性,以上性质不需要通过化学变化表现出来的,属于物理性质;(2)在450℃时能与氯气(Cl2)发生...
点评:
本题考点: 化学性质与物理性质的差别及应用.
考点点评: 本题难度不大,掌握物理性质与化学性质的区分方法即可解答.1年前查看全部
- (2013•朝阳区二模)硅是信息产业、太阳能电池光电转化的基础材料.锌还原四氯化硅是一种有着良好应用前景的制备硅的方法,
(2013•朝阳区二模)硅是信息产业、太阳能电池光电转化的基础材料.锌还原四氯化硅是一种有着良好应用前景的制备硅的方法,该制备过程示意如下:
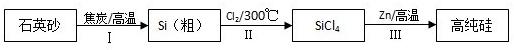
(1)焦炭在过程Ⅰ中作______剂.
(2)过程Ⅱ中的Cl2用电解饱和食盐水制备,制备Cl2的化学方程式是2NaCl+2H2O
2NaOH+Cl2↑+H2↑通电 .2NaCl+2H2O.
2NaOH+Cl2↑+H2↑通电 .
(3)整个制备过程必须严格控制无水.
①SiCl4遇水剧烈水解生成SiO2和一种酸,反应的化学方程式是______.
②干燥Cl2时,从有利于充分干燥和操作安全的角度考虑,需将约90℃的潮湿氯气先冷却至12℃,然后再通入到浓H2SO4中.冷却的作用是______.
(4)Zn还原SiCl4的反应如下:
反应1:400℃~756℃,SiCl4(g)+2Zn(l)⇌Si(s)+2ZnCl2(l)△H1<0
反应2:756℃~907℃,SiCl4(g)+2Zn(l)⇌Si(s)+2ZnCl2(g)△H2<0
反应3:907℃~1410℃,SiCl4(g)+2Zn(g)⇌Si(s)+2ZnCl2(g)△H3<0
①对于上述三个反应,下列说法合理的是______.
a.升高温度会提高SiCl4的转化率b.还原过程需在无氧的气氛中进行
c.增大压强能提高反应的速率d.Na、Mg可以代替Zn还原SiCl4
②实际制备过程选择“反应3”,选择的理由是______.
③已知Zn(l)═Zn(g)△H=+116KJ/mol.若SiCl4的转化率均为90%,每投入1mol SiCl4,“反应3”比“反应2”多放出______kJ的热量.
(5)用硅制作太阳能电池时,为减弱光在硅表面的反射,采用化学腐蚀法在其表面形成粗糙的多孔硅层.腐蚀剂常用稀HNO3和HF的混合液.硅表面首先形成SiO2,最后转化为H2SiF6.用化学方程式表示SiO2转化为H2SiF6的过程______. 潇格1年前1
潇格1年前1 -
 ouyuanxin_123 共回答了19个问题
ouyuanxin_123 共回答了19个问题 |采纳率84.2%解题思路:(1)在氧化还原反应中,化合价升高的元素发生还原反应;
(2)电解饱和食盐水的方法制备氯气,阳极,溶液中氯离子失电子发生氧化反应生成氯气,阴极,溶液中氢离子得到电子发生还原反应,生成氢气;
(3)①SiCl4遇水剧烈水解生成SiO2和一种酸,据此信息找出反应物和生成物,结合质量守恒书写化学方程式;
②水的沸点为100℃,浓硫酸具有吸水性,溶于水放热,据此解答;
(4)①△H<0表示放热,根据平衡移动的原理解答;
②反应2与反应1比较,反应2产物为固体和气体比反应1更易于分离,反应3与反应2比较,温度高,反应速率更快;
③根据盖斯定律可以计算化学反应的焓变;
(5)氟化氢跟二氧化硅反应生成四氟化硅和水,四氟化硅和氟化氢直接反应生成H2SiF6;(1)在过程Ⅰ中发生反应2C+SiO2
高温
.
Si+2CO↑中,C从0价变为一氧化碳中的+2价,发生氧化反应是还原剂;
故答案为:还原剂;
(2)电解饱和食盐水的方法制备氯气,阳极,溶液中氯离子失电子发生氧化反应生成氯气,2Cl--2e=Cl2↑,阴极,溶液中氢离子得到电子发生还原反应,生成氢气,2H++2e-═H2↑,总的反应为2NaCl+2H2O
通电
.
2NaOH+Cl2↑+H2↑,
故答案为:2NaCl+2H2O
通电
.
2NaOH+Cl2↑+H2↑;
(3)①根据SiCl4遇水剧烈水解生成SiO2和一种酸信息,反应物是SiCl4和水,生成物为二氧化硅,根据氧原子守恒,水分子前的系数为2,根据氢原子和氯原子守恒,另一产物为氯化氢,氯化氢前的系数为4,据此即可写出化学反应方程式,
故答案为:SiCl4+2H2O═SiO2+4HCl;
②干燥Cl2时,从有利于充分干燥和操作安全的角度考虑,需将约90℃的潮湿氯气先冷却至12℃,此时使水蒸气冷凝,然后再通入到浓H2SO4中,进入浓硫酸的水量少了,保证浓硫酸的良好吸水性,水和浓硫酸作用放热,所以进入硫酸的水少了,能降低放出的热量,
故答案为:使水蒸气冷凝减少进入浓硫酸的水量保持持续的吸水性并降低放出的热量;
(4)①对于三个反应,反应热都是△H<0表示放热,
a.升高温度,平衡向吸热的方向移动,所以会降低SiCl4的转化率,故a错误;
b.Si遇氧气在高温的条件下反应生成二氧化硅,所以还原过程需在无氧的气氛中进行,b正确;
c.有气体参加的反应,增大压强,能加快反应的速率,对于三个反应,都有气体参与,所以增大压强,能提高反应的速率,故c正确;
d.Na、Mg都是还原性比较强的金属,可以代替Zn还原SiCl4,故d正确;
故答案为:bcd;
②反应2与反应1比较,反应2产物为固体和气体比反应1更易于分离,反应3与反应2比较,反应物都为气态,温度高,反应速率更快,所以实际制备过程选择“反应3”,温度高反应速率快;与前两个反应比较更易于使硅分离使化学平衡向右移动提高转化率,
故答案为:温度高反应速率快;与前两个反应比较更易于使硅分离使化学平衡向右移动提高转化率;
③每投入1mol SiCl4,有2molZn参加反应,“反应3”与“反应2”比较,反应2中锌为液态,根据Zn(l)═Zn(g)△H=+116KJ/mol,若SiCl4的转化率均为90%,“反应3”比“反应2”多放出116KJ/mol×2×90%=208.8KJ,
故答案为:208.8;
(5)二氧化硅和氢氟酸:SiO2+4HF=SiF4↑+2H2O;SiF4+2HF=H2SiF6,所以用稀HNO3和HF的混合液,硅表面首先形成SiO2,最后转化为H2SiF6的化学方程式为SiO2+6HF═H2SiF6+2H2O,
故答案为:SiO2+6HF═H2SiF6+2H2O;点评:
本题考点: 制备实验方案的设计;用盖斯定律进行有关反应热的计算;化学平衡的影响因素.
考点点评: 本题考查锌还原四氯化硅制备硅,涉及化学平衡移动、电解等知识,掌握平衡移动原理的运用,掌握硅及其化合物的性质是解答的关键,题目难度中等.1年前查看全部
- 硅是信息产业、太阳能电池光电转化的基础材料。锌还原四氯化硅是一种有着良好应用前景的制备硅的方法,该制备过程示意如下:
硅是信息产业、太阳能电池光电转化的基础材料。锌还原四氯化硅是一种有着良好应用前景的制备硅的方法,该制备过程示意如下:
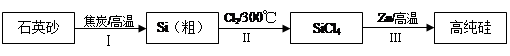
(1)焦炭在过程Ⅰ中作______剂。
(2)过程Ⅱ中的Cl 2 用电解饱和食盐水制备,制备Cl 2 的化学方程式是 。
(3)整个制备过程必须严格控制无水。
①SiCl 4 遇水剧烈水解生成SiO 2 和一种酸,反应的化学方程式是 。
②干燥Cl 2 时,从有利于充分干燥和操作安全的角度考虑,需将约90℃的潮湿氯气先冷却至12℃,然后再通入到浓H 2 SO 4 中。冷却的作用是 。
(4)Zn还原SiCl 4 的反应如下:
反应1: 400℃~756℃ ,SiCl 4 (g) + 2Zn(l) Si(s) + 2ZnCl 2 (l) ΔH 1 <0
Si(s) + 2ZnCl 2 (l) ΔH 1 <0
反应2: 756℃~907℃ ,SiCl 4 (g) + 2Zn(l) Si(s) + 2ZnCl 2 (g) ΔH 2 <0
Si(s) + 2ZnCl 2 (g) ΔH 2 <0
反应3: 907℃~1410℃,SiCl 4 (g) + 2Zn(g) Si(s) + 2ZnCl 2 (g) ΔH 3 <0
Si(s) + 2ZnCl 2 (g) ΔH 3 <0
① 对于上述三个反应,下列说法合理的是_____。
a.升高温度会提高SiCl 4 的转化率 b.还原过程需在无氧的气氛中进行
c.增大压强能提高反应的速率 d.Na、Mg可以代替Zn还原SiCl 4
② 实际制备过程选择“反应3”,选择的理由是 。
③ 已知Zn(l)=Zn(g) ΔH =" +116" KJ/mol 。若SiCl 4 的转化率均为90%,每投入1mol SiCl 4 ,“反应3”比“反应2”多放出_____kJ的热量。
(5)用硅制作太阳能电池时,为减弱光在硅表面的反射,采用化学腐蚀法在其表面形成粗糙的多孔硅层。腐蚀剂常用稀HNO 3 和HF的混合液。硅表面首先形成SiO 2 ,最后转化为H 2 SiF 6 。用化学方程式表示SiO 2 转化为H 2 SiF 6 的过程 。 love_gill1年前1
love_gill1年前1 -
 kitty2423 共回答了16个问题
kitty2423 共回答了16个问题 |采纳率93.8%1年前查看全部
- 一个关于化学上判断熔沸点的问题额RT.四氯化硅和四氟化硅谁熔沸点高呢?大家都知道是四氯化硅,原因是它的相对分子质量大,分
一个关于化学上判断熔沸点的问题
额RT.四氯化硅和四氟化硅谁熔沸点高呢?大家都知道是四氯化硅,原因是它的相对分子质量大,分子间作用力大,所以熔沸点高.但是…根据离子极化理论来看,氯离子的半径大,变形性大,极化作用强,极性减弱,因此四氯化硅的熔沸点反倒低.请问这是为什么呢?而且如果推广来看的话离子极化理论说阴离子半径大的变形性大极化作用强极性减弱熔沸点降低,但阴离子半径越大说明分子质量大这样熔沸点是高的啊?跪求大神指点囧rz ddchow1年前2
ddchow1年前2 -
 skywinning 共回答了13个问题
skywinning 共回答了13个问题 |采纳率84.6%你这属于对离子极化理论的滥用.离子极化理论适用于以离子性为主的同系列的物质性质比较,不能推广到其他物质.
SiF4 和 SiCl4 明显是共价化合物,不能用离子极化理论的.离子化合物和共价化合物的递变性规律是相反的,不可混为一谈.1年前查看全部
- 四氯化硅常温下雨水反应生成硅酸,由硅酸变成二氧化硅是直接脱去一分子水吗?
 enryqiao1年前3
enryqiao1年前3 -
 congcong1124 共回答了16个问题
congcong1124 共回答了16个问题 |采纳率93.8%按你说的,生成的并不是硅酸,而是偏硅酸,如果是偏硅酸就是了.
但是真实的是生成H4SiO4,这样也能生成二氧化硅但是确是脱去了两分子水的.化学式简单的,就不写了.1年前查看全部
- 四氯化硅和碳化硅熔点大小比较,及原因,物质结构方面,
 ajian11201年前1
ajian11201年前1 -
 兰德梅克 共回答了20个问题
兰德梅克 共回答了20个问题 |采纳率90%四氯化硅是分子晶体,碳化硅是原子晶体,所以碳化硅的熔点远远高于四氯化硅.
所谓分子晶体,例如四氯化硅,一个分子就是SiCl4,也就是说这个分子式就确定了这个物质分子的构成,分子间依靠分子间作用力结合;而SiC,理论上每一个颗粒都是一个分子,SiC不是分子式,只是代表了Si和C的配比是1:1;整个结构依靠化学键结合,所以熔点极高1年前查看全部
- 二氧化硅如何能转化成四氯化硅
 木字中间1年前2
木字中间1年前2 -
 吉音纱罗 共回答了21个问题
吉音纱罗 共回答了21个问题 |采纳率90.5%sio2+2c==2co+si
si+2cl2==sicl41年前查看全部
- 您好…请问一下:四氯化硅、四氟化硅、四碘化硅分别是分子晶体、原子晶体还是离子晶体?
您好…请问一下:四氯化硅、四氟化硅、四碘化硅分别是分子晶体、原子晶体还是离子晶体?
还有个问题就是:哺乳动物成熟的红细胞有哪些特性? 郁闷卡夫卡1年前3
郁闷卡夫卡1年前3 -
 颓废荒原 共回答了16个问题
颓废荒原 共回答了16个问题 |采纳率81.3%四氯化硅(无色透明状液体)、四氟化硅(气体)、四碘化硅都是分子晶体.成熟红细胞无细胞核,而且也无线粒体、核蛋白体等细胞器,不能进行核酸和蛋白质的生物合成,也不能进行有氧氧化,血糖是其唯一的能源.1年前查看全部
- 四氯化硅和甲苯加水后固体的什么,液体的是水和苯么?分开后水和苯还有刺鼻的气味么?
 亦若烟火1年前1
亦若烟火1年前1 -
 新阳街边看风景 共回答了16个问题
新阳街边看风景 共回答了16个问题 |采纳率93.8%不是,四氯化硅易水解生成原硅酸和氯化氢:SiCl4 + 4H2O == H4SiO4↓ + 4HCl
所以四氯化硅和甲苯加水后会得到白色沉淀,得到的液体上层是甲苯,下层是盐酸.1年前查看全部
- 某种硅(Si)的单质为银灰色晶体,常用作半导体材料,不溶于水,在450℃时能与氯气发生反应只生成四氯化硅.请根据上述信息
某种硅(Si)的单质为银灰色晶体,常用作半导体材料,不溶于水,在450℃时能与氯气发生反应只生成四氯化硅.请根据上述信息,归纳整理:
(1)该晶体硅的物理性质是______(答出两点即可);
(2)该晶体硅的化学性质是______. 冷娃娃1年前3
冷娃娃1年前3 -
 洪亮_abc 共回答了9个问题
洪亮_abc 共回答了9个问题 |采纳率88.9%解题思路:根据物理性质和化学性质的定义进行分析.物质的物理性质是指不需要通过化学变化表现出来的性质;物质的化学性质是指在化学变化中表现出来的性质.(1)某种硅(si)的单质为银灰色晶体,不溶于水,分别描述的是颜色、状态、溶解性;常用作半导体材料,说明硅具有导电性,以上性质不需要通过化学变化表现出来的,属于物理性质;(2)在450℃时能与氯气(Cl2)发生...
点评:
本题考点: 化学性质与物理性质的差别及应用.
考点点评: 本题难度不大,掌握物理性质与化学性质的区分方法即可解答.1年前查看全部
- 四氯化硅与水后生成一种固体,是什么、
 wxchao20061年前1
wxchao20061年前1 -
 andy0302 共回答了22个问题
andy0302 共回答了22个问题 |采纳率95.5%在潮湿空气中水解而成硅酸和氯化氢,同时发生白烟.对皮肤有腐蚀性.
SiCl4+3H2O==H2SiO3↓+4HCl1年前查看全部
- 四氯化硅中硅的化合价氮化硅Si3N4中氮的化合价
 欢子Ю1年前7
欢子Ю1年前7 -
 dadog76 共回答了18个问题
dadog76 共回答了18个问题 |采纳率100%因为硅要和4个氯形成离子键所以四氧化硅中的硅是正4价,以此类推氮化硅中的氮是+3价1年前查看全部
- 四氯化硅和水反应是复分解反应吗?
四氯化硅和水反应是复分解反应吗?
SiCl4+4H2O=H4SiO4+4HCl是复分解反应吗? 淡小雅1年前1
淡小雅1年前1 -
 不吃cc 共回答了15个问题
不吃cc 共回答了15个问题 |采纳率86.7%这要看生成物中是否有气体,水或沉淀生成,有的话就是复分解反应.(有水生成的也可能是中和反应,但复分解反应包括中和反应,且中和反应不是四大基本反应类型之一)1年前查看全部
- 某种硅的单质为银白色晶体,常用于做半导体,不溶于水,在加热时能与氯气发生反应只生成四氯化硅.氯原子的核电荷数为17,相对
某种硅的单质为银白色晶体,常用于做半导体,不溶于水,在加热时能与氯气发生反应只生成四氯化硅.氯原子的核电荷数为17,相对原子质量为35.请根据上述信息回答:
①该晶体硅的物理性质是______(回答出两点即可).
②写出硅与氯气反应的文字表式硅+氯气
四氯化硅450℃ 硅+氯气.
四氯化硅450℃
③氯原子的核外电子数为______,中子数为______. 密码查寻1年前1
密码查寻1年前1 -
 解了就解了 共回答了20个问题
解了就解了 共回答了20个问题 |采纳率90%解题思路:①物质的物理性质是指不需要通过化学变化表现出来的性质,物理性质主要包括:颜色、状态、气味、密度、硬度、熔点、沸点等.
②根据题意,找出反应物、生成物、反应条件,写出反应的化学方程式即可.③
③根据原子中核电荷数=核外电子数和相对原子质量=中子数+质子数分析.①某种硅(si)的单质为银白色晶体,不溶于水,分别描述的是颜色、状态、溶解性;常用作半导体材料,说明硅具有导电性,故填:银白色晶体,不溶于水.
②由题意,反应物是硅与氯气,生成物是四氯化硅,反应条件是450℃,反应的文字表达式为硅+氯气
450℃
四氯化硅,故填:硅+氯气
450℃
四氯化硅.
③氯原子的核电荷数为17,根据原子中核电荷数=核外电子数可知,氯原子的核外电子数为17;根据原子中相对原子质量=中子数+质子数可知,氯原子的中子数为35-17=18,故填:17;18.点评:
本题考点: 化学性质与物理性质的差别及应用;原子的有关数量计算;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,掌握物理性质与化学性质的区分方法、文字表达式的书写方法等是正确解答本题的关键.1年前查看全部
- 四氯化硅与水蒸气反应生成H2SiO4和HCl的方程式怎么配平?是H2SiO4!不是别的化学式!
 ever_cn1年前4
ever_cn1年前4 -
 yyzsz 共回答了19个问题
yyzsz 共回答了19个问题 |采纳率68.4%方程式如下
SiCl4 + 4H2O = 4HCl + H4SiO4
确实是生成H4SiO4而不是H2SiO4,你自己做错了
水蒸气,你可以把条件改成高温的,也没有错
祝你学习进步
望采纳O(∩_∩)O谢谢1年前查看全部
- 有谁知道四氯化硅SiCl4和氮气N2在氢气H2的保护下反应制取氮化硅的方程式
 水花语1年前1
水花语1年前1 -
 PLMsir 共回答了21个问题
PLMsir 共回答了21个问题 |采纳率95.2%也可用化学气相沉积法,使SiCl4和N2在H2气氛保护下反应,产物Si3N4积在石墨基体上,形成一层致密的Si3N4层.此法得到的氮化硅纯度较高,其反应如下:
SiCl4+2N2+6H2→Si3N4+12HCl1年前查看全部
- 请问用硅化镁法制备硅烷气,会产生四氯化硅(SiCl4)吗?
请问用硅化镁法制备硅烷气,会产生四氯化硅(SiCl4)吗?
即:Mg2Si+NH4Cl+液氨 生成SiH4,MgCl2·6NH3 外还生成什么?尤其是会不会生成四氯化硅. 海角_浪子1年前2
海角_浪子1年前2 -
 大孙村民 共回答了20个问题
大孙村民 共回答了20个问题 |采纳率95%Mg 2Si+4NH 4 Cl ===SiH 4 +4NH3 +2MgCl21年前查看全部
- 四氯化硅与氢气氧气反应化学方程式
 wfgdlj1年前2
wfgdlj1年前2 -
 hdfzhou3 共回答了21个问题
hdfzhou3 共回答了21个问题 |采纳率90.5%SiCl4+2H2==高温==Si+4HCl
SiCl4+O2==高温==SiO2+2Cl21年前查看全部
- 4.试解释四氯化碳不易水解,而四氯化硅却易于水解.
 厉兵秣马1年前2
厉兵秣马1年前2 -
 yongyin1998 共回答了17个问题
yongyin1998 共回答了17个问题 |采纳率100%SiCl4水解的过程是:
1,水分子和SiCl4中的Si结合(O的孤对电子占据Si的d轨道)以配位键形成一个中间体
2,一个Cl结合水上的一个H并脱离
3,如此类推,直至到全部的Cl都脱离
这个过程要求Si上有3d空轨道(这样才能和氧的孤电子对形成配位键),由于C没有d空轨道(因为没有2d),所以就不能接受氧上的孤电子对,就不能进行水解.1年前查看全部
- 四氯化硅水解的化学方程式是?
 mgq11281年前2
mgq11281年前2 -
 买好衣服 共回答了19个问题
买好衣服 共回答了19个问题 |采纳率94.7%四氯化硅受热或遇水分解放热
在潮湿空气中水解而成硅酸和氯化氢,方程式如下:
SiCl4 + 3H2O == H2SiO3 + 4HCl 或 SiCl4 + 4H2O == H4SiO4 + 4HCl1年前查看全部
- 在硅的冶炼中,通常用氢气在高温下还原四氯化硅的方法制得硅,同时生成氯化氢.请回答:
在硅的冶炼中,通常用氢气在高温下还原四氯化硅的方法制得硅,同时生成氯化氢.请回答:
(1)该反应的化学方程式为SiCl4+2H2
Si+4HCl高温 .SiCl4+2H2.
Si+4HCl高温 .
(2)现需冶炼2.8kg硅,至少需要消耗氢气多少升(标准状况)? abcjjj561年前1
abcjjj561年前1 -
 hmily121579 共回答了18个问题
hmily121579 共回答了18个问题 |采纳率94.4%解题思路:(1)根据反应物、生成物及反应条件书写方程式;
(2)根据Si和氢气之间的关系计算.(1)反应物是四氯化硅、氢气,生成物是HCl和Si,反应条件是高温,所以反应方程式为SiCl4+2H2
高温
.
Si+4HCl,故答案为:SiCl4+2H2
高温
.
Si+4HCl;
(2)2.8kg=2800g,n(Si)=[2800g/28g/mol]=100mol,设需要氢气体积为x,
SiCl4+2H2
高温
.
Si+4HCl
44.8L1mol
x 100mol
44.8L:1mol=x:100mol
x=[44.8L×100mol/1mol]=4480L,
答:需要消耗氢气体积是4480L.点评:
本题考点: 硅和二氧化硅;化学方程式的有关计算.
考点点评: 本题以硅为载体考查方程式的书写、根据方程式计算,根据方程式书写规则、方程式中各个物理量的关系即可解答,题目难度不大.1年前查看全部
- 为什么四氯化硅遇水容易分解?共价键不是很稳定么,怎么氯原子那么容易被取代?
 孩儿来福1年前2
孩儿来福1年前2 -
 jack_york 共回答了17个问题
jack_york 共回答了17个问题 |采纳率76.5%可以对比CCl4和SiCl4来分析.
C位于第二周期,有2个电子层,最外层只有s和p两个亚层.CCl4中C为sp3杂化,C的所有价电子均已成键,因此CCl4不水解.
Si位于第三周期,有3个电子层,最外层有s、p、d三个亚层.SiCl4中Si也为sp3杂化,Si的所有价电子也均已成键.但与C不同的是Si的最外层还有空的d轨道,Si原子可以利用这个空d轨道与OH(-)结合,生成[SiCl4(OH)](-)离子(空间构型为三角双锥),然后脱去Cl(-),生成SiCl3(OH),以此类推,最后生成Si(OH)4(即H4SiO4,原硅酸).全过程如下:
SiCl4 ——[+ OH(-)]—→ [SiCl4(OH)](-) ——[- Cl(-)]—→ SiCl3(OH)
——[+ OH(-)]—→ [SiCl3(OH)2](-) ——[- Cl(-)]—→ SiCl2(OH)2
——[+ OH(-)]—→ [SiCl2(OH)3](-) ——[- Cl(-)]—→ SiCl(OH)3
——[+ OH(-)]—→ [SiCl(OH)4](-) ——[- Cl(-)]—→ Si(OH)4(即H4SiO4)1年前查看全部
- 英语翻译四氯化硅是生产多晶硅的废料,对环境有很大的破坏作用,对四氯化硅的利用不仅能够变废为宝,还能够促进新产业的发展.本
英语翻译
四氯化硅是生产多晶硅的废料,对环境有很大的破坏作用,对四氯化硅的利用不仅能够变废为宝,还能够促进新产业的发展.本文根据四氯化硅与氢氧化钙的水解反应原理,设计出四氯化硅与氢氧化钙的反应制备出硅酸钙的工艺,全面分析工艺组成中的四氯化硅水解系统、原硅酸脱水系统、硅酸钙生成系统的特点,研究工艺过程的影响因素,通过试验,制备出的硅酸钙符合国家标准;在此基础上探讨了工艺副产物的利用.本文的研究有助于解决多晶硅生产废物的严重污染问题,又可大幅度降低多晶硅生产成本,极大提高产业经济效益,对发展***多晶硅和太阳能产业具有十分重要的作用. ss2010081年前1
ss2010081年前1 -
 ysy_f 共回答了20个问题
ysy_f 共回答了20个问题 |采纳率90%The silicon tetrachloride is produces the polycrystalline silicon the waste material, has the very big destructive effect to the environment, not only can recycle waste to the silicon tetrachloride use, but also can promote the new industrial development.This article according to the silicon tetrachloride and the calcium hydroxide hydrolitic reaction principle, designs the silicon tetrachloride and the calcium hydroxide response prepares the calcium silicate the craft, analyzes in the craft composition comprehensively the silicon tetrachloride hydrolysis system, the ortho-silicic acid dehydration system, the calcium silicate production system characteristic, the research technological process influence factor, through the experiment, the calcium silicate which prepares conforms to the national standards; Has discussed the craft by-product use in this foundation.This article research is helpful to the solution polycrystalline silicon production waste serious contamination concern, also may reduce the polycrystalline silicon production cost large scale, enhances the industrial economic efficiency enormously, to develops our country polycrystalline silicon and the solar energy industry has the extremely vital role.1年前查看全部
- 为什么四氟化硅是气态,四氯化硅是液态,------
 kugookk5201年前2
kugookk5201年前2 -
 霓沫 共回答了25个问题
霓沫 共回答了25个问题 |采纳率100%因为四氟化硅和四氯化硅都是分子晶体
随着物质分子量的增大
分子间作用力加强
熔沸点也随着升高
导致SiF4是气态
SiCl4是液态
祝你新年快乐1年前查看全部
- 四氯化硅遇水放出什么气体,性质是什么
 fairyezono1年前4
fairyezono1年前4 -
 迷茫的沛翔 共回答了20个问题
迷茫的沛翔 共回答了20个问题 |采纳率100%SiCl4+4H2O=H4SiO4+4HCl
会有原硅酸和盐酸气雾生成
盐酸的性质楼主知道的1年前查看全部
- 常温常压下四氯化硅是气体吗?四氯化硅和四氯化碳谁的熔点高?
 玉骨儿1年前1
玉骨儿1年前1 -
 cocohuke 共回答了15个问题
cocohuke 共回答了15个问题 |采纳率93.3%四氯化碳熔点:-22.8度
四氯化硅熔点:-70度
四氯化碳沸点76.8度,
四氯化硅沸点57.6度,常温下液体
在高三的化学书上会有一张比较分子晶体熔点的图,其中四氯化碳和四氯化硅就是特例.并不是所有的熔点都随相对分子质量而增大.只是大多数情况下是那样.1年前查看全部
- 四氯化硅和水反应方程式怎么写
 大胆浆糊1年前3
大胆浆糊1年前3 -
 amable木木 共回答了15个问题
amable木木 共回答了15个问题 |采纳率80%SiCl4+4H2O=H4SiO4+4HCl 四氯化硅和四氯化锡等物质也极易水解SiCl4+4H2O=H4SiO4+4HCl,SnCl4+4H2O=Sn(OH)4+4HCl,也就是它们在空气中合形成HCl酸雾1年前查看全部
- 四氯化硅和水蒸气反应生成H4SiO4和水怎么配平?
 swmblood1年前1
swmblood1年前1 -
 gyx318 共回答了19个问题
gyx318 共回答了19个问题 |采纳率84.2%不反应啊1年前查看全部
- 四氯化硅与锌的反应条件是什么?
 悲伤流成河淹ff你1年前1
悲伤流成河淹ff你1年前1 -
 f251h 共回答了16个问题
f251h 共回答了16个问题 |采纳率100%利用锌和四氯化硅在1000℃反应可以生成太阳能级多晶硅和ZnCl2,ZnCl2熔融电解生成Zn和Cl2,1年前查看全部
- 四氯化硅为什么是气体写错了是为什么易水解
 hong阿宏1年前3
hong阿宏1年前3 -
 dsdskdkssdk 共回答了20个问题
dsdskdkssdk 共回答了20个问题 |采纳率100%易水解的离子一般是弱酸跟阴离子(碳酸氢根),弱碱跟阳离子(铁离子),硅就属于后者.1年前查看全部
- 为什么四氯化硅比四氯化碳易水解?
 101103121年前1
101103121年前1 -
 mtp6035777 共回答了19个问题
mtp6035777 共回答了19个问题 |采纳率78.9%因为Si有空轨道1年前查看全部
- 硅与氯气生成四氯化硅的文字表达式
 litao9951年前1
litao9951年前1 -
 kygk 共回答了18个问题
kygk 共回答了18个问题 |采纳率83.3%硅 + 氯气 =(一定条件下)= 四氯化硅1年前查看全部
- 为什么粗硅和氯气反应会生成四氯化硅而不是二氯化硅?
 十月小君1年前1
十月小君1年前1 -
 梦蝶女 共回答了18个问题
梦蝶女 共回答了18个问题 |采纳率100%因为氯的氧化性很强,把硅氧化成高价态1年前查看全部
- 四氟化硅 四氯化硅 熔点怎样比较
 麻二哥哥1年前3
麻二哥哥1年前3 -
 liaoshan5 共回答了20个问题
liaoshan5 共回答了20个问题 |采纳率90%四氟化硅熔点-90.2℃
四氯化硅熔点-70℃
两种物质都是非极性分子,和氢键没有关系.
但是四氯化硅体积大,范德华力中的色散力大.1年前查看全部
- (14分)高纯硅是当今科技的核心材料。工业上,用氢气还原四氯化硅制得高纯硅的反应为SiCl 4 (g)+2H 2 (g)
(14分)高纯硅是当今科技的核心材料。工业上,用氢气还原四氯化硅制得高纯硅的反应为SiCl 4 (g)+2H 2 (g)
 Si(s)+4HCl(g)。已知SiCl 4 可完全水解生成硅酸和盐酸。向容积为1L的密闭容器中充入一定量的SiCl 4 (g)和H 2 (g),分别在T 1 和T 2 温度时进行反应。SiCl 4 的物质的量随时间变化情况如下表所示:
Si(s)+4HCl(g)。已知SiCl 4 可完全水解生成硅酸和盐酸。向容积为1L的密闭容器中充入一定量的SiCl 4 (g)和H 2 (g),分别在T 1 和T 2 温度时进行反应。SiCl 4 的物质的量随时间变化情况如下表所示: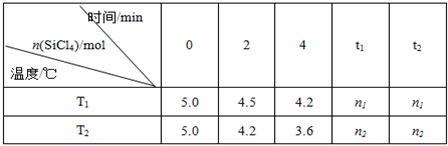
(1)T 1 时,反应开始的2 min内,用HCl表示的反应速率为 。
(2)该反应的平衡常数表达式为:K= 。
(3)保持其他条件不变,下列措施可提高SiCl 4 转化率的是 。
a.充入更多的SiCl 4 (g)
b.充入更多的H 2 (g)
c.及时分离出Si(s)
d.使用催化剂
e.将容器的体积扩大一倍
(4)据上表中的数据分析:T 1 T 2 (填“>”或“<”,下同),理由是 。已知n 1 >n 2 ,ΔH 0。
(5)有同学认为,采用水淋法来吸收生成的HCl,可以提高SiCl 4 的转化率。该认识 (填“合理”或“不合理”),理由是 。
(6)将平衡后的混合气体溶于水,取少量上层清液,向其中滴加足量的AgNO3溶液,反应后过滤,取沉淀向其中加入Na 2 S溶液,可观察到 。 我的英雄PBJ1年前1
我的英雄PBJ1年前1 -
 syslcy 共回答了14个问题
syslcy 共回答了14个问题 |采纳率92.9%(14分)
(1)1.0 mol/(L • min)(2分) (2)(2分)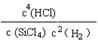
(3)be (2分)
(4)< (1分) T 2 时反应速率快(2分)> (1分)
(5)不合理(1分) SiCl 4 遇水完全水解生成硅酸和盐酸(2分)
(6)白色沉淀转化为黑色沉淀(1分)
(1)在T 1 时,反应开始的2 min内消耗的SiCl 4 的量是0.5mol,所以生成的HCl的量是2.0mol。因此用HCl表示的反应速率为1.0 mol/(L • min)。
(2)平衡常数是指在一定条件下,可逆反应达到平衡是生成物浓度的幂之积和反应物浓度的幂之积的比值。根据方程式可写出该反应的平衡常数表达式,需要注意的是在表达式中不能出现固体或纯液体的。
(3)因为这是一个体积增大的可逆反应,因此将容器的体积扩大一倍,平衡向正反应方向移动,增大反应物的转化率,e正确。充入更多的SiCl 4 (g),平衡虽然向正反应方向移动,但会降低自身的转化率,而提高氢气的转化率,所以a不正确,b正确。Si(s)是固体不影响平衡,c不正确。催化剂能同等程度改变正逆反应速率,但不会影响平衡,但不正确。故正确的答案是be。
(4)根据表中数据可知在相同时间内温度为T 2 反应速率快,因为温度越高,速率越快,故T 2 大于T 1 。n 1 >n 2 说明前者的转化率低于后者,即温度越高反应物的转化率越大,所以正反应是吸热反应。即ΔH大于0。
(5)由于SiCl 4 遇水完全水解生成硅酸和盐酸,所以采用水淋法来吸收生成的HCl是错误的。
(6)平衡后的混合气体溶于水,所得溶液中含有盐酸,滴加AgNO 3 溶液将生成AgCl沉淀,过滤后向沉淀中加入Na 2 S溶液,则沉淀颜色将由白色转化为黑色,这是因为Ag 2 S比AgCl更难溶,沉淀将向生成更难溶的物质转化。1年前查看全部
- 在硅与氯气反应制四氯化硅的装置中为什么要将反应产物先通入放在冷水中的集气瓶内然后再通过碱石灰?通...
在硅与氯气反应制四氯化硅的装置中为什么要将反应产物先通入放在冷水中的集气瓶内然后再通过碱石灰?通...
在硅与氯气反应制四氯化硅的装置中为什么要将反应产物先通入放在冷水中的集气瓶内然后再通过碱石灰?通过碱石灰是为了除氯气,但为什么还要先通入置于冷水中的集气瓶内,也就是为什么要让四氯化硅和氯气的混合气体先变为液态? xx残留1年前1
xx残留1年前1 -
 dudu961 共回答了16个问题
dudu961 共回答了16个问题 |采纳率93.8%为了让四氯化硅气体先变为液态与氯气分离1年前查看全部
- 计算机工业所用的单晶硅要求达到99,99%以上的纯度在制造过程中利用四氯化硅和和氢气在高温下反应制取高纯硅,同时生成氯化
计算机工业所用的单晶硅要求达到99,99%以上的纯度在制造过程中利用四氯化硅和和氢气在高温下反应制取高纯硅,同时生成氯化氢 写出其化学方程式
 寒风扫落叶1年前1
寒风扫落叶1年前1 -
 jiangxu1986 共回答了15个问题
jiangxu1986 共回答了15个问题 |采纳率86.7%Si(粗硅)十2Cl2=加热=SiCl4
SiCl4十2H2=加热=Si(纯硅)十4HCl1年前查看全部
- 提问:四氯化硅与干燥的氢气反应制备纯硅,为保证实验的成功,需保证实验装置的气密性,
提问:四氯化硅与干燥的氢气反应制备纯硅,为保证实验的成功,需保证实验装置的气密性,
控制温度以及()原因是() 虫虫很想飞1年前1
虫虫很想飞1年前1 -
 孟希笔谈 共回答了18个问题
孟希笔谈 共回答了18个问题 |采纳率72.2%控制温度以及(保持干燥无水)原因是(SiCl4能与水反应)1年前查看全部
- 关于碳族元素1,C3O2与水反应的方程式?2,为什么四氯化硅易水解而四氯化碳难水解?
 liebhaber1年前1
liebhaber1年前1 -
 qingsky 共回答了20个问题
qingsky 共回答了20个问题 |采纳率85%1,C3O2+H2O=HOOC-CH2-COOH,即得到丙二酸
工业上有这个反应
2,C在第二周期,最外层有4个轨道,1个s,3个p,在CCl4中,4个轨道上都放了电子对,很稳定了.
Si是第三周期,虽然与C很象,3s2,3p2,但其实还存在3d轨道,只是没有电子放,但有这样的空轨道,就有可能接受其它的电子,如接受H2O提供的电子,因此可以水解.
本质,是C的配位数只能是4,且在CCl4中都用上了,而Si的配位数可以更大,如H2[SiF6]中,Si就和6个F结合,配位数达到了6.
第二个问题,不知道你能否理解,决定于你们的结构化学学到什么难度.1年前查看全部
- 求H2,四氯化硅生成硅单质的化学式的化学式
 6six61年前2
6six61年前2 -
 liufang1215225 共回答了13个问题
liufang1215225 共回答了13个问题 |采纳率92.3%你好,反应方程式是:
SiCl4+H2=(高温)Si+4HCl
这是精制单质硅的其中一步的反应方程式
祝你开心
望采纳谢谢1年前查看全部
- 氢气与氧气氯气关系四氯化硅在氢乞中会还原为氯化氢与硅.还原中不能有氧气.为什么?是不是氢气与氧反应生成水.氢气就没有了.
氢气与氧气氯气关系
四氯化硅在氢乞中会还原为氯化氢与硅.还原中不能有氧气.为什么?是不是氢气与氧反应生成水.氢气就没有了.就没氢气还原了.也就是说在一千多度时.氧与氯同在氢会与哪个反应? 夜子19821年前1
夜子19821年前1 -
 oul9 共回答了25个问题
oul9 共回答了25个问题 |采纳率80%因为氧气是氧化剂,而氯离子也有氧化性,所以氧气会干扰生成物,还有,氢气会先和氧化性强的反应,也就是说如果有样的话回想和氧反应.若反应完氢气有剩余,才会和四氯化硅反应.1年前查看全部
- 在粗硅提纯的第二步、需要还原四氯化硅、是否可以使用二氧化碳?为什么?
 westor_wang1年前1
westor_wang1年前1 -
 神奇猪猪 共回答了16个问题
神奇猪猪 共回答了16个问题 |采纳率87.5%高温、去氧环境下进行.利用氢气的还原性.高温无氧,粗硅与氯气反应,生成氯化硅,然后氯化硅高温下与氢气反应,得到纯硅和氯化氢 硅电池高能耗1年前查看全部
- 在氢气还原四氯化硅的反应中,氢气的作用是什么?
 yunlifei19861年前2
yunlifei19861年前2 -
 zgmin12 共回答了24个问题
zgmin12 共回答了24个问题 |采纳率83.3%是还原剂1年前查看全部
大家在问
- 1找出2组反义词体育健儿们为了给祖国争光,不怕酷热,不畏严寒,不分昼夜的苦练本领,他们不是也像流着的河一样不知疲倦吗?
- 2初一有理数分数加减法混合运算,要例题和答案.
- 3烯丙醇可用溴水检验吗?为什么?
- 4谁有初中一年级的方程题,急用!要初中一年级的方程题,有解答的
- 5形容一个事物跟另一个事物一样好的成语
- 6什么实验能证明空气中有氧气,水蒸气?
- 7为了改善生态环境,防止水土流失,某村计划在荒坡上种480棵树,由于青年志愿者的支援,
- 8请用因式分解法解下列方程(2x+3)²=24x 3(x-3)=(x-3)² 1.2y-0.04=9y²
- 9提前祝自己生日快乐用英语怎么翻译
- 10祝我们生日快乐怎么翻译成英语
- 11用分子解释为什么淀粉遇碘会变蓝
- 12若把公元2009年记做正2009那么负80年表示?
- 13如果把公元2008年记作+2008,那么-296表示为
- 14平行宇宙用什么理论知识理解?
- 15相对论是否绝对正确?他与量子论在哪里冲突?

