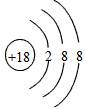
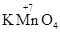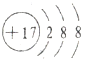用元素符号或化学式表示:(1)2个铁原子______(2)4个氢分子______(3)3个铝离子______(4)+7价
 薔薇淚2022-10-04 11:39:540条回答
薔薇淚2022-10-04 11:39:540条回答(1)2个铁原子______
(2)4个氢分子______
(3)3个铝离子______
(4)+7价的锰元素
| +7 |
| Mn |
| +7 |
| Mn |
(5)硫酸铁______
(6)2个硝酸根离子______
(7)氯离子的结构示意图______
(8)碳酸钠______.

已提交,审核后显示!提交回复
共0条回复
相关推荐
- 用元素符号或化学式表示:(1)2个水分子______;(2)空气中体积分数最大的气体______;(3)3个氢原子___
用元素符号或化学式表示:
(1)2个水分子______;
(2)空气中体积分数最大的气体______;
(3)3个氢原子______;
(4)8个钠离子______. 萧狼791年前1
萧狼791年前1 -
 坚持到底04 共回答了20个问题
坚持到底04 共回答了20个问题 |采纳率95%解题思路:(1)分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字.
(2)空气中体积分数最大的气体是氮气,写出其化学式即可.
(3)原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.
(4)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字.(1)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则2个水分子可表示为:2H2O.
(2)空气中体积分数最大的气体是氮气,其化学式为:N2.
(3)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故3个氢原子表示为:3H.
(4)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字,故8个钠离子可表示为:8Na+.
故答案为:(1)2H2O;(2)N2;(3)3H;(4)8Na+.点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本题难度不大,主要考查同学们对常见化学用语(分子符号、原子符号、化学式、离子符号等)的书写和理解能力.1年前查看全部
- 下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为______.
族
周期ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0 二 ① ② 三 ③ ④ ⑤ ⑥ ⑦ ⑧ 四 ⑨ ⑩
(2)地壳中含量最多的金属元素是______.
(3)写出②与④形成的化合物的电子式______.
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是______,碱性最强的是______,呈两性的氢氧化物是______.
(5)写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式:______.
(6)写出⑤与氢氧化钠溶液反应的化学方程式:______. hplsuj1年前0
hplsuj1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 用元素符号或化学式表示空气中占体积最大的气体是______,空气中支持燃烧的气体是______;地壳中含量最多的金属元素
用元素符号或化学式表示空气中占体积最大的气体是______,空气中支持燃烧的气体是______;地壳中含量最多的金属元素是______;氮气______;
(1)5个二氧化硫分子______;
(2)3个镁离子______;
(3)2Ca2+______
(4)+3价的铝元素+3 Al +3 Al
(5)一个硫酸根离子______. 心无殇1年前1
心无殇1年前1 -
 sissi22098 共回答了18个问题
sissi22098 共回答了18个问题 |采纳率94.4%解题思路:本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.由空气的成分及其体积分数(氮气78%、氧气21%、稀有气体0.94%、二氧化碳0.03%、其他气体和杂质0.03%),可以推断出:空气中体积分数最大的气体是N2.
由于氧气具有助燃性,能支持燃烧,氧分子属于双原子分子,化学式是02;
地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,其中含量最多的金属元素是铝元素,其元素符号为:Al.
氮气是一种气态非金属单质,是一种双原子分子构成的,故填:N2;
(1)分子的表示方法:正确书写物质的化学式,如二氧化硫分子是多原子分子,可表示为:SO2,表示多个该分子,就在其化学式前加上相应的数字,故5个二氧化硫分子可表示为:5SO2;
(2)一个镁离子带两个单位的正电荷,用Mg2+表示,那么,3个镁离子就是3Mg2+;
(3)根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故2Ca2+表示两个钙离子;
(4)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以+3价的铝元素,故可表示为:
+3
Al;
(5)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,因此一个硫酸根离子表示为SO42-.
故答案为:N2;02;Al;N2;(1)5SO2;(2)3Mg2+;(3)两个钙离子;(4)
+3
Al;(5)SO42-.点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.1年前查看全部
- 表是元素周期表的一部分.根据表中10种元素,用元素符号或化学式填空.
表是元素周期表的一部分.根据表中10种元素,用元素符号或化学式填空.
(1)在 ①~⑩元素中金属性最强的金属元素是______;族
周期ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0 2 ① ② 3 ③ ④ ⑤ ⑥ ⑦ 4 ⑧ ⑨ ⑩
(2)在 ①~⑥元素所形成的气态氢化物中最不稳定的分子式是______;
(3)在 ①~⑩元素中单质化学性质最稳定的原子结构示意图为______;
(4)在 ①~⑩元素的最高价氧化物的水化物中酸性最强的分子式是______;
(5)⑤、⑥、⑧、⑨所形成的离子中,半径最大的是______;
(6)⑨和⑩的原子序数之差为______.
(7)⑩生成两种常见氧化物,它们的分子式是______和______. 歌声飞满天1年前1
歌声飞满天1年前1 -
 三三四四五五 共回答了22个问题
三三四四五五 共回答了22个问题 |采纳率95.5%解题思路:由元素在周期表中位置,可知①为C、②为O、③为Al、④为Si、⑤为S、⑥为Cl、⑦为Ar、⑧为K、⑨为Ca、⑩为Se.
(1)同周期自左而右金属性减弱,同主族自上而下金属性增强;
(2)元素非金属性越强,其氢化物越稳定;
(3)稀有气体Ar原子核外最外层为稳定结构,化学性质最不活泼,Ar原子核外有18个电子,有3个电子层,各层电子数为2、8、8;
(4)上述元素的最高价氧化物的水化物中酸性最强是高氯酸;
(5)电子层结构相同,核电荷数越大离子半径越小;
(6)⑨和⑩均处于第四周期,⑨位于第2列,⑩位于第16列,第四周期中每列容纳1种元素,故二者原子序数之差等于所在列数之差;
(7)Se与S同主族,可知Se的常见化合价为+4、+6,据此书写其氧化物化学式.由元素在周期表中位置,可知①为C、②为O、③为Al、④为Si、⑤为S、⑥为Cl、⑦为Ar、⑧为K、⑨为Ca、⑩为Se.(1)同周期自左而右金属性减弱,同主族自上而下金属性增强,故上述元素中K元素金属性最强,故答案为:K...
点评:
本题考点: 元素周期律和元素周期表的综合应用.
考点点评: 本题考查元素周期表与元素周期律,难度不大,侧重对元素周期律的考查,注意把握元素周期表的结构,掌握金属性、非金属性强弱比较.1年前查看全部
- 用元素符号或化学式填空:①氩元素______;
用元素符号或化学式填空:
①氩元素______;
②4个二氧化硫分子______;
③氮气______;
④7个银原子______;
⑤3个硫酸根离子______;
⑥碳酸镁______;
⑦氧化铝中铝元素的化合价
2O3+3 Al .
2O3+3 Al  clsb1年前1
clsb1年前1 -
 zlg19811209 共回答了17个问题
zlg19811209 共回答了17个问题 |采纳率82.4%解题思路:书写元素符号时,第一个字母要大写,第二个字母要小写;化学符号周围的数字表示不同的意义:符号前面的数字,表示原子或分子个数;右上角的数字表示一个离子所带的电荷数;右下角的数字表示几个原子构成一个分子;元素正上方的数字表示元素的化合价.一个二氧化硫分子是由一个硫原子和两个氧原子构成的,一个氮气分子是由两个氮原子构成的;一个硫酸根离子带两个单位的负电荷,碳酸镁中镁元素的化合价是+2价,碳酸根的化合价是-2价;氧化铝中铝元素的化合价是+3价.书写元素符号时,第一个字母要大写,第二个字母要小写;符号前面的数字,表示原子、离子或分子个数;一个二氧化硫分子是由一个硫原子和两个氧原子构成的,一个氮气分子是由两个氮原子构成的;一个硫酸根离子带两个单位的负电荷,碳酸镁中镁元素的化合价是+2价,碳酸根的化合价是-2价;氧化铝中铝元素的化合价是+3价;故答案为:①Ar ②4SO2③N2 ④7Ag ⑤3SO42- ⑥MgCO3⑦
+3
Al2O3点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本考点考查了化学式和离子符号的书写,化学式书写的一般规律是:正前负后,然后利用十字交叉法;元素符号、化学式、化学方程式等化学用语的书写是中考的重要考点之一,要加强练习,理解应用.本考点主要出现在选择题和填空题中.1年前查看全部
- 用元素符号或化学式表示空气中最多的气体是______,空气中第二位的气体是______;地壳中含量最多的元素是_____
用元素符号或化学式表示空气中最多的气体是______,空气中第二位的气体是______;地壳中含量最多的元素是______,自然界中常温下呈液态的金属是______;2个氢分子______;2个氢原子______;2个氢离子______;2个铁离子______;氧化亚铁______;硫酸铝______.
 上yy兰依1年前1
上yy兰依1年前1 -
 wlx622 共回答了18个问题
wlx622 共回答了18个问题 |采纳率83.3%解题思路:熟练掌握空气中各成分的含量,记住地壳中前五种元素的排名;本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义.按体积分数计算,空气中氮气约占78%,所以空气中含量最多的气体是氮气;空气中第二位的气体是氧气;地壳中元素含量前五的元素是:氧、硅、铝、铁、钙,所以地壳中含量最多的元素是氧;自然界中常温下呈液态的金属是汞;
分子的表示方法:正确书写物质的化学式,表示多个分子,就在其化学式前加上相应的数字,所以2个氢气分子可表示为2H2;
原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.所以2个氢原子,就可表示为2H;
离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.2个氢离子可表示为2H+;2个铁离子表示为2Fe3+;
氧化亚铁化学式是FeO;硫酸铝化学式是Al2(SO4)3
故答案为:N2;O2;O;Hg;2H2;2H;2H+;2Fe3+;FeO;Al2(SO4)3点评:
本题考点: 化学式的书写及意义;化学符号及其周围数字的意义.
考点点评: 解答本题要掌握空气的成分、地壳中元素的含量和理解元素符号的含义,只有这样才能对相关方面的问题做出正确的判断.1年前查看全部
- 用元素符号或化学式表示:①2个氮分子______,②最简单的有机物______,③硫在空气中燃烧的产物______,④人
用元素符号或化学式表示:
①2个氮分子______,②最简单的有机物______,③硫在空气中燃烧的产物______,④人体缺乏会导致骨质疏松的元素______. xwc198311051年前1
xwc198311051年前1 -
 凌彦 共回答了15个问题
凌彦 共回答了15个问题 |采纳率86.7%①根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,因此2个氮分子表示为:2N 2 ;故答案为:2N 2 ;
②最简单的有机物是甲烷,化学式为:CH 4 ;故答案为:CH 4 ;
③硫在空气中燃烧的产物是二氧化硫;化学式为:SO 2 ;故答案为:SO 2 ;
④人体缺乏该元素会导致骨质疏松,故答案为:Ca.1年前查看全部
- 用元素符号或化学式填空(1)①2个氮原子______;②显正2价的镁元素+2Mg+2Mg;③3个水分子______;④2
用元素符号或化学式填空
(1)①2个氮原子______;②显正2价的镁元素+2 Mg ;③3个水分子______;④2个氧原子______.+2 Mg
(2)试选用“>”或“<”或“=”填空
①在空气中二氧化碳的体积分数______氧气的体积分数;
②钠离子核内质子数______核外电子数;
③一定质量的氯酸钾中含氧元素a g,加热完全分解后,生成氧气的质量______a g.
④小华想量取A mL液体,量取时他仰视量筒读数,则实际所取液体体积______A mL. wh25428361年前1
wh25428361年前1 -
 春江花yy 共回答了20个问题
春江花yy 共回答了20个问题 |采纳率100%解题思路:书写元素符号时,第一个字母要大写,第二个字母要小写;化学式书写的一般规律是:正前负后,然后利用十字交叉法.化学符号周围的数字表示不同的意义:符号前面的数字,表示原子或分子个数,一个水分子是由两个氢原子和一个氧原子构成的;右上角的数字表示一个离子所带的电荷数;右下角的数字表示几个原子构成一个分子;元素正上方的数字表示元素的化合价.空气中各成分的体积分数分别是:氮气78%、氧气21%、稀有气体0.94%、二氧化碳0.03%、水蒸气和其它气体和杂质0.03%.钠离子核内质子数是11,核外电子数是10;根据质量守恒定律,氯酸钾中的氧元素全部转化为氧气,因此相等;量取A mL液体,量取时他仰视量筒读数时,读数比实际药品偏小.(1)符号前面的数字,表示原子或分子个数,因此2个氮原子是2N,2个氧原子是2O;元素正上方的数字表示元素的化合价,正2价标在镁元素的正上方,因此显正2价的镁元素是
+2
Mg;一个水分子是由两个氢原子和一个氧原子构成的,因此3个水分子是3H2O;故答案为:2N;
+2
Mg;3H2O;2O;
(2)空气中各成分的体积分数分别是:氧气21%、二氧化碳0.03%,因此二氧化碳的体积分数小于氧气的体积分数;钠离子核内质子数是11,核外电子数是10,因此钠离子核内质子数大于核外电子数;根据质量守恒定律,氯酸钾中的氧元素全部转化为氧气,因此相等;量取A mL液体,量取时他仰视量筒读数时,读数比实际药品偏小;故答案为:<;>;=;>;点评:
本题考点: 化学符号及其周围数字的意义;测量容器-量筒;空气的成分及各成分的体积分数;原子和离子的相互转化;质量守恒定律及其应用.
考点点评: 本考点考查了化学式和离子符号的书写、空气的成分、质量守恒定律等,要加强记忆各知识点,并理解应用.本考点主要出现在选择题和填空题中.1年前查看全部
- 下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在③~⑦元素中,原子半径最大的元素其离子结构示意图为______主族
周期IA ⅡA ⅢA ⅣA VA ⅥA ⅦA 0 二 ① ② 三 ③ ④ ⑤ ⑥ ⑦ ⑧ 四 ⑨ ⑩
(2)按要求写出下列两种物质的电子式:①的氢化物______;碱性最强的最高价氧化物的对应的水化物______;
(3)在⑦与⑩的单质中,化学性质较活泼的是______(填化学式),可用什么化学反应说明该事实(写出反应的化学方程式):______. winddiyi1年前1
winddiyi1年前1 -
 goldenlin 共回答了21个问题
goldenlin 共回答了21个问题 |采纳率85.7%解题思路:由元素在周期表中位置,可知①为N、②为F、③为Na、④为Mg、⑤为Al、⑥为Si、⑦为Cl、⑧为Ar、⑨为K、⑩为Br.
(1)同周期自左而右原子半径减小,在③~⑦元素中原子半径最大的为Na,钠离子质子数为11,核外有10个电子层,有2个电子层,各电子数为2、8;
(2)①的氢化物为NH3,分子中N原子与H原子之间形成1对共用电子对;碱性最强的最高价氧化物的对应的水化物为KOH,由钾离子与氢氧根离子构成;
(3)同主族自上而下非金属性减弱,单质活泼性减弱,可以用单质之间的相互置换说明该事实.由元素在周期表中位置,可知①为N、②为F、③为Na、④为Mg、⑤为Al、⑥为Si、⑦为Cl、⑧为Ar、⑨为K、⑩为Br.
(1)同周期自左而右原子半径减小,在③~⑦元素中原子半径最大的为Na,钠离子质子数为11,核外有10个电子层,有2个电子层,各电子数为2、8,钠离子结构示意图为: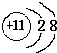 ,
,
故答案为: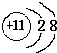 ;
;
(2)①的氢化物为NH3,分子中N原子与H原子之间形成1对共用电子对,电子式为: ;碱性最强的最高价氧化物的对应的水化物为KOH,由钾离子与氢氧根离子构成,电子式为:
;碱性最强的最高价氧化物的对应的水化物为KOH,由钾离子与氢氧根离子构成,电子式为: ,
,
故答案为: ;
; ;
;
(3)同主族自上而下非金属性减弱,单质活泼性减弱,故活泼性Cl2>Br2,可以用单质之间的相互置换说明该事实,反应方程式为:Cl2+2KBr═2KCl+Br2,
故答案为:Cl2;Cl2+2KBr═2KCl+Br2.点评:
本题考点: 元素周期律和元素周期表的综合应用.
考点点评: 本题考查元素周期表与元素周期律综合应用,难度不大,注意掌握元素金属性、非金属性强弱比较.1年前查看全部
- 如图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
如图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为______;周期
族ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0 2 ① ② ③ 3 ④ ⑤ ⑥ ⑦ ⑧ ⑨ 4 ⑩
(2)地壳中含量最多的金属元素是______,写出元素②④以原子个数比1:2形成化合物的电子式______.
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是______,碱性最强的是______;
(4)写出③、⑦、⑧对应的简单离子的还原性由强到弱的次序______.
(5)②和⑥组成的化合物属于______晶体(填写晶体类型). 绚烂烟花_evens1年前0
绚烂烟花_evens1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2007•顺义区二模)下列各组元素中,元素符号的大写字母相同的一组是( )
(2007•顺义区二模)下列各组元素中,元素符号的大写字母相同的一组是( )
A.汞、镁、银
B.钠、钡、钙
C.金、银、铝
D.氮、钠、锰 coperion1年前1
coperion1年前1 -
 foxjacky513 共回答了17个问题
foxjacky513 共回答了17个问题 |采纳率94.1%解题思路:本题主要考查学生对元素符号的记忆情况,只要熟记常见的27种元素符号,经过互相比较即可解答.A、汞、镁、银的元素符号分别为:Hg、Mg、Ag,大写字母不相同,不符合题意;
B、钠、钡、钙的元素符号分别为:Na、Ba、Ca,大写字母不相同,不符合题意;
C、金、银、铝的元素符号分别为:Au、Ag、Al,大写字母相同都是A,符合题意;
D、氮、钠、锰的元素符号分别为:N、Na、Mn,大写字母不相同,不符合题意.
故选C.点评:
本题考点: 元素的符号及其意义.
考点点评: 本题较简单,关键是要熟记常见元素的符号,要注意元素符号的第一个字母一定大写,第二个字母要小写,即“一大二小”规则.1年前查看全部
- 用元素符号和化学式表示1.2个钙原子2.4个氢原子3.4个二氧化硫分子4.氢元素5.氧气6.氯化钙7.五氧化二磷8.2个
用元素符号和化学式表示
1.2个钙原子2.4个氢原子3.4个二氧化硫分子4.氢元素5.氧气6.氯化钙7.五氧化二磷8.2个氮分子 greatwall19721年前3
greatwall19721年前3 -
 梦也无涯 共回答了17个问题
梦也无涯 共回答了17个问题 |采纳率100%2Ca 4H 4SO2 H O2 CaCl P2O5 2N21年前查看全部
- 如图是元素周期表的一部分,表中的①~⑧中元素,用元素符号或化学式填空回答:
如图是元素周期表的一部分,表中的①~⑧中元素,用元素符号或化学式填空回答:
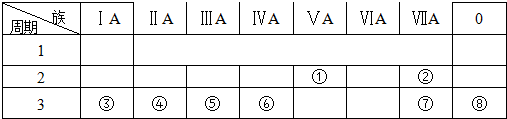
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为______;
(2)地壳中含量最多的金属元素是______;
(3)⑥在元素周期表中位于第______周期,第______族;
(4)②______(填“有”、“无”)最高正化合价,最低化合价是______;
(5)③与⑤最高价氧化物对应的水化物相互反应的离子方程式:______;
(6)写出⑤的单质与氢氧化钠反应的化学方程式:______. angelsula1年前1
angelsula1年前1 -
 wwy834 共回答了17个问题
wwy834 共回答了17个问题 |采纳率94.1%解题思路:由元素在周期表中位置,可知①为N、②为F、③为Na、④为Mg、⑤为Al、⑥为Si、⑦为Cl、⑧为Ar.
(1)稀有气体Ar最不活泼,Ar原子核外电子数为18,有3个电子层,各层电子数为2、9、8;
(2)地壳中含量最高的金属元素为铝;
(3)由⑥在周期表的位置可知其位于第三周期ⅣA族;
(4)氟元素没有最高正化合价,其最低负化合价=最外层电子数-8;
(5)氢氧化钠与氢氧化铝反应生成偏铝酸钠与水;
(6)铝与氢氧化钠溶液反应生成偏铝酸钠与氢气.由元素在周期表中位置,可知①为N、②为F、③为Na、④为Mg、⑤为Al、⑥为Si、⑦为Cl、⑧为Ar.
(1)稀有气体Ar最不活泼,Ar原子核外电子数为18,有3个电子层,各层电子数为2、9、8,原子结构示意图为: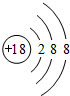 ,
,
故答案为: ;
;
(2)地壳中含量最高的金属元素为铝,故答案为:Al;
(3)由⑥在周期表的位置可知其位于第三周期ⅣA族,故答案为:三、ⅣA;
(4)氟元素没有最高正化合价,其最低负化合价=7-8=-1,故答案为:无;-1;
(5)氢氧化钠与氢氧化铝反应生成偏铝酸钠与水,反应离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(6)铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑.点评:
本题考点: 元素周期律和元素周期表的综合应用.
考点点评: 本题考查元素周期表与元素周期律等,比较基础,侧重对基础知识的巩固.1年前查看全部
- (12分)下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
(12分)下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是 ;可用于制半导体材料的元素是_______; 非金属性最强的是 。ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0 1 A 2 D E K G 3 B C J F H I
(2)最高价氧化物的水化物碱性最强的是 ,该物质的水溶液与C最高价氧化物的水化物反应的离子方程式是
H最高价氧化物的水化物是
(3)由A、K两种元素组成的含10个电子的化合物的结构式是 ,
B的氧化物的电子式是 ,该氧化物属于 晶体。 kezhunguo1年前1
kezhunguo1年前1 -
 酒鬼花生米 共回答了23个问题
酒鬼花生米 共回答了23个问题 |采纳率95.7%(1)Ar Si F (2)NaOH略 HClO (3)H-O-H; ; 离子
ⅠA1年前查看全部
- (18分)下表是元素周期表的一部分,回答下列有关问题:(用元素符号或化学式填空)
(18分)下表是元素周期表的一部分,回答下列有关问题:(用元素符号或化学式填空)
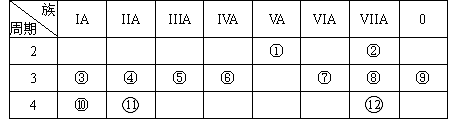
(1)写出下列元素符号:①________,⑥________,⑦________。
(2)画出原子的结构示意图:④________,⑤________,⑧________。
(3)在这些元素中,最活泼的金属元素是________,最活泼的非金属元素是________,最不活泼的元素是________。
(4)在这些元素的最高价氧化物对应水化物中,酸性最强的是________,碱性最强的是________,呈两性的氢氧化物是________。
(5)在③与④中,化学性质较活泼的是________,怎样用化学实验证明:答:________
在⑧与⑿中,化学性质较活泼的是________,怎样用化学实验证明?答:____________。(用化学反应方程式表示) hqinghua1年前1
hqinghua1年前1 -
 不过如次 共回答了22个问题
不过如次 共回答了22个问题 |采纳率86.4%(1)①N;⑥Si;⑦S;(2) ;
; ;
;
(3)K;F;Ar(4)HClO 4 ;KOH;Al(OH) 3 ;
(5)Na;与H 2 O反应; Cl 2 ;Cl 2 +2NaBr=2NaCl+Br 2
考查元素周期表的结构和元素周期律的应用。根据元素在周期表中的位置可判断①~⑫分别为N、F、Na、Mg、Al、Si、S、Cl、Ar、K、Ca、Br。根据元素周期律可知同周期自左向右非金属性逐渐增强,金属性逐渐减弱。同主族自上而下金属性逐渐增强,非金属性逐渐减弱。所以①~⑫金属性最强的是K,非金属性最强的是F。稀有气体的最外层电子已经达到稳定结构,所以性质最不活泼。金属性越强,最高价氧化物的水化物的碱性越强。非金属性越强,最高价氧化物的水化物的酸性越强。所以酸性最强的是HClO 4 ,碱性最强的是KOH,两性的是Al(OH) 3 。比较元素的金属性强弱可以利用金属单质和水或酸反应的剧烈程度,或者是相互之间的置换能力等。比较元素的非金属性强弱,也可以利用单质之间的相互置换能力,或者与氢气化合的难易程度以及相应氢化物的稳定性等。1年前查看全部
- 用元素符号或化学式填空:①水银______ ②约占空气总体积的
用元素符号或化学式填空:
①水银______②约占空气总体积的21%的气体是______③正三价的铁元素+3 Fe +3 Fe
④硫酸铜______
⑤根据各粒子结构示意图写出粒子符号: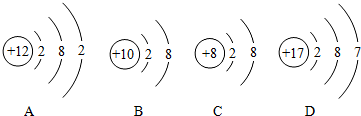
A______ B______ C______D______. buy2re1年前1
buy2re1年前1 -
 石雨19811212 共回答了17个问题
石雨19811212 共回答了17个问题 |采纳率94.1%解题思路:首先根据题意确定物质的化学名称,然后根据书写化学式与元素符号的方法和步骤写出物质的化学式与元素符号即可.①水银属于金属单质,直接用元素符号表示其化学式,其化学式为Hg.
②约占空气总体积的21%的气体是氧气,氧气属于气态非金属单质,在元素符号的右下角写上表示分子中所含原子数的数字,其化学式为:O2.
③元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以正3价的铁元素,故可表示为:
+3
Fe;
④硫酸铜由金属铜离子和硫酸根离子组成,铜显+2价,硫酸根显-2价,根据正价在前,负价在后,正负化合价的代数和为零可以写出其化学式为CuSO4,
⑤A核内质子数是12,决定元素的种类为镁元素,核外电子的数目等于核内质子数所以是原子,表示为Mg;
B核内质子数是10,决定元素的种类为氖元素,核外电子的数目等于核内质子数为原子,表示为Ne;
C核内质子数是8,决定元素的种类为氧元素,核外电子的数目大于核内质子数,所以是阴离子O2-;
D核内质子数是17,决定元素的种类为氯元素,核外电子的数目等于核内质子数为原子,表示为Cl;
故答案为:①Hg②O2③
+3
Fe;
④CuSO4⑤A、Mg;
B、Ne;
C、O2-;
D、Cl;点评:
本题考点: 化学符号及其周围数字的意义;原子结构示意图与离子结构示意图;化学式的书写及意义.
考点点评: 本题主要考查同学们对常见化学用语(原子符号、分子符号、化学式、化合价、离子符号等)的书写和理解能力及学生原子结构示意图的有关知识.1年前查看全部
- 下表是周期表中的一部分,根据A—J在周期表中的位置,用元素符号或化学式回答下列问题: (1)
下表是周期表中的一部分,根据A—J在周期表中的位置,用元素符号或化学式回答下列问题: 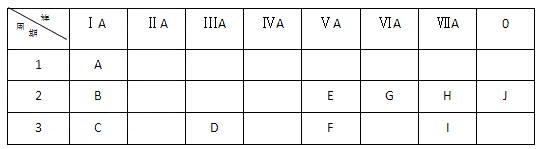
(1) 在D、E、F、H中,原子半径最大的是______________;
(2) B和H形成的化合物的电子式是____________;
(3) 其最高价氧化物的水化物,碱性最强的是___________,酸性最强的是____________;
(4)表中元素,化学性质最不活泼的是_________,氧化性最强的单质是___________;
(5)A分别与 E、F、G形成的化合物中,最稳定的____________;
(6)写出C的最高价氧化物的水化物和D的最高价氧化物的水化物反应的离子方程式_______________。 GREATQDTX1年前1
GREATQDTX1年前1 -
 ll王玫瑰 共回答了19个问题
ll王玫瑰 共回答了19个问题 |采纳率100%(1)Al;
(2)“略”;
(3)NaOH ;HClO4;
(4)Ne ;F 2 ;
(5)H 2 O;
(6)OH - +Al(OH) 3 = AlO 2 - + 2H 2 O1年前查看全部
- 下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答 (1)在这些元素中,化学性质最不活泼的原子的原
下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答 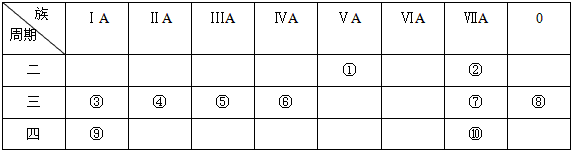
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为________________
(2)地壳中含量最多的金属元素是________________
(3)用电子式表示②与④形成化合物的过程_________________________。
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是_________,碱性最强的是_________,呈两性的氢氧化物是____________。
(5)写出⑤与氢氧化钠反应的化学方程式:________________________________。 写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式:________________________________。
(6)某元素R的气态氢化物为HXR,且R在该氢化物中的质量分数为94%,8.5g的HXR气体在标准状态下的体积是5.6L。则HXR的相对分子量为________________;HXR的化学式为________________。 fs18cp1年前1
fs18cp1年前1 -
 帝释天王 共回答了12个问题
帝释天王 共回答了12个问题 |采纳率91.7%1年前查看全部
- (11分,最后一空为2分,其余各1分)下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问
(11分,最后一空为2分,其余各1分)下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在这些元素中,最易失电子的元素是 ,非金属性最强的元素是主族
周期IA IIA IIIA IVA VA VIA VIIA 0 二 ① ② 三 ③ ④ ⑤ ⑥ ⑦ ⑧ 四 ⑨ ⑩
(2)化学性质最不活泼的元素的原子结构示意图为
(3)元素的最高价氧化物对应的水化物中酸性最强的酸是 ,碱性最强的
碱是 呈两性的氢氧化物是  可能相似的问题-
1年前1个回答
-
(16分)下表是元素周期表的一部分, 针对表中的①~⑩种元素,
1年前1个回答
-
1年前1个回答
你能帮帮他们吗
-
1年前
-
1年前
-
1年前
-
1年前
-
1年前
Copyright © 2022 YULUCN.COM - 雨露学习互助 - 17 q. 0.034 s. - webmaster@yulucn.com gatus1年前1
gatus1年前1 -
 887776666 共回答了14个问题
887776666 共回答了14个问题 |采纳率100%(1)K F (2)Ar (3)HClO 4 KOH Al(OH) 3 (4)Na Cl(5)Cl 2 Cl 2 +2KBr=2KCl+Br 2
(1)1年前查看全部
- 下图是元素周期表的一部分,表中的①~⑩各代表一种元素,用元素符号或化学式填空回答:
下图是元素周期表的一部分,表中的①~⑩各代表一种元素,用元素符号或化学式填空回答:
(1)以上元素构成的金属单质中与水反应最剧烈的金属与水反应的化学方程式是______,
族
周期IA IIA IIIA IVA VA VIA VIIA 0 二 ① ② 三 ③ ④ ⑤ ⑥ ⑦ ⑧ 四 ⑨ ⑩
(2)金属单质与氢氧化钠能反应的是______.(填元素符号)
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的物质是______,碱性最强的物质是______.(填化学式)
(4)气态氢化物最稳定的化学式是______.
(5)写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式______.
(6)写出⑦通入⑩的钠盐溶液的化学方程式______. xuyia1年前1
xuyia1年前1 -
 小争 共回答了18个问题
小争 共回答了18个问题 |采纳率100%根据元素周期表中元素的分布,可以推知表中的元素,①为N,②为F,③为Na,④为Mg,⑤为Al,⑥为Si,⑦为Cl,⑧为Ar,⑨为K,⑩为Br.
(1)同周期元素,从左到右金属性越来越弱,同主族元素,从上到下金属性越来越强,金属性最强的是K,和水反应最剧烈,方程式为:2K+2H 2 O=2KOH+H 2 ↑,
故答案为:2K+2H 2 O=2KOH+H 2 ↑;
(2)金属铝既能和强酸反应又能和强碱反应,故答案为:Al;
(3)同周期元素的原子,从左到右最高价氧化物对应的水化物的酸性逐渐增强,碱性逐渐减弱,同主族元素的原子,从上到下最高价氧化物对应的水化物的碱性逐渐增强,酸性逐渐减弱,所以酸性最强的是高氯酸,碱性最强的是氢氧化钾,故答案为:HClO 4 ;KOH;
(4)同周期元素的原子,从左到右得电子能力逐渐增强,氢化物越来越稳定,同主族元素的原子,从上到下得电子能力逐渐减弱,氢化物越来越不稳定,所以氢化物最稳定的是HF,故答案为:HF;
(5)氢氧化铝是两性氢氧化物,能和强碱反应,实质是:Al(OH) 3 +OH - =[Al(OH) 4 ] - ,故答案为:Al(OH) 3 +OH - =[Al(OH) 4 ] - ;
(6)氯气能将溴单质从其盐中置换出来,即Cl 2 +2NaBr=2NaCl+Br 2 ,故答案为:Cl 2 +2NaBr=2NaCl+Br 2 .1年前查看全部
- 用元素符号或化学式表示:(1)地壳中含量最多的元素______;(2)空气中含量最多的气体是______.
 herolisa1年前1
herolisa1年前1 -
 fyh_1030 共回答了20个问题
fyh_1030 共回答了20个问题 |采纳率90%解题思路:地壳中含量前五位的元素为:氧、硅、铝、铁、钙.而空气中含量最多的气体是氮气.(1)地壳中含量最多的元素是氧元素,其元素符号为O.故答案为:O
(2)氮气约占空气体积的78%因此空气中含量最多的是氮气;故答案为:N2点评:
本题考点: 地壳中元素的分布与含量.
考点点评: 要求学生熟练掌握在地壳中含有的最多的元素为氧元素.同时空气中含量最多的气体为氮气,并且要会用元素符号或化学式表示.1年前查看全部
- 用元素符号或化学式表示:(1)2个铁原子 (2)4个氢分子 (3)3个铝离子 (4)氧
用元素符号或化学式表示:
(1)2个铁原子 (2)4个氢分子 (3)3个铝离子
(4)氧化亚铜 (5)高锰酸钾中锰元素显+7价
(6)硫酸铁 (7)2个硝酸根离子
(8)氯离子的结构示意图 (9)图中2的意义
 佚流1年前1
佚流1年前1 -
 书生要hh 共回答了20个问题
书生要hh 共回答了20个问题 |采纳率80%1年前查看全部
- 用元素符号或化学式表示:(1)氢分子______(2)镁离子______(3)碘原子______(4)氢氧根离子____
用元素符号或化学式表示:
(1)氢分子______(2)镁离子______(3)碘原子______
(4)氢氧根离子______(5)二价的硫______(6)2个水分子______ 3695112541年前1
3695112541年前1 -
 sobsky 共回答了19个问题
sobsky 共回答了19个问题 |采纳率89.5%(1)根据氢分子两个氢原子组成,因此氢分子表示为 H 2 ,故答案为:H 2 ;
(2)根据离子符号在元素符号的右上角标明离子所带电荷数及电性,因此镁离子表示为 Mg 2+ ,故答案为:Mg 2+ ;
(3)根据原子用元素符号表示,因此碘原子表示为 I,故答案为:I;
(4)根据离子符号在元素符号的右上角标明离子所带电荷数及电性,氢氧根离子 OH - ,故答案为:OH - ;
(5)根据元素的化合价应标在元素符号的正上方,+-在前数字在后,二价的硫表示为
+2
S 故答案为:
+2
S ;
(6)2个水分子 2H 2 O,故答案为:2H 2 O.1年前查看全部
- 请用化学符号、元素符号的意义或数字“2”的意义填写下列空白:
请用化学符号、元素符号的意义或数字“2”的意义填写下列空白:
①3个氢原子______,②2个亚铁离子______,③SO42-______,④Hg表示______,⑤2Al3+______. wdx-661年前1
wdx-661年前1 -
 mei1102 共回答了15个问题
mei1102 共回答了15个问题 |采纳率100%解题思路:根据原子、离子、元素的表示方法及表示的意义进行分析解答.(1)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故3个氢原子表示为:3H;
(2)根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字;因此2个亚铁离子表示为:2Fe2+;
(3)根据离子的表示方法及右上角数字表示的意义,SO42-表示一个硫酸根离子带两个单位负电荷;
(4)根据元素符号表示的意义,Hg表示汞元素,还表示一个汞原子;
(5)根据离子的表示方法,2Al3+表示两个铝离子.
故答案为:(1)3H;(2)2Fe2+;(3)一个硫酸根离子带两个单位负电荷;(4)汞元素或一个汞原子;(5)两个铝离子.点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础.1年前查看全部
- 用元素符号或化学式表示(1)空气中含量第二的元素与地壳中含量最多的金属元素形成的化合物______;(2)食醋中的主要酸
用元素符号或化学式表示
(1)空气中含量第二的元素与地壳中含量最多的金属元素形成的化合物______;
(2)食醋中的主要酸性物质______;(3)2个铁离子______;
(4)形成化合物种类最多的元素______. nked1年前1
nked1年前1 -
 FUJING123 共回答了23个问题
FUJING123 共回答了23个问题 |采纳率87%解题思路:(1)根据空气中含量第二的元素为O;地壳中含量最多的金属元素为Al;依据化合价,利用十字交叉法写出化学式;
(2)根据食醋中的主要酸性物质是醋酸,写出其化学式解答;
(3)根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字;进行解答;
(4)根据含有碳元素的化合物属于有机物,有机物的种类繁多,达到了几千万种,远远多于无机物的种类.进行解答.(1)根据空气中含量第二的元素为O;地壳中含量最多的金属元素为Al;依据化合价,利用十字交叉法写出两种元素形成的化合物化学式为:Al2O3;
故答案为:Al2O3;
(2)根据食醋中的主要酸性物质是醋酸,其化学式为:CH3COOH; 故答案为:CH3COOH;
(3)根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字;因此2个铁离子表示为:2Fe3+;故答案为;2Fe3+;
(4)根据含有碳元素的化合物属于有机物,有机物的种类繁多,达到了几千万种,远远多于无机物的种类.因此形成化合物种类最多的元素为碳元素,表示为:C;
故答案为:C.点评:
本题考点: 化学式的书写及意义;有机物与无机物的区别;碳单质的物理性质及用途;常见元素与常见原子团的化合价.
考点点评: 解答本题要充分理解物质的组成元素方面的知识,只有这样才能对相关方面的问题做出正确的判断.1年前查看全部
- 下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在这些元素中,最易失电子的元素是 ,非金属性最强的元素是 ;ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅧA 0 二 ① ② 三 ③ ④ ⑤ ⑥ ⑦ ⑧ 四 ⑨ ⑩
(2)化学性质最不活泼的元素是 ,其原子的原子结构示意图为
(3)元素的最高价氧化物对应的水化物中酸性最强的是 ,呈两性的氢氧化物是  可能相似的问题-
(16分)下表是元素周期表的一部分, 针对表中的①~⑩种元素,
1年前1个回答
-
下表是元素周期表的一部分,按要求填空(均填元素符号或化学式):
1年前1个回答
你能帮帮他们吗
Copyright © 2022 YULUCN.COM - 雨露学习互助 - 17 q. 0.031 s. - webmaster@yulucn.com 丢失在梦里1年前1
丢失在梦里1年前1 -
 中原大虾 共回答了18个问题
中原大虾 共回答了18个问题 |采纳率94.4%1年前查看全部
- 下表是元素周期表的一部分,根据A-K在周期表中的位置,用元素符号或化学式回答下列问题.
下表是元素周期表的一部分,根据A-K在周期表中的位置,用元素符号或化学式回答下列问题.
(1)写出D、G的元素符号______、______
周期
族ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0 1 A 2 D F H 3 B C E G I J 4 K
(2)A到K中化学性质最不活泼的是______
(3)最高价氧化物对应的水化物碱性最强的是______(写化学式、下同),酸性最强的是______
(4)C的氢氧化物与I的氢化物反应的化学方程式:______
(5)请设计一个实验比较I和K单质氧化性的强弱______ 写出该反应的离子方程式为______. 晴天晴空1年前1
晴天晴空1年前1 -
 有97个昆虫 共回答了20个问题
有97个昆虫 共回答了20个问题 |采纳率95%解题思路:(1)由元素在周期表中位置,可知A为氢,B为Na,C为Al,D为碳,E为Si,F为氮,G为磷,H为氟,I为Cl,J为Ar,K为Br;(2)稀有气体的化学性质最不活泼;(3)上述元素中Na的金属性最强,故氢氧化钠碱性最强,F元素没有最高价含氧酸,上述元素中,最高价含氧酸中高氯酸的酸性最强;(4)氢氧化铝与盐酸反应生成氯化铝与水;(5)利用单质之间的相互置换进行验证.(1)由元素在周期表中位置,可知A为氢,B为Na,C为Al,D为碳,E为Si,F为氮,G为磷,H为氟,I为Cl,J为Ar,K为Br,故答案为:C;P;
(2)稀有气体Ar的化学性质最不活泼,故答案为:Ar;
(3)上述元素中Na的金属性最强,故NaOH的碱性最强,F元素没有最高价含氧酸,上述元素中,最高价含氧酸中HClO4的酸性最强,故答案为:NaOH;HClO4;
(4)氢氧化铝与盐酸反应生成氯化铝与水,反应方程式为:Al(OH)3+3HCl=AlCl3+3H2O,
故答案为:Al(OH)3+3HCl=AlCl3+3H2O;
(5)利用单质之间的相互置换进行验证,具体方案为:将氯水滴入溴化钠溶液中颜色变深,有关离子方程式为:Cl2+2Br-=2Cl-+Br2,
故答案为:将氯水滴入溴化钠溶液中颜色变深;Cl2+2Br-=2Cl-+Br2.点评:
本题考点: 元素周期律和元素周期表的综合应用.
考点点评: 本题考查元素周期表与元素周期律综合应用,难度不大,注意掌握非金属性、金属性强弱比较及实验事实.1年前查看全部
- Mg与N2反应电子式,就是元素符号外面很多点的那种
 cc的真善美1年前0
cc的真善美1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 用元素符号或化学式填空 3个硫原子 硝酸 8个水分子 2个镁离子
 mcse9804161年前0
mcse9804161年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 用元素符号或化学式填空:(1)3个氮分子______; (2)4个硫离子______;(3)n个铜
用元素符号或化学式填空:
(1)3个氮分子______;
(2)4个硫离子______;
(3)n个铜原子______;
(4)正五价的磷元素+5 P .+5 P  tudor_1年前1
tudor_1年前1 -
 shun504 共回答了17个问题
shun504 共回答了17个问题 |采纳率82.4%解题思路:(1)分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字.
(2)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字.
(3)原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.
(4)化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后.(1)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则三个氮分子可表示为:3N2.
(2)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字,故4个硫离子可表示为:4S2-.
(3)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故n个铜原子表示为:nCu.
(4)由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故正五价的磷元素可表示为:
+5
P.
故答案为;(1)3N2;(2)4S2-;(3)nCu;(4)
+5
P.点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本题难度不大,主要考查同学们对常见化学用语(原子符号、分子符号、化合价、离子符号等)的书写和理解能力.1年前查看全部
- 表是周期表中的一部分,根据A-I在周期表中的位置,用元素符号或化学式回答下列问题:
表是周期表中的一部分,根据A-I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是______,只有负价而无正价的是______,氧化性最强的单质是______,还原性最强的单质是______;族
周期ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0 1 A 2 D E G I 3 B C F H
(2)最高价氧化物的水化物碱性最强的是______,酸性最强的是______,呈两性的是______;
(3)A分别与D、E形成的化合物中,最稳定的______;
(4)在B、C、D、E、F、G、H中,原子半径最大的是______.
(5)B的最高价氧化物与C的最高价氧化物对应水化物溶液反应的离子方程式为______. 毁毁1年前1
毁毁1年前1 -
 chsitian 共回答了20个问题
chsitian 共回答了20个问题 |采纳率85%解题思路:根据元素在周期表中的位置知,A、B、C、D、E、F、G、H、I分别是H、Na、Al、C、N、P、F、Cl、Ne元素,
(1)表中元素,化学性质最不活泼的是稀有气体,只有负价而无正价的是F元素,元素的非金属性越强,其单质的氧化性越强;元素的金属性越强,其单质的还原性越强;
(2)元素的金属性越强,其最高价氧化物的水化物碱性越强,元素的非金属性越强,其最高价氧化物的水化物酸性越强(F、O除外),呈两性的是Al(OH)3;
(3)A分别与D、E形成的化合物分别是CH4、NH3,元素的非金属性越强,其氢化物越稳定;
(4)原子的电子层数越多其原子半径越大,同一周期元素中,原子半径随着原子序数的增大而减小;
(5)B的最高价氧化物的水化物是NaOH,C的最高价氧化物对应水化物是Al(OH)3,二者反应生成四羟基合铝酸钠.根据元素在周期表中的位置知,A、B、C、D、E、F、G、H、I分别是H、Na、Al、C、N、P、F、Cl、Ne元素,
(1)表中元素,化学性质最不活泼的是稀有气体为Ne,只有负价而无正价的是F元素,元素的非金属性越强,其单质的氧化性越强,所以单质氧化性最强的是F2;元素的金属性越强,其单质的还原性越强,所以单质还原性最强的是Na,故答案为:Ne;F;F2;Na;
(2)元素的金属性越强,其最高价氧化物的水化物碱性越强,金属性最强的是Na,所以碱性最强的是NaOH,元素的非金属性越强,其最高价氧化物的水化物酸性越强(F、O除外),所以元素最高价氧化物的水化物酸性最强的是 HClO4,呈两性的是Al(OH)3;
故答案为:NaOH;HClO4;Al(OH)3;
(3)A分别与D、E形成的化合物分别是CH4、NH3,元素的非金属性越强,其氢化物越稳定,元素的非金属性N>C,所以氢化物的稳定性氨气较稳定,故答案为:NH3;
(4)原子的电子层数越多其原子半径越大,同一周期元素中,原子半径随着原子序数的增大而减小,所以这几种元素中原子半径最大的是Na,故答案为:Na;
(5)B的最高价氧化物的水化物是NaOH,C的最高价氧化物对应水化物是Al(OH)3,二者反应生成四羟基合铝酸钠,离子方程式为OH-+Al(OH)3=[Al(OH)4]-,
故答案为:OH-+Al(OH)3=[Al(OH)4]-.点评:
本题考点: 元素周期律和元素周期表的综合应用.
考点点评: 本题考查了元素周期表和元素周期律的综合应用,熟记元素周期律并灵活运用元素周期律解答问题,题目难度不大.1年前查看全部
- 以下用元素符号或化学式表示干冰、天然气的主要成分、3个二氧化氮分子、2个磷原子、5个硫酸根离子.利用红磷除去空气中的氧气
以下用元素符号或化学式表示干冰、天然气的主要成分、3个二氧化氮分子、2个磷原子、5个硫酸根离子.利用红磷除去空气中的氧气的化学方程式
 xiaoping4u1年前1
xiaoping4u1年前1 -
 zeng2000n 共回答了10个问题
zeng2000n 共回答了10个问题 |采纳率100%干冰=CO2 天然气= CH4 3个二氧化氮分子=3NO 2个磷原子=2P 5个硫酸根离子=SO4 上面写2- 点燃 利用红磷除去空气中的氧气的化学方程式 = 4p + 2o2 ==== 2P2O5 (已配平~) 希望能帮到您~1年前查看全部
- 在短周期内1~18号元素内,用元素符号或化学式回答相关的问题.
在短周期内1~18号元素内,用元素符号或化学式回答相关的问题.
(1)除稀有气体外,原子半径最大的是______;离子半径最大的是______
(2)最高价氧化物对应的水化物呈两性的物质是______
(3)最高价氧化物对应的水化物酸性最强的是______ lljkent1年前1
lljkent1年前1 -
 CLON23 共回答了13个问题
CLON23 共回答了13个问题 |采纳率84.6%钠,硫离子,铝,氯1年前查看全部
- 那个中学化学元素符号的诗歌是什么?我记得开头是 氢是H 氧是O.还有,该怎样才能更快更牢的记住谁谁谁分别是第几元素?.
 11175201年前1
11175201年前1 -
 W0RCR 共回答了19个问题
W0RCR 共回答了19个问题 |采纳率89.5%碳是C,磷是P, 铅的符号是Pb. Cu铜,Ca钙, 钨的符号W. H氢,S硫, 硅的符号Si. 金Au,银Ag, 镁的符号Mg. 钠Na,氖Ne, 汞的符号Hg. 硼是B,钡Ba, 铁的符号Fe. 锌Zn,锰Mn, 锡的符号Sn. 钾是K,碘是I, 氟的符号是F. 氧是O,氮是N, 溴的符号是Br. Al铝,Cl氯,锑的符号Sb.1年前查看全部
- 用元素符号来表示物质组成(包括分之、原子、离子组成)的式子叫做_______,物质的化学式是由_______测定出来的.
 我的Moonblue1年前1
我的Moonblue1年前1 -
 semao123 共回答了16个问题
semao123 共回答了16个问题 |采纳率81.3%化学式
化合价1年前查看全部
- 酸用元素符号怎么表示,如碳酸钠元素符号为
 tianti121年前4
tianti121年前4 -
 快乐阳春面 共回答了19个问题
快乐阳春面 共回答了19个问题 |采纳率94.7%酸一般都带氧元素,碳酸钠为Na2CO3
硫酸钾:K2SO4等等1年前查看全部
- 氢用元素符号怎么表示
 zhxzhen1年前1
zhxzhen1年前1 -
 dream_xu 共回答了14个问题
dream_xu 共回答了14个问题 |采纳率85.7%H1年前查看全部
- 老师让背元素周期表,元素符号和相对原子质量,有没有快的方法
 又看繁华1年前1
又看繁华1年前1 -
 zhuliang1991 共回答了22个问题
zhuliang1991 共回答了22个问题 |采纳率100%我们都是五个五个来背的,没什么技巧,元素周期表必须死记硬背1年前查看全部
- 用元素符号或化学式表示 4个二氧化碳分子 3个钾原子 八个二氧化氮分子 七个氮原
用元素符号或化学式表示 4个二氧化碳分子 3个钾原子 八个二氧化氮分子 七个氮原
用元素符号或化学式表示 4个二氧化碳分子 3个钾原子 八个二氧化氮分子 七个氮原子 一个氢分子 深圳地王1年前1
深圳地王1年前1 -
 jgikgft 共回答了21个问题
jgikgft 共回答了21个问题 |采纳率95.2%4CO2 3K 8NO2 7N H21年前查看全部
- 用元素符号或化学式填空:2个五氧化二磷分子____
 纽纽0771年前1
纽纽0771年前1 -
 陈小夭 共回答了17个问题
陈小夭 共回答了17个问题 |采纳率82.4%2P2O5
第一个2,表示2个分子 ;第二个2,2为下标,表示每个五氧化二磷分子中含有两个P原子;第三个5,5为下标,表示每个五氧化二磷分子中含有5个O原子1年前查看全部
- 金属 活动顺序表 元素符号口诀
 蓝无痕1年前1
蓝无痕1年前1 -
 ttttttttaa 共回答了12个问题
ttttttttaa 共回答了12个问题 |采纳率83.3%对对对1年前查看全部
- 用元素符号或化学式表示:(1)氧元素______;(2)2个铁原子______;(3)两个镁离子______;(4)氢气
用元素符号或化学式表示:
(1)氧元素______;
(2)2个铁原子______;
(3)两个镁离子______;
(4)氢气______;
(5)氦气______;
(6)氧化铝______. 很初步1年前1
很初步1年前1 -
 梦舞九天 共回答了18个问题
梦舞九天 共回答了18个问题 |采纳率88.9%解题思路:(1)书写元素符号时应注意:①有一个字母表示的元素符号要大写;②由两个字母表示的元素符号,第一个字母大写,第二个字母小写.
(2)原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.
(3)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字.
(4)氢气属于气态非金属单质,在元素符号的右下角写上表示分子中所含原子数的数字.
(5)氦气属于稀有气体单质,直接用元素符号表示其化学式.
(6)氧化铝中铝元素显+3价,氧元素显-2价,写出其化学式即可.(1)氧元素的元素符号为:O.
(2)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个铁原子表示为:2Fe.
(3)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字,故两个镁离子可表示为:2Mg2+.
(4)氢气属于气态非金属单质,在元素符号的右下角写上表示分子中所含原子数的数字,其化学式为:H2.
(5)氦气属于稀有气体单质,直接用元素符号表示其化学式,其化学式为He.
(6)氧化铝中铝元素显+3价,氧元素显-2价,其化学式为Al2O3.
故答案为:(1)O;(2)2Fe;(3)2Mg2+;(4)H2;(5)He;(6)Al2O3.点评:
本题考点: 化学符号及其周围数字的意义;化学式的书写及意义.
考点点评: 本题难度不大,主要考查同学们对常见化学用语(元素符号、原子符号、化学式、离子符号等)的书写和理解能力.1年前查看全部
- 下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式回答:
下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式回答:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为______族
周期ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0 二 ① ② 三 ③ ④ ⑤ ⑥ ⑦ ⑧ 四 ⑨ ⑩
(2)地壳中含量最多的金属元素是______.
(3)用电子式表示②与④形成化合物的过程______.
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是______,碱性最强的是______,呈两性的氢氧化物是______.
(5)写出⑤与氢氧化钠反应的化学方程式:______.
写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式:______. 猪猪宝宝1年前0
猪猪宝宝1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 用元素符号或化学式等化学用语填空:(1).请用化学用语表示:5个钾原子______ 4个铵根离子______ 2
用元素符号或化学式等化学用语填空:(1).请用化学用语表示:5个钾原子______ 4个铵根离子______ 2
用元素符号或化学式等化学用语填空:
(1).请用化学用语表示:5个钾原子______4个铵根离子______2个氯离子______氧化铝中铝的化合价为+3价______二氧化硅______一个硫酸根离子______
(2)按要求写出下列数字“2”表达的含义:(每空1分)
①Mg2+______
②2
O______、______.+2 Fe
 子羽07251年前1
子羽07251年前1 -
 lubing1114 共回答了19个问题
lubing1114 共回答了19个问题 |采纳率89.5%(1)原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.所以2个钾原子,就可表示为 2K,故答案为:2K;
离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.但铵根离子是由多个原子组成的离子,整体带1个单元位的正电荷,表示为NH4+若表示多个该离子,就在其元素符号前加上相应的数字,所以答案为4NH4+;氯离子带一个单位负电荷,所以符号为:Cl-,2个氯离子为:2Cl-;由于硫酸根离子带了2个单位负电荷,所以一个硫酸根离子可表示为:SO42-;
元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,氧化铝中铝的化合价为+3价,可表示为
+3
Al2O3
氧化物的写法是其它元素写在左边,氧元素写在右边,数字写在该元素的右下角,所以二氧化硅表示为:SiO2 ;
(2)①右上角数字表示一个离子中所带的电荷数,所以表示一个镁离子带两个单位的正电荷;②数字后面是化学式表示分子个数,元素符号正上方的数字表示的是该元素所显的化合价,所以前面的2表示两个氧化亚铁分子,正上方的2表示氧化亚铁中铁元素显+2价.
故答案为:(1)5K;4NH4+;2Cl-;
+3
Al2O3;SiO2;SO42-;
(2)①一个镁离子带两个单位的正电荷;②两个氧化亚铁分子;氧化亚铁中铁元素显+2价.1年前查看全部
- 如图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空
如图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为______
族
周期ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0 二 ① ② 三 ③ ④ ⑤ ⑥ ⑦ ⑧ 四 ⑨ ⑩
(2)在这些元素中,地壳中含量最多的金属元素是______
(3)用电子式表示②与④形成化合物的过程______.
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是______,碱性最强的是______,呈两性的氢氧化物是______
(5)写出⑤与氢氧化钠溶液反应的化学方程式:______.
写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式:______.
(6)某元素R的气态氢化物为H X R,且R在该氢化物中的质量分数为94%,8.5g的H X R气体在标准状态下的体积是5.6L.则H X R的相对分子量为______;H X R的化学式为______. chendanzhi19841年前0
chendanzhi19841年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 下列各组元素中,元素符号的大写字母完全相同的是:
下列各组元素中,元素符号的大写字母完全相同的是:
氯、钙、铜
铝、银、氢
氖、钠、硅
镁、锰、锌 lzm88121年前1
lzm88121年前1 -
 一叶清舟my 共回答了11个问题
一叶清舟my 共回答了11个问题 |采纳率72.7%选氯、钙、铜.
氯Cl、钙Ca、铜Cu
铝Al、银Ag、氢H
氖Ne、钠Na、硅Si
镁Mg、锰Mn、锌Zn1年前查看全部
- 化学式的书写错误的类型主要有:A、元素符号或原子团书写错误;B、元素符号或原子团的顺序颠倒;C、遗漏括号;D、原子或离子
化学式的书写错误的类型主要有:A、元素符号或原子团书写错误;B、元素符号或原子团的顺序颠倒;C、遗漏括号;D、原子或离子个数未约分.试判断下列化学式的错误类型:并将其序号填在相应的位置.
序号 名称与化学式 错误类型(填序号) (1) 氧化钙Ca2O2 DD (2) 氯化铵NH3Cl AA (3) 氢氧化铝AlOH3 CC (4) 硫化锌SZn BB  pdslf1年前1
pdslf1年前1 -
 刀刀迷 共回答了24个问题
刀刀迷 共回答了24个问题 |采纳率91.7%解题思路:根据物质的名称来分析物质的组成元素,再利用构成来分析原子或离子个数的关系,从而得出化学式书写是否正确及错误的地方.(1)因氧化钙是由钙、氧元素组成,由化合价可知钙、氧离子个数相等,其化学式为CaO,
则Ca2O2中离子个数未约分,故答案为:D;
(2)因氯化铵是由铵根离子和氯离子构成,氯化铵的化学式为NH4Cl,则NH3Cl中原子团书写错误,
故答案为:A;
(3)因氢氧化铝是由铝离子和氢氧根离子构成,由铝的化合价为+3价,氢氧根的化合价为-1价,
则化学式为Al(OH)3,显然AlOH3中遗漏括号,故答案为:C;
(4)因硫化锌是由硫元素和锌元素组成,一般金属元素在前,则硫化锌的化学式为ZnS,显然SZn中
元素符号的顺序颠倒,故答案为:B.点评:
本题考点: 化学式的书写及意义.
考点点评: 本题考查化学式的书写,学生应熟悉物质的组成、构成、元素符号、原子团等来解答,明确化学式书写的规律和方法是解答的关键.1年前查看全部
- 用元素符号或化学式等化学用语填空:
用元素符号或化学式等化学用语填空:
(1)某气体在空气中占地着%(体积百分含量),保持5的化学性质的最小粒子是______;
(2)氢氧根离子______;
(3)地壳中含量最多的金属元素形成的离子______;
(了)含硫元素的质量分数为了0%的氧化物______. theseorthose1年前1
theseorthose1年前1 -
 周围人家 共回答了21个问题
周围人家 共回答了21个问题 |采纳率90.5%解题思路:(1)根据在空气中占78%(体积百分含量),保持它的化学性质的最小粒子是氮分子解答;
(2)根据离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字解答;
(3)根据地壳中含量最多的金属元素形成的离子是铝离子,写出离子符号;
(4)根据根据物质中某元素的质量分数=[元素原子的相对原子质量×原子个数/相对分子质量]×100%,进行解答;(1)在空气中占78%(体积百分含量)是氮气,保持他的化学性质的最左粒子是氮分子,其化学式为:N2.
(2)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1左电荷时,1要省略.若表示多左该离子,就在其离子符号前加上相应的数字,故氢氧根离子可表示为:OH-.
(3)地壳中含量最多的金属元素形成的离子是铝离子,铝离子可表示为:Al3+.
(4)设含硫元素的质量分数为40%的氧化物的化学式为SxOy;可得
40%=[32x/32x+16y×100%,解答
x
y=
1
3]由此可得 该氧化物的化学式为 SO3;
答案:
(1)N2 (2)OH- (3)Al3+ (4)SO3点评:
本题考点: 化学符号及其周围数字的意义.
考点点评: 本题难度不大,主要考查同学们对常见化学用语(分子符号、化学式、离子符号等)的书写和理解能力.1年前查看全部
- 初中化学第一学期那些需要必须背的有哪些、?例如元素符号等、
 zhuangzie1年前4
zhuangzie1年前4 -
 seedoef 共回答了19个问题
seedoef 共回答了19个问题 |采纳率94.7%首先必须把元素周期表前二十的元素背下来.
然后把常见离子符号记住恩.
于是还要记住常见物质化学方程式.(其实把常见的元素符号背下来,根据化学式名称拼写规则写就可以了.基本上不用记)
常见的化学方程式要记清楚.每个单元都有几个重点化学方程式.
相对原子质量那些不用记恩.用多了有的也记住了~考卷上是会告诉这些的.
常见元素的化合价要记住恩.
很多东西总是写啊总是写自然就记住了.可以编成顺口溜来记~
加油~(≥▽≤)/~1年前查看全部
大家在问
- 1语文一题★☆★☆沈石溪说:"动物小说折射的是人类社会.动物所拥有的独特的生存方式和生存哲学,应该引起同样具有生物属性的人
- 2金属能否在溶液中发生置换反应的依据是
- 3棱长为5厘米的正方体体积相当于多少个棱长为1分米的正方体体积
- 4根据半导体理论,一般半导体材料的电阻率和绝对温度之间的关系 要公式
- 5为什么一氧化氮,二氧化氮,氧气在两种混合比下溶于水无剩余
- 6-I heard that you _____ in a big company.What was it
- 7甲 ,乙两人去商店买东西,他们所带的钱数之比为7:6,甲用掉50元,乙用掉60元,二人余下钱数之比为3:2则余下钱数分别
- 8修改病句 开学初,我制定了学习计划和决心.
- 9关于乙醇,乙酸,苯,乙烯乙醇,乙酸,苯,乙烯这4中物质中,哪些可以加成,哪些可以取代哪些可以和溴水反应,又分别是什么反应
- 102点整时,时针与分针的夹角为60°,再过( )分钟,时针与分针第一次成60°角.保你加经验值
- 11一间教室宽6米,长是宽的1.5倍,裏面坐56个学生上课,平均每个学生约占多少平方米?(得数保留两位小数)
- 1230毫升的酒瓶,装满1千瓶,共计需要多少酒?
- 13(2012•安庆二模)如图所示,三位同学用同一组器材进行了下面三项操作:甲同学用水平方向的力拉木块A在长木板B上匀速运动
- 14某同学将浑浊的湖水样品倒入烧杯中,先加入白色粉末搅拌溶解,静置一会后,用下列图1所示的装置进行过滤,请问:
- 15为什么回答完问题不给采纳或感谢 我们帮你回答问题你好歹给个感谢大家都不容易