在——mol硫酸铝中含有0.3mol硫酸根离子,其中含有铝离子——个
 市井大人2022-10-04 11:39:543条回答
市井大人2022-10-04 11:39:543条回答
已提交,审核后显示!提交回复
共3条回复
 rao_wei 共回答了21个问题
rao_wei 共回答了21个问题 |采纳率95.2%- 在0.1mol硫酸铝中含有0.3mol硫酸根离子,其中含有铝离子0.2NA个
0.1mol Al2(SO4)3含有硫酸根离子0.1*3=0.3mol
含有铝离子0.1*2=0.2mol 1mol含有NA个 那么0.2mol含有0.2NA个 - 1年前
 倪侃 共回答了267个问题
倪侃 共回答了267个问题 |采纳率- 在0.1mol硫酸铝中含有0.3mol硫酸根离子,其中含有铝离子0.2NA个
- 1年前
 凉面vv 共回答了53个问题
凉面vv 共回答了53个问题 |采纳率- 0.1mol的Al2(SO4)3中含有0.3molSO4(2-),其中含有铝离子0.2mol,1.204*10^23个
- 1年前
相关推荐
- 请给出下列化学方程式及现象铝丝浸入硫酸镁溶液中铝丝浸入硫酸铜溶液中铝丝浸入硫酸铝溶液中铝丝浸入硝酸银溶液中
 huangming5211年前1
huangming5211年前1 -
 gg幽竹 共回答了12个问题
gg幽竹 共回答了12个问题 |采纳率75%铝丝浸入硫酸镁溶液中没有明显现象.(无)
铝丝浸入硫酸铜溶液中铝条表面附有一层红铜,直观现象为铝条变红.(化学方程式 2Al+3CuSo4=3Cu+Al2(So4)3 )
铝丝浸入硫酸铝溶液中没有明显现象.
铝丝浸入硝酸银溶液中铝条表面先附有一层白色物质,后迅速变黑.(银被氧化) 化学方程式 Al+3AgNO3=3Ag+Al(NO3)3 ,4Ag+O2=2Ag2O1年前查看全部
- 20g铜锌铝混合,与500g 盐酸完全反应,生成物晒干后有68g 硫酸铝,硫酸铜,硫酸锌,求生成氢气多少?
 抒蕾2201年前1
抒蕾2201年前1 -
 looking4murong 共回答了21个问题
looking4murong 共回答了21个问题 |采纳率95.2%0.83g,应该是与硫酸反应吧,题目写与盐酸反应了.
硫酸根的质量是68-20=48g
SO42-和H2都来自于H2SO4,现在知道了SO42-的质量,用SO42-的质量除以H2SO4中SO42-的质量分数得到的就是H2SO4的质量,H2SO4的质量减去SO42-的质量就是H2的质量.
H2SO4的质量是40/(96/98)=40.83g
生成H2的质量是40.83-40=0.83g1年前查看全部
- 懂化学的来:硫酸铝与硫酸铵反应,求质量比
懂化学的来:硫酸铝与硫酸铵反应,求质量比
已知硫酸铝中三氧化二铝含量为15.6%,硫酸铵含量为氮含量21%,求质量比是多少? kangtazm1年前4
kangtazm1年前4 -
 绝望的土豆片 共回答了17个问题
绝望的土豆片 共回答了17个问题 |采纳率88.2%Al2(SO4)3,分子量342.15 Al2O3 94
mol硫酸铝~1mol氧化铝
硫酸铝铵中氧化铝的含量为47/233=27.5% 其纯度15.6/27.5=56.7%
(NH4)2SO4 132 N 14
1mol硫酸铵~2molN 28/132=21% 其纯度100%
Al2(SO4)3+(NH4)2SO4+12H2O→2NH4Al(SO4)2·12H2O
342 132
56.7 21.8
质量比56.7 :21.8= 2.6 :11年前查看全部
- 在氯化铝和硫酸铝的混合溶液中,已知铝离子和氯离子个数比为5:3,若溶液中铝离子数为5n时,则硫酸根离子的个数约为( )
在氯化铝和硫酸铝的混合溶液中,已知铝离子和氯离子个数比为5:3,若溶液中铝离子数为5n时,则硫酸根离子的个数约为( )
A. 8n
B. 4n
C. 6n
D. 2n 小猪啃大熊1年前1
小猪啃大熊1年前1 -
 haha127 共回答了15个问题
haha127 共回答了15个问题 |采纳率93.3%解题思路:在氯化铝中,铝离子和氯离子的个数比是1:3,在硫酸铝中,铝离子和硫酸根离子的个数比是2:3.硫酸铝和氯化铝的个数比是2:1时,铝离子和氯离子个数比为5:3,因为每2个硫酸铝中含有4个铝离子,每1个氯化铝中含有1个铝离子和3个氯离子;若溶液中铝离子数为5n时,硫酸铝的个数是2n,则硫酸根离子的个数约为6n.
故选C.点评:
本题考点: 化学式的书写及意义;常见元素与常见原子团的化合价.
考点点评: 解答本题要掌握氯化铝和硫酸铝中阳离子和阴离子个数比,再根据相关方面的数据进行分析、判断,从而得出正确的结论.1年前查看全部
- 用硫化钠溶液加入到硫酸铝中将得到什么产物
 lanqianwei371年前1
lanqianwei371年前1 -
 1221326358 共回答了14个问题
1221326358 共回答了14个问题 |采纳率85.7%双水解.硫酸钠,氢氧化铝,硫化氢1年前查看全部
- 酸碱滴定反应配置了100mL的硫酸和硫酸铝的混合液,用浓度为0.2mol|L的氢氧化钠溶液作滴定反应,得到pH值走势图.
酸碱滴定反应
配置了100mL的硫酸和硫酸铝的混合液,用浓度为0.2mol|L的氢氧化钠溶液作滴定反应,得到pH值走势图.如下图 V是滴定反应中碱的体积
问题:分析图像,AB BC DE EF每段图像是分别表示什么反应?
先说我的答案:AB段应该是酸碱中和反应,理由是,B点是拐角点,应该是表示出现第一个沉淀物分子
BC是铝离子和碱生成沉淀物,理由是,pH值不变
DE段应该是沉淀物和碱生成偏铝酸钠,E点是拐角点,表示最后一个沉淀物消失.
我不知道这样分析对不对,因为我无法说明AB段,为什么pH值是3.8,而不是7.而且CD段为什么有个PH的突变?
希望网友能够帮忙解答.谢谢

 冷寒夜1年前2
冷寒夜1年前2 -
 he1234 共回答了20个问题
he1234 共回答了20个问题 |采纳率100%你分析的是正确的.
AB就是酸碱中和,最后在B点溶液变为了硫酸铝,铝离子的水解程度比较大,所以溶液PH=3.8,然后BC开始产生沉淀,这点也符合事实,事实上PH1年前查看全部
- 硫酸铝是由+3价的铝元素和-2价的硫酸根组成写出其化学式
 longlzf1年前3
longlzf1年前3 -
 林中空地568 共回答了18个问题
林中空地568 共回答了18个问题 |采纳率77.8%Al2(SO4)31年前查看全部
- 1mol/L的 AL2(SO4)3 [硫酸铝]溶液 中 AL3+离子是2mol每升吗?
1mol/L的 AL2(SO4)3 [硫酸铝]溶液 中 AL3+离子是2mol每升吗?
或者要考虑铝离子的水解? saool1年前1
saool1年前1 -
 wutuliang 共回答了8个问题
wutuliang 共回答了8个问题 |采纳率100%不是,铝形成的碱是弱碱(弱酸根和弱碱根在水中都要发生水解).铝在水中要发生水解反应是 Al3+3H2O=Al3(OH)3+3H+ 从而铝的浓度就不可能是2mol每升,只可能比它小.1年前查看全部
- 1.碳酸钠在水中的电离方程式 2.硫酸 3.硝酸 4.硝酸铜 5.碳酸氢钙 6.硝酸铵 7.硫酸铝 8.高锰酸钾 9.氯
1.碳酸钠在水中的电离方程式 2.硫酸 3.硝酸 4.硝酸铜 5.碳酸氢钙 6.硝酸铵 7.硫酸铝 8.高锰酸钾 9.氯酸钾 10.氢氧化钙 11.磷酸钠 12.硝酸钡 13 氯化铁 14.氯化铵
 wyjie20021年前1
wyjie20021年前1 -
 liulimei 共回答了23个问题
liulimei 共回答了23个问题 |采纳率82.6%1.Na2CO3==2Na++HCO3- 2.H2SO4==2H++SO42- 3.HNO3==H++NO3- 4.Cu(NO3)2==Cu2++2NO3- 5.Ca(HCO3)2==Ca2++2HCO3- 6.NH4NO3==NH4++NO3- 7.Al2(SO4)3==2Al3++3SO42- 8.KMnO4==K++MnO4- 9.KCl==K++Cl- 10.Ca(OH)2==Ca2++2OH- 11.Na3PO4==3Na++PO43- 12.Ba(NO3)2==Ba2++2NO3- 13.FeCl3==Fe3++3Cl- 14.NH4Cl==NH4++Cl-1年前查看全部
- 硫酸铝溶液与少量(过量)氨水分别反应的化学方程式
硫酸铝溶液与少量(过量)氨水分别反应的化学方程式
1.硫酸铝溶液与少量氨水反应
2.硫酸铝溶液与过量氨水反应
3.硝酸铵溶液与氢氧化钠溶液加热
4.硫酸铵溶液与氢氧化钡溶液反应
5.氯化铝溶液与过量的氢氧化钠溶液反应
6.氯化铝溶液逐渐加入氢氧化钠溶液至过量
7.氨被氧化铜氧化
8.二氧化硫气体使氯化铁溶液变成浅绿色
麻烦大家会写哪个就写出来、一定要正确的喔. cancerdumb1年前2
cancerdumb1年前2 -
 甜心sweet 共回答了18个问题
甜心sweet 共回答了18个问题 |采纳率88.9%1.Al2(SO4)3+6NH3·H2O==2Al(OH)3↓+3(NH4)2SO4
2.少量过量没区别吧
3.NH4NO3+NaOH=NaNO3+NH3+H2O
4.(NH4)SO4+Ba(OH)2=BaSO4(沉淀符号)+NH3.H2O
5.AlCl3+3NaOH=Al(OH)3+3NaCl
6.AlCl3+3NaOH=Al(OH)3+3NaCl
Al(OH)3+NaOH=NaAlO2+2H2O
7.2NH3+3CuO=N2+3Cu+3H2O(加热)
8.2FeCl3+SO2+2H2O=2FeCl2+H2SO4+2HCl1年前查看全部
- 硫酸铝和偏铝酸钠大反应
 盛泽阿狗1年前1
盛泽阿狗1年前1 -
 多喝头不疼 共回答了24个问题
多喝头不疼 共回答了24个问题 |采纳率87.5%Al2(SO4)3 + 6NaAlO2 + 12H2O = 8Al(OH)3↓ + 3Na2SO41年前查看全部
- 向0.02mol的硫酸铝溶液中加入30ml氢氧化钠溶液 充分反应得到0.78克沉淀 求氢氧化钠物质的量浓度(2个答案
 teamos1年前2
teamos1年前2 -
 小脚香香 共回答了24个问题
小脚香香 共回答了24个问题 |采纳率91.7%1、氢氧化钠不足,即铝元素以氢氧化铝和铝离子的形式存在
n(NaOH)=(0.78÷78)×3=0.03mol
c(NaOH)=0.03÷0.03=1mol/L
2、氢氧化钠较多,即铝元素以氢氧化铝和偏铝酸根的形式存在
n(NaOH)=0.02×2×4-(0.78÷78)=0.15mol
c(NaOH)=0.15÷0.03=5mol/L1年前查看全部
- 化学式硫酸铝Al2(SO4)3中正电荷是多少?负电荷是多少?
 拾乐斋1年前1
拾乐斋1年前1 -
 kisswlj 共回答了21个问题
kisswlj 共回答了21个问题 |采纳率90.5%每个铝离子带3个正电荷,每个硫酸根带2个负电荷.一个硫酸铝有6个正电荷和负电荷1年前查看全部
- 少量浓氨水滴入硫酸铝溶液中.
 im1231年前1
im1231年前1 -
 芝道111 共回答了17个问题
芝道111 共回答了17个问题 |采纳率88.2%浓氨水和铝离子生成偏铝酸更离子1年前查看全部
- 0.5mol的硫酸铝中铝离子的物质的量?
 嘬了一大口1年前1
嘬了一大口1年前1 -
 阿修罗之吻 共回答了20个问题
阿修罗之吻 共回答了20个问题 |采纳率100%0.5mol的硫酸铝中铝离子的物质的量=1mol1年前查看全部
- 在一定量硫酸铝和硫酸锌中,硫酸离子物质的量共2摩尔,吕离子和锌离子物质的量比为2:3,求硫酸锌质量.
在一定量硫酸铝和硫酸锌中,硫酸离子物质的量共2摩尔,吕离子和锌离子物质的量比为2:3,求硫酸锌质量.
请每一步详细讲解
为什么硫酸铝与硫酸锌之比为1:硫酸离子的比为1:1呢?
请速回答 wlw3151年前4
wlw3151年前4 -
 jackychou1225 共回答了14个问题
jackychou1225 共回答了14个问题 |采纳率92.9%硫酸锌的质量=硫酸锌的物质的量*(65+32+16*4)
设锌的物质的量为3x铝的为2x
则有3x+2x/2*3=2 mol
得x=1/3
硫酸锌物质的量为1 mol
所以 硫酸锌的质量为161
三楼是烂写的~怎么可能还有硫酸根离子之比呢?我这个是计算出来的~最原始~最准确~最易懂~你看得懂吗?1年前查看全部
- 以下离子方程式如何书写?硫酸铝溶液中通入过量氨水 稀硫酸中加入铁粉 醋酸溶液与水垢中的碳酸钙反应
 power5981年前3
power5981年前3 -
 塞北银狐 共回答了15个问题
塞北银狐 共回答了15个问题 |采纳率93.3%1.硫酸铝溶液与氨水反应可生成氢氧化铝沉淀和硫酸铵,氢氧化铝不能溶于弱碱,
则该反应为Al2(SO4)3+3NH3.H2O═2Al(OH)3↓+3(NH4)2SO4,
其离子反应为2Al3++3NH3.H2O═2Al(OH)3↓+3NH4+,
2.Fe+2H+=Fe2++H2↑
3.CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O1年前查看全部
- 铁与下列物质溶质中反应,溶液增加的是( ) 硫酸铝 硫酸铜 硫酸 硝酸银
 ssqy0011年前4
ssqy0011年前4 -
 小豆丁 共回答了21个问题
小豆丁 共回答了21个问题 |采纳率95.2%硫酸
活泼性:Al>Fe>(H2)>Cu>Ag
Fe+H2SO4=FeSO4+H2↑
Fe+CuSO4=FeSO4+Cu
Fe+3AgNO3=Fe(NO3)3+3Ag
铁与硫酸铝不反应
相对原子量:Ag>Cu>Fe>Al>(H2)
找既反应,又比铁“轻”的 对应的溶液,即是硫酸.1年前查看全部
- .将0.1mol/L的硫酸钾溶液,0.2mol/L的硫酸铝溶液和纯水混合
.将0.1mol/L的硫酸钾溶液,0.2mol/L的硫酸铝溶液和纯水混合
,要使混和溶液中 的浓度分别为0.1mol/L,0.1mol/L,0.2mol/L,则所取三种溶液的体积比依次是
A.x051:1:1 B.2:1:2 C.1:1:2 D.2:1:1 tornado2003com1年前2
tornado2003com1年前2 -
 jaenking 共回答了20个问题
jaenking 共回答了20个问题 |采纳率90%设溶液混合后有XL,则钾离子.铝离子.硫酸根离子的物质的量为:0.1Xmol,0.1Xmol,0.2Xmol
原硫酸钾溶液中钾离子的浓度为0.2mol/L硫酸根离子0.1mol/L
原硫酸铝溶液中氯离子浓度为0.4mol/L硫酸根离子0.6mol/L
则可以得出需要0.1X/0.2L的原硫酸钾溶液
0.1X/0.4L的原硫酸铝溶液
X-0.1X/0.2-0.1X/0.4的纯水
最后得出1/2:1/4:1/4=2:1:11年前查看全部
- 将硫酸钾,硫酸铝,硫酸铝钾三种盐混合后溶于硫酸酸化的水中
将硫酸钾,硫酸铝,硫酸铝钾三种盐混合后溶于硫酸酸化的水中
测得c(SO42-)=0.105mol/L,c(Al3+)=0.055mol/L
c(K+)=0.035mol/L求该溶液的pH…… 天龙啸风1年前1
天龙啸风1年前1 -
 非常道618 共回答了20个问题
非常道618 共回答了20个问题 |采纳率95%根据溶液呈电中性求解.
溶液中只含有阴离子SO42-,阳离子有K+、Al3+、H+
据此可以列式:0.105*2=c(H+)+0.055*3+0.035(注意离子带电荷数)
计算得c(H+)=0.03mol/L
然后就可以求出pH了1年前查看全部
- 为什么向硫酸铝中加过量的氢氧化钠溶液在加了三摩尔的铝离子后生成的沉淀最多
 潭江马1年前3
潭江马1年前3 -
 牛牛走过 共回答了26个问题
牛牛走过 共回答了26个问题 |采纳率88.5%铝离子+氢氧根(3摩尔)=氢氧化铝(沉淀)
氢氧化铝+氢氧根(1摩尔)=偏铝酸钠1年前查看全部
- 完成下列离子方程式。⑴醋酸钠溶液中加入足量的稀硫酸:___________________________。⑵硫酸铝溶液
完成下列离子方程式。
⑴醋酸钠溶液中加入足量的稀硫酸:___________________________。
⑵硫酸铝溶液中加入过量氨水:____________________________。
⑶电解MgCl 2 溶液:___________________________。
⑷NaHCO 3 溶液加足量石灰水:_____________________________。 66684281年前1
66684281年前1 -
 我输光了 共回答了17个问题
我输光了 共回答了17个问题 |采纳率100%⑴CH 3 COO - +H + = CH 3 COOH;⑵Al 3+ +3NH 3 . H 2 O=Al(OH) 3 ↓+3NH 4 + ;⑶Mg 2 + +2Cl - +2H 2 O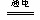 H 2 ↑+ Cl 2 ↑+Mg(OH) 2 ↓;⑷HCO 3 - +Ca 2+ + OH - = CaCO 3 ↓+ H 2 O。
H 2 ↑+ Cl 2 ↑+Mg(OH) 2 ↓;⑷HCO 3 - +Ca 2+ + OH - = CaCO 3 ↓+ H 2 O。
⑴醋酸钠溶液中加入稀硫酸生成弱电解质CH 3 COOH,其离子方程式为:CH 3 COO - +H + = CH 3 COOH;⑵硫酸铝溶液中加入过量氨水,生成的Al(OH) 3 沉淀不会继续溶解到过量的氨水中,其离子方程式为:Al 3+ +3NH 3 . H 2 O=Al(OH) 3 ↓+3NH 4 + ;⑶电解MgCl 2 溶液生成的OH - 会与Mg 2 + 生成Mg(OH) 2 沉淀,其离子方程式为:Mg 2 + +2Cl - +2H 2 O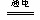 H 2 ↑+ Cl 2 ↑+Mg(OH) 2 ↓;⑷NaHCO 3 溶液加足量石灰水反应,首先是HCO 3 - + OH - = CO 3 2 - + H 2 O,然后生成的CO 3 2 - 与Ca 2+ 反应生成CaCO 3 沉淀,其总离子方程式为:HCO 3 - +Ca 2+ + OH - = CaCO 3 ↓+ H 2 O。
1年前查看全部
H 2 ↑+ Cl 2 ↑+Mg(OH) 2 ↓;⑷NaHCO 3 溶液加足量石灰水反应,首先是HCO 3 - + OH - = CO 3 2 - + H 2 O,然后生成的CO 3 2 - 与Ca 2+ 反应生成CaCO 3 沉淀,其总离子方程式为:HCO 3 - +Ca 2+ + OH - = CaCO 3 ↓+ H 2 O。
1年前查看全部
- 向氢氧化钠中逐滴加入硫酸铝溶液 向硫酸铝溶液中逐滴加入氢氧化钠
 zyc852101年前1
zyc852101年前1 -
 gmj0416 共回答了19个问题
gmj0416 共回答了19个问题 |采纳率89.5%出不出现沉淀咋地.
向氢氧化钠中逐滴滴加硫酸铝溶液先是氢氧根过量发生Al3+ + 4OH- =AlO2- + 2H2O 没有沉淀
随着硫酸铝加入铝离子过量发生反应Al3+ + 3AlO2 - + 6H2O == 4Al(OH)3↓ 生成白色沉淀
向硫酸铝中逐滴滴加Al2(SO4)3 + 6NAOH == 2Al(OH)3 + 3NA2SO4(加少量氢氧化钠,出白色沉淀)Al(OH)3 + NaOH == NaAlO2 + 2H2O(随着氢氧化钠的过量,白色沉淀消失)1年前查看全部
- 怎么除去硫酸钠废水中的硫酸铝,考虑过变成氢氧化铝,但是要怎么控制
 ljt577231年前3
ljt577231年前3 -
 songweian 共回答了20个问题
songweian 共回答了20个问题 |采纳率85%首先不能碱过量,这个你知道了,人为控制很难做到不过量然后就要考虑pH值.加Na2CO3可以让Al3+与CO2-发生双水解,不用担心pH值的问题.过量Na2CO3加入后,铝离子就沉淀了这时候用漏斗滤纸过滤,取滤液,滴加稀硫酸,滴到没...1年前查看全部
- 氯化钙氯化锌氯化钡氯化铝氯化钾氯化银氯化铁氯化亚铁氯化铜氯化亚铜硫酸钠硫酸铜硫酸锌硫酸镁硫酸钡硫酸钙硫酸铝硫酸铁硫酸亚铁
氯化钙
氯化锌
氯化钡
氯化铝
氯化钾
氯化银
氯化铁
氯化亚铁
氯化铜
氯化亚铜
硫酸钠
硫酸铜
硫酸锌
硫酸镁
硫酸钡
硫酸钙
硫酸铝
硫酸铁
硫酸亚铁
硫酸铵
硫酸钾
碳酸钙
碳酸钾
碳酸钠
碳酸银
碳酸钡
碳酸镁
碳酸锌
碳酸铵
硝酸钾
硝酸钠
硝酸银
硝酸钙
硝酸镁
硝酸钡
硝酸锌
硝酸铜
硝酸铁
硝酸亚铁
硝酸铵
硝酸汞 海岸之珠1年前2
海岸之珠1年前2 -
 charmcao 共回答了20个问题
charmcao 共回答了20个问题 |采纳率100%氯化钙CaCl2
氯化锌ZnCl2
氯化钡BaCL2
氯化铝AlCl3
氯化钾KCl
氯化银AgCl
氯化铁FeCl3
氯化亚铁FeCl2
氯化铜CuCl2
氯化亚铜CuCl
硫酸钠Na2SO4
硫酸铜CuSO4
硫酸锌ZnSO4
硫酸镁MgSO4
硫酸钡BaSO4
硫酸钙CaSO4
硫酸铝Al2(SO4)3
硫酸铁Fe2(SO4)3
硫酸亚铁FeSO4
硫酸铵(NH4)2SO4
硫酸钾K2SO4
碳酸钙CaCO3
碳酸钾K2CO3
碳酸钠Na2CO3
碳酸银Ag2CO3
碳酸钡BaCO3
碳酸镁MgCO3
碳酸锌ZnCO3
碳酸铵(NH4)2CO3
硝酸钾KNO3
硝酸钠NaNO3
硝酸银AgNO3
硝酸钙Ca(NO3)2
硝酸镁Mg(NO3)2
硝酸钡Ba(NO3)2
硝酸锌Zn(NO3)2
硝酸铜Cu(NO3)2
硝酸铁Fe(NO3)3
硝酸亚铁Fe(NO3)2
硝酸铵NH4NO3
硝酸汞Hg(NO3)21年前查看全部
- 关于质量守恒定律的题目1.常用的泡沫灭火器中有硫酸铝和碳酸氢钠两种溶液,灭火时发生反应的化学方程式为:AI2(SO4)3
关于质量守恒定律的题目
1.常用的泡沫灭火器中有硫酸铝和碳酸氢钠两种溶液,灭火时发生反应的化学方程式为:AI2(SO4)3+6NaHCO3→3Na2SO4+2X↓+6CO2 ↑,则X所表示的物质的化学式为_____.
2.生活离不开水.在日常生活中常需要净化水.
1)茶杯内的纱网可将茶叶与茶水分离,便于饮用,该设计利用的化学原理是_______.
2)自制净水器常加入________,用于除去水中的异味和色素.
3)游泳池水中常加入漂白粉目的是___________.其中制取漂白粉的反应原理是______.
Ca(CIO)2是漂白粉的有效成份,该物质中CI的化合价为_________.
4)明矾(KAI(SO4)2▪12H2O),式量为_________.
有过程的话最好了, connie20041年前2
connie20041年前2 -
 yenian96 共回答了20个问题
yenian96 共回答了20个问题 |采纳率100%1 根据质量守恒定律,原子个数守恒可知 x:Al(OH)3
2 过滤;活性炭;消毒、漂白;2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O;+1
4741年前查看全部
- 在200mL 1moL/L 硫酸铝溶液中,加入2moL/L氢氧化钠溶液后,产生15.6g的沉淀时,消耗氢氧化钠溶液的体积
在200mL 1moL/L 硫酸铝溶液中,加入2moL/L氢氧化钠溶液后,产生15.6g的沉淀时,消耗氢氧化钠溶液的体积为? 有两种答案,要计算过程的.
 fly_12091年前1
fly_12091年前1 -
 hq19 共回答了14个问题
hq19 共回答了14个问题 |采纳率92.9%硫酸铝与氢氧化钠反应式如下:Al2(SO4)3 + 6NaOH = 3Na2SO4 + 2Al(OH)3↓ 依据反应式,15.6g氢氧化铝沉淀的量为15.6/78=0.2mol,硫酸铝的量为0.2*1=0.2mol,说明反应不完全,氢氧化钠不过量.消耗氢氧化钠溶液的体积为 15.6g / 78g/mol * 6 / 2 / 2moL/L = 0.3L = 300ml 注:式中6 / 2为反应式中氢氧化钠与氢氧化铝的量的比;78g/mol为氢氧化铝的摩尔质量.1年前查看全部
- 硫酸铝溶液加热蒸发后得到的固体是什么?亚硫酸钠溶液蒸干得到的固体是----原因
 泪落心海1年前2
泪落心海1年前2 -
 雪城哀怜 共回答了16个问题
雪城哀怜 共回答了16个问题 |采纳率100%硫酸铝家人蒸发后得到的应该是硫酸铝的水合物,即十六水硫酸铝,具体的产物是什么要看加热到什么程度,86.5℃时失去部分结晶水,250℃失去全部结晶水,如果是加强热会分解为三氧化硫和氧化铝.
亚硫酸钠溶液蒸干得到的固体,若不和空气接触,得到的事亚硫酸钠的水合物,加热到150℃失去结晶水,温度在高则易分解为硫酸钠和硫化钠的混合物;若和空气接触,则蒸发得到的是硫酸钠.
补充:铝离子在加热条件下水解,水解产物为氢氧化铝和氢离子,而氢氧化铝是弱碱,不能与氢离子共存;若想铝离子水解成氢氧化铝,则对应的酸根应为弱酸酸根,硫酸根是强酸的酸根离子.1年前查看全部
- 请教几个离子方程式1用惰性电极电解硫酸铜溶液2在硫酸铝溶液中加入偏铝酸钠溶液3在酸性高锰酸钾溶液中滴加双氧水产生气体4金
请教几个离子方程式
1用惰性电极电解硫酸铜溶液
2在硫酸铝溶液中加入偏铝酸钠溶液
3在酸性高锰酸钾溶液中滴加双氧水产生气体
4金属镁和氯化铁溶液共热
(能写几个都可以) 含笑31年前3
含笑31年前3 -
 我只喜欢ァ 共回答了17个问题
我只喜欢ァ 共回答了17个问题 |采纳率94.1%1用惰性电极电解硫酸铜溶液
2Cu(2+)+2H2O==2Cu+4H(+)+O2
2在硫酸铝溶液中加入偏铝酸钠溶液
Al(3+)+3AlO2(-)+6H2O=4Al(OH)3
3在酸性高锰酸钾溶液中滴加双氧水产生气体
5H2O2+2MnO4(-)+6H(+)=2Mn(2+)+5O2+8H2O
4金属镁和氯化铁溶液共热
2Fe(3+)+Mg=2Fe(2+)+Mg(2+)
2Fe(3+)+3H2O===2Fe(OH)3+6H(+)
Mg+2H(+)=Mg(2+)+H21年前查看全部
- 硫酸铝水解方程式,再解释铝为什么不守恒?
 ada_jiajia1年前2
ada_jiajia1年前2 -
 yihg123 共回答了16个问题
yihg123 共回答了16个问题 |采纳率100%Al2(SO4)3 + 6H2O = 2Al(OH)3 + 3H2SO4
守恒不守恒得从什么角度来看,如果是从整个反应体系来看,还是守恒的1年前查看全部
- 【急】向硫酸铝溶液中通入氨气反应离子式
 我爱迪士尼1年前1
我爱迪士尼1年前1 -
 renmiss 共回答了19个问题
renmiss 共回答了19个问题 |采纳率94.7%Al3+ +3 NH3+ 3H2O=Al(OH)3+ 3NH4+1年前查看全部
- 硫酸、氢氧化钾、氢氧化钡、硫酸钠、硫酸铝、盐酸在水中发生电离的电离方程式
 火星蟑螂1年前2
火星蟑螂1年前2 -
 全额为如下 共回答了20个问题
全额为如下 共回答了20个问题 |采纳率90%H2SO4=2H++SO42-
KOH=K++OH-
Ba(OH)2=Ba2++2OH-
Na2SO4=2Na++SO42-
Al2(SO4)3=2Al3++3SO42-
HCl=H++Cl-1年前查看全部
- Vml硫酸铝溶液中含有mgsSO42-,则溶液中AL3+物质的量浓度
Vml硫酸铝溶液中含有mgsSO42-,则溶液中AL3+物质的量浓度
选项分别是 250m/48v 250m/72v 125m/18v 125m/72v 哪个正确 象鸟一样飞翔的心1年前4
象鸟一样飞翔的心1年前4 -
 han325120 共回答了23个问题
han325120 共回答了23个问题 |采纳率95.7%应该是125m/18v .
因为硫酸根的质量为m (mg),换算为摩尔数浓度为:C = 1000m / ( 96 × v ) (mol/L)
又因为Al2(SO4)3 == 2Al3+ + 3(SO4)2-;
所以,折算为 [Al3+] 摩尔浓度为:
[Al3+] = C / 3 ×2
= 2000m / ( 3×96 × v )
= 125m / 18v (mol/L)1年前查看全部
- 下列离子方程式中,正确的是( ) A.氨水与硫酸铝溶液反应:Al 3 + +3OH - =Al(OH) 3 ↓ B.稀
下列离子方程式中,正确的是()
A.氨水与硫酸铝溶液反应:Al 3 + +3OH - =Al(OH) 3 ↓ B.稀硫酸滴在铜片上:Cu+2H + =Cu 2 + +H 2 ↑ C.氢氧化铝与盐酸反应:Al(OH) 3 +3H + =Al 3 + +3H 2 O D.铜片插入硝酸银溶液中:Cu+Ag + =Cu 2 + +Ag  pepsimm1年前1
pepsimm1年前1 -
 有人叫我丫头 共回答了18个问题
有人叫我丫头 共回答了18个问题 |采纳率94.4%C
1年前查看全部
- 写出下列物质溶于水的电离方程式(1)氢氧化钙(2)硫酸铝(3)硝酸铵(4)硫酸氢钠
 shellyhxh1年前2
shellyhxh1年前2 -
 hzlopo 共回答了15个问题
hzlopo 共回答了15个问题 |采纳率86.7%1:ca+ OH-
2:AL3+ SO4 2-
3:NH4+ NO3-
4:HSO4- NA+1年前查看全部
- 硫酸铝可除去碱性废水中的悬浮颗粒,不能除去酸性废水中的悬浮颗粒,是因为酸抑制水解吗?为什么?为什么碱性废水中的就可以除去
硫酸铝可除去碱性废水中的悬浮颗粒,不能除去酸性废水中的悬浮颗粒,是因为酸抑制水解吗?为什么?为什么碱性废水中的就可以除去?碱会促进水解吗?
 太阳日眼1年前1
太阳日眼1年前1 -
 bocog1876 共回答了22个问题
bocog1876 共回答了22个问题 |采纳率72.7%是因为酸抑制水解.
硫酸铝可除去碱性废水中的悬浮颗粒是利用铝水解生成的Al(OH)3,如果水中含酸,铝的水解被抑制,自然就不起作用了.
碱可以促进铝的水解.有利于除去碱性废水中的悬浮颗粒.1年前查看全部
- 某混合物中含有硫酸钠和硫酸铝,经实验测知,硫元素的质量分数为25%,则该混合物中铝元素的的质量分数为?
 sweetttea1年前2
sweetttea1年前2 -
 小小小爱心 共回答了17个问题
小小小爱心 共回答了17个问题 |采纳率94.1%设Na2SO4和Al2(SO4)3物质的量分别是x和y
则有:(32x+96y)/(142x+342y)=25%
得x:y=3:1(142x+342y)
所以Na2SO4和Al2(SO4)3物质的量之比=3:1
所以铝元素的质量分数=2*27/(142*3+342)=7%1年前查看全部
- 有下列七种溶液:A、氢氧化钠溶液;B、氢氧化钡溶液;C、硫酸铝溶液;D、明矾溶液;E、混有少量硝酸的硫酸镁溶液;F、氯化
有下列七种溶液:A、氢氧化钠溶液;B、氢氧化钡溶液;C、硫酸铝溶液;D、明矾溶液;E、混有少量硝酸的硫酸镁溶液;F、氯化铁溶液;任取其中的一种溶液(甲)逐滴加入到另一种溶液(乙)中至过量,观察到自始至终均有白色沉淀.试回答下列问题:
(1)产生上述实验现象的试剂组合有(请用字母代号逐一列出,表格各栏可填满,可不填满,也可补充)
(2)请在下列坐标中作出第1组实验所得沉淀的物质的量(n 沉淀 /mol)随B溶液体积(V B /L)变化的曲线.组别 1 2 3 4 5 6 7 8 甲 B 乙 D
(3)如图是某一组实验中所得沉淀的物质的量(n 沉淀 /mol)随甲溶液中溶质的物质的量(n 甲 /mol)变化的曲线.符合图(右)曲线的试剂组合是:甲______(填化学式)、乙______(填化学式).
 999感冒药1年前1
999感冒药1年前1 -
 接龙822 共回答了20个问题
接龙822 共回答了20个问题 |采纳率95%(1)B(氢氧化钡溶液)+D(明矾溶液) 自始至终都有白色沉淀(BaSO 4 );B(氢氧化钡溶液)+C(硫酸铝溶液) 自始至终都有白色沉淀(BaSO 4 );B(氢氧化钡溶液)+E(混有少量硝酸的硫酸镁溶液) 自始至终都有白色沉淀(BaSO 4 );这三组中的甲、乙两种物质互相交换,又得到3种组合,共有6种组合,另A(氢氧化钠溶液)+E(混有少量硝酸的硫酸镁溶液),将A加入到E中开始没有白色沉淀生成,则有:
组别 1 2 3 4 5 6 7 8
甲 B C B E E D
乙 C B E B A B 故答案为:
组别 1 2 3 4 5 6 7 8
甲 B C B E E D
乙 C B E B A B (2)将氢氧化钡溶液逐滴加入明矾溶液中,当
n[Ba(O H) 2 ]
n[KAl( SO 4 ) 2 ] =
3
2 时,产生沉淀的物质的量最大,此时反应式为:
3Ba(OH) 2 +2KAl(SO 4 ) 2 =3BaSO 4 ↓+2Al(OH) 3 ↓+K 2 SO 4 ;当
n[Ba (OH) 2 ]
n[KAl ( SO 4 ) 2 ] =2 时,产生沉淀的物质的量最小,反应为:
2Ba(OH) 2 +KAl(SO 4 ) 2 =2BaSO 4 ↓+KAlO 2 +2H 2 O;产生1 mol Al(OH) 3 沉淀时需消耗3 mol OH - ,溶解1 mol Al(OH) 3 沉淀时需消耗1 mol OH - ,据此作出图象如下:
,故答案为:
;
(3)甲为Ba(OH) 2 ,乙为HNO 3 和MgSO 4 的混合溶液时,符合给出的图示关系,原理:将Ba(OH) 2 溶液逐滴加入HNO 3 和MgSO 4 的混合溶液中,开始加入的Ba(OH) 2 将HNO 3 中和,产生的沉淀只有BaSO 4 ;等到将HNO 3 完全被中和后再继续滴加Ba(OH) 2 溶液,在产生BaSO 4 沉淀的同时还会产生Mg(OH) 2 沉淀,图象中线的斜率增大(陡度增大);等到溶液中的 完全沉淀后,再继续滴加Ba(OH) 2 溶液,只产生Mg(OH) 2 沉淀,此时图象中直线的斜率变小,当溶液中的Mg 2+ 完全沉淀后,产生的沉淀量保持不变(图象保持水平).
故答案为:Ba(OH) 2 ;HNO 3 和MgSO 41年前
81年前查看全部
- 向50ml1mol/L的硫酸铝溶液中加入100mlKOH溶液中加入100mlKOH溶液,充分反映后得到3.9g沉淀则KO
向50ml1mol/L的硫酸铝溶液中加入100mlKOH溶液中加入100mlKOH溶液,充分反映后得到3.9g沉淀则KOH物质量浓度
我根本就一点不会,真的谢谢你了, 32byk1年前1
32byk1年前1 -
 WA心若 共回答了20个问题
WA心若 共回答了20个问题 |采纳率95%n(Al2(SO4)3)=0.05*1=0.05mol;n(Al3+)=2*0.05=0.1mol;
n(Al(OH)3)=3.9/78=0.05mol;
(1)n(KOH)=0.05*3=0.15mol;c=0.15/0.1=1.5mol/L
(2)还有0.05molAl2+变成AlO2-需要消耗0.05*4=0.2mol;c=(0.2+0.15)/0.1=3.5mol/L1年前查看全部
- 硫酸铝溶液与少量氢氧化钠溶液的反应方程式
 lucifer06101年前1
lucifer06101年前1 -
 tmar39127 共回答了24个问题
tmar39127 共回答了24个问题 |采纳率87.5%少量
Al3+ + 3OH- === Al(OH)3沉淀
过量
Al3+ + 4OH- === AlO2- + 2H2O
区别,前者有沉淀生成,后者先出现沉淀然后沉淀消失1年前查看全部
- 向50ml 1mol/L的硫酸铝溶液中加入100mlKOH溶液,充分反应得到3.9g沉淀,则KOH溶液的物质的量的浓度可
向50ml 1mol/L的硫酸铝溶液中加入100mlKOH溶液,充分反应得到3.9g沉淀,则KOH溶液的物质的量的浓度可能是?
 你们的青蛙哥哥1年前2
你们的青蛙哥哥1年前2 -
 yuyiyuiyi 共回答了14个问题
yuyiyuiyi 共回答了14个问题 |采纳率100%c(KOH)=0.05*3/0.1=1.5mol/L
c(KOH)=(0.05*3 + 0.05*4)/0.1=3.5mol/L1年前查看全部
- 实验设计:氢氧化铝制取和氢氧化铝两性的验证.(试剂:盐酸,氢氧化钠溶液,硫酸铝溶液,氨水)谢
 tiats10031年前2
tiats10031年前2 -
 凌乱711 共回答了14个问题
凌乱711 共回答了14个问题 |采纳率100%因为氢氧化铝只能溶于强碱不溶于弱碱,所以要用弱碱制氢氧化铝,用强碱溶氢氧化铝.
1、取少量硫酸铝溶液,加入足量氨水,生成白色沉淀(即氢氧化铝的制取)
2、把沉淀分装2个试管,分别滴入盐酸,氢氧化钠溶液,发现沉淀都消失,证明氢氧化铝具有两性.1年前查看全部
- 能正确表示下列反应的离子方程式是( ) A.硫酸铝溶液中加入过量氨水 Al 3+ +3OH - =Al(OH
能正确表示下列反应的离子方程式是( ) A.硫酸铝溶液中加入过量氨水Al 3+ +3OH - =Al(OH) 3 ↓ B.碳酸钠溶液中加入澄清石灰水Ca(OH) 2 +CO 3 2- =CaCO 3 ↓+2OH - C.冷的氢氧化钠溶液中通入氯气Cl 2 +2OH - =ClO - +Cl - +H 2 O D.稀硫酸中加入铁粉2Fe+6H + =2Fe 3+ +3H 2 ↑  hlnhly1年前1
hlnhly1年前1 -
 封印酒舞 共回答了21个问题
封印酒舞 共回答了21个问题 |采纳率90.5%A.硫酸铝溶液中加入过量氨水的离子反应为Al 3+ +3NH 3 .H 2 O=Al(OH) 3 ↓+3NH 4 + ,故A错误;
B.碳酸钠溶液中加入澄清石灰水的离子反应为Ca 2+ +CO 3 2- =CaCO 3 ↓,故B错误;
C.冷的氢氧化钠溶液中通入氯气的离子反应为Cl 2 +2OH - =ClO - +Cl - +H 2 O,故C正确;
D.稀硫酸中加入铁粉的离子反应为Fe+2H + =Fe 2+ +H 2 ↑,故D错误;
故选C.1年前查看全部
- 怎么制取硫酸铝晶体?有的人说加热硫酸铝溶液结晶,但是这样不会促使铝离子水解吗?
 thirtyfour1年前2
thirtyfour1年前2 -
 漫游fish 共回答了13个问题
漫游fish 共回答了13个问题 |采纳率84.6%因为硫酸是不挥发性酸.硫酸铝如果水解,那么水解产物是氢氧化铝和硫酸,硫酸不挥发,那么硫酸仍旧会溶解氢氧化铝.所以硫酸铝不水解.
我所说的水解是蒸发结晶的强烈的水解.不是单纯在溶液中的水解.1年前查看全部
- 硫酸锌,硫酸镁,硫酸铜,硫酸铝是固体还是液体?
硫酸锌,硫酸镁,硫酸铜,硫酸铝是固体还是液体?
按理说应该是固体,但是Cu2O+H2SO4=CuSO4+Cu+H2O这个反应里面又把生成的cuso4算成是液体,为什么? 人里面哪有我1年前1
人里面哪有我1年前1 -
 meb5838 共回答了20个问题
meb5838 共回答了20个问题 |采纳率85%硫酸是水溶液,含水,而且因为有水生成,硫酸铜溶于水.1年前查看全部
- 碳酸钠与硫酸铝一定可以看到白色胶状沉淀和无色气体?为什么错
碳酸钠与硫酸铝一定可以看到白色胶状沉淀和无色气体?为什么错
题目说了两溶液,是不是与量有关 allen_huang1年前2
allen_huang1年前2 -
 stevenlee30 共回答了21个问题
stevenlee30 共回答了21个问题 |采纳率100%如果碳酸钠浓溶液,而硫酸铝是稀溶液,且是向碳酸钠溶液中滴加少量硫酸铝溶液,就无法看到无色气体.一般情况下两者能出白色胶状沉淀和无色气体是按照3:2的比例反应,双水解进行到底:3CO3^2- +2Al^3+ 3H2O = 2Al(OH)3↓+3CO2↑,如果碳酸根较多,铝离子水解产生的H+只能将碳酸根转化为碳酸氢根,就无法看到无色气体现象,白色沉淀倒是可以看到.
因此遇到这种带有“一定”字眼的判断,一定要小心,尤其是量的问题
若还有不明白的,欢迎继续追问!1年前查看全部
- (1)硫酸铝溶液中滴过量氨水?(2)二氧化硅于氢氧化钠反应?(3)四氧化三铁加入盐酸中?(4)金属铝与氢氧化...
(1)硫酸铝溶液中滴过量氨水?(2)二氧化硅于氢氧化钠反应?(3)四氧化三铁加入盐酸中?(4)金属铝与氢氧化...
(1)硫酸铝溶液中滴过量氨水?(2)二氧化硅于氢氧化钠反应?(3)四氧化三铁加入盐酸中?(4)金属铝与氢氧化钠溶液反应?的化学反应方程式 jinxb1年前2
jinxb1年前2 -
 小桔灯 共回答了19个问题
小桔灯 共回答了19个问题 |采纳率84.2%1、Al2(SO4)3+6NH3H2O=2Al(OH)3↓+3(NH4)2SO4
2、SiO2+2NaOH=Na2SiO3+H2O
3、Fe3O4+8HCl=FeCl2+2FeCl3+4H2O
4、2Al+2NaOH+2H2O=2NaAlO2+3H2↑1年前查看全部
- 注:“铝与硫酸反应产生硫酸铝和氢气”中的“硫酸”是稀的还是浓的?
注:“铝与硫酸反应产生硫酸铝和氢气”中的“硫酸”是稀的还是浓的?
输入链接也可! acoav0ib1年前1
acoav0ib1年前1 -
 zll054 共回答了17个问题
zll054 共回答了17个问题 |采纳率100%稀的
铝和浓硫酸反应钝化,不产生氢气1年前查看全部
- 多少摩尔硫酸铝含a克铝离子(请写出详细解答过程)
 带着梦想克流浪1年前1
带着梦想克流浪1年前1 -
 打渔 共回答了13个问题
打渔 共回答了13个问题 |采纳率92.3%agAL3+的物质的量n=a/27(mol)
1molAl2(SO4)3含有2molAl3+
所以(a/27)/2=a/54molAl2(SO4)3含有a克铝离子.1年前查看全部
大家在问
- 1分fen第一声可以组什么词
- 2已知2a-1的平方根为±根号3,3a-2b+1的平方根为±3,求4a-b的平方根.
- 3在函数中 一个直角三角形两边相等 记为X 面积记为Y Y关于X的自变量为 Y=0.5X*X 求X的取值范围 为何X可等于
- 4一道完成时的选择题(英语)求解Has you finished the book?--Yes,I ______ it y
- 5初一下册《社戏》的结尾表达了作者怎样的思想感情?
- 6这道题怎么做:将下面的词语补充完整
- 7为了庆祝六一儿童节,龙门新华书店实行买4套儿童百科全书送1套的优惠活动。张老师一次卖了4套,每套便宜多少钱?(每套原价4
- 8雪 祝勇 1.、理清文章思路,按实力对(3)(5)(6)段的内容用两字加以概括.(1)品雪——(2)喜雪——(3)___
- 9谁帮我写一篇英语作文作文内容根据“Make a good impression”和“Choose the bestuni
- 10将画线字的音节补充完整或看拼音写出汉字,并按要求做题。
- 11阅读下面的三则材料,写出你探究的结果.(答出三点即可)
- 1210毫升量筒能装5.80毫升水吗
- 13如图为植物体的几种主要组织,请分析回答问题.
- 14朱熹《观书有感》中 蕴含“不断学习新知识,就能达到新境界”这一哲理的是诗句是--------------------
- 15如图是元素周期表中钠元素的相关信息及其原子结构示意图,请回答下列问题:
