(2013•西华县二模)酸、碱、盐是几类有广泛用途的重要化合物.
 笑青风2022-10-04 11:39:541条回答
笑青风2022-10-04 11:39:541条回答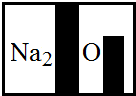 (2013•西华县二模)酸、碱、盐是几类有广泛用途的重要化合物.
(2013•西华县二模)酸、碱、盐是几类有广泛用途的重要化合物.(1)酸和碱在组成和性质方面有很多共同的特点,请任写出其中的一条.
(2)氢氧化钙是一种常见的碱,列举其在生产、生活中的一种用途.
(3)某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如右图)的溶液,他们对此产生了兴趣.
提出问题:这瓶溶液究竟是什么?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
①小明根据标签上的组成元素认为一定不可能是______(提示:只有其中一种).
②小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是:
设计实验:为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验.
| 实验操作 | 实验现象 |
| 取少量样品于试管中,慢慢滴加BaCl2溶液 | 出现白色沉淀 |
| 静置一段时间后,倾去上层清液,向沉淀中滴加稀盐酸 | 白色沉淀全部溶解,并产生大量气泡 |
实验反思:④小强认为上述设计实验还可简化,也能达到目的.小强的实验操作是:
(4)若73 g质量分数为20%的盐酸与127g氢氧化钠溶液恰好完全中和,试计算反应后所得溶液中溶质的质量分数.

已提交,审核后显示!提交回复
共1条回复
 秋风不落叶 共回答了20个问题
秋风不落叶 共回答了20个问题 |采纳率90%- 解题思路:(1)根据酸、碱组成中都含有氢元素,都能使指示剂变色,有腐蚀性进行回答;
(2)氢氧化钙显碱性,且比较廉价,农业上常用来改良酸性土壤,并可用来配制农药波尔多液等;
(3)①该标签显示该物质中一定含有钠元素、氧元素,而氯化钠不含有氧元素,据此判断;
②碳酸氢钠和硝酸钠的化学式中钠元素的右下角数字是1,而不是2;
③硫酸钠、碳酸钠可与氯化钡溶液反应分别生成硫酸钡、碳酸钡沉淀,不过硫酸钡沉淀与稀盐酸不反应,碳酸钡沉淀可与稀盐酸反应生成氯化钡、水和二氧化碳,据此推测该瓶溶液,并书写反应方程式;
④据碳酸钠可与盐酸反应生成二氧化碳,而硫酸钠与盐酸不反应设计实验进行验证步骤更简洁;
(4)据溶质的质量=溶液的质量×溶质的质量分数可计算出反应的盐酸溶质的质量,并结合方程式计算出氯化钠的质量,进而计算溶液的溶质质量分数.(1)酸、碱在组成和性质上的相似点有:组成中都含有氢元素,都能使指示剂变色,有腐蚀性等;
(2)氢氧化钙显碱性,且比较廉价,农业上常用来改良酸性土壤,并可于硫酸铜反应用来配制农药波尔多液,还是一种常用的建筑材料等;
(3)①该标签显示该物质中一定含有钠元素、氧元素,而氯化钠不含有氧元素,所以从组成上可以判断该物质一定不是氯化钠;
②碳酸氢钠和硝酸钠的化学式中钠元素的右下角数字是1,而不是2,所以不可能是碳酸氢钠和硝酸钠;
③硫酸钠、碳酸钠可与氯化钡溶液反应分别生成硫酸钡、碳酸钡沉淀,但硫酸钡沉淀与稀盐酸不反应,碳酸钡沉淀可与稀盐酸反应生成氯化钡、水和二氧化碳,所以根据向沉淀中加入稀盐酸,白色沉淀全部溶解,并产生大量气泡可知该瓶溶液是碳酸钠溶液,碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,反应方程式是BaCl2 +Na2CO3═BaCO3↓+2NaCl;
④碳酸钠可与盐酸反应生成二氧化碳,而硫酸钠与盐酸不反应,所以可取样品滴加稀盐酸观察是否有气泡生成进行判断,这样操作步骤更简洁;
(4)设反应后生成氯化钠的质量为 x
HCl+NaOH═NaCl+H2 O
36.5 58.5
73g×20% x
[36.5/73g×20% ]=[58.5/x]
x=23.4 g
反应后所得溶液的质量分数为:
[23.4g/73g+127g]×100%═11.7%
故答案为:(1)组成上都含有氢元素(或都能使指示剂变色或都有腐蚀性等);
(2)改良酸性土壤(或粉刷墙壁、配制农药波尔多液等);
(3)①氯化钠;
②这两种物质的化学式中Na元素的右下角不会有2;
③碳酸钠溶液; BaCl2 +Na2CO3═BaCO3↓+2NaCl;
④取少量无色溶液样品于试管中,慢慢滴加稀盐酸;
(4)答:反应后所得溶液的质量分数为11.7%.点评:
本题考点: 酸的化学性质;缺失标签的药品成分的探究;有关溶质质量分数的简单计算;常见碱的特性和用途;碱的化学性质;常见离子的检验方法及现象;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式;根据化学反应方程式的计算.
考点点评: 本题考查知识较为全面,既考查了酸、碱、盐的性质,还考查了学生依据所学知识进行计算、分析解答问题的能力,是一道不错的题目. - 1年前
相关推荐
- (2右13•西华县二模)左列实验中,能观察到的现象是( )
(2右13•西华县二模)左列实验中,能观察到的现象是( )
A.红磷燃烧产生大量白色烟雾
B.铁丝在空气中剧烈燃烧,火星四射
C.硫在空气中燃烧,发出明亮的蓝紫色火焰
D.木炭还原氧化铜的过程中,黑色固体变成红色 lonely-walker1年前1
lonely-walker1年前1 -
 海南椰狼 共回答了15个问题
海南椰狼 共回答了15个问题 |采纳率86.7%解题思路:A、根据红磷在空气中燃烧的现象进行分析判断.
B、根据铁丝在空气中燃烧的现象进行分析判断.
C、根据硫在空气中燃烧的现象进行分析判断.
D、根据木炭还原氧化铜的实验现象进行分析判断.A、红磷在空气中燃烧时,产生大量的白烟,而不是白色烟雾,故选项说法错误.
B、铁丝在空气中只能烧至发红,不会产生火星,故选项说法错误.
C、硫在空气中燃烧,发出微弱的淡蓝色火焰,故选项说法错误.
D、木炭具有还原性,能与黑色的氧化铜反应生成红色铜和二氧化碳气体,故反应过程中会观察到黑色固体变成红色;故选项说法正确.
故选D.点评:
本题考点: 氧气与碳、磷、硫、铁等物质的反应现象.
考点点评: 本题难度不大,掌握常见物质燃烧的现象、木炭还原氧化铜的实验现象即可正确解答;但在描述物质燃烧的现象时,需要注意光和火焰、烟和雾的区别.1年前查看全部
- (2013•西华县一模)如图A~G均为初中化学中常见的物质.其中A、C组成元素相同,E是红色单质,它们之间的转化关系.则
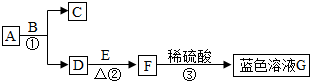 (2013•西华县一模)如图A~G均为初中化学中常见的物质.其中A、C组成元素相同,E是红色单质,它们之间的转化关系.则:反应①的化学方程式:2H2O2
(2013•西华县一模)如图A~G均为初中化学中常见的物质.其中A、C组成元素相同,E是红色单质,它们之间的转化关系.则:反应①的化学方程式:2H2O2
2H2O+O2↑MnO2 .2H2O2,其中B物质在该反应中起______作用;反应②的化学方程式为
2H2O+O2↑MnO2 .2Cu+O2
2CuO△ .2Cu+O2;反应③属于基本类型中的______反应.
2CuO△ . 专用qq61年前1
专用qq61年前1 -
 栗田梅子 共回答了19个问题
栗田梅子 共回答了19个问题 |采纳率84.2%解题思路:根据题干提供的信息进行分析,E是红色单质,则E是铜;F与硫酸反应生成蓝色溶液G,则G是硫酸铜,说明F中含有铜元素,D与E反应,则D可能是氧气,F是氧化铜;A和C组成元素相同,且A能生成氧气,则A是过氧化氢,C是水,据此解答.E是红色单质,则E是铜;F与硫酸反应生成蓝色溶液G,则G是硫酸铜,说明F中含有铜元素,D与E反应,则D可能是氧气,F是氧化铜;A和C组成元素相同,且A能生成氧气,则A是过氧化氢,C是水,B可能是二氧化锰,带入框图,推断合理;
反应①是过氧化氢在二氧化锰的催化作用下生成水和氧气,故填:2H2O2
MnO2
.
2H2O+O2↑,催化;
反应②是铜和氧气在加热的条件下反应生成氧化铜,故填:2Cu+O2
△
.
2CuO;
反应③是氧化铜与稀硫酸反应生成硫酸铜和水,该反应是两种化合物互相交换成分生成两种新的化合物的反应,属于复分解反应,故填:复分解.点评:
本题考点: 物质的鉴别、推断;化学式的书写及意义;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题为框图型物质推断题,完成此类题目,可以依据题干提供的信息,结合框图,找准解题的突破口,直接得出物质的化学式,然后顺推或逆推或由两边向中间推得出其他物质的化学式.1年前查看全部
- (2013•西华县一模)化学与生活密切相关.水果、蔬菜能为人体提供的主要营养素是______;人体缺______
(2013•西华县一模)化学与生活密切相关.水果、蔬菜能为人体提供的主要营养素是______;人体缺______ 元素会导致骨质疏松和易患佝偻病;含小苏打的药物治疗胃酸过多症的化学方程式为______.
 果__果1年前1
果__果1年前1 -
 lc天生乐天派 共回答了16个问题
lc天生乐天派 共回答了16个问题 |采纳率87.5%解题思路:水果、蔬菜中含有丰富的维生素;
人体缺钙容易患佝偻病或骨质疏松症;
小苏打是碳酸氢钠的俗称,能和稀盐酸反应.水果、蔬菜能为人体提供的主要营养素是维生素.
故填:维生素.
青少年缺钙容易患佝偻病,中老年缺钙容易患骨质疏松症.
故填:钙.
碳酸氢钠和稀盐酸反应能生成氯化钠、水和二氧化碳,反应的化学方程式为:NaHCO3+HCl═NaCl+H2O+CO2↑.
故填:NaHCO3+HCl═NaCl+H2O+CO2↑.点评:
本题考点: 生命活动与六大营养素;书写化学方程式、文字表达式、电离方程式;人体的元素组成与元素对人体健康的重要作用.
考点点评: 人体如果缺乏某些营养素时容易患病,因此要均衡地摄取各种食物,以保证对各种营养素的均衡吸收,促进人体健康发展.1年前查看全部
- (2014•西华县一模)下列图示的实验操作正确的是( )
(2014•西华县一模)下列图示的实验操作正确的是( )
A.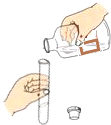
倾倒液体
B.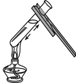
给液体加热
C.
过滤浑浊的水
D.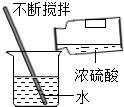
稀释浓硫酸 甘8511251年前1
甘8511251年前1 -
 衡阳清河 共回答了22个问题
衡阳清河 共回答了22个问题 |采纳率95.5%解题思路:A、运用标签对着手心、瓶塞要倒放、试剂瓶口要紧靠试管口倾倒分析;
B、运用给试管中的液体加热时的注意问题解答;
C、运用过滤要领“一帖二低三靠”解答;
D、运用浓硫酸的稀释方法解答.A、向试管中倾倒液体时,标签对着手心、瓶塞要倒放、试剂瓶口要紧靠试管口倾倒,故A错;
B、给试管中的液体加热,液体体积不应超过试管容积的[1/3],故B错;
C、过滤操作中的要领是“一帖二低三靠”,图示操作不符合操作要领,故C错;
D、浓硫酸稀释时,应把浓硫酸沿着器壁缓缓注入水中,并不断用玻璃棒搅拌,使热量迅速散失,故D正确
故答案为:D点评:
本题考点: 液体药品的取用;给试管里的液体加热;浓硫酸的性质及浓硫酸的稀释;过滤的原理、方法及其应用.
考点点评: 掌握常见实验基本操作的注意事项是解决此类题目的关键.1年前查看全部
- (2014•西华县一模)请回答下列有关金属的问题.
(2014•西华县一模)请回答下列有关金属的问题.
(1)铝是活泼金属,为什么通常铝锅却很耐腐蚀?
(2)铁在空气中生锈的原因是铁跟______发生了反应.
(3)A、B、C三种金属固体,将A和B浸入稀硫酸中,B溶解并产生氢气,A无变化;将A和C浸入硝酸银溶液中,A表面有银析出而C无变化.
①判断A、B、C和银四种金属的活动性由强到弱的顺序______.
②具体确定一种A后,写出A与硝酸银溶液反应的化学方程式______. xiaoqianqian19831年前1
xiaoqianqian19831年前1 -
 cwei200408 共回答了21个问题
cwei200408 共回答了21个问题 |采纳率85.7%解题思路:(1)根据氧化铝的特点考虑;
(2)根据生锈的原因分析解答;
(3)金属的活动性顺序最初是由化学家根据金属间的置换反应,还有金属跟水和各种酸、碱的反应总结而成.(1)铝与氧气反应生成的氧化铝是一层致密的氧化膜,使内部的铝与氧气隔绝,对内部的铝起到保护作用;
(2)铁的生锈是铁与空气中的氧气和水共同作用的结果;
(3)①B能与稀H2SO4反应而A不能,推知B的活动性大于A的活动性;②由“A和C浸入AgNO3溶液中,A表面有Ag析出而C无变化”推知:A的活动性大于Ag,而C的活动性小于Ag,综上所述则有B>A>Ag>C,选用的A,其活动性要排在H与Ag之间即可,如Cu、Hg等;
故答案为:(1)铝与空气中的氧气反应,其表面生成致密的氧化铝薄膜起保护作用
(2)氧气、水
(3)①B、A、Ag、C ②Cu+2AgNO3═Cu(NO3)2+2Ag点评:
本题考点: 金属的化学性质;金属活动性顺序及其应用;金属锈蚀的条件及其防护;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题综合考查的是金属的化学性质及其性质的应用和化学方程式的书写.1年前查看全部
- (2014•西华县三模)下列变化中有一种和其它三种有本质区别的是( )
(2014•西华县三模)下列变化中有一种和其它三种有本质区别的是( )
A.矿石粉碎
B.纸张燃烧
C.酒精挥发
D.海水晒盐 lshy6541年前1
lshy6541年前1 -
 bty1012 共回答了20个问题
bty1012 共回答了20个问题 |采纳率85%解题思路:化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.A、矿石粉碎过程中只是形状发生改变,没有新物质生成,属于物理变化.
B、纸张燃烧过程中有新物质二氧化碳等生成,属于化学变化.
C、酒精挥发过程中只是状态发生改变,没有新物质生成,属于物理变化.
D、海水晒盐过程中没有新物质生成,属于物理变化.
故选:B.点评:
本题考点: 化学变化和物理变化的判别.
考点点评: 本题难度不大,解答时要分析变化过程中是否有新物质生成,若没有新物质生成属于物理变化,若有新物质生成属于化学变化.1年前查看全部
- (2013•西华县一模)稀土元素是一类有重要用途的资源.金属元素铈(Ce)是一种常见的稀土元素,右图是铈在周期表中的位置
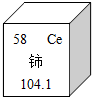 (2013•西华县一模)稀土元素是一类有重要用途的资源.金属元素铈(Ce)是一种常见的稀土元素,右图是铈在周期表中的位置图,则铈元素的原子序数是______,铈的相对原子质量是______.
(2013•西华县一模)稀土元素是一类有重要用途的资源.金属元素铈(Ce)是一种常见的稀土元素,右图是铈在周期表中的位置图,则铈元素的原子序数是______,铈的相对原子质量是______.  jscs1年前1
jscs1年前1 -
 屋里潮湿下脚小心 共回答了19个问题
屋里潮湿下脚小心 共回答了19个问题 |采纳率89.5%解题思路:根据图中元素周期表可以获得的信息:原子序数、相对原子质量、元素符号、元素种类等,元素符号左边的数字表示原子序数,元素名称下方的数字表示相对原子质量,进行分析解答即可.根据铈元素在元素周期表中的一格所获取的信息,该元素的原子序数为58,铈的相对原子质量是140.1.
故答案为:58;140.1.点评:
本题考点: 元素周期表的特点及其应用.
考点点评: 本题难度不大,考查学生灵活运用元素周期表中元素的信息及辨别元素种类的方法进行分析解题的能力.1年前查看全部
- (2014•西华县三模)水是生命之源.
(2014•西华县三模)水是生命之源.
(1)生活中通常采用______的方法可以降低水的硬度.
(2)自来水厂净化水的步骤为:取水→沉降→过滤→吸附→消毒,其中消毒属于______变化(选填“物理”或“化学”).消毒时常用二氧化氯,制取二氧化氯的反应是:C12+2NaClO2═2NaCl+2ClO2,反应前后各物质中均含有氯元素,其中氯元素的最高化合价是______. seafxz1年前1
seafxz1年前1 -
 天Ya_Google 共回答了13个问题
天Ya_Google 共回答了13个问题 |采纳率84.6%解题思路:(1)根据硬水和软水中含有的物质不同进行分析.
(2)本题主要考查学生对净化水方法的理解,同时以此为背景,又考查化学变化和物理变化的判断,解答时要对各种净水方法进行深入分析,然后再作回答.(1)硬水给生产和生活带来很多麻烦,我们通常可用肥皂水来区分硬水和软水,生活中可以通过煮沸的方法降低水的硬度;
(2)自来水厂净化过程中消毒,一般消毒剂能破坏细菌中的物质,从而使细菌失去活性,在该过程中生成了其他物质,是化学变化;
Cl2中氯元素的化合价为0,NaClO2中氯的化合价:(+1)+x+(-2)×2=0,x=+3,NaCl中氯的化合价为-1价,ClO2中氯的化合价:x+(-2)×2=0,x=+4;故氯元素的化合价为+4价;
故答案为:(1)加热煮沸;(2)化学(3)+4点评:
本题考点: 硬水与软水;自来水的生产过程与净化方法;有关元素化合价的计算;化学变化和物理变化的判别.
考点点评: 水是人类宝贵的自然资源,与水相关的化学知识是化学考查热点之一,如水的组成及水电解实验、性质、用途、硬水和软水、节约水资源、水污染及防治等内容.1年前查看全部
- (2014•西华县三模)下列物质由离子构成的是( )
(2014•西华县三模)下列物质由离子构成的是( )
A.铁
B.硫酸铜
C.氧气
D.金刚石 yiran1027781年前1
yiran1027781年前1 -
 推理游戏_毛利 共回答了15个问题
推理游戏_毛利 共回答了15个问题 |采纳率100%解题思路:根据金属、大多数固态非金属单质、稀有气体单质等由原子构成,有些物质是由分子构成的,如水、氢气等,有些物质是由离子构成的,如氯化钠,进行分析判断即可.A、铁属于金属单质,是由铁原子直接构成的,故选项错误.
B、硫酸铜是由铜离子和硫酸根离子构成的,故选项正确.
C、氧气属于气态非金属单质,是由氧分子构成的,故选项错误.
D、金刚石属于固态非金属单质,是由碳原子直接构成的,故选项错误.
故选:B.点评:
本题考点: 物质的构成和含量分析.
考点点评: 本题难度不大,主要考查了构成物质的微观粒子方面的知识,掌握常见物质的粒子构成是正确解答本题的关键.1年前查看全部
- (2013•西华县一模)(1)铁制品锈蚀,实际上是铁跟空气中的______ 发生了化学反应.
(2013•西华县一模)(1)铁制品锈蚀,实际上是铁跟空气中的______ 发生了化学反应.
(2)将生锈的铁片放入硫酸和硫酸铜的混合溶液中,可能发生的反应有______个,写出其中一个反应的化学方程式______.
(3)在CuSO4和Al2(SO4)3的混合溶液中,加入一定量的铁粉充分反应,过滤后得到滤液和固体剩余物.向该剩余物中加入足量的稀盐酸,有气泡产生.则滤液中一定含有哪些金属离子(写离子符号)______. 0y8pb1年前1
0y8pb1年前1 -
 yuxin_leong 共回答了18个问题
yuxin_leong 共回答了18个问题 |采纳率88.9%解题思路:解:(1)铁与氧气和水充分接触时容易生锈,水和氧气同时存在是铁生锈的必要条件;显酸性的溶液、盐溶液能够促进金属生锈;
(2)铁锈能和稀硫酸反应,铁能和稀硫酸、硫酸铜反应;
(3)排在金属活动性顺序前面的金属,能够把排在后面的金属从它的盐溶液中置换出来.(1)铁制品锈蚀,实际上是铁跟空气中的水和氧气发生了化学反应.
故填:水和氧气.
(2)将生锈的铁片放入硫酸和硫酸铜的混合溶液中,可能发生的反应有:Fe2O3+3H2SO4═Fe2 (SO4) 3+3H2O,Fe+H2 SO4=FeSO4+H2 ↑,Fe+CuSO4═FeSO4+Cu.
故填:3;Fe2O3+3H2SO4═Fe2 (SO4) 3+3H2O.
(3)铝比铁活泼,铁比铜活泼,向CuSO4和Al2(SO4)3的混合溶液中,加入一定量的铁粉时,铁不能和硫酸铝反应,能和硫酸铜反应生成硫酸亚铁和铜;
向该剩余物中加入足量的稀盐酸,有气泡产生,说明固体剩余物中含有铁,进一步说明硫酸铜已经完全反应,则滤液中一定含有的金属离子是亚铁离子和铝离子,符号分别是Fe 2+,Al3+.
故填:Fe 2+、Al3+.点评:
本题考点: 金属锈蚀的条件及其防护;金属的化学性质;酸的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 书写化学方程式时要注意四步,一是反应物和生成物的化学式要正确,二是遵循质量守恒定律,三是写上必要的条件,四是看是否有“↑”或“↓”.1年前查看全部
- (2014•西华县一模)化学与人类的衣、食、住、行密切相关,下列说法不正确的是( )
(2014•西华县一模)化学与人类的衣、食、住、行密切相关,下列说法不正确的是( )
A.衣料中的棉和涤纶都属于合成有机高分子材料
B.汽车用天然气代替汽油作燃料可减少空气污染
C.加碘食盐和铁强化酱油都可补充人体必需的微量元素
D.建造高楼大厦所用到的钢和生铁是铁的两种合金 打碎北冰洋1年前1
打碎北冰洋1年前1 -
 米兰的风 共回答了19个问题
米兰的风 共回答了19个问题 |采纳率89.5%解题思路:A、根据衣料中的棉属于天然材料进行解答;
B、根据汽车用天然气代替汽油作燃料可减少空气污染进行解答;
C、根据碘和铁是人体所需的微量元素进行解答;
D、根据钢和生铁是铁的两种合金进行解答.A、衣料中的棉属于天然材料,而涤纶属于合成有机高分子材料,故A错误;
B、汽车用天然气代替汽油作燃料可减少空气污染,故B正确;
C、碘和铁是人体所需的微量元素,所以加碘食盐和铁强化酱油都可补充人体必需的微量元素,故C正确;
D、钢和生铁是铁的两种合金,故D正确.
故选:A.点评:
本题考点: 有机高分子材料的分类及鉴别;生铁和钢;常用燃料的使用与其对环境的影响;人体的元素组成与元素对人体健康的重要作用.
考点点评: 本题主要考查物质的性质和用途,物质具有多种性质,解答时应该理解物质的用途是由物质的哪种性质决定的.1年前查看全部
- (2014•西华县一模)周日小红去商店购买电热水壶,售货员给他一份推销××牌电热水壶的宣传广告,其内容如表.请你根据广告
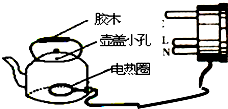 (2014•西华县一模)周日小红去商店购买电热水壶,售货员给他一份推销××牌电热水壶的宣传广告,其内容如表.请你根据广告提供的信息作答或计算:[c水=4.2×103 J/(kg•℃)]
(2014•西华县一模)周日小红去商店购买电热水壶,售货员给他一份推销××牌电热水壶的宣传广告,其内容如表.请你根据广告提供的信息作答或计算:[c水=4.2×103 J/(kg•℃)]
(1)请你观察电热水壶的构造,仿照下面的例子说出一条生活与物理的相关道理:例:壶把手上安装胶木,利用了胶木是绝缘体,对人体更安全的原理.
(2)在一标准大气压下,烧开一满壶20℃水,水吸收的热量是多少?
(3)请通过计算说明此广告的真假;
X X牌节能电热水壶优点:高效、节能、省时,在1标准大气压下,烧开一壶初温为20℃的水仅需5min! 额定电压 220V 额定功率 1 000W 容积 2L 超温保护器熔断温度 110℃  liubo1991年前1
liubo1991年前1 -
 天天就爱睡懒觉 共回答了23个问题
天天就爱睡懒觉 共回答了23个问题 |采纳率73.9%解题思路:(1)根据茶壶上小孔,结合大气压和连通器的特点进行分析;
(2)先根据密度公式求出水的质量,然后根据吸热公式求出水吸收的热量;
(3)比较加热水所需能量及3min内电水壶消耗的能量,可知广告的真伪.(1)茶壶盖上的小孔能保证与大气相通,使壶身和壶嘴构成连通器,水容易倒出来.
(2)由密度公式可得,一壶水的质量:m=ρV=1.0×103kg/m3×2×10-3m3=2kg,
Q吸=cm△t=c水=4.2×103 J/(kg•℃)×2kg×(100℃-20℃)=6.72×105J;
(3)Q放=W=Pt=1000W×300s=3×105J.
∵Q吸>Q放
∴此广告不科学.
答:(1)茶壶盖上的小孔能保证与大气相通,使壶身和壶嘴构成连通器,水容易倒出来.
(2)水吸收的热量是6.72×105J.
(3)因为吸收的热量大于放出的热量,因此为虚假广告.点评:
本题考点: 电功与热量的综合计算.
考点点评: 本题考查物理知识在生活中的应用,在生活中要做有心人,将身边的用品所用到的物理知识要多做分析.1年前查看全部
- (2014•西华县三模)铜制品久置在潮湿的空气中表面会有绿点出现,其主要成分铜绿[Cu2(OH)2CO3]受热分解生成三
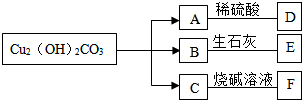 (2014•西华县三模)铜制品久置在潮湿的空气中表面会有绿点出现,其主要成分铜绿[Cu2(OH)2CO3]受热分解生成三种氧化物.现有如图所示的转化关系(部分生成物已略去).
(2014•西华县三模)铜制品久置在潮湿的空气中表面会有绿点出现,其主要成分铜绿[Cu2(OH)2CO3]受热分解生成三种氧化物.现有如图所示的转化关系(部分生成物已略去).
写出D物质的化学式______;
C→F的化学方程式为______;
E和F反应的化学方程式为______.
写出E在农业生产中的一种用途______. 张青芳1年前1
张青芳1年前1 -
 liulingdeshu 共回答了21个问题
liulingdeshu 共回答了21个问题 |采纳率76.2%解题思路:根据已有的知识进行分析,铜绿分解能生成水、二氧化碳和氧化铜,氧化铜能与稀硫酸反应生成硫酸铜和水,水能与氧化钙反应生成氢氧化钙,二氧化碳能与氢氧化钠反应生成碳酸钠和水,据此解答.铜绿分解能生成水、二氧化碳和氧化铜,氧化铜能与稀硫酸反应生成硫酸铜和水,故A是氧化铜,D是硫酸铜;水能与氧化钙反应生成氢氧化钙,故B是水,E是氢氧化钙;二氧化碳能与氢氧化钠反应生成碳酸钠和水,故C是二氧化碳,F是碳酸钠,带入框图,推断合理;
D是硫酸铜,故填:CuSO4;
二氧化碳能与氢氧化钠反应生成碳酸钠和水,故填:2NaOH+CO2═Na2CO3+H2O;
氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故填:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
氢氧化钙具有碱性,在农业上可以用于改良酸性土壤,故填:改良酸性土壤.点评:
本题考点: 物质的鉴别、推断;盐的化学性质;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题为框图式物质推断题,完成此题,关键是依据题干叙述找准解题的突破口,然后推导出其他物质的化学式.1年前查看全部
- (2013•西华县二模)如图是A、B两种固体物质的溶解度曲线.请回答下列问题:
 (2013•西华县二模)如图是A、B两种固体物质的溶解度曲线.请回答下列问题:
(2013•西华县二模)如图是A、B两种固体物质的溶解度曲线.请回答下列问题:
(1)P点的意义是______.
(2)将接近饱和的A物质的水溶液,变成饱和溶液的方法有______(答出一种即可).
(3)t2℃时,将30g A物质放入50g水中,充分搅拌,所得溶液的质量是______g. 三又四分之一柱香1年前1
三又四分之一柱香1年前1 -
 风米全球4 共回答了13个问题
风米全球4 共回答了13个问题 |采纳率100%解题思路:(1)根据溶解度曲线上的交点的意义分析.P点是溶解度曲线的交点,说明两物质在该温度下溶解度相等;
(2)根据A物质的溶解度随温度的变化情况,从而确定饱和溶液和不饱和溶液的转化方法;
(3)根据 t2℃时,A物质的溶解度进行计算.(1)由溶解度曲线的意义可知,曲线上的P点是溶解度曲线的交点,说明在t2℃时,A、B的溶解度相等;
(2)由A物质溶解度曲线的意义可知,A物质的溶解度随温度的升高而增大.所以,将接近饱和的A物质的水溶液,变成饱和溶液的方法有降低温度(增加溶质A或蒸发溶剂);
(3)由A物质溶解度曲线的意义可知,t2℃时,A物质的溶解度是50g.所以,t2℃时,将30g A物质放入50g水中,充分搅拌,只能溶解25g,所得溶液的质量是75g.
故答为:(1)t1℃时,A、B的溶解度相等; (2)降低温度; (3)75.点评:
本题考点: 固体溶解度曲线及其作用.
考点点评: 解读溶解度以及曲线的含义,要特别注意强调溶解度概念的要素:温度、100g溶剂、饱和.忽略以上要素就是一个错误的结论.1年前查看全部
- (2014•西华县三模)最常用的溶剂是______;天然气的主要成分燃烧的化学方程式是CH4 +2O2 点燃&
(2014•西华县三模)最常用的溶剂是______;天然气的主要成分燃烧的化学方程式是CH4 +2O2
CO2 +2H2O点燃 .CH4 +2O2.
CO2 +2H2O点燃 . hill841年前1
hill841年前1 -
 ii 共回答了15个问题
ii 共回答了15个问题 |采纳率80%解题思路:根据常见的溶剂分析;根据天然气燃烧生成水和二氧化碳进行解答;水是最常用的溶剂;天然气是常用的燃料,它的主要成分的名称是甲烷,甲烷燃烧生成水和二氧化碳,化学方程式CH4 +2O2
点燃
.
CO2 +2H2O.
故答案为:水(H2O);CH4+2O2
点燃
.
CO2+2H2O点评:
本题考点: 常见的溶剂;书写化学方程式、文字表达式、电离方程式;常用燃料的使用与其对环境的影响.
考点点评: 在解此类题时,要根据反应原理和方程式的书写规则进行书写方程式.1年前查看全部
- (2013•西华县二模)地壳中含量最高的金属元素是______.石灰水显碱性是由于溶液中存在大量的______(用离子符
(2013•西华县二模)地壳中含量最高的金属元素是______.石灰水显碱性是由于溶液中存在大量的______(用离子符号表示).
 yq1123581年前1
yq1123581年前1 -
 hanskiller 共回答了16个问题
hanskiller 共回答了16个问题 |采纳率93.8%解题思路:根据地壳中各元素含量的排序及元素的分类进行分析判断;根据碱性溶液中含有氢氧根离子进行书写即可.地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,其中含量最多的金属元素是铝元素;石灰水显碱性是由于溶液中存在大量的氢氧根离子,其离子符号为:OH-.
故答案为:铝;OH-.点评:
本题考点: 地壳中元素的分布与含量;碱的化学性质;元素的简单分类.
考点点评: 本题难度不大,掌握常见化学用语(分子符号、离子符号等)的书写方法、地壳里各元素的含量等即可正确解答本题.1年前查看全部
- (2013•西华县二模)下列实验操作中不正确的是( )
(2013•西华县二模)下列实验操作中不正确的是( )
A.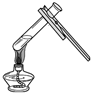
加热液体
B.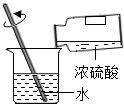
稀释浓硫酸
C.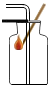
验满二氧化碳
D.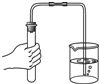
检查气密性 lightginger1年前1
lightginger1年前1 -
 天高云淡_独秀峰 共回答了22个问题
天高云淡_独秀峰 共回答了22个问题 |采纳率81.8%解题思路:A、根据给试管中的液体加热的方法进行分析判断.
B、根据浓硫酸的稀释方法进行分析判断.
C、根据二氧化碳的验满方法进行分析判断.
D、根据检查装置气密性的方法进行分析判断.A、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的[1/3],图中所示操作正确.
B、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散,图中所示操作正确.
C、验满二氧化碳时,应将燃着的木条放在集气瓶口,不能伸入瓶中,图中所示操作错误.
D、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气;图中所示操作正确.
故选C.点评:
本题考点: 给试管里的液体加热;浓硫酸的性质及浓硫酸的稀释;检查装置的气密性;二氧化碳的检验和验满.
考点点评: 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.1年前查看全部
- (2013•西华县二模)二甲醚(C2H6O)以其无污染、易于制造的特征,可能成为一种全新的替代能源而普及.下列有关二甲醚
(2013•西华县二模)二甲醚(C2H6O)以其无污染、易于制造的特征,可能成为一种全新的替代能源而普及.下列有关二甲醚的说法正确的是( )
A.二甲醚由9个原子构成
B.二甲醚的相对分子质量为38
C.二甲醚属于氧化物
D.二甲醚和甲烷完全燃烧的产物相同 laiaijie1年前1
laiaijie1年前1 -
 卡啊 共回答了35个问题
卡啊 共回答了35个问题 |采纳率82.9%解题思路:A.根据标在元素符号右下角的数字表示一个分子中所含原子的个数;进行解答;
B.根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行解答;
C.根据氧化物是指由两种元素组成且其中一种是氧元素的化合物,进行判断;
D.根据二甲醚与甲烷分别在氧气中燃烧后的产物,进行解答.A.根据标在元素符号右下角的数字表示一个分子中所含原子的个数;可知1个二甲醚分子由9个原子构成;故A说法错误;
B.根据相对分子的质量为组成分子的各原子的相对原子质量之和,可得二甲醚的相对分子质量
是:12×2+6×1+16=46,故B说法错误;
C.根据氧化物是指由两种元素组成且其中一种是氧元素的化合物,而二甲醚由C、H、O三种元素组成,所以二甲醚不属于氧化物;故C说法错误;
D.根据二甲醚与甲烷分别在氧气中燃烧后的产物都是二氧化碳和水,故D说法正确;
故选D.点评:
本题考点: 有关化学式的计算和推断;从组成上识别氧化物;相对分子质量的概念及其计算;完全燃烧与不完全燃烧.
考点点评: 本题考查学生对化学式含义及氧化物概念的理解,并能灵活应用的能力.1年前查看全部
- (2013•西华县二模)请用所学化学知识解释下列问题.
(2013•西华县二模)请用所学化学知识解释下列问题.
(1)金刚石、石墨和C60 都是由碳元素组成的单质,但它们的物理性质有很大的差异,其原因是______.
(2)铝制品抗腐蚀性能很好,原理是______(用化学方程式表示).
(3)稀硫酸除铁锈:______(用化学方程式表示).
(4)工业上电解饱和食盐水可制取烧碱、H2、氯气(Cl2),请写出该反应的化学方程式:2NaCl+2H2O
2NaOH+Cl2↑+H2↑通电 .2NaCl+2H2O.
2NaOH+Cl2↑+H2↑通电 . 十年深海1年前1
十年深海1年前1 -
 糖小包包 共回答了19个问题
糖小包包 共回答了19个问题 |采纳率94.7%解题思路:(1)物质的结构决定物质的性质,物质的性质决定物质的用途;
(2)铝的化学性质比较活泼,在通常情况下能被空气中的氧气氧化,形成一层致密的氧化物保护膜;
(3)铁锈的主要成分是氧化铁,能和稀硫酸反应生成硫酸铁和水;
(4)电解饱和食盐水能生成氢氧化钠、氢气和氯气.(1)因为碳原子的排列方式不同,所以金刚石、石墨和C60 的物理性质有很大的差异.
故填:碳原子的排列方式不同.
(2)铝在通常情况下能和氧气反应生成氧化铝,化学方程式为:4Al+3O2═2Al2O3.
故填:4Al+3O2═2Al2O3.
(3)稀硫酸除铁锈的化学方程式为:Fe2O3+3H2SO4═Fe2(SO4) 3+3H2O.
故填:Fe2O3+3H2SO4═Fe2(SO4) 3+3H2O.
(4)电解饱和食盐水的化学方程式为:2NaCl+2H2O
通电
.
2NaOH+Cl2↑+H2↑.
故填:2NaCl+2H2O
通电
.
2NaOH+Cl2↑+H2↑.点评:
本题考点: 碳元素组成的单质;金属的化学性质;酸的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 书写化学方程式时要注意四步,一是反应物和生成物的化学式要正确,二是遵循质量守恒定律,三是写上必要的条件,四是看是否有“↑”或“↓”.1年前查看全部
- (2014•西华县一模)热水瓶用久后,瓶胆内壁常附着一层水垢[主要成分是CaCO3和Mg(OH)2],可用______来
(2014•西华县一模)热水瓶用久后,瓶胆内壁常附着一层水垢[主要成分是CaCO3和Mg(OH)2],可用______来洗涤,写出一个有关反应的化学方程式______.
 seek1年前1
seek1年前1 -
 至尊风云 共回答了14个问题
至尊风云 共回答了14个问题 |采纳率85.7%解题思路:根据酸的化学性质:能与碳酸盐反应生成盐、水和二氧化碳,与碱反应生成盐和水,写出反应的化学方程式即可.热水瓶瓶胆内壁常附着一层水垢(主要成分是碳酸钙和氢氧化镁),能与盐酸反应,则水垢可以用试剂盐酸来洗涤.
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
盐酸与氢氧化镁反应生成氯化镁和水,反应的方程式为:Mg(OH)2+2HCl=MgCl2+2H2O.
故答案为:稀盐酸;CaCO3+2HCl═CaCl2+H2O+CO2↑(或2HCl+Mg(OH)2═MgCl2+2H2O).点评:
本题考点: 酸的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,掌握酸的化学性质、化学方程式的书写方法是正确解答本题的关键.1年前查看全部
- (2013•西华县一模)自来水厂常用氯气消毒,是因为氯气和水反应生成的HClO具有杀菌消毒作用,反应的化学方程式为Cl2
(2013•西华县一模)自来水厂常用氯气消毒,是因为氯气和水反应生成的HClO具有杀菌消毒作用,反应的化学方程式为Cl2+H2O=X十HClO,X的化学式是______;化学反应中,氯元素呈现的化合价分别是______.
 树的永远回忆1年前1
树的永远回忆1年前1 -
 无声无痕 共回答了14个问题
无声无痕 共回答了14个问题 |采纳率92.9%解题思路:根据质量守恒定律可知反应前后各种原子的种类和数目不变求出化学式;根据单质化合价为零,化合物中正负化合价代数和为零求出化合价.由Cl2+H2O=X十HClO可知反应物中含有2个氯原子、2个氢原子、1个氧原子,生成物中含有1个氢原子、1个氯原子、1个氧原子,所以还少1个氢原子、1个氯原子,所以X的化学式是:HCl;Cl2属于单质化合价为零,HCl中氢为+1价,所以氯为-1价,HClO中设氯化合价为K则:+1+K+(-2)=0解得K=+1价;
故答案为:HCl;0、-1,+1.点评:
本题考点: 质量守恒定律及其应用;有关元素化合价的计算.
考点点评: 解答本题关键是要能灵活运用质量守恒定律求化学式的方法,知道在化合物中正负化合价代数和为零.1年前查看全部
- (2014•西华县一模)一根长条形磁铁a固定在水平桌面上,一根小条形磁体b被弹簧悬挂在磁铁a的S极正上方,如图所示.当将
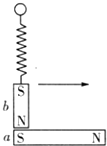 (2014•西华县一模)一根长条形磁铁a固定在水平桌面上,一根小条形磁体b被弹簧悬挂在磁铁a的S极正上方,如图所示.当将小磁体b水平向右移动直至磁铁a的右端N极正上方的过程中,弹簧的长度将( )
(2014•西华县一模)一根长条形磁铁a固定在水平桌面上,一根小条形磁体b被弹簧悬挂在磁铁a的S极正上方,如图所示.当将小磁体b水平向右移动直至磁铁a的右端N极正上方的过程中,弹簧的长度将( )
A.先变长,后变短
B.先变短,后变长
C.不断地变长
D.不断地变短 qiubin1231年前1
qiubin1231年前1 -
 小小成夕 共回答了18个问题
小小成夕 共回答了18个问题 |采纳率88.9%解题思路:根据条形磁体两极磁性最强而中间磁性最弱,和磁极间的作用规律分析.条形磁体两极磁性最强而中间磁性最弱,且同名磁极相互排斥,异名磁极相互吸引,当挂着的磁体向右移动时,相互吸引力逐渐减小,而过了大磁体中点后,相互排斥力逐渐增大,故可以得出弹簧的长度是逐渐变短的.
故选D.点评:
本题考点: 磁性、磁体、磁极;磁极间的相互作用.
考点点评: 本题考查了条形磁体的磁性特点和磁极间的作用规律:同名磁极相互排斥,异名磁极相互吸引.1年前查看全部
- (2014•西华县三模)根据如图微观示意图回答问题:
(2014•西华县三模)根据如图微观示意图回答问题:
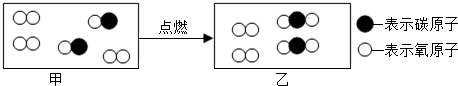
(1)写出该反应的化学方程式.
(2)请从微观角度写出甲和乙均属于混合物的判断依据.
(3)写出检验生成物的化学方程式. 小坭子1年前1
小坭子1年前1 -
 sanxi1963 共回答了20个问题
sanxi1963 共回答了20个问题 |采纳率100%解题思路:(1)根据反应的微观示意图,分析反应物、生成物,写出反应的方程式;
(2)根据甲、乙物质的微观构成分析;
(3)根据生成物的性质分析、写出反应的方程式.由反应的微观示意图和质量守恒定律可知,各物质反应的微粒个数关系是:
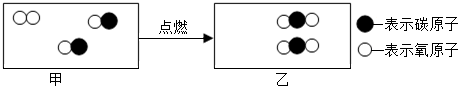
(1)由上述图示可知,一氧化碳燃烧生成了二氧化碳,反应的方程式是:2CO+O2
点燃
.
2CO2;
(2)由甲、乙物质的微观构成可知,甲、乙都是由不同种分子构成的物质.属于混合物;
(3)由上述分析可知,生成物是二氧化碳,常用澄清的石灰水进行检验,反应的方程式是:CO2+Ca(OH)2=CaCO3↓+H2O(1分).
故答为:(1)2CO+O2
点燃
.
2CO2; (2)甲和乙中都含有不同的分子.(3)CO2+Ca(OH)2=CaCO3↓+H2O.点评:
本题考点: 微粒观点及模型图的应用;纯净物和混合物的判别;书写化学方程式、文字表达式、电离方程式.
考点点评: 根据微观示意图,明确反应前后分子的构成、种类及个数,根据微观与宏观的对应关系,可以达到对所发生反应的判断.1年前查看全部
- (2014•西华县一模)小刚发现自己家利用太阳能晒水的大水桶是白色的,而邻居家的是黑色的,小刚想探究不同颜色物体的吸收太
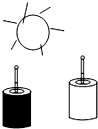 (2014•西华县一模)小刚发现自己家利用太阳能晒水的大水桶是白色的,而邻居家的是黑色的,小刚想探究不同颜色物体的吸收太阳光的本领是否相同了,于是他做了如下实验:将同样多、温度相同的水分别倒入两个矿泉水瓶中,用白纸和黑纸分别将瓶子包起来(如图)然后将两个瓶子放在太阳光下,每隔3分钟测一测瓶中水的温度.经过半个小时的实验,小明得到的两瓶中的水温变化情况如表所示:
(2014•西华县一模)小刚发现自己家利用太阳能晒水的大水桶是白色的,而邻居家的是黑色的,小刚想探究不同颜色物体的吸收太阳光的本领是否相同了,于是他做了如下实验:将同样多、温度相同的水分别倒入两个矿泉水瓶中,用白纸和黑纸分别将瓶子包起来(如图)然后将两个瓶子放在太阳光下,每隔3分钟测一测瓶中水的温度.经过半个小时的实验,小明得到的两瓶中的水温变化情况如表所示:
小刚对上述的实验数据进行了分析,得出了一个初步的结论.日照时间(min) 0 3 6 9 12 15 18 21 24 27 30 白纸瓶水温(0C) 23 24 25 25 26 27 27 28 29 29 30 黑纸瓶水温(0C) 23 25 26 27 28 29 30 31 32 33 34
(1)小刚得出的结论是:______.
(2)在这次过程中,小明所运用的科学研究方法是:______. 我是三原一角1年前1
我是三原一角1年前1 -
 beyond1 共回答了15个问题
beyond1 共回答了15个问题 |采纳率100%解题思路:(1)两瓶内装有相同质量、初温相同的水,通过比较在相同时间内水温升高的多少,根据吸热公式得出哪个瓶内吸热少,判断白纸和黑纸吸热性能;
(2)实验过程中将同样多、温度相同的水分别倒入两个矿泉水瓶中,放在太阳光下,每隔3分钟测一测瓶中水的温度;物体吸收热量的多少通过加热时间的长短得出.(1)由题知,两瓶内水的质量相同、初温相同,因为Q吸=cm△t,在相同的时间内(30min),黑纸瓶水温升高的多,水吸热多,所以黑纸的吸热性能好于白纸,由此我们得出的结论是:黑色物体比白色物体吸热本领强;
(2)物理学中对于多因素(多变量)的问题,常常采用控制因素(变量)的方法,把多因素的问题变成多个单因素的问题.每一次只改变其中的某一个因素,而控制其余几个因素不变,从而研究被改变的这个因素对事物的影响,分别加以研究,最后再综合解决,这种方法叫控制变量法.
故答案为:(1)黑色物体吸收太阳光本领强;(2)控制变量法.点评:
本题考点: 控制变量法与探究性实验方案.
考点点评: 此题主要是探究物质吸热能力的大小,应用的方法是控制变量法.1年前查看全部
- (2014•西华县三模)从物质分类的角度看,与氯化钠、水、铁属于同一类别的是( )
(2014•西华县三模)从物质分类的角度看,与氯化钠、水、铁属于同一类别的是( )
A.干冰
B.果汁
C.牛奶
D.空气 精灵格格1年前1
精灵格格1年前1 -
 嘻嘻0694 共回答了13个问题
嘻嘻0694 共回答了13个问题 |采纳率92.3%解题思路:氯化钠、水、铁均是由一种物质组成的,均属于纯净物,据此进行分析判断.氯化钠、水、铁均是由一种物质组成的,均属于纯净物.
A、干冰是固态的二氧化碳,是由一种物质组成的,属于纯净物,故选项正确.
B、果汁中含有水、维生素等,属于混合物,故选项错误.
C、牛奶中含有水、蛋白质等,属于混合物,故选项错误.
D、空气中含有氮气、氧气、二氧化碳等多种物质,属于混合物,故选项错误.
故选:A.点评:
本题考点: 纯净物和混合物的判别.
考点点评: 本题难度不大,掌握纯净物、混合物的特征是正确解答本题的关键.1年前查看全部
- (2014•西华县三模)下列对应的化学方程式书写正确的是( )
(2014•西华县三模)下列对应的化学方程式书写正确的是( )
A.正常雨水的pH约为5.6的原因:SO2+H2O═H2SO3
B.用含氢氧化镁的药物治疗胃酸过多症:2HCl+Ma(OH)2═MgCl2+2H2O
C.用盐酸除去氢氧化钾溶液中的碳酸钾:K2CO3+2HCl═2KCl+H2O+CO2↑
D.用稀硫酸除铁锈:H2SO4+FeO═FeSO4+H2O 李欣1年前1
李欣1年前1 -
 alibaba2007 共回答了19个问题
alibaba2007 共回答了19个问题 |采纳率89.5%解题思路:根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.A.正常雨水的pH约为5.6的原因二氧化碳与水反应生成碳酸,正确的化学方程式为:CO2+H2O═H2CO3.
B.该化学方程式书写完全正确.
C.盐酸既能与碳酸钾反应,也能与氢氧化钾反应,此方法错误;
D.铁锈的主要成分是氧化铁,反应的化学方程式为:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
故选B.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断;化学方程式正误判断方法是:先看化学式是否正确,再看配平,再看反应条件,再看气体和沉淀,最后短线改成等号.1年前查看全部
- (2013•西华县一模)(1)氢氧化钾与氢氧化钠溶液的化学性质非常相似,请说明原因.
(2013•西华县一模)(1)氢氧化钾与氢氧化钠溶液的化学性质非常相似,请说明原因.
(2)长期暴露在空气中的氢氧化钾溶液也会发生变质.请分别选用两种不同类别的物质,检验某氢氧化钾溶液已经变质(写试剂的化学式)______、______. 夜色太黑不宜飙车1年前1
夜色太黑不宜飙车1年前1 -
 什么都不算什么 共回答了19个问题
什么都不算什么 共回答了19个问题 |采纳率73.7%解题思路:(1)氢氧化钾与氢氧化钠都属于碱,碱具有相似的化学性质;
(2)氢氧化钾能够吸收空气中的二氧化碳,二氧化碳和氢氧化钾反应能生成碳酸钾和水.(1)氢氧化钠、氢氧化钾溶于水时,都能够电离出自由移动的氢氧根离子,所以氢氧化钾与氢氧化钠溶液的化学性质非常相似.
(2)氢氧化钾变质后,能够生成碳酸钾,碳酸钾属于碳酸盐,能和稀盐酸反应生成二氧化碳气体,碳酸钾能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钾;可以用稀盐酸、石灰水来检验氢氧化钾溶液是否已经变质,稀盐酸和石灰水中溶质的化学式分别是HCl、Ca(OH)2.
故填:HCl;Ca(OH)2.点评:
本题考点: 碱的化学性质;盐的化学性质.
考点点评: 化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,有助于提高观察实验、进行实验的能力.所以,对化学实验不仅要认真观察,还应掌握设计实验、观察实验现象的方法.1年前查看全部
- (2014•西华县一模)由于家庭电路中各种用电器都是______联的,用电器的增多会导致供电线路上的电流增大,这样家庭电
(2014•西华县一模)由于家庭电路中各种用电器都是______联的,用电器的增多会导致供电线路上的电流增大,这样家庭电路就会因______而造成干路电流过大.
 高速路口的风速1年前1
高速路口的风速1年前1 -
 leledelaopo 共回答了13个问题
leledelaopo 共回答了13个问题 |采纳率84.6%解题思路:家庭电路中的用电器都是并联的;且家庭电路电流过大的原因有两个;发生短路和用电器的总功率过大.家庭电路中,各用电器是并联的,即各个用电器的电压是相同的;据公式I=[P/U]可知,总功率越大,干路中的电流就会越大,根据焦耳定律Q=I2Rt,当电流过大时,干路导线会产生大量的热能,使导线温度升高,容易引起火灾.
故答案为:并;用电器总功率过大;点评:
本题考点: 家庭电路电流过大的原因.
考点点评: 知道家庭电路中用电器的连接方法及家庭电路中电流过大的原因是解决该题的关键;1年前查看全部
- (2014•西华县一模)物质的性质和用途是化学的重要研究内容.洗涤剂能除去油污,是因为它具有______功能;酒精常用作
(2014•西华县一模)物质的性质和用途是化学的重要研究内容.洗涤剂能除去油污,是因为它具有______功能;酒精常用作燃料,酒精燃烧的化学方程式为C2H5OH+3O2
2CO2+3H2O点燃 .C2H5OH+3O2.
2CO2+3H2O点燃 . grace3301年前1
grace3301年前1 -
 zqm43 共回答了21个问题
zqm43 共回答了21个问题 |采纳率85.7%解题思路:根据乳化作用的定义洗涤剂能使植物油分散成无数细小的液滴,而不聚成大的油珠,这些细小的液滴能随着水冲走,这种现象属于乳化作用.
根据反应物和生成物及其质量守恒定律可以书写化学方程式.洗涤剂具有乳化作用,能将大的油滴分散成细小的油滴随水冲走,这些细小的液滴能随着水冲走,故用洗涤剂能较好的除去餐具上的油污,是利用了洗涤剂具有乳化功能.
酒精燃烧生成水和二氧化碳,反应的化学方程式为:C2H5OH+3O2
点燃
.
2CO2+3H2O.
故答案为:乳化、C2H5OH+3O2
点燃
.
2CO2+3H2O点评:
本题考点: 乳化现象与乳化作用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,了解乳化作用的原理掌握质量守恒定律和化学方程式的书写方法是解决本题的关键.1年前查看全部
- 为什么半年内周口发生两次地震会在一个地方.(2010年10月24日在河南省周口市太康县、扶沟县、西华县交界
 yuanci20041年前1
yuanci20041年前1 -
 yiren315 共回答了16个问题
yiren315 共回答了16个问题 |采纳率93.8%2012来了1年前查看全部
- (2014•西华县一模)在微观、宏观之间建立联系是化学学习的特点.
 (2014•西华县一模)在微观、宏观之间建立联系是化学学习的特点.
(2014•西华县一模)在微观、宏观之间建立联系是化学学习的特点.
(1)在水、铜、氯化钠三种物质中,由离子构成的物质是______.
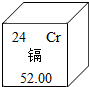
(2)据报道,某些药企业生产的胶囊中“镉”超标,长期服用会引起“镉中毒”.镉元素的相关信息如图所示.请回答:镉元素的核电荷数为______;镉原子失去3个电子所形成的离子符号为______;“镉中毒”中的镉是指______(填“分子”、“单质”或“元素”).
(3)下图是某密闭容器中某反应的微观示意图,“ ”和“
”和“ ”分别表示不同的原子,反应后方框内应再填入下列选项中的1个微粒是______ (填序号).
”分别表示不同的原子,反应后方框内应再填入下列选项中的1个微粒是______ (填序号).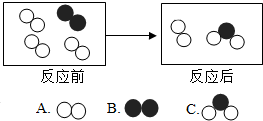
(4)下图是某反应的微观示意图,请从微观粒子变化的角度分析该反应的实质.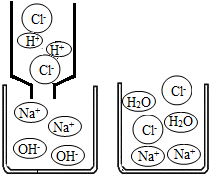
(5)酸和碱在组成和性质方面有很多共同的特点,请任写出其中的一条.
(6)质量分数为20%的氢氧化钠溶液40g与一定质量的稀硫酸恰好完全反应,计算生成硫酸钠的质量是多少. 旭棒棒1年前1
旭棒棒1年前1 -
 MEo0爱0o 共回答了17个问题
MEo0爱0o 共回答了17个问题 |采纳率76.5%解题思路:(1)根据构成物质的微粒分析回答;
(2)根据元素周期表的一个格提供的信息分析回答;
(3)根据质量守恒定律反应前后原子的种类及数目不变分析;
(4)根据反应的微观示意图,分析酸碱反应的实质;
(5)根据酸碱的组成和性质分析回答;
(6)根据反应的方程式进行计算.(1)在水、铜、氯化钠三种物质中,由离子构成的物质是氯化钠;
(2)由元素周期表的意义可知,镉元素的核电荷数=原子序数=24,镉原子失去3个电子形成带三个单位正电荷的镉离子,符号为:Cr3+;“镉中毒”中的镉是指“元素”.
(3)根据质量守恒定律反应前后原子的种类及数不变可知,反应后方框内应再填入下列选项中的1个微粒是C.
(4)由反应的微观示意图可知,该反应的实质是:H+ 和OH-结合生成水分子.
(5)由酸碱的组成和性质可知,在酸中都含有氢元素,都能与碱发生中和反应等;
(6)设生成硫酸钠的质量为x
2NaOH+H2SO4═Na2SO4+2H2O
2×40 142
40g×20% x
[2×40/142=
40g×20%
x] 解得:x═14.2g
故答为:(1)氯化钠;(2)24,Cr3+、元素;(3)C;(4)H+ 和OH-结合生成水分子;(5)都含有氢元素(或都能发生中和反应、能使酸碱指示剂变色、有腐蚀性等);(6)生成硫酸钠的质量是14.2g.点评:
本题考点: 微粒观点及模型图的应用;酸的化学性质;碱的化学性质;中和反应及其应用;分子、原子、离子、元素与物质之间的关系;元素周期表的特点及其应用;根据化学反应方程式的计算.
考点点评: 解答本题的关键是掌握核电荷数、质子数、核外电子数的关系及酸碱中和反应的实质、微粒观点及模型图的应用,只有这样才能对问题做出正确的判断.1年前查看全部
- (2013•西华县二模)请根据下图回答问题:
(2013•西华县二模)请根据下图回答问题:
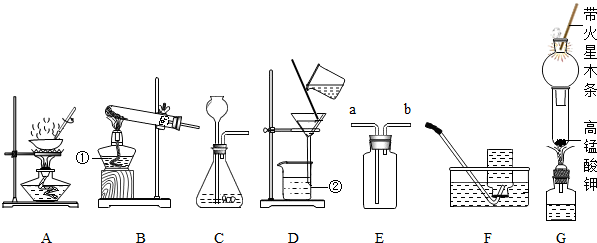
(1)实验室用B装置制取氧气,反应的方程式为:2KMnO4
K2MnO4+MnO2+O2↑△ .2KMnO4;收集装置若选E,用排空气法收集氧气,则气体应从______(填“a”或“b”) 端进入;若用装置F收集氧气,收集气体前,需要将集气瓶内先充满水,应如何进行操作?
K2MnO4+MnO2+O2↑△ .
(2)实验室常用C装置制取CO2,反应后,要得到氯化钙固体需要用到上述的______装置(填序号).
(3)某微型实验装置如上图G,该装置相当于上图装置的______(填序号). william_wu_qq1年前1
william_wu_qq1年前1 -
 浮云游子Y 共回答了14个问题
浮云游子Y 共回答了14个问题 |采纳率92.9%解题思路:(1)根据B装置的特点分析氧气的制取方法及反应原理;根据氧气的密度比空气大,选择进气口;根据用排水法收集气体的操作方法分析;
(2)根据反应后的物质杂质、氯化钙和水的性质分析分离方法;
(3)根据装置特点及所用反应物分析解答.(1)装置B适合加热高锰酸钾制取氧气,反应产生锰酸钾、二氧化锰和氧气,反应的方程式为:2KMnO4
△
.
K2MnO4+MnO2+O2↑;因为氧气的密度比空气大,因此进气口是长管;若用排水法收集氧气,集气瓶内装满水的方法是:将集气瓶充满水,用玻璃片盖住瓶口,然后把盛满水的集气瓶连同玻璃片一起倒立在盛水的水槽内;
(2)实验室制取二氧化碳后的物质有石灰石中含有的难溶性杂质、生成的氯化钙和水,因此要先通过过滤除去难溶性杂质,再通过蒸发除去水,即可得到氯化钙;
(3)图G是用加热高锰酸钾的方法制取氧气,与装置中的B原理是一样的;
故答案为:(1)2KMnO4
△
.
K2MnO4+MnO2+O2↑;a;将集气瓶充满水,用玻璃片盖住瓶口,然后把盛满水的集气瓶连同玻璃片一起倒立在盛水的水槽内;(2)AD(3)B.点评:
本题考点: 氧气的制取装置;氧气的收集方法;制取氧气的操作步骤和注意点;二氧化碳的实验室制法.
考点点评: 本题较综合的考查了学生对实验室制取氧气的反应原理、注意事项、常用仪器、装置选取方法等知识的掌握和应用,要加强平时知识的积累,才能结合具体情景分析解答相关问题.1年前查看全部
- (2014•西华县一模)根据安全用电常识,完成家庭电路连接:
 蓝色风06031年前1
蓝色风06031年前1 -
 Anni野蛮女友 共回答了22个问题
Anni野蛮女友 共回答了22个问题 |采纳率86.4%1年前查看全部
- (2013•西华县一模)下列图示的实验操作中,正确或能达到实验目的是( )
(2013•西华县一模)下列图示的实验操作中,正确或能达到实验目的是( )
A.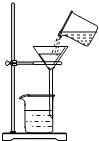
过滤
B.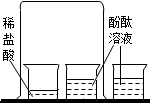 探究分子的运动
探究分子的运动
C.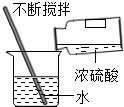
稀释浓硫酸
D.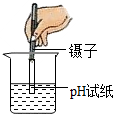
测溶液的pH 微笑通过1年前1
微笑通过1年前1 -
 phihb5 共回答了22个问题
phihb5 共回答了22个问题 |采纳率100%解题思路:A、过滤液体时,要注意“一贴、二低、三靠”的原则.
B、酚酞溶液遇酸性溶液不变色,遇碱性溶液变红色,稀盐酸显酸性.
C、根据浓硫酸的稀释方法进行分析判断.
D、根据用pH试纸测定未知溶液的pH时的方法进行分析判断.A、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流,图中所示操作错误.
B、酚酞溶液遇酸性溶液不变色,遇碱性溶液变红色;稀盐酸显酸性,不能使酚酞溶液变红色,观察不到明显的现象,不能用于探究分子的运动,图中所示操作错误.
C、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散,图中所示操作正确.
D、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH;不能将pH试纸伸入待测液中,以免污染待测液,图中所示操作错误.
故选C.点评:
本题考点: 过滤的原理、方法及其应用;浓硫酸的性质及浓硫酸的稀释;溶液的酸碱度测定;分子的定义与分子的特性.
考点点评: 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.1年前查看全部
- (2014•西华县一模)天然气的主要成分是______,农业上可用作复合肥料的一种物质______.
 maoxh1年前1
maoxh1年前1 -
 晾干了的黄花鱼 共回答了20个问题
晾干了的黄花鱼 共回答了20个问题 |采纳率80%解题思路:根据天然气的主要成分是甲烷,硝酸钾中含有氮元素和钾元素进行解答.天然气的主要成分是甲烷,化学式为CH4;硝酸钾中含有氮元素和钾元素,所以硝酸钾属于复合肥.
故答案为:CH4;KNO3.点评:
本题考点: 常用燃料的使用与其对环境的影响;常见化肥的种类和作用.
考点点评: 解答本题要掌握物质的分类方法,只有这样才能对各种物质进行正确的分类.1年前查看全部
- (2014•西华县一模)反应MnO2+4HCl(浓) △ . Mn
(2014•西华县一模)反应MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑常用于实验室制取氯气.该反应的反应物和生成物中,不存在的物质种类是( )△ .
A.单质
B.氧化物
C.碱
D.盐 paul091年前1
paul091年前1 -
 JOSE篮 共回答了12个问题
JOSE篮 共回答了12个问题 |采纳率91.7%解题思路:根据物质的组成分析解答.酸是由氢元素和酸根组成的化合物;碱是由金属元素和氢氧根组成的化合物;盐是由金属元素(或铵根)与酸根组成的化合物;单质是由同种元素组成的纯净物.A、在该反应的反应物和生成物中,C12是由同种元素组成的纯净物,属于单质,故不符合题意;
B、在该反应的反应物和生成物中,H2O是由氢氧两种元素组成水的化合物,属于氧化物.故不符合题意;
C、在该反应的反应物和生成物中,不存在由金属元素和氢氧根组成的化合物,没有碱.故符合题意;
D、在该反应的反应物和生成物中,MnCl2是由金属元素与酸根组成的化合物,属于盐,不符合题意.
故选:C.点评:
本题考点: 单质和化合物的判别;常见的氧化物、酸、碱和盐的判别.
考点点评: 了解各类物质的组成特点并会判别,是解答此类题的关键.1年前查看全部
- (2014•西华县三模)向盛有一定质量AgNO3和Cu(NO3)2的混合溶液中的烧杯中逐渐加入Zn粉,并边加边搅拌,溶液
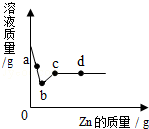 (2014•西华县三模)向盛有一定质量AgNO3和Cu(NO3)2的混合溶液中的烧杯中逐渐加入Zn粉,并边加边搅拌,溶液质量与加入Zn的质量关系如图所示.
(2014•西华县三模)向盛有一定质量AgNO3和Cu(NO3)2的混合溶液中的烧杯中逐渐加入Zn粉,并边加边搅拌,溶液质量与加入Zn的质量关系如图所示.
(1)a点的溶液中含有的金属离子有哪些(写离子符号)?
(2)写出b~c(不包括b点)段反应的化学方程式.
(3)d点的固体中含有几种物质? bb2002521年前1
bb2002521年前1 -
 漠子阳 共回答了9个问题
漠子阳 共回答了9个问题 |采纳率88.9%解题思路:根据金属与盐溶液的反应进行分析,在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,且置换时先把最弱的金属置换出来,并通过各反应的关系进行溶液质量的变化分析.在金属活动性顺序中,Zn>Cu>Ag,向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,与两种溶质依次发生反应
Zn+2AgNO3=Zn(NO3)2+2Ag
65 216
所以析出银的过程是溶液质量减少的过程;
Zn+Cu(NO3)2=Zn(NO3)2+Cu
65 64
所以析出铜的过程是溶液质量增加的过程.
(1)在a点时,硝酸银没有全部参加反应,溶液中含有硝酸银、硝酸铜和生成的硝酸锌,溶质是三种,因此对应的溶质的金属离子有:Ag+、Cu2+、Zn2+;
(2)b~c段是硝酸银全部参加反应完后锌和硝酸铜反应的过程,因此反应的方程式为:Zn+Cu(NO3)2═Zn(NO3)2+Cu;
(3)d点时锌过量,因此固体含有置换出的银和铜及过量的锌.
故答案为:(1)Ag+、Cu2+、Zn2+ (2)Zn+Cu(NO3)2═Zn(NO3)2+Cu
(3)3点评:
本题考点: 金属的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了金属活动性顺序的应用,要求学生熟悉金属的活动性顺序表,能利用活动性判断反应的发生,还要结合坐标分析各段的意义1年前查看全部
- (2013•西华县一模)如图是某输液瓶标签上的部分内容.由此可知,葡萄糖中碳、氢、氧三种元素的质量最简比为______.
 (2013•西华县一模)如图是某输液瓶标签上的部分内容.由此可知,葡萄糖中碳、氢、氧三种元素的质量最简比为______.要把20g这种葡萄糖溶液稀释为1%的溶液,需要水的质量为______ g.
(2013•西华县一模)如图是某输液瓶标签上的部分内容.由此可知,葡萄糖中碳、氢、氧三种元素的质量最简比为______.要把20g这种葡萄糖溶液稀释为1%的溶液,需要水的质量为______ g.  lcf78961年前1
lcf78961年前1 -
 shuangxi1980 共回答了21个问题
shuangxi1980 共回答了21个问题 |采纳率90.5%解题思路:根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
根据溶液稀释前后,溶质的质量不变,结合题意进行分析解答.葡萄糖中碳、氢、氧三种元素的质量最简比为(12×6):(1×12):(16×6)=6:1:8.
由某输液瓶标签上的部分内容可知,20g这种葡萄糖溶液的溶质质量分数为5%,
设要加水的质量为x,根据溶液稀释前后,溶质的质量不变,
则20g×5%=(20g+x)×1% x=80g.
故答案为:6:1:8;80.点评:
本题考点: 元素质量比的计算;用水稀释改变浓度的方法.
考点点评: 本题难度不大,掌握有关化学式的计算、溶液稀释前后溶质的质量不变是正确解答本题的关键所在.1年前查看全部
- (2014•西华县三模)如图为某学生设计的探究可燃物燃烧条件的实验.请回答:
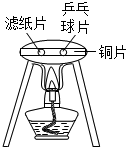 (2014•西华县三模)如图为某学生设计的探究可燃物燃烧条件的实验.请回答:
(2014•西华县三模)如图为某学生设计的探究可燃物燃烧条件的实验.请回答:
(1)通过此探究实验,可以说明燃烧的条件之一是什么?
(2)实验结束后,用灯帽可将酒精灯熄灭,该灭火方法的主要原理是什么? mangyuanty1年前1
mangyuanty1年前1 -
 gq55567 共回答了24个问题
gq55567 共回答了24个问题 |采纳率95.8%解题思路:根据燃烧的条件是:物质具有可燃性;可燃物与氧气接触;温度达到可燃物的着火点及灭火的方法分析.(1)滤纸、乒乓球碎片都与氧气接触,加热时它们先后燃烧起来,说明它们的着火点不同,可以说明燃烧的条件之一为可燃物的温度达到着火点才能燃烧;
故填:可燃物的温度达到着火点才能燃烧;
(3)实验结束后,用灯帽可将酒精灯熄灭,其灭火原理是使可燃物与氧气隔绝;
故填:使可燃物与氧气隔绝.点评:
本题考点: 燃烧与燃烧的条件;灭火的原理和方法.
考点点评: 本题考查了燃烧的条件和灭火的措施的探究,依据是物质燃烧需要三个条件:可燃物、与氧气接触、温度达到着火点,这三个条件缺一不可,因此,只要破坏燃烧的条件,就可以实现灭火.1年前查看全部
- (2013•西华县二模)(1)除去Na2SO4溶液中少量的Na2CO3,不能选用盐酸的原因是什么?
(2013•西华县二模)(1)除去Na2SO4溶液中少量的Na2CO3,不能选用盐酸的原因是什么?
(2)测定某溶液的pH时,先用水将pH试纸润湿会使结果______.(填“偏大”、“偏小”、“不变”或“无法确定”) 老乡1年前1
老乡1年前1 -
 磕打虫 共回答了13个问题
磕打虫 共回答了13个问题 |采纳率92.3%解题思路:(1)除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
(2)用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH.不能用水湿润pH试纸,否则稀释了待测溶液,使溶液的酸碱性减弱,测定结果不准确,据此进行分析判断.(1)Na2CO3能与盐酸反应生成氯化钠、水和二氧化碳,能除去杂质但引入了新的杂质氯化钠,不符合除杂原则.
(2)用水湿润pH试纸,稀释了待测溶液,使溶液的酸碱性减弱,若测定的是酸性溶液,则会使测定结果变大;若测定的是碱性溶液,则会使测定结果变小;若测定的是中性溶液,则会使测定结果不变;由于不知溶液的酸碱性,故无法确定测定结果.
故答案为:(1)引入了新的杂质氯化钠;(2)无法确定.点评:
本题考点: 物质除杂或净化的探究;溶液的酸碱度测定.
考点点评: 本题难度不大,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)、用pH试纸测定未知溶液的pH时的方法是正确解题的关键1年前查看全部
- (2014•西华县一模)小明将氢氧化钠溶液与硝酸钡溶液混合,发现无明显现象.一段时间后,他再次取敞口放置的上述两种溶液进
(2014•西华县一模)小明将氢氧化钠溶液与硝酸钡溶液混合,发现无明显现象.一段时间后,他再次取敞口放置的上述两种溶液进行混合,结果出现了白色沉淀.用化学方程式解释上述现象.
 韩剧迷妹妹1年前1
韩剧迷妹妹1年前1 -
 tanfeiblack 共回答了20个问题
tanfeiblack 共回答了20个问题 |采纳率80%解题思路:根据氢氧化钠溶液的性质回答,氢氧化钠溶液能吸收空气中的二氧化碳而生成碳酸钠.氢氧化钠溶液滴入硝酸钡溶液中,结果发现溶液中出现了白色沉淀:原因可能是NaOH溶液变质了,与空气中的CO2反应生成了Na2CO3,Na2CO3溶液与Ba(NO3)2溶液发生复分解反应生成了BaCO3白色沉淀.
反应的化学方程式分别为:CO2+2NaOH═Na2CO3+H2O;Na2CO3+Ba(NO3)2═BaCO3↓+2NaNO3.点评:
本题考点: 碱的化学性质;盐的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,考查氢氧化钠的化学性质、复分解反应发生的条件,掌握氢氧化钠的化学性质、复分解反应发生的条件正确解答本题的关键.1年前查看全部
- 刚刚是地震了吗?现在知道了北京时间2011年3月8日0时19分在河南省周口市太康县、扶沟县、西华县交界(北纬34.0,东
刚刚是地震了吗?
现在知道了
北京时间2011年3月8日0时19分在河南省周口市太康县、扶沟县、西华县交界(北纬34.0,东经114.6)发生4.3级地震,震源深度10公里. cole211年前1
cole211年前1 -
 红楼 共回答了20个问题
红楼 共回答了20个问题 |采纳率100%北京时间2011年3月8日0时19分在河南省周口市太康县、扶沟县、西华县交界(北纬34.0,东经114.6)发生4.3级地震,震源深度10公里.1年前查看全部
- 太康:北京时间2011-03-08 00:19 在河南省周口市太康县、扶沟县、西华县交界(北纬34.0,东经114.6)
太康:北京时间2011-03-08 00:19 在河南省周口市太康县、扶沟县、西华县交界(北纬34.0,东经114.6) 发生4.
 酿母f反抗1年前1
酿母f反抗1年前1 -
 toap 共回答了17个问题
toap 共回答了17个问题 |采纳率82.4%北京时间2011-03-08 00:19 在河南省周口市太康县、扶沟县、西华县交界(北纬34.0,东经114.6) 发生4.3级地震,深度10公里.1年前查看全部
- (2014•西华县三模)如图是实验室制取气体的常用装置.
(2014•西华县三模)如图是实验室制取气体的常用装置.
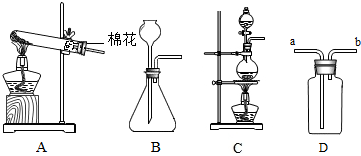
(1)请写出用A装置制取氧气的化学方程式
(2)在实验室里,可以用浓盐酸与二氧化锰在加热条件下起反应制取氯气(Cl2),则制取氯气应选择的发生装置是______(填装置标号).
(3)若用D装置除去CO2中混有的水蒸气,则装置内应装的试剂为______,气体应从______(填“a”或“b”)端通入. PengSd861年前1
PengSd861年前1 -
 arlq6i 共回答了23个问题
arlq6i 共回答了23个问题 |采纳率95.7%解题思路:制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.二氧化碳可以用浓硫酸干燥,应该长进短出;在实验室里,可以用浓盐酸与二氧化锰在加热条件下起反应制取氯气(Cl2),则制取氯气应选择的发生装置是C.(1)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;故答案为:2KMnO4
△
.
K2MnO4+MnO2+O2↑;
(2)在实验室里,可以用浓盐酸与二氧化锰在加热条件下起反应制取氯气(Cl2),则制取氯气应选择的发生装置是C,故答案为:C
(3)实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳可以用浓硫酸干燥,应该长进短出;故答案为:浓硫酸;a;点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;常见气体的检验与除杂方法;实验室制取氧气的反应原理;书写化学方程式、文字表达式、电离方程式.
考点点评: 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和气体的干燥等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.1年前查看全部
大家在问
- 1请问一下谁知道我国最早的诗歌总集是什么?了解的告诉下哟,十分谢谢了9N
- 2甲种酒精溶液中有酒精6升,水9升,乙种酒精溶液中有酒精9升,水3升,要配置50%的酒精溶液7升,两种酒精溶液各需多少升?
- 3告别昨天,把握今天,迎接明天……用英语怎么说
- 4已知一个四棱台的底面是正方形,侧面是全等的等腰梯形,上底面边长为3,下底面边长为6,侧棱长为4, 求一下表面积
- 5bring,take,fetch,get,carry有什么区别
- 6如果告诉的是原子的质量而非原子核的质量,那算质量亏损时要减去电子质量吗(反应物中还有一个电子)
- 7如图 将直角三角形abc沿直线bc向右平移后 到达三角形DEF的位置 如果ab=8 be=4 dh03 求阴影部分的面积
- 8列竖式计算,并用乖法验算:40.3/65=?怎么算,
- 9fine,little,far,unusual,calm,ill,worried,clever,thirsty的比较级和
- 10This gift is ___________ everyone. [
- 11百度一下我心目中的英雄英语作文80词
- 12如果I是角ABC,∠ACB的外角平分线的反向延长线的交点,设∠A和∠BIC为x、y,求x、y的关系式,并求x的取
- 1330度与60度的硅胶多少比例混炼出50度的硅胶
- 14画出以A(3,-1)、B(-1,1)、C(1,3)为顶点的△ABC的区域(包括各边),写出该区域所表示的二元一次不等式组
- 15已知函数f (x)= cosxsin( x+π/3)-√3cos²x+√3/4,x属于R.(1