(2014•路桥区模拟)某溶液,只可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、NO2-、CO32-、NO
 讨厌圣诞2022-10-04 11:39:541条回答
讨厌圣诞2022-10-04 11:39:541条回答①第一份加足量AgNO3溶液后,有5.84g白色沉淀产生,沉淀中加入足量稀盐酸充分反应,有棕色气体产生,沉淀颜色不变,但是质量减少0.1g;
②将产生的气体全部通入过量的澄清石灰水,又得到白色沉淀1.0g,该沉淀能溶于稀盐酸产生无色气体;
③第二份加入过量浓NaOH溶液,加热使产生的气体全部放出,用50mL0.5mol•L-1的硫酸溶液恰好完全吸收,酸也不剩余.
根据上述实验,以下推测不正确的是( )
A.原溶液一定不存在较大浓度的H+、Mg2+
B.原溶液确定含NH4+、NO2-、CO32-,且物质的量之比为5:2:1
C.不能确定原溶液是否含有K+、NO3-
D.实验中产生的棕色气体遇空气颜色会加深

已提交,审核后显示!提交回复
共1条回复
 儿子七个月 共回答了16个问题
儿子七个月 共回答了16个问题 |采纳率100%- 根据①可知该白色沉淀中一定含有亚硝酸银,亚硝酸银与盐酸反应生成氯化银与亚硝酸,亚硝酸不稳定分解生成NO、NO2和水,所以原溶液中一定含有NO2-,则H+一定不能大量共存;
根据②可知该白色沉淀应该是碳酸钙,物质的量为:[1.0g/100g/mol]=0.01mol,所以气体中含有CO2,这说明反应①中生成的白色沉淀一定有碳酸银,则原溶液中一定含有CO32-,则Mg2+就一定不能大量共存;根据碳原子守恒,CO32-的物质的量是0.01mol,5.84g沉淀中亚硝酸银沉淀的质量为:5.84g-0.01mol×276g/mol=3.08g,因此亚硝酸银的物质的量为:[3.08g/154g/mol]=0.02mol,则原溶液中NO2-的物质的量是0.02mol;
根据③可知,该气体一定是氨气,因此原溶液中含有NH4+;用50mL0.5mol/L的硫酸溶液恰好完全吸收,酸也不剩余,硫酸的物质的量是0.5mol/L×0.05L=0.025mol,则氨气的物质的量为:0.025mol×2=0.05mol,则原溶液中NH4+的物质的量是0.05mol,
A.根据以上分析可知,原溶液中一定不存在较大浓度的H+、Mg2+,故A正确;
B.根据以上分析可知,原溶液一定存在NH4+、NO2-、CO32-,且物质的量之比为:0.05mol:0.02mol:0.01mol=5:2:1,故B正确;
C.根据电荷守恒可知,原溶液中一定还含有NO3-,但K+不能确定是否存在,故C错误;
D.实验中产生的棕色气体中含有NO,遇空气生成红棕色NO2,所以颜色会加深,故D正确;
故选C. - 1年前
相关推荐
- (2014•路桥区模拟)A、B、C、D、E五种短周期元素,它们的原子序数依次增大,最外层电子数之和为19.A的周期数等于
(2014•路桥区模拟)A、B、C、D、E五种短周期元素,它们的原子序数依次增大,最外层电子数之和为19.A的周期数等于族序数,在短周期中D元素的原子半径最大,C与E质子数之比为1:2,B与C形成的化合物在大气中排放易产生光化学烟雾.则下列说法正确的是( )
A.B的气态氢化物稳定性较C的强
B.C与D形成的一种化合物与水反应能产生C2单质
C.均由A、C、D、E四种元素形成的两种盐不能相互反应
D.B的最高价氧化物对应的水化物与其最低价氢化物反应生成的化合物为共价化合物 寻盐记1年前1
寻盐记1年前1 -
 一二一一 共回答了22个问题
一二一一 共回答了22个问题 |采纳率100%解题思路:A、B、C、D、E五种短周期元素,它们的原子序数依次增大,B与C形成的化合物在大气中排放易产生光化学烟雾,二者形成氮的氧化物,可推知B为N元素、C为O元素;C与E质子数之比为1:2,则E的质子数=8×2=16,则E为S元素;在短周期中D元素的原子半径最大,则D为Na元素;5元素最外层电子数之和为19,则A的最外层电子数=19-5-6-1-6=1,且A的周期数等于族序数,则A为H元素,据此解答.A、B、C、D、E五种短周期元素,它们的原子序数依次增大,B与C形成的化合物在大气中排放易产生光化学烟雾,二者形成氮的氧化物,可推知B为N元素、C为O元素;C与E质子数之比为1:2,则E的质子数=8×2=16,则E为S元素;在短周期中D元素的原子半径最大,则D为Na元素;5元素最外层电子数之和为19,则A的最外层电子数=19-5-6-1-6=1,且A的周期数等于族序数,则A为H元素,
A.非金属性N<O,故N的气态氢化物稳定性较O的弱,故A错误;
B.C与D形成的化合物Na2O2与水反应能产生O2单质,故B正确;
C.均由H、O、Na、S四种元素形成的两种盐为亚硫酸氢钠、硫酸氢钠,二者反应生成硫酸钠、二氧化硫与水,故C错误;
D.B的最高价氧化物对应的水化物为硝酸,其最低价氢化物为氨气,二者反应生成硝酸铵,硝酸铵属于离子化合物,故D错误,
故选B.点评:
本题考点: 原子结构与元素周期律的关系.
考点点评: 本题考查结构性质位置关系应用,推断元素是解题关键,侧重对基础知识的巩固考查,难度不大.1年前查看全部
- (2014•路桥区模拟)如图甲是CO2电催化还原为碳氢化合物的工作原理示意图,用一种钾盐水溶液作电解液;图乙是用H2还原
(2014•路桥区模拟)如图甲是CO2电催化还原为碳氢化合物的工作原理示意图,用一种钾盐水溶液作电解液;图乙是用H2还原CO2制备甲醇的工作原理示意图,硫酸为电解质溶液.下列说法不正确的是( )
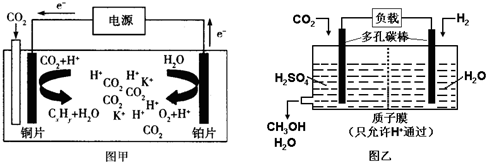
A.甲中铜片作阴极,K+向铜片电极移动
B.乙中正极发生的电极反应为CO2+6e-+6H+═CH3OH+H2O
C.甲中若CxHy为C2H4,则生成1mol C2H4的同时生成2mol O2
D.乙中H2SO4的作用是增强溶液的导电性 sunshine12451年前1
sunshine12451年前1 -
 美丽男孩 共回答了19个问题
美丽男孩 共回答了19个问题 |采纳率78.9%解题思路:甲图中:CO2电催化还原为碳氢化合物,由电子流向可知,则通入CO2的一极为电解池的阴极,另一极为阳极,阳极上氢氧根离子失电子生成氧气,乙图中,燃料电池的正极上氧气发生得电子的还原反应.A.电解时,电子流向是:阳极→正极→负极→阴极,铜为阴极,所以阳离子K+向铜片电极移动,故A正确;
B.由图可知乙中正极上是二氧化碳发生得电子的还原反应的过程,发生的电极反应为CO2+6e-+6H+═CH3OH+H2O,故B正确;
C.若CxHy为C2H4,则电解的总反应为:2CO2+2H2O
通电
.
3O2+C2H4,所以生成1 mol C2H4的同时生成3 molO2,故C错误;
D.乙中电解质溶液H2SO4的作用是增强导电性,故D正确;
故选C.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查学生电解池的工作原理知识,侧重于学生的分析能力的考查,注意两极反应式的书写以及氧化还原反应之间的关系,注意规律的总结是关键,难度不大.1年前查看全部
- (2011•路桥区模拟)在盒子里放有三张分别写着数字[1/3]、2、π的卡片,从中随机抽取1张卡片,是无理数的概率是
(2011•路桥区模拟)在盒子里放有三张分别写着数字[1/3]、
、π的卡片,从中随机抽取1张卡片,是无理数的概率是2 [2/3][2/3]. 因为她身1年前1
因为她身1年前1 -
 我爱柔然 共回答了24个问题
我爱柔然 共回答了24个问题 |采纳率95.8%解题思路:根据题意可得:3张小卡片上分别写着数字[1/3]、
、π的卡片,其中无理数为2
、π、有两个,则从中随机抽取一张卡片,抽到无理数的概率是[2/3].2 ∵3张小卡片上分别写着数字[1/3]、
2、π的卡片,其中无理数为
2、π、有两个,
根据概率的求法,
∴从中随机抽取1张卡片,是无理数的概率是[2/3],
故答案为[2/3].点评:
本题考点: 概率公式.
考点点评: 本题主要考查了概率的求法,如果一个事件有n种可能,而且这些事件的可能性相同,其中事件A出现m种结果,那么事件A的概率P(A)=[m/n],难度适中.1年前查看全部
- (2014•路桥区模拟)随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气
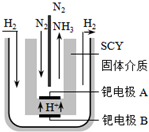 (2014•路桥区模拟)随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气稀释的氮气,分别通入一个加热到570℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图).下列有关说法中正确的是( )
(2014•路桥区模拟)随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气稀释的氮气,分别通入一个加热到570℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图).下列有关说法中正确的是( )
A.电解法合成氨的电解池中能用水作电解质溶液的溶剂
B.钯电极B连接的是电源的负极
C.钯电极A的电极反应式为:N2+6e-+6H+═2NH3
D.当有0.3mol电子转移时,有2.688L NH3生成 朵朵3841年前1
朵朵3841年前1 -
 我是你的他_ 共回答了19个问题
我是你的他_ 共回答了19个问题 |采纳率94.7%解题思路:反应总方程式为N2+3H2⇌2NH3,反应中N元素化合价降低,被还原,应为电解池阴极反应,电解方程式为N2+6e-+6H+═2NH3,H元素化合价升高,被氧化,应为电解池阳极反应,电极方程式为H2-2e-=2H+,以此解答该题.A.在电解法合成氨的电解池中不能用水作电解质溶液的溶剂,原因是新法合成氨电解池的反应温度是570℃时,水为水蒸气,故A错误;
B.由氢离子移动方向可知A为银极,B为阳极,阳极连接电源正极,故B错误;
C.A为阴极,发生还原反应,电解方程式为N2+6e-+6H+═2NH3,故C正确;
D.由于气体存在的条件不一定为标准状况下,则不能确定气体的体积,故D错误.
故选C.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题综合考查原电池和电解质知识,为高频考点,侧重于学生的分析能力的考查,注意把握电化学工作原理,难度不大,注意相关基础知识的积累.1年前查看全部
- (2014•路桥区模拟)采用一定手段破坏细胞中的内质网,下列各项受影响最小的是( )
(2014•路桥区模拟)采用一定手段破坏细胞中的内质网,下列各项受影响最小的是( )
A.浆细胞加工合成抗体
B.性腺细胞合成并分泌性激素
C.兴奋在突触处的传递
D.各种生物膜在结构与功能上的联系 不准下雨1年前1
不准下雨1年前1 -
 付秋菊_cc 共回答了18个问题
付秋菊_cc 共回答了18个问题 |采纳率94.4%解题思路:1、内质网与分泌蛋白加工相关,故对分泌蛋白影响较大,抗体为分泌蛋白,故影响较大.
2、性激素为脂质,内质网与脂质合成相关,故影响较大.
3、兴奋在突触处的传递通过神经递质传递,而递质通过细胞膜的胞吐释放,故影响较小.
4、内质网是生物膜系统膜面积最大、分布最广的生物膜,与其他生物膜联系密切,故影响较大.A、内质网能对蛋白质进行加工和脂质合成的车间,故浆细胞合成加工抗体与内质网有关,A错误;
B、性细胞合成和分泌性激素,内质网有关脂质的合成有关,B错误;
C、兴奋在突触处的传递发生信号的变化,与高尔基体有关,C正确;
D、各种生物膜的结构上的联系,与内质网密切相关,D错误.
故选:C.点评:
本题考点: 细胞器中其他器官的主要功能;细胞器之间的协调配合.
考点点评: 本题考查内质网的功能,意在考查学生的识记和理解能力,属于中档题.1年前查看全部
- (2014•路桥区模拟)下列说法不正确的是( )
(2014•路桥区模拟)下列说法不正确的是( )
A.在自然界中存在的单质,一定具备化学性质稳定、不与其它物质发生反应这一特征
B.100多年前,英国曾耗巨资改建高炉,试图延长CO和Fe2O3的接触时间,以减少CO的排放,这违背了化学反应都有一定限度这一基本原理
C.在溶液中,有色物质参与的反应,可以用分光光度计来测定其化学反应速率
D.虽然碳酸钙分解需要吸收大量的热,但在高温条件下也能自发进行 泥罢罢1年前1
泥罢罢1年前1 -
 caixinle 共回答了20个问题
caixinle 共回答了20个问题 |采纳率95%解题思路:A.氧气性质活泼,但是能够存在于自然界中;
B.CO和Fe2O3的反应为可逆反应,可逆反应不能进行到底,存在一定限度;
C.分光光度计是测定化学反应速率的一种方法;
D.反应能否自发进行取决与△H-T△S是否小于0.A.氧气为活泼非金属单质,能够与很多物质发生反应,但是能够在自然界中存在,故A错误;
B.CO和Fe2O3的反应为可逆反应,所以不能沿一个方向进行到底,故B正确;
C.在溶液中,有色物质参与的反应,可以用分光光度计来测定其化学反应速率,故C正确;
D.虽然碳酸钙分解需要吸收大量的热,但在高温条件下也能满足△H-T△S<0,能够自发进行,故D正确;
故选:A.点评:
本题考点: 化学的主要特点与意义;化学反应的基本原理;反应热和焓变.
考点点评: 本题考查了化学的特点和意义、可逆反应的特点、反应自发进行的判断依据,题目难度中等,注意一个反应能否自反进行与反应的焓变与熵变都有关系.1年前查看全部
- (2011•路桥区模拟)如图,已知:点B、F、C、E在一条直线上,BC=EF,AB=DE.
(2011•路桥区模拟)如图,已知:点B、F、C、E在一条直线上,BC=EF,AB=DE.
(1)请你只添加一个条件(不再加辅助线),使△ABC≌△DEF,你添加的条件是______;
(2)在你添加的条件后,证明△ABC≌△DEF.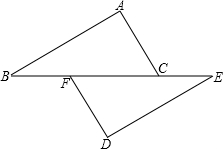
 青春不存在1年前1
青春不存在1年前1 -
 冲冠一怒为红颜 共回答了25个问题
冲冠一怒为红颜 共回答了25个问题 |采纳率96%(1)∠B=∠E或AC=DF,
(2)证明:当∠B=∠E时
在△ABC和△DEF中
BC=EF
∠B=∠E
AB=DE,
∴△ABC≌△DEF(SAS).1年前查看全部
- 求台州市路桥区八年级上数学期末统考卷(二)的参考答案!是一开头是奥林匹克轴对称什么的选择题的那张
 aztec0001年前1
aztec0001年前1 -
 孤寂的鹰 共回答了19个问题
孤寂的鹰 共回答了19个问题 |采纳率84.2%神怡的感觉.通过教学,既能培养学生的审美眼光,也能培养学1年前查看全部
- (2014•路桥区模拟)如图为果蝇的染色体组成示意图,请据图回答:
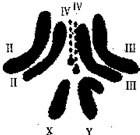 (2014•路桥区模拟)如图为果蝇的染色体组成示意图,请据图回答:
(2014•路桥区模拟)如图为果蝇的染色体组成示意图,请据图回答:
(1)已知果蝇的Ⅲ号染色体上有黑檀体基因.现将黑檀体无眼果蝇与灰体有眼果蝇杂交,获得的F1均为灰体有眼果蝇,说明无眼为______性状;再将F1雌雄果蝇相互杂交,若F2表现型及比例为______,则可推测控制无眼的基因不在Ⅲ号染色体上;将无眼基因与位于Ⅱ号染色体上的基因进行重组实验时,若实验结果与上述实验结果______,则可推测控制无眼的基因极可能位于Ⅳ号染色体上.
(2)已知控制果蝇翅型的基因在Ⅱ号染色体上.如果在一翅型正常的群体中,偶然出现一只卷翅的雄性个体,这种卷翅究竟是由于基因突变的直接结果,还是由于卷翅基因的“携带者”偶尔交配后出现的呢?
①分析:如果卷翅是由于基因突变的直接结果,则该卷翅雄性个体最可能为______(纯合子/杂合子);如果卷翅是由于卷翅基因的“携带者”偶尔交配后出现的,则该卷翅雄性个体最可能为______.
②探究实验方案设计:______.
③结论:如果后代出现______,则卷翅是由于基因突变的直接结果;如果后代出现______,则卷翅是由于卷翅基因的“携带者”偶尔交配后出现的. 阳阳20051年前1
阳阳20051年前1 -
 南dd以北 共回答了17个问题
南dd以北 共回答了17个问题 |采纳率100%解题思路:阅读题干和题图可知,本题涉及的知识有基因的自由组合定律和染色体变异,明确知识点后梳理相关的基础知识,然后解析题图结合问题的具体提示综合作答.(1)果蝇的III号染色体为常染色体,亲代为黑檀体无眼果蝇与灰体有眼果蝇杂交,子一代全部为灰体有眼果蝇,说明有眼对无眼为显性,无眼为隐性性状,灰体对黑檀体为显性性状,黑檀体为隐性性状.如果无眼的基因不在III号染色体上,那么体色与有无眼就遵循自由组合定律,由此可知如果F2表现型灰体有眼:灰体无眼:黑檀体有眼:黑檀体无眼=9:3:3:1就遵循自由组合定律.将无眼基因与位于Ⅱ号染色体上的基因进行重组实验时,若实验结果与上述实验结果相似,说明该基因不在II号染色体上,这些性状和性别没关系,那最可能位于IV号染色体上.
(2)①基因突变的频率很低,如果卷翅是基因突变的直接结果,所以最可能是杂合子.如果由于卷翅基因的“携带者”偶尔交配后出现的,携带者提供一个卷翅基因,这个雄性个体表现出卷翅,最可能是隐性纯合子.
②要探究卷翅究竟是由于基因突变的直接结果,还是由于卷翅基因的“携带者”偶尔交配后出现的就用这只卷翅雄性个体与多只正常雌性个体交配.
③如果后代卷翅个体与正常个体且数量比接近1:1,这只雄性果蝇应该是杂合子,应是基因突变的直接结果.如果后代全部是正常个体或正常个体数量多于卷翅个体,这只雄果蝇应该是纯合子,应是由于卷翅基因的“携带者”偶尔交配后出现的.
故答案为:
(1)隐性 灰体有眼:灰体无眼:黑檀体有眼:黑檀体无眼=9:3:3:1相似
(2)①杂合子隐性纯合子②用这只卷翅雄性个体与多只正常雌性个体交配
③卷翅个体与正常个体且数量比接近1:1全部是正常个体或正常个体数量多于卷翅个体点评:
本题考点: 基因的自由组合规律的实质及应用.
考点点评: 本题考查遗传相关知识点,考查考生从图形中提取信息,分析以及对遗传定律知识点的理解和实际运用解决问题的能力.1年前查看全部
- (2014•路桥区模拟)下列说法正确的是( )
(2014•路桥区模拟)下列说法正确的是( )
A.某烷烃的名称为2,2,4,4-四甲基-3,3,5-三乙基己烷
B.等质量的甲醛与乳酸[CH3CH(OH)COOH]完全燃烧消耗氧气的量不相等
C.结构片段为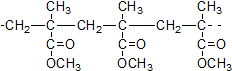 的高聚物,是其单体通过缩聚反应生成
的高聚物,是其单体通过缩聚反应生成
D.化合物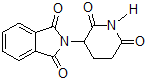 在酸性条件下水解,所得溶液加碱后加热有NH3生成
在酸性条件下水解,所得溶液加碱后加热有NH3生成  oiaa1年前1
oiaa1年前1 -
 我-79 共回答了24个问题
我-79 共回答了24个问题 |采纳率91.7%解题思路:A、根据烷烃的命名原则进行判断;
B、醛和乳酸的最简式相同,等质量的二者完全燃烧时消耗的氧气的量相同;
C、根据该高聚物的主链全部为C可知,该高聚物是通过加聚反应生成的高分子化合物;
D、该化合物中含有肽键,酸性条件下水解生成铵离子,加碱溶液后加热,铵离子与氢氧根离子反应成氨气.A、烷烃的主链为己烷,不可能存在5-乙基,说明选取的主链不是最长的,最长主链含有7个C主链为庚烷,正确命名应该为2,2,4,4,5-五甲基-3,3-二乙基-庚烷,故A错误;
B、甲醛分子式CH2O,乳酸的最简式为CH2O,所以等质量的甲醛与乳酸[CH3CH(OH)COOH]完全燃烧消耗氧气的量相等,故B错误;
C、根据该高分子化合物的结构片段可知,主链只含有碳原子,该高分子化合物是通过加聚反应生成的,故C错误;
D、化合物 在酸性条件下水解产物中含有铵离子,然后在碱性溶液中加热,铵离子与氢氧根离子反应生成氨气,故D正确;
在酸性条件下水解产物中含有铵离子,然后在碱性溶液中加热,铵离子与氢氧根离子反应生成氨气,故D正确;
故选D.点评:
本题考点: 有机化合物命名;有机物分子中的官能团及其结构;聚合反应与酯化反应.
考点点评: 本题考查了有机物的命名,题目难度不大,该题注重了基础性试题的考查,侧重对学生基础知识的检验和训练,该题的关键是明确有机物的命名原则,然后结合有机物的结构简式灵活运用即可,有利于培养学生的规范答题能力.1年前查看全部
- (2014•路桥区模拟)A、B、C、D、E为原子序数依次增大的5种短周期元素,A最外层电子数是其电子层数的两倍;B能形成
(2014•路桥区模拟)A、B、C、D、E为原子序数依次增大的5种短周期元素,A最外层电子数是其电子层数的两倍;B能形成双原子阴离子;C与B能形成两种常见的离子化合物,B、E同主族,C、D、E的最高价氧化物对应的水化物之间两两皆能反应生成盐和水.请回答下列问题:
(1)B的双原子阴离子电子式为______:用化学式表示一种由B、C、E组成的物质______.
(2)B的氢化物比E的氢化物的沸点______ (填“高”或“低”),理由是______.
(3)B、C、D组成化合物的水溶液与过量AB2反应的离子方程式______.
(4)已知X是由上述五种元素中的两种组成的离子化合物,其离子具有相同的电子层结构,气体甲是天然气的主要成分.
i.写出反应①的化学方程式______.
ii.若红色固体乙是一种单质,写出反应③的化学方稈式CH4+4CuO
4Cu+CO2+2H2O高温 .CH4+4CuO.
4Cu+CO2+2H2O高温 .
(5)若某气体含有AB2和EB2中的一种或两种,请设计实验方案,探究该气体的成分______. 猪在狂笑1年前1
猪在狂笑1年前1 -
 6805711 共回答了16个问题
6805711 共回答了16个问题 |采纳率93.8%解题思路:A、B、C、D、E为原子序数依次增大的5种短周期元素,A最外层电子数是其电子层数的两倍,只能碳或硫,结合原子序数可知,A为碳;B能形成双原子阴离子,则B为O元素;B、E同主族,则E为S元素;C与B能形成两种常见的离子化合物,且C、D、E的最高价氧化物对应的水化物之间两两皆能反应生成盐和水,应是氢氧化铝与强酸、强碱的反应,则C为Na、D为Al,据此解答.A、B、C、D、E为原子序数依次增大的5种短周期元素,A最外层电子数是其电子层数的两倍,只能碳或硫,结合原子序数可知,A为碳;B能形成双原子阴离子,则B为O元素;B、E同主族,则E为S元素;C与B能形成两种常见的离子化合物,且C、D、E的最高价氧化物对应的水化物之间两两皆能反应生成盐和水,应是氢氧化铝与强酸、强碱的反应,则C为Na、D为Al,
(1)B的双原子阴离子为O22-,电子式为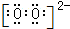 ,由O、Na、S组成的物质有:Na2SO4、Na2SO3、Na2S2O4 等,
,由O、Na、S组成的物质有:Na2SO4、Na2SO3、Na2S2O4 等,
故答案为: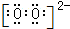 ;Na2SO4、Na2SO3、Na2S2O4 (任意一种);
;Na2SO4、Na2SO3、Na2S2O4 (任意一种);
(2)水分子之间存在氢键,故沸点比硫化氢高,
故答案为:高;水分子之间存在氢键;
(3)O、Na、Al组成化合物为NaAlO2,其水溶液与过量CO2反应的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
故答案为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(4)气体甲是天然气的主要成分,则甲为CH4,X是由上述五种元素中的两种组成的离子化合物,其离子具有相同的电子层结构,且X与水反应得到甲烷与沉淀,应是金属碳化物与水反应,可推知X为Al4C3,反应得到的沉淀为氢氧化铝,甲烷与CuO反应得到红色固体单质乙为Cu,根据电子转移守恒可知有二氧化碳生成,同时生成水,
i.反应①的化学方程式为:Al4C3+12H2O=4Al(OH)3↓+3CH4↑,
ii.反应③的化学方程式为:CH4+4CuO
高温
.
4Cu+CO2+2H2O,
故答案为:Al4C3+12H2O=4Al(OH)3↓+3CH4↑;CH4+4CuO
高温
.
4Cu+CO2+2H2O;
(5)若某气体含有CO2和SO2中的一种或两种,请设计实验方案,探究该气体的成分,实验方案为:将气体依次通过盛有酸性高锰酸钾溶液、品红溶液、澄清石灰水的洗气瓶,若酸性高锰酸钾溶液褪色(或变浅),且品红不褪色、澄清石灰水变浑浊,为SO2、CO2的混合气体,若只有酸性高锰酸钾溶液褪色(或变浅),为SO2气体,若只有澄清石灰水变浑浊,为CO2气体,
故答案为:将气体依次通过盛有酸性高锰酸钾溶液、品红溶液、澄清石灰水的洗气瓶,若酸性高锰酸钾溶液褪色(或变浅),且品红不褪色、澄清石灰水变浑浊,为SO2、CO2的混合气体,若只有酸性高锰酸钾溶液褪色(或变浅),为SO2气体,若只有澄清石灰水变浑浊,为CO2气体.点评:
本题考点: 位置结构性质的相互关系应用;无机物的推断.
考点点评: 本题考查结构性质位置关系应用、无机物推断、实验方案设计等,(4)中X推断为易错点、难点,注意利用碳化钙进行迁移,难点中等.1年前查看全部
- (2014•路桥区模拟)在某一溶液中可能含有下列几种离子:K+、Fe3+、Ag+、Ba2+、NO2-、AlO2-、CO3
(2014•路桥区模拟)在某一溶液中可能含有下列几种离子:K+、Fe3+、Ag+、Ba2+、NO2-、AlO2-、CO32-、SO32-、SO42-.某该溶液进行有关实验,实验步骤及结果如下:
①向溶液中加入过量稀盐酸,得到气体甲和溶液甲;
②向溶液甲中加入过量NH4HCO3溶液,得到白色沉淀乙、气体乙和溶液乙;
③向溶液乙中加入过量Ba(OH)2溶液并加热,得到白色沉淀丙、气体丙和溶液丙.
④检验气体甲、气体乙、气体丙,都只含有一种成分,而且各不相同.
下列说法正确的是( )
A.气体甲可能为CO2 或者SO2
B.沉淀丙中一定含有BaCO3,可能含有BaSO4
C.该溶液中肯定存在的离子有K+、AlO2-、SO32-、SO42-、NO2-
D.只根据实验①能得出溶液中一定没有Fe3+、Ag+、Ba2+,K+是否存在无法确定 58会一58民1年前1
58会一58民1年前1 -
 蒙面黑8 共回答了21个问题
蒙面黑8 共回答了21个问题 |采纳率81%解题思路:在某一溶液中可能含有下列几种离子:K+、Fe3+、Ag+、Ba2+、NO2-、AlO2-、CO32-、SO32-、SO42-.某该溶液进行有关实验,实验步骤及结果如下:
①向溶液中加入过量稀盐酸,得到气体甲和溶液甲,则含有CO32-、SO32-中的至少一种离子,一定不含Fe3+、Ag+、Ba2+,气体甲是二氧化碳或是二氧化硫;
②向溶液甲中加入过量NH4HCO3溶液,得到白色沉淀乙、气体乙和溶液乙,一定含有AlO2-,沉淀乙是氢氧化铝,气体乙是二氧化碳;
③向溶液乙中加入过量Ba(OH)2溶液并加热,得到白色沉淀丙、气体丙和溶液丙,则一定会含有SO42-,
④检验气体甲、气体乙、气体丙,都只含有一种成分,而且各不相同,则气体分别是:二氧化硫、二氧化碳和氨气.在某一溶液中可能含有下列几种离子:K+、Fe3+、Ag+、Ba2+、NO2-、AlO2-、CO32-、SO32-、SO42-.某该溶液进行有关实验,实验步骤及结果如下:
①向溶液中加入过量稀盐酸,得到气体甲和溶液甲,则含有CO32-、SO32-中的至少一种离子,一定不含Fe3+、Ag+、Ba2+,气体甲是二氧化碳或是二氧化硫;
②向溶液甲中加入过量NH4HCO3溶液,得到白色沉淀乙、气体乙和溶液乙,一定含有AlO2-,沉淀乙是氢氧化铝,气体乙是二氧化碳;
③向溶液乙中加入过量Ba(OH)2溶液并加热,得到白色沉淀丙、气体丙和溶液丙,则沉淀一定有BaCO3;
④检验气体甲、气体乙、气体丙,都只含有一种成分,而且各不相同,则气体分别是:二氧化硫、二氧化碳和氨气.
A、向溶液中加入过量稀盐酸,得到气体甲和溶液甲,则含有CO32-、SO32-中的至少一种离子,体乙是二氧化碳,气体甲SO2,故A错误;
B、沉淀丙中一定含有Ba(OH)2溶液和过量NH4HCO3溶液反应生成的BaCO3,可能含有BaSO4,故B正确;
C、该溶液中肯定存在的离子有K+、AlO2-、SO32-,故C错误;
D、根据实验①能得出溶液中一定没有Fe3+、Ag+、Ba2+,根据电荷守恒吗,则K+一定存在,故D错误.
故选B.点评:
本题考点: 常见阳离子的检验;常见阴离子的检验.
考点点评: 本题考查了离子检验的实验方法和反应现象分析判断,熟练掌握离子共存的条件及离子性质是解题关键,题目难度中等.1年前查看全部
- (2014•路桥区模拟)下列说法不正确的是( )
(2014•路桥区模拟)下列说法不正确的是( )
A.制摩尔盐时用酒精洗涤产品,制阿司匹林时用冷水洗涤产品
B.培养明矾晶体时,为得到较大颗粒的晶体,应自然冷却,并静置过夜
C.铁钉镀锌前,先要用砂纸打磨直至表面变得光滑,然后放入氢氧化钠溶液中浸泡5分钟,用水洗净后还需放入稀盐酸中浸泡,再用水洗净
D.做“食醋总酸含量的测定”实验时,必须先将市售食醋稀释10倍,然后用洗净的酸式滴定管量取一定体积的稀释液于洁净的锥形瓶中,锥形瓶不需要先用醋酸溶液润洗 jsjjzyc1年前1
jsjjzyc1年前1 -
 keven_li 共回答了14个问题
keven_li 共回答了14个问题 |采纳率85.7%解题思路:A.摩尔盐在有机溶剂中的溶解度小,阿司匹林的溶解度随温度的升高而增大;
B.应使饱和溶液缓慢冷却;
C.电镀前应除掉表面的杂质;
D.酸式滴定管需要润洗.A.摩尔盐在有机溶剂中的溶解度小,因此制摩尔盐时用酒精洗涤产品,可以减少晶体的溶解;阿司匹林的溶解度随温度的升高而增大,因此制阿司匹林时用冷水洗涤产品可以减少固体的溶解,故A正确;
B.应使饱和溶液缓慢冷却才能得到较大颗粒的晶体,故B正确;
C.电镀前应放入稀盐酸中浸泡除掉表面的杂质,故C正确;
D.酸式滴定管需要润洗,不润洗相当于稀释了溶液,故D错误.
故选D.点评:
本题考点: 物质的分离、提纯和除杂;化学实验方案的评价.
考点点评: 本题考查物质的分离、提纯和除杂,明确得到较大颗粒的晶体的方法是解题的关键,难度不大.1年前查看全部
- (2014•路桥区模拟)神经系统的组成及结构功能的相关表述,错误的是( )
(2014•路桥区模拟)神经系统的组成及结构功能的相关表述,错误的是( )
A.轴突末梢能分泌出神经递质依赖于膜的流动性,轴突末梢也可能含有神经递质的受体,该受体也是一种通道蛋白
B.膝跳反射需要一种最简单的反射弧--二元反射弧,即涉及两条神经
C.下丘脑的神经细胞因为兼有内分泌功能也可以包含在内分泌系统中
D.静息状态时,若神经细胞膜对Na+通透性增大,会导致静息电位的绝对值减小 jackychou12251年前1
jackychou12251年前1 -
 紫堇暮蓝 共回答了19个问题
紫堇暮蓝 共回答了19个问题 |采纳率94.7%解题思路:神经调节的基本方式是反射,其结构基础是反射弧,由感受器、传入神经、神经中枢、传出神经、效应器五部分构成.神经递质存在于突触前膜的突触小泡中,只能由突触前膜释放,然后作用于突触后膜,因此兴奋只能从一个神经元的轴突传递给另一个神经元的细胞体或树突.神经纤维未受到刺激时,K+外流,细胞膜内外的电荷分布情况是外正内负,当某一部位受刺激时,Na+内流,其膜电位变为外负内正.明确知识点,梳理相关知识,根据选项描述结合基础知识做出判断.A、轴突末梢依赖于膜的流动性,通过胞吐方式分泌出神经递质;轴突末梢没有神经递质的受体,只有树突和胞体的膜上有神经递质的受体,A错误;
B、膝跳反射需要一种最简单的反射弧--二元反射弧,即涉及两条神经:传入神经元和传出神经元,B正确;
C、下丘脑的神经细胞因为兼有内分泌功能,能分泌生长激素、促激素等,所以可包含在内分泌系统中,C正确;
D、静息状态时,若神经细胞膜对Na+通透性增大,导致Na+内流,则会导致静息电位的绝对值减小,D正确.
故选:A.点评:
本题考点: 反射弧各部分组成及功能;细胞膜内外在各种状态下的电位情况;神经冲动的产生和传导.
考点点评: 本题考查神经系统的组成及结构功能的相关知识,意在考查学生的识记能力和判断能力,运用所学知识综合分析问题和解决问题的能力.1年前查看全部
大家在问
- 1(a+b+c)(a^2+b^2+c^2)>=9abc
- 2已知函数f(x)满足f(x+y)+f(x-y)=2f(x)f(y),且f(0)不等于0.若f(2)=0,求f(4)和f(
- 3若a1,a2是正实数,则有a1平方\a2+a2平方\a1大于等于a1+a2
- 4用英语记录一两件你感动遗憾的事.同时为你将来生活做一点设计.用过去式和将来时和完成事 急
- 5Today is my birthday . Happy birthday to myself ! Thanks a l
- 6已知数据25,21,23,27,29,24,22,26,27,26,25,25,26,28,30,28,29,26,24
- 72x除以x-y等于( )除以(x-y)*(x+y)啊 请高手解答
- 8叙事诗、抒情诗、送别诗、哲理诗、咏物诗、咏史诗、山水田园诗各一首
- 9求消字 那几个英文字母 还有数字
- 10如果生物逐渐灭绝,对人类有什么后果?
- 11求《飘》(乱世佳人)中经典句子 中英文对照!
- 12物理应该怎么学啊本人是属于理科白痴型的,但偏偏又选了理科,数理化都是弱项,笔记照记,但上课除了数学课都听不下去,今年我已
- 13三个质点A、B、C的运动轨迹如图所示,三个质点同时从N点出发,分别做速度大小不变的运动,同时到达M点,下列说法中正确的是
- 14单项选择...1、__________ woman in __________ red is a famous movi
- 15新老师 请问回家作业量控制在多少呢
