(2014•番禺区一模)查处酒后驾驶采用的“便携式乙醇测量仪”以燃料电池为工作原理,在酸性环境中,理论上乙醇可以被完全氧
 哀思你2022-10-04 11:39:541条回答
哀思你2022-10-04 11:39:541条回答A.电池内部H+由正极向负极移动
B.另一极的电极反应式为:O2+4e-+2H2O=4OH-
C.乙醇在正极发生反应,电子经过外电路流向负极
D.电池总反应为:2CH3CH2OH+O2→2CH3CHO+2H2O

已提交,审核后显示!提交回复
共1条回复
 就要来了 共回答了10个问题
就要来了 共回答了10个问题 |采纳率90%- 解题思路:乙醇酸性燃料电池中,乙醇被氧化,应为电池负极,正极上氧气得电子和氢离子反应生成水,电极反应式为O2+4e-+4H+=2H2O,由CH3CH2OH-2e-→X+2H+可知,X应为CH3CHO,应为2CH3CH2OH+O2→2CH3CHO+2H2O,原电池工作时,电子由负极经外电路流向正极.
A.原电池工作时,阳离子向正极移动,故A错误;
B.电解质溶液呈酸性,正极反应式为O2+4e-+4H+=2H2O,故B错误;
C.原电池工作时,电子由负极经外电路流向正极,故C错误;
D.由CH3CH2OH-2e-→X+2H+可知,X应为CH3CHO,则电池总反应为2CH3CH2OH+O2→2CH3CHO+2H2O,故D正确.
故选D.点评:
本题考点: 化学电源新型电池.
考点点评: 本题以化学电源新型电池为载体考查了原电池原理,难度不大,易错选项是B,写电极反应式时要注意结合溶液的酸碱性;在酸性溶液,生成物中不能有氢氧根离子生成;在碱性溶液中,生成物中不能有氢离子生成. - 1年前
相关推荐
- (2014•番禺区一模)小楠同学用如图所示的电路“研究导体中的电流跟导体电阻”的关系,他先后将5Ω、15Ω和25Ω的定值
 (2014•番禺区一模)小楠同学用如图所示的电路“研究导体中的电流跟导体电阻”的关系,他先后将5Ω、15Ω和25Ω的定值电阻接入电路A、B两点间,闭合开关S,读出电流表示数(如表).由实验数据可以看出电流I与电阻R并不成反比.你认为实验中出现这样结果的主要原因是什么?如何改进?
(2014•番禺区一模)小楠同学用如图所示的电路“研究导体中的电流跟导体电阻”的关系,他先后将5Ω、15Ω和25Ω的定值电阻接入电路A、B两点间,闭合开关S,读出电流表示数(如表).由实验数据可以看出电流I与电阻R并不成反比.你认为实验中出现这样结果的主要原因是什么?如何改进?
电阻R/Ω 5 15 25 电流I/A 0.6 0.3 0.2  itokumo1年前1
itokumo1年前1 -
 尘彦 共回答了13个问题
尘彦 共回答了13个问题 |采纳率100%解题思路:探究电流跟电阻的关系时,采用控制变量法,改变定值电阻的大小,通过移动滑动变阻器的滑片,保持电压一定,记录电流大小,从而研究电流跟电阻的关系.“研究导体中的电流跟导体电阻”的实验应采取控制变量法,控制电阻R两端的电压不变,然后改变R的阻值,以5Ω、15Ω和25Ω的定值电阻接入电路读出电流表的示数;因电阻R与滑动变阻器串联,电阻R的改变,使电路A、B两点间的电压发生改变,不能满足电阻R两端的电压保持不变的条件,所以实验数据中电流I与电阻R不成反比;因此为了保持电阻R两端的电压不变;在电阻R两端并接上一个电压表,调节滑动变阻器,使电压表的示数保持不变.
答:原因是:未能保持电阻R两端的电压不变;
改进方法:在电阻R两端并接上一个电压表,调节滑动变阻器,使电压表的示数保持不变.点评:
本题考点: 探究电流与电压、电阻的关系实验.
考点点评: 探究电流与电阻关系时,要应用控制变量法,控制电阻两端电压保持不变.1年前查看全部
- (2014•番禺区一模)厕所清洁剂中含有盐酸.如果不慎洒到大理石地面上,会发出嘶嘶声并有气体产生.这种气体是( )
(2014•番禺区一模)厕所清洁剂中含有盐酸.如果不慎洒到大理石地面上,会发出嘶嘶声并有气体产生.这种气体是( )
A.CO2
B.CO
C.H2
D.02 hbtlan1年前1
hbtlan1年前1 -
 stevevnpeng444 共回答了15个问题
stevevnpeng444 共回答了15个问题 |采纳率93.3%解题思路:大理石的主要成分是碳酸钙,碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳.稀盐酸和大理石中的碳酸钙反应生成的气体是二氧化碳.
故选:A.点评:
本题考点: 酸的化学性质.
考点点评: 厕所清洁剂中含有盐酸,应该尽量避免滴在金属器皿、大理石板上,以防腐蚀这些物品.1年前查看全部
- (2014•番禺区一模)打开收音机的开关,将旋钮调到没有电台的位置,并将音量开大.取一节干电池和一根导线,靠近收音机将导
(2014•番禺区一模)打开收音机的开关,将旋钮调到没有电台的位置,并将音量开大.取一节干电池和一根导线,靠近收音机将导线的一端与电池的一极相连,再用导线的另一端与电池的另一极时断时续的接触,会听到收音机发出“咔咔”声,这一现象说明周围的空间存在( )
A.超声波
B.电磁波
C.X光线
D.紫外线 我是拉拉鼓1年前1
我是拉拉鼓1年前1 -
 goatboy 共回答了20个问题
goatboy 共回答了20个问题 |采纳率90%解题思路:要解答本题需掌握:变化的电流周围存在着电磁波,以及收音机能接收电磁波.导线的一端与电池的一极相连,再用导线的另一端与电池的另一极时断时续的接触,这时导线中就有变化的电流,故周围就会产生电磁波,产生的电磁波被收音机接收,故能听到“咔咔”的声音.
故选B.点评:
本题考点: 电磁波的产生.
考点点评: 本题主要考查学生对电磁波的产生的了解和掌握,是一道基础题.1年前查看全部
- (2008•番禺区一模)△PAB和△PMN是顶角相等的两个等腰三角形,PA=PB,PM=PN,PM≠PB.
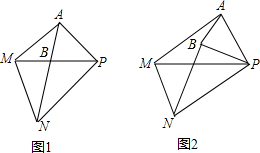 (2008•番禺区一模)△PAB和△PMN是顶角相等的两个等腰三角形,PA=PB,PM=PN,PM≠PB.
(2008•番禺区一模)△PAB和△PMN是顶角相等的两个等腰三角形,PA=PB,PM=PN,PM≠PB.
(1)如图1,若P、B、M共线,判断AM=BN是否成立,并说明理由;
(2)将△PAB绕点P旋转角度α后(如图2),(1)中结论仍然成立吗?为什么?
(3)试用直尺和圆规在图2中作∠PAM和∠PBN的角平分线(不写作法,保留作图痕迹),分别交PM、PN于点C、D,连接CN、MD,试判断在旋转过程中线段CN和MD有怎样的大小关系,并对你的结论给予证明. 视点壹仟1年前1
视点壹仟1年前1 -
 bnbyoung 共回答了20个问题
bnbyoung 共回答了20个问题 |采纳率85%解题思路:(1)证△PAM≌△PBN即可;
(2)①当a=180°-∠APB时,求出即可;②当a=180°-∠APB时,根据SAS证△PAM≌△PBN即可;
(3)①当α=180°-∠APB时,此时∠PAM和∠PBN的交平分线不存在,②当α≠180°-∠APB时,证△CPA≌△DPB,推出CP=DP,根据SAS证△MDP≌△NCP即可.(1)AM=BN成立.
理由:在△PAM和△PBN中,由已知有
PA=PB,∠MPA=∠NPB,PM=PN,
∴△PAM≌△PBN(SAS),
∴AM=BN.
(2)将△PAB绕点P旋转角度a后,AM=BN也能成立.
理由:①当a=180°-∠APB时,
恰好M、P、A共线,N、P、B也共线,有
AM=AP+PM=BP+PN=BN成立.
②当a=180°-∠APB时,
在△PAM和△PBN中,由题设有
PA=PB,PM=PN,
∵∠APB=∠MPN,
∴∠APB+α=∠MPN+α,
∴∠MPA=∠BPN,
∴△PAM≌△PBN(SAS),
∴AM=BN.
(3)在旋转过程中线段CN和MD的大小关系是CN=MD.
证明:①当α=180°-∠APB时,M、P、A共线,N、P、B共线,
此时∠PAM和∠PBN的交平分线不存在.
②当α≠180°-∠APB时,CN=MD,
证明:由(2)知△PAM≌△PBN,
∴∠MAP=∠NBP,
∵AC、BD分别是∠PAM何∠PBN的角平分线,
∴∠CAP=∠DBP,
∵PA=PB,
∴∠CPA=∠DPB,
∴△CPA≌△DPB,
∴CP=DP,
在△MDP和△NCP中,CP=DP,∠DPM=∠CPN,MP=NP,
∴△MDP≌△NCP,
∴CN=MD.点评:
本题考点: 全等三角形的判定与性质;等腰三角形的性质;旋转的性质.
考点点评: 本题主要考查对全等三角形的性质和判定,等腰三角形的性质,旋转的性质等知识点的理解和掌握,能综合运用性质进行推理是解此题的关键.1年前查看全部
- (2006•番禺区二模)在铝箔燃烧实验中,最能说明该变化是化学变化的现象是( )
(2006•番禺区二模)在铝箔燃烧实验中,最能说明该变化是化学变化的现象是( )
A.铝箔变小
B.放出大量的热
C.发出耀眼的强光
D.生成白色固体 曹31年前1
曹31年前1 -
 wwsstl 共回答了23个问题
wwsstl 共回答了23个问题 |采纳率95.7%解题思路:利用化学变化的本质特征是有新物质生成的知识,并结合新物质产生的明显特征解决.A、B、C、D四个选项中只有生成白色固体说明生成了不同于银白色铝箔的新固体,也就是生成了不同于铝的新的物质,符合化学变化的本质特征.
故选D点评:
本题考点: 化学变化的基本特征.
考点点评: 此题是对化学变化特征的考查,只要有新物质生成的变化就是化学变化1年前查看全部
- (2012•番禺区一模)一元二次方程x(x-2)=0根的情况是( )
(2012•番禺区一模)一元二次方程x(x-2)=0根的情况是( )
A.没有实数根
B.只有一个实数根
C.有两个相等的实数根
D.有两个不相等的实数根 初_夏1年前1
初_夏1年前1 -
 可泡 共回答了22个问题
可泡 共回答了22个问题 |采纳率95.5%解题思路:先把原方程变形为:x2-2x=0,然后计算△,得到△=4>0,根据△的含义即可判断方程根的情况.原方程变形为:x2-2x=0,
∵△=(-2)2-4×1×0=4>0,
∴原方程有两个不相等的实数根.
故选:D.点评:
本题考点: 解一元二次方程-因式分解法.
考点点评: 本题考查了一元二次方程ax2+bx+c=0,(a≠0)根的判别式△=b2-4ac:当△>0,原方程有两个不相等的实数根;当△=0,原方程有两个相等的实数根;当△<0,原方程没有实数根.1年前查看全部
- (2006•番禺区二模)在复合化肥硝酸钾中含有少量氯化钠.某课外活动小组拟测定此化肥中硝酸钾的含量,按下列步骤进行实验:
(2006•番禺区二模)在复合化肥硝酸钾中含有少量氯化钠.某课外活动小组拟测定此化肥中硝酸钾的含量,按下列步骤进行实验:
①称取该化肥样品10.0g;
②将样品加水溶解制成溶液;
③加入过量的硝酸银试剂,过滤;
④用蒸馏水反复洗涤沉淀多次;
⑤将沉淀小心干燥,称量,测得固体质量为2.87g;
⑥数据处理,经计算,确定化肥中硝酸钾的质量分数.
请根据上述实验步骤回答下列问题:
(1)步骤③中过滤操作所需要的仪器中除烧杯、铁架台(带铁圈)、玻璃棒外,还需要的仪器是______.
(2)步骤②和步骤③都使用到玻璃棒,但它的目的不同,在步骤②的目的是______,在步骤③的目的是______.
(3)步骤③中加入硝酸银试剂发生反应的化学方程式______.
(4)步骤③加入过量硝酸银试剂的目的是______.
(5)请计算化肥中硝酸钾的质量分数为______. fulongdanruo1年前1
fulongdanruo1年前1 -
 就是普通人 共回答了35个问题
就是普通人 共回答了35个问题 |采纳率94.3%解题思路:(1)沉淀和溶液分离的方法是过滤,过滤用到的玻璃仪器为:玻璃棒、漏斗和滤纸、烧杯;
(2)根据玻璃棒在溶解、过滤中的作用解答
(3)硝酸银与溶液中的氯化钠反应生成氯化银和硝酸钠;
(4)根据溶液中生成物和没反应的物质考虑;
(5)找出已知量,利用化学方程式计算即可.(1)把不溶于液体的固体与液体分离的方法是过滤;过滤用到的玻璃仪器为:玻璃棒、漏斗和滤纸、烧杯.故答案为:漏斗和滤纸
(2)玻璃棒在溶解中的作用是加快溶解速度,在过滤中的作用是引流.
(3)硝酸银与溶液中的氯化钠反应生成氯化银和硝酸钠,方程式为AgNO3+NaCl=AgCl↓+NaNO3
(3)硝酸银与氯化钠反应能生成氯化银沉淀和硝酸钠,所以滤液中含有Na+和NO3-,硝酸钾没参加反应,所以还含有K+,又因为加入的硝酸银过量,所以还含有Ag+.故答案为:Ag+、Na+、K+、NO3-
(4)步骤③加入硝酸银试剂的目的是与氯化钠反应生成沉淀,因此加入过量的目的是使氯离子完全转化成沉淀.
(5)由题意知,生成的氯化银质量为2.87g,设氯化钠的质量为X
AgNO3+NaCl=AgCl↓+NaNO3
58.5 143.5
X 2.87g
[58.5/x]=[143.5/2.87g]
x=1.17g
硝酸钾的质量为10g-1.17g=8.83g
硝酸钾的质量分数为[8.83g/10g]×100%=88.3%
故答案为:(1)漏斗和滤纸 (2)搅拌加快溶解 引流过滤液
(3)AgNO3+NaCl=AgCl↓+NaNO3 (4)为了让Cl- 沉淀完全 (5)88.3%点评:
本题考点: 盐的化学性质;过滤的原理、方法及其应用;书写化学方程式、文字表达式、电离方程式;根据化学反应方程式的计算.
考点点评: 本题主要考查了除杂质的问题,并根据加入的试剂对反应物的成分进行探究,以及对利用化学方程式进行计算作了考查;解答此类题目一定要认真分析,不能有一丝的马虎.1年前查看全部
- (2014•番禺区一模)小罗用一个凸透镜及相关器材,探究凸透镜的成像规律.
(2014•番禺区一模)小罗用一个凸透镜及相关器材,探究凸透镜的成像规律.
(1)在图甲画出入射光线经凸透镜后的折射光线.
(2)如图乙,用图甲中的凸透镜进行实验,在光屏上恰好得到一个清晰的蜡烛的像,请你详尽地描述这个像的特点:______.______(选填“照相机”、“投影仪”或“放大镜”)就是利用该成像规律工作的.
(3)小罗把自己的近视眼镜放在凸透镜与蜡烛之间,发现光屏上的像变得模糊不清.他应当将光屏______(选填“靠近”或“远离”)凸透镜,可再次得到清晰的像. SuperXia1年前1
SuperXia1年前1 -
 kkuopl 共回答了18个问题
kkuopl 共回答了18个问题 |采纳率100%解题思路:(1)由图示可知,入射光线过焦点,根据入射光线的特点,可以画出对应的折射光线.
(2)投影仪是根据当物距处于焦距和2倍焦距之间时,凸透镜成倒立放大实像的原理制成.
(3)近视眼镜是凹透镜,凹透镜对光线有发散作用.发散的含义是使会聚的光线变为平行光,或会聚的光线推迟会聚.(1)入射光线过焦点,经过凸透镜折射后,则折射光线将平行主光轴射出.故画图如下:
(2)当物距为12cm时,此时2f>u>f,移动光屏可以在光屏上得到一个倒立、放大的实像,投影仪是根据这个原理制成的;
(3)近视眼镜是凹透镜,凹透镜放在凸透镜与烛焰之间,凹透镜对光线有发散作用,会使原来会聚的像推迟会聚成像,所以他应当将光屏远离凸透镜,可再次得到清晰的像.
故答案为:(1)
(2)倒立放大实像;投影仪;
(3)远离.点评:
本题考点: 凸透镜成像规律及其探究实验.
考点点评: 本题考查了凸透镜的特殊光线,凹透镜的对光线的作用,凸透镜成像情况和应用,本题综合性比较强,有一定的难度.1年前查看全部
- (2011•番禺区一模)如图所示是探究凸透镜成像的实验装置示意图.已知凸透镜的焦距是20cm,光具座上A、B、C三点分别
 (2011•番禺区一模)如图所示是探究凸透镜成像的实验装置示意图.已知凸透镜的焦距是20cm,光具座上A、B、C三点分别用于放置器材,其中B点应该放______(填“凸透镜”、“光屏”或“蜡烛”).若此时光屏上刚好得到清晰的缩小的像,则蜡烛是放在______点,BC的距离要______ (“大于”、“等于”或“小于”)40cm.此时只需移动______点上放置的器材,光屏上又会得到清晰的放大的像.
(2011•番禺区一模)如图所示是探究凸透镜成像的实验装置示意图.已知凸透镜的焦距是20cm,光具座上A、B、C三点分别用于放置器材,其中B点应该放______(填“凸透镜”、“光屏”或“蜡烛”).若此时光屏上刚好得到清晰的缩小的像,则蜡烛是放在______点,BC的距离要______ (“大于”、“等于”或“小于”)40cm.此时只需移动______点上放置的器材,光屏上又会得到清晰的放大的像.  冉雪峰1年前1
冉雪峰1年前1 -
 范冰冰的苹果 共回答了26个问题
范冰冰的苹果 共回答了26个问题 |采纳率88.5%当凸透镜成实像时,像与物分居凸透镜的两侧,所以凸透镜在中间,故B点放置凸透镜.
当成倒立缩小的实像时,物距大于二倍焦距,像距小于二倍焦距大于一倍焦距,由此可知,此时的物距大于像距,所以蜡烛放在离凸透镜较远的C点.
由于凸透镜的焦距为20cm,物距大于二倍焦距,所以BC间的距离要大于40cm.
根据凸透镜成像的情况可知,当物距改变时,像距也要改变,而此时要求只移动一个 器材成像,也就是说只移动一个器材同时改变物距和像距,所以只能移动B点的凸透镜.
故 答案为:凸透镜;C;大于;B.1年前查看全部
- (2014•番禺区一模)下列物质在空气中燃烧的现象叙述错误的是( )
(2014•番禺区一模)下列物质在空气中燃烧的现象叙述错误的是( )
A.木炭:发出红光
B.硫磺:蓝紫色火焰
C.红磷:大量白烟
D.铁丝:红热不燃烧 二贝儿颅1年前1
二贝儿颅1年前1 -
 竹性清凉 共回答了23个问题
竹性清凉 共回答了23个问题 |采纳率91.3%解题思路:A、根据木炭在空气中燃烧的现象进行分析判断.
B、根据硫磺在空气中燃烧的现象进行分析判断.
C、根据红磷在空气中燃烧的现象进行分析判断.
D、根据铁丝在空气中燃烧的现象进行分析判断.A、木炭在空气中燃烧,只能烧至发红,不会产生红光,故选项说法错误.
B、硫磺在空气中燃烧,产生淡蓝色火焰,故选项说法错误.
C、红磷在空气中燃烧,产生大量的白烟,故选项说法正确.
D、铁丝在空气中只能烧至发红,不会产生火星,故选项说法正确.
故选:AB.点评:
本题考点: 氧气与碳、磷、硫、铁等物质的反应现象.
考点点评: 本题难度不大,掌握常见物质燃烧的现象即可正确解答;在描述物质燃烧的现象时,需要注意光和火焰、烟和雾的区别.1年前查看全部
- (2013•番禺区一模)三瓶没有标签的白色粉末是Ba(NO3)2、MgCl2和CaO.请设计一个实验方案进行鉴别,并贴上
(2013•番禺区一模)三瓶没有标签的白色粉末是Ba(NO3)2、MgCl2和CaO.请设计一个实验方案进行鉴别,并贴上标签.叙述实验操作、预期现象和结论.
提供的试剂有:蒸馏水提供的仪器有:试管,胶头滴管
实验操作 预期现象与结论  36634991年前1
36634991年前1 -
 qingdaomuye 共回答了20个问题
qingdaomuye 共回答了20个问题 |采纳率85%解题思路:CaO溶于水放出热量,MgCl2溶液能和Ca(OH)2溶液反应产生沉淀,Ba(NO3)2和Ca(OH)2溶液不反应.根据三种物质不同的性质,可以先溶于水,与水反应并放出热量的白色粉末是CaO,然后取少量Ca(OH)2溶液分别滴入另外两种溶液中,能产生沉淀的溶液是MgCl2,无现象的是
Ba(NO3)2.
故答案是:故答案为:
分别取少量三种待鉴别的固体于三支试管中,加入足量水溶解 反应剧烈且伴有大量热量放出的原白色粉末是CaO,固体溶解的原固体是Na2CO3 和KCl
使用胶头滴管取少量Ca(OH)2溶液分别滴入另外两个试管中 有沉淀生成的试管里原固体是MgCl2,无明显现象的试管里原固体是Ba(NO3)2点评:
本题考点: 酸、碱、盐的鉴别.
考点点评: 同时对多种物质进行鉴别时,采取根据物质的性质的异同对物质进行分类的方法,可使复杂的鉴别变得有条理.1年前查看全部
- (2014•番禺区一模)在水溶液中能大量共存的一组是( )
(2014•番禺区一模)在水溶液中能大量共存的一组是( )
A.Ba2+、Na+、SO32-、Cl-
B.MnO4-、SO42-、K+、H+
C.Al3+、Mg2+、NO3-、HCO3-
D.Fe3+、Na+、SCN-、Cl- 来自yy的狼1年前1
来自yy的狼1年前1 -
 netbarman 共回答了21个问题
netbarman 共回答了21个问题 |采纳率95.2%解题思路:如离子之间不发生复分解反应生成沉淀、气体、水或不发生氧化还原反应、互促水解等反应,则可大量共存,以此解答.解;A.Ba2+与SO32-反应生成沉淀而不能大量共存,故A错误;
B.离子之间不发生任何反应,可大量共存,故B正确;
C.Al3+与HCO3-发生互促水解反应而不能大量共存,故C错误;
D.Fe3+与SCN-发生络合反应而不能的共存,故D错误.
故选B.点评:
本题考点: 离子共存问题.
考点点评: 本题考查离子共存问题,为高考常见题型和高频考点,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意相关离子的性质以及反应类型的判断,易错点为D,注意发生络合反应的特点,难度不大.1年前查看全部
- (2008•番禺区一模)炎热的夏天,小明到餐厅就餐,要了一杯加冰的可乐,看到冰块浮在液面上,纸杯外壁出现了一层水珠、小明
(2008•番禺区一模)炎热的夏天,小明到餐厅就餐,要了一杯加冰的可乐,看到冰块浮在液面上,纸杯外壁出现了一层水珠、小明在用吸管喝可乐时,想到以下问题,请你帮他回答:
(1)纸杯的外壁上为什么会出现一层水珠?
(2)为什么能够用吸管喝饮料? likaikai1年前1
likaikai1年前1 -
 tears2004 共回答了12个问题
tears2004 共回答了12个问题 |采纳率83.3%解题思路:(1)纸杯外壁上的小水珠是空气中的水蒸气变成的,是液化现象;
(2)这是大气压作用的结果,不是人吸上来的.答:(1)因为杯子的外壁温度较低,杯子附近的水蒸气遇冷液化成小水珠附在杯子的外壁上.
(2)用吸管喝饮料时,先吸出管里的空气,管里的气压降低,在外界大气压的作用下,把饮料压进吸管并进入嘴里.点评:
本题考点: 液化及液化现象;大气压强的存在.
考点点评: 本题考查生活中的液化现象和生活中的大气压现象,由于与生活联系紧密,是中考的热点.1年前查看全部
- (2009•番禺区一模)在Rt△ABC中,∠C=90°,∠A=60°,AC=4cm,长为1cm的线段MN在△ABC的边A
 (2009•番禺区一模)在Rt△ABC中,∠C=90°,∠A=60°,AC=4cm,长为1cm的线段MN在△ABC的边AB上沿AB方向以1(cm/s)的速度向点B运动(运动开始时点M与点A重合),过M、N分别作AB的垂线交直角边于P、Q两点(如图),设线段MN运动的时间为t(s)时,△BNQ的面积为ycm2.
(2009•番禺区一模)在Rt△ABC中,∠C=90°,∠A=60°,AC=4cm,长为1cm的线段MN在△ABC的边AB上沿AB方向以1(cm/s)的速度向点B运动(运动开始时点M与点A重合),过M、N分别作AB的垂线交直角边于P、Q两点(如图),设线段MN运动的时间为t(s)时,△BNQ的面积为ycm2.
(1)求出y与t的函数关系式,并写出自变量t的取值范围;
(2)当MN运动几秒钟后,y最大,最大值为多少?
(3)线段MN运动过程中,四边形MNQP有可能成为矩形吗?若有可能,求出此时t的值;若不可能,说明理由. notaled1年前0
notaled1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2006•番禺区二模)向烧杯里加入10mL质量分数为4%的氢氧化钠溶液后测定溶液的pH值.然后用滴管慢慢滴入质量分数为
 (2006•番禺区二模)向烧杯里加入10mL质量分数为4%的氢氧化钠溶液后测定溶液的pH值.然后用滴管慢慢滴入质量分数为4%的盐酸溶液,搅拌,充分反应.
(2006•番禺区二模)向烧杯里加入10mL质量分数为4%的氢氧化钠溶液后测定溶液的pH值.然后用滴管慢慢滴入质量分数为4%的盐酸溶液,搅拌,充分反应.
请填表回答溶液中溶质的组成可能有几种(可以不填满)
溶液中的溶质 验证的实验方法 观察到的实验现象  发酒疯的笨笨1年前1
发酒疯的笨笨1年前1 -
 醉也dd 共回答了19个问题
醉也dd 共回答了19个问题 |采纳率94.7%解题思路:向氢氧化钠溶液中逐滴加入盐酸,氢氧化钠和盐酸发生中和反应生成氯化钠和水,根据反应物的量的改变,溶液中的溶质也会逐渐发生变化,可用pH试纸测定溶液的pH来确定溶液中的溶质.根据NaOH+HCl═NaCl+H2O可知,开始滴入盐酸时,氢氧化钠过量,溶液中的溶质是氢氧化钠和氯化钠;当酸碱恰好完全中和时,溶液中的溶质是氯化钠,溶液呈中性;继续滴加盐酸,盐酸会过量,溶液呈酸性.
故答案为:
溶液中的溶质 验证的实验方法 观察到的实验现象
NaOHNaCl 用pH试纸测定 测定的溶液pH值比原来的小,但溶液的pH值大于7
NaCl 用pH试纸测定 测定的溶液pH值为7
NaCl HCl 用pH试纸测定 测定的溶液pH值小于7
溶液中的溶质 验证的实验方法 观察到的实验现象
点评:
本题考点: 中和反应及其应用;溶液的酸碱度测定.
考点点评: 了解酸碱中和的实质和溶液pH的变化是解题的关键,此题难度中等.1年前查看全部
- (2014•番禺区一模)A、B两种装置如图所示,根据实验室里制取气体的原理回答下列问题(所选装置图用其代号字母表示).
 (2014•番禺区一模)A、B两种装置如图所示,根据实验室里制取气体的原理回答下列问题(所选装置图用其代号字母表示).
(2014•番禺区一模)A、B两种装置如图所示,根据实验室里制取气体的原理回答下列问题(所选装置图用其代号字母表示).
(1)用过氧化氢和二氧化锰制取氧气可采用的装置是______,反应的化学方程式为2H2O2
2H2O+O2↑MnO2 .2H2O2,其中二氧化锰起______作用;
2H2O+O2↑MnO2 .
(2)用高锰酸钾制取氧气可采用的装置是______,制取氧气的反应化学方程式为2KMnO4
K2MnO4+MnO2+O2↑△ .2KMnO4.
K2MnO4+MnO2+O2↑△ .
(3)实验室制取二氧化碳时,选用的发生装置是______. 星空小狮王1年前1
星空小狮王1年前1 -
 nidexiaogou 共回答了24个问题
nidexiaogou 共回答了24个问题 |采纳率91.7%解题思路:(1)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳.(1)用过氧化氢和二氧化锰制取氧气时不需要加热,应该用A装置作为发生装置;
反应的化学方程式为:2H2O2
MnO2
.
2H2O+O2↑,其中二氧化锰起催化作用.
故填:A;2H2O2
MnO2
.
2H2O+O2↑;催化.
(2)用高锰酸钾制取氧气需要加热,应该用B装置作为发生装置,反应的化学方程式为:2KMnO4
△
.
K2MnO4+MnO2+O2↑.
故填:B;2KMnO4
△
.
K2MnO4+MnO2+O2↑.
(3)碳酸钙和稀盐酸反应不需要加热,应该用A装置作为发生装置.
故填:A.点评:
本题考点: 氧气的制取装置;氧气的收集方法;二氧化碳的实验室制法;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查化学方程式的书写和实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.1年前查看全部
- (2014•番禺区一模)下列实验方案中,设计合理的是( )
(2014•番禺区一模)下列实验方案中,设计合理的是( )
A.用酒精浸泡捣烂的某些植物的花瓣可制酸碱指示剂
B.用燃烧木炭的方法制备纯净的二氧化碳气体
C.用氢氧化钠除去铁钉表面的铁锈
D.点燃的木条可区分N2和CO2 online蛋蛋1年前1
online蛋蛋1年前1 -
 冷水泡方便面 共回答了19个问题
冷水泡方便面 共回答了19个问题 |采纳率94.7%解题思路:A、根据某些植物的花瓣中含有能够遇酸碱会变色的物质,进行分析判断.
B、实验室制备二氧化碳气体,操作要简单,制取气体要纯,据此进行分析判断.
C、根据铁锈的主要成分是氧化铁,不能与氢氧化钠溶液反应,进行分析判断.
D、根据N2和CO2均不能支持燃烧进行分析判断.A、用酒精浸泡捣烂的某些植物的花瓣的浸出液中可能含有能够遇酸碱会变色的物质,可作酸碱指示剂,可用于试验食醋的酸性,故该实验方案设计合理.
B、燃烧木炭的方法不容易操作和收集气体,并能产生一氧化碳,制得的气体不纯净,故该实验方案设计不合理.
C、铁锈的主要成分是氧化铁,不能与氢氧化钠溶液反应,不能用氢氧化钠除去铁钉表面的铁锈,故该实验方案设计不合理.
D、N2和CO2均不能支持燃烧,不能用点燃的木条区分N2和CO2,故该实验方案设计不合理.
故选:A.点评:
本题考点: 化学实验方案设计与评价;常见气体的检验与除杂方法;酸碱指示剂及其性质;碱的化学性质;碳的化学性质.
考点点评: 本题难度不大,但综合性较强,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.1年前查看全部
- (2014•番禺区一模)PX别称对二甲苯(C8H10),是重要的化工原料.我们的衣服、矿泉水瓶等日常消费品的生产都离不开
(2014•番禺区一模)PX别称对二甲苯(C8H10),是重要的化工原料.我们的衣服、矿泉水瓶等日常消费品的生产都离不开PX.下列有关PX的说法正确的是( )
A.PX是高分子化合物
B.PX中的碳元素、氢元素元素质量比为49:5
C.PX的相对分子质量为108
D.PX中碳元素的质量分数90.6% lidsenta1年前1
lidsenta1年前1 -
 cclany 共回答了14个问题
cclany 共回答了14个问题 |采纳率100%解题思路:A、高分子化合物的相对分子质量在几万、几十万甚至几百万考虑;B、根据元素质量=元素的相对原子质量×原子个数;C、根据相对分子质量的计算方法考虑;D、根据碳元素的质量分数计算方法考虑.A、高分子化合物的相对分子质量在几万、几十万甚至几百万,PX的相对分子质量为106,不属于高分子化合物,故A错;
B、碳、氢元素的质量比为(12×8):(1×10)=48:5,故B错;
C、对二甲苯的相对分子质量=12×8+1×10=106,故C错;
D、PX中碳元素的质量分数:[12×8/106]×100%=90.6%,故D正确.
故选D.点评:
本题考点: 有机物的特征、分类及聚合物的特性;相对分子质量的概念及其计算;元素质量比的计算;元素的质量分数计算.
考点点评: 本题考查化学式的意义及计算,物质中组成元素的质量比为各元素的相对原子质量与原子个数乘积的比.1年前查看全部
- (2012•番禺区一模)下表是KNO3和NaCl在一定温度(t℃)的溶解度(g).回答下列问题
(2012•番禺区一模)下表是KNO3和NaCl在一定温度(t℃)的溶解度(g).回答下列问题
(1)根据上表数据绘制KNO3和NaCl的溶解度曲线.
温度(℃)
溶解度(g)0 10 20 30 40 50 60 70 80 NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3 37.8 38.4 KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 138 169 
(2)在______℃KNO3和NaCl两种物质的溶解度相等.
(3)95℃时,在248g溶液中含有110g的KNO3和38g的NaCl,溶液中水的质量为______g.
将95℃的溶液降温到70℃,过滤.保持过滤液温度仍为70℃,过滤液中的阳离子是______.过滤出的固体是______,质量约为______g.
(4)将上述70℃的过滤液再冷却到20℃,过滤.保持过滤液温度为20℃,则过滤液中的溶质是______.过滤出的固体是______,质量约为______ g. overlong1年前1
overlong1年前1 -
 lanceman 共回答了17个问题
lanceman 共回答了17个问题 |采纳率88.2%解题思路:(1)根据图表提供的不同温度下物质的溶解度绘制硝酸钾和氯化钠的溶解度曲线;
(2)根据溶解度曲线图:两种物质溶解度曲线的交点表示该温度下两物质的溶解度相同;
(3)根据溶液的质量=溶质的质量+溶剂的质量分析解答;并根据氯化钠和硝酸钾在70℃时的溶解度分析解答;
(4)根据20℃时硝酸钾、氯化钠的溶解度判断滤液中的溶质和析出晶体的质量.(1)氯化钠和硝酸钾的溶解度曲线为:

(2)由溶解度曲线可知:约在23℃时两物质的溶解度相交于一点,溶解度相同;
故答案为:23℃;
(3)在248g溶液中含有110g的KNO3和38g的NaCl,溶液中水的质量为248g-110g-38g=100g;
在70℃时氯化钠的溶解度是37.8g,硝酸钾的溶解度是138g,所以当降到70℃时有氯化钠析出,质量为38g-37.8g-0.2g,此时形成的是硝酸钾的不饱和溶液,氯化钠的饱和溶液;
故答案为:100;K+、Na+; NaCl;0.2;
(4)将上述70℃的过滤液再冷却到20℃,过滤.保持过滤液温度为20℃,20℃时氯化钠的溶解度是36g,硝酸钾的溶解度是31.6g;则过滤液中的溶质是硝酸钾和氯化钠,析出氯化钠的质量是37.8g-36.0g=1.8g,析出的硝酸钾的质量为:110g-31.6g=79.4g,则过滤出的固体的质量是:1.8g+79.4g=80.2g;
故答案为:NaCl、KNO3; NaCl、KNO3;80.2.点评:
本题考点: 固体溶解度曲线及其作用.
考点点评: 本题重点考查了溶解度曲线的绘制和对溶解度曲线的应用,能很好的培养学生分析和解决问题的能力.1年前查看全部
- (2010•番禺区一模)画出光源A点在水中的像,并在图中完成反射、折射光路图.
 ↖╳↘1年前0
↖╳↘1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2011•番禺区一模)如图,将一个边长为1的正方形纸片ABCD折叠,使点B落在边AD上(不与A、D重合),MN为折痕,
(2011•番禺区一模)如图,将一个边长为1的正方形纸片ABCD折叠,使点B落在边AD上(不与A、D重合),MN为折痕,折叠后B′C′与DN交于P.

(1)P判断△MAB′与△NC′P是否相似?并说明理由;
(2)当B落在什么位置上时,折叠起来的梯形MNC′B′面积最小,并求此时两纸片重叠部分的面积. guojianhui1年前1
guojianhui1年前1 -
 luzuokun 共回答了21个问题
luzuokun 共回答了21个问题 |采纳率81%解题思路:(1)求两三角形相似,只需证明其中的两个对应角相等即可;
(2)先求出梯形MNC′B′面积最小时,点B的位置,两纸片重叠部分的面积即是梯形MNC′B′的面积减去三角形NPC'的面积.(1)△MAB′与△NC′P相似,
其理由如下:∵∠NC′P=∠B′AM=90°,
又∵∠B′PD+∠PB′D=90°,∠DB′P+∠MB′A=90°,
∴∠MB′A=∠B′PD,
又由∠NPC′=∠B′PD,
∴∠MB′A=∠NPC′,
∴△MAB′∽△NC′P.
(2)如图,过N作NR⊥AB与R,
则RN=BC=1,
连BB′,交MN于Q.则由折叠知,
△MBQ与△MB′Q关于直线MN对称,即△MBQ≌△MB′Q,
有BQ=B′Q,MB=MB′,MQ⊥BB′.
∵∠A=∠MQB,
∴△MQB∽△B′AB,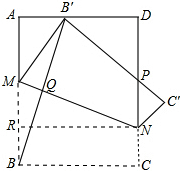
∴[AB′/MQ]=[AB/BQ]=[BB′/MB].
设AB′=x,则BB′2=1+x2,BQ=
1
2
1+x2,代入上式得:
BM=B'M=[1/2(1+x2).
在Rt△MRN和Rt△B′AB中,
∠MNR+∠BMQ=90°,∠ABB′+∠BMQ=90°,
∴∠MNR=∠ABB′,
∵AB=BC,BC=RN,
∴AB=RN,
∴Rt△MRN≌Rt△B′AB,
∴MR=AB′=x.
故C'N=CN=BR=MB-MR=
1
2(1+x2)-x=
1
2](x-1)2.
∴S梯形MNC′B′=[1/2][[1/2](x-1)2+[1/2](x2+1)]×1=[1/2](x2-x+1)=[1/2](x-[1/2])2+[3/8],
得当x=[1/2]时,即B落在AD的中点处时,梯形面积最小,其最小值[3/8].
此时,C′N=[1/8],BM=[5/8],AM=[3/8],
由(1)得
S△NPC′
S△MB′A=(
NC′
AM点评:
本题考点: 相似三角形的判定与性质;二次函数的最值;全等三角形的判定与性质;翻折变换(折叠问题).
考点点评: 本题考查了相似三角形的判定、二次函数的最值、全等三角形的判定和性质及翻转变换,是一道综合题,有一定的难度,这要求学生要熟练掌握各部分知识,才能顺利解答这类题目.1年前查看全部
- (2014•番禺区一模)生石灰是白色的块状物,应用非常广泛.
(2014•番禺区一模)生石灰是白色的块状物,应用非常广泛.
(1)生石灰的主要成分为(填化学式)______;
(2)在食品包装中,常用生石灰作干燥剂,其干燥原理是(用化学方程式表示)______;
(3)在农村,生石灰也常用于畜禽栏舍的消毒.畜禽出栏后,将生石灰用水调成20%的石灰乳,涂刷墙面和地面.某农户误将生石灰直接撒在猪圈中消毒,一段时间后发现猪的蹄部干燥开裂,有的甚至出现灼伤、溃疡,原因是______. wuxianzhi1081年前1
wuxianzhi1081年前1 -
 catherineyao 共回答了12个问题
catherineyao 共回答了12个问题 |采纳率91.7%解题思路:根据物质的性质进行分析,氧化钙能与水反应生成氢氧化钙,同时放出大量的热,可以用作干燥剂,生成的氢氧化钙能与空气中的二氧化碳反应生成坚硬的碳酸钙.(1)生石灰的主要成分是氧化钙,其化学式为CaO;
(2)氧化钙与水反应生成氢氧化钙,可以用作干燥剂,所以本题答案为:CaO+H2O═Ca(OH)2;
(3)氧化钙能与水反应放出大量的热,使猪的蹄部干燥开裂,有的甚至出现灼伤、溃疡;Ca(OH)2对皮肤具有腐蚀性.所以本题答案为:生石灰与水反应会放出大量热;Ca(OH)2对皮肤具有腐蚀性.
故答案为:(1)Ca O(2)Ca O+H2O=Ca(OH)2(3)①CaO可与猪蹄表面的水分反应而吸收水分,并且放出大量的热,可能导致灼伤;
②Ca(OH)2对皮肤具有腐蚀性.点评:
本题考点: 生石灰的性质与用途;常见碱的特性和用途;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了氧化钙的有关性质,完成此题,可以依据已有的知识进行.1年前查看全部
- (2011•番禺区一模)(1)图为某同学做“观察水的沸腾”实验时测沸水温度的情形.他的错误是温度计的液泡碰到容器底(或壁
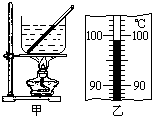 (2011•番禺区一模)(1)图为某同学做“观察水的沸腾”实验时测沸水温度的情形.他的错误是温度计的液泡碰到容器底(或壁)温度计的液泡碰到容器底(或壁).纠正错误后,他观察到水沸腾时,温度计的读数如图所示,则水的沸点是99℃99℃.水的沸点低于100℃的原因可能是当地大气压小于一个标准大气压当地大气压小于一个标准大气压.
(2011•番禺区一模)(1)图为某同学做“观察水的沸腾”实验时测沸水温度的情形.他的错误是温度计的液泡碰到容器底(或壁)温度计的液泡碰到容器底(或壁).纠正错误后,他观察到水沸腾时,温度计的读数如图所示,则水的沸点是99℃99℃.水的沸点低于100℃的原因可能是当地大气压小于一个标准大气压当地大气压小于一个标准大气压.
(2)在水平桌面上使用天平测石块的质量时发现横梁有点向右倾斜,如图1所示.要将它调到平衡状态,必须进行的步骤是把游码移到标尺的左端,然后调平衡螺母把游码移到标尺的左端,然后调平衡螺母.图2表示用排水法测量石块的体积,则石块的体积是1010cm3.已知石块的质量为26g,则石块的密度为2.6×1032.6×103kg/m3.
 skybaobei1年前1
skybaobei1年前1 -
 442197 共回答了18个问题
442197 共回答了18个问题 |采纳率83.3%(1)在使用温度计时,温度计的玻璃泡不能碰到容器底或容器壁,由图甲知,温度计的玻璃泡碰到容器底了.
图乙中温度计的分度值为1℃,所以温度计的示数为99℃.测得水的沸点低于标准大气压下的沸点,所以当时气压可能低于标准大气压.
故答案为:温度计的液泡碰到容器底(或壁 ); 99℃; 当地大气压小于一个标准大气压.
(2)使用天平调平前,要把天平的游码移动到标尺左端的零刻线处.
由图2知,水的体积是50ml,石块和水的总体积是60ml,所以石块的体积是10cm3.
所以石块的密度是:ρ=
m
V=
26g
10cm3=2.6g/cm3=2.6×103kg/cm3.
故答案为:把游码移到标尺的左端,然后调平衡螺母;10; 2.6×103.1年前查看全部
- (2011•番禺区一模)如图,AB是⊙O的直径,AE平分∠BAF交⊙O于点E,过点E作直线与AF垂直,交AF延长线于点D
(2011•番禺区一模)如图,AB是⊙O的直径,AE平分∠BAF交⊙O于点E,过点E作直线与AF垂直,交AF延长线于点D
 ,交AB延长线于点C.
,交AB延长线于点C.
(1)判断CD是否是⊙O的切线,并说明理由.
(2)若sinC=
,⊙O的半径为1,求DE的长.1 2  akuccc1年前0
akuccc1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2014•番禺区一模)若关于x的方程x2+2x+m=0没有实数根,则实数m的取值范围是( )
(2014•番禺区一模)若关于x的方程x2+2x+m=0没有实数根,则实数m的取值范围是( )
A.m<1
B.m>-1
C.m>1
D.m<-1 小子781年前1
小子781年前1 -
 无意苦争春01 共回答了13个问题
无意苦争春01 共回答了13个问题 |采纳率84.6%解题思路:根据判别式的意义得到△=22-4m<0,然后解不等式即可.根据题意得△=22-4m<0,
解得m>1.
故选C.点评:
本题考点: 根的判别式.
考点点评: 本题考查了一元二次方程ax2+bx+c=0(a≠0)的根的判别式△=b2-4ac:当△>0,方程有两个不相等的实数根;当△=0,方程有两个相等的实数根;当△<0,方程没有实数根.1年前查看全部
- (2013•番禺区一模)图分别是音叉、钢琴与长笛发出的C调1(do)的波形图,其中不正确的是( )
(2013•番禺区一模)图分别是音叉、钢琴与长笛发出的C调1(do)的波形图,其中不正确的是( )

A.三者都是乐音的波形
B.三者都是噪声的波形
C.三者的频率相同
D.三者的响度相同 olipher1年前1
olipher1年前1 -
 1jl7lv 共回答了15个问题
1jl7lv 共回答了15个问题 |采纳率86.7%解题思路:(1)频率是1s物体振动的次数,相同时间内振动越快,频率越大.音调跟频率有关,频率越大,音调越高.
(2)振幅是物体振动时偏离原位置的大小,偏离原位置越大,振幅越大.响度跟振幅有关,振幅越大,响度越大.
(3)从声音的波形上分析,噪声的波形是杂乱无章、不规则的,乐音的波形是规则的.如图可知,三幅图中音叉、钢琴、长笛振动的快慢相同,三者的频率相同,因此音调相同;偏离原位置相同,因此响度相同;三者波形是规则的,故都是乐音的波形.只有选项B不正确.
故选B.点评:
本题考点: 频率及音调的关系;响度与振幅的关系;噪声及来源.
考点点评: 通过物体振动的波形图,判断物体振动频率的大小,判断物体的振幅,从而判断音调和响度,考查学生对图象的识别能力.1年前查看全部
- (2010•番禺区二模)下列运算正确的是( )
(2010•番禺区二模)下列运算正确的是( )
A.a6-a3=a3
B.a3+a3=2a3
C.(a3)2=a5
D.a6÷a3=a2 zz2d1年前1
zz2d1年前1 -
 大海啸叔叔 共回答了17个问题
大海啸叔叔 共回答了17个问题 |采纳率88.2%解题思路:根据合并同类项,只把系数相加减,字母与字母的次数不变;幂的乘方,底数不变指数相乘;同底数幂相除,底数不变指数相减,对各选项计算后利用排除法求解.A、a6与a3不是同类项不能合并,故本选项错误;
B、a3+a3=2a3,正确;
C、应为(a3)2=a3×2=a6,故本选项错误;
D、应为a6÷a3=a6-3=a3,故本选项错误.
故选B.点评:
本题考点: 同底数幂的除法;合并同类项;幂的乘方与积的乘方.
考点点评: 本题主要考查合并同类项法则,幂的乘方的性质,同底数幂的除法,熟练掌握运算性质是解题的关键,不是同类项的不能合并.1年前查看全部
- (2014•番禺区一模)(1)学校开展拔河比赛,为使本班获得好成绩,同学们纷纷献计献策.你认为要赢得拨河比赛应注意哪些事
(2014•番禺区一模)(1)学校开展拔河比赛,为使本班获得好成绩,同学们纷纷献计献策.你认为要赢得拨河比赛应注意哪些事项(写出其中一项)______,解释那样做的原因
 ______.
______.
(2)小芳同学按照如图所示装置对动滑轮特点进行了探究,记录的数据如下表.
通过分析数据.她觉得与“使用动滑轮能省一半的力”的结论偏差较大.你认为实验中出现这样结果的主要原因是______;分析表中数据还发现:该装置的机械效率随物重的增大而______. 毕业llll1年前1
毕业llll1年前1 -
 歪鸟 共回答了24个问题
歪鸟 共回答了24个问题 |采纳率87.5%解题思路:(1)滑动摩擦力的大小与压力大小和接触面的粗糙程度有关.要改变摩擦力的大小通常保是持压力大小不变,改变接触面的粗
糙程度,接触面越粗糙,滑动摩擦力越大;或者保持接触面的粗糙程度不变,改变压力的大小,压力越大,滑动摩擦力
越大.
(2)滑轮组中如果忽略滑轮自重和摩擦力的大小,使用动滑轮能省一半的力,如果考虑动滑轮自重,则F=[1/2](G动+G物).(1)拔河比赛取胜的关键在于滑动摩擦力的大小,因为滑动摩擦力的大小与压力大小和接触面的粗糙程度有关,所以拔河比赛中为使本班获得好成绩应尽量增大滑动摩擦力的大小,其方法是:选体重比较大的同学(增大压力)或穿鞋地有花纹的运动鞋(增大接触面的粗糙程度).
原因:体重越大,运动员对地面的压力越大,在接触面的粗糙程度不变,压力越大,滑动摩擦力越大.
鞋地有花纹的运动鞋能增大接触面的粗糙程度,在压力一定时,接触面越粗糙,滑动摩擦力越大.
(2)由表中数据可知,随着物重的增加,测力计的示数变大,但比物重的一半要大,这与“使用动滑轮能省一半的力”的结论偏差较大.其主要原因是没有考虑滑轮的自重.
分析表中数据还发现:该装置的机械效率随物重的增大而增大.
故答案为:(1)选体重比较大的同学(或穿鞋底有花纹的运动鞋);压力越大滑动摩擦力越大(或接触面越粗糙滑动摩擦力越大)
(2)没有考虑滑轮的自重;增大.点评:
本题考点: 探究摩擦力的大小与什么因素有关的实验;动滑轮及其工作特点.
考点点评: 本题的解题关键有两个:(1)知道增大摩擦力大小的方法;(2)知道动滑轮重力影响拉力的大小.1年前查看全部
- (2008•番禺区一模)用化学用语表示下列物质或反应:
(2008•番禺区一模)用化学用语表示下列物质或反应:
(1)硫酸铁fe2(so4)3fe2(so4)3;
(2)3个镁离子3mg2+3mg2+;由60个碳原子构成的碳-60分子c60c60;
(3)用适量***将热水瓶胆壁上的水垢(主要成分是mg(oh)2和caco3)除去.反应的化学方程式是mg(oh)2+2hcl=mgcl2+2h2o;caco3+2hcl=mgcl2+2h2o+co2↑mg(oh)2+2hcl=mgcl2+2h2o;caco3+2hcl=mgcl2+2h2o+co2↑.
(4)氢氧化钡溶解于水的电离方程式ba(oh)2=ba2++2oh-ba(oh)2=ba2++2oh-. since921371年前1
since921371年前1 -
 autu 共回答了23个问题
autu 共回答了23个问题 |采纳率87%(1)铁的化合价为+3价,硫酸根离子-2价,十字交叉再约简,原子团个数不为1要加括号;
(2)3个镁离子是在镁离子前面放上3,镁是显+2价所以离子是带2个单位的正电荷;60个碳原子在碳右下角放上60就行了;
(3)相互交换成分,写化学式要根据化合价来写,再注意配平,注明条件;
(4)根据电离方程式的写法,注意正负电荷总数要相等.
故答案为:(1)Fe2(SO4)3;(2)3Mg2+;C60;(3)Mg(OH)2+2HCl=MgCl2+2H2O;CaCO3+2HCl=MgCl2+2H2O+CO2↑;(4)Ba(OH)2=Ba2++2OH-1年前
71年前查看全部
- (2014•番禺区一模)下列液体不能导电的是( )
(2014•番禺区一模)下列液体不能导电的是( )
A.澄清石灰水
B.氢氧化钠溶液
C.蒸馏水
D.稀盐酸 w6risq4kdwqdqw1年前1
w6risq4kdwqdqw1年前1 -
 junlvqingshen 共回答了18个问题
junlvqingshen 共回答了18个问题 |采纳率94.4%解题思路:物质导电有两种原因,一是金属,有能自由移动的电子;二是能够产生自由移动离子的溶液,据此进行分析判断.A、澄清石灰水中存在自由移动的钙离子和氢氧根离子,能够导电,故选项错误.
B、氢氧化钠溶液中存在自由移动的钠离子和氢氧根离子,能够导电,故选项错误.
C、蒸馏水是由水分子构成的,不存在能自由移动离子,不能导电,故选项正确.
D、稀盐酸中存在自由移动的氢离子和氯离子,能够导电,故选项错误.
故选:C.点评:
本题考点: 溶液的导电性及其原理分析.
考点点评: 本题难度不大,掌握物质导电的原因并能灵活运用是正确解答此类题的关键.1年前查看全部
- (2014•番禺区一模)下列实验操作正确的是( )
(2014•番禺区一模)下列实验操作正确的是( )
A.在量筒中配制100毫升10%的NaOH溶液
B.过滤时滤纸边缘应低于漏斗边缘
C.测定溶液酸碱性时,为使现象更明显,加入的指示剂越多越好
D.用PH试纸测PH值时,应先用水把试纸湿润,再滴待测液 Toicp1年前1
Toicp1年前1 -
 迷蒙丝丝 共回答了24个问题
迷蒙丝丝 共回答了24个问题 |采纳率91.7%解题思路:A、根据量筒的使用注意事项分析;
B、根据过滤液体时,要注意一贴二低三靠的原则;
C、根据指示剂的使用分析;
D、根据用pH试纸测定未知溶液的pH的方法进行分析判断.A、量筒只用来量取液体,不能用于配制溶液,故错误;
B、过滤液体时,要注意一贴二低三靠的原则:一贴:用少量水润湿的滤纸要紧贴漏斗壁,二低:滤纸边缘低于漏斗边缘、滤液低于滤纸边缘,三靠:烧杯紧靠玻璃棒、玻璃棒靠在三层滤纸上、漏斗下端口紧靠烧杯内壁.故正确;
C、指示剂起到指示作用即可,多加浪费,故错误;
D、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH.不能用水湿润pH试纸,否则稀释了待测溶液,使溶液的酸碱性减弱,测定结果不准确,故错误.
故选:B.点评:
本题考点: 测量容器-量筒;过滤的原理、方法及其应用;溶液的酸碱度测定;溶液的酸碱性测定.
考点点评: 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.1年前查看全部
- (2013•番禺区模拟)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列推
 (2013•番禺区模拟)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列推断正确的是( )
(2013•番禺区模拟)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列推断正确的是( )
A.T的氧化物是光导纤维的主要成分
B.W的氢化物的化学式为HCl
C.R的最高正价氧化物的水化物是弱电解质
D.Q与氢形成的化合物均含极性共价键 canner_six1年前1
canner_six1年前1 -
 1314579 共回答了16个问题
1314579 共回答了16个问题 |采纳率93.8%解题思路:短周期元素Q、R、T、W,根据元素所处的位置,可确定T、W为第三周期的元素,Q、R为第二周期元素,T所处的周期序数与族序数相等,则T为Al元素,故Q为C元素,R为N元素,W为S元素,据此结合选项解答.短周期元素Q、R、T、W,根据元素所处的位置,可确定T、W为第三周期的元素,Q、R为第二周期元素,T所处的周期序数与族序数相等,则T为Al元素,故Q为C元素,R为N元素,W为S元素,
A、T的氧化物是三氧化二铝,光导纤维的主要成分是二氧化硅,故A错误;
B、W为硫元素,其气态氢化物为H2S,故B错误;
C、R为N元素,其最高价氧化物对应水化物为HNO3,属于强酸,是强电解质,故C错误;
D、Q为C元素,与氢形成的化合物为烃,一定含有C-H,故均含极性共价键,故D正确;
故选D.点评:
本题考点: 位置结构性质的相互关系应用.
考点点评: 本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识,难度不大,注意整体把握元素周期表的结构.1年前查看全部
- (2008•番禺区一模)某化学课外活动小组的同学,用称取一定量的石灰石为原料制取烧碱,主要步骤如下图所示:
(2008•番禺区一模)某化学课外活动小组的同学,用称取一定量的石灰石为原料制取烧碱,主要步骤如下图所示:

(1)写出步骤①②③的化学方程式:
①CaCO3
CaO+CO2↑高温 .CaCO3.
CaO+CO2↑高温 .
②______.
③______.
(2)计算:
Ⅰ、石灰石主要成分(碳酸钙)的相对分子质量是:______;
Ⅱ、50g含碳酸钙70%的石灰石中,其碳酸钙的质量是______g;
Ⅲ、上述石灰石可得含氧化钙的生石灰______g.
Ⅳ、加入纯碱的质量不少于______ g
(3)分离和提纯
步骤④的操作是______.
步骤⑤的操作是______. 摘星抱月1年前1
摘星抱月1年前1 -
 yy114 共回答了22个问题
yy114 共回答了22个问题 |采纳率81.8%解题思路:根据已有的知识进行分析,碳酸钙高温能分解能生成氧化钙和二氧化碳,氧化钙能与水反应生成氢氧化钙,氢氧化钙能与碳酸钠反应生成氢氧化钠和碳酸钙,要将不溶性固体和液体分离,可以使用过滤的方法,要从溶液中分离出可溶性固体,可以使用蒸发结晶的方法.(1)碳酸钙高温能分解能生成氧化钙和二氧化碳,氧化钙能与水反应生成氢氧化钙,氢氧化钙能与碳酸钠反应生成氢氧化钠和碳酸钙,所以本题答案为:①CaCO3 高温 . CaO+CO2↑;②CaO+H2O═Ca(OH)2;③...
点评:
本题考点: 碳酸钙、生石灰、熟石灰之间的转化;混合物的分离方法;书写化学方程式、文字表达式、电离方程式.
考点点评: 不同考查了碳酸钙、氧化钙以及氢氧化钙的有关计算,完成此题,可以依据已有的知识结合题干提供的信息进行.1年前查看全部
- (2014•番禺区一模)有两个定值电阻,R1的阻值为10Ω,R2的电流与电压关系图线如图甲所示.
(2014•番禺区一模)有两个定值电阻,R1的阻值为10Ω,R2的电流与电压关系图线如图甲所示.

(1)R2的阻值是多大?
(2)当R1与R2串联在电路中,如图乙,电流表的示数如图丙,电源电压多大?
(3)如把R1与R2并联在电源电压为3V的电路中,如图丁所示,闭合开关S,电流表的示数多大?总电阻多大?(保留两位小数) 圣城家园1年前1
圣城家园1年前1 -
 受mm吧 共回答了12个问题
受mm吧 共回答了12个问题 |采纳率100%解题思路:(1)根据R2的U-I图象,选择图象上任意一点所对应的电压电流,根据R=[U/I]计算R2的阻值;
(2)根据串联电路的电阻特点可计算出电路中的总电阻,根据电流表的量程和分度值,读出电流表的示数,根据U=IR计算电源电压;
(3)已知电压和电阻,根据I=[U/R]计算各支路的电流,根据并联电路的电流规律计算出电路中的总电流,即电流表示数,根据R=[U/I]计算总电阻的大小.(1)由图甲可知,当R2两端电压U2=3V时,电流I2=0.6A,则由欧姆定律得R2=
U2
I2=[3V/0.6Ω]=5Ω;
(2)由图乙可知,R1与R2串联,由串联电路的电阻特点可知,电路中的总电阻R=R1+R2=10Ω+5Ω=15Ω,
丙图中电流表的量程为0~0.6A,分度值为0.02A,电流表的读数为0.3A,即电路中的电流I=0.3A,
∵I=[U/R],
∴电源电压U'=IR=0.3A×15Ω=45V;
(3)由图丁可知,R1与R2并联,此时电路两端的电压等于电源电压U=3V,电流表接在干路中,测量干路中的总电流,
此时通过R1的电流为I1=[U
R1=
3V/10Ω]=0.3A,
此时通过R2的电流为I2=[U
R2=
3V/5Ω]=0.6A,
则此时电流表的示数即电路中的总电流I'=I1+I2=0.3A+0.6A=0.9A;
电路中的总电阻R'=[U/I′]=[3V/0.9A]=3.33Ω.
答:(1)R2的阻值为5Ω;
(2)电源电压为45V;
(3)电流表的示数为0.9A;电路中的总电阻为3.33Ω.点评:
本题考点: 欧姆定律的应用.
考点点评: 本题考查了电阻、电压、电流的计算,解题的关键是能够熟练运用欧姆定律和其变形公式,还需要掌握U-I图象并能根据图象计算电阻,熟知串并联电路的特点,会准确读出电表的示数.1年前查看全部
- (2008•番禺区一模)如图,⊙O内切于△ABC,切点分别为D、E、F,若∠B=40°,∠C=60°,则∠EDF的大小为
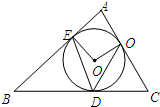 (2008•番禺区一模)如图,⊙O内切于△ABC,切点分别为D、E、F,若∠B=40°,∠C=60°,则∠EDF的大小为______.
(2008•番禺区一模)如图,⊙O内切于△ABC,切点分别为D、E、F,若∠B=40°,∠C=60°,则∠EDF的大小为______.  finza1年前1
finza1年前1 -
 冰夜心冷 共回答了15个问题
冰夜心冷 共回答了15个问题 |采纳率86.7%解题思路:首先根据三角形的内角和定理求得∠A=70°.再根据切线的性质定理和四边形的内角和定理,得∠EOF=100度.再根据圆周角定理,得∠EDF=50°.∵∠B=40°,∠C=60°,
∴∠A=80°,
∴∠EOF=100度,
∴∠EDF=[1/2]∠EOF=50°.点评:
本题考点: 三角形的内切圆与内心.
考点点评: 此题综合运用了切线的性质定理、圆周角定理和三角形的内角和定理、四边形的内角和定理.1年前查看全部
- (2014?番禺区一模)对大气污染物SO2、NOx进行研究具有重要环保意义.请回答下列问题:(1)为减少SO2的
(2014?番禺区一模)对大气污染物SO2、NOx进行研究具有重要环保意义.请回答下列问题:(1)为减少SO2的
 (2014?番禺区一模)对大气污染物SO2、NOx进行研究具有重要环保意义.请回答下列问题:
(2014?番禺区一模)对大气污染物SO2、NOx进行研究具有重要环保意义.请回答下列问题:
(1)为减少SO2的排放,常采取的措施是将煤转化为清洁气体燃料.
已知:H2(g)+[1/2O2 ssj03241年前1
ssj03241年前1 -
 不醉不归的我 共回答了12个问题
不醉不归的我 共回答了12个问题 |采纳率91.7%(1)①H2(g)+
1
2O2(g)=H2O(g)△H=-241.8kJ?mol-1
②C(s)+
1
2O2(g)=CO(g)△H=-110.5kJ?mol-1
依据盖斯定律计算②-①得到C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ?mol-1;
故答案为:C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ?mol-1;
(2)①在1.0L密闭容器内经过5s反应达到平衡,测得NO为8.0×10-4mol,5s内该反应的平均速率ν(NO)=
8×10-4mol
1.0L
5s]=1.6×10-4 mol/(L?s),依据化学方程式写出反应的平衡常数为:
c2(NO)
c(N2)c(O2);
故答案为:1.6×10-4 mol/(L?s),
c2(NO)
c(N2)c(O2);
②气缸温度越高,单位时间内NO排放量越大,原因是温度升高,反应速率加快,平衡右移,
故答案为:温度升高,反应速率加快,平衡右移;
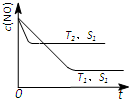
(3)①、温度T2到达平衡的时间短,反应速率快,故温度T2>T1,温度越高,平衡时NO的浓度越高,说明升高温度平衡向逆反应移动,故正反应为放热反应,即△H<0,
故答案为:<;
②、催化剂的表面积S1>S2,则催化剂S1到达平衡的时间比催化剂S2短,催化剂不影响平衡移动,平衡时NO的浓度相同,故c(NO) 在T1、S2条件下达到平衡过程中的变化曲线为: ,故答案为:
,故答案为: .
1年前查看全部
.
1年前查看全部
- (2011•番禺区一模)一个盒子里装有1个红球、1个黄球和2个蓝色球,它们除颜色外都相同.若随机地从盒子里一次取出两个球
(2011•番禺区一模)一个盒子里装有1个红球、1个黄球和2个蓝色球,它们除颜色外都相同.若随机地从盒子里一次取出两个球,则这两个球都是蓝色球的概率是[1/6][1/6].
 155484741年前0
155484741年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2013•番禺区一模)如图,已知E、F分别是平行四边形ABCD的边AB、CD上的两点,且∠CBF=∠ADE.
 (2013•番禺区一模)如图,已知E、F分别是平行四边形ABCD的边AB、CD上的两点,且∠CBF=∠ADE.
(2013•番禺区一模)如图,已知E、F分别是平行四边形ABCD的边AB、CD上的两点,且∠CBF=∠ADE.
(1)求证:△ADE≌△CBF;
(2)判定四边形DEBF是否是平行四边形? pipi13131年前0
pipi13131年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2014•番禺区一模)下列说法正确的是( )
(2014•番禺区一模)下列说法正确的是( )
A.两种物质相互反应能够生成盐和水,该反应一定是中和反应
B.生铁的硬度一定比纯铁大
C.常温下溶液的pH>7,溶质的一定是碱
D.在化合物中,金属元素一定是正价,非金属元素一定是负价 llqg22311年前1
llqg22311年前1 -
 cat5826 共回答了19个问题
cat5826 共回答了19个问题 |采纳率94.7%解题思路:A、根据中和反应是酸和碱反应生成盐和水的反应进行分析;
B、根据合金的硬度比纯金属的硬度大进行分析;
C、根据PH值测出的是溶液的酸碱度进行分析;
D、根据在化合物中,金属、非金属都可以显示正价进行分析.A、中和反应是酸和碱反应生成盐和水的反应,但是生成盐和水的反应不一定是中和反应,氢氧化钠和二氧化碳反应生成碳酸钠和水,但是该反应不是中和反应,故A错误;
B、合金的硬度比纯金属的硬度大,生铁是合金,所以生铁的硬度一定比纯铁大,故B正确;
C、常温下溶液的pH>7,只能说明该溶液是碱性溶液,而不一定是碱溶液,碳酸钠的pH值大于7,但是碳酸钠是盐溶液,故C错误;
D、在化合物中,金属、非金属都可以显示正价,比如在硫酸铜中,铜显+2价,硫显+6价,故D错误.
故选:B.点评:
本题考点: 中和反应及其应用;生铁和钢;溶液的酸碱性与pH值的关系;化合价规律和原则.
考点点评: 本题考查了常见概念及规律的推理,在解此类题时,可以依据学过的知识分析解答,要求同学们熟记有关的规律、概念,以便能够灵活应用.1年前查看全部
- (2012•番禺区一模)下列途述正确的是( )
(2012•番禺区一模)下列途述正确的是( )
A.化学反应过程中都会发生放热现象
B.在化学反应中只有燃烧反应才能放出热量
C.化学反应伴随着能量变化
D.人类利用的能量都是通过化学反应获得的 歪三1年前1
歪三1年前1 -
 cdut_mathren 共回答了22个问题
cdut_mathren 共回答了22个问题 |采纳率86.4%解题思路:此题是关于化学中有关能量来源的判断问题,解题时必须熟知物理变化和化学变化中能量变化问题.A、化学变化过程中既有放热现象,如:燃烧反应,金属与水或酸反应,酸碱中和反应,大部分的化合反应等.同时也有吸热现象,比如大部分的分解反应,碳和二氧化碳反应,碳和高温水蒸气反应等.
B、在化学反应中放出热量的不仅仅是燃烧反应,比如金属与水或酸反应,酸碱中和反应,大部分的化合反应等也会放热.
碳酸钙的分解反应.
C、化学变化不但生成新物质而且还会伴随着能量的变化,这种能量变化经常表现为热能、光能和电能的放出或吸收.炸药、石油、煤炭、蓄电池等储存的能量,都是靠化学反应释放出来的.所以化学变化中一定伴随着能量变化是对的.
D、不完全是,比如水能、风能、地热能、海洋能等就不是通化学反应而获得的.
故选C.点评:
本题考点: 物质发生化学变化时的能量变化;资源综合利用和新能源开发.
考点点评: 解答此类题型时,在掌握能量来源和利用的基础的同时,可以借用排除法进行筛选,即可选出正确的答案.1年前查看全部
- (2009•番禺区一模)下列说法不正确的是( )
(2009•番禺区一模)下列说法不正确的是( )
A.煤是化石燃料
B.用于奥运“祥云”火炬的丙烷是一种清洁燃料
C.乙烯是高分子化合物
D.蛋白质、糖类、脂肪和水等都是营养素 lxuyun1年前1
lxuyun1年前1 -
 iLoveStitch 共回答了20个问题
iLoveStitch 共回答了20个问题 |采纳率90%解题思路:A、根据化石燃料的定义和类别进行判断.
B、根据丙烷燃烧的产物对环境的影响进行分析.
C、根据高分子化合物的概念和特征进行分析.
D、根据营养素的分类进行判断.A、化石燃料主要包括煤、石油和天然气等天然资源.所以选项正确.
B、丙烷燃烧生成二氧化碳和水,对环境影响很小,属于清洁能源,所以选择正确.
C、高分子化合物的分子量很大,乙烯的分子量很小,所以选项错误.
D、生命活动的六大营养素包含蛋白质、糖类、脂肪、维生素、水和无机盐,所以选项正确.
故选C点评:
本题考点: 化石燃料及其综合利用;常用燃料的使用与其对环境的影响;有机高分子材料的分类及鉴别;人体的元素组成与元素对人体健康的重要作用.
考点点评: 本题主要考查化石燃料、能源的分类及生命活动的营养素等相关知识.1年前查看全部
- (2012•番禺区一模)春耕生产期间,各地都在保障农业生产所需的化肥供应.下列物质中属于复合肥的是( )
(2012•番禺区一模)春耕生产期间,各地都在保障农业生产所需的化肥供应.下列物质中属于复合肥的是( )
A.草木灰K2CO3
B.磷酸氢二铵 (NH4)2HPO4
C.尿素CO(NH2)2
D.磷矿粉有效成分Ca3(PO4)2 刺老芽1年前1
刺老芽1年前1 -
 danielfy 共回答了12个问题
danielfy 共回答了12个问题 |采纳率91.7%解题思路:含有氮元素的肥料称为氮肥.含有磷元素的肥料称为磷肥.含有钾元素的肥料称为钾肥.同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥.
A、草木灰中含有钾元素;
B、磷酸氢二铵中含有氮元素和磷元素;
C、尿素中含有氮元素;
D、磷矿粉中含有磷元素.A、草木灰中含有钾元素、属于钾肥,故不符合题意;
B、磷酸氢二铵中含有氮元素和磷元素,属于复合肥,故符合题意;
C、尿素中含有氮元素,属于氮肥,故不符合题意;
D、磷矿粉中含有磷元素,属于磷肥,故不符合题意.
故选B点评:
本题考点: 常见化肥的种类和作用.
考点点评: 本题主要考查化肥的种类,属于基础知识,容易做好.1年前查看全部
- (2013•番禺区一模)已知a>b,则下列不等式成立的是( )
(2013•番禺区一模)已知a>b,则下列不等式成立的是( )
A.a-c>b-c
B.a+c<b+c
C.ac>bc
D.[a/c>b c] 赞
xiaomianju 幼苗
共回答了23个问题采纳率:78.3% 举报
解题思路:分别根据不等式的基本性质对各选项进行逐一分析即可.A、∵a>b,∴a-c>b-c,故此选项正确;
B、∵a>b,∴a+c>b+c,故此选项错误;
C、∵a>b,当c>0时,ac>bc,当c<0时,ac<bc,故此选项错误;
D、∵a>b,当c>0时,[a/c]>[b/c],当c<0时,[a/c]<[b/c],故此选项错误.
故选:A.点评:
本题考点: 不等式的性质.
考点点评: 此题主要考查的是不等式的基本性质,解答此题的关键注意不等式的两边同时乘以或除以一个负数时,不等号的方向要改变.1年前
9可能相似的问题-
1年前1个回答
-
1年前1个回答
-
1年前1个回答
你能帮帮他们吗
Copyright © 2022 YULUCN.COM - 雨露学习互助 - 17 q. 0.034 s. - webmaster@yulucn.com sdyiyiliuliu1年前1
sdyiyiliuliu1年前1 -
 xiaomianju 共回答了23个问题
xiaomianju 共回答了23个问题 |采纳率78.3%解题思路:分别根据不等式的基本性质对各选项进行逐一分析即可.A、∵a>b,∴a-c>b-c,故此选项正确;
B、∵a>b,∴a+c>b+c,故此选项错误;
C、∵a>b,当c>0时,ac>bc,当c<0时,ac<bc,故此选项错误;
D、∵a>b,当c>0时,[a/c]>[b/c],当c<0时,[a/c]<[b/c],故此选项错误.
故选:A.点评:
本题考点: 不等式的性质.
考点点评: 此题主要考查的是不等式的基本性质,解答此题的关键注意不等式的两边同时乘以或除以一个负数时,不等号的方向要改变.1年前查看全部
- (2013•番禺区模拟)下列叙述正确的是( )
(2013•番禺区模拟)下列叙述正确的是( )
A.0.1 mol•L-1醋酸溶液中:c(H+)=c(CH3COO- )+c(OH- )
B.中和pH与体积都相同的硫酸和醋酸,消耗NaOH的量后者大于前者
C.同温度同浓度的NaOH和澄清石灰水中,水的电离程度相同
D.NaHCO3溶液中:c(Na+)>c(HCO3-)>c(H2CO3)>c(OH-)>c(H+) wenge11年前1
wenge11年前1 -
 思维时间 共回答了21个问题
思维时间 共回答了21个问题 |采纳率100%解题思路:A.根据溶液的电荷守恒进行判断;
B.醋酸为弱电解质,不能完全电离,与硫酸等pH时浓度较大;
C.同温度同浓度的NaOH和澄清石灰水,OH-浓度不同;
D.NaHCO3为强碱弱酸盐,根据HCO3-+H2O⇌H2CO3+OH-判断.溶液中存在c(OH-)>c(H2CO3).A.醋酸溶液中存在电荷守恒,应有c(H+)=c(CH3COO- )+c(OH- ),故A正确;
B.醋酸为弱电解质,电离程度较小,远小于0.5,与硫酸等pH时浓度较大,则中和pH与体积都相同的硫酸和醋酸,消耗NaOH的量后者大于前者,故B正确;
C.同温度同浓度的NaOH和澄清石灰水,OH-浓度不同,则对水的电离影响程度不同,故C错误;
D.NaHCO3为强碱弱酸盐,溶液中存在HCO3-+H2O⇌H2CO3+OH-,因溶液中还存在H+,说明水电离产生的H+并没有全部与HCO3-结合生成H2CO3,则溶液中存在c(OH-)>c(H2CO3),故D错误.
故选AB.点评:
本题考点: 离子浓度大小的比较;弱电解质在水溶液中的电离平衡;盐类水解的应用.
考点点评: 本题考查离子浓度大小比较,解答本体要要注意把握弱电解质的电离以及盐类水解的特征,从电荷守恒、物料守恒以及质子守恒的角度分析,题目难度中等.1年前查看全部
- (2014•番禺区一模)如图所示,在测定杠杆机械效率的实验中,竖直向上匀速拉动弹簧测力计,使挂在杠杆OB下面的物块缓慢上
 (2014•番禺区一模)如图所示,在测定杠杆机械效率的实验中,竖直向上匀速拉动弹簧测力计,使挂在杠杆OB下面的物块缓慢上升至虚线位置:
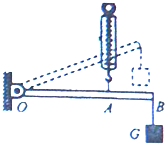
(2014•番禺区一模)如图所示,在测定杠杆机械效率的实验中,竖直向上匀速拉动弹簧测力计,使挂在杠杆OB下面的物块缓慢上升至虚线位置:
(1)请在图中画出杠杆在水平位置时,杠杆所受测力计拉力(为杠杆的动力)的力臂L1,此杠杆是______杠杆(选填“省力”、“费力”、“等臂”).
(2)图中测力计的示数F为2.5N,测力计上升的高度s为0.2m.物块中G为1.5N,物块上升的高度h为0.3m,则提升物体做的功为______J,机械效率为______. pretty-girl1年前1
pretty-girl1年前1 -
 Deathwang 共回答了20个问题
Deathwang 共回答了20个问题 |采纳率95%解题思路:(1)支点到动力作用线的垂线段为动力臂;根据动力臂和阻力臂的关系判断杠杆的种类;(2)在实验中,弹簧测力计向上拉力做的功是总功,克服钩码重力做的功是有用功,克服摩擦以及杠杆自重做的功是额外功;杠杆的机械效率可以根据公式η=W有W总来计算.(1)过支点作动力作用线的垂线段,即动力臂L1;如下图所示:

弹簧测力计的分度值是0.1N,读数是:2.5N;动力臂小于阻力臂,因此是费力杠杆.
(2)W有=Gh=1.5N×0.3m=0.45J;
W总=FS=2.5N×0.2m=0.5J;
η=
W有
W总×100%=[0.45J/0.5J]×100%=90%.
故答案是:(1)费力;(2)0.5;90%.点评:
本题考点: 杠杆机械效率的测量实验.
考点点评: 机械效率计算的关键是明确有用功和总功,一般来说,使用机械所用外力做的功是总功,而克服提升重物重力做的功是有用功.1年前查看全部
- (2014•番禺区一模)25℃时,下列说法正确的是( )
(2014•番禺区一模)25℃时,下列说法正确的是( )
A.氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+)
B.pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-)
C.pH=12的NaOH溶液与等体积pH=2的醋酸溶液混合后所得溶液显酸性
D.将0.1mol/L的氨水溶液加水稀释10倍,溶液中离子浓度都减少 wintding1年前1
wintding1年前1 -
 渔人得利 共回答了20个问题
渔人得利 共回答了20个问题 |采纳率85%解题思路:A、根据电荷守恒分析;
B、NaHCO3溶液中HCO3-的水解程度大于电离程度;
C、醋酸为弱酸在溶液中部分电离,醋酸的浓度大于其溶液中的氢离子的浓度;
D、加水稀释Kw不变.A、溶液中存在电荷守恒:c(Cl-)+c(OH-)=c(H+)+c(NH4+),已知pH=7,则c(OH-)=c(H+),所以c(Cl-)=c(NH4+),故A错误;
B、NaHCO3溶液中HCO3-的水解程度大于电离程度,则c(H2CO3)>c(CO32-),由于电离和水解的程度较小,则c(HCO3-)>c(H2CO3),所以溶液中浓度关系为:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-),故B正确;
C、醋酸为弱酸在溶液中部分电离,醋酸的浓度大于其溶液中的氢离子的浓度,则c(醋酸)>0.01mol/L,NaOH是强电解质完全电离,则c(NaOH)=0.01mol/L,所以二者混合后醋酸过量,溶液显酸性,故C正确;
D、将0.1mol/L的氨水溶液加水稀释10倍,Kw=c(OH-)×c(H+)不变,c(OH-)减小,则c(H+)增大,故D错误;
故选BC.点评:
本题考点: 盐类水解的应用;酸碱混合时的定性判断及有关ph的计算.
考点点评: 本题考查了弱酸的电离和盐的水解,主要涉及了电荷守恒的应用、溶液中离子浓度的比较、混合溶液酸碱性的判断等,题目考查的知识点较多,题目难度中等.1年前查看全部
- (2014•番禺区一模)对大气污染物SO2、NOx进行研究具有重要环保意义.请回答下列问题:
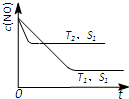 (2014•番禺区一模)对大气污染物SO2、NOx进行研究具有重要环保意义.请回答下列问题:
(2014•番禺区一模)对大气污染物SO2、NOx进行研究具有重要环保意义.请回答下列问题:
(1)为减少SO2的排放,常采取的措施是将煤转化为清洁气体燃料.
已知:H2(g)+[1/2O2 田中春雨1年前1
田中春雨1年前1 -
 明月清泉cmz 共回答了21个问题
明月清泉cmz 共回答了21个问题 |采纳率95.2%解题思路:(1)依据热化学方程式和盖斯定律计算得到所需让化学方程式;
(2)①计算出平衡时各种物质的物质的量,结合反应速率计算方法和平衡常数的表达式完成;
②汽缸温度越高,单位时间内NO排放量越大,说明平衡正向进行,温度越高速率越快;
(3)①根据到达平衡的时间,判断温度高低,再根据不同温度下到达平衡时NO的浓度高低,判断温度对平衡的影响,据此判断反应热效应;
②催化剂的表面积S1>S2,则催化剂S1到达平衡的时间比催化剂S2短,催化剂不影响平衡移动,平衡时NO的浓度相同,据此作图.(1)①H2(g)+[1/2O2(g)=H2O(g)△H=-241.8kJ•mol-1
②C(s)+
1
2O2(g)=CO(g)△H=-110.5kJ•mol-1
依据盖斯定律计算②-①得到C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ•mol-1;
故答案为:C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ•mol-1;
(2)①在1.0L密闭容器内经过5s反应达到平衡,测得NO为8.0×10-4mol,5s内该反应的平均速率ν(NO)=
8×10-4mol
1.0L
5s]=1.6×10-4 mol/(L•s),依据化学方程式写出反应的平衡常数为:
c2(NO)
c(N2)c(O2);
故答案为:1.6×10-4 mol/(L•s),
c2(NO)
c(N2)c(O2);
②气缸温度越高,单位时间内NO排放量越大,原因是温度升高,反应速率加快,平衡右移,
故答案为:温度升高,反应速率加快,平衡右移;
(3)①、温度T2到达平衡的时间短,反应速率快,故温度T2>T1,温度越高,平衡时NO的浓度越高,说明升高温度平衡向逆反应移动,故正反应为放热反应,即△H<0,
故答案为:<;
②、催化剂的表面积S1>S2,则催化剂S1到达平衡的时间比催化剂S2短,催化剂不影响平衡移动,平衡时NO的浓度相同,故c(NO) 在T1、S2条件下达到平衡过程中的变化曲线为: ,故答案为:
,故答案为: .
.点评:
本题考点: 化学平衡常数的含义;热化学方程式;化学反应速率的影响因素.
考点点评: 本题主要考查热化学方程式书写,化学反应速率、影响化学平衡的因素、化学平衡图象以及热化学方程式的书写等,难度不大,(3)中注意根据“先拐先平数值大”原则判断温度高低是关键,作图时注意到达平衡的时间与平衡时NO的浓度.1年前查看全部
- (2007•番禺区一模)某化工厂常用电解纯净的饱和食盐水的方法来得到烧碱溶液,再经浓缩、蒸发等步骤制造固体烧碱.某化学兴
(2007•番禺区一模)某化工厂常用电解纯净的饱和食盐水的方法来得到烧碱溶液,再经浓缩、蒸发等步骤制造固体烧碱.某化学兴趣小组要分析该化工厂仓库里的固体烧碱样品.
(1)小组成员猜测该样品中含有碳酸钠,支持这种猜测的依据是(用化学方方程式表示)______.小组成员选用了三种不同类别的试剂,进行实验,验证猜想,并得出结论,碳酸钠确实存在.请你将实验过程中涉及的化学方程式填在下表中.
(2)现已知样品中含有氯化钠、氢氧化钠、碳酸钠,设计一个实验方案,来证实一定含有氯化钠存在.化学方程式 试剂1 试剂2 试剂3 
请写出试剂X的化学式______
请写出①反应的化学方程式______
请写出②反应的化学方程式______. 烟雨楼家族之烟灰1年前1
烟雨楼家族之烟灰1年前1 -
 钱之光 共回答了20个问题
钱之光 共回答了20个问题 |采纳率85%解题思路:(1)烧碱易潮解,潮解之后容易和空气中的二氧化碳反应,检验烧碱变质的方法就是根据碳酸钠的化学性质来选择合适的试剂来鉴别
(2)加入试剂A后生成了气体可知X为酸,但是考虑到后边的反应中加入了硝酸银,所以此时要排除氯离子和硫酸根离子的干扰,故应该选择稀硝酸,可以据此答题(1)烧碱露置于空气中时易于空气中的二氧化碳反应而变质,在验证烧碱是否变质实际上就是验证碳酸钠的存在,故可以据其性质来区分,要注意的是当用盐酸时要向把氢氧化钠反应掉,然后才会有气体产生,故本题的答案为:CO2+2NaOH=Na2CO3+H2O
化学方程式
试剂1 Na2CO3 +CaCl2═2NaCl+CaCO3↓
试剂2 Na2CO3+Ca(OH)2═2NaOH+CaCO3↓
试剂3
NaOH+HCl=NaCl+H2O
Na2CO3+2HCl=2NaCl+CO2↑+H2O (2)加入X生成了气体可知X为酸,但是考虑到后边的反应中加入了硝酸银,所以此时要排除氯离子和硫酸根离子的干扰,故应该选择稀硝酸,当加入稀硝酸时除了和碳酸钠反应,还要和氢氧化钠发生中和反应,在混合物中能和硝酸银生成白色沉淀的是氯化钠,
故本题答案为:HNO3 NaOH+HNO3=NaNO3+H2O; Na2CO3+2HNO3=2NaNO3+CO2↑+H2ONaCl+AgNO3=AgCl↓+NaNO3点评:
本题考点: 酸、碱、盐的鉴别;电解水实验.
考点点评: 解答本题要求学生熟练掌握酸、碱、盐的化学性质,并能根据物质之间能否反应及其反应的实验现象来得出结论,熟记化学方程式:CO2+2NaOH=Na2CO3+H2O;Na2CO3+Ca(OH)2═2NaOH+CaCO3↓; NaOH+HCl=NaCl+H2O.1年前查看全部
- (2009•番禺区二模)下列关于石油的叙述中正确的是( )
(2009•番禺区二模)下列关于石油的叙述中正确的是( )
A.石油是一种化工产品
B.石油是一种纯净物
C.石油产品发电
D.将石油分馏可得到多种产品 我的nn1年前1
我的nn1年前1 -
 ukhfjhl 共回答了16个问题
ukhfjhl 共回答了16个问题 |采纳率93.8%解题思路:A、石油是一种自然形成的物质;
B、石油中含有多种烷烃和其它种类的物质;
C、石油产品一般不用来发电;
D、石油中含有汽油、煤油、柴油等多种物质,通过分馏可以达到这些物质.A、石油不是化工产品.故选项错误;
B、石油不是纯净物.故选项错误;
C、石油产品一般不用来发电.故选项错误;
D、将石油分馏可得到多种产品.故选项正确.
故选D.点评:
本题考点: 石油的组成;石油加工的产物.
考点点评: 本题主要考查石油的组成,解答时要理解石油是一种宝贵的自然资源,其中含有很多重要的物质.1年前查看全部
大家在问
- 1描写心情的词语,描写颜色的词语,描写景色的词语?
- 2化学应该复习那些啊,我是60分左右的人,求大神回答
- 31:若分段函数f(x)=(1) x2-x-1,x大于等于2或x小于等于-1 (2)1,-1
- 4墨西哥与美国在地理上的相同和不同点
- 5书上说,鱼儿离不开水。用学过的一首古诗中的两句话,概括含义。
- 6以“My dream job”为题写一篇短文,词数70左右。主要从以下几个方面来写:你梦想的职业是什么?为什么喜欢这个职
- 7某班级同学用如图(a)所示的装置验证加速度a和力F、质量m的关系.甲、乙两辆小车放在倾斜轨道上,小车甲上固定一个力传感器
- 8You best可以用在书信结尾吗?
- 9给起一个“浮”字开头的后面跟三个名字的.名词,比如浮生如斯,浮生若梦.
- 10词语归类.今天就需要!骨瘦如柴,目不转睛,亭亭玉立,眉开眼笑,眉清目秀,身材魁梧,悬崖峭壁,田地荒芜,表里如一,助人为乐
- 11三年级数学竖式计算题
- 12(1)写出下列溶液中溶剂的化学式:白磷的二硫化碳溶液______;75%的酒精溶液(医疗消毒用)______;
- 13根据下列规律填数1/2,1/6,1/12,1/20,1/30,______,1/56
- 14用配方法解方程:1、x^2-x-7/4=0 2、 4x^2-6x-3=0 3、x(x+4)=8x+12 (写详细点)
- 15过平面上的一点,能画出______条直线.通过平面上的两点,能画出______条直线.



