铜器生锈的化学式是什么?二氧化硫形成酸雨的化学式是什么?
 free_over2022-10-04 11:39:541条回答
free_over2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 wbd715 共回答了13个问题
wbd715 共回答了13个问题 |采纳率76.9%- 2Cu+O2+CO2+H2O==Cu2CO3(OH)2
1:SO2+H2O=H2SO3 2H2SO3+O2=2H2SO4
2:2SO2+O2==(粉尘催化)==2SO3 SO3+H2O=H2SO4
不过应该是第一种反应进行的容易些 - 1年前
相关推荐
- 小明发现从不同地点收集到的两个铜器(一个是纯铜做的,一个是青铜做的)中,纯铜器的铜绿比青铜器的少,他据此分析认为青铜比纯
小明发现从不同地点收集到的两个铜器(一个是纯铜做的,一个是青铜做的)中,纯铜器的铜绿比青铜器的少,他据此分析认为青铜比纯铜易锈蚀,小明的分析是否全面,请说明理由
 混在虚拟世界1年前1
混在虚拟世界1年前1 -
 全明星allstar 共回答了20个问题
全明星allstar 共回答了20个问题 |采纳率100%不全面,首先,不能确定时间的长短,其次不了解各个器皿所处的外界条件,是酸性环境还是中性环境,能直接造成锈蚀的影响1年前查看全部
- (2004•红山区)是真是假:橘子皮上出现的青绿色霉点和铜器上生出青绿色的锈斑有什么本质区别?______.
 3096343561年前1
3096343561年前1 -
 xiaovsyi 共回答了16个问题
xiaovsyi 共回答了16个问题 |采纳率81.3%解题思路:生物具有一下特征:1、生物的生活需要营养.2、生物能够进行呼吸.3、生物能排出体内产生的废物.4、生物能够对外界刺激作出反应.5、生物能够生长和繁殖.6、除病毒外,生物都是由细胞构成的.橘子皮上出现青绿色霉点是青霉菌利用橘子皮营养物质组建自身物质而进行的一系列生命活动现象,而铜绿是一种化学反应,是非生命现象.
所以橘子皮上出现的青绿色霉点属于生命现象,而铜器上生出青绿色的锈斑属于非生命现象.
故答案为:橘子皮上出现的青绿色霉点属于生命现象,而铜器上生出青绿色的锈斑属于非生命现象.点评:
本题考点: 生物的特征.
考点点评: 解答此类题目的关键是理解生物的特征.1年前查看全部
- 铜器表面的铜绿在隔绝空气加热后,反应生成氧化铜、二氧化碳和水,是推测铜绿的组成并写出理由
 cxcyxl1年前1
cxcyxl1年前1 -
 hhhsb 共回答了12个问题
hhhsb 共回答了12个问题 |采纳率100%Cu2(OH)2CO3
理由:因为在隔绝空气加热后,反应生成氧化铜、二氧化碳和水,说明铜绿中含有Cu,H,O,C等元素,根据Cu(OH)2=CuO+H2O,CuCO3=CuO+CO2,推测铜绿的组成为Cu2(OH)2CO31年前查看全部
- 铜器生锈属于不属于物理变化和化学变化?
 嚼槟榔的人1年前7
嚼槟榔的人1年前7 -
 sun0603 共回答了23个问题
sun0603 共回答了23个问题 |采纳率87%化学变化,因为有新物质生成,铜锈1年前查看全部
- (2008•杭州)年代久远的铜器表面往往生有绿色铜锈,其主要成份为化合物:碱式碳酸铜[Cu2(OH)2CO3],其化学性
(2008•杭州)年代久远的铜器表面往往生有绿色铜锈,其主要成份为化合物:碱式碳酸铜[Cu2(OH)2CO3],其化学性质类似于碱和碳酸钙.若要除去铜器表面上的铜锈,可用稀盐酸或稀硫酸与反应生成溶液和气体除去.
(1)写出稀硫酸和碱式碳酸铜反应的化学方程式:______.
(2)列式计算:2000克溶质质量分数为2.5%的硫酸溶液,可以和多少克碱式碳酸铜反应?(保留1位小数;相对原子质量:H-1;C-12;Cu-64;O-16;S-32) zxc26511年前1
zxc26511年前1 -
 dagang3231 共回答了24个问题
dagang3231 共回答了24个问题 |采纳率95.8%解题思路:(1)依据碱式碳酸铜具备碱和碳酸盐的性质分析该物质与酸反应的产物;
(2)利用以上的方程式和反应的硫酸的质量可求出反应的碱式碳酸铜的质量;(1)由于碱式碳酸铜具备碱和碳酸盐的性质,所以[Cu2(OH)2CO3]和硫酸反应的产物是硫酸铜、水和二氧化碳,方程式为Cu2(OH)2C03+2H2S04=2CuS04+CO2↑+3H2O;
(2)设:可以和x克碱式碳酸铜反应
Cu2(OH)2C03+2H2S04=2CuS04+CO2↑+3H2O
222 196
x 2000g×2.5%
[222/x=
196
2000g×2.5%]
x=56.6g
故答案为:(1)Cu2(OH)2C03+2H2S04=2CuS04+CO2↑+3H2O;(2)答:可以和56.6克碱式碳酸铜反应.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 此题是对信息利用和化学方程式计算考查题,解题的关键是利用信息书写出相关的方程式;1年前查看全部
- (2009•济宁)人类从石器时代进入铜器时代,继而进入铁器时代,铜作为金属材料一直被广泛应用着.下面冶炼铜的方法中,利用
(2009•济宁)人类从石器时代进入铜器时代,继而进入铁器时代,铜作为金属材料一直被广泛应用着.下面冶炼铜的方法中,利用了置换反应的是( )
①C+2CuO
2Cu+CO2↑高温 .
②CO+CuO
Cu+CO2高温 .
③H2+CuO═Cu+H2O
④Fe+CuSO4=Cu+FeSO4
A.①②③
B.①③④
C.②③④
D.①② Tikey1年前1
Tikey1年前1 -
 pq4475 共回答了21个问题
pq4475 共回答了21个问题 |采纳率85.7%解题思路:本题考查置换反应的概念,反应物中是一种单质和一种化合物,生成物也是一种单质和一种化合物.A、②是化合物与化合物反应生成单质和化合物,不符合置换反应的概念,故A错误.
B、①③④都是单质和化合物反应生成单质和化合物,属于置换反应,故B正确.
C、②是化合物与化合物反应生成单质和化合物,不符合置换反应的概念,故C错误.
D、②是化合物与化合物反应生成单质和化合物,不符合置换反应的概念,故D错误.
故选B.点评:
本题考点: 置换反应及其应用.
考点点评: 可以利用单质和化合物的判断,紧扣概念来分析置换反应.1年前查看全部
- 铜和铁一样容易生锈,铜表面生成绿色铜锈,为了探究铜锈的组成,某兴趣小组从铜器上取下绿色粉未,按如下步骤进行实验。请回答下
铜和铁一样容易生锈,铜表面生成绿色铜锈,为了探究铜锈的组成,某兴趣小组从铜器上取下绿色粉未,按如下步骤进行实验。请回答下列问题:
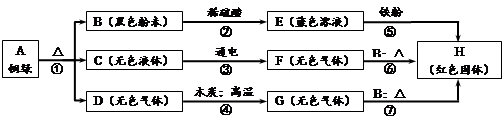
(1)写出B物质的化学式 ,步骤⑤的化学方程式为 ;
(2)步骤③得到两种气体,请简述其中一种气体的检验方法 ;
(3)步骤④可以得到煤气(主要成分是H 2 和CO)的一种成分,写出步骤⑦的化学方程
式 ;通过以上实验可知,铜绿的组成元素是 。 许愿的许愿1年前1
许愿的许愿1年前1 -
 rainyday1 共回答了22个问题
rainyday1 共回答了22个问题 |采纳率90.9%(1)CuO, Fe+Cu S O 4 =FeSO 4 +Cu(2)
根据物质的相互反应规律和特殊的现象找出突破点:E为蓝色溶液,E中一定含有有铜离子,B为黑色粉末,和稀硫酸反应生成E,可知B为氧化铜,E为硫酸铜,E和铁反应生成红色固体H,H为铜,C 在通电条件下可分解,则C为水,水通电生成的气体F和氧化铜加热生成铜,说明F具有还原性,则F为氢气.G和氧化铜加热生成铜,说明G具有还原性,具有还原性的气体主要是氢气和一氧化碳,G是由无色气体D和木炭高温反应生成的,G中含有碳元素,则G为一氧化碳,D为二氧化碳.进行解答1年前查看全部
- 铜器在潮湿的空气中,表面会慢慢地生成一层铜锈[Cu 2 (OH) 2 CO 3 ].该反应的化学方程式为:______.
 2900797111年前1
2900797111年前1 -
 roadsign 共回答了15个问题
roadsign 共回答了15个问题 |采纳率100%在潮湿的空气中,铜可以和水、氧气、二氧化碳等物质反应生成碱式碳酸铜,反应的化学方程式为:2Cu+H 2 O+CO 2 +O 2 ═Cu 2 (OH) 2 CO 3 .
故答案为:2Cu+H 2 O+CO 2 +O 2 ═Cu 2 (OH) 2 CO 3 .1年前查看全部
- 铜器铁器和陶器出现时间的先后顺序是什么?
 arline74191年前1
arline74191年前1 -
 DspSage 共回答了13个问题
DspSage 共回答了13个问题 |采纳率84.6%先陶器,再铜器,最后铁器.1年前查看全部
- 铜器在空气中容易“生锈”,生成“铜绿”,该物质的主要成分是(),它是一种()
铜器在空气中容易“生锈”,生成“铜绿”,该物质的主要成分是(),它是一种()
色()状的固体,()溶于水,但能与稀盐酸反应,该反应的现象有:固体渐渐溶解,产生(),溶液由()色变为()色 jiangguanjun1年前6
jiangguanjun1年前6 -
 飘苇渡江 共回答了28个问题
飘苇渡江 共回答了28个问题 |采纳率89.3%主要成分:碱式碳酸铜
绿色,粉末,不溶水
产生气泡,溶液无色变蓝色1年前查看全部
- 自己在家里如何能融化铜?我想自己做个铜器,可不知道如何能用手边最容易得到的工具盒材料来融化铜
 sophia_zhng1年前1
sophia_zhng1年前1 -
 sanwanjie 共回答了21个问题
sanwanjie 共回答了21个问题 |采纳率66.7%楼上的,只是得到铜,如何让他成为器物呢?肯定要浇注啊呵呵1年前查看全部
- 铜绿的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它能跟酸反应生成铜盐、水和二氧化碳.某同学用小刀把家中旧铜器上的铜
铜绿的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它能跟酸反应生成铜盐、水和二氧化碳.某同学用小刀把家中旧铜器上的铜绿刮下,用来依次制取较纯净的硫酸铜、氧化铜和铜(为避免掺入固体杂质,他没有采用金属或碳置换化合物中的铜的方法).制取步骤分为四步:

(1)填写下面表示制取步骤的方框图(方框内填写所制取物质的化学式).
(2)写出A操作过程中涉及的反应的化学方程式.
(3)如果实验装置及生成铜以前的操作都正确,但最后没有生成铜,这是因为______. 方塔tt1年前1
方塔tt1年前1 -
 卡能通考勤机 共回答了17个问题
卡能通考勤机 共回答了17个问题 |采纳率82.4%解题思路:(1)铜绿的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它能跟酸反应生成铜盐、水和二氧化碳,氢氧化铜加热之后会发生反应:Cu(OH)2
CuO+H2O,氢气能置换出氧化铜中的铜;△ .
(2)根据(1)的分析写出化学方程式即可;
(3)氢气还原氧化铜实验结束后,应继续通氢气至铜冷却,否则生成的铜又可与氧气发生反应生成氧化铜,使实验失败.(1)①因为“铜绿的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它能跟酸反应生成铜盐、水和二氧化碳”化学方程式为:Cu2(OH)2CO3+2H2SO4=2+3H2O+CO2↑;故A中所制取物质为CuSO4;
②氢氧化铜加热之后会发生反应:Cu(OH)2
△
.
CuO+H2O,故C中所制取物质为CuO;
③氢气能置换出氧化铜中的铜,化学方程式为:H2+CuO=Cu+H2O,故D中所制取物质为Cu;
(2)A操作过程中涉及的反应的化学方程式为:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑;
(3)如果实验装置及生成铜以前的操作都正确,但最后没有生成铜,这是因为反应结束时没有继续通氢气,使生成的铜又被氧化了.
故答案为:(1)A、CuSO4,C、CuO,D、Cu;
(2)Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑;
(3)反应结束时没有继续通氢气,使生成的铜又被氧化了.点评:
本题考点: 物质的鉴别、推断;实验操作注意事项的探究;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 此题主要是考查同学们的综合分析能力,不但要求同学们具备有关化合物的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力.解题时需要认真分析题目给出的条件,联系实际,逐一分析推断.1年前查看全部
- (2009•大连)铜器在空气中久置,表面会生成一层绿色固体,俗称“铜绿”.为了探究铜绿的生成与哪些物质有关,化学活动小组
 (2009•大连)铜器在空气中久置,表面会生成一层绿色固体,俗称“铜绿”.为了探究铜绿的生成与哪些物质有关,化学活动小组的同学采用右图装置加热干燥的铜绿,观察到绿色固体变成黑色,试管口有水滴出现,澄清石灰水变浑浊.
(2009•大连)铜器在空气中久置,表面会生成一层绿色固体,俗称“铜绿”.为了探究铜绿的生成与哪些物质有关,化学活动小组的同学采用右图装置加热干燥的铜绿,观察到绿色固体变成黑色,试管口有水滴出现,澄清石灰水变浑浊.
(1)由上述实验可知,铜绿中一定含有的元素是______,由此推断,空气中一定参加反应的物质是______,不能确定是否参加反应的物质是______.
(2)设计对比实验,探究不能确定的物质是否参加了反应. 青格里0011年前1
青格里0011年前1 -
 tysq 共回答了19个问题
tysq 共回答了19个问题 |采纳率94.7%解题思路:(1)根据质量守恒定律的实质以及反应现象可以判断铜绿的元素组成和参加反应的物质;
(2)通过控制反应条件比较铜生锈的难易程度来判断是否有氧气参加反应.(1)由反应现象可知,绿色固体变成黑色的氧化铜,说明铜绿中含有铜和氧,试管口有水滴出现,说明铜绿中含有氢和氧,澄清石灰水变浑浊是因为生成了二氧化碳,说明铜绿中含有碳和氧,则铜绿中含有的元素是铜、碳、氢、氧,因为水和二氧化碳中都含有氧元素,故不能确定氧气是否参加反应.
(2)要确定氧气是否参与铜生锈,可设计一个有氧气、二氧化碳、水同时存在的环境和一个只有水和二氧化碳存在的环境,通过比较铜能否生锈以及生成的快慢来判断.
故答案为:(1)铜、碳、氢、氧,二氧化碳、水,氧气.
(2)取两片打磨好的铜片分别半浸入两只盛有经煮沸并迅速冷却的蒸馏水的试管中,将其中一支试管充满二氧化碳气体,塞紧橡皮塞;将另一支试管充满氧气和二氧化碳气体的混合气体,塞紧橡皮塞.根据两支试管中铜片表面是否出现铜绿来判断氧气是否参加了反应.点评:
本题考点: 实验探究物质的组成成分以及含量;物质的元素组成.
考点点评: 解答此题熟练运用质量守恒定律,能设计不同的对比实验,通过控制变量来达到实验目的.1年前查看全部
- 某兴趣小组从铜器上取下绿色粉末,设计如下实验步骤进行探究铜绿的组成.
某兴趣小组从铜器上取下绿色粉末,设计如下实验步骤进行探究铜绿的组成.

(1)写出:B物质的化学式______;
(2)我国古代有“曾青得铁则化为铜”的记载,这是现代湿法冶金的原理.这与上述实验方案中第______步骤(填数字编号)相似;化学方程式为______.
(3)写出第③步反应的化学方程式是2H2O
2H2↑+O2↑通电 .2H2O.
2H2↑+O2↑通电 . MSKAOSOAS1年前1
MSKAOSOAS1年前1 -
 andy82426 共回答了25个问题
andy82426 共回答了25个问题 |采纳率92%解题思路:首先找突破口,从框图中看,B为黑色粉末,初中学过的黑色粉末有木炭、铁粉、氧化铜,E为蓝色溶液、H为红色固体,E+铁→H,推测H为Cu,B为CuO,则F、G为还原性气体,初中学过的还原性气体只有H2和CO,再根据C通电得F,推出F为H2、G为CO,进一步推出C为水,D为二氧化碳,此题即可迎刃而解.(1)E中一定含有铜离子,蓝色溶液E和铁反应生成红色固体H,则H为铜,蓝色溶液E为硫酸铜溶液,黑色粉末B和稀硫酸反应生成蓝色溶液E,则黑色粉末B为氧化铜,无色液体C在通电条件下能分解,则C为水,G和氧化铜加热能生成铜,说明G具有还原性,具有还原性的气体一般是氢气和一氧化碳,G是由D和木炭高温反应生成的,G中含有碳元素,G为一氧化碳,则D为二氧化碳;
(2)湿发冶铜的原理是Fe+CuSO4═FeSO4+Cu,所以该原理与⑤所示的反应非常相似;
(3)③为无色液体C在通电条件下能发生反应,可知无色液体C为水,化学方程式为 2H2O
通电
.
2H2↑+O2↑;
故答案为:(1)CuO;(2)⑤;Fe+CuSO4═FeSO4+Cu;(3)2H2O
通电
.
2H2↑+O2↑;点评:
本题考点: 物质的鉴别、推断;书写化学方程式、文字表达式、电离方程式.
考点点评: 根据一些物质特殊的物理或化学性质即可确定该物质,找到解答的突破点,然后根据突破点逐步确定每种物质.本题的突破点就是物质的颜色,抓住这点,即可解答.1年前查看全部
- 用什么方法可以除去铜器表面的锈
 lokoko71年前1
lokoko71年前1 -
 dsawee 共回答了13个问题
dsawee 共回答了13个问题 |采纳率84.6%1、用160克细木屑、60克化石粉,240克麦麸子和在一起倒入50克左右的醋,调成浆糊一样,涂在铜器上,风吹干后,铜锈就脱掉了.2、用超声波洗槽清洗,千万注意时间不要太长,而且要经常翻动铜镜正反面,一分钟就要翻次面.洗槽底部一般有两三个超声波发射源,当槽水有些浑浊时一定要及时更换蒸馏水,再继续清洗,否则水里的锈末会像喷砂一样击打铜器表面.3、可取一小粒草酸放在锈渍处,滴上几滴温水,轻轻揉擦,然后再用清水洗干净.注意操作要快,避免腐蚀.4、如有鲜柠檬,可榨出其汁液滴在锈渍上揉擦之,反复数次,直至锈渍除去,再用肥皂水洗净.5、用10%的醋酸液揩拭锈渍,或将沾污部分浸泡在醋酸液里,第二天再用清水漂洗干净.6、用10%的柠檬溶液或10%的草酸溶液将锈渍处润湿,然后泡入浓盐水中,第二天洗涤漂净.1年前查看全部
- (1)铜器长期暴露在空气中,表面会生成铜绿,其成分可表示为Cu2(OH)2CO3,从其组成分析,铜绿由______种元素
(1)铜器长期暴露在空气中,表面会生成铜绿,其成分可表示为Cu2(OH)2CO3,从其组成分析,铜绿由______种元素组成.
(2)写出下列化学反应的化学方程式(要注明反应条件),并在括号内填写基本反应类型.
①电解水2H2O
2H2↑+O2↑通电 .2H2O;(______)
2H2↑+O2↑通电 .
②铁在氧气中燃烧3Fe+2O2
Fe3O4点燃 .3Fe+2O2.(______)
Fe3O4点燃 . penny1011年前1
penny1011年前1 -
 ID封了998 共回答了14个问题
ID封了998 共回答了14个问题 |采纳率100%(1)由Cu、O、H、C四种元素组成;
(2)反应物是水,生成物是氢气和氧气,反应条件是通电,用观察法配平即可,由于反应物是一种,生成物是两种属于分解反应;反应物是铁和氧气,生成物是四氧化三铁,用观察法配平即可,反应条件是点燃,由于反应物为两种,生成物是一种,所以为化合反应.
故答案为:(1)④;(2)①2H2O
通电
.
2H2↑+O2↑;分解反应;②3Fe+2O2
点燃
.
Fe3O4;化合反应.1年前查看全部
- 铜器生锈和自行车爆胎 属于化学变化还是物理变化
 Tadek1年前1
Tadek1年前1 -
 不知到无知 共回答了19个问题
不知到无知 共回答了19个问题 |采纳率100%铜器生锈属于化学变化
自行车爆胎属于物理变化1年前查看全部
- 铜器长期暴露在空气中会生成铜绿(俗称铜锈).为探究铜锈的组成,小明在老师的指导下,按图装置进行实验:
 铜器长期暴露在空气中会生成铜绿(俗称铜锈).为探究铜锈的组成,小明在老师的指导下,按图装置进行实验:
铜器长期暴露在空气中会生成铜绿(俗称铜锈).为探究铜锈的组成,小明在老师的指导下,按图装置进行实验:
(1)A仪器的名称是______.
(2)实验中观察到试管壁有水珠出现,说明铜绿中含有______元素;澄清石灰水变浑浊,说明铜绿中还含有______元素,同时铜绿逐渐变黑.
思考:①在此实验装置中,大试管的管口略向下倾斜的原因是______.
②在反应完全,停止加热时,针对熄灭酒精灯和把导管移出液面这两步操作,你认为应该先进行的操作是______.
(3)从装置中取下大试管并冷却到室温,然后向大试管中加入足量的稀硫酸,充分振荡,静置后观察溶液变蓝,发生反应的化学方程式为______.据此,小明得出铜绿是由______元素组成.铜生锈可能是铜与空气中的氧气、水和______共同作用生成的.为了防止铜器在空气中锈蚀,可采取的措施是______. ww_hjd1年前1
ww_hjd1年前1 -
 clm42897 共回答了14个问题
clm42897 共回答了14个问题 |采纳率100%解题思路:(1)熟记常见仪器的名称;(2)根据质量守恒定律回答;①根据给试管内固体加热的注意事项考虑;②根据错误操作造成的后果考虑;(3)根据方程式的写法,质量守恒定律,防止生锈的方法考虑.(1)给试管加热提供热源的仪器是酒精灯;
(2)试管壁有水珠出现说明有水生成,根据质量守恒定律可知反应前后元素种类不变,所以说明铜绿中含有氢元素和氧元素;澄清石灰水变浑浊说明有二氧化碳生成,所以说明铜绿中含有碳元素;
①由于铜绿药品中含有水分,如果大试管的管口略向上倾斜时,水分受热变为水蒸气,在试管口冷凝成水滴,倒流入试管底部,使试管炸裂;
②如果先熄灭酒精灯,会因为试管内温度降低,压强减小,水会沿着导管倒吸入试管内,使试管炸裂;
(3)向大试管中加入足量的稀硫酸,发生反应的反应物是氧化铜和硫酸,生成物是硫酸铜和水;加入硫酸溶液变蓝,说明溶液中含有铜元素,所以铜绿中含有铜元素,由第(2)题中已经知道铜绿中含有碳、氢、氧元素组成,所以铜绿是由碳、氢、氧、铜四种元素组成;由于铜绿中含有碳元素,所以铜生锈必须由空气中含有碳元素的物质参加,所以二氧化碳参加了反应,防止生锈只要控制住铜生锈的条件即可;保持铜器的清洁干燥可以使铜不与水分接触、涂油可以隔绝空气,都能起到防止生锈的目的.
故答案为:(1)酒精灯;(2)氢、氧(或H、O);碳(或C);①防止冷凝水回流到试管底部,使试管炸裂;②把导管移出液面;(3)CuO+H2SO4═CuSO4+H2O;铜、氢、氧、碳;二氧化碳;保持铜器的清洁干燥、涂油等.点评:
本题考点: 实验探究物质的组成成分以及含量.
考点点评: 解答本题的关键是要根据质量守恒定律,在反应前后元素种类不变,由铜绿分解生成二氧化碳和水、氧化铜,就可以判断铜绿是由铜、氢、氧、碳四种元素组成.1年前查看全部
- (2012•南昌)铜器表面的锈斑会不断增多,橘子表面的霉斑也会不断增加.
(2012•南昌)铜器表面的锈斑会不断增多,橘子表面的霉斑也会不断增加.
(1)你认为铜锈 (属于、不属于)生物,判断的依据是______(答出一条即可);橘子上的霉______(属于、不属于)生物.
(2)显微镜下观察可见,绝大多数生物是由______构成的. 清流石1年前1
清流石1年前1 -
 香白丹 共回答了17个问题
香白丹 共回答了17个问题 |采纳率58.8%解题思路:此题考查的知识点是生物的特征,还涉及生物体的构成,分析解答.(1)、生物的特征.1、生物的生活需要营养.2、生物能够进行呼吸.3、生物能排出体内产生的废物.4、生物能够对外界刺激作出反应.5、生物能够生长和繁殖.6、除病毒外,生物都是由细胞构成的.判断是不是生物的依据是看其是否具有生物的特征,如铜锈不能呼吸,不具有生物的六大特征,不属于生物.橘子上的霉,是青霉,属于真菌,从橘子登食物上获得营养物质,并进行繁殖,具有生物的特征,属于生物.
(2)、病毒的结构简单,由蛋白质外壳和内部的遗传物质组成,没有细胞结构,所以病毒这种生物不是由细胞构成的.
除病毒外细胞是生物体结构和功能的基本单位.
故答案为:(1)不属于;锈(或生物的其他特征);属于
(2)细胞点评:
本题考点: 生物的特征.
考点点评: 解答此类题目的关键是理解生物的特征,明确除病毒外,生物体都是由细胞构成的.1年前查看全部
- 高8厘米直径2-3厘米的圆柱状铜器上面带盖,盖上有字,是什么东东?
 付雪1年前3
付雪1年前3 -
 taiketaike 共回答了15个问题
taiketaike 共回答了15个问题 |采纳率93.3%铜 的体积=15.7*8*5+3.14*3*3*24=1306.24立方厘米
则圆锥体积=1/3*3.14*8*8*高=1306.24
高=6.5厘米1年前查看全部
- (2011•海珠区一模)铜器长期暴露在空气中,表面会生成铜绿[其成分可表示为Cu2(OH)2CO3],从其组成分析,预测
(2011•海珠区一模)铜器长期暴露在空气中,表面会生成铜绿[其成分可表示为Cu2(OH)2CO3],从其组成分析,预测铜绿能与______(任举一例)反应.
 白云飞彩霞1年前1
白云飞彩霞1年前1 -
 的确良16 共回答了15个问题
的确良16 共回答了15个问题 |采纳率80%解题思路:根据铜绿的组成,猜测其化学性质;铜绿[Cu2(OH)2CO3]中含有碳酸根和氢氧根,则铜绿能与酸反应,且生成水和放出气体二氧化碳;
故答案为:HCl(或H2SO4、HNO3);点评:
本题考点: 金属锈蚀的条件及其防护;质量守恒定律及其应用.
考点点评: 碳酸盐都能与酸反应生成气体二氧化碳,与酸反应生成二氧化碳的一定含有碳酸根.1年前查看全部
- (2011•丹东)某化学兴趣小组对铜器表面生成的绿色铜锈展开如下探究,请回答有关问题.
(2011•丹东)某化学兴趣小组对铜器表面生成的绿色铜锈展开如下探究,请回答有关问题.
(1)探究铜锈的组成.
【实验过程】
实验一:
实验二:另取少量铜锈隔绝空气加热,发现绿色粉末变黑色,试管壁上有水珠.实验步骤 实验现象 实验结论 a.取少量铜锈于试管中,加入适量稀硫酸 固体溶解,产生气泡,溶液呈______色 铜锈中含有Cu2+ b.将生成气体通入______ ______ 铜锈中含有CO32-
【实验结论】综合以上两实验,可以确认铜锈中含有______种元素.
(2)探究铜生锈的条件.
【猜想】同学们对空气中有哪些物质参与了铜的生锈作出以下三种猜想:①CO2、H2O ②O2、H2O ③CO2、H2O、O2
根据铜锈的组成元素并结合铁生锈的知识,你认为上述猜想错误的是______(填序号).
【实验设计】为验证另外两种猜想,同学们设计了下图中A、B两个对比实验,请你在方框内完成实验B的设计.(语言叙述或画图说明均可)______.
【预计结论】若A中的铜生锈,B中的铜不生锈,则正确的猜想是______(填序号). 游乐儿you1年前1
游乐儿you1年前1 -
 钢铁是怎样生锈的 共回答了22个问题
钢铁是怎样生锈的 共回答了22个问题 |采纳率95.5%(1)铜锈能和稀硫酸反应生成硫酸铜、水和二氧化碳,硫酸铜溶液是蓝色的,二氧化碳能使澄清的石灰水变浑浊.故填:蓝;石灰水中;石灰水变浑浊.
由稀硫酸和铜锈反应的生成物可知,铜锈中含有铜元素和碳元素;由铜锈隔绝空气加热的生成物可知,铜锈中含有氢元素和氧元素;所以铜锈中含有铜元素、碳元素、氢元素和氧元素等4种元素.故填4.
(2)根据铜锈的组成元素并结合铁生锈的知识,你认为上述猜想错误的是②,因为②中不含有碳元素,根据质量守恒定律可知,如果是②,则铜锈中不可能含有碳元素.故填:②.
B中的实验设计为:在密封的试管中,铜片的一部分浸入蒸馏水中,另一部分只与二氧化碳充分接触.故填:在密封的试管中,铜片的一部分浸入蒸馏水中,另一部分只与二氧化碳充分接触.
若A中的铜生锈,B中的铜不生锈,说明铜生锈时需要氧气参加.故填:③.1年前查看全部
- 在潮湿环境中久置的铜器,其表面会发生锈蚀,生成铜绿,设计实验,探究铜器锈蚀的因素有哪些?【急】
 dolphin9991年前1
dolphin9991年前1 -
 咋这么矫情呢 共回答了28个问题
咋这么矫情呢 共回答了28个问题 |采纳率89.3%控制变量原理
,4个小铜片,取4根洁净试管,编号
1,只放入小铜片
2,放小铜片,上端密封
3,放小铜片,加水浸没,加一层油
,4,放小铜片,加入少量水
然后放置一段时间,观察表面锈蚀情况,对比1年前查看全部
- 铜绿的主要成分是碱式碳酸铜〔Cu2(OH)2CO3〕,它能跟酸反应生成铜盐、水和二氧化碳.某同学用小刀把家中旧铜器上的铜
铜绿的主要成分是碱式碳酸铜〔Cu2(OH)2CO3〕,它能跟酸反应生成铜盐、水和二氧化碳.某同学用小刀把家中旧铜器上的铜绿刮下,用来依次制取较纯净的硫酸铜、氧化铜和铜(为避免掺入固体杂质,他没有采用金属或碳置换化合物中的铜的方法).制取步骤分为四步.
铜绿+A→硫酸铜+B→氢氧化铜+C→氧化铜+D→铜.则ABCD是? 好奇11年前1
好奇11年前1 -
 mummyreturns 共回答了16个问题
mummyreturns 共回答了16个问题 |采纳率93.8%Cu2(OH)2CO3 + 2H2SO4 == 2CuSO4 + CO2↑ + 3H2O
A
CuSO4 + 2NaOH == Cu(OH)2↓ + Na2SO4
B
Cu(OH)2 =△= CuO + H2O 这一步什么都不用加,直接加热就行了
CuO + H2 =△= Cu + H2O
D1年前查看全部
- 纯的铜器是什么颜色?
 xuzl66661年前1
xuzl66661年前1 -
 alice00 共回答了13个问题
alice00 共回答了13个问题 |采纳率84.6%紫色1年前查看全部
- 烧开水的铜器壶底上,有凹凸不平的同心圆圈,它们能起到____作用,还能起到_____的作用
 CXM63001年前1
CXM63001年前1 -
 临门一脚差 共回答了21个问题
临门一脚差 共回答了21个问题 |采纳率100%一个是增大受热面积,加快烧水的速度,充分节约能源,另一个是增大摩擦系数,防滑的.
烧开水的铜器壶底上,有凹凸不平的同心圆圈,它们能起到__加快烧水的速度__作用,还能起到___防滑__的作用1年前查看全部
- 下列过程中,没有发生化学变化的是( ) A.醋除水垢 B.粮食酿酒 C.金块抽丝 D.铜器锈蚀
 清风掠颖1年前1
清风掠颖1年前1 -
 江67 共回答了17个问题
江67 共回答了17个问题 |采纳率94.1%A、用醋酸清洗水垢的过程中水垢的主要成分碳酸钙和醋酸反应有新物质二氧化碳等生成,属于化学变化;
B、粮食酿酒的过程中有新物质酒精等生成,属于化学变化;
C、金块抽丝的过程中只是物质的形状发生了改变,没有新物质生成,属于物理变化;
D、铜器锈蚀过程中有新物质铜锈生成,属于化学变化.
故选C.1年前查看全部
- 下列生活经验中,正确的是( ) A.用石灰水刷洗坐便池 B.用棉纱球蘸取食醋擦拭铜器上的铜绿 C.等体积的热水比凉水溶
下列生活经验中,正确的是( ) A.用石灰水刷洗坐便池 B.用棉纱球蘸取食醋擦拭铜器上的铜绿 C.等体积的热水比凉水溶解食盐的量要大得多 D.家里冰箱中有异味时,可以放一块烧过的蜂窝煤除臭  wCzm1片留在1年前1
wCzm1片留在1年前1 -
 黑衣魔笛手 共回答了23个问题
黑衣魔笛手 共回答了23个问题 |采纳率91.3%A、石灰水显碱性,不能用于洗刷便池,故A错误;
B、铜锈能与醋酸反应,可以使用食醋洗去铜器上的铜绿,故B正确;
C、食盐的溶解度受温度影响变化不大,所以同体积的热水比凉水溶解的食盐的量不会大很多,故C错误;
D、烧过的蜂窝煤具有吸附性,能吸附异味,故D正确;
故选BD.1年前查看全部
- 除去铜器表面的氧化物用什么1.稀硝酸2.浓硝酸3.稀硫酸4.浓硫酸
 wyjoo11年前4
wyjoo11年前4 -
 互相拥抱美好时光 共回答了18个问题
互相拥抱美好时光 共回答了18个问题 |采纳率94.4%3 稀硫酸
其他1 2 4答案的酸都具有强氧化性会与铜发生反应,而稀硫酸只跟铜表面的氧化物氧化铜发生反应,与铜不发生反应1年前查看全部
- 为什么铜器的锈是绿色的那
 jsxzsp1年前1
jsxzsp1年前1 -
 yy最高 共回答了17个问题
yy最高 共回答了17个问题 |采纳率88.2%铜与空气中的氧气、二氧化碳和水等物质反应产生的物质,又称铜锈(铜绿).化学式为Cu2(OH)2CO3,又名孔雀石(主要成分是Cu2(OH)2CO3,非纯净物),是一种名贵的矿物宝石,属于碱式碳酸盐,是盐的一种.1年前查看全部
- 铜器长时间露置在潮湿的空气里,表面都会有一层绿色的物质,俗称铜绿,化学名称:碱式碳酸铜[Cu2( OH
铜器长时间露置在潮湿的空气里,表面都会有一层绿色的物质,俗称铜绿,化学名称:碱式碳酸铜[Cu2( OH )2 CO3].请完成下列问题.
(1)根据其化学式,得出铜生锈可能是铜与空气中的氧气、水和______共同反应的结果.
【问题探究】
研究小组欲探究一表面生锈的铜片中铜绿的质量分数,称取该样品10.0g放入D中进行如图实验:
【查阅资料】
1.铜绿不稳定,加热时易分解成三种氧化物.
2.C、E、F中装有碱石灰(CaO与NaOH的固体混合物),碱石灰可以用来吸收二氧化碳和水蒸气;
3.B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭,推拉注射器的作用是鼓入空气.
【实验步骤】
①组装好装置
②反复推拉注射器
③称量E的质量
④关闭弹簧夹,加热D处试管直到反应不再进行
⑤打开弹簧夹,再次反复缓缓推拉注射器
⑥再次称量E的质量.
【实验分析】
(2)写出D装置中发生的两个化学方程式
①铜绿受热分解的化学方程式Cu2(OH)2CO3
2CuO+H2O+CO2↑△ .Cu2(OH)2CO3,绿色粉末逐渐变为______色.
2CuO+H2O+CO2↑△ .
②铜加热2Cu+O2
2CuO△ .2Cu+O2.
2CuO△ .
(3)在操作①中,同学们一致认为缺少了一个重要步骤,在实验前应先______.
(4)C的作用是______,F的作用是______.
(5)步骤⑤的作用是______.若不进行步骤⑤的操作,则所测得的铜绿的质量分数______(填“偏大”、“偏小”、“无影响”).
【定量计算】
(6)反应结束后,测得E装置的质量增加了0.62g,则铜绿在样品中所占质量分数为______.
【实验反思】
(7)小明同学提出可以通过测D装置反应后的质量的减少即为反应生成的水和二氧化碳来计算,同学们经过思考否定了这种方案,理由是______.
【实验再探究】
【查阅资料】
1.铜绿可与稀硫酸反应生成硫酸铜、水以及一种能使石灰水变浑浊的气体.
2.含有硫酸根离子的化合物溶液与氯化钡溶液反应会产生白色沉淀.
【实验方案】
取10g表面生锈的铜样品,加入稍过量的稀硫酸,充分反应后过滤,洗涤,干燥,称得滤渣的质量即为铜的质量.
(8)写出铜绿与硫酸反应的化学方程式______.
(9)证明所加稀硫酸过量的现象是______,滤液中含有的溶质有______和______.
(10)判断滤渣铜已洗涤干净的操作方法及现象是______. gsblues1年前1
gsblues1年前1 -
 但使主人能醉客 共回答了20个问题
但使主人能醉客 共回答了20个问题 |采纳率85%解题思路:(1)根据碱式碳酸铜化学式和质量守恒定律,推测;
(2)根据反应物、反应条件、生成物,可以书写铜绿受热分解和铜加热的化学方程式;
(3)有气体参与反应或需要气体反应的装置,都必须检查装置气密性;
(4)利用碱石灰的作用回答;
(5)打开弹簧夹,再次反复缓缓推拉注射器,即让生成的二氧化碳和水充分被E吸收;
(6)反应结束后,测得E装置的质量增加了0.62g,则可知二氧化碳和水的质量,则可求铜绿在样品中所占质量分数.
(7)知道:E装置增加的质量即为反应生成的水和二氧化碳.
(8)根据资料“铜绿可与稀硫酸反应生成硫酸铜、水以及一种能使石灰水变浑浊的气体”,则可知铜绿与硫酸反应的化学方程式.
(9)根据资料“含有硫酸根离子的化合物溶液与氯化钡溶液反应会产生白色沉淀”,则可证明所加稀硫酸是否过量;
(10)利用称量E装置的质量是否增加,判断滤渣铜已洗涤干净.(1)根据碱式碳酸铜化学式[Cu2( OH )2 CO3]和质量守恒定律,则得出铜生锈可能是铜与空气中的氧气、水和 二氧化碳共同反应的结果.
【实验分析】
(2)①根据反应物、反应条件、生成物,可以书写铜绿受热分解的化学方程式 Cu2(OH)2CO3
△
.
2CuO+H2O+CO2↑,绿色粉末逐渐变为 黑色.
②根据反应物、反应条件、生成物,可以书写铜加热的化学方程式 2Cu+O2
△
.
2CuO.
(3)在操作①中,实验前应先 检查装置的气密性.
(4)根据“碱石灰(CaO与NaOH的固体混合物),碱石灰可以用来吸收二氧化碳和水蒸气”,则可推测C的作用是 吸收二氧化碳和水蒸气,F的作用是 防止空气中的二氧化碳和水蒸气等杂质气体进入到E,影响二氧化碳和水分质量的测定.
(5)步骤⑤该操作中推注射器时缓缓的目的是使生成的二氧化碳、水蒸气吸收充分.若不进行步骤⑤的操作,生成的二氧化碳和水不能被充分吸收,使得结果偏小.故填:偏小.
(6)反应结束后,测得E装置的质量增加了0.62g,则二氧化碳和水的质量为0.62g,则碱式碳酸铜的质量为2.22g,故样品中所占质量分数为[2.22g/10.0g×100%=22.2%.
(7)小明同学提出可以通过测D装置反应后的质量的减少即为反应生成的水和二氧化碳来计算,同学们经过思考否定了这种方案,理由是 E装置增加的质量即为反应生成的水和二氧化碳.
(8)根据资料“铜绿可与稀硫酸反应生成硫酸铜、水以及一种能使石灰水变浑浊的气体”,则可写出铜绿与硫酸反应的化学方程式 Cu2(OH)2CO3 +2H2SO4=2CuSO4+3H2O+CO2↑.
(9)根据资料“含有硫酸根离子的化合物溶液与氯化钡溶液反应会产生白色沉淀”,则可证明所加稀硫酸过量的现象是 与氯化钡溶液反应会产生白色沉淀,滤液中含有的溶质有 氯化氢和 硫酸铜.
(10)判断滤渣铜已洗涤干净的操作方法及现象是 称量E装置的质量不再增加.
故答案为:(1)二氧化碳;
(2)①Cu2(OH)2CO3
△
.
]2CuO+H2O+CO2↑,黑.②2Cu+O2
△
.
2CuO.
(3)检查装置的气密性.
(4)吸收二氧化碳和水蒸气,防止空气中的二氧化碳和水蒸气等杂质气体进入到E,影响二氧化碳和水分质量的测定.
(5)使碱石灰充分吸收二氧化碳和水蒸气.偏小
(6)22.2%.
(7)E装置增加的质量即为反应生成的水和二氧化碳.
(8)Cu2(OH)2CO3 +2H2SO4=2CuSO4+3H2O+CO2↑.
(9)与氯化钡溶液反应会产生白色沉淀,氯化氢和 硫酸铜.
(10)称量E装置的质量不再增加点评:
本题考点: 实验探究物质的组成成分以及含量;常见气体的检验与除杂方法;酸的化学性质;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题的关键是要充分理解物质的性质和实验目的,只有这样才能对问题做出正确的判断.1年前查看全部
- 请问如何在原有的铜器上再镀一层铜?
 星星蓝孩1年前1
星星蓝孩1年前1 -
 techiel 共回答了20个问题
techiel 共回答了20个问题 |采纳率90%其实你的问题和在Fe上镀铜啊 镀金是一个原理
使用一个电解池 铜器放在阴极 阳极放电别的铜件(废铜也可以)
电解池溶液时你就是用硫酸铜吧
然后通电开始操作就OK拉
要是我回答的不是你说的意思 或者有疑问请Hi我 哟1年前查看全部
- 古文铜器易书是什么意思
 rbr20041年前1
rbr20041年前1 -
 897747 共回答了16个问题
897747 共回答了16个问题 |采纳率100%有一士人尽掊其家所有约百余千鬻书,将以入京.至中途,遇一士人,取书目阅之,爱其书而贫,不能得.家有数古铜器,将以货之.而鬻书者雅有好古器之癖,一见喜甚,乃曰:‘毋庸货也,我将与汝估其直而两易之.’于是尽以随行之书换数十铜器,亟返其家.
译文:
有一读书人敛聚尽家中所的物品约有一千几百文钱用来买书,把书带着进京.到达中途,遇到一个同样的读书人,拿着他的书目看了看,喜爱他的书却因为自己贫穷,不能获得.家中有几十个古铜器,拿来卖了(买书).买书的有雅癖喜爱收集古器.一看到古器很是高兴,于是就说:“不要卖了,我把这些书赐予你,估计一下价钱,两个人交换它们(书与古器).就这样,买书的用尽随带的书,换取了几十个铜器,急忙返回他的家中去了.1年前查看全部
- 铜器在潮湿的空气中,表面会慢慢地生成一层铜锈[Cu2(OH)2CO3].该反应的化学方程式为:______.
 阆苑胜事可断肠1年前1
阆苑胜事可断肠1年前1 -
 pigu911 共回答了17个问题
pigu911 共回答了17个问题 |采纳率94.1%解题思路:根据所学知识结合质量守恒定律,来判断反应物和生成物,并正确地书写化学方程式.在潮湿的空气中,铜可以和水、氧气、二氧化碳等物质反应生成碱式碳酸铜,反应的化学方程式为:2Cu+H2O+CO2+O2═Cu2(OH)2CO3.
故答案为:2Cu+H2O+CO2+O2═Cu2(OH)2CO3.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题要正确的书写反应物和生成物的化学式,同时书写化学方程式时要遵循质量守恒定律,注意化学方程式的配平.1年前查看全部
- 某兴趣小组从铜器上取下绿色粉未,设计如下实验步骤探究铜绿的组成。 (1)推断B、C、H是何种物质,写出它们的化学式:B
某兴趣小组从铜器上取下绿色粉未,设计如下实验步骤探究铜绿的组成。 
(1)推断B、C、H是何种物质,写出它们的化学式:B __________ ;C_________;H__________。
(2)从图中转化关系可以初步判断,铜绿的组成元素有 ________________________ 。
(3)图中第②步反应的化学方程式是 ____________________________ 。
(4)图中第⑤步反应的化学方程式是 ____________________________ 。 王大炮1年前1
王大炮1年前1 -
 b311 共回答了16个问题
b311 共回答了16个问题 |采纳率87.5%1年前查看全部
- 铜绿的主要成分是碱式碳酸铜〔Cu2(OH)2CO3〕,它能跟酸反应生成铜盐、水和二氧化碳.某同学用小刀把家中旧铜器上的铜
铜绿的主要成分是碱式碳酸铜〔Cu2(OH)2CO3〕,它能跟酸反应生成铜盐、水和二氧化碳.某同学用小刀把家中旧铜器上的铜绿刮下,用来依次制取较纯净的硫酸铜、氧化铜和铜(为避免掺入固体杂质,他没有采用金属或碳置换化合物中的铜的方法).制取步骤分为四步:
(1)填写下面表示制取步骤和方法的方框图(方框内填写所制取物质的化学式,方框前的横线上填写所加入的试剂及简要操作).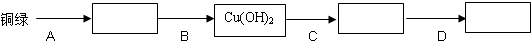
(2)根据上面的操作步骤,在下列所示仪器中选择实验所需用的仪器编号和名称______.
(3)写出A、C操作过程中涉及的反应的化学方程式______、Cu(OH)2
CuO+H2O△ .Cu(OH)2.
CuO+H2O△ .
(4)如果实验装置及生成铜以前的操作都正确,但最后没有生成铜,这是因为______. 八班精英1年前1
八班精英1年前1 -
 1231232007 共回答了26个问题
1231232007 共回答了26个问题 |采纳率92.3%解题思路:利用题设信息“铜绿的主要成分是碱式碳酸铜,它能跟酸反应生成铜盐、水和二氧化碳”,可推断为得到硫酸铜应使碱式碳酸铜与硫酸反应,然后利用硫酸铜与氢氧化钠反应得到氢氧化铜的沉淀,再对不溶性的碱氢氧化铜进行加热分解产生氧化铜,最后利用具有还原性的氢气在加热条件下还原氧化铜,从而避免掺入固体杂质得到较为纯净的铜.(1)把铜绿与稀硫酸混合充分反应后过滤得到硫酸铜溶液,向所得硫酸铜溶液中滴加氢氧化钠溶液至沉淀不再产生时过滤,把过滤得到的氢氧化铜沉淀进行加热分解得到氧化铜,最后利用氢气在加热条件下还原氧化铜即可达到获得不含固体杂质铜的制取目的;
(2)取铜绿于烧杯中,加入适量稀硫酸用玻璃棒搅拌,充分反应后过滤,向过滤所的硫酸铜溶液中加入氢氧化钠溶液并不断搅拌;完成以上操作需要使用漏斗、烧杯、玻璃棒、滴管、铁架参(带铁圈)等仪器;把过滤得到的氢氧化铜沉淀放在试管中加热,全部全黑色,通入氢气进行还原直到全部变为光亮的红色的铜;完成以上操作需要使用酒精灯、试管、氢氢气的玻璃导管、铁架台(带铁夹)等仪器.因此完成该实验需要使用的仪器为:(1)试管、(3)烧杯、(4)酒精灯、(5)通氢气的玻璃导管、(6)漏斗、(7)滴管、(9)铁架台(带铁圈和铁夹)、⑽玻璃棒;
(3)操作A加入稀硫酸,硫酸与碱式碳酸铜反应可生成硫酸铜、水和二氧化碳,反应的化学方程式为Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑;操作C为对氢氧化铜加热,氢氧化铜受热分解生成氧化铜和水,反应的化学方程式为Cu(OH)2
△
.
CuO+H2O;
(4)由于铜在高温下能与氧气发生反应生成氧化铜,因此在铜未冷却便停止通氢气,则会导致还原出的铜又被氧化成氧化铜,出现实验装置及生成铜以前的操作都正确,但最后没有生成铜的意外结果.
故答案为:
(1)铜绿
稀硫酸
搅拌过滤CuSO4
NaOH溶液
搅拌过滤Cu(OH)2
△
CuO
H2
△Cu;
(2)选出的仪器:(1)试管、(3)烧杯、(4)酒精灯、(5)通氢气的玻璃导管、(6)漏斗、(7)滴管、(9)铁架台(带铁圈和铁夹)、⑽玻璃棒;
(3)Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑;Cu(OH)2
△
.
CuO+H2O;
(4)铜未冷却便停止通氢气,结果铜又被氧化成氧化铜.点评:
本题考点: 物质的相互转化和制备;常用仪器的名称和选用;书写化学方程式、文字表达式、电离方程式.
考点点评: 利用所涉及物质的性质、变化规律及实验的具体要求,分析制取流程以理解所设计的实验过程,从而解答实验中所涉及的相关问题.1年前查看全部
- 铜器表面容易生成一层薄薄的铜绿[主要成分是Cu2(OH)2CO3],请写出铜在潮湿的空气
铜器表面容易生成一层薄薄的铜绿[主要成分是cu2(oh)2co3],请写出铜在潮湿的空气
发生电化学腐蚀时的负极反应式
用***除去铜器表面的铜绿,该反应的化学方程式为 香香宝宝1年前2
香香宝宝1年前2 -
 最爱思远1 共回答了20个问题
最爱思远1 共回答了20个问题 |采纳率90%正极:Cu-2e=(Cu2+)
负极:2(H+)+O2+4e=2(OH-)
总反应:CO2+H2O+O2+2Cu=Cu2(OH)2CO3
Cu2(OH)2CO3+5HCl=2CuCl2+3H2O+CO2↑1年前查看全部
- 铜器在潮湿的空气中,表面会慢慢地生成一层铜锈[Cu2(OH)2CO3].该反应的化学方程式为:______.
 雨夜留香1年前2
雨夜留香1年前2 -
 可漂小熊猪猫猫 共回答了25个问题
可漂小熊猪猫猫 共回答了25个问题 |采纳率92%解题思路:根据所学知识结合质量守恒定律,来判断反应物和生成物,并正确地书写化学方程式.在潮湿的空气中,铜可以和水、氧气、二氧化碳等物质反应生成碱式碳酸铜,反应的化学方程式为:2Cu+H2O+CO2+O2═Cu2(OH)2CO3.
故答案为:2Cu+H2O+CO2+O2═Cu2(OH)2CO3.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题要正确的书写反应物和生成物的化学式,同时书写化学方程式时要遵循质量守恒定律,注意化学方程式的配平.1年前查看全部
- (6分)某兴趣小组从铜器上取下绿色粉末,设计如下实验步骤进行探究铜绿的组成。
(6分)某兴趣小组从铜器上取下绿色粉末,设计如下实验步骤进行探究铜绿的组成。

⑴写出:B物质的化学式 ;铜绿的组成元素 。
⑵我国古代有“曾青得铁则化为铜”的记载,这是现代湿法冶金的原理。这与上述实验方案中第 步骤(填数字编号)相似;化学方程式为 。
⑶写出第③步反应的化学方程式是 。
⑷在设计方案中有⑤⑥⑦三种冶炼铜的方法,通过比较请从资源、能源或环境等方面,说出其中一种方案所具有的优点: 。 emperorofsh1年前1
emperorofsh1年前1 -
 wbw0710 共回答了13个问题
wbw0710 共回答了13个问题 |采纳率100%1年前查看全部
- (2007•六合区模拟)某兴趣小组从铜器上取下绿色粉未,设计如下实验步骤进行探究铜绿的组成.
(2007•六合区模拟)某兴趣小组从铜器上取下绿色粉未,设计如下实验步骤进行探究铜绿的组成.

(1)写出:B物质的化学式CuOCuO;铜绿的组成元素Cu、H、O、CCu、H、O、C.
(2)我国古代有“曾青得铁则化为铜”的记载,这是现代湿法冶金的原理.这与上述实验方案中第⑤⑤步骤相似;化学方程式为Fe+CuSo4=FeSO4+CuFe+CuSo4=FeSO4+Cu.
(3)写出第③步反应的化学方程式是2H2O
2H2↑+O2↑2H2O通电 .
2H2↑+O2↑.通电 .
(4)在设计方案中有三种冶炼铜的方法,通过比较请从资源、能源或环境等方面,说出其中一种方案所具有的优点:用铁和硫酸铜反应的方法冶炼铜操作简单,不需加热(其他合理答案可给分)用铁和硫酸铜反应的方法冶炼铜操作简单,不需加热(其他合理答案可给分). huihui05041年前1
huihui05041年前1 -
 biypm810 共回答了26个问题
biypm810 共回答了26个问题 |采纳率96.2%解题思路:E为蓝色溶液,E中一定含有有铜离子,B为黑色粉末,和稀硫酸反应生成E,可知B为氧化铜,E为硫酸铜,E和铁反应生成红色固体H,H为铜,C 在通电条件下可分解,则C为水,水通电生成的气体F和氧化铜加热生成铜,说明F具有还原性,则F为氢气.G和氧化铜加热生成铜,说明G具有还原性,具有还原性的气体主要是氢气和一氧化碳,G是由无色气体D和木炭高温反应生成的,G中含有碳元素,则G为一氧化碳,D为二氧化碳.(1)黑色粉末B和稀硫酸反应生成蓝色溶液E,E中一定含有铜离子,则黑色粉末B为氧化铜,蓝色溶液E为硫酸铜溶液,硫酸铜和铁反应生成红色固体H,则H为铜,无色液体C在通电条件下能分解,则C为水,G和氧化铜加热能生成铜,说明G具有还原性,具有还原性的气体一般是氢气和一氧化碳,G是由D和木炭高温反应生成的,G中含有碳元素,G为一氧化碳,则D为二氧化碳,根据化学反应前后元素的种类不变可知铜绿的组成元素为 Cu O C H
故选CuO Cu、O、C、H
(2)湿发冶金术的原理是Fe+CuSo4=FeSO4+Cu,故答案为:⑤Fe+CuSo4=FeSO4+Cu
(3)无色液体C在通电条件下能发生反应,可知无色液体C为水,故答案为:2H2O
通电
.
2H2↑+O2↑
(4)一般不加热,操作简便,污染少,节约能源的方案为好的方案,故答案为:用铁和硫酸铜反应的方法冶炼铜操作简单,不需加热.点评:
本题考点: 实验探究物质的组成成分以及含量;常见金属的冶炼方法;物质的元素组成;化学式的书写及意义;反应现象和本质的联系;书写化学方程式、文字表达式、电离方程式.
考点点评: 解本类型题的关键是根据明显现象找到突破点,然后根据突破点逐步确定每种物质.1年前查看全部
- 某兴趣小组从铜器上取下绿色粉未,设计如下实验步骤探究铜绿的组成. (1)推断B、C是何种物质,写出它们的化学式:B __
某兴趣小组从铜器上取下绿色粉未,设计如下实验步骤探究铜绿的组成. 
(1)推断B、C是何种物质,写出它们的化学式:B _________ ;C _________ .
(2)从图中转化关系可以初步判断,铜绿的组成元素有 _________ .
(3)图中第③步反应的化学方程式是 _________ .
(4)图中第⑤步反应的化学方程式是 _________ . totti4921年前1
totti4921年前1 -
 梦幻晶莹1213 共回答了20个问题
梦幻晶莹1213 共回答了20个问题 |采纳率95%1年前查看全部
- 考古发掘出铜器表面有一沉厚厚的铜绿 试用化学方程式解释铜绿形成的原因
 wszgr000011年前1
wszgr000011年前1 -
 danielchi 共回答了18个问题
danielchi 共回答了18个问题 |采纳率94.4%在潮湿的空气中,与空气中的水,二氧化碳和氧气发生一连串的复杂的化学反应,最终形成的
2Cu+H2O+CO2+O2=Cu2(OH)2CO31年前查看全部
- 钢铁生锈 铜器生锈 氢氧化钠固体潮解变质 二氧化硫形成酸雨 这4个化学式怎么写
钢铁生锈 铜器生锈 氢氧化钠固体潮解变质 二氧化硫形成酸雨 这4个化学式怎么写
急用 wandge1年前1
wandge1年前1 -
 火星毛毛 共回答了18个问题
火星毛毛 共回答了18个问题 |采纳率100%2so2+o2=2so3 so3+h2o=h2so4
氢氧化钠固体潮解变质没有方程式的
2cu+co2+o2+h2o=cu2(oh)2co31年前查看全部
- 一个圆锥铜器,底面直径为6cm,高为3cm,它的体积是多少立方厘米?
一个圆锥铜器,底面直径为6cm,高为3cm,它的体积是多少立方厘米?
如果每立方厘米铜重8.9克,这个铜重多少千克? 传媒骄子1年前2
传媒骄子1年前2 -
 沧海升龙 共回答了21个问题
沧海升龙 共回答了21个问题 |采纳率90.5%体积=3×3×3.14×3×1/3=28.26立方厘米
质量=28.26×8.9=251.514克=0.251514千克1年前查看全部
- 中国是一个文明古国,在考古中有大量的出土金属文物,发现其中铜器年代较铁器久远
中国是一个文明古国,在考古中有大量的出土金属文物,发现其中铜器年代较铁器久远
且留存数量也较多.有同学认为这也能证明铁的金属活动性比铜强.你是否同意这种看法.理由. suyang06061年前1
suyang06061年前1 -
 心碎迷惘 共回答了23个问题
心碎迷惘 共回答了23个问题 |采纳率95.7%同意,炼铁不易被掌握,铜较容易被提炼加工,且较铁更以保存1年前查看全部
- 1.酒精挥发 2.汽油能燃烧3.铜器生锈4.二氧化硫具有刺激性气味5.植物的光合作用6.水冻冰
1.酒精挥发 2.汽油能燃烧3.铜器生锈4.二氧化硫具有刺激性气味5.植物的光合作用6.水冻冰
物理变化-------
化学变化-------
物理性质-------
化学性质------- cpp44711年前3
cpp44711年前3 -
 bclzscxs 共回答了21个问题
bclzscxs 共回答了21个问题 |采纳率81%物理变化-------酒精挥发,水冻冰
化学变化-------汽油能燃烧,铜器生锈,植物的光合作用
物理性质-------二氧化硫具有刺激性气味
化学性质-------1年前查看全部
- 归纳出商朝铜器工艺精湛的表现.
 娇喘息息1年前2
娇喘息息1年前2 -
 CNN_CEO 共回答了22个问题
CNN_CEO 共回答了22个问题 |采纳率86.4%品种齐全,样式精美,数量大,做工精细,主要用来祭祀和日常用品,代表作有四羊方尊和司母戊鼎.1年前查看全部
- 请问这个铜器是什么年代的?请问价值几何?香炉底部写有“官”字样,不过我看着也像“宣”.请专家鉴定...
请问这个铜器是什么年代的?请问价值几何?香炉底部写有“官”字样,不过我看着也像“宣”.请专家鉴定...
香炉底部写有“官”字样,不过我看着也像“宣”.请专家鉴定.

 钟河1年前1
钟河1年前1 -
 清风和舞 共回答了16个问题
清风和舞 共回答了16个问题 |采纳率93.8%此款为清早、中期仿明兽耳宣德炉,根据图片看,包浆厚实,如果有底款照片可能判断更加准确一些了,估价1500-4000之间,值得收藏!1年前查看全部
大家在问
- 1有一个等腰直角三角形,它的最长边边长为6厘米,这个三角形的面积是多少平方厘米?
- 224克不纯的氧化铁(杂质中不含铁元素)跟足量的一氧化碳在高温下反应后,得到11.2克铁.求原混合物中氧化铁的质量分数(精
- 3在试管前口通入C0到试管中与铁触媒反应,试管后口装置一个含碱石灰的干燥管B,称取 15.2g 铁触媒进行上述实验.充分反
- 4贾平凹的《月迹》中第35节中“那月亮不是我们按在天空中的印章吗?”这句话的理解?
- 5有一个棱形金砖,它的底是一个梯形,它的梯形的上底是5cm,下底是7cm,高是3cm,整个棱形高9cm.(a)求它的体积.
- 6已知函数f(x)=a的次方减2分之5a加3为增函数且f(2)=2.(1)求函数解析式,(2)证明函
- 7We must ____ ____ _____ ______(保持身体健康)
- 8假如地球3天没有太阳光,一片黑暗,二氧化碳量增加,人类能撑过三天么
- 9检验氧气,氮气,二氧化碳,空气应该用燃着的木条还是带火星的木条?
- 10木条在空气中和氧气中燃烧,火焰分别为什么颜色?
- 11观看【茅屋为秋风所破歌】和【观刈麦】这两首古诗回答下列问题.
- 12提示语在前面时用什么标点符号
- 13已知集合M={x|x2-4>0},N={x∈Z|x2-6x+13a-4
- 14成语,什么.什么教什么
- 15求曲线4x^2+y^2-4x+2y-8=0在y轴上截得的线段长




