无水乙酸又称冰醋酸(熔点16.6℃).在室温较低时,无水乙酸就会凝结成像冰一样的晶体.请简单说明在实验中若遇到这种情况时
 华能电厂2022-10-04 11:39:542条回答
华能电厂2022-10-04 11:39:542条回答
已提交,审核后显示!提交回复
共2条回复
 大聪 共回答了24个问题
大聪 共回答了24个问题 |采纳率91.7%- 解题思路:根据“冰醋酸(熔点16.6℃)”的特点(在室温较低时,无水乙酸就会凝结成像冰一样的晶体),只要使冰醋酸的温度稍微高于室温,它就会变成液态可以取出;只要把试剂瓶带到高于16.6℃的地方即可,当然方法多种.
因为冰醋酸的熔点16.6℃,所以可以把试剂瓶带到大于16.6℃的地方或者水浴稍微加热或者用热毛巾捂热等等
故正确答案:水浴微热、用热毛巾热敷、将试剂瓶拿到高于16.6℃的房间内等等点评:
本题考点: 混合物的分离方法;固体溶解度的影响因素.
考点点评: 本题是一道开放性的实验设计题,难度不是很大,考查了学生根据物质的特点,解决实际问题的能力. - 1年前
 luoxiangyang 共回答了79个问题
luoxiangyang 共回答了79个问题 |采纳率- ...加热一下
- 1年前
相关推荐
- 无水乙醇又称冰醋酸(熔点16.6|摄氏度).在温度较低时,无水乙酸就会凝结成像冰一样的晶体.在试验中若遇到这种情况时.将
无水乙醇又称冰醋酸(熔点16.6|摄氏度).在温度较低时,无水乙酸就会凝结成像冰一样的晶体.在试验中若遇到这种情况时.将如何从试剂瓶中取出
 黑电脑1年前6
黑电脑1年前6 -
 wangying16 共回答了9个问题
wangying16 共回答了9个问题 |采纳率88.9%将试剂瓶放入温水中,待试剂可以流动时,再取出
(我们做实验时,遇到试剂凝结了,就是这样处理的)1年前查看全部
- (1)无水乙酸又称冰醋酸(熔点16.6℃).在室温较低时,无水乙酸就会凝结成像冰一样的晶体.请简单说明在实验中若遇到这种
(1)无水乙酸又称冰醋酸(熔点16.6℃).在室温较低时,无水乙酸就会凝结成像冰一样的晶体.请简单说明在实验中若遇到这种情况时,你将如何从试剂瓶中取出无水乙酸?______
(2)某有机物的结构简式为HOOC-CH=CHOH.
①请你写出该有机物官能团的名称:______、______、______.
②验证该有机物中含有-COOH官能团常采用的方法是______,产生的现象为______. yangzhen52771年前1
yangzhen52771年前1 -
 nn见客 共回答了15个问题
nn见客 共回答了15个问题 |采纳率86.7%解题思路:(1)根据“冰醋酸(熔点16.6℃)”的特点(在室温较低时,无水乙酸就会凝结成像冰一样的晶体),只要使冰醋酸的温度稍微高于室温,它就会变成液态可以取出;只要把试剂瓶带到高于16.6℃的地方即可,当然方法多种;
(2)①根据有机物的结构特点判断有机物含有的官能团;
②羧基具有酸的通性:使石蕊试液变红、能和碳酸钠反应生成二氧化碳等等.(1)因为冰醋酸的熔点16.6℃,所以可以把试剂瓶带到大于16.6℃的地方或者水浴稍微加热或者用热毛巾捂热等,
故答案为:水浴微热、用热毛巾热敷、将试剂瓶拿到高于16.6℃的房间内等;
(2)①根据有机物的结构简式可知,该有机物含有羟基、羧基、碳碳双键三种官能团,故答案为:羟基;羧基;碳碳双键.
②羧基具有酸的通性,能使石蕊试液变红,能和碳酸钠反应生成二氧化碳等,所以可用碳酸钠溶液或石蕊试液验证.
故答案为:用该物质和碳酸钠溶液反应是否有气泡生成或能否使石蕊试液变红;产生气泡或变红.点评:
本题考点: 有机物的结构和性质;有机物分子中的官能团及其结构.
考点点评: 本题考查了官能团的判断、物质的性质等知识点,难度不大,结构决定性质,性质体现结构,熟记官能团的性质是解题的关键.1年前查看全部
- 乙酸的挥发性?为什么无水乙酸叫冰醋酸?
 广东小曾1年前1
广东小曾1年前1 -
 CHITRON 共回答了18个问题
CHITRON 共回答了18个问题 |采纳率88.9%(1)乙酸的挥发性较强 但相同条件下乙醇的挥发性比乙酸强
(2)凝固点为 16.635℃ 所以低于这个温度纯净的醋酸就会凝结成冰状晶体 和冰很相似
所以无水乙酸可以叫冰醋酸1年前查看全部
- 固体醋酸叫做冰醋酸,我看冰醋酸的定义是无水乙酸啊.
 微薇小蓝1年前5
微薇小蓝1年前5 -
 靓女终结者 共回答了18个问题
靓女终结者 共回答了18个问题 |采纳率100%冰醋酸是乙酸的俗名
乙酸是有机化学里的属于羧酸类
凝固点很低一般在16 °C 就凝固成固体 成为冰醋酸
而固体醋酸主要成分为醋酸 可能还有别的杂质
所以不能笼统的说1年前查看全部
- 乙酸酐和冰醋酸、无水乙酸、醋酸一样吗?几个之间有什么关系?
 幽雅的表子1年前1
幽雅的表子1年前1 -
 小红红红 共回答了14个问题
小红红红 共回答了14个问题 |采纳率92.9%首先,乙酸酐是两分子乙酸脱去一分子水而形成的酸酐,而无水乙酸如果在略低于室温的温度下即16.7℃,就能够转化为一种冰状晶体,故在实际中无水醋酸称为冰醋酸,比如化学试剂店里卖的分析纯规格的醋酸是为冰醋酸,但还是没有达到绝对的无水!醋酸就是我们平常说的乙酸的别名咯,呵呵,希望你能明白1年前查看全部
- 甲醛与格氏试剂反应的条件是什么是无水乙醚还是无水乙酸
 梁山伯OL1年前1
梁山伯OL1年前1 -
 mytheone 共回答了17个问题
mytheone 共回答了17个问题 |采纳率100%乙醚
记得格氏试剂在乙醚里才可以作用1年前查看全部
- 纯冰醋酸和氢氧化钠能反应吗?RT,注意,是无水乙酸跟氢氧化钠反应!
 yqysy1年前1
yqysy1年前1 -
 llgq7412 共回答了22个问题
llgq7412 共回答了22个问题 |采纳率81.8%我认为不可以.虽然这个反应生成水,但绝对无水的环境,不考虑氢氧化钠自动受潮吸水,它不能电离哪怕一个分子!
没有溶液,根本不能电离,那么这个分子的离子键会很强大,醋酸本来就是弱酸,更是如此,所以不能反映1年前查看全部
- (1)无水乙酸又称冰醋酸(熔点16.6℃).在室温较低时,无水乙酸就会凝结成像冰一样的晶体.请简单说明在实验中若遇到这种
(1)无水乙酸又称冰醋酸(熔点16.6℃).在室温较低时,无水乙酸就会凝结成像冰一样的晶体.请简单说明在实验中若遇到这种情况时,你将如何从试剂瓶中取出无水乙酸?______
(2)某有机物的结构简式为HOOC-CH=CHOH.
①请你写出该有机物官能团的名称:______、______、______.
②验证该有机物中含有-COOH官能团常采用的方法是______,产生的现象为______. 面包补丁1年前1
面包补丁1年前1 -
 linzeqiuzi 共回答了20个问题
linzeqiuzi 共回答了20个问题 |采纳率90%解题思路:(1)根据“冰醋酸(熔点16.6℃)”的特点(在室温较低时,无水乙酸就会凝结成像冰一样的晶体),只要使冰醋酸的温度稍微高于室温,它就会变成液态可以取出;只要把试剂瓶带到高于16.6℃的地方即可,当然方法多种;
(2)①根据有机物的结构特点判断有机物含有的官能团;
②羧基具有酸的通性:使石蕊试液变红、能和碳酸钠反应生成二氧化碳等等.(1)因为冰醋酸的熔点16.6℃,所以可以把试剂瓶带到大于16.6℃的地方或者水浴稍微加热或者用热毛巾捂热等,
故答案为:水浴微热、用热毛巾热敷、将试剂瓶拿到高于16.6℃的房间内等;
(2)①根据有机物的结构简式可知,该有机物含有羟基、羧基、碳碳双键三种官能团,故答案为:羟基;羧基;碳碳双键.
②羧基具有酸的通性,能使石蕊试液变红,能和碳酸钠反应生成二氧化碳等,所以可用碳酸钠溶液或石蕊试液验证.
故答案为:用该物质和碳酸钠溶液反应是否有气泡生成或能否使石蕊试液变红;产生气泡或变红.点评:
本题考点: 有机物的结构和性质;有机物分子中的官能团及其结构.
考点点评: 本题考查了官能团的判断、物质的性质等知识点,难度不大,结构决定性质,性质体现结构,熟记官能团的性质是解题的关键.1年前查看全部
- 酯是重要的有机合成中间体,请回答下列问题 (1)实验室制取乙酸乙酯的实验中,烧瓶中除加入乙醇、浓硫酸和无水乙酸外,还应放
酯是重要的有机合成中间体,请回答下列问题 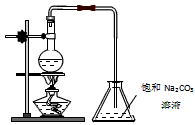
(1)实验室制取乙酸乙酯的实验中,烧瓶中除加入乙醇、浓硫酸和无水乙酸外,还应放入碎瓷片,其目的是______________。烧瓶中发生的反应的化学方程式为____________________________。
(2)欲提高乙酸的转化率,可采取的措施有______________、______________等。
(3)锥形瓶内收集的乙酸乙酯粗产品中所含杂质主要有__________________________。
(4)实验时可观察到锥形瓶中有气泡产生,用离子方程式表示产生气泡的原因:____________________________。
(5)此反应以浓硫酸作为催化剂,可能会造成产生大量酸性废液,催化剂重复使用困难等问题。现代研究表明质子酸离子液体可作此反应的催化剂,实验数据如下表所示(乙酸和乙醇以等物质的量混合)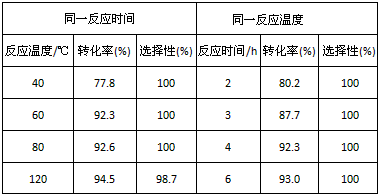
(说明:选择性100%表示反应生成的产物是乙酸乙酯和水)
根据表中数据,下列_________(填编号),为该反应的最佳条件。
A. 120℃,4h B. 80℃,2h C. 60℃,4h D. 40℃,3h Eileebing1年前1
Eileebing1年前1 -
 艺术大使 共回答了18个问题
艺术大使 共回答了18个问题 |采纳率94.4%1年前查看全部
- 在温度较低时,怎样从试剂瓶中取出无水乙酸
 不知为妙1年前2
不知为妙1年前2 -
 就是_不服 共回答了17个问题
就是_不服 共回答了17个问题 |采纳率82.4%温度低于17度时!乙酸为固体!又称为冰醋酸!只需稍微加热即可使冰醋酸融化!就可以取出了!1年前查看全部
- (2009•静安区二模)25℃时,将一定量的冰醋酸(即无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法
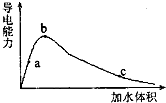 (2009•静安区二模)25℃时,将一定量的冰醋酸(即无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
(2009•静安区二模)25℃时,将一定量的冰醋酸(即无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
A.醋酸的电离度:a<b<c
B.溶液的pH值:b<a<c
C.a、b、c三点的溶液都有:c(H+)=c(CH3COO-)+c(OH-)
D.从b点到c点,溶液中
的比值减小c(CH3COO−) c(CH3COOH)  北上成功1年前1
北上成功1年前1 -
 迷糊喵喵 共回答了15个问题
迷糊喵喵 共回答了15个问题 |采纳率93.3%A.醋酸为弱电解质,加水促进电离,浓度越小,电离程度越大,则乙酸的电离程度:a<b<c,故A正确;
B.电离程度反应了氢离子的浓度,溶液导电能力越大,离子浓度越大,氢离子浓度越大,pH越小,故B正确;
C.根据溶液的电荷守恒可知,a、b、c三点的溶液都有:c(H+)=c(CH3COO-)+c(OH-),故C正确;
D.从b点到c点,促进醋酸电离,溶液中醋酸根离子个数增大,醋酸分子个数减小,所以溶液中
c(CH3COO−)
c(CH3COOH)的比值增大,故D错误;
故选:D.1年前查看全部
- 25℃时,将一定量的冰醋酸(无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图1所示.
25℃时,将一定量的冰醋酸(无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图1所示.
请完成下列问题: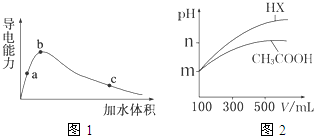
(1)上述a、b、c三点对应醋酸的电离程度最大的是______(填“a”、“b”、“c”),三点对应溶液中c(OH-)由大到小的顺序为______.
(2)c点对应的溶液中c(H+)与c(CH3COO-)+c(OH-)的关系为前者______(填“大于”“小于”“等于”)后者.
(3)从a点到b点,溶液中
的比值______(填“增大”、“减小”、“等于”).cCH3COO− cCH3COOH
(4)25℃时,体积均为100mL、pH=m的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图2所示.则稀释前两溶液中c(OH-)=______,HX的电离平衡常数______(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数.
(5)若用pH试纸进行实验,你能否区分上述HX和CH3COOH两种酸溶液?若能,请简述操作过程;若不能,请说明理由.______. iamhunhun1年前1
iamhunhun1年前1 -
 280994383 共回答了15个问题
280994383 共回答了15个问题 |采纳率100%解题思路:(1)溶液浓度越小,醋酸的电离程度越大;溶液中离子浓度越大其导电能力越强,氢离子浓度越大,氢氧根离子浓度越小;
(2)c点对应的溶液中根据电荷守恒判断;
(3)根据电离平衡常数是定值,结合从a点到b点氢离子浓度在变大分析;
(4)根据pH=-lgc(H+)计算出氢离子浓度,再根据Kw计算氢氧根浓度;由图可知,稀释相同的倍数,HX的pH变化程度大,则酸性HX强,电离平衡常数大;
(5)稀释会促进弱电解质的电离,故弱酸的PH变化小,据此分析;(1)溶液体积越大,溶液浓度越小,醋酸的电离程度越大,所以a、b、c三点中醋酸的电离程度最大的是c,溶液中离子浓度越大其导电能力越强,所以氢离子浓度大小顺序是b>a>c,则c(OH-)由大到小的顺序为c>a>b;
故答案为:c;c>a>b;
(2)c点对应的溶液中根据电荷守恒,则有c(H+)=c(CH3COO-)+c(OH-),故答案为:等于;
(3)因为从a点到b点电离平衡常数是定值即
C(CH 3COO −)C(H +)
C(CH3COOH)不变,又根据图象从a点到b点氢离子浓度在变大,所以溶液中
cCH3COO−
cCH3COOH的比值在减小,故答案为:减小;
(4)根据pH=-lgc(H+)=m,则氢离子浓度为10-m,又Kw=c(H+)c(OH-)=10-14,所以氢氧根浓度为10m-14;由图可知,稀释相同的倍数,pH变化大的酸酸性强,由图可知,HX的pH变化程度大,则HX酸性强,电离平衡常数大,故答案为:10m-14;大于;
(5)稀释会促进弱电解质的电离,故弱酸的PH变化小,可鉴别,具体操作为:取等体积的两种溶液分别稀释100倍,用玻璃棒分别蘸取稀释后的两溶液滴在两张PH试纸上,其显示的颜色与比色卡对照,PH较大的是HX溶液;故答案为:能;取等体积的两种溶液分别稀释100倍,用玻璃棒分别蘸取稀释后的两溶液滴在两张PH试纸上,其显示的颜色与比色卡对照,PH较大的是HX溶液;点评:
本题考点: 弱电解质在水溶液中的电离平衡.
考点点评: 本题考查弱酸的电离及酸性的比较、pH与酸的稀释等,注意水解规律中越弱越水解和稀释中强的变化大来分析解答,综合性较大,题目难度中等.1年前查看全部
大家在问
- 1选择溪流而放弃大海是因为溪流().
- 2剪不断 理还乱一句中“还”字的读音到底是什么?听很多人读haí 但中央电视台里我听读的是huán?
- 310.8乘以9.
- 4一元二次方程两根相乘等于什么?相加呢?
- 5I think it ___Tom belong to还是belongs to
- 62、一个三角形的最小内角是500,这个三角形一定是( ).A、锐角三角形 B、直角三角形 C、钝角三角形 D、
- 756和7的最大公因数和最小的公倍数
- 8怎样用向量法解立体几何
- 9CO与H2混合后,平均相对分子质量是H2的3.6倍,则CO与H2的物质的量的比为( )
- 10现有A.B.C.D.E.F六种短周期元素,原子序数依次增大.已知A与D,C与E分别同主族,D.E.F同周期.A.B的最外
- 11在英语中什么情况下“a”会变:“an”?
- 12副团用英语单词怎么拼写
- 13把一根竹竿插入水中,露出水面0.5米,插入泥中4分之1米,水深2又2分之1米.这根竹竿有多长?
- 14一根竹竿插入水池中,入池底泥中部分占全长的四分之一,水中部分比泥中部分长三分之二米,露出水面1米,问竹竿长为多少?用
- 1599*22+88*33+77*44+66*55 简便运算

