水电解的实验中观察到的现象,正确的是?A正极产生氧气 B与电源正极相连的试管内汇集的气体体积大 C与电源正负两级相连的试
 fgfg32022-10-04 11:39:541条回答
fgfg32022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 jowook5277zl 共回答了13个问题
jowook5277zl 共回答了13个问题 |采纳率84.6%- C正确.作为现象应该是观察得到的,D质量是看不见的,A只能看见气体汇集,不能说明是氧气,B是错的
- 1年前
相关推荐
- 请问在高中及之前的范围内,有哪些物质是可以电解的?比如水电解、氧化铝电解...
 coffinren1年前1
coffinren1年前1 -
 sdfsdfsdfFFSDS 共回答了20个问题
sdfsdfsdfFFSDS 共回答了20个问题 |采纳率90%所有的盐,但alcl3不是哦他是共价键!还有所有的酸和碱,强弱不同罢了,水.注意有机物如乙醇就不是,判断是否能组成原电池是要注意!1年前查看全部
- 水电解产生氢气和氧气与氢气和氧气燃烧生成水,这二个反应是可逆反应吗?
 bin07051年前1
bin07051年前1 -
 xuemei99 共回答了19个问题
xuemei99 共回答了19个问题 |采纳率94.7%不是啊,反应条件不一样,那个反应的吉普斯自由能负的很多,所以反应的平衡常数很大,可视为完全反应,不是可逆反应.1年前查看全部
- 水电解后产生的气压+重力+氢燃烧也不够完成再次电解的能量吗?为什么?
 板栗头1年前1
板栗头1年前1 -
 亚平 共回答了21个问题
亚平 共回答了21个问题 |采纳率100%楼主,各种能量的转换都是有损耗的.
在楼主所提到的“循环”中:单单就氢气燃烧的热到电的转化,效率估计就不到30%,所以在无外加能量的条件下无法循环.1年前查看全部
- 氯化钠跟水电解生成什么?
 躺在云端1年前2
躺在云端1年前2 -
 摇动的春天 共回答了20个问题
摇动的春天 共回答了20个问题 |采纳率90%2NaCl+2H2O==通电==2NaOH+H2↑+Cl2↑所以生成物应该是阳极氯气,阴极氢气,溶液变为氢氧化钠1年前查看全部
- 氯化钠与水电解属于什么反应那是否可说反应中氯元素被氧化?
 田云铭1年前3
田云铭1年前3 -
 突出重维 共回答了22个问题
突出重维 共回答了22个问题 |采纳率90.9%高中属于氧化还原反应1年前查看全部
- 水电解后就是H跟O吧?
 azuresigh1年前4
azuresigh1年前4 -
 ginkgoer 共回答了17个问题
ginkgoer 共回答了17个问题 |采纳率76.5%这是你的考题么?如果是的话你这样回答就错了
正确的说法应该是H离子跟O离子!
记住 水电解后是出离子而不是直接的H或者O1年前查看全部
- 水电解是水的化学性质吗
 shiwoying1年前5
shiwoying1年前5 -
 爱人小春 共回答了22个问题
爱人小春 共回答了22个问题 |采纳率95.5%是的 严格来说 是电化学性质.1年前查看全部
- 水电解试验证明水中含有演员苏很氢元素,那么水中是有氢分子氧分子还是氢原子氧原子啊
 圣_诞_节1年前2
圣_诞_节1年前2 -
 hyj_jack 共回答了21个问题
hyj_jack 共回答了21个问题 |采纳率95.2%一个水分子由两个氢原子和一个氧原子构成的
水由很多很多水分子构成1年前查看全部
- 水电解时加入不同的电解质会对其速率产生不同的影响吗,比如加入酸和碱,或者不同浓度的电解质溶液?
 4364yrwe1年前1
4364yrwe1年前1 -
 穿ii是一种文化 共回答了13个问题
穿ii是一种文化 共回答了13个问题 |采纳率92.3%水电解时加入不同的电解质会对其速率产生的影响是差不多的.
除非加入的电解质会改变电解过程,否则都只能直到增强导电作用.既然只是增加导电性,那么无论哪种电解质,初其实都差别不大.1年前查看全部
- 水电解和蒸馏净化水 哪个是化学反应
 ciscc1年前1
ciscc1年前1 -
 都市边沿人 共回答了22个问题
都市边沿人 共回答了22个问题 |采纳率81.8%水电解是化学反应,因为他生成氢气和氧气.而蒸馏净化水未产生新的物质,所以为物理变化.1年前查看全部
- 酸根遇到水电解的氢离子是否能体现氧化还原性
 笑看流年1年前1
笑看流年1年前1 -
 wonjen 共回答了18个问题
wonjen 共回答了18个问题 |采纳率100%要看是什么酸盐
如果是含硝酸根的弱碱盐
一定会有强氧化性
打个比方 NH4NO3+H20====NH3.H2O+H离子+NO3离子
此时溶液有硝酸根而且是酸性 所以会有强氧化性.1年前查看全部
- 水电解是氧化还原反应么?如果是,那水是还原剂还是氧化剂?
 27854141年前2
27854141年前2 -
 有只小狗 共回答了20个问题
有只小狗 共回答了20个问题 |采纳率95%是,即使氧化剂又是还原剂,只要有价态的改变就按氧化剂还原剂说1年前查看全部
- 水为什么是电解质?水电解时,如果滴入酚酞,在正极的周围会有淡红吗?
 gg品质1年前1
gg品质1年前1 -
 2fzzksfisc6on4 共回答了28个问题
2fzzksfisc6on4 共回答了28个问题 |采纳率96.4%因为水可以电解出氢离子和氧离子.所以水是电解质.
所谓的电解质,就是可以在某一个条件下点解出阳离子和阴离子.而水就可以点解.(至于为什么,是因为客观存在的,不需要你去研究,你只需要记住这个结论即可)1年前查看全部
- 水电解得到氢气和氧气不纯的原因有哪些
 大大大青蛙1年前3
大大大青蛙1年前3 -
 风中捕影 共回答了26个问题
风中捕影 共回答了26个问题 |采纳率88.5%水不纯是他们胡说了.
除了一些酸碱盐会影响气体.其他的都不会.
主要是气密性不好.1年前查看全部
- 请写出水电解的文字表达式
 qq1年前3
qq1年前3 -
 wxl82512 共回答了20个问题
wxl82512 共回答了20个问题 |采纳率95%水→氢气+氧气,箭头上面写通电1年前查看全部
- 说水电解生成氢气和氧气水中就含有氢分子和氧分子
说水电解生成氢气和氧气水中就含有氢分子和氧分子
这句话对吗 为什么不对呢 说某种物质有什么原子组成或什么分子组成总弄不清 谁给我仔细讲一下啊 liouhuei1年前5
liouhuei1年前5 -
 shw315 共回答了18个问题
shw315 共回答了18个问题 |采纳率94.4%显然错的.1年前查看全部
- 水电解生成氢气和氧气,说明水中含有氢分子和氧分子.这句话对吗?
 穿睡袍的宝儿1年前1
穿睡袍的宝儿1年前1 -
 炭中和 共回答了17个问题
炭中和 共回答了17个问题 |采纳率88.2%不对 水的组成是氢元素(H)与氧元素(O) 氢分子是H2 氧分子是O2 所以不对1年前查看全部
- 水电解后质量减小,是否意味组成水的元素不存在 化学
 kof_ljx1年前2
kof_ljx1年前2 -
 9630258 共回答了19个问题
9630258 共回答了19个问题 |采纳率100%否,水电解后生成氢气和氧气,并以气体的形式进入大气中,水所减少的质量即为这部分气体的质量.1年前查看全部
- 水电解产生什么物质?
 o蓝色1年前1
o蓝色1年前1 -
 neyman 共回答了20个问题
neyman 共回答了20个问题 |采纳率85%氢气和氧气1年前查看全部
- 为何水电解后会出现黑色絮凝状物质?
 huangcunzhang1年前2
huangcunzhang1年前2 -
 qrw7617_cn 共回答了25个问题
qrw7617_cn 共回答了25个问题 |采纳率92%问题出在电解设备上.
你看到这个现象所用的设备,电极为铁(铜)和铝.铁被氧化了导致很多脏东西出来,其实你仔细观察,会发现其中还有个电极在不断的冒泡,那是氢气.
正确的电解设备用的电极用该是钛金的.这种物质稳定,不会与水中的氧气反应,你也看不到你所说的现象.1年前查看全部
- 1MOL水电解转移几摩尔电子 还有关于转移电子数 怎么求
 lpwdp1年前1
lpwdp1年前1 -
 小毛球Jacobs 共回答了15个问题
小毛球Jacobs 共回答了15个问题 |采纳率93.3%转移2mol电子,转移的电子数是2*6.02*10^23个电子.这要根据反应方程式.1mol谁电解得到1mol氢气.化合价降低2 则转移了2mol电子.1年前查看全部
- 求水电解方程式表示的意义
 alanyang1231年前1
alanyang1231年前1 -
 DEDEWANG 共回答了20个问题
DEDEWANG 共回答了20个问题 |采纳率90%[教具准备]课件、磁性小黑板、磁性卡片、试管、锌粒、稀盐酸、氢氧化钠溶液、硫酸铜溶液1年前查看全部
- 在水电解的实验中,有新物质生成吗
 北在北极1年前1
北在北极1年前1 -
 jll1982 共回答了19个问题
jll1982 共回答了19个问题 |采纳率73.7%有啊,生成H2和O2.1年前查看全部
- 在水电解试验中,水发生变化了吗
 NPST1年前4
NPST1年前4 -
 sz113 共回答了18个问题
sz113 共回答了18个问题 |采纳率94.4%两试管中都有气泡产生,液面下降.电池正极所连一端(试管1),生成能使带火星木条复燃的无色气体.与电池负极一段相连的试管中(试管2),气体被点燃,并有轻微爆鸣声.试管1和试管2中气体体积比约为1:2.
水的性质没有变,只是水的量在减少1年前查看全部
- 一道初中科学课上的化学题“水电解”
一道初中科学课上的化学题“水电解”
我们知道,水可以电解出“氢气”和“氧气”.
那么,请问1度电可以将水电解出多少kg的氢气和氧气? smap1231年前3
smap1231年前3 -
 蓝梦蓝心 共回答了14个问题
蓝梦蓝心 共回答了14个问题 |采纳率92.9%在298.15K,101.3Kpa的标准状态下,液态水的的标准Gibbs生成自由能是-237.1kJ/mol,反过来电解水消耗的能量就是237.1kJ/mol.一度电是一千瓦小时即3600千焦,因此,在无能量损耗的最理想状况下,可以生成15.18mol氧气和30.37mol氢气.具体的体积必须用van der waals方程算.理想气体一摩尔大约是0.0224立方米.
利用体积和密度再求出各自的质量.
这显然超出初中生的能力范围.我也是初中生,不太理解~
但我知道等分子量的不同气体其体积是一样的.1年前查看全部
- 空间实验室“天宫一号”他供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合他可充电
 空间实验室“天宫一号”他供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合他可充电电池.如n为RFC工作原理示意n,有关说法正确他是( )
空间实验室“天宫一号”他供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合他可充电电池.如n为RFC工作原理示意n,有关说法正确他是( )
A.转移0.1mol电子时,a电极产生1.12LH2(标准状况)
B.b电极上发生的电极反应是:2H2O+2e-=H2↑+2OH-
C.c电极上进行还原反应,B电池中的H+可以通过隔膜进入A池
D.d电极上发生的电极反应是:O2+4H++4e-=2H2O dayangzining1年前1
dayangzining1年前1 -
 芭比娃娃麗 共回答了18个问题
芭比娃娃麗 共回答了18个问题 |采纳率94.4%解题思路:依据图示ab电极是电解池的电极,由电源判断a为阴极产生的气体是氢气,b为阳极产生的气体是氧气;c、d电极是原电池的正、负极,c是正极,d是负极;电解池中的电极反应为:b电极为阳极失电子发生氧化反应:4OH--4e-=2H2O+O2↑,a电极为阴极得到电子发生还原反应:4H++4e-=2H2↑,原电池中是酸性溶液,电极反应为:d为负极失电子发生氧化反应:2H2-4e-=4H+,c电极为正极得到电子发生还原反应:O2+4H++4e-=2H2O,结合电极上的电子守恒分析计算.电解池s的电极反应为:b电极为阳极失电子发生氧化反应:4手H--4e-=rHr手+手r↑;a电极为阴极得到电子发生还原反应:4H++4e-=rHr↑;
原电池s是酸性溶液,电极反应为:d为负极失电子发生氧化反应:rHr-4e-=4H+;c电极为正极得到电子发生还原反应:手r+4H++4e-=rHr手;
A、阳极电极反应计算,当有w.1 w手四电子转移时,a电极产生1.1r四Hr故A正确;
B、b电极上发生的电极反应是4手H--4e-=rHr手+手r↑,故B错误;
C、c电极上进行还原反应,B池s的H+可以通过隔膜进入A池,故C正确;
D、d电极上发生的电极反应是:rHr-4e-=4H+;故D错误;
故选AC.点评:
本题考点: 原电池和电解池的工作原理.
考点点评: 本题考查了化学电源新型电池,主要考查原电池和电解池的工作原理,电极判断,电极反应,关键是原电池中电解质溶液是酸性环境,注意电极书写.1年前查看全部
- 电解PbSO4+H2O的本质是水电解吗?
电解PbSO4+H2O的本质是水电解吗?
如果是水电解的话,为什么在原电池-铅蓄电池中,反应为
PbSO4+H2O=Pb+PbO+H2SO4
而不是H2O=H2!+O2!
双硫化理论是什么? 郁郁欢欢1年前2
郁郁欢欢1年前2 -
 hohofish 共回答了10个问题
hohofish 共回答了10个问题 |采纳率100%是双硫化理论,水的电解反应属副反应.1年前查看全部
- (2014•常德模拟)水电解的过程可用图示表示,微粒运动变化的先后顺序是( )
(2014•常德模拟)水电解的过程可用图示表示,微粒运动变化的先后顺序是( )

A.①②③④
B.③②①④
C.②①④③
D.④①③② 蓝幽子1年前1
蓝幽子1年前1 -
 yuefeng0909 共回答了20个问题
yuefeng0909 共回答了20个问题 |采纳率95%解题思路:根据化学变化的实质进行分析.在化学变化中,分子分解成原子,原子再重新结合成新的分子.由化学变化的实质可知,水电解的过程中微粒运动变化的先后顺序是:水分子分解成氢原子和氧原子,每两个氢原子结合成一个氢分子,大量的氢分子聚集成氢气;每两个氧原子结合成一个氧分子,大量的氧分子聚集成氧气.微粒运动变化的先后顺序是:②①④③.所以:
A、微粒运动变化的先后顺序不是①②③④,故A错误;
B、微粒运动变化的先后顺序不是③②①④,故B错误;
C、微粒运动变化的先后顺序是②①④③,故C正确;
D、微粒运动变化的先后顺序不是④①③②,故D错误.
故选C.点评:
本题考点: 微粒观点及模型图的应用.
考点点评: 本题主要考查了微观粒子发生反应时的先后顺序方面的问题.可以根据化学反应的实质进行分析回答.1年前查看全部
- 用化学式或化学方程式填空(1)小苏打______(2)碘酒中的溶剂______(3)水电解的化学方程式2H2O 通电 .
用化学式或化学方程式填空
(1)小苏打______
(2)碘酒中的溶剂______
(3)水电解的化学方程式2H2O
2H2↑+O2↑通电 .2H2O.
2H2↑+O2↑通电 . yang1231年前1
yang1231年前1 -
 mt17530 共回答了19个问题
mt17530 共回答了19个问题 |采纳率89.5%解题思路:首先根据题意确定物质的化学名称,然后根据书写化学式、化学方程式的方法和步骤写出相应的化学式或化学方程式即可.(1)小苏打是碳酸氢钠的俗称,其化学式为:NaHCO3.
(2)碘酒是碘的酒精溶液,酒精是溶剂,其化学式为:C2H5OH.
(3)水通电分解生成氢气和氧气,反应的化学方程式为:2H2O
通电
.
2H2↑+O2↑.
故答案为:(1)NaHCO3;(2)C2H5OH;(3)2H2O
通电
.
2H2↑+O2↑.点评:
本题考点: 化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,熟练掌握常见物质的性质、用途、组成及化学式与化学方程式的书写是正确解答本题的关键所在.1年前查看全部
- 水电解产生氢气,很简单的公式和原理,为什么学化学的到现在还没有研制一种材料可以让反应顺利进行?
水电解产生氢气,很简单的公式和原理,为什么学化学的到现在还没有研制一种材料可以让反应顺利进行?
none iam691年前5
iam691年前5 -
 dj188 共回答了25个问题
dj188 共回答了25个问题 |采纳率88%这些过程也是能量守恒的,
必须有外面的能量加入,反应才会发生.
就算找到一种材料使反应发生,这种材料也必须释放出能量
跟电解是一样的1年前查看全部
- 一公斤水电解后得氢和氧,他们燃烧后还有没有1KG
一公斤水电解后得氢和氧,他们燃烧后还有没有1KG
电解一KG水,得氢气和氧气,让他们充分燃烧,得到的水还有没有一KG?
他们能在真空中燃烧吗? li373551年前1
li373551年前1 -
 feiniao1980 共回答了20个问题
feiniao1980 共回答了20个问题 |采纳率80%这是不可能的!
问题是这个一定比例的氢气和氧气是不可能完全燃烧的.因为随着燃烧的进行,氢气和氧气的浓度都降低,降到不能燃烧的程度,燃烧自然停止.除非,在燃烧的过程中,不断的压缩体积,直到无穷无穷小的地步.所以,是不可能实现的.1年前查看全部
- 从分子的角度解释下列实验事实1.水电解生成氢气和氧气2.水加热变成水蒸气
 一只巴巴拉1年前2
一只巴巴拉1年前2 -
 注册萝卜 共回答了23个问题
注册萝卜 共回答了23个问题 |采纳率91.3%水通电,水分子分离成氧原子和氢原子,两个氢原子构成一个氢分子,两个氧原子构成氧分子.加热水,水分子之间的间隔增大.1年前查看全部
- 1.用水电解来收集氧气的方法可行吗?2.氧化镁Mg3o2中,那个氮的化学价怎么求?
 花舞残梦love仔1年前1
花舞残梦love仔1年前1 -
 全心爱COCO 共回答了20个问题
全心爱COCO 共回答了20个问题 |采纳率90%1、用水电解是可以收集到氧气的,就是正极上收集到的气体就是氧气,负极上收集到的是氢气.
2、镁燃烧时,大部分跟氧气反应,生成氧化镁,少量镁跟氮气反应生成的氮化镁.因为镁是+2价(被夺了2个电子),所以氮化镁里的氮就应该是 -3价(负3价,得到3个电子).这样,镁一共被夺走6个电子,而氮一共得到6个电子.1年前查看全部
- 电解水时,常在水中加入少量硫酸以增强水的导电性,若用8%的硫酸100g通直流电进行水电解的食盐,一段时间后,硫酸的溶质质
电解水时,常在水中加入少量硫酸以增强水的导电性,若用8%的硫酸100g通直流电进行水电解的食盐,一段时间后,硫酸的溶质质量分数变为10%,则被电解的水的质量为
A 10g B 20g C 25g D30g kinsowfox1年前1
kinsowfox1年前1 -
 hytanubis 共回答了22个问题
hytanubis 共回答了22个问题 |采纳率90.9%吓死我,不是食盐是实验吧
点解的是水而不是硫酸
那么溶质的质量不变
原来的溶质是100×8%=8g
那么根据最后的质量分数是10%得到
溶液质量是8/0.1=80g
点解了水是100-80=20g
选B1年前查看全部
- 电解池和原电池问题为什么点解硫酸实质是水电解?硫酸不是也电离H+离子吗?还有原电池中,用中性点解质,Fe和石墨做电极,F
电解池和原电池问题
为什么点解硫酸实质是水电解?硫酸不是也电离H+离子吗?
还有原电池中,用中性点解质,Fe和石墨做电极,Fe与O2反应,这时,为什么Fe会氧化成2+而不是3+?氧气不是有强氧化性吗? ll博客91年前3
ll博客91年前3 -
 yushoujun 共回答了21个问题
yushoujun 共回答了21个问题 |采纳率90.5%电解池中,电解的实质是阴阳离子电解硫酸时,你得明确此时溶液中的阳离子只有氢离子,不存在活泼性的先后,而阴离子有硫酸根和氢氧根(水中的),就存在氧化的先后问题了,是先氧化硫酸根还是氢氧根了.根据活泼性可知(这个活泼性是需要背下来的,氢氧根活泼性大于酸根离子,比如硫酸根,磷酸根,碳酸根等,并且活泼性大的先反应),氢氧根先被氧化,也就是说在阳极,氢氧根被氧化,在阴极,氢离子被还原,就相当于电解水了.
至于Fe和石墨做电极,Fe与O2反应,这时,为什么Fe会氧化成2+而不是3+,是因为一般情况下铁只能失电子成二价,Fe只会氧化成2+ 在空气中Fe2+会变成三价,也就是说在溶液中的反应,只能氧化到正二价,不容易到正三价.1年前查看全部
- 关于电解氢氧化钠溶液的问题.我们知道电解稀氢氧化钠溶液其实是一个电解水的过程,但是当水电解的差不多了得到浓氢氧化钠溶液后
关于电解氢氧化钠溶液的问题.
我们知道电解稀氢氧化钠溶液其实是一个电解水的过程,但是当水电解的差不多了得到浓氢氧化钠溶液后就开始电解氢氧化钠了.
问:开始电解氢氧化钠时,氢氧化钠溶液的浓度也该是多少? 江采苹1年前3
江采苹1年前3 -
 benbenaimengmeng 共回答了16个问题
benbenaimengmeng 共回答了16个问题 |采纳率87.5%这种情形是不会出现的.
正象rocket004 所说,水逐渐分解后,溶液中氢氧化钠浓度会越来越高,达到饱和程度后就开始有固体氢氧化钠析出,那么溶液开始保持饱和溶液的浓度,当水全部分解后,反应就结束了.因为固体氢氧化钠是不导电的.
要想电解氢氧化钠,必须要将纯氢氧化钠加热到熔融状态才可以进行.1年前查看全部
- 在水电解的实验中,所收集氢气与氧气的气体体积比约为1:2,那么水分解后生成氢气和氧气的分子数比为1:2
 887663501年前1
887663501年前1 -
 韦青 共回答了24个问题
韦青 共回答了24个问题 |采纳率91.7%题目出错啦!
在水电解的实验中,所收集氢气与氧气的气体体积比约为2:1,不是1:2
当然,生成的氢气和氧气的分子数比也为2:1
水电解2H2O = 2H2+O21年前查看全部
- 为了探究水电解的微观过程,某同学做了一些下图所示的分子、原子的模型,若用“ ”表示氢原子,用“ ”表示氧原子,其中能保持
为了探究水电解的微观过程,某同学做了一些下图所示的分子、原子的模型,若用“
 ”表示氢原子,用“
”表示氢原子,用“ ”表示氧原子,其中能保持氢气的化学性质的粒子是
”表示氧原子,其中能保持氢气的化学性质的粒子是A. 
B. 
C. 
D. 
 amny80001年前1
amny80001年前1 -
 小鱼amy 共回答了20个问题
小鱼amy 共回答了20个问题 |采纳率90%A
氢气是由氢分子构成的,其化学性质是由氢分子保持的.
A、表示的是氢分子,所以正确.
B、表示的是两个单个的氢原子,所以错误.
C、表示的是水分子,所以错误.
D、表示的是单个的氢原子和氧原子,所以错误.
故选A.1年前查看全部
- 当含有少量NaNO3的水电解时,在阴极会产生出 气体;同时其附近还会形成
当含有少量NaNO3的水电解时,在阴极会产生出 气体;同时其附近还会形成
性的溶液(填“酸”或“中”或“碱”) tonarinototoro1年前1
tonarinototoro1年前1 -
 金yy然 共回答了17个问题
金yy然 共回答了17个问题 |采纳率100%当含有少量NaNO3的水电解时,在阴极会产生出(H2)气体;同时其附近还会形成
(碱)性的溶液(填“酸”或“中”或“碱”)
两极反应: 阴:4H2O + 4e- = 2H2(^) + 4OH- (所以阴极附近碱性)
阳: 4OH- -4e- = O2(^) + 2H2O
注: 阴极也可以: 4H+ +4e-=2H2(^)1年前查看全部
- (2011•镇江一模)下图是某空间站能量转化系统局部示意图,其中水电解系统及燃料电池系统中的溶液均采用KOH溶液.下列有
(2011•镇江一模)下图是某空间站能量转化系统局部示意图,其中水电解系统及燃料电池系统中的溶液均采用KOH溶液.下列有关说法错误的是( )

A.该能量转化系统中的水可以循环使用
B.水电解系统实现由电能到化学能的转化,燃料电池系统实现由化学能到电能的转化
C.水电解系统中的溶液采用KOH溶液,是为了增强水的导电性
D.燃料电池系统产生的能量实际上来自于水 _小新_1年前1
_小新_1年前1 -
 xbox44 共回答了18个问题
xbox44 共回答了18个问题 |采纳率77.8%解题思路:根据空间站能量转化系统局部示意图,利用水的分解反应和燃料电池中的反应来分析反应中的能量变化.A、由转化图可知,该系统中水既可分解也可生成,是循环使用的,说法正确,故A错误;
B、水电解是电能转化为化学能,燃料电池是利用化学反应产生能量,则是化学能转变为电能,说法正确,故B错误;
C、水电解系统中的溶液采用KOH溶液,使离子的浓度变大,导电性增强,说法正确,故C错误;
D、燃料电池系统产生的能量来源于所发生的化学反应,则说法错误,故D正确.
故选D.点评:
本题考点: 物质发生化学变化时的能量变化;电解水实验;溶液的导电性及其原理分析.
考点点评: 本题利用信息来考查化学与能源问题,注重了与生活实际的紧密联系,也体现了利用所学课本知识能够学以致用.1年前查看全部
- 关于将水电解成氢和氧的问题?我直接用把插头剪掉,然后接通电源,用电线里的正负线插入水中,可以电解么?会不会有危险呢?额?
 零下一度的冬天1年前1
零下一度的冬天1年前1 -
 aampt 共回答了18个问题
aampt 共回答了18个问题 |采纳率83.3%电解要用直流电1年前查看全部
- 水电解产生氢气和氧气 乙炔在空气中燃烧 化学方程式反应现象 急
 光武uu1年前3
光武uu1年前3 -
 pigdou 共回答了17个问题
pigdou 共回答了17个问题 |采纳率94.1%2H2O=电解=2H2↑+O2↑
2C2H2+5O2=4CO2+2H2O1年前查看全部
- 水电解.食盐水溶液电解,氢气这边独自冒泡,氧气这里没有明显反应.氢气氧气也不是2:1.还有一种绿绿的“恶心”的东西.这是
水电解.食盐水溶液电解,氢气这边独自冒泡,氧气这里没有明显反应.氢气氧气也不是2:1.还有一种绿绿的“恶心”的东西.这是什么情况?

 xiaoyao2951年前3
xiaoyao2951年前3 -
 重庆帮幻海 共回答了15个问题
重庆帮幻海 共回答了15个问题 |采纳率93.3%谁放的食盐水,这是要毒死人的节奏啊!氧气那一级(正极)产生的是剧毒的氯气啊!
食盐的主要成分是NaCl(氯化钠).一旦把氯化钠放在水中,那就不是电解水,而是电解盐酸了!
盐酸电解生成氢气和氯气,两种气体体积之比是1:1
本来电解水是可以产生氢气和氧气的,但就是因为氯气比氧气活泼,所以氯化钠中的氯先氧气一步电离出来了.氯气就是黄绿色的.
不过少量还是不会有太大问题的,不用太担心.1年前查看全部
- 下图是某空间站能量转化系统局部示意图,其中水电解系统及燃料电池系统中的溶液均采用KOH溶液.下列有关说法错误的是( )
下图是某空间站能量转化系统局部示意图,其中水电解系统及燃料电池系统中的溶液均采用KOH溶液.下列有关说法错误的是( )
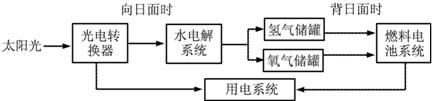
A.该能量转化系统中的水可以循环使用
B.燃料电池系统中溶液pH逐渐增大
C.水电解系统中的溶液采用KOH溶液,是为了增强水的导电性
D.燃料电池系统产生的能量实际上来自于水 tang_find1年前1
tang_find1年前1 -
 mwx236 共回答了19个问题
mwx236 共回答了19个问题 |采纳率94.7%解题思路:根据空间站能量转化系统局部示意图可知,向日面时发生水的分解反应,背日面时发生氢气和氧气生成水的电池反应,再结合系统中KOH溶液的变化来分析解答.A、由转化系统可知,水分解后还可再生成,则水是循环使用的,说法正确,故A错误;
B、因燃料电池系统中的溶液是KOH溶液,有水生成可使溶液的浓度变小,OH-的浓度变小,则PH变小,说法错误,故B正确;
C、水电解系统中的溶液采用KOH溶液,离子的浓度大有利于溶液的导电,则说法正确,故C错误;
D、燃料电池系统产生的能量来源于化学反应产生的化学能,属于化学能转变为电能,不是来源于水,说法错误,故D正确;
故选BD.点评:
本题考点: 物质发生化学变化时的能量变化;电解水实验.
考点点评: 本题以信息的形式来考查化学反应与能量的关系,学生应明确存在的化学反应和溶液的溶质来解答,注意该习题的相关变式如溶液改用稀硫酸.1年前查看全部
- 请用化学方程式写出实验制取氧气的三种方法?2.写出水电解的化学方程式?
 回到梦里1年前0
回到梦里1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 在水电解的实验中,在器械或水的哪个部分出现气泡?
 很懒的薄荷1年前1
很懒的薄荷1年前1 -
 asu2007 共回答了14个问题
asu2007 共回答了14个问题 |采纳率85.7%通直流电,所以用的是电池,
电池的正负两极都出现气泡啊,负极产生氢气,正极产生氧气
氢气和氧气的产生的比是2:11年前查看全部
- 下列有关热化学方程式及其叙述正确的是 A.氢气的燃烧热为-285.5kJ/mo1,则水电解的热化学方程式为:
下列有关热化学方程式及其叙述正确的是
A.氢气的燃烧热为-285.5kJ/mo1,则水电解的热化学方程式为:
2H 2 O(1) =2H 2 (g)+O 2 (g);△H=+285.5KJ/mo1B.1mol甲烷完全燃烧生成CO 2 和H 2 O(1)时放出890kJ热量,它的热化学方程式为
1/2CH 4 (g)+O 2 (g)= 1/2CO 2 (g)+H 2 O(1);△H= 一445kJ/molC.已知2C(s)+O 2 (g)=2CO(g);△H= 一221kJ·mol -1 ,则C的燃烧热为一110.5kJ/mo1 D.HF与NaOH溶液反应:H + (aq)+OH — (aq)=H 2 O(1);△H= 一57.3kJ/mol  wangbindq1年前1
wangbindq1年前1 -
 ihihllby 共回答了12个问题
ihihllby 共回答了12个问题 |采纳率91.7%B
1年前查看全部
- 用微粒的观点解释下列现象碘受热升华和凝华;打气筒里的空气加压时体积明显减小,给水加压时体积无明显变化;水电解生成氢气和氧
用微粒的观点解释下列现象
碘受热升华和凝华;打气筒里的空气加压时体积明显减小,给水加压时体积无明显变化;水电解生成氢气和氧气
化学题 fyh_10301年前1
fyh_10301年前1 -
 天tian1026 共回答了15个问题
天tian1026 共回答了15个问题 |采纳率86.7%1、碘受热升华:
碘受热,碘分子的运动更加剧烈(初一教过的吧、),于是碘分子之间的距离增大,原本的固体的密度就减小、就升华为气体.、
2、打气筒里的空气加压时体积明显减小,给水加压时体积无明显变化:
空气的分子之间的间隙比较大(就是说密度比较小、)那么它们之间的空隙就比较容易被挤压变小(体积减小);而水的分子间隙比较小不容易被压缩.
3、水电解生成氢气和氧气:
水通直流电的时候,水分子(分子式H2O、),就拆分成氢原子和氧原子(H和O),然后氢原子和氧原子又自由组合,组成氢气和氧气(H2和O2)、
就是这样~~1年前查看全部
- 水电解成氢气和氧气能说明分子可分成原子吗?
水电解成氢气和氧气能说明分子可分成原子吗?
***受热生成汞和氧气呢? 静碧1年前3
静碧1年前3 -
 r511 共回答了15个问题
r511 共回答了15个问题 |采纳率86.7%两个都可以1年前查看全部
大家在问
- 1“伯父摸着胡子,笑了笑,说:‘哈哈!还是我记性好.’”这句话在课文中表面上是说( )实际上( ).
- 2what's the matter和what's wrong 的区别如题
- 3英语翻译翻译一个地址,地址是:内蒙古巴彦淖尔市杭锦后旗市政维护站.
- 4推断近年来艾比湖水域面积变化趋势并说明变化原因,而且阐述艾比湖为什么成为天山北坡经济带盐尘暴策源地的原因.求解答拜托了
- 5同学们在向校园里欢唱的小鸟打招乎是什么修辞
- 6talk to sb 的例句
- 7三角形底0.4米,高0.6米,它的面积是______.
- 8用一种试剂一次就能将澄清石灰水、氢氧化钠溶液、稀盐酸三种无色溶液区分开来的是( )
- 9如图是某化学反应的微观示意图,下列说法正确的是( )
- 10人类探索宇宙的真正含义 1.从科学技术发展看 2.从经济效益看 3.从社会效益看 4.从综合效益看
- 11杜甫的绝句诗可以出哪些题目?"迟日江山丽,春风花草香.泥融飞燕子,沙暖睡鸳鸯."关于情怀、某个字的深层含义的题目和答案!
- 12二十年以后的地球 作文
- 13麻烦一个较完整的解题过程!
- 14华(huà)怎么组词
- 15我爱绿叶 作者抒发了怎样的思想感情
