1氢硒酸放在空气中长期保存易变质,其可能发生的化学方程式为_____
 姓焦博士2022-10-04 11:39:542条回答
姓焦博士2022-10-04 11:39:542条回答2.稀硫酸中加入过氧化钠溶液后,则可使铜顺利溶解,化学反应方程式为_____

已提交,审核后显示!提交回复
共2条回复
 只说几句 共回答了16个问题
只说几句 共回答了16个问题 |采纳率93.8%- 1.2H2Se+O2==2H2O+2Se
2.2Na2O2+2H2O==4NaOH+O2↑
2Cu+O2==2CuO
CuO+H2SO4==CuSO4+H2O - 1年前
 风心涧 共回答了4个问题
风心涧 共回答了4个问题 |采纳率- 有过氧化钠溶液存在?
- 1年前
相关推荐
- 氧族元素的题2 工业上从含硒的废料中提取硒的方法之一是用H2SO4和NaNO3处理废料,获得亚硒酸和少量硒酸,加入盐酸共
氧族元素的题
2 工业上从含硒的废料中提取硒的方法之一是用H2SO4和NaNO3处理废料,获得亚硒酸和少量硒酸,加入盐酸共热,硒酸被转化为亚硒酸:
2HCl+H2SeO4=H2SeO3+Cl2↑+H2O
再将SO2通入亚硒酸的溶液中,单质硒即析出.据此,下列叙述正确的是( )
A.H2SeO4氧化性弱于Cl2
B.二氧化硫的还原性强于Se
C.亚硒酸的氧化性弱于硫酸
D.析出1molSe需H2SeO3、SO2、H2O各1mol
但是不明白怎么选的,其他答案错在哪 ctjmly5101年前1
ctjmly5101年前1 -
 兰槿 共回答了16个问题
兰槿 共回答了16个问题 |采纳率93.8%A、错误.反应2HCl+H2SeO4=H2SeO3+Cl2↑+H2O,Se元素的价态降低,显氧化性,是氧化剂,Cl2是氧化产物,所以H2SeO4氧化性强于Cl2(氧化性:氧化剂大于氧化产物)
B、正确.SO2通入亚硒酸,有硒析出,则SO2被氧化成硫酸根,是还原剂,还原剂的还原性大于还原产物,还原产物是Se
C、错误.同B中,亚硒酸是氧化剂,而硫酸是氧化产物
D、错误.可以得到反应方程式H2SeO3 + 2SO2 + H2O = 2H2SO4 + Se,所以需要的是2mol的SO21年前查看全部
- (d如1d•崇明县二模)氢硒酸(HdSe)中硒元素的化合价为( )
(d如1d•崇明县二模)氢硒酸(HdSe)中硒元素的化合价为( )
A.-2
B.+1
C.+2
D.-1 514514lrg1年前1
514514lrg1年前1 -
 riverdspriver 共回答了21个问题
riverdspriver 共回答了21个问题 |采纳率90.5%解题思路:根据化合物的化学式H2Se,利用化合物中各元素的化合价代数和为0的原则,由化合物中氢元素为+1价,计算化合物中Se元素的化合价.设化合物H6Se中Se元素的化合价为x,根据化合物中各元素的化合价代数和为2,则有(+6)×6+x=2,解得x=-6;
故选9.点评:
本题考点: 化学式的书写及意义;有关元素化合价的计算.
考点点评: 根据化合物中各元素的化合价代数和为0,利用化合物的化学式可计算出其中未知的元素化合价.1年前查看全部
- 强酸的化学式高锰酸、盐酸、硫酸、硝酸、高氯酸、硒酸、氢溴酸、氢碘酸、氯酸 帮我写 出来!
 kid276769821年前1
kid276769821年前1 -
 右眼看尽世间冷暖 共回答了21个问题
右眼看尽世间冷暖 共回答了21个问题 |采纳率71.4%高锰酸HMnO4 盐酸HCl 硫酸H2SO4 硝酸HNO3 高氯酸HClO4 硒酸H2SeO4 氢溴酸HBr 氢碘酸HI 氯酸HClO3
希望采纳1年前查看全部
- 下列酸中酸性最强的是:A氢硫酸 B亚硫酸 C硒酸 D硫酸
 小李肥肠1年前7
小李肥肠1年前7 -
 lankan 共回答了16个问题
lankan 共回答了16个问题 |采纳率106.3%硒酸
中文名称:硒酸
英文名称:selenic acid
CAS No.:7783-08-6
分子式:H2SeO4
分子量:144.98
理化特性
主要成分:纯品
外观与性状:白色六方柱晶体,极易吸潮.
熔点(℃):58
沸点(℃):260(分解)
相对密度(水=1):2.95
溶解性:易溶于水,不溶于氨水,溶于硫酸.
主要用途:用作鉴别甲醇和乙醇的试剂,及硒盐制备.
其它理化性质:160
健康危害:本品吸湿性腐蚀性强.对眼睛、皮肤、粘膜和呼吸道有刺激作用.吸入、口服或经皮肤吸收中毒重者可致死.可引起化学性支气管炎、肺炎或肺水肿.慢性影响:可有头痛、眩晕、疲倦、食欲减退等表现.
燃爆危险:本品不燃,具强腐蚀性、强刺激性,可致人体灼伤.
危险特性:具有强氧化性与强酸性(均强于硫酸).其水溶液有腐蚀性和强烈的刺激性.1年前查看全部
- 用化学方程式来说明硒酸的一条化学性质
 memory_12141年前1
memory_12141年前1 -
 CHECAL 共回答了16个问题
CHECAL 共回答了16个问题 |采纳率81.3%硒酸
化学式H2SeO4,式量144.97.纯硒酸是无色六方柱晶体,相对密度为3.004,熔点为58℃(易过冷),沸点为260℃(分解),极易潮解,易溶于水,不易挥发,有毒!无水硒酸溶于水,其浓度可高达99%.溶于硫酸不溶于液氨,在乙醇中分解.其稀水溶液和硫酸的酸性接近,第一步也是完全电离的,K2=1.1×10-2(25℃).硒酸的氧化性强于硫酸,不但能氧化硫化氢、二氧化硫、I-,Br-等,中等浓度硒酸就能氧化Cl-,是强氧化剂,如:
H2SeO4+6H++6I-=Se+3I2+4H2O
H2SeO4+2H++2Cl-=SeO2+Cl2+2H2O
浓硒酸与盐酸混合有氯产生,故与王水一样,可溶解铂、金.热的无水硒酸不但能溶解银,也能溶解金.高浓度时,也能使有机物炭化,其氧化性强于浓硫酸.是常用的化学试剂,可用来制备硒酸盐,也用做测定甲醇或鉴别甲醇和乙醇的试剂.将亚硒酸盐与强氧化剂作用,如:
Ag2SeO3+Br2+H2O=2AgBr↓+H2SeO4
然后滤出沉淀溴化银,煮沸赶走多余的溴即得硒酸
硒酸和硫酸性质相似,但氧化性要比硫酸强,可以象王水一样溶解Au,Pt.碲酸的是弱酸,氧化性也不强.
2Au+6H2SeO4=Au2(SeO4)3+3H2SeO3+3H2O1年前查看全部
- 有机酸,磷酸(中强酸),亚硫酸(中强酸),高氯酸(最强含氧酸),硅酸(不溶性酸),氢卤酸,硒酸(比硫酸强),次氯酸(氧化
有机酸,磷酸(中强酸),亚硫酸(中强酸),高氯酸(最强含氧酸),硅酸(不溶性酸),氢卤酸,硒酸(比硫酸强),次氯酸(氧化性).硅酸,HF酸,亚硫酸等 乙酸 醋酸,磷酸.谁能分别介绍下?
 ydongls1年前1
ydongls1年前1 -
 dyn宝贝 共回答了15个问题
dyn宝贝 共回答了15个问题 |采纳率100%有机酸 有很多 如醋酸(乙酸)等
亚硫酸 有还原性
硅酸 十分弱的酸 不溶
次氯酸 光照下分解成氧气和氯化氢
氢氟酸 卤族元素组成氢化物的特殊一个 是弱酸
不过 可以和二氧化硅反应1年前查看全部
- (2007•宜昌)硒元素(Se)有防癌、抗癌作用.某饮料中含有FeSeO3(硒酸亚铁),则硒元素的化合价为( )
(2007•宜昌)硒元素(Se)有防癌、抗癌作用.某饮料中含有FeSeO3(硒酸亚铁),则硒元素的化合价为( )
A.-4
B.0
C.+3
D.+4 bosan7977991年前1
bosan7977991年前1 -
 lovebaby_z 共回答了17个问题
lovebaby_z 共回答了17个问题 |采纳率88.2%解题思路:根据硒酸亚铁的化学式为FeSeO3,利用铁元素和氧元素的化合价及化合物中正负化合价的代数和为0来解答.在FeSeO3中,由名称可知铁元素的化合价为+2价,氧元素的化合价为-2价,
设硒元素的化合价为x,
根据化合物中正负化合价的代数和为0,则
(+2)+x+(-2)×3=0
解得x=+4
故选D.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题考查化合价的计算,学生应熟悉常见元素在化合物中的化合价,并能用化合价计算的原则来进行计算.1年前查看全部
- 硒酸与烧碱发生中和反应的化学方程式
 dengzhitt88881年前3
dengzhitt88881年前3 -
 欣缘Q 共回答了15个问题
欣缘Q 共回答了15个问题 |采纳率93.3%H2SeO4+2NaOH=Na2SeO4+2H2O1年前查看全部
- “北大富硒康”中含有硒酸根离子 (SeO42-),则在硒酸根离子中的硒元素的化合价为
“北大富硒康”中含有硒酸根离子 (SeO42-),则在硒酸根离子中的硒元素的化合价为
a.+4价 b.+6价 c.-2价 d.-4价 blueautumn1年前1
blueautumn1年前1 -
 losic 共回答了21个问题
losic 共回答了21个问题 |采纳率85.7%B.+6价
SeO4 2- 这个化学式说明硒酸根离子比硒酸根多出2个电荷,O的化合价是-2,四个O会缺少8个电荷.为了满足空缺,两个电荷是外来的,那就还差6个电荷.所以硒为.+6价.1年前查看全部
- 氢硒酸放在空气中长气保存易变质是什么原因
 HAHO6251年前2
HAHO6251年前2 -
 hommver 共回答了18个问题
hommver 共回答了18个问题 |采纳率100%楼上说了半天,都没说到点子上,氧、硫、硒、碲、钋都属于元素周期表VIA族,该族元素自上而下得电子能力逐渐减弱,即氧化性逐渐减弱;氧、硫、硒的气态氢化物稳定性渐次减弱,还原性渐次增强.所以氢硒酸有较强的还原性,其还原性比氢硫酸,氢硫酸置于空气中被氧气氧化生成硫单质和水,同样,氢硒酸放在空气中,更易被空气中的氧气氧化,生成硒单质和水.硒的比重为水的四倍多,所以楼上说硒单质会漂浮在液体表面纯属杜撰!
请看以下“百度百科”中“氧族元素”的词条链接:1年前查看全部
- 硒元素(符号为Se),具有抗衰老、抑制癌细胞的功能,如图是硒原子的有关信息,其中硒酸H2SeO4与硫酸化学性质相似,请根
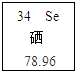 硒元素(符号为Se),具有抗衰老、抑制癌细胞的功能,如图是硒原子的有关信息,其中硒酸H2SeO4与硫酸化学性质相似,请根据相关知识填写下列空格:
硒元素(符号为Se),具有抗衰老、抑制癌细胞的功能,如图是硒原子的有关信息,其中硒酸H2SeO4与硫酸化学性质相似,请根据相关知识填写下列空格:
①硒酸Se的化合价______价;
②硒原子的原子核内的质子数为______;
③在含丰富硒的土壤上种植的白莲、甘薯、大米等,由于含丰富的硒被称为富硒产品,富硒产品中的“硒”指的是______(选填“元素”、“分子”或“原子”);
④这种硒酸与氢氧化钠的中和反应的化学方程式:______. 心情好一切都好1年前1
心情好一切都好1年前1 -
 mingfei606 共回答了21个问题
mingfei606 共回答了21个问题 |采纳率90.5%解题思路:①根据在化合物中正负化合价代数和为零,进行解答;
②根据图结合原子序数=核内质子数进行分析;
③由题意可知,富硒产品中的“硒”指的是元素,它存在于物质的化合物中;
④根据题中信息结合化学方程式的书写进行分析.①根据在化合物中正负化合价代数和为零,设H2SeO4中Se元素的化合价为x,则:(+1)×2+x+(-2)×4=0,解答x=+6;
②根据原子序数=核内质子数,硒原子的原子序数是34,因此硒原子的原子核内的质子数为34;
③由题意可知,富硒产品中的“硒”指的是元素;
④硒酸与氢氧化钠的中和反应的化学方程式2NaOH+H2SeO4=Na2SeO4+2H2O;
故答案为:①+6;②34;③元素;④H2SeO4+2NaOH═Na2SeO4+2H2O.点评:
本题考点: 元素周期表的特点及其应用;有关元素化合价的计算;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查学生根据化学式计算元素的化合价、元素周期表的有关知识以及化学方程式的书写等,难度不大.1年前查看全部
- (2006•西城区一模)葡萄含有丰富的非金属元素硒(Se),人体如果缺硒可能会引起皮肤病变.在硒酸(化学式为H2SeO4
(2006•西城区一模)葡萄含有丰富的非金属元素硒(Se),人体如果缺硒可能会引起皮肤病变.在硒酸(化学式为H2SeO4)中,Se元素的化合价是( )
A.+2价
B.+3价
C.+4价
D.+6价 爱情渣子1年前1
爱情渣子1年前1 -
 3802926 共回答了21个问题
3802926 共回答了21个问题 |采纳率100%解题思路:根据化合物的化学式H2SeO4,利用化合物中各元素的化合价代数和为0的原则,由化合物中氢为+1价、氧为-2价,计算化合物中Se元素的化合价.化合物中氢为+1价、氧为-2价,设化合物H2SeO4中Se元素化合价为x,依化合物中各元素化合价代数和为零的原则,有(+1)×2+x+(-2)×4=0,解之得x=+6;
故选D.点评:
本题考点: 有关元素化合价的计算.
考点点评: 根据化合物中各元素的化合价代数和为0,利用化合物的化学式可计算其中未知的元素化合价.1年前查看全部
- 硒酸根离子中,硒元素的化合价是多少?有化学式的.
硒酸根离子中,硒元素的化合价是多少?有化学式的.
硫酸根离子化学式:SeO右上角上是2-,右下角是4,说说怎么算, ddanfu1年前7
ddanfu1年前7 -
 panjun0203 共回答了13个问题
panjun0203 共回答了13个问题 |采纳率92.3%+6.氧元素的化合价是-2,有4个那么负化合价总和就是-8,为了保证离子带2个负电,那么Se就是+61年前查看全部
- 浓硒酸与浓硫酸谁的氧化性更强 为什么?
 佛生1年前1
佛生1年前1 -
 光头麦兜 共回答了14个问题
光头麦兜 共回答了14个问题 |采纳率85.7%应该是浓硫酸把
因为从元素周期表来说,S的非金属性比较强,所以高价S的氧化性应该更强些1年前查看全部
- 怎样提纯溶解在硒酸里面的黄金(含有其他金属)
 cc天使宝宝猪猪1年前1
cc天使宝宝猪猪1年前1 -
 feng1823 共回答了18个问题
feng1823 共回答了18个问题 |采纳率94.4%电解.1年前查看全部
- 硒酸比硫酸酸性强的原因书上说硒酸比硫酸酸性强,但是S在Se前,按常规来说应该是酸性应该是硫酸强,是Se原子发生什么特殊变
硒酸比硫酸酸性强的原因
书上说硒酸比硫酸酸性强,但是S在Se前,按常规来说应该是酸性应该是硫酸强,是Se原子发生什么特殊变化吗?请详细解释一下,好的加分. 天亦无几1年前1
天亦无几1年前1 -
 你谁是谁的谁 共回答了12个问题
你谁是谁的谁 共回答了12个问题 |采纳率100%在比较稀的溶液中,酸性是一样的.但是当硫酸浓度过28.4%时,硒酸的浓度将强于硫酸,的确它们的一级电离是完全的,但二级电离则硒酸稍大于硫酸,硒酸电离度是98.48%,硫酸电离度是97.2%-98.04.浓硒酸的氧化性高于硫酸,与硝酸混溶氧化金铂.
对于硒酸而言,这已是了不起的.因为按周期律来说应该是硫酸酸性强,实际上碲酸就是弱酸,而硒酸的酸性不逊于硫酸,这已是反常了.
另外,硒酸的氧化性比硫酸强.硒酸可以氧化氢氯酸为氯气.1年前查看全部
- 硫酸和硒酸哪个酸性更强?
 xiaotuzizhu1年前1
xiaotuzizhu1年前1 -
 hddxp 共回答了14个问题
hddxp 共回答了14个问题 |采纳率78.6%酸性差不多,但浓硒酸氧化性比浓硫酸强好多1年前查看全部
- 浓硒酸与盐酸混合产生黄绿色气体化学方程式是什么?
浓硒酸与盐酸混合产生黄绿色气体化学方程式是什么?
第三个回答里的H2SeO3貌似应该掰开成H2O和SeO2,谢谢各位 苍龙七宿-心宿1年前1
苍龙七宿-心宿1年前1 -
 gaowuchi 共回答了21个问题
gaowuchi 共回答了21个问题 |采纳率95.2%H2SeO4 (浓)+ 2 HCl ==== Cl2 ↑ + H2SeO3 +H2O1年前查看全部
- 硒酸和硫酸的酸性比较?如题硫酸更强吗?可是有的书上说硒酸比硫酸强啊我们的化学老师说差不多都是强酸但是作业里硬要我们比较.
 临水黯然1年前1
临水黯然1年前1 -
 huaweill 共回答了17个问题
huaweill 共回答了17个问题 |采纳率94.1%因为硫的非金属性更强,硫酸比硒酸强,而浓度而变化的吧.浓硫酸酸性不强,很稀的硫酸也弱1年前查看全部
- 硫酸与硒酸酸性强弱比较
 到處爬的抱抱熊1年前1
到處爬的抱抱熊1年前1 -
 爱没有理由 共回答了22个问题
爱没有理由 共回答了22个问题 |采纳率90.9%酸性:电离产生H+的能力,硫酸强于硒酸
氧化性:中心原子得电子的能力,硒酸强于硫酸.1年前查看全部
- 关于盐酸、硒酸、高铁酸的问题盐酸、硒酸、高铁酸都是强酸吗?它们性质都如何?把硒酸溶入浓盐酸,再将高铁酸溶入其中会怎样?等
关于盐酸、硒酸、高铁酸的问题
盐酸、硒酸、高铁酸都是强酸吗?它们性质都如何?
把硒酸溶入浓盐酸,再将高铁酸溶入其中会怎样?
等等,氯气不也溶于其中吗? dearcarrie1年前3
dearcarrie1年前3 -
 czc_1005 共回答了18个问题
czc_1005 共回答了18个问题 |采纳率100%硒酸和硫酸的性质相似,浓硒酸的氧化性比浓硫酸要强许多,热的浓硒酸可以溶解Cu、Ag和Au生成相应的硒酸盐.
你说的这三种酸都是强酸.
高铁酸具有强氧化性,也很不稳定.
以上正确.
50%硒酸即可氧化Cl-为Cl2,所以硒酸溶入浓盐酸就释放出氯气.
硒酸浓度问题——如果溶液中H+够多的话,H2SeO4的电离就会受到抑制.而且50%也不算很浓(一般说的浓硫酸的浓度要在70%以上).如果很稀的话才可能观察不到现象.
氯气溶解度——在水中也才能溶解2体积多一些.何况溶液强酸性又有大量Cl-,破坏了平衡(Cl2(aq)+H2O(l)=H+(aq)+ClO-(aq)+H+(aq)+Cl-(aq)),Cl2溶解度应该比在水中的更小.
高铁酸是氧化性最强的酸,放入浓盐酸中先与水反应生成氢氧化铁,氢氧化铁再和盐酸反应生成氯化铁和水1年前查看全部
大家在问
- 1问题"what did you say just now?"答案为什么用“I asked how Iopen the d
- 2请问有木有人会伽玛函数的积分?x用1-1/N代入,接下来怎么算啊?我数学很不咋地,
- 3例如一边是dv一边是dt,为了消去dv和dt可以用积分,为什么都是用定积分,不能用不定积分吗,也可以消去啊?虽说可能有范
- 4在某温度下,将2 mol A和3 mol B充入一密闭容器中,发生反应:aA(g)+B(g)C(g)+D(g),5
- 5床头捉刀人 魏武将见匈奴使,
- 6( )海填一个方位的字
- 7物理受平衡力时可能做匀速直线运动,方向如何?
- 8One warm day when I was walking in my backyard, I saw a pine
- 9德国诗人莱辛有这样一著名诗句“追求真理比占有真理更宝贵。”其所包含的哲学道理是 A.真理是具体的有条件的 B.改造世界比
- 10Suddenly it began to rain.to rain是什么句子成分,请说出理由,
- 11已知函数f(x)=(4x²-7)/(2-x),x∈[0,1],设a≥1,函数g(x)=x³-3a
- 12人鱼的旋律(一) 作文
- 13简述麦克斯韦电磁场理论建立的意义.
- 14二分之一加二分之一的二次方加二分之一的三次方以次类推到N次方结果用含N的算式表示
- 15如果旗杆在影子的西面,那么太阳在旗杆的( )面
