絮凝反应池后用什么沉淀池深度处理的沉淀池选用,地方足够大,用斜板害怕堵塞,一般在给水厂用斜板得多,污水中水回用用的多吗,
 自由水果2022-10-04 11:39:542条回答
自由水果2022-10-04 11:39:542条回答深度处理的沉淀池选用,地方足够大,用斜板害怕堵塞,一般在给水厂用斜板得多,污水中水回用用的多吗,有什么缺点

已提交,审核后显示!提交回复
共2条回复
 zouyuansen 共回答了14个问题
zouyuansen 共回答了14个问题 |采纳率100%- 我也是初步涉及该行业,就我厂而言,污水中水回用就是用的斜板沉淀池.用该池前提是你的絮凝剂要加足够量,设计的沉淀时间要足够,同时要根据实际情况,规定该沉淀池的及时排泥,防止长时间不排泥会发生堵塞现象.随时交流.
- 1年前
 拳脚无情 共回答了1个问题
拳脚无情 共回答了1个问题 |采纳率- 中水回用也有用斜板沉淀的,防止堵塞主要是在前期絮凝沉淀要做好,絮凝沉淀区的设计好了,就不会堵塞。
- 1年前
相关推荐
- 凝集和絮凝的过程有何区别?如何将两者结合使用?
 王舟田1年前1
王舟田1年前1 -
 humourousboy 共回答了14个问题
humourousboy 共回答了14个问题 |采纳率85.7%凝集要加入其它物质(如:水解凝集剂),使发酵液中的胶体脱离稳定状态而凝集;原因:表面电荷的简单中和、消除表明稳定的双电荷层、氢键缔合.絮凝是悬浮粒子间的相互作用.1年前查看全部
- 洗煤水絮凝后为什么上浮将聚丙烯酰胺溶解后按一定比例加入洗煤水中,絮凝后不沉淀却上浮,请专家指教
 gracekd1年前2
gracekd1年前2 -
 11nana 共回答了21个问题
11nana 共回答了21个问题 |采纳率95.2%请问楼主是大试的反应还是小试,小试在量筒里面是上浮的,如果是大试的话,可能聚丙烯酰胺的选型有问题,建议楼主可以在废水中加入少量聚铁,可以改善.1年前查看全部
- 高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝、助凝、杀菌、除臭为一体的新型高效多功能绿色水处理剂,具有良好的应用前景
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝、助凝、杀菌、除臭为一体的新型高效多功能绿色水处理剂,具有良好的应用前景.其生产工艺如图:

已知:
①2KOH+Cl2═KCl+KClO+H2O(条件:温度较低)
②6KOH+3C12═5KCl+KClO3+3H2O(条件:温度较高)
回答下列问题:
(1)该生产工艺应在______(填“温度较高”或“温度较低”)的情况下进行.
(2)写出工业上制取Cl2的化学方程式2NaCl+2H2O
2NaOH+H2↑+Cl2↑通电 .2NaCl+2H2O.
2NaOH+H2↑+Cl2↑通电 .
(3)写出Fe(NO3)3在强碱性条件下与KClO反应制K2FeO4的离子方程式______.
(4)在“反应液I”中加KOH固体的目的是______(填序号).
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3化为KClO
(5)从环境保护的角度看,制备Na2FeO4(实际应用中Na2FeO4可替代K2FeO4使用)较好的方法为电解法,其装置如图Ⅰ所示.
①电解过程中阳极的电极反应式为______.
②图Ⅰ装置中的电源采用NaBH4(硼元素的化合价为+3)和H2O2作原料的燃料电池,电源工作原理如图Ⅱ所示.工作过程中该电源的正极反应式为______. 小良小富1年前1
小良小富1年前1 -
 whataboyyboy 共回答了20个问题
whataboyyboy 共回答了20个问题 |采纳率95%解题思路:(1)由工艺流程及③可知,利用Fe(NO3)3与KClO制备K2FeO4,由信息②可知温度较高KOH与Cl2 反应生成的是KClO3;
(2)工业是利用电解饱和食盐水制取氯气;
(3)次氯酸跟有强氧化性;
(4)由工艺流程可知,反应液I中有过量的Cl2反应,生成更多的KClO;
(5)①Na2FeO4能消毒、净水的原因高价铁具有氧化性,能消毒杀菌,生成Fe3+形成胶体,具有吸附悬浮物的净水的作用,电解时阳极Fe失电子发生氧化反应,电极反应方程式为Fe+8OH--6e-═FeO42-+4H2O
②正极H2O2发生还原反应,得到电子被还原生成OH-.(1)由工艺流程及③可知,利用Fe(NO3)3与KClO制备K2FeO4,由信息②可知温度较高KOH与Cl2 反应生成的是KClO3.由信息①可知,在低温下KOH与Cl2 反应生成的是KClO.故选择低温较低,故答案为:温度较低;
(2)工业是利用电解饱和食盐水制取氯气.反应方程式为:2NaCl+2H2O
通电
.
2NaOH+H2↑+Cl2↑,故答案为:2NaCl+2H2O
通电
.
2NaOH+H2↑+Cl2↑;
(3)次氯酸跟有强氧化性,嫩将三价铁离子氧化为高铁酸根,离子方程式:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5 H2O,故答案为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5 H2O;
(4)由工艺流程可知,反应液I中有过量的Cl2反应,加KOH固体的目的是与过量的Cl2继续反应,生成更多的KClO.
A.与过量的Cl2继续反应,生成更多的KClO,故A正确;
B.由信息②可知温度较高KOH与Cl2 反应生成的是KClO3,不利用KClO生成、浪费原料,故B错误;
C.由工艺流程及③可知,利用Fe(NO3)3与KClO制备K2FeO4,故C正确;
D.由信息可知,该条件下KClO3 不能转化为KClO,故D错误.
故选:AC;
(5)①Na2FeO4能消毒、净水的原因高价铁具有氧化性,能消毒杀菌,生成Fe3+形成胶体,具有吸附悬浮物的净水的作用,电解时阳极Fe失电子发生氧化反应,电极反应方程式为Fe+8OH--6e-═FeO42-+4H2O;
故答案为:Fe+8OH--6e-═FeO42-+4H2O;
②NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,正极上H2O2发生还原反应,得到电子生成OH-,其电极反应为:H2O2+2e-=2OH-;
故答案为:H2O2+2e-=2OH-.点评:
本题考点: 物质分离和提纯的方法和基本操作综合应用;电解原理.
考点点评: 本题考查学生阅读题目获取信息的能力、对工艺流程的理解与条件的控制、对物质的量浓度理解、原电池和电解池原理等,难度中等,需要学生具有扎实的基础知识与灵活运用知识解决问题的能力,注意基础知识的掌握.1年前查看全部
- 有机高分子混凝剂,主要是由于以下哪些作用,促进水中颗粒物絮凝的
有机高分子混凝剂,主要是由于以下哪些作用,促进水中颗粒物絮凝的
a压缩双电层b吸附架桥作用c吸附电中和d沉淀物的网捕作用 o9jj1年前1
o9jj1年前1 -
 dingfp 共回答了20个问题
dingfp 共回答了20个问题 |采纳率95%吸附架桥作用c吸附电中和d沉淀物的网捕作用1年前查看全部
- 加药絮凝处理含煤废水热电厂常用的加絮凝剂絮凝沉淀过滤处理寒梅废水的成本怎样?平均处理每吨水的成本大概是多少?
 kk箭8881年前1
kk箭8881年前1 -
 helensang 共回答了13个问题
helensang 共回答了13个问题 |采纳率100%看你水里面SS怎么样了,SS高的话混凝剂加的比较多一点,混凝絮凝也可能多级,这样成本会高一些,一般来说吨水费用2毛以内1年前查看全部
- 聚铝 絮凝后沉淀怎么处理混凝沉淀法处理污水后,沉淀一般 是怎么处理的.如果只是一般的填埋,那不是只是将污染转移了么?因为
聚铝 絮凝后沉淀怎么处理
混凝沉淀法处理污水后,沉淀一般 是怎么处理的.如果只是一般的填埋,那不是只是将污染转移了么?
因为絮凝本身只是个物理吸附过程,并没有像生化法一样将污水中的污染物给分解利用了 yuan13311231年前1
yuan13311231年前1 -
 ejine 共回答了16个问题
ejine 共回答了16个问题 |采纳率68.8%没有像生化法一样将污水中的污染物给分解,压缩后就是环保废渣,这样的废渣一般很好卖的,有专门人会回收的.也可以有其他处理方式,因为处理的水质不同,所以可行度不是统一的1年前查看全部
- 怎样优化絮凝剂的絮凝效果
 非洲的秋千1年前1
非洲的秋千1年前1 -
 city_time 共回答了20个问题
city_time 共回答了20个问题 |采纳率75%混凝原理:压缩双电层作用、吸附架桥作用.脱稳的胶粒相互聚结,称为凝聚;由高分子物质吸附架桥作用而使微粒相互粘结的过程,称为絮凝.凝聚和絮凝总称为混凝.
影响混凝效果的主要因素有:水温、水质、水力条件、混凝剂的种类和用量等.
1、水温.水温低时,无机盐混凝剂水解(吸热反应)困难;同时,水温低,粘度大,不利于脱稳胶体相互絮凝.因此,因保证适宜的水温.
2、PH值.不同的混凝剂,只使用一定的PH值范围.如采用硫酸铝混凝剂,在PH为5.7.8时效果较好;PH较高时,生成的氢氧化铝被溶解成偏铝酸盐,从而失去混凝作用.
3、水力条件.混凝过程可分为混合和反应阶段.混合阶段要求快速和剧烈搅拌,是药剂迅速均匀地扩散到全部水中以创造良好的水解和聚合条件,使胶体脱稳并借助胶体的布朗运动和紊动水流进行凝聚.但是,对于高分子混凝剂,混合的作用主要是使药剂在水中均匀分散,对“快速”和“剧烈”要求并不重要.
4、混凝剂的种类和用量.处理不同种类的废水应该选择不同的混凝剂,而混凝剂的用量则按水的浓度及分离要求决定.1年前查看全部
- a2o 工艺 出水水质变差水厂采用倒置a2o工艺,处理每天4万吨.工艺为 进水-水解酸化-缺氧-厌氧-好氧-二沉池-絮凝
a2o 工艺 出水水质变差
水厂采用倒置a2o工艺,处理每天4万吨.工艺为 进水-水解酸化-缺氧-厌氧-好氧-二沉池-絮凝沉淀池(进池之前可投药品聚铝,但效果不好很久不用了)-加氯消毒槽-出水.目前每天进水量控制在3.6万左右,进水cod400,bod/cod为0.3左右,氨氮20--30mg/L,出水标准一级B.昨天进水进了一股酸性废水,水量大约3000方,PH为4左右(平时一般为7左右).今天出水cod偏高,测得数值为56mg/L,而且不断增高到60多,出水超标.出水ss较高,水有点发黄(平时出水cod在50以下),出水氨氮很正常,今天测得曝气池污泥浓度为5300mg/L,SV30为 45%,都比较正常(和平时差不多),沉降速度比较快,但上清液有小絮状颗粒,上面还有漂浮的像油状的一些漂浮物.曝气池也有浮泥,回流污泥有点发白,水面上也有漂浮的油状小颗粒.
1.设计污泥负荷为0.085,设计污泥浓度为4000,但运行中5500也比较正常,只是有不少浮泥,镜检一般是轮虫较多,很少见到钟虫.请问是污泥浓度过高吗?是不是负荷太低了
2.目前我采取措施是减少进水量,减少了回流比为100%(平时回流是200%),以增加好氧停留时间.因风机故障目前只能使用唯一一台.
3.每天都在排剩余污泥,但不知道如何控制该排除多少,所有经常搞得污泥浓度不太稳定,但维持在5000以上.请问如何计算该排出多少污泥?
4.请高手和专家提出其他运行建议,. 爱上雷丝的小猪1年前1
爱上雷丝的小猪1年前1 -
 燕七1 共回答了14个问题
燕七1 共回答了14个问题 |采纳率78.6%我的意见是:1,你没有提到磷的问题,
2,没有提到溶解氧的问题;
3,微生物镜检,按你说的应该有问题了,应该知道,钟虫对好氧法的作用,
4,污泥浓度不太稳定的原因应该和生产环节有关,总进水前没有设调节池吗,
5,我认为污泥量降低是负荷小的原因;
6,不能只注意BOD/COD的比值,还应该注意N/P比值,怎样提高降解率,条件很多的,污泥颜色发白,我的印象是泥龄问题
7,有漂浮污泥,表面上看是沉降问题,实际上和曝气量、N/P比,回流比等多重因素有关.每天的物理控制量要根据你自己的实际情况才能确定,1年前查看全部
- PAM絮凝的最佳ph值范围是多少
 小被儿1年前1
小被儿1年前1 -
 qq45854092 共回答了17个问题
qq45854092 共回答了17个问题 |采纳率88.2%PH=7-91年前查看全部
- 高铁酸钾(K 2 Fe0 4 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂,其生产工艺如下:
高铁酸钾(K 2 Fe0 4 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂,其生产工艺如下:

已知:2Fe(NO 3 ) 3 +3KClO+10KOH=2K 2 FeO 4 +6KNO 3 +3KCl+5H 2 O
回答下列问题 :
(1)将Cl 2 通入KOH溶液中发生反应的离子方程式是____________。
(2)写出工业上制取Cl 2 的化学方程式____________。
(3)在“反应液I”中加入KOH固体的目的是____________。
(4)K 2 FeO 4 可作为新型多功能水处理剂的原因是____________。
(5)配制KOH溶液时,将61.6g KOH固体溶解在100 mL水中,所得溶液的密度为1.47 g • mL - 1 ,则该溶液的物质的量浓度为____________。
(6)从“反应液II”中分离出K 2 Fe0 4 后,副产品是___________ (写化 学 式)。
(7)该工艺每得到1.98kgK 2 FeO 4 ,理论上消耗Cl 2 的物质的量为______mol。 愚若智1年前1
愚若智1年前1 -
 QWE4123ASD 共回答了10个问题
QWE4123ASD 共回答了10个问题 |采纳率90%1年前查看全部
- 聚合氯化铝(PAC)絮凝机理是什么?
 卡欧斯1年前2
卡欧斯1年前2 -
 cnawen75 共回答了17个问题
cnawen75 共回答了17个问题 |采纳率88.2%对水中胶体及颗粒物具有高度电中和桥联功能,并可强力去除金属离子,性状稳定.在水中与胶体颗粒所带的负电荷瞬间产生中和作用,使胶体脱稳,胶体颗粒迅速絮凝,并进一步架桥生成大絮团而快速沉淀.1年前查看全部
- 污水为什么只有经过二次絮凝才清澈
污水为什么只有经过二次絮凝才清澈
采用一次絮凝,不管加多少药出水都有色度,如果将出水在加少量相同的药剂后,出水就清了,这是为什么呢? 塔塔s1年前1
塔塔s1年前1 -
 xiaomangzhou 共回答了14个问题
xiaomangzhou 共回答了14个问题 |采纳率85.7%污水不是只有经过二次絮凝才清澈,一次絮凝到二次絮凝之间通常指折点,就是到了絮凝的剂量,此刻絮体粗大在重力的作用下沉降,去除的是细小颗粒性悬浮物,而水色指色度是附着在水体中不能去除,那么经过二次絮凝即逐级的处理才使水色降低.1年前查看全部
- (2014•莆田)材料一:传统水处理工艺-经典“四部曲”(①过滤②絮凝③消毒④沉淀),被列为人类20世纪最重要的发明之一
(2014•莆田)材料一:传统水处理工艺-经典“四部曲”(①过滤②絮凝③消毒④沉淀),被列为人类20世纪最重要的发明之一.为了提高水质,有些水厂增加了活性炭处理工序.
材料二:《生活饮用水卫生标准》中,允许使用的消毒剂有Cl2,NH2Cl(一氯铵),O3,ClO2;水的总硬度(以CaCO3计)不超过450mg/L.
(1)活性炭处理工艺中,主要利用活性炭具有______能力;
(2)“四部曲”正确的工艺顺序为______(填序号);
(3)四种消毒剂中,属于单质的是______;
(4)若以Ca2+计,水的总硬度不超过______mg/L. 琳心零星1年前1
琳心零星1年前1 -
 jianbukan8 共回答了22个问题
jianbukan8 共回答了22个问题 |采纳率90.9%解题思路:根据已有的知识进行分析,活性炭具有吸附性;根据净化水的程度进行解答;单质是由一种元素组成的纯净物;根据题干提供的数据进行计算.(1)活性炭具有吸附性能吸附色素和异味,故填:吸附;
(2)净化水时,要先除去颗粒大的杂质,使用絮凝剂明矾,然后沉降后再进行过滤;最后消毒,故填:②④①③;
(3)氯气和臭氧是由一种元素组成的纯净物,属于单质,故填:Cl2、O3;
(4)碳酸钙中钙离子的含量为:
40
100×100%=40%,故以Ca2+计,水的总硬度不超过450mg/L×40%=180mg/L,故填:180.点评:
本题考点: 自来水的生产过程与净化方法;单质和化合物的判别;碳单质的物理性质及用途;化合物中某元素的质量计算.
考点点评: 本题考查了水的净化、根据化学式的计算等知识,了解相关知识是解答的关键.1年前查看全部
- 聚丙烯酰胺在100度高温下能加入,能长时间起到絮凝作用吗?
 海蓝贝壳1年前3
海蓝贝壳1年前3 -
 神仙老头 共回答了24个问题
神仙老头 共回答了24个问题 |采纳率91.7%不能
高于60度,就很容易降解了.1年前查看全部
- 高铁酸钾(K 2 FeO 4 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。工业上常采用NaClO氧化法生产,其
高铁酸钾(K 2 FeO 4 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。工业上常采用NaClO氧化法生产,其生产工艺如下:

主要反应为:3NaClO+2Fe(NO 3 ) 3 +10NaOH = 2Na 2 FeO 4 ↓+3NaCl+6NaNO 3 +5H 2 O
Na 2 FeO 4 +2KOH=K 2 FeO 4 +2NaOH。
(1)写出反应①的离子方程式: 。
(2)从“混合物II”中分离出K 2 FeO 4 后,会有副产品,它们都是重要的化工产品,其中一种在工业上用作氯碱工业原料的物质是 。
(3)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。图Ⅰ为不同的温度下,Fe(NO 3 ) 3 不同质量浓度对K 2 FeO 4 生成率的影响;图Ⅱ为一定温度下,Fe(NO 3 ) 3 质量浓度最佳时,NaClO浓度对K 2 FeO 4 生成率的影响。
图Ⅰ 图Ⅱ
根据上图分析:工业生产中最佳温度为 ℃,此时Fe(NO 3 ) 3 与NaClO两种溶液最佳质量浓度之比为 。 小hei1年前1
小hei1年前1 -
 alexgen01 共回答了16个问题
alexgen01 共回答了16个问题 |采纳率93.8%(1)Cl 2 +2OH - =Cl - +ClO - +H 2 O (2)NaCl (3)① 26 1.2
1年前查看全部
- 芬顿试剂处理完废水,调完pH絮凝时有大量小气泡,是我用的双氧水过量还是比例有问题?废水的COD为7680mg/L,我用的
芬顿试剂处理完废水,调完pH絮凝时有大量小气泡,是我用的双氧水过量还是比例有问题?废水的COD为7680mg/L,我用的30%双氧水的体积分别为3,4,5,6毫升,亚铁离子跟双氧水的摩尔比是1:8,1:10,1:12,1:20,1:30,1:6,1:5,1:1都试过,1:6以上的调碱后沉淀很多,絮凝效果不好,处理效果也不好.6ml双氧水1:10时处理效果最好能达到50%,但絮凝时有小气泡很是影响絮凝所用的时间.摩尔比为1:10时,双氧水用3,4,5毫升都试过了,有气泡,请问那些小气泡是双氧水在碱性条件下分解的氧吗?怎么解决气泡问题,好让絮凝效果更好?
 淡淡云起1年前1
淡淡云起1年前1 -
 uhx2dn 共回答了22个问题
uhx2dn 共回答了22个问题 |采纳率95.5%你在加双氧水的时候废水ph是多少,反应完以后ph调到了多少,然后你取处理废水水样是1ml吗?还有30%的芬顿处理你这个cod的废水,低于5ml效果是不佳的,理论的cod:H2O2=1:2.13,说实话,你这个cod用芬顿,简直就是土豪,哈哈1年前查看全部
- 高铁酸钾是一种高效的多功能水处理剂,具有氧化、吸附、絮凝、、助凝、杀菌、除臭等作用,高铁酸钾的开发和利用正日益显示出其广
高铁酸钾是一种高效的多功能水处理剂,具有氧化、吸附、絮凝、、助凝、杀菌、除臭等作用,高铁酸钾的开发和利用正日益显示出其广阔的应用前景。其制备路线如下:


试回答下列问题
(1)操作①搅拌的目的是:_______________________。
(2)操作③名称是:______________________________。
(3)次氯酸钠浓度对高铁酸钾产率有一定影响,当高铁酸钾产率最高时,NaClO的物质的量浓度约为;_________。配制该质量浓度的溶液所需的玻璃仪器有:__________________。
(4)反应器中,NaOH、NaClO及Fe(NO 3 ) 3 反应的化学方程式:
_____________________________________________________ 芭比娃娃之可爱版1年前1
芭比娃娃之可爱版1年前1 -
 xiangnidejing 共回答了13个问题
xiangnidejing 共回答了13个问题 |采纳率92.3%1年前查看全部
- 高铁酸钾( K 2 FeO 4 )是一种集强氧化性、吸附、絮凝于一体的新型多功能水处理剂,生产工艺如下: 已
高铁酸钾( k 2 feo 4 )是一种集强氧化性、吸附、絮凝于一体的新型多功能水处理剂,生产工艺如下: 
已知:
①温度较低时:2koh+cl 2 =kcl+kclo+h 2 o
②温度较高时:6koh+3cl 2 =5 kcl+kclo 3 +3h 2 o
③fe(no 3 ) 3 +kclo+koh→k 2 feo 4 +kno 3 +kcl+h 2 o(未配平)
(1)该生产应在温度________的情况下进行(填“较高”或“较低”);
(2)请配***应③:
口fe(no 3 ) 3 +口kclo+口koh→口k 2 feo 4 +口kno 3 +口kcl+h 2 o
(3) k 2 feo 4 具有强氧化性的原因为___________;
(4)在“反应液i”中加koh固体的目的是____________;
a.为下一步反应提供反应物
b.与“反应液i”中过量的cl 2 继续反应,生成更多的kclo
c.koh同体溶解时会放出较多的热量,有利于提高反应速率
d.使副产物kclo 3 转化为kclo
(5)从“反应液Ⅱ”中分离出k 2 feo 4 晶体后,可以得到的副产品有 ____(写化学式)。 gf0bc1年前1
gf0bc1年前1 -
 ede2005 共回答了16个问题
ede2005 共回答了16个问题 |采纳率87.5%(1)较低
(2) 2Fe(NO 3 ) 3 +3KClO+10KOH=2K 2 FeO 4 + 6KNO 3 +3KCl+5H 2 O
(3)Fe元素化合价为+6价,易得电子
(4)AB
(5)KNO 3 、KCl1年前查看全部
- 高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.利用Fe(NO2)3、NaClO和KOH等为
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.利用Fe(NO2)3、NaClO和KOH等为原料制备高铁酸钾的生产流程如下:

已知:NaOH和NaClO的混合液是通过氯气和烧碱溶液反应制取的.
(1)第①步所加人的混合液中仅含三种溶质,除NaOH和NaClO外,还含有______ (填化学式)
(2)写出第①步中Na0H、NaC10与Fe(NQ3)3发生反应的离子方程式:______
(3)Fe(NO2)3溶液的浓度对产品的产率有较大的影响,现要配制1000mL5mol.L-Fe(NO3)3溶液,需要的玻璃仪器有量筒、烧杯、______、______、______.第③步说明此温度下K2FeO4的溶解度______(填“>”、“<”或“=”)Na2FeO4的溶解度.
(4)若第②步所加NaOH溶液中含有160g NaOH.实验结束后,将第②、③步所得滤液以及第④步所得洗涤液全部收集,恰好可得8L混合液,测得其中Na+浓度为2.5mol.L-,则理论上制得的纯K2FeO4的质量为______.(假定各步均恰好反应完全) 兵爷爷1年前1
兵爷爷1年前1 -
 szmay2007 共回答了21个问题
szmay2007 共回答了21个问题 |采纳率95.2%解题思路:硝酸铁溶液中加入氢氧化钠和次氯酸钠反应得到氯化钠高铁酸钠的混合溶液,加入氢氧化钠蒸发浓缩冷却结晶,过滤洗涤得到高铁酸钠固体,在固体中加入饱和氢氧化钾溶液过滤得到高铁酸钾粗产品,经过重结晶洗涤干燥得到较纯的K2FeO4;
(1)第①步所加人的混合液中仅含三种溶质,除NaOH和NaClO外,还应含有NaCl;
(2)第①步中Na0H、NaC10与Fe(NQ3)3发生反应生成高铁酸盐和氯离子;
(3)依据溶液配制的步骤和过程分析判断需要的玻璃仪器;
(4)第②步所加NaOH溶液中含有160g NaOH物质的量为4mol,恰好可得8L混合液,测得其中Na+浓度为2.5mol.L-1,钠元素物质的量=8L×2.5mol/L=20mol,依据氯元素守恒可知,第一步含有钠元素16mol,结合化学方程式中定量关系,每生成3molClO-离子,同时生成3molNaCl,即每2molFe3+参加费用的NaClO为3mol,NaOH为10mol,同时有3molNaCl混在原氢氧化钠和次氯酸钠呵呵溶液中,原Fe(NO3)3为2mol;则K2FeO4为2mol;硝酸铁溶液中加入氢氧化钠和次氯酸钠反应得到氯化钠高铁酸钠的混合溶液,加入氢氧化钠蒸发浓缩冷却结晶,过滤洗涤得到高铁酸钠固体,在固体中加入饱和氢氧化钾溶液过滤得到高铁酸钾粗产品,经过重结晶洗涤干燥得到较纯的K2FeO4;
(1)第①步所加人的混合液中仅含三种溶质,除NaOH和NaClO外,还应含有NaCl;
故答案为:NaCl;
(2)第①步中Na0H、NaC10与Fe(NQ3)3发生反应生成高铁酸盐和氯离子,反应的离子方程式为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O;
故答案为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O;
(3)依据溶液配制的步骤和过程分析判断需要的玻璃仪器,要配制1000mL5mol.L-Fe(NO3)3溶液,需要的玻璃仪器有量筒、烧杯、1000ml容量瓶、胶头滴管、玻璃棒;第③步是Na2FeO4转化为K2FeO4,说明此温度下K2FeO4的溶解度小于Na2FeO4;
故答案为:1000ml容量瓶、胶头滴管、玻璃棒;<;
(4)第②步所加NaOH溶液中含有160g NaOH物质的量为4mol,恰好可得8L混合液,测得其中Na+浓度为2.5mol.L-1,钠元素物质的量=8L×2.5mol/L=20mol,依据氯元素守恒可知,第一步含有钠元素16mol,结合化学方程式中定量关系,每生成3molClO-离子,同时生成3molNaCl,即每2molFe3+参加费用的NaClO为3mol,NaOH为10mol,同时有3molNaCl混在原氢氧化钠和次氯酸钠呵呵溶液中,原Fe(NO3)3为2mol;则K2FeO4为2mol,质量=2mol×198g/mol=396g;
故答案为:396g;点评:
本题考点: 物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题考查了物质提纯的理解应用,实验基本操作,物质性质的分析应用,注意离子方程式书写方法和化学方程式计算,掌握基础是关键,题目难度中等.1年前查看全部
- 重复加PAC和PAM会不会对絮凝效果有影响
重复加PAC和PAM会不会对絮凝效果有影响
现有一工程是这样设计的:生化出水加PAC和PAM后沉淀,沉淀污泥回流自生化池曝气.调试过程中二沉池出水有很多悬浮物.后在二沉池后再加了一套气浮,同样加的PAC和PAM,气浮出水悬浮物依然很多.在这个系统中,污泥加药沉淀后回流被曝气打散,后又加药沉淀,很多物质没有沉下来的,又加同样的药剂气浮,结果依然不令人满意.我想请教一下这种现象是不是由于药剂添加问题引起的? notice1年前1
notice1年前1 -
 恩希1 共回答了13个问题
恩希1 共回答了13个问题 |采纳率100%估计会吧.一般都是试验确定加PAC和PAM的
而且一般就加PAM在污泥调试的时候.
你在www.***.org问一下嘛1年前查看全部
- 我们活性污泥结构松散,絮凝差,排放水浑浊,其中还夹杂着许多细小的污泥颗粒,这是什么原因?
我们活性污泥结构松散,絮凝差,排放水浑浊,其中还夹杂着许多细小的污泥颗粒,这是什么原因?
我们的污泥结构松散,菌胶团生长不好,请问哪位大师可以给我讲下怎样的环境利于菌胶团的生长?菌胶团生长好了,是否我们的水质浑浊的情况能够好转?,
怎样的环境适合菌胶团的生长繁殖? 冰是睡着的水么1年前1
冰是睡着的水么1年前1 -
 huair_321 共回答了23个问题
huair_321 共回答了23个问题 |采纳率87%菌胶团生长好了,水质浑浊的情况能够好转,可以测定曝气池的溶解氧,小于2.0mg/l或B/C比低也是好氧菌活性差的原因.1年前查看全部
- 水处理中聚合氯化铝絮凝效果不佳的原因是什么?
水处理中聚合氯化铝絮凝效果不佳的原因是什么?
在水处理当中```加药量是一致的```原水流量也是差不多的```为什么所起的效果会不同````一个池的矾花很好````另一个池就没有效果?
水源是相同的````可是确实出现了这样的问题````我也是考虑了很久```也查过加药的管子````药确实加进去的```可是效果就是不能达到一致````一边效果好的沉淀池的浊度是0.5左右```差的那边的浊度有1.3````
我想了很久都想不出为什么会这样````
希望这方便懂的朋友可以帮我解释一下```谢了```` slowleen1年前4
slowleen1年前4 -
 130hongfei 共回答了13个问题
130hongfei 共回答了13个问题 |采纳率92.3%楼主用的是干粉的还是液体的,聚合氯化铝的反应架桥出矾花需要一点时间,如果你用的货没有问题,那么你就必须保证所有的条件都相同,加药时间、搅拌速度、原水PH等等.我觉得应该是出在搅拌的问题上,建议楼主将絮凝不好的那个池子搅拌调整一下.1年前查看全部
- 电镀污水还原后加PAM为何产生不了絮凝
 紫梦萌1年前4
紫梦萌1年前4 -
 alan3 共回答了18个问题
alan3 共回答了18个问题 |采纳率83.3%还原后废水ph是好多,一般8.5以上加PAM才有会出现絮凝现象1年前查看全部
- 高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.利用Fe(NO2)3、NaClO和KOH等为
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.利用Fe(NO2)3、NaClO和KOH等为原料制备高铁酸钾的生产流程如下:

已知:NaOH和NaClO的混合液是通过氯气和烧碱溶液反应制取的.
(1)第①步所加人的混合液中仅含三种溶质,除NaOH和NaClO外,还含有______ (填化学式)
(2)写出第①步中Na0H、NaC10与Fe(NQ3)3发生反应的离子方程式:______
(3)Fe(NO2)3溶液的浓度对产品的产率有较大的影响,现要配制1000mL5mol.L-Fe(NO3)3溶液,需要的玻璃仪器有量筒、烧杯、______、______、______.第③步说明此温度下K2FeO4的溶解度______(填“>”、“<”或“=”)Na2FeO4的溶解度.
(4)若第②步所加NaOH溶液中含有160g NaOH.实验结束后,将第②、③步所得滤液以及第④步所得洗涤液全部收集,恰好可得8L混合液,测得其中Na+浓度为2.5mol.L-,则理论上制得的纯K2FeO4的质量为______.(假定各步均恰好反应完全) 123456abc1年前1
123456abc1年前1 -
 水平21 共回答了19个问题
水平21 共回答了19个问题 |采纳率89.5%解题思路:硝酸铁溶液中加入氢氧化钠和次氯酸钠反应得到氯化钠高铁酸钠的混合溶液,加入氢氧化钠蒸发浓缩冷却结晶,过滤洗涤得到高铁酸钠固体,在固体中加入饱和氢氧化钾溶液过滤得到高铁酸钾粗产品,经过重结晶洗涤干燥得到较纯的K2FeO4;
(1)第①步所加人的混合液中仅含三种溶质,除NaOH和NaClO外,还应含有NaCl;
(2)第①步中Na0H、NaC10与Fe(NQ3)3发生反应生成高铁酸盐和氯离子;
(3)依据溶液配制的步骤和过程分析判断需要的玻璃仪器;
(4)第②步所加NaOH溶液中含有160g NaOH物质的量为4mol,恰好可得8L混合液,测得其中Na+浓度为2.5mol.L-1,钠元素物质的量=8L×2.5mol/L=20mol,依据氯元素守恒可知,第一步含有钠元素16mol,结合化学方程式中定量关系,每生成3molClO-离子,同时生成3molNaCl,即每2molFe3+参加费用的NaClO为3mol,NaOH为10mol,同时有3molNaCl混在原氢氧化钠和次氯酸钠呵呵溶液中,原Fe(NO3)3为2mol;则K2FeO4为2mol;硝酸铁溶液中加入氢氧化钠和次氯酸钠反应得到氯化钠高铁酸钠的混合溶液,加入氢氧化钠蒸发浓缩冷却结晶,过滤洗涤得到高铁酸钠固体,在固体中加入饱和氢氧化钾溶液过滤得到高铁酸钾粗产品,经过重结晶洗涤干燥得到较纯的K2FeO4;
(1)第①步所加人的混合液中仅含三种溶质,除NaOH和NaClO外,还应含有NaCl;
故答案为:NaCl;
(2)第①步中Na0H、NaC10与Fe(NQ3)3发生反应生成高铁酸盐和氯离子,反应的离子方程式为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O;
故答案为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O;
(3)依据溶液配制的步骤和过程分析判断需要的玻璃仪器,要配制1000mL5mol.L-Fe(NO3)3溶液,需要的玻璃仪器有量筒、烧杯、1000ml容量瓶、胶头滴管、玻璃棒;第③步是Na2FeO4转化为K2FeO4,说明此温度下K2FeO4的溶解度小于Na2FeO4;
故答案为:1000ml容量瓶、胶头滴管、玻璃棒;<;
(4)第②步所加NaOH溶液中含有160g NaOH物质的量为4mol,恰好可得8L混合液,测得其中Na+浓度为2.5mol.L-1,钠元素物质的量=8L×2.5mol/L=20mol,依据氯元素守恒可知,第一步含有钠元素16mol,结合化学方程式中定量关系,每生成3molClO-离子,同时生成3molNaCl,即每2molFe3+参加费用的NaClO为3mol,NaOH为10mol,同时有3molNaCl混在原氢氧化钠和次氯酸钠呵呵溶液中,原Fe(NO3)3为2mol;则K2FeO4为2mol,质量=2mol×198g/mol=396g;
故答案为:396g;点评:
本题考点: 物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题考查了物质提纯的理解应用,实验基本操作,物质性质的分析应用,注意离子方程式书写方法和化学方程式计算,掌握基础是关键,题目难度中等.1年前查看全部
- 1、在测氨氮时,预处理絮凝沉淀时ph值为调至10.5左右?2、在过滤时为什么要弃去20ml滤液?3、如何提高校准
 娜娜52671年前1
娜娜52671年前1 -
 185054619 共回答了21个问题
185054619 共回答了21个问题 |采纳率90.5%1、这是因为你加入絮凝剂在该pH值下才会有最优的絮凝效果,这个是必须要做到的.
2、这主要是考虑避免滤纸中组分对氨氮测试效果的影响;
3、不知道你说的校准是哪一步的校准,但是为了测准氨氮,其实有很多的细节注意,你可以参照我下面的回答.1年前查看全部
- 高铁酸钾(K 2 FeO 4 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.工业上常采用NaClO氧化法生产,其
高铁酸钾(K 2 FeO 4 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.工业上常采用NaClO氧化法生产,其生产工艺如下: 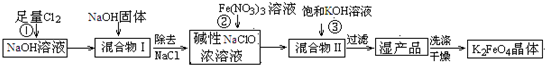
主要反应为:3NaClO+2Fe(NO 3 ) 3 +10NaOH=2Na 2 FeO 4 ↓+3NaCl+6NaNO 3 +5H 2 ONa 2 FeO 4 +2KOH=K 2 FeO 4 +2NaOH.
(1)写出反应①的离子方程式: .
(2)从“混合物II”中分离出K 2 FeO 4 后,会有副产品 (写化学式),它们都是重要的化工产品,具体说出其中一种物质的用途 .
(3)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响.图Ⅰ为不同的温度下,Fe(NO 3 ) 3 不同质量浓度对K 2 FeO 4 生成率的影响;图Ⅱ为一定温度下,Fe(NO 3 ) 3 质量浓度最佳时,NaClO浓度对K 2 FeO 4 生成率的影响.
根据图分析:工业生产中最佳温度为 ℃,此时Fe(NO 3 ) 3 与NaClO两种溶液最佳质量浓度之比为 .
(4)K 2 FeO 4 在水溶液中易水4FeO 4 2- +10H 2 O
4Fe(OH) 3 +8OH - +3O 2 ↑.在提纯K 2 FeO 4 时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 溶液(填序号).
A.H 2 OB.CH 3 COONa、异丙醇C.NH 4 Cl、异丙醇D.Fe(NO 3 ) 3 、异丙醇
(5)将适量K 2 FeO 4 溶解于pH=4.74的溶液中,配制成c(FeO 4 2- )=1.0mmol?L -1 的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO 4 2- )的变化,结果见图Ⅲ.该实验的目的是 .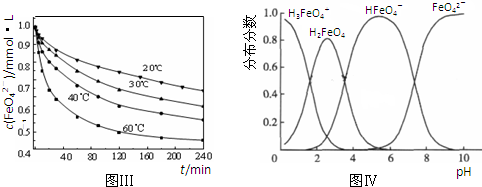
(6)FeO 4 2- 在水溶液中的存在形态如图Ⅳ所示.下列说法正确的是 (填字母).
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=10的这种溶液中加硫酸至pH=2,HFeO 4 - 的分布分数逐渐增大
C.向pH=6的这种溶液中加KOH溶液,发生反应的离子方程式为:HFeO 4 - +OH - =FeO 4 2- +H 2 O. yeahlum1年前1
yeahlum1年前1 -
 科幻世界 共回答了19个问题
科幻世界 共回答了19个问题 |采纳率100%/1年前查看全部
- 絮凝性细菌分泌的具有絮凝活性的高分子化合物,能与石油污水中的悬浮颗粒和有机物等形成絮状沉淀,起到净化污水的作用。为进一步
絮凝性细菌分泌的具有絮凝活性的高分子化合物,能与石油污水中的悬浮颗粒和有机物等形成絮状沉淀,起到净化污水的作用。为进一步提高对石油污水的净化效果,将絮凝性细菌和石油降解菌融合,构建目的菌株。其流程图如下。据图回答: 

(1)溶菌酶的作用是________________。
(2)PEG的作用是____________________________________________________。
(3)经处理后,在再生培养基上,未融合的A、B难以生长。图中AB融合菌能生长和繁殖的原因是____________________________________________________________________。
(4)目的菌株的筛选:筛选既能分泌具有絮凝活性的化合物,又能在含有__________的培养基上生长的AB融合菌,选择效果最好的作为目的菌株。
(5)为探究目的菌株不同发酵时间发酵液的絮凝效果,将目的菌株进行发酵培养,定时取发酵液,加入石油污水中:同时设置_____________________________为对照组。经搅拌、静置各3分钟后,分别测定上层水样的石油浓度和COD值(COD值越高表示有机物污染程度越高),计算石油去除率和COD去除率,结果如上图。
(6)目的菌的种群增长曲线是________型。在40~44小时,发酵液对石油污水的净化效果最好,其原因是________________。 trueyin1年前1
trueyin1年前1 -
 四海兄弟一世情缘 共回答了12个问题
四海兄弟一世情缘 共回答了12个问题 |采纳率91.7%(1)分解细胞壁
(2)诱导原生质体融合
(3)两亲本失活部位不同,融合后活性部位互补
(4)石油
(5)不加发酵液的石油污水
(6)S 此期间,目的菌及其产生的絮凝活性高分子化合物的含量高1年前查看全部
- 草酸钙怎么沉淀絮凝处理一种废水,含草酸,用钙离子沉淀,但形成的沉淀是细小的颗粒,不絮凝成团,一般的滤纸都滤不住.有什么好
草酸钙怎么沉淀絮凝
处理一种废水,含草酸,用钙离子沉淀,但形成的沉淀是细小的颗粒,不絮凝成团,一般的滤纸都滤不住.有什么好的办法么? 落花流情20081年前1
落花流情20081年前1 -
 麻辣hoho 共回答了17个问题
麻辣hoho 共回答了17个问题 |采纳率88.2%添加絮凝剂使沉淀絮凝成大的颗粒,然后过滤或者自然沉淀.
比如PAC,具体说明你可以去百度百科查,我懒的写了
使用时一定要注意絮凝剂的使用条件,比如水体的PH,温度等,这影响到絮凝效果的好坏.1年前查看全部
- 高铁酸钾是一种高效的多功能水处理剂,具有氧化、吸附、絮凝、助凝、杀菌、除臭等作用,高铁酸钾的开发和利用正日益显示出其广阔
高铁酸钾是一种高效的多功能水处理剂,具有氧化、吸附、絮凝、助凝、杀菌、除臭等作用,高铁酸钾的开发和利用正日益显示出其广阔的应用前景.其制备路线如下:
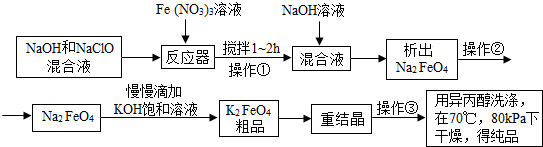
试回答下列问题
(1)操作①搅拌的目的是______.
(2)操作②与操作③相同,该操作的名称是______
(3)慢慢滴加KOH饱和溶液发生的复分解反应的化学方程式为______.
(4)高铁酸钾作为净水剂对人的身体还有一个的好处是补铁,K2FeO4中铁元素的化合价为______价
(5)操作③后剩余的母液中,可循环使用的物质的化学式是______. bnliner1年前1
bnliner1年前1 -
 miraclecai 共回答了23个问题
miraclecai 共回答了23个问题 |采纳率91.3%解题思路:(1)根据玻璃棒搅拌的作用分析
(2)根据分离混合物的方法分析
(3)根据复分解反应的特点及化学方程式的书写原则书写方程式
(4)根据化合物中正负化合价的代数和为0分析
(5)根据重结晶后母液中的溶质分析(1)氢氧化钠和NaClO的混合液中加入硝酸亚换溶液发生化学反应,为使其充分反应可用玻璃棒搅拌.
(2)操作②与操作③都是将固体从液体中分离出来,因此可采用过滤
(3)慢慢滴加KOH饱和溶液后,氢氧化钾和高铁酸钠发生复分解反应生成高铁酸钾和氢氧化钠,化学方程式为 2KOH+Na2FeO4=K2FeO4+2NaOH.
(4)K2FeO4中钾元素+1价,氧元素-2价,根据正负化合价的代数和为0可知铁元素的化合价为+6价
(5)操作③后剩余的母液中还含有氢氧化钠溶液可循环使用.
故答案为:(1)使其充分反应.
(2)过滤
(3)2KOH+Na2FeO4=K2FeO4+2NaOH.
(4)+6
(5)NaOH点评:
本题考点: 物质的相互转化和制备.
考点点评: 本题结合高铁酸钾(K2FeO4)的制备主要考查了氧化还原反应的知识、离子的检验等,培养了学生运用知识的能力.1年前查看全部
- 如何提高聚丙烯酰胺的絮凝效果?需要那些条件?
如何提高聚丙烯酰胺的絮凝效果?需要那些条件?
使用中发现在絮凝过程中无法生成矾花;且在沉淀过程中出水时乳白色,在沉淀池溢流口上有许多白色沉淀物. 聚丙烯酰胺的使用是否还有一些前提的条件? justjump1年前3
justjump1年前3 -
 candy8866 共回答了19个问题
candy8866 共回答了19个问题 |采纳率100%在使用聚丙烯酰胺时,需要考虑以下几点:1、水温水温低时,因无机盐类混凝剂的水解是吸热反应,不利于混凝剂如硫酸铝的水解,且水温低时水的粘度大,颗粒的布朗运动强度减弱,不利于胶体脱稳和絮凝物的成长.铝盐作为混凝剂...1年前查看全部
- 预处理絮凝沉淀时ph值为何调至10.5左右
 蝴蝶剑上飞1年前1
蝴蝶剑上飞1年前1 -
 一飘797 共回答了13个问题
一飘797 共回答了13个问题 |采纳率100%应该调至7-9的范围最好,絮凝效果最佳,如果你要调到10.5左右可能是考虑到了聚合氯化铝的ph值,因为聚合氯化铝的ph值为3.5-5之间1年前查看全部
- 在添加了絮凝剂的污水处理后,絮凝物想要再次利用,请问是用什么方法可以去除絮凝剂或者破坏絮凝效果,请问用什么办法
 烛影摇红柠檬醉1年前1
烛影摇红柠檬醉1年前1 -
 成都肥肠粉 共回答了19个问题
成都肥肠粉 共回答了19个问题 |采纳率78.9%这是可以降低药剂消耗、减少污泥产量的好思路
你的问题需要详细的污水背景和运行参数
我试试给你提点建议
已有污水处理场合自来水厂实现无药剂运行,减量应当可以实现.1年前查看全部
- 电絮凝处理的PH以多少为佳.
 hdcctvzy1年前2
hdcctvzy1年前2 -
 jason2007r1 共回答了20个问题
jason2007r1 共回答了20个问题 |采纳率90%61年前查看全部
- PAM的絮凝机理聚丙烯酰胺的絮凝机理,最好再解释一下为什么随着投药量的变化会出现有顶点的抛物线.还有它的处理效果为什么会
PAM的絮凝机理
聚丙烯酰胺的絮凝机理,最好再解释一下为什么随着投药量的变化会出现有顶点的抛物线.还有它的处理效果为什么会受溶液pH的影响 enjoy231年前1
enjoy231年前1 -
 iimlzy 共回答了18个问题
iimlzy 共回答了18个问题 |采纳率83.3%问的好,这个问题我想了很久,大家交流下想法吧.
简单来讲PAM能使悬浮物质通过电中和,架桥吸附作用起的絮凝作用.一般和悬浮物的性质,动电位,黏度.浊度和悬浮液的PH有关.
第二个问题PAM的含量高了,会影响悬浮物上面的动电位吧,使吸附架桥作用力变小了吧.就是水变的粘了,PAM量过了,已经不反应了,那么就相当于清水里加PAM,粘的不得了,你想在胶水里好沉淀吗.
第三个问题PH对于沉淀都有影响,即使加的是PAC也影响,这个影响是影响的水里的悬浮物的沉淀,假如是强酸,那悬浮物都溶解掉了,腐蚀性是一方面,离子不适合PH也是一方面,铜离子不能在酸里沉淀的吧,这个你看下化学好了.1年前查看全部
- 高铁酸钾是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.其生产工艺如下:
 yy561年前1
yy561年前1 -
 badoudou 共回答了10个问题
badoudou 共回答了10个问题 |采纳率80%(1)温度较低 2分
(2)2,3,10;2,6,3,5 3分
(3)AC 2分
(4)5.6m/33 L 3分
(5)在pH=11.50的溶液中,OH-浓度大,使FeO42-+10H2O 4Fe(OH)3+
8OH-+3O2↑平衡向左移动(合理答案也给分). 2分1年前查看全部
- 硫酸铝絮凝原理是什么啊,是al离子和oH根离子生成沉淀吗?
 最爱猪腩肉1年前3
最爱猪腩肉1年前3 -
 以前都这样 共回答了21个问题
以前都这样 共回答了21个问题 |采纳率95.2%其根本原因在于它能提供大量的络合离子,且能够强烈吸附胶体微粒,通过吸附、桥架、交联作用,从而使胶体凝聚.同时还发生物理化学变化,中和胶体微粒及悬浮物表面的电荷,降低了δ电位,使胶体微粒由原来的相斥变为相吸,破坏了胶团稳定性,使胶体微粒相互碰撞,从而形成絮状混凝沉淀,沉淀的表面积可达(200~1000)m2/g,极具吸附能力1年前查看全部
- 水处理树脂原水硬度2600mg/l(没写错),以caco3计.预处理加絮凝、沉淀,貌似效果不很好.为降低硬度,加用001
水处理树脂
原水硬度2600mg/l(没写错),以caco3计.预处理加絮凝、沉淀,貌似效果不很好.为降低硬度,加用001-7强酸树脂软化,产水40T/H,罐体1500*2800mm.树脂装2/3.根据公式算出最多一小时就得交换,但卖树脂的商家给出的公式是9小时交换一次,为什么? 魅郎1年前1
魅郎1年前1 -
 mIqnzex 共回答了19个问题
mIqnzex 共回答了19个问题 |采纳率89.5%根据你所描述,留有百分之十的树脂安全空间的话,也只能产58吨水就得再生,也就是一个小时多点,树脂商家给出的公式不要去探讨了,理论和现实永远是两码事
7个硬度以上就做双级软化,楼上的大可不必
本人13mmol/L以下全是用单级,产水完全能够稳定到0.03mmol/L
楼主的水硬度实在是够高,50个以上硬度我也只做过一次
你的情况要采用3级软化了,前2级处理后产水可以达到500mg/L左右,经过第三级处理就完全达标了
最好的配置是:
前两级6个1.1米直径的罐(没有这规格可以定做) ,3个一组,两用一备,第三级两个罐一用一备 树脂填充的要尽量高,留下一点反洗空间就行 ,这样就可以保证稳定的连续24小时供水1年前查看全部
- 为什么我所配制的淀粉溶液总是会有白色的絮凝?
 第一册1年前1
第一册1年前1 -
 accbd 共回答了21个问题
accbd 共回答了21个问题 |采纳率90.5%配制淀粉溶液,首先用少量凉水把淀粉调成稀糊状,然后倒入煮沸的开水中,并且在不断搅拌中继续煮沸3分钟左右,最后放冷至室温.静置几个小时后(最好放置过夜),倾取上清液就可以了.另外淀粉溶液不能使用太长时间,长时间不用也会出现白色絮状和沉淀.1年前查看全部
- 污水处理沉淀池是怎么工作的水是怎么流的?絮凝的沉淀又在哪里?有沉淀池的解说图就更好了斜板沉淀池
 thyd1年前1
thyd1年前1 -
 baker2 共回答了18个问题
baker2 共回答了18个问题 |采纳率88.9%水怎么流的?不同的污水来源,工艺是不一样的,一般的生活污水工艺是:污水---格栅---沉砂池---生物处理---二沉池你可以去百度文库找水处理方面的ppt看看.了解一下水处理构筑物怎么工作的.沉淀池有初沉池和二沉池.对于...1年前查看全部
- 在沉淀过程中,絮凝颗粒相互聚结的途径有哪些
 说了我就上当了1年前1
说了我就上当了1年前1 -
 ff贴之用 共回答了16个问题
ff贴之用 共回答了16个问题 |采纳率93.8%去除胶体表面电荷后的布朗运动和流体湍流状态下的颗粒碰撞,再就是高分子药剂的吸附架桥和悬浮泥渣层的网捕过滤.1年前查看全部
- 高铁酸钾(K 2 FeO 4 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺流程如下:
高铁酸钾(K 2 FeO 4 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺流程如下:
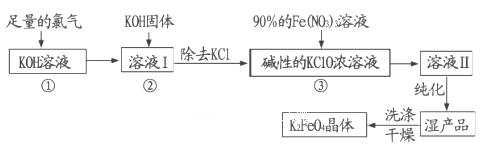
请同答下列问题:
(l)写出向KOH溶液中通入足量Cl 2 发生反应的离子方程式_______ 。
(2)在溶液I中加入KOH固体的目的是______(填编号)。
(3)从溶液Ⅱ中分离出K 2 FeO 4 后,还会有副产品KNO 3 ,KCl,则反应③中发生的离子反应方程式为_______。每制得59.4克K 2 FeO 4 ,理论上消耗氧化剂的物质的量为____ mol。A.为下一步反应提供碱性的环境 B.使KClO 3 转化为KClO C.与溶液I中过量的Cl 2 继续反应,生成更多的KClO D.KOH固体溶解时会放出较多的热量,有利于提高反应速率
(4)高铁酸钾(K 2 FeO 4 )作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:_______ FeO 4 2 - +_______ H 2 O="_______" Fe(OH) 3 (胶体)+_______O 2 ↑+_______OH - 。
(5)从环境保护的角度看,制备K 2 FeO 4 较好的方法为电解法,其装置如图所示。电解过程中阳极的电极反应式为________。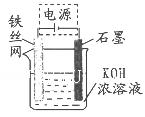
(6)高铁电池是一种新型二次电池,电解液为碱溶液,其反应式为:3Zn(OH) 2 +2Fe(OH) 3 +4KOH-----3Zn+2K 2 FeO 4 +8H 2 O,放电时电池的负极反应式为________ 。 lvchaohahaha1年前1
lvchaohahaha1年前1 -
 huang123tao 共回答了11个问题
huang123tao 共回答了11个问题 |采纳率81.8%1年前查看全部
- 高铁酸钾(K 2 FeO 4 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下 (1)反应①应在温度
高铁酸钾(K 2 FeO 4 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下 
(1)反应①应在温度较低的情况下进行。因在温度较高时KOH与Cl 2 反应生成的是KClO 3 。写出在温度较高时KOH 与Cl 2 反应的化学方程式______________________,当反应中转移5mol电子时,消耗的氯气是
___________mol。
(2)在反应液I中加入KOH固体的目的是___________(填编号)。
A.与反应液I中过量的Cl 2 继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使KClO 3 转化为KClO
(3)从溶液II中分离出K 2 FeO 4 后,还会有副产品KNO 3 、KCl,则反应③中发生的离子反应方程式为
___________________________。
(4)如何判断K 2 FeO 4 晶体已经洗涤干净______________________。
(5)高铁酸钾(K 2 FeO 4 )作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,其离子反应是:
____FeO 4 2- +____H 2 O→_____Fe(OH) 3 (胶体)+_____O 2 ↑+______完成并配平方程式将完整的离子方程式写在下方:______________________。 追求真理吧1年前1
追求真理吧1年前1 -
 venus88 共回答了23个问题
venus88 共回答了23个问题 |采纳率91.3%(1)6KOH+3Cl 2 ==KClO 3 +5KCl+3H 2 O;3
(2)AC
(3)2Fe 3+ +3ClO - +10OH - ==2FeO 4 2- +3Cl - +5H 2 O
(4)取最后一次的洗涤液,加硝酸银溶液,无白色沉淀则已被洗净
(5)4FeO 4 2- +10H 2 O=4Fe(OH) 3 (胶体)+3O 2 ↑+8OH -1年前查看全部
- 聚合氯化铝絮凝后发红色!含量是26%的!用别人23多点的就不会出现红色!镀锌管厂的污水处理!
聚合氯化铝絮凝后发红色!含量是26%的!用别人23多点的就不会出现红色!镀锌管厂的污水处理!
我去现场看了下!聚铝的池里红色物体是一种颗粒没有溶解!请问怎么办?是什么东西 thornbird0071年前1
thornbird0071年前1 -
 cyg12388 共回答了13个问题
cyg12388 共回答了13个问题 |采纳率92.3%含量28%的,颜色是棕黄色,溶解后看上去有点发红1年前查看全部
- 如何去除氯离子,能不能用物理化学方法絮凝去除?
 _牛小牛_1年前1
_牛小牛_1年前1 -
 00000097 共回答了16个问题
00000097 共回答了16个问题 |采纳率87.5%不知道你说的是什么当中的氯离子.
水中那种大量的氯离子用成盐法进行去除.含量较低的氯离子只能用离子交换柱(树脂)进行吸附(有时会附加活性炭).含量低时也会用反渗透进行处理.
以上是工程中的应用,这是个世界难题,不能做到最好,只能尽量去除.1年前查看全部
大家在问
- 1表明听众听得入了神的词语有
- 2植树节作文300字以上内容具体,语句通顺.
- 3在湖上划船我可以说boat on the river吗
- 4正y乘负y等于多少?怎么乘的?
- 5我想要每个段落的第一个字相同,例如:"附近的快速链接、给大家快乐圣诞节.“前面同时添加“我”字
- 6如何确定可能饱和的溶液达到饱和状态
- 7食之无味,弃之可惜如何理解这句话的意思?
- 8I like ( )day,but I do not like( )
- 9高职关于集合数学题设全集U=R,集合A={X|-4小于X小于4},B={X|X大于3},求A并B,Cu(A并B)要详细步
- 10Internet dating has become one of the biggest and most succe
- 11y=1/(tanx-cotx)的周期和值域是什么?
- 12二十一分之4减三分之2加三分之一+二十一分之8 要用简便方法
- 13look!he is l ____ on the ground
- 14六年级上册寒假作业65页的题怎么做
- 15联系实际,谈谈如何在其他课程中学习语文



