(2014•东兴区一模)二十一世纪是海洋开发与利用的世纪,我市规划确立了“蓝色经济”发展战略,海洋化学资源的综合利用将是
 cvmeow2022-10-04 11:39:541条回答
cvmeow2022-10-04 11:39:541条回答问题一:海水制镁过程中如何富集镁离子?
甲、乙、丙三位同学各自提出自己的设想:甲:直接往海水中加入石灰乳.乙:高温加热蒸发海水后,加入石灰乳.丙:向晒盐后的卤水中,加入石灰乳.通过分析比较,你认为______的设想最为经济合理(选填“甲”、“乙”或“丙”).
问题二:粗盐纯化过程中如何除去可溶性杂质?
粗盐中含有硫酸钠、氯化钙等杂质.提纯时,先向粗盐水中加过量的氢氧化钡溶液,目的是完全除尽硫酸钠;再加过量的碳酸钠溶液,除去杂质阳离子;滤去沉淀,向滤液中加入______,将溶液的pH调为7,即得到精盐水.
问题三:海水“制碱”的产物成分是什么?
同学们从某企业取回少量碳酸氢钠受热完全分解后的固体样品,为确定其成分,进行了如下探究:
【提出猜想】
甲的猜想:样品中只含有碳酸钠;
乙的猜想:样品中含有碳酸钠和氢氧化钠;
丙的猜想:样品中只含有氢氧化钠.
他们做出上述三种猜想的科学依据是______.
【实验、记录与分析】
| 步骤 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量样品于试管中,加水完全 溶液,再加入过量______ | 生成白色沉淀 | 丙的猜想 不成立 |
| 2 | 取步骤1反应后的溶液于试管中 ______ | ______ | 只有甲的 猜想成立 |

已提交,审核后显示!提交回复
共1条回复
 口粮至亲 共回答了20个问题
口粮至亲 共回答了20个问题 |采纳率75%- 解题思路:问题一:从节约原料,方法可行的角度分析即可;
问题二:从除掉杂质时一定不能引入新的杂质,并结合酸碱盐之间的反应规律分析解答;
问题三:依据质量守恒定律的元素守恒规律,猜测产物的情况;从判断溶液中是否具有碳酸根,以及去除溶液中的碳酸根后是否还含有氢氧化钠的角度对问题进行分析即可;问题一:三种方式中甲需要大量的石灰乳,乙则需要加热消耗能量,只有丙的方式节约原料和能源且可行;
问题二:从除杂的原理出发可知,当粗盐中含有硫酸钠、氯化钙等杂质时一般是先加入过量的氢氧化钡,以除掉溶液中的硫酸根离子(与钡离子结合成硫酸钡沉淀),再加入过量的碳酸钠,以除掉溶液中的钙离子(与碳酸根结合成碳酸钙)和剩余的钡离子(与碳酸根结合成碳酸钡沉淀),此时溶液中的杂质离子是多余的碳酸根离子和氢氧根离子,所以此时加入盐酸调节溶液的pH为7,即可除掉碳酸根离子和氢氧根离子;
问题三:由于化学反应前后元素的种类不变,所以才有以上三种猜测;
丙的猜想不成立,则可检验溶液中是否含有碳酸钠,只要加入氯化钡的溶液并生成白色沉淀(碳酸根离子会与钡离子结合成碳酸钡沉淀),则可说明并不成立;
取上述反应后的溶液继续试验,如果溶液呈碱性则有氢氧化钠的存在,不呈碱性则无氢氧化钠的存在;
故答案为:问题一:丙;问题二:稀盐酸;
问题三:化学反应前后元素的种类不变或元素守恒;氯化钡溶液;滴加无色酚酞试液;无明显现象.点评:
本题考点: 对海洋资源的合理开发与利用;氯化钠与粗盐提纯;盐的化学性质;质量守恒定律及其应用.
考点点评: 本题属于实验探究题,并通过实验探究来鉴定了物质的组成,既有实验过程的探究,又有结论的探究.解题时首先根据题目的信息和查阅的资料,然后设计实验方案、进行实验,最后得出正确的结论,符合科学探究的基本环节. - 1年前
相关推荐
- (2014•东兴区一模)从H、C、O、Na四种元素中,选择适当的元素,用化学式按下列要求填空.
(2014•东兴区一模)从H、C、O、Na四种元素中,选择适当的元素,用化学式按下列要求填空.
①化石燃料,沼气的主要成分:______
②重要的化工原料俗称苛性钠:______. 5418050101年前1
5418050101年前1 -
 你还是算了吧 共回答了25个问题
你还是算了吧 共回答了25个问题 |采纳率100%解题思路:首先根据题意确定物质的化学名称,然后根据题目所提供的元素、书写化学式的方法写出物质的化学式即可.①沼气的主要成分是甲烷,甲烷的化学式为:CH4;
②苛性钠是氢氧化钠的俗称,其化学式为:NaOH.
故答案为:①CH4;②NaOH.点评:
本题考点: 化学式的书写及意义.
考点点评: 本题难度不大,熟练掌握常见物质的性质、用途、组成及化学式的书写是正确解答此类题的关键所在.1年前查看全部
- (2014•东兴区一模)已知硝酸钾的溶解度随着温度的升高而增加,现有以下方法:
(2014•东兴区一模)已知硝酸钾的溶解度随着温度的升高而增加,现有以下方法:
A.加溶剂水B.加溶质硝酸钾C.升高温度D.降低温度
(1)能减小硝酸钾溶解度的方法是______;
(2)能便不饱和硝酸钾溶液变成饱和溶液的方法有______. 7531598521年前1
7531598521年前1 -
 wangya105 共回答了22个问题
wangya105 共回答了22个问题 |采纳率90.9%解题思路:(1)固体的溶解度受到溶质和溶剂两方面性质的影响,同时还有温度的影响,气压对固体的溶解度几乎无影响;
(2)大多数物质的不饱和溶液变为饱和溶液,常用的方法有:增加溶质,蒸发溶剂,降低温度,据此进行分析解答.(1)硝酸钾的溶解度随着温度的降低而减小,降低温度能减小硝酸钾溶解度;溶解度不受溶剂质量、溶液质量多少的影响,故加溶剂水、加溶质硝酸钾不会改变硝酸钾的溶解度;
(2)硝酸钾的溶解度随着温度的降低而减小,加入KNO3固体,能使接近饱和的KNO3溶液变成饱和溶液;降低温度可使接近饱和的KNO3溶液变成饱和溶液.
故答案为:(1)D;(2)BD.点评:
本题考点: 固体溶解度的影响因素;饱和溶液和不饱和溶液相互转变的方法.
考点点评: 本题难度不大,掌握固体的溶解度的影响因素、大多数物质不饱和溶液变成饱和溶液一般采用的方法是正确解答本题的关键.1年前查看全部
- (2014•东兴区一模)将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间
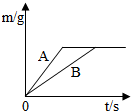 (2014•东兴区一模)将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,请回答下列问题:
(2014•东兴区一模)将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,请回答下列问题:
(1)写出锌与稀硫酸反应的化学方程式______.
(2)对于该图象的理解,下列说法正确的是______(填序号).
①A表示锌和稀硫酸的反应曲线
②反应结束后两种金属一定都有剩余
③反应结束后稀硫酸都没有剩余
④反应结束后消耗两种金属的质量相等
⑤反应结束后所得溶液质量相等. 战无不胜1年前1
战无不胜1年前1 -
 因为漠燃 共回答了22个问题
因为漠燃 共回答了22个问题 |采纳率95.5%解题思路:(1)锌与稀硫酸反应生成氢气和硫酸锌,根据反应物、生成物,书写化学方程式;
(2)由已知:“等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸充分反应”:
①锌的活动性比铁的活动性强,等质量的金属,锌反应的时间短;
②由图示可知:生成的氢气的质量相等,所以硫酸均反应完;由方程式分析,二者反应结束后,可能金属都有剩余,也可能锌恰好反应完,铁有剩余;
③由图示可知:生成的氢气的质量相等,所以硫酸均反应完;
④由方程式分析可知:相等质量的铁和锌与硫酸反应,铁生成氢气多;
⑤因为“等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸充分反应”,所以反应物的总质量相等;依据质量守恒定律,反应后溶液的质量=反应前的总质量-气体的质量-不溶物的质量,图示中生成氢气的质量相等,但剩余的不溶物的质量不同,所以反应结束后所得溶液质量不相等.(1)锌与稀硫酸反应生成氢气和硫酸锌,则其化学方程式为Zn+H2SO4═ZnSO4+H2↑,
(2)由已知:“等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸充分反应”进行分析:
①锌的活动性比铁的活动性强,所以等质量的金属,锌反应的时间短,正确;
②由图示可知:生成的氢气的质量相等,所以硫酸均反应完;Zn+H2SO4═ZnSO4+H2↑,Fe+H2SO4═FeSO4+H2↑,由方程式分析可知:如果锌恰好反应,则铁有剩余;故错误;
③置换反应是金属置换酸中的氢元素,所以若生成的氢气的质量相等,硫酸均反应完;故正确;
④根据化学方程式Fe+H2SO4═FeSO4+H2↑,可知每56g铁生成2g氢气,根据化学方程式Zn+H2SO4═ZnSO4+H2↑,可知每65g锌反应生成2g氢气;所以若是相等质量的铁和锌与硫酸反应,铁生成氢气多,而不会相等,故错误;
⑤因为“等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸充分反应”,所以反应物的总质量相等;依据质量守恒定律,反应后溶液的质量=反应前的总质量-气体的质量-不溶物的质量,图示中生成氢气的质量相等,但剩余的不溶物的质量不同,所以反应结束后所得溶液质量不相等.故错误;
故选①③.
故答案为:(1)Zn+H2SO4═ZnSO4+H2↑;(2)①③.点评:
本题考点: 金属的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题结合图象对金属与酸的反应进行了细致的考查,能很好的考查学生对知识的掌握和应用能力,要结合相关知识认真分析.1年前查看全部
- (2014•东兴区一模)硫酸和盐酸既是实验室常用的试剂,也是重要的化工原料.它们既有相似之处,又有不同之点.
(2014•东兴区一模)硫酸和盐酸既是实验室常用的试剂,也是重要的化工原料.它们既有相似之处,又有不同之点.
(1)它们都能除铁锈,写出盐酸与铁锈主要成分反应的化学方程式______.
(2)请写出把硫酸转变为盐酸的化学方程式______. zwmg1年前1
zwmg1年前1 -
 海水正蓝422 共回答了20个问题
海水正蓝422 共回答了20个问题 |采纳率80%解题思路:酸的通性有:
①都能使紫色石蕊试液变红,不能使无色酚酞变色;
②能够和活泼金属反应生成氢气;
③能够和金属氧化物反应生成盐和水;
④能够和碱反应生成盐和水;
⑤能够和某些盐反应生成新酸和新盐;酸溶液都是酸性溶液,它们的pH都小于7.(1)由于酸溶液都能和某些金属氧化物发生复分解反应生成盐和水,方程式为:Fe2O3+6HCl═2FeCl3+3H2O
(2)把硫酸转变成盐酸,即把硫酸中的硫酸根离子转变成氯离子,也就是把硫酸根离子转化成沉淀,因此应加入适量的氯化钡溶液,方程式为:H2SO4+BaCl2═BaSO4↓+2HCl.
故答案为:
(1)Fe2O3+6HCl═2FeCl3+3H2O;
(2)H2SO4+BaCl2═BaSO4↓+2HCl.点评:
本题考点: 酸的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不是很大,主要考查了酸的有关的化学性质,从而培养学生对知识的灵活运用的能力.1年前查看全部
- (2014•东兴区一模)A、B、C、D都是初中化学中常见物质,A是人类赖以生存的一种无色液体,D是一种黑色固体,具有如图
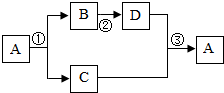 (2014•东兴区一模)A、B、C、D都是初中化学中常见物质,A是人类赖以生存的一种无色液体,D是一种黑色固体,具有如图所示的转化关系(反应条件、其他反应物及多余产物均略去):
(2014•东兴区一模)A、B、C、D都是初中化学中常见物质,A是人类赖以生存的一种无色液体,D是一种黑色固体,具有如图所示的转化关系(反应条件、其他反应物及多余产物均略去):
(1)写出①反应的化学方程式2H2O
2H2↑+O2↑通电 .2H2O;
2H2↑+O2↑通电 .
(2)D可能是______(填化学式). lihh2081年前1
lihh2081年前1 -
 zhenfei_27 共回答了16个问题
zhenfei_27 共回答了16个问题 |采纳率93.8%解题思路:根据A是人类赖以生存的一种无色液体,所以A是水,水通电分解会生成氢气和氧气,所以B、C是氢气或氧气中的一种,B能转化生成黑色固体D,且D能与C反应生成水,则可能是发生的氢气还原金属氧化物的反应,所以C是氢气,B是氧气,D可能是氧化铜或四氧化三铁,然后将推出的各种物质代入转化关系中验证即可.A是人类赖以生存的一种无色液体,所以A是水,水通电分解会生成氢气和氧气,所以B、C是氢气或氧气中的一种,B能转化生成黑色固体D,且D能与C反应生成水,则可能是发生的氢气还原金属氧化物的反应,所以C是氢气,B是氧气,D可能是氧化铜或四氧化三铁,水在通电的条件下生成氢气和氧气,氧气和铁在点燃的条件下生成四氧化三铁,氧气和铜在加热的条件下生成氧化铜,氢气和氧化铁或氧化铜在高温或加热的条件下生成水,推出的各种物质均满足题中的转化关系,推导合理,所以D可能是氧化铁或氧化铜;
反应①是水在通电的条件下生成氢气和氧气,化学方程式为:2H2O
通电
.
2H2↑+O2↑.
故答案为:(1)2H2O
通电
.
2H2↑+O2↑;
(2)CuO或Fe3O4.点评:
本题考点: 物质的鉴别、推断;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
考点点评: 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.1年前查看全部
- (2014•东兴区一模)归纳总结是学习化学的重要方法,下面是某同学对有关知识的总结,请你填写空格:如图表示几种化合物能通
 (2014•东兴区一模)归纳总结是学习化学的重要方法,下面是某同学对有关知识的总结,请你填写空格:如图表示几种化合物能通过一步反应转化为含镁化合物M.如图中物质M属于______(选填“单质”、“氧化物”、“酸”、“碱”或“盐”);从①-③表示的化学反应中任选一个,写出化学方程式______.
(2014•东兴区一模)归纳总结是学习化学的重要方法,下面是某同学对有关知识的总结,请你填写空格:如图表示几种化合物能通过一步反应转化为含镁化合物M.如图中物质M属于______(选填“单质”、“氧化物”、“酸”、“碱”或“盐”);从①-③表示的化学反应中任选一个,写出化学方程式______.  二只牛牛1年前1
二只牛牛1年前1 -
 绝对任性 共回答了14个问题
绝对任性 共回答了14个问题 |采纳率92.9%解题思路:根据图示进行分析,酸和盐属于化合物,为并列关系;根据图示可以看出硫酸锌、氧化镁和硫酸都能转化生成M,故M是硫酸镁,属于盐类物质,氧化镁能与硫酸反应生成硫酸镁.硫酸锌、氧化镁和硫酸都能转化生成M,M是含镁化合物,故M是硫酸镁,属于盐类物质;
氧化镁能与硫酸反应生成硫酸镁和水,反应物是氧化镁和硫酸,生成物是硫酸镁和水,已经平了,所以方程式是:MgO+H2SO4═MgSO4+H2O.
故答案为:盐; MgO+H2SO4═MgSO4+H2O.点评:
本题考点: 物质的相互转化和制备;酸的化学性质;盐的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了物质类别的关系以及物质间的转化,完成此题,可以依据物质的性质进行.1年前查看全部
- (2014•东兴区一模)利用不同物质性质不同区分或分离物质是化学科学的重要方法,下面区分各级物质的方法中,不合理的是(
(2014•东兴区一模)利用不同物质性质不同区分或分离物质是化学科学的重要方法,下面区分各级物质的方法中,不合理的是( )
被区分的物质 区分方法 A.冰、干冰 各取一块置于表面皿中,观察有无白雾生成 B.硬水、软水 各取50mL分别滴加等量肥皂水,搅拌,观察产生泡沫多少 C.生石灰、熟石灰 各取一药匙分别置于20mL水中,搅拌,测量温度 D.烧碱、纯碱 各取少量溶液于试管中,分别滴加酚酞试夜,观察颜色变化
A.A
B.B
C.C
D.D 胡言乱语吧1年前1
胡言乱语吧1年前1 -
 saintsoul 共回答了15个问题
saintsoul 共回答了15个问题 |采纳率80%A、把冰和干冰露置,产生明显白雾且无液体出现的是干冰,而能融化成液体的是冰,现象不同,可以鉴别,故A正确;
B、各取50mL样品分别滴加等量肥皂水,搅拌,产生泡沫多的是软水,产生泡沫少的是硬水,现象不同,可以鉴别,故B正确;
C、氧化钙和水反应生成氢氧化钙会放出大量的热,氢氧化钙溶于水温度基本不变,取样品溶于水,溶液温度明显升高的是氧化钙,溶液温度基本不变的是氢氧化钙,现象不同,可以鉴别,故C正确;
D、碳酸钠溶液显碱性,能使无色酚酞变红色,氢氧化钠是碱,也能使无色酚酞变红色,现象相同,不能鉴别,故D错误.
故选:D.1年前查看全部
大家在问
- 1一水桶装有水,现在把桶中的水加到原来的2倍,连桶共重3千克;若把水加到原来的3倍,这是连桶共重4千克.
- 2请问WTO和IT翻译成汉语分别是什么意思?
- 3He spent a lot of time _ _ with friends.他花了大量时间和朋友喝酒.
- 4以尽量简洁的语言,概括下面这段文字所叙述的主要事实。(不超过 26 个字)
- 5氢氧化钠只要拿出来放在空气中 就会迅速吸收水分子成为液态的剧毒
- 6如果汽车以每秒120公里速度,那么每秒多少米
- 7李汉荣的转身有何匠心之处
- 8第一类曲面积分与地二类曲面积分关于这两类积分 如你所说 第一类是关于标量函数的积分第二类是关于向量函数的积分 是不是可以
- 9教室个面积大约是55平方分米.______(判断对错)
- 10下列各图是进行O 2 、CO 2 的实验室制取和有关性质的实验装置. (1)写出标号①的仪器名称: _________
- 11长期饮用蒸馏水有益健康吗
- 12是说线路板的孔大对加工过的线路板检查标准,孔大小于limit
- 13星星小学六年级共有100人其中男生40人女生60人男生人数占全年级人数的百分之几
- 14在下面句子的横线上恰当的填写日常生活中的谦辞雅语
- 15乙醇与乙酸发生酯化反应,乙醇中断裂的化学键
